
- •Основные правила при работе в химической лаборатории.
- •Требования к технике безопасности при работе в химической лаборатории.
- •Оформление лабораторного журнала.
- •Лабораторная работа №1.
- •Посуда общего назначения
- •Посуда специального назначения
- •Мерная посуда.
- •Лабораторная работа №2.
- •Лабораторная работа №3.
- •Лабораторная работа №4.
- •Лабораторная работа №5.
- •Лабораторная работа № 6.
- •Лабораторная работа № 7.
- •Лабораторная работа №8.
- •Лабораторная работа №9.
- •Ю.И. Сухарев, и.Ю. Апаликова, н.В. Пыхова, и.Ю.Лебедева. Химия коллоидных систем; Учеб. Пособие по лабораторным работам - Челябинск: Изд-во ЧелГу, 2008. - 45 с.
- •Содержание
Лабораторная работа №5.
Получение хромокалиевых квасцов
Цель работы:получить хромокалиевые квасцы и определить выход продукта реакции от теоретически возможного.
Оборудование и реактивы:
1. Стакан 50 мл.;
2. Пипетка с делениями 5 мл.;
3. Пипетка с делениями 10 мл.;
3. Воронка Бюхнера и колба Бунзена;
4. Мерный цилиндр 50мл;
5. Весы;
6. Палочка стеклянная;
7. Кристаллизатор;
8. Бихромат калия K2Cr2O7;
9. Этиловый спирт 95 %;
10. Раствор этилового спирта 50%;
11. Фильтры.
Схема реакции:
K2Cr2O7 + C2H5OH + H2SO4 = K2SO4 + Cr2(SO4)3 + C2H4O + H2O
Ход работы:
1. На аналитических весах взвесить (20,5) г бихромата калия, массу навески с точностью до 0,01 г записать в рабочий журнал.
2. В стакан емкостью 50 мл вносят навеску бихромата калия и растворяют ее в 20 мл воды.
3. К полученному раствору осторожно под тягой добавить 2,25 мл концентрированной серной кислоты.
4. Стакан с раствором охладить в кристаллизаторе с водой. Затем очень медленно при перемешивании и охлаждении добавить 6 мл этилового спирта (или 8 мл изопропилового).
5. После введения спирта стакан оставить в кристаллизаторе с холодной водой на 30 – 40 мин. В течение этого времени на дне стакана должны выпасть кристаллы квасцов. В том случае, если выпадения кристаллов не наблюдается в раствор внести затравку из нескольких кристалликов квасцов.
6. Выпавшие кристаллы отфильтровывать на воронке Бюхнера, отмыть 4 мл 50% этанола, высушить на фильтре и взвесить с точностью до 0.01г.
7. Рассчитать выход продукта по формуле:
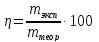
где:
mэксп– масса полученного вещества;
mтеор. – теоретическая масса продукта, рассчитывается из уравнения реакции и массы исходного бихромата калия.
8. Сделать вывод по работе и составить отчет.
Лабораторная работа № 6.
Изучение свойств буферных растворов
Цель работы:изучить свойства ацетатного и аммиачного буферных растворов.
Оборудование и реактивы:
1. pH-метр;
2. Стаканы, 50мл;
3. Пипетка, 10мл;
4. Уксусная кислота CH3COOH, 0,1М раствор;
5. Ацетат натрия CH3COONa, 0,1М раствор;
6. Аммиак NH3, 0,1 М раствор;
7. Хлорид аммония NH4Cl, 0,1 М раствор;
8. Соляная кислота HCl, 0,1н. раствор;
9. Гидроксид натрия NaOH, 0,1н. раствор.
Ход работы:
1. Приготовить ацетатный буферный раствор, для чего поместить в 2 стаканчика по 10 мл 0,1М растворов уксусной кислоты и ацетата натрия.
2. Приготовить аммиачный буферный раствор, смешав в 2 других стаканчиках по 10 мл 0,1М растворов аммиака и хлорида аммония.
3. Измерить значения рН буферных растворов и дистиллированной воды. Полученные данные занести в таблицу.
4. В три стаканчика (1-ый с дистиллированной водой, 2-ой с ацетатным буферным раствором, 3-ий с аммиачным буферным раствором) добавить по одной капле 0,1Н раствора HCl. Перемешать, измерить рН. результаты измерений занести в таблицу.
5. Повторить опыты по п.4, добавляя 0,1Н раствор NaOH.
6. Рассчитать рН полученных буферных растворов, результаты занести в таблицу.
Таблица. Значение рН буферных растворов
|
ацетатная смесь |
аммиачная смесь |
вода |
значение рН |
|
|
|
|
исходный раствор |
|
|
|
|
после добавления HCl |
|
|
|
|
после добавления NaOH |
|
|
|
|
расчетные значения рН исходных растворов |
7. Сделать выводы и составить отчет по работе.
