
- •2.1. Физические и химические свойства белков.
- •2.1.1. Кислотно-основные свойства белковых молекул
- •2.1.2. Растворимость белков.
- •2.1.3. Денатурация белков
- •2.2. Классификация и краткая характеристика отдельных групп белков.
- •2.2.1. Фибриллярные и глобулярные белки.
- •2.2.1.1. Фибриллярные белки
- •2.2.1.2. Структура глобулярных белков
- •2.3. Простые и сложные белки
- •2.3.1. Простые белки
- •2.3.2. Сложные белки
- •2.4. Биологические функции белков
Лекция 2а
2.1. Физические и химические свойства белков.
Белки, как и другие органические соединения, обладают рядом физико-химических свойств, которые обусловлены структурой их молекул.
Химические свойства белков отличаются исключительным разнообразием. Обладая аминокислотными радикалами различной химической природы, белковые молекулы способны вступать в разнообразные реакции.
2.1.1. Кислотно-основные свойства белковых молекул
Подобно аминокислотам, белки сочетают в себе, как основные, так и кислотные свойства, т. е. являются амфотерными полиэлектролитами.
В белках основной вклад в формирование кислотно-основных свойств вносят заряженные радикалы, расположенные на поверхности белковой глобулы.
Основные свойства белков связаны с такими аминокислотами, как аргинин, лизин и гистидин (т. е. имеют дополнительные амино- или иминогруппы).
Кислотные свойства белков связаны с присутствием глутаминовой и аспарагиновой аминокислот (имеют дополнительную карбоксильную группу).
2.1.2. Растворимость белков.
Каждый белок обладает определённой растворимостью, зависящей от природы самого белка и состава растворителя.
Растворимость белка зависит от:
а) аминокислотного состава, т. е. от заряда белковой молекулы: чем больше белок содержит полярных и заряженных аминокислотных радикалов, тем выше его растворимость.
б) наличия гидратного слоя (полярные и заряженные радикалы аминокислот связывают диполи воды, которые и образуют вокруг молекулы белка гидратный слой).
Добавление к водному раствору белка водоотнимающих веществ (спирт, ацетон) вызывает разрушение гидратного слоя и белок выпадает в осадок.
2.1.3. Денатурация белков
Специфические биологические функции белков, например ферментов или гормонов, зависят от их конформации, нарушения которой могут привести к потере биологической активности. В связи с этим, о белке, обладающем нормальной конформацией, говорят, что он находится в нативном (естественном) состоянии.
Нативный белок это белок, который обладает конформацией (пространственной структурой), обусловливающей специфическую биологическую функцию молекулы.
Довольно мягкие изменения физических условий, в том числе изменения pH, температуры или обработка водными растворами некоторых органических веществ (детергентов, этанола или мочевины), могут нарушить эту конформацию. В белках, подвергнутых таким воздействиям, происходит денатурация (Рис. 2.1):
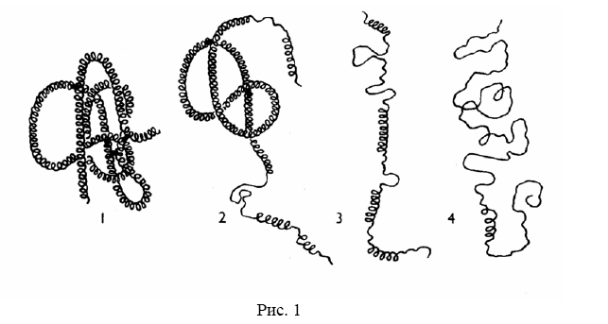
Рис. 2.1. Денатурация белковой молекулы
Денатурация белков - это разрушение четвертичной, третичной и частично вторичной структур путём разрыва слабых нековалентных взаимодействий, (водородных, ионных, гидрофобных) и дисульфидных связей, сопровождающихся потерей функции белка.
Следует различать денатурацию и деградацию белков. При деградации происходит фрагментация первичной структуры и образование фрагментов белковой макромолекулы, т. е. образуются биологически неактивные олигопептиды.
Примером денатурации белковой молекулы может служить тепловая денатурация белков в растворах при 50-60º, обусловленная разрывом нековалентных взаимодействий, при помощи которых образуется третичная структура.
Денатурация, осуществляемая в мягких условиях, часто оказывается обратимой, т. е. при удалении денатурирующего агента происходит восстановление (ренатурация) нативной конформации белковой молекулы. Для ряда белков восстановление может быть 100%-м, причём это касается ни только водородных и гидрофобных связей, но и дисульфидных мостиков.
При обратимой денатурации восстанавливается и биологическая активность белков.
Эти данные служат дополнительным доказательством того, что вторичная и третичная структуры белков предопределены аминокислотной последовательностью.
