
- •Лекция 1 введение
- •1. Формальная кинетика
- •1.1. Общие понятия
- •1.2. Скорость химической реакции
- •1.3. Обратимые и необратимые реакции.
- •Лекция 2
- •Кинетическая классификация химических реакций
- •Порядок реакции
- •Реакции 1гопорядка Гомогенные реакции
- •Реакции второго порядка
- •Методы определения порядка реакции
- •Лекция 3 влияние температуры на скорость химической реакции
- •Энергия активации
- •Методы определения энергии активации:
- •Лекция 4 теория соударений
- •Теория активированного комплекса.
- •Кинетика гетерогенных химических реакций
- •Поверхность раздела
- •Лекция 5 природа поверхности раздела
- •Площадь поверхности раздела
- •Геометрия поверхности раздела
- •Лекция 6 диффузионно-кинетическая теория гетерогенного реагирования
- •Выбор моделей процессов гетерогенного реагирования
- •Лекция 7.
- •Лекция 8
- •Диффузия газа через пограничную пленку, как лимитирующая стадия процесса.
- •Лекция 9
- •Скорость процессов при уменьшении размеров сферических частиц.
- •Кинетика гетерогенных химических реакций, сопровождающихся образованием твердого продукта реакции.
- •Лекция 11.
- •Кинетические модели топохимических реакций.
- •Лекция 12 кинетические уравнения, выведенные на основании представлений о цепном механизме развития реакций
- •Реакции газ - твердое адсорбционно-химические стадии гетерогенных химических реакций
- •Лекция 13 Хемосорбция
- •Теория адсорбции лЭнгмюра.
- •Лекция 14 Методы исследования кинетики гетерогенных реакций газ – твердое.
- •Характеристика методов и их аппаратурного оформления.
- •Лекция 15
- •Техника экспериментальных термогравиметрических исследований кинетики реакций твердое - газ:
- •Неизотермическая кинетика
- •Лекция 16 Гетерогенные процессы в системе «газ –жидкость» (газожидкостные реакции)
- •Описание массопередачи между газом и жидкостью.
Кинетика гетерогенных химических реакций, сопровождающихся образованием твердого продукта реакции.
Если на поверхности реагирующего твердого вещества образуется твердый продукт реакции, кинетика реакции будет определяться характером этого покрытия.
В случае пористой пленки, она не будет оказывать сопротивление реагентам, подходящим к поверхности раздела, и слой продукта не будет влиять на скорость реакции. В случае непористой пленки, реагент должен будет диффундировать через этот защитный слой, пока не достигнет поверхности раздела. Кинетика такой реакции будет заметно отличаться.






1


2
Время
Схема образования пористого Рисунок 23. Кинетика окисления продукта реакции. гладкой поверхности металлов:
непористый и 2 - пористый оксиды.
Сопротивление, вызванное диффузионным слоем, существует, как при непористом, так и при пористом продукте реакции, и оно может определять весь процесс. Если на поверхности образуется пористый продукт реакции и процесс контролируется диффузией через пограничный слой, скорость такого процесса будет выражаться уравнением:
![]() (102)
(102)
Для сферических частиц:
![]() (103)
(103)
В этом случае, хотя площадь поверхности раздела уменьшается со временем, эффективная площадь поверхности через которую происходит диффузия, остается постоянной.
Если продукт реакции непористый, то сопротивлением пограничного слоя можно пренебречь по сравнению с сопротивлением слоя продуктов реакции. Если толщина слоя продукта y, аM– масса твердого продукта реакции в момент времени, тоy = kM, гдеk– константа. Диффузия через слой твердого продукта будет выражаться уравнением:
![]() (104)
(104)
где n– стехиометрический коэффициент.
В отдельном случае, когда С является постоянной величиной, т.е. когда осуществляется непрерывный подвод реагента :
![]() (105)
(105)
![]() (106)
(106)
Уравнение (106) обычно называют параболическим законом и было выведено Тамманом.
1








9

Время
½(мин.)
Рисунок 24. Окисление железа по параболическому закону: 1 – 9750С, 9 – 6500С.
Значение константы в вышеприведенном уравнении может быть рассчитано при = 0, М = М0. Тогда уравнение принимает вид:
![]() (107)
(107)
В виде прореагировавшей доли = 1 – М/М0параболическое уравнение может быть преобразовано:

![]() (108)
(108)
Если твердое вещество имеет сферическую поверхность, выше приведенное решение неприменимо, поскольку Fнепрерывно уменьшается во время реакции. Было предложено несколько решений этой задачи: часть из них приближенные, часть точные.
Приближенное решение Яндера (1927г.)
Скорость роста продукта реакции обратно пропорционально его толщине:
![]() ,
гдеy– толщина
слоя продукта иk– константа пропорциональности.
,
гдеy– толщина
слоя продукта иk– константа пропорциональности.
Следовательно:
![]() (109)
(109)
Если r0– начальный радиус частицы, то прореагировавшая доля будет
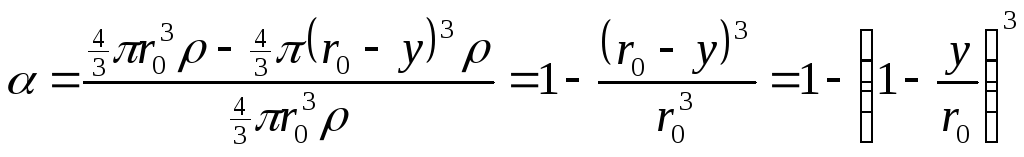 ;
;
![]() ;
;![]() ;
;
![]() (110)
(110)
Подставляя значение yв уравнение (109), получим
 (111)
(111)
График 1-(1-)1/32относительно времени даст прямую линию.


1
1

2
0,5

0
5 10 15 20
время , ч
Рисунок 25. Кинетика реакции 2Ni+O2= 2NiOпо Яндеру:
1 – шарики 149 мкм, 11300С; 2 – шарики 74 мкм, 10400С.
Неточность уравнения (111) объясняется следующими причинами:
Уравнение составлено для плоской поверхности. Оно применимо, только для шара с большим радиусом по сравнению с толщиной слоя продукта.
Уравнение справедливо только тогда, когда объем непрореагировавшего ядра плюс объем продукта реакции равен объему первоначального материала. Это приблизительно соответствует действительности только на ранних стадиях реакции.
Упрощенная модель Кранка (1957), Гинстлинга и Броунштейна (1950).




 r0 r1
r0 r1




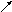




r
Рисунок 26. Образование непористого слоя продуктов реакции:
r0– первоначальный радиус;Ci– концентрация на поверхности раздела фаз; 1 – непористый слой продукта; 2 – непрореагировавшее ядро.
Если I– число молей реагента диффундирующих за времячерез слой продукта, то согласно закону Фика:

![]() (112)
(112)
Для процесса, контролируемого диффузией, Ci= 0, следовательно:
![]() (113)
(113)
Рассмотрим простой случай, когда С – постоянна.
Прореагировавшая доля
![]()

![]() (114)
(114)
Число молей непрореагировавшего твердого вещества, имеющегося в любой момент времени , будет
![]() гдеМ– молекулярная масса реагирующего
вещества;- плотность реагирующего вещества.
гдеМ– молекулярная масса реагирующего
вещества;- плотность реагирующего вещества.
Следовательно:
![]() (115)
(115)
Но скорость изменения Nпропорциональна потоку реагентаI, диффундирующего через сферическую оболочку толщинойr0 – r1.
Следовательно:
![]() ,
гдеn– стехиометрический
коэффициент.
,
гдеn– стехиометрический
коэффициент.
Поэтому

Выражая r1в виде, получим:
![]()

 (116)
(116)
Это означает, что графическая зависимость 1-2/3-(1-)2/3 от времени будет представлена прямой линией.





1,0
1-2/3-(1-)2/3
1
0,5
2
Время,
ч
10 15 25
Рисунок 27. Кинетика реакции 2Ni+O2= 2NiOпо Кранку – Гинстлингу – Броунштейну:
1 – d= 74 мкм,t= 10400C; 2 –d= 149 мкм,t= 11300C.
Уравнение (116) точнее чем уравнение Яндера, но веже оно справедливо для степени превращения вещества на 90%. Это объясняется тем, что не была принята во внимание поправка на изменение объема сферы во время реакции.
