
- •Патофизиология печени
- •Недостаточность печени Общая этиология и патогенез нарушений функций печени
- •Патогенез повреждения гепатоцитов.
- •3. Индукция апоптоза гепатоцитов:
- •Механизм повреждения гепатоцитов токсическими агентами.
- •Гепатиты
- •Хронические гепатиты
- •Цирроз печени
- •Печеночно-клеточная недостаточность
- •Патогенез печеночной энцефалопатии и комы
- •Нарушение обезвреживающей и клиренсной функций печени
- •Роль печени в нарушении обмена веществ
Нарушение обезвреживающей и клиренсной функций печени
При ряде заболеваний печени, особенно при циррозах, ее обезвреживающая функция, как правило, угнетается. Выпадает
функция ретикулоэндотелиальной системы («блокада» фагоцитоза продуктами распада клеток), появляются гемодинамические изменения (портокавальные анастомозы, снижение кровоснабжения печени). Результаты этих нарушений сравнивают с последствиями портокавального шунтирования, когда системный кровоток наполняется продуктами, поступившими из кишечника по воротной вене. Это приводит к эндотоксемии - возникают лихорадка, лейкоцитоз, гемолиз эритроцитов, почечная недостаточность, что особенно выражено при печеночной коме.
|
Роль печени в нарушении обмена веществ
Нарушение углеводного обмена.
Печень участвует в поддержании нормального уровня глюкозы в сыворотке крови путем гликогеногенеза, гликогенолиза и глюконеогенеза.
Гомеостаз глюкозы часто нарушается при циррозе печени. Как правило, при этом определяют гипергликемию и снижение толерантности к глюкозе. Уровень же инсулина в плазме или в норме, или повышен, что связано с устойчивостью к нему. Устойчивость к инсулину объясняется абсолютным снижением способности печени метаболизировать глюкозу после нагрузки вследствие уменьшения массы функционирующих гепатоцитов. У больных циррозом печени снижение реакции на инсулин, возможно, связано с рецепторными и пострецепторными аномалиями в гепатоцитах.
При циррозе печени может повышаться и уровень лактата в сыворотке крови в связи со сниженной способностью печени утилизировать его для глюконеогенеза.
При тяжелом остром гепатите, как правило, отмечается гипогликемия, а при циррозах печени это наступает в конечной стадии - при печеночной недостаточности. У больных циррозом печени при исследовании натощак уменьшается роль углеводов как источника энергии (2% при циррозе и 38% у здоровых) и увеличивается роль жиров (соответственно 86 и 45%). Это сопровождается мобилизацией триацилглицеролов в качестве источника энергии. В конечной стадии цирроза гипогликемия объясняется снижением способности печени (из-за обширного поражения ее паренхимы) синтезировать гликоген и уменьшением выработки инсулиназы (фермента, разрушающего инсулин).
В норме галактоза, поступающая в организм в составе молочного сахара, превращается в глюкозу, но при нарушениях функцио-
нального состояния печени (при острых и хронических ее заболеваниях) способность использовать галактозу снижена.
|
Нарушение белкового и ферментного обменов при заболеваниях печени проявляется в изменении: расщепления белков (до аминокислот), синтеза белков, дезаминирования, трансаминирования, декарбоксилирования аминокислот, образования мочевины, мочевой кислоты, аммиака, креатина.
Вследствие этого возникают следующие нарушения:
1. Гипопротеинемия - снижение уровня белка обычно отражает нарушение белково-синтетической функции печени.
2. Изменение состава глобулинов (высокий уровень α2- и особенно β-глобулинов) - может отмечаться при билиарном циррозе печени и служит дифференциальным признаком отличия этого вида цирроза от других.
|
3. Диспротеинемия развивается при синтезе в печени качественно измененных глобулинов (парапротеинов - макроглобулинов, криоглобулинов).
4. Нарушение метаболизма аминокислот возникает при тяжелых поражениях печени и приводит к повышению уровня свободных аминокислот в крови и моче (аминоацидемия, аминоацидурия). При фульминантном гепатите отмечается генерализованная аминоацидурия с преимущественной экскрецией цистина и тирозина, что является прогностически неблагоприятным признаком.
5. Геморрагический синдром развивается вследствие нарушения синтеза факторов свертывания и ингибиторов коагуляции и фибринолиза (см. выше раздел 18.1.3).
6. Увеличение остаточного азота и аммиака в крови обнаруживается при нарушении синтеза мочевины (показатель тяжелой печеночной недостаточности).
7. Повышение содержания в крови ряда ферментов (аминотрансфераз, γ-глутамилтранспептидазы и др.) Наибольшее диагностическое значение имеет определение в сыворотке крови активности аминотрансфераз - АлАТ и АсАТ. Их активность является наиболее надежным показателем цитолитического процесса при поражении печени.
|
Из маркеров холестаза (экскреторные ферменты) наибольшее клиническое значение приобретает определение в крови активности щелочной фосфатазы. Источниками этого фермента, кроме печени, являются костная ткань, кишечник, плацента, однако главным выделительным органом является печень. Поэтому повышение активности щелочной фосфатазы является важным показателем нарушения желчеоттока (холестаза). Наиболее высокая гиперферментемия регистрируется при подпеченочной желтухе и билиарном циррозе. При остром вирусном гепатите уровень щелочной фосфатазы в сыворотке крови обычно либо нормальный, либо повышается до умеренных значений. Диагностическая ценность определения активности изоферментов данного фермента возрастает в связи с тем, что высокий уровень его активности может указывать на возможность опухолей различной локализации.
Нарушение жирового обмена.
Жировой обмен при патологии печени характеризуется:
1) нарушением расщепления и всасывания жиров пищи в кишечнике, что связано с дефицитом желчных кислот при патологии желчеобразования и желчевыделения;
2) нарушением синтеза и окисления триацилглицеролов, фосфолипидов, липопротеинов, холестерина;
3) увеличением образования кетоновых тел.
В патогенезе жировой дистрофии печени можно выделить следующие основные механизмы:
а) поступление жира в печень;
б) снижение синтеза фосфолипидов и повышение образования триацилглицеролов из жирных кислот;
в) снижение окисления жирных кислот и липолиза;
|
г) нарушением выхода жира из печени вследствие пониженного образования липопротеинов очень низкой плотности (ЛПОНП - основная транспортная форма удаления триацилглицеролов из печени) или недостатка продукции липокаина поджелудочной железой.
Гепатиты и циррозы нередко сопровождаются снижением образования этерифицированного холестерина или уменьшением общего его количества в крови, нарушением синтеза и окисления холестерина, выведения его с желчью. Гиперхолестеринемия при механической желтухе возникает в результате поступления холестерина в составе желчи в кровь, а также за счет нарушения синтеза желчных кислот из холестерина.
Нарушение обмена гормонов.
Нарушение обмена гормонов и биологически активных веществ при патологии печени проявляется в изменении:
а) синтеза гормонов (из фенилаланина образуется тирозин - предшественник тироксина, трийодтиронина, катехоламинов), транспортных белков (транскортина, связывающего 90% глюкокортикоидов);
б) инактивации гормонов (конъюгации стероидных гормонов с глюкуроновой и серной кислотами, ферментативного окисления катехоламинов под влиянием аминооксидаз, расщепления инсулина инсулиназой);
в) инактивации биологически активных веществ (окислительного дезаминирования серотонина и гистамина). Поражение печени и нарушение инактивации таких гормонов, как инсулин, тироксин, кортикостероиды, андрогены, эстрогены ведет к изменению их содержания в крови и развитию соответствующей эндокринной патологии. Уменьшение дезаминирования БАВ может усугубить клинические проявления аллергии при патологии печени.
Нарушение обмена витаминов.
Нарушение обмена витаминов при патологии печени характеризуется:
а) уменьшением всасывания жирорастворимых витаминов (ретинола, эргокальциферола, токоферола и др.) в результате нарушения желчевыделительной функции печени;
б) нарушением синтеза витаминов и образования активных форм (ретинола из каротина, активных форм витамина В6 и др.);
в) нарушением депонирования витаминов (цианокобаламина, фолиевой, никотиновой кислот и др.) и их экскреции. В результате нарушения обмена витаминов многие патологические процессы в печени могут сопровождаться гиповитаминозами.
|
НАРУШЕНИЕ ЖЕЛЧЕОБРАЗОВАТЕЛЬНОЙ И ЖЕЛЧЕВЫДЕЛИТЕЛЬНОЙ (ЭКСКРЕТОРНОЙ) ФУНКЦИИ ПЕЧЕНИ
Гепатоциты секретируют желчь, в состав которой входят желчные кислоты, холестерин, фосфолипиды, жирные кислоты, желчные пигменты, муцин, вода и другие вещества.
Печень принимает участие в синтезе, ме
таболизме и экскреции желчных пигментов (рис. 18-2). В звездчатых эндотелиоцитах печени, макрофагах костного мозга, селезенки из гема разрушенных эритроцитов образуется под влиянием фермента гемоксигеназы биливердин, который при участии фермента биливердинредуктазы превращается в билирубин (неконъюгированный, свободный, непрямой); в крови он связывается с альбумином, образуя нерас-
|
Желтуха (icterus) -
симптомокомплекс,
характеризующийся желтой окраской
кожи, склер, более глубоко расположенных
тканей и
сопровождающийся
повышенной концентрацией желчных
компонентов в сыворотке крови и в
некоторых биологических жидкостях.
Видимая желтуха появляется при
гипербилирубинемии более 35 мкмоль/л.
Принято различать билирубинофильные
и билирубинофобные ткани. Кожа, слизистые
оболочки и внутренняя стенка кровеносных
сосудов окрашиваются наиболее сильно.

Различают три типа желтухи: надпеченочную, печеночную и подпеченочную. Гипербилирубинемия отмечается во всех случаях.
Надпеченочная (гемолитическая) желтуха, не связанная с поражением печени, возникает в связи с повышенным гемолизом эритроцитов и нарушением метаболизма билирубина.
О сновными
признаками этой
желтухи являются повышение уровня
билирубина преимущественно за счет
неконъюгированной фракции, отсутствие
билирубина в мочемолизе уровень
билирубина в сыворотке крови повышается
лишь в 2-3 раза (40-60 мкмоль/л) и редко
достигает 100 мкмоль/л.
сновными
признаками этой
желтухи являются повышение уровня
билирубина преимущественно за счет
неконъюгированной фракции, отсутствие
билирубина в мочемолизе уровень
билирубина в сыворотке крови повышается
лишь в 2-3 раза (40-60 мкмоль/л) и редко
достигает 100 мкмоль/л.
П еченочная
желтуха (паренхиматозная или гепатоцеллюлярная)
развивается при острых и хронических
заболеваниях печени любой этиологии
(вирусной, алкогольной, аутоиммунной),
а также при тяжело протекающих инфекциях
(тифы, малярия, острая пневмония), сепсисе,
отравлениях грибами, фосфором, хлороформом
и другими ядами.
еченочная
желтуха (паренхиматозная или гепатоцеллюлярная)
развивается при острых и хронических
заболеваниях печени любой этиологии
(вирусной, алкогольной, аутоиммунной),
а также при тяжело протекающих инфекциях
(тифы, малярия, острая пневмония), сепсисе,
отравлениях грибами, фосфором, хлороформом
и другими ядами.
При печеночно-клеточной желтухе имеет место комплексное нарушение функций печени, касающееся как метаболизма, так и
транспорта билирубина. В ее основе лежит повреждение функции и структуры гепатоцитов - цитолитический синдром, приводящий к печеночно-клеточной недостаточности.
Холестатическая желтуха (внутрипеченочный холестаз) может наблюдаться как самостоятельное явление или чаще осложняет цитолитический синдром. Холестаз может проявляться как на уровне гепатоцита, когда нарушается метаболизм компонентов желчи, так и на уровне желчных ходов, при этом имеется билирубинемия, а выделение уробилиновых соединений с мочой и калом снижено.
Энзимопатические желтухи обусловлены нарушением метаболизма билирубина в гепатоцитах. Речь идет о парциальной форме печеночной недостаточности, связанной с уменьшением или невозможностью синтеза ферментов, участвующих в пигментном обмене. По происхождению эти желтухи, как правило, наследственные.
В зависимости от механизма развития выделяют следующие формы желтух:
«Ядерная» желтуха - тяжелая форма желтухи новорожденных, при которой желчные пигменты и дегенеративные изменения обнаруживают в ядрах больших полушарий и стволах головного мозга (свободный билирубин, не включенный в связь с альбумином, проникает через гематоэнцефалический барьер и окрашивает ядра головного мозга - отсюда термин «ядерная» желтуха). Данная желтуха характеризуется следующим: у новорожденных на 3-6 день жизни исчезают спинальные рефлексы, отмечается гипертонус мышц туловища, резкий плач, сонливость, беспокойные движения конечностей, судороги, нарушение дыхания, может наступить его остановка и смерть. Если ребенок выживает, то могут развиться глухота, параличи, отставание умственного развития.
Подпеченочная желтуха (механическая или обструктивная) развивается при возникновении препятствия току желчи по внепеченочным желчным протокам.
Причинами возникновения являются:
а) обтурация печеночного и общего желчного протоков камнем, паразитами, опухолью;
б) сдавление желчных протоков опухолью близлежащих органов, кистами;
в) сужение желчных протоков послеоперационными рубцами, спайками;
г) дискинезия желчного пузыря в результате нарушения иннервации.
При подпеченочной желтухе наблюдаются болевой синдром, тошнота, рвота, расстройства стула. Длительный холестаз сопровождается увеличением печени, что зависит от переполнения ее застойной желчью и увеличения массы печеночной ткани. В начале развития механической желтухи печеночные клетки еще продолжают вырабатывать желчь, но отток ее по обычным путям нарушен, и она изливается в лимфатические щели, попадая оттуда в кровь. В крови повышается в основном количество связанного билирубина. Выделение уробилина с мочой отсутствует, выделение стеркобилина с калом понижено или незначительно. В крови содержатся все составные части желчи, в том числе и желчные кислоты, приводящие к развитию холемии. Кроме того, для данного вида желтухи характерна ахолия, причиной которой является стойкое нарушение выведения желчи по желчным капиллярам (что приводит к внутрипеченочному холестазу), протокам и из желчного пузыря.
|
С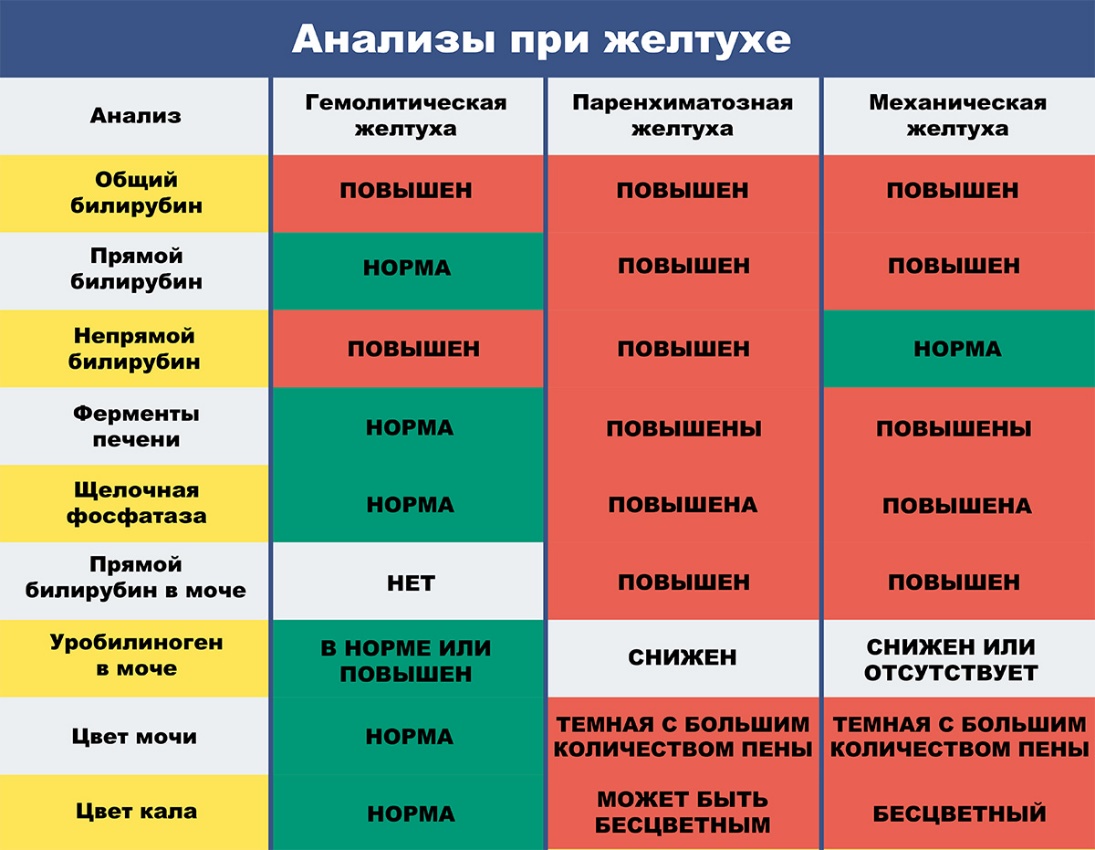 индром
ахолии - состояние, характеризующееся
значительным уменьшением или прекращением
поступления желчи в кишечник, сочетающееся
с нарушением полостного и мембранного
пищеварения.
индром
ахолии - состояние, характеризующееся
значительным уменьшением или прекращением
поступления желчи в кишечник, сочетающееся
с нарушением полостного и мембранного
пищеварения.
При этом синдроме наблюдаются:
а) стеаторея (потеря организмом жиров с калом в результате нарушения эмульгирования и усвоения жира в кишечнике из-за дефицита желчи);
б) дисбактериоз;
в) кишечная аутоинфекция и интоксикация вследствие выпадения бактерицидного действия желчи, что способствует активации процессов гниения и брожения в кишечнике и развитию метеоризма;
г) дефицит жирорастворимых витаминов (А, Д, Е, К), приводящий к нарушению сумеречного зрения, деминерализации костей с развитием остеомаляции и переломов, снижению эффективности системы антиоксидантной защиты тканей, развитию геморрагического синдрома;
д) обесцвеченный кал вследствие снижения или отсутствия желчи в кишечнике.
Желчекаменная болезнь - одно из наиболее распространенных заболеваний, занимающее третье место после сердечно-сосудистой патологии и сахарного диабета. В России распространенность этого заболевания колеблется в пределах 3-12%.
По химическому составу выделяют три типа желчных камней: холестериновые (содержание холестерина 79% и выше), черные пигментные и коричневые пигментные. Холестериновые и черные пигментные камни формируются главным образом в желчном пузыре, коричневые - в желчных протоках. В России чаще встречаются холестериновые камни (80-90%).
Выделяют 4 основные группы факторов, принимающих участие в образовании холестериновых камней:
1) способствующие насыщению желчи холестерином;
2) способствующие осаждению холестерина;
3) вызывающие нарушение функций желчного пузыря;
4) приводящие к нарушению энтерогепатической циркуляции желчных кислот.
Факторы, способствующие насыщению желчи холестерином:
• возраст (с возрастом повышается содержание холестерина в желчи;
• пол (женщины болеют желчекаменной болезнью в 3-4 раза чаще, чем мужчины). Половые различия связывают с гормональным фоном. Холелитиаз нередко встречается у повторно рожавших женщин. Во время беременности страдает эвакуаторная функция желчного пузыря, что в последующем приводит к образованию желчных камней;
• наследственность (риск образования желчных камней в 2-4 раза выше у лиц, родственники которых страдают желчекаменной болезнью;
• ожирение (увеличивается синтез и экскреция холестерина);
• питание (пища с высоким содержанием холестерина, рафинированные углеводы). Считается, что употребление кофе по 2-3 чашки в день уменьшает риск образования желчных камней;
• лекарственные препараты (эстрогены, оральные контрацептивы и др.);
• болезни печени. Высказывается мнение, что лица с HbsAg имеют риск образования желчных камней.
Факторы, способствующие осаждению холестерина:
• белки желчи (наибольшее значение имеет муцин-гликопротеиновый гель - N-аминопептидаза, иммуноглобулины, фосфолипаза С и др.);
• билирубинаткальция. В центре холестериновых камней находится билирубин, и, по-видимому, кристаллы холестерина осаждаются в желчном пузыре на белково-пигментные комплексы.
Факторы, приводящие к нарушению основных функций желчного пузыря (сокращение, всасывание, секреция). Нарушение опорожнения желчного пузыря, что наблюдается при метеоризме, беременности, уменьшении чувствительности и числа рецепторов к холецистокинину, метионину и др., которые являются стимуляторами двигательной активности. Установлено, что с возрастом снижается чувствительность рецепторов желчного пузыря к стимуляторам (холецистокинину). Сократительную функцию желчного пузыря снижают соматостатин, атропин, желчные кислоты и др. средства.
Факторы, приводящие к нарушению энтерогепатической циркуляции желчных кислот:
• заболевания терминального отдела тонкой кишки;
• резекция подвздошной кишки;
• заболевания тонкой кишки с тяжелым нарушением всасывания (например, глютеновая энтеропатия), а также резекция тонкой кишки с нарушением всех основных видов обмена и всасывания желчных кислот;
• желчные свищи (способствуют массивной потере желчных кислот).
|
