
- •Лекарственные формы для инъекций
- •Оглавление
- •Контрольные вопросы
- •1. Общая характеристика лекарственных форм для инъекций
- •3. Технологическая схема получения ампулированных лекарственных форм
- •4. Изготовление ампул
- •Стеклодрота
- •Получение безвакуумных ампул
- •5. Подготовка ампул к наполнению
- •Мойки ампул
- •6. Получение и подготовка растворителя
- •Через мембрану
- •7. Проблема исходных лекарственных и вспомогательных веществ
- •8. Дополнительная подготовка лекарственных и вспомогательных веществ
- •1) Очистке от химических примесей
- •2) Очистке от пирогенных веществ
- •9. Изотонирование
- •10. Стабилизация растворов
- •Факторы, влияющие на гидролиз солей
- •Гидролиз солей сильных оснований и слабых кислот
- •Гидролиз солей сильных кислот и слабых оснований
- •Гидролиз солей слабых кислот и слабых оснований
- •Гидролиз сложных эфиров
- •Гидролиз аминов кислот
- •Гидролиз сложных углеводов
- •Гидролиз сердечных гликозидов
- •Стабилизация растворов легкоокисляющихся веществ
- •Комплексообразователи (отрицательные катализаторы)
- •Пути предотвращения окислении лекарственных веществ
- •11. Введение консервантов
- •12. Стандартизация
- •13. Очистка растворов от механических включений
- •При помощи фильтра-грибка
- •14. Ампулирование
- •Раствора из капилляров
- •14. 3. Стерилизация
- •Термические методы стерилизации
- •Химические методы стерилизации
- •Стерилизации фильтрованием
- •Радиационная стерилизация
- •Стерилизация ультрафиолетовой радиацией
- •Ультразвуковая стерилизация
- •14.4. Оценка качества продукции и бракераж
- •1. Герметичность
- •2. Стерильность
- •3. Механические включения
- •Чистоты раствора в ампулах
- •4. Пирогенность
- •4.1.1. Биологический фармакопейный метод
- •15. Маркировка и упаковка
- •16. Регенерация растворов из отбракованных ампул
- •17. Общая аппаратурная схема производства
- •Инъекционных растворов
- •18. Медицинское стекло
- •19. Определение основных показателей качества медицинского стекла
- •20. Выщелачивание стекла
- •Действие на стекло кислых растворов
- •Действие на стекло щелочных растворов
- •Взаимодействие стекла с растворами солей
- •21. Особенности технологии некоторых растворов для инъекций
- •22. Получение угля активированного
- •23. Особенности изготовления масляных растворов в ампулах
- •24. Жировые эмульсии для парентералъного питания
- •Способы изготовления эмульсий:
- •Характеристика наиболее распространенных эмульсий
- •25. Суспензии для инъекционного введения
- •Характеристика наиболее распространенных суспензий для инъекционного введения
- •26. Инъекционные растворы с мечеными радиоактивными атомами
- •27. Порошки лиофильные во флаконах
- •28. Шприц-ампулы
- •29. Шприц-ручки
- •30. Одноразовые шприцы, заполненные лекарствами
- •31. Двойные ампулы
- •Обучающий контролирующий тест с эталонами ответов
- •8) Выберите требования gmp к персоналу, участвующему в производстве инъекционных лекарственных форм.
- •9) Подготовка ампул к наполнению включает операции:
- •Литература
- •Учебное издание
- •Лекарственные формы для инъекций
6. Получение и подготовка растворителя
Растворители для изготовления растворов для инъекций классифицируются на неводные и водные.
6.1. Неводные растворители обладают различной растворяющей способностью, антигидролизными, стабилизирующими, бактерицидными и другими свойствами. Их подразделяют на следующие группы:
Одноатомные спирты (этиловый и бензиловый спирт и др.).
Многоатомные спирты (пропиленгликоль, бутиленгликоль, глицерин и др.).
Эфиры (метиловый и этиловый эфиры олеиновой кислоты, бензилбензоат и др.).
Амиды (метилацетамид, диметилацетамид и др.).
Сульфоксиды и сульфоны (диметилсульфоксид, сульфолан и др.).
Жирные масла (оливковое, персиковое и др.).
К неводным растворителям предъявляются следующие требования:
высокая растворяющая способность;
фармакологическая индифферентность;
химическая совместимость;
устойчивость при хранении;
доступность и дешевизна;
прозрачность;
термостойкость;
температура кипения – более 100 оС (для проведения тепловой стерилизации;
температура замерзания – не выше +5 оС ;
биологическая совместимость по величине осмотическо го давления и значению рН среды;
вязкость и текучесть растворов не должны замедлять вcaсывание, затруднять фильтрование и наполнение ампул;
химическая чистота;
стабильность;
должны относиться к группе практически нетоксичных или малотоксичных веществ.
Спирты одно- и многоатомные. Применяются, в основном, как сорастворители (солюбилизаторы) в комплексе с водой для инъекций в качестве промежyтoчных растворителей. Так, например, спирт этиловый применяется для растворения некоторых противоопухолевых препаратов, нерастворимых ни воде; ни в маслах. При этом лекарственные вещества растворяют в небольшом количестве этанола, смешивают с оливковым маслом (получается эмульсия), затем спирт отгоняют под вакуумом и получают масляный раствор. Кроме того, этанол в концентрации от 2 до 3% применяется для улучшения растворимости эризимина, конваллотоксина, строфантина К. Глицерин растворяется в воде и этаноле, используется в концентрации до 30%. Смесь этанола и глицерина служит растворителем для получения 0,02% раствора целанида. ПЭГ-100-600 растворяет легкогидролизующиеся вещества. Пропиленгликоль смешивается с водой и этанолом и применяется в этой смеси в концентрации до 60% в качестве растворителя сердечных гликозидов, антибиотиков, витаминов А и Д. Спирт поливиниловый рекомендован как солю6илизатор и стабилизатор для водных суспензий. Сорбит и маннит в концентрации 60% в воде предложены для получения растворов легкогидролизующихся лекарственных веществ.
Простые и сложные эфиры. Метиловый и этиловый эфиры олеиновой кислоты, бензилбензоат применяются для улучшения растворимости гормонов и сердечных гликозидов. Heкoтopыe из них используются как заменители масла и являются при этом менее вязким растворителями, способствуют более быстрому рассасыванию лекарственных препаратов.
Амиды. N1-N – диметиламид, N-β – оксиэтиллактамид, метилацетамид, диметилацетамид, добавленные к воде в концентрации 10-50%, применяются для изготовления стабильных растворов антибиотиков.
Сульфоксиды и сульфоны. Высокую растворяющую способность имеют диметилсульфоксид и сульфолан (тетраметиленсульфон). Они обладают незначительной токсичностью и смешиваются почти со всеми растворителями.
Масла жирные. Для инъекций применяют маловязкие, невысыхающие масла, легкопроходимые через узкий канал иглы. По ГФ XI издания для изготовления инъекционных растворов разрешено применять масла: миндальное, персиковое, а по техническим условиям и оливковое масло. За рубежом применяют соевое, арахисовое, кунжутное, подсолнечное, хлопковое и кукурузное масла высокой степени очистки. Важным требованием к ним является отсутствие влаги, так как при наличии воды находящиеся в маслах липазы вызывают ферментативный гидролиз триглицеридов и фосфолипидов с образованием свободных жирных кислот. Последние, в свою очередь, подвержены радикально-цепному окислению, в результате которого в масле образуются гидропероксиды, пероксиды, свободные радикалы и другие реакционноспособные соединения. Образующиеся продукты гидролиза могут взаимодействовать со многими лекарственными и вспомогательными веществами, изменяя их свойства. Тепловая стерилизация ускоряет эти процессы. В безводной среде гибель микроорганизмов происходит не за счет гидролиза белков клеточной оболочки, а под действием пиролитического разложения белка при температуре, более высокой, чем режим стерилизации водных paстворов. Многие лекарственные вещества не являются термостойкими, поэтому масла стерилизуют отдельно в суховоздушных стерилизаторах. В полуохлажденном масле растворяют лекарственное вещество, раствор фильтруют под давлением, наполняют ампулы, шприцевым способом, запаивают и вновь стерилизуют паром под давлением при 110 оС 30 минут.
6.2. Смешанные растворители – это смеси растворителей, обладающие лучшей растворяющей способностью, чем их отдельные компоненты. Такое явление названо сорастворением, а отдельные компоненты – сорастворителями.
Смешанные растворители применяются для растворения веществ, нерастворимых в индивидуальных растворителях. Примерами смешанных растворителей могут служить:
1. Смесь воды с глицерином.
2. Смесь воды с пропиленгликолем.
3. Смесь воды, спирта и глицерина.
4. Смесь миндального или персикового масла с бензилбензоатом и др.
6.3. Вода для инъекций. Качество воды для инъекций регламентируется ФС 42-26-20-97, согласно которой она может быть получена методами дистилляции и обратного осмоса.
Вода для инъекций должна выдерживать испытания, предъявляемые к воде очищенной, кроме того, должна быть апирогенной.
Получение воды, для инъекций складывается из следующих операций:
ВР-4.1. Подготовка воды
ВР-4.2. Дистилляция воды (Обратный осмос)
ВР-4.3. Контроль качества воды для инъекций
Подготовка воды перед дистилляцией является ответственной операцией, т.к. удаление из воды солей, ПАВ и других соединений уменьшает пеноо6разование и, следовательно, выделение воды в паровую фазу. Кроме того, снижается образование накипи и увеличивается срок службы дистиллятора. Очистка воды способствует удалению многих микроорганизмов и пирогенных веществ.
Природная вода – это слабый раствор солей (Na+: Са2+, Mg2+, Fe3+, CI-, SO42-, РО4 2- , CO3 2-) и др. соединений.
Подготовка воды включает осаждение кальция и магния гидрокарбонатов с помощью кальция гидроксида и осаждение кальция и магния сульфатов и хлоридов-натрия карбонатом. Для коагуляции коллоидных примесей применяют аммоний сульфат или квасцы алюмокалиевые, которые также связывают и аммиак.
Многие органические вещества и микроорганизмы разрушаются обработкой калия перманганатом. Но наиболее полная очистка от примесей осуществляется с помощь следующих способов:
1) Ионный обмен
2) Электродиализ
3) Ультрафильтрация
4) Испарение через мембрану
Ионный обмен осуществляется, с помощью специальных ионообменных смол-ионитов. Иониты-сетчатые полимеры разной степени сшивки, гелевой или микропористой структуры, ковалентносвязанные с ионогенными группами. Диссоциация этих групп в воде или растворах дает ионную пару – фиксированный на полимере ион и подвижный противоион, который обменивается на ионы одноименного заряда. Иониты подразделяются на:
1) катиониты – смолы, содержащие кислую карбоксильную или сульфоновую группы, которые способны обменивать ион водорода на ионы щелочных и щелочноземельных металлов;
2) аниониты – продукты полимеризации аминов с формальдегидом, способные обменивать гидроксил (ОН-)-ион на анионы (CI1-,SO4 2- и др.).
Процесс ионного обмена последовательно на катионите и анионите протекает по следующей схеме (на примере кальция хлорида):
2
 К-Н
+ CaCI2
К2-Са
+2HCI
К-Н
+ CaCI2
К2-Са
+2HCI
А -ОН + HCI А-СI +Н2О,
Где: К – полимерный кaркаc катионита,
А – полимерный каркас анионита.
В фармацевтической промышленности для очистки воды используют сульфокатиониты КУ-l, КУ-2 и пористый КУ-23, а также слабоосновные аниониты марки ЭДЭ-1OП и сильноосновные аниониты АВ-17 и АВ-20 (более современные).
Процесс обессоливания с помощью ионообменных смол проводится в ионообменных колоннах (рис. 15): водопроводная вода пропускается сначала через катионит, затем через анионит (или наоборот). Насыщение ионообменников определяют по изменению реакции среды с помощью pH-метра. Перед регенерацией иониты взрыхляют обратным током водопроводной воды. Катиониты регенерируют в несколько приемов: 1, 0,7 и 4% раствором кислоты хлористоводородной. Перед сливом в канализацию кислоту из колонки нейтрализуют мраморной крошкой. Аниониты восстанавливаются в три приёма: 2,6; 1,6 и 0,8% раствором натрия гидроксида. После обработки растворами реагентов колонки промывают водой до заданного значения рН. Деминерализованная вода используется для мойки дрота, ампул; вспомогательных материалов и питания аквадистилляторов.
Распределение активности поглощения различных катионов на катионообменной колонке характеризуется определенной закономерностью и может быть представлена следующим рядом:
Са2+ > Mg2+ > K1+ > NH41+ > Na1+
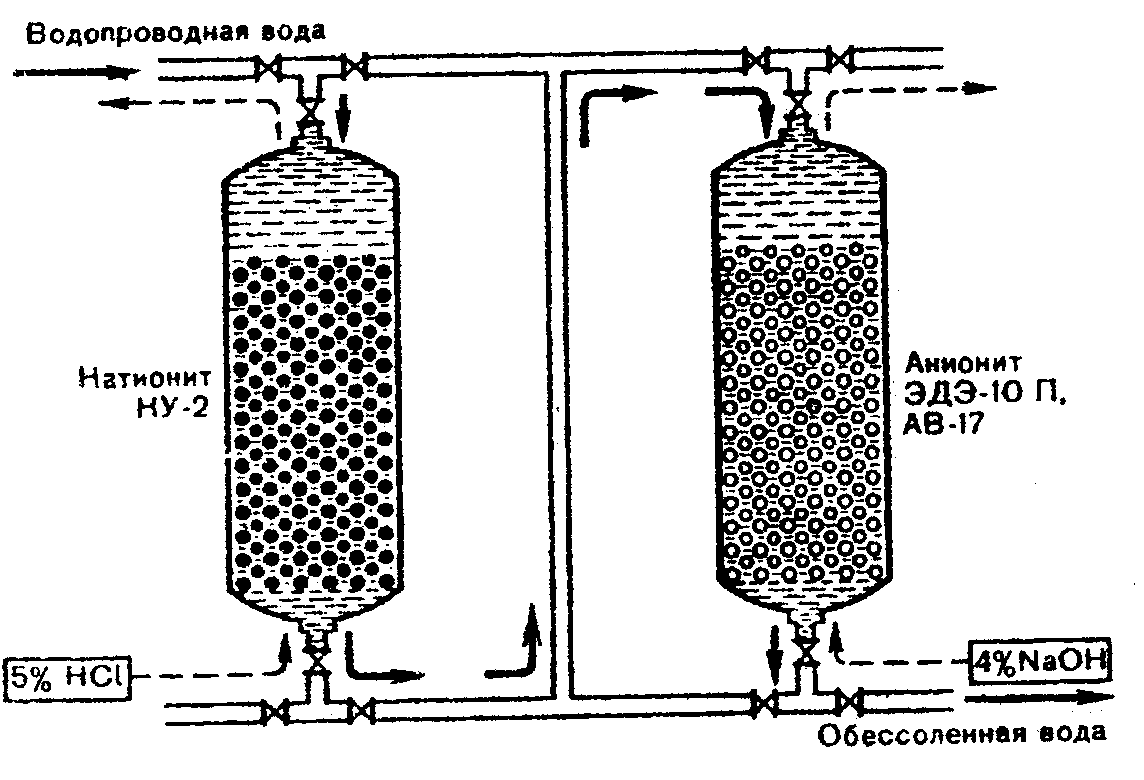
Рис. 15. Ионообменная установка
(В.И. Чуешов, 2002)
Так как ион натрия обладает наименьшей величиной подвижности, он первым начнет вытесняться в фильтрат более подвижными катионами магния и кальция. Появление в фильтрате ионов натрия указывает на то, что колонка отработала и требует регенерации.
Электродиализ – метод разделения, основанный на направленном движении ионов под влиянием постоянного тока в сочетании с селективным действием мембран. В качестве ионоо6менных мембран применяют: катионитовые, проницаемые только для катионов, и анионитовые, проницаемые только для анионов. Электродиализ проводят в электродиализных установках ЭДУ – 1000 производительностью 100 и 1000 м3/сут., схема которых представлена на рис. 16.
Жесткую воду прокачивают между 2-мя мембранами в электрическом поле. Ионы растворенных веществ, двигаясь к противоположно заряженным электродам, проходят через мембрану. Пресная вода, очищенная от солей, выводится из средней части установки.
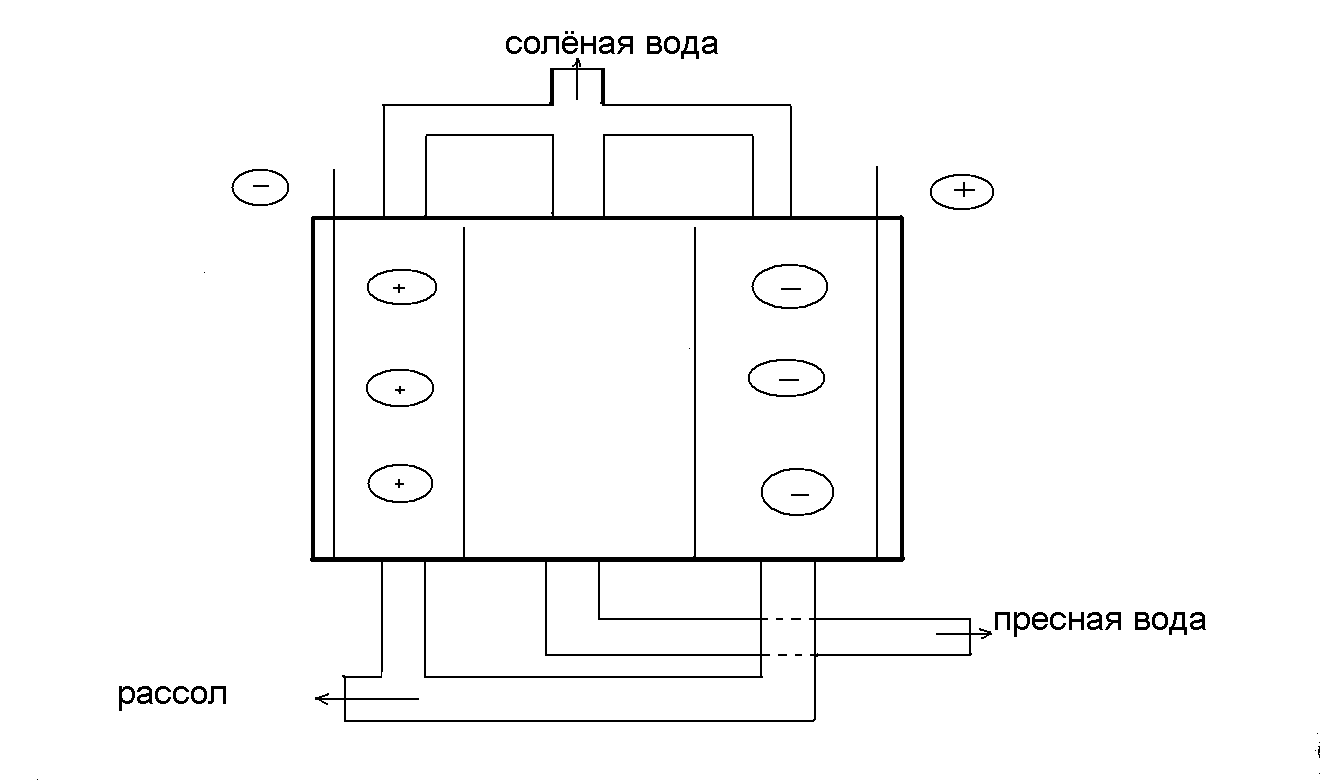
Рис. 16. Установка для электродиализа
Ультрафильтрация и диализ. Эти процессы основаны на различии скоростей диффузии веществ через полупроницаемую мембрану, разделяющую концентрированный и разбавленный растворы. Поэтому их используют для разделения веществ, значительно различающихся по молекулярным массам (ВМС, полимеров коллоидов и взвесей), а значит и по коэффициентам диффузии.
Испарение через мембрану. Данный метод основан на том, что растворитель проходит через мембрану и в виде пара удаляется с её поверхности в токе инертного газа или путем вакуумирования (рис.17). Затем пар переводится в жидкое состояние в конденсаторе-холодильнике. Для этой цели используют мембраны из целлофана, полиэтилена и ацетатцеллюлозы.
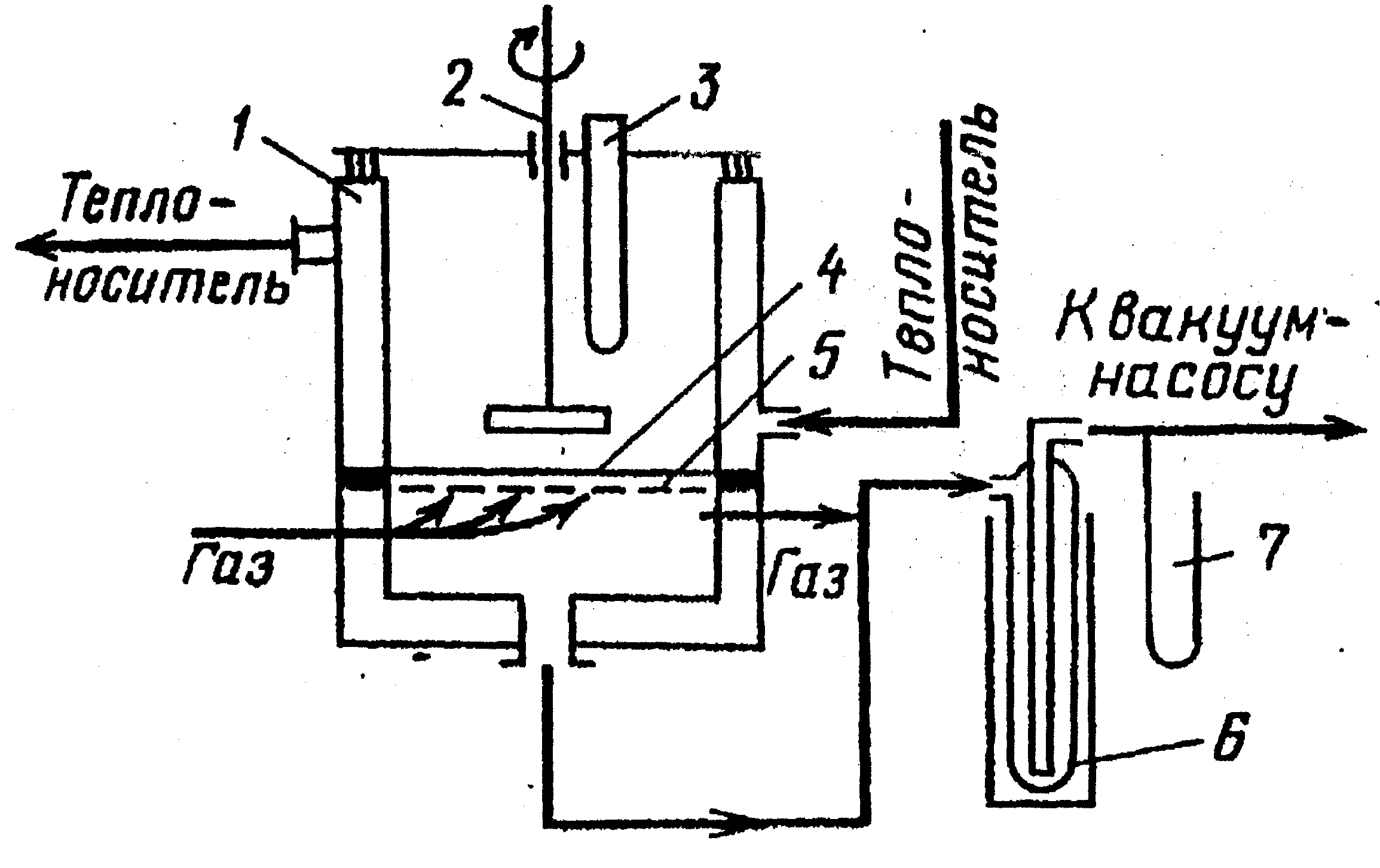
Рис. 17. Установка для разделения жидких смесей испарением
