
5 курс / Госпитальная педиатрия / Детская_эндокринология_Парамонова_Н_С_,_Жемойтяк_В
.pdf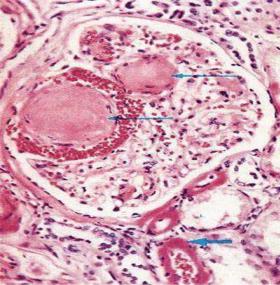
лосклероза, терминальная стадия которого характеризуется развитием хронической почечной недостаточности (ХПН).
Частота ДН зависит от длительности СД и выявляется у 40–45% пациентов с СД 1 типа.
Классификация ДН (формулировка диагноза):
1.Стадия микроальбуминурии.
2.Стадия протеинурии с сохранной выделительной функцией почек.
3.Стадия ХПН.
1-я стадия – доклиническая, 2-я и 3-я – клинические. Большинство авторов маркером повреждения почек считают
внутриклубочковую гипертензию (гиперфильтрацию), клинически определяемую по повышению скорости клубочковой фильтрации (СКФ) более 140 мл/мин. Кроме того, считается информативным определение функционального почечного резерва (ФПР), под которым понимают способность почек отвечать приростом СКФ на воздействие определенного стимула (например, пероральной нагрузки белком).
Опасность ДН у пациентов с СД обусловлена:
медленным и постепенным развитием;
отсутствием клинических проявлений на ранних этапах;
высоким уровнем АД;
тяжелым состоянием при ХПН;
малоэффективным лечением на терминальных стадиях
ХПН.
Рисунок 1.3. – Диабетическая нефропатия
61
Доклинические стадии ДН:
1 стадия гиперфункции – гиперфильтрация, гипертрофия почек, нормоальбуминурия (<30 мг/сут.). Дебют СД.
2 стадия начальных структурных изменений – утолщение базальной мембраны клубочков, гиперфильтрация, нормоальбуминурия (<30 мг/сут.). Стаж 2–5 лет.
3 стадия микроальбуминурии – (МАУ) >30 мг/сут. Нормальная или умеренно повышенная СКФ. Стаж более 5 лет.
Клинические стадии:
4 стадия выраженной ДН – протеинурия, артериальная гипертензия, снижение СКФ, склероз 50–75% клубочков. Стаж более 10–15 лет.
5 стадия уремии – снижение СКФ <10 мл/мин, тотальный гломерулосклероз. Стаж более 10–15 лет.
Скрининг на ДН
Последовательность скрининга на ДН включает:
Если в общем анализе мочи белок не обнаружен – трехкратное обследование на микроальбуминурию (МАУ): 1 раз
–в 6–8-часовой порции мочи тест-полоской, при положительном результате – определение МАУ в суточной моче еще дважды с интервалом 3–4 недели.
Если МАУ выявлена однократно, констатируется интермиттирующая МАУ, если 2–3 раза – персистирующая МАУ. Если МАУ не обнаружена, а СКФ >150 мл/мин., повторить исследование МАУ через 3 месяца.
Дальнейшая тактика:
При обнаружении МАУ – лечение с последующим контролем.
При отсутствии МАУ – скрининг с вышеобозначенной кратностью.
Лечение МАУ:
1.Детям и подросткам с персистирующей МАУ и нормальным уровнем АД показано назначение ингибиторов АПФ (ренитек 5–10 мг/сут., рамиприл 2,5–5 мг/сут.) курсом не менее 3 месяцев. При достижении нормоальбуминурии лечение прекратить, контроль МАУ 1 раз в 3 месяца.
2.У пациентов с положительной динамикой снижения МАУ терапию продолжить до 6–9 месяцев. Контроль МАУ и АД.
62
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
3.У пациентов с отсутствием эффекта в течение 3 месяцев – повысить дозу ингибиторов АПФ в 1,5–2 раза.
Лечение протеинурии:
1.При протеинурии и нормальном АД показано длительное лечение ингибиторами АПФ в дозах, указанных для лечения МАУ, с перерывами до 1 месяца 1 раз в полгода.
2.При протеинурии и повышенном АД лечить дозами ингибиторов АПФ, позволяющими поддерживать АД в пределах возрастных нормативов.
3.При протеинурии ограничить суточное потребление белка до 0,8–0,6 г/сут. (40–60 г/сут.); при артериальной гипертензии – ограничить употребление поваренной соли. В диету ввести ежедневное употребление морской рыбы (скумбрия, треска).
При неэффективности ингибиторов АПФ – перевод на препараты – ингибиторы рецепторов к ангиотензину II (лазартан или козоар 25 мг/сут. при нормальном АД, до 50 мг/сут. при повышенном АД).
Диспансерное наблюдение при ДН включает контроль:
компенсации углеводного обмена, определение HbAlc 1 раз в 3 месяца;
контроль МАУ и протеинурии – 1 раз в 3 месяца;
СКФ – 1–2 раза в год;
креатинин, мочевина, общий белок, альбумин, липидограмма, электролиты (калий, натрий) – 1–2 раза в год;
контроль АД – ежедневно.
Диабетическая невропатия
Выявляется у 50% пациентов с диабетической невропатией. Поражается центральная и периферическая нервная система. Основные проявления периферической невропатии у детей –
боли в ногах и парестезии, болезненность мышц голеней, нарушение вибрационной, тактильной, температурной и болевой чувствительности.
Поражаются в первую очередь дистальные отделы нижних конечностей.
Клиническая классификация (Nathan D., 1993):
1. Симметричные нейропатии:
сенсорно-моторная периферическая невропатия;
63
автономная невропатия с преимущественным поражением сердечно-сосудистой, мочеполовой систем, желудочнокишечного тракта.
2. Очаговые (асимметричные) невропатии:
мононейропатия;
радикулопатия.
Основные проявления сенсорно-моторной периферической невропатии у детей – наличие болевого синдрома, парестезии, снижение сухожильных рефлексов. Реже отмечаются нарушения тактильной, температурной, болевой и вибрационной чувствительности.
Сердечно-сосудистая форма автономной невропатии протекает в виде тахикардии покоя и ортостатической гипотонии; же- лудочно-кишечная форма – в виде гастропареза и атонии толстой кишки. Наблюдаются раннее насыщение, тошнота, рвота, запор или диарея в ночное время, потеря веса. Мочеполовая форма автономной невропатии проявляется снижением чувства наполнения мочевого пузыря и позывов на мочеиспускание, урежением частоты мочеиспусканий и повышением риска развития инфекций.
Лечение
Перспективно назначение жирорастворимых форм витаминов группы В, биодоступность и эффективность которых выше по сравнению с водорастворимыми аналогами. Препараты: Мильгамма драже 100, Бенфогамма. Детям с 7 до 10 лет назначать по 1–2 др./сут., старше 10 лет – 3 др./сут. Курс – 6 недель. Парентеральное внутримышечное введение показано при болевых формах невропатии.
Патогенетически показано применение препаратов на основе α-липоевой кислоты (тиоктацид, берлитион).
Механизм их действия:
защита от действия свободных радикалов;
снижение образования конечных продуктов гликирования;
участие в регуляции липидного обмена;
гепатопротекторный эффект;
дезинтоксикационное действие;
снижение интенсивности болевого синдрома. Расчет дозы тиоктацида – 10–15 мг/кг/сут. Курс – 3 месяца.
64
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Рекомендуемая схема введения: начать с внутривенного капельного введения тиоктацида в течение 10 дней, затем перейти на пероральный прием препарата; курс лечения – 3 месяца. Необходимо помнить, что липоевая кислота снижает потребность в инсулине, поэтому для профилактики гипогликемии инфузии проводить после приема пищи (завтрака).
Диабетическая хейропатия
Симптомокомплекс выявляется у 15–30% подростков с СД 1 типа. Вариант диабетической остеоартропатии. Это первый предвестник осложнений, обусловленных хронической гипергликемией. Яркий признак – «рука праведника». Чаще нарушается разгибание мизинцев, но могут быть поражены все пальцы и суставы.
При тяжелом течении СД могут формироваться осложнения в виде симптомокомплексов, свидетельствующих о длительной декомпенсации заболевания. К ним относятся синдромы Мориака и Сомоджи.
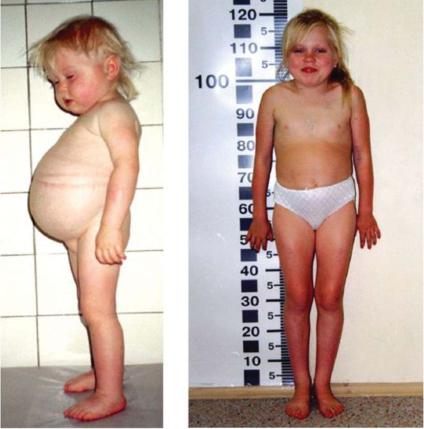
Синдром Мориака
Рисунок 1.4. – Синдром Мориака
65
Он включает:
задержку физического (снижение скорости роста) и полового развития;
избыточное отложение подкожно-жировой клетчатки на туловище, лице;
гепатомегалию.
Лечение данного синдрома сводится к более строгому контролю и коррекции дозы инсулина, а также соблюдению диеты.
Синдром Сомоджи (синдром хронической передо-зировки инсулина)
При данной патологии индуцированная инсулином гипогликемия приводит к повышению уровня контринсулярных гормонов (адреналин, глюкагон, гормон роста, глюкокортикостероиды) и ответной «рикошетной» гипергликемии. Если причина гипергликемии не уточняется, то увеличение дозы инсулина для коррекции гипергликемии приводит к еще более выраженной гипергликемии.
Для пациентов с синдромом Сомоджи характерно:
синдром передозировки инсулина – следует думать, если на фоне гипергликемии и положительного ацетона бывают гипогликемии;
суточная доза инсулина обычно выше средней;
темпы роста нормальные, масса тела нормальная или повышенная;
наблюдаются резкие колебания гликемии в течение суток;
гликированный гемоглобин умеренно повышен;
без высокой глюкозурии может появляться ацетон в моче;
повышение суточной дозы инсулина усиливает декомпенсацию углеводного обмена;
интеркуррентные заболевания и снижение суточной дозы инсулина улучшают показатели углеводного обмена.
Модификация дозы инсулина в зависимости от уровня гликемии
Перед каждой иньекцией инсулина пациенту с СД положено определять уровень сахара крови в капиллярной крови. При его повышении производится коррекция дозы короткодействующего инсулина следующим образом.
66
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Таблица 1.9. – Коррекция дозы инсулина при гипергликемии
|
Склонность |
Исходный уровень |
Доза инсулина на |
|
Возраст |
к гипогли- |
гликемии |
каждые «лишние» |
|
|
кемии |
(ммоль/л) |
3 ммоль/л |
|
Дошкольники |
|
выше 10,0–11,1 |
не более 0,25 ЕД |
|
Школьники |
есть |
выше 10,0–11,1 |
0,5–1,0 ЕД |
|
|
нет |
выше 8,0 |
||
|
|
|||
Подростки и |
есть |
выше 10,0–11,1 |
1,0–2,0 ЕД |
|
взрослые |
нет |
выше 8,0 |
||
|
Таблица 1.10. – Время приема пищи и коррекция дозы инсулина
Гликемия |
Время инъекции |
Изменения дозы инсулина |
(ммоль/л) |
(мин. до еды) |
(Актрапид) |
<4,0 |
15 |
-2 ЕД |
4,0–8,0 |
30 |
Без изменений |
8,0–10,0 |
45 |
Без изменений |
>10,0 |
60 |
+2 ЕД |
>13,3 |
60 |
+2 ЕД |
Модификация дозы инсулина при наличии ацетонурии и интеркуррентных заболеваний
Анализ мочи на ацетон проводится в следующих случаях:
повышение уровня гликемии выше 15 ммоль/л в течение 24 часов или при ухудшении самочувствия;
во время болезни;
при тошноте и рвоте;
перед усиленной физической нагрузкой.
При каждом инфекционном заболевании у детей с СД
потребность в инсулине возрастает. Это объясняется развивающейся относительной тканевой резистентностью к инсулину и повышенным выделением гормонов стресса. Необходим более частый контроль углеводного обмена. Быстро нарастающая гипергликемия должна быть корригирована увеличением дозы инсулина короткого действия и введением дополнительных инъек-
ций. В большинстве случаев дозу инсулина повышают на 20%
от обычной.
При тяжелой рвоте дозу инсулина снижают на 50%, при необходимости корригируют ее дополнительными инъекциями пролонгированного инсулина. Если рвота не прекращается, если
67
больной ребенок отказывается от питья, необходима госпитализация для лечения электролитных нарушений и эксикоза.
Острые осложнения сахарного диабета у детей
Острые осложнения делятся на 2 группы:
гипогликемические состояния, вплоть до комы
осложнения, протекающие на фоне гипергликемии:
ξдиабетический кетоацидоз;
ξгипергликемический гиперосмолярный статус (гиперосмолярная некетоацидотическая кома) критериями которого являются: концентрация глюкозы в плазме >33,3 ммоль/л; рH >7,3, бикарбонаты >15 ммоль/л; эффективная осмолярность в сыворотке крови >320 мосмоль/кг; нарушение сознания: ступор или кома; небольшая кетонурия, отсутствие или легкая кетонемия;
ξлактатацидоз: при молочнокислом варианте ДКА (лактатацидоз) у пациента могут преобладать резкие боли в области грудной клетки, в сердце, мышцах, животе. Быстро появляется и нарастает одышка, кетоз отсутствует или выражен
слабо, гипергликемия невыраженная (до 15–17 ммоль/л). К лактатацидозу приводит недостаточное кровоснабжение тканей.
Диабетический кетоацидоз
Диабетический кетоацидоз (ДКА) – определяется как ост-
рая диабетическая декомпенсация обмена веществ, проявляющаяся резким повышением уровня глюкозы и концентрации кетоновых тел в крови, появлением их в моче и развитием метаболического ацидоза, при различной степени нарушения сознания или без нее, требующая экстренной госпитализации пациента.
На сегодняшний день ДКА является тяжелым осложнением СД с высоким риском для жизни. ДКА может развиться у детей как с впервые выявленным сахарным диабетом (до 26% детей), так и у давно страдающих данной патологией (до 15% госпитализированных с СД).
ДКА – более 20% вновь выявленного диабета 1 типа, из них дети до 2 лет – более 50%. У детей младше 5 лет ДКА отличается более тяжелым течением.
Осложнения ДКА (в хронологическом порядке): гиповолемический шок, отек головного мозга, гипокалиемия, ДВС, инфекция.
68
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Исследования показали, что чем младше ребенок, тем ниже у него уровень С-пептида при выявлении СД. Наиболее стремительно ухудшается состояние у детей в возрасте до 2 лет. У них же чаще всего наблюдается запаздывание с постановкой правильного диагноза. В этом возрасте с ДКА начинается манифестация сахарного диабета у 71% детей.
Этиология
Все причины ДКА являются следствием острого, прогрессирующего недостатка инсулина и/или повышенной потребно-
сти в нем. Ими являются:
несвоевременная диагностика сахарного диабета;
неадекватное мониторирование и дозирование инсулина в период повышенной потребности в нем: любые острые и/или обострения хронических заболеваний, в том числе, инфекционные, хирургические вмешательства и травмы, тяжелый стресс, в том числе, психологический (особенно у подростков), пубертатный возраст, беременность;
пропуск или отмена инсулина самим пациентом (в том числе, с суицидальными целями), несоблюдение врачебных рекомендаций по инсулинотерапии и диете;
ошибки в назначении или введении дозы инсулина;
неисправности в системах введения инсулина (шприцручках, инсулиновых помпах);
недостаточный контроль (и самоконтроль) уровня глюкозы крови, недостаточное образование пациента/родителей в вопросах сахарного диабета;
длительная терапия антагонистами инсулина (глюкокортикоидами, диуретиками, гипотензивными средствами, половыми гормонами и др.).
Патогенез ДКА
ДКА является комплексным нарушением метаболизма. Основными его проявлениями являются гипергликемия, метаболический ацидоз и кетонемия с кетонурией.
Дефицит инсулина приводит к нарушению утилизации глюкозы тканями и гипергликемии. Внутриклеточный энергетический голод вызывает усиленную секрецию всех контринсулярных гормонов (в первую очередь, глюкагона и катехоламинов,
атакже кортизола и гормона роста), в результате чего усили-
69
ваются процессы гликогенолиза (распад гликогена до глюкозы) и глюконеогенеза: протеолиза с синтезом глюкозы из аминокислот, образующихся при распаде белков; активируется липолиз, что приводит к нарастанию уровеня свободных жирных кислот и глицерина. Все эти процессы способствует усилению продукции глюкозы и приводят к нарастанию гипергликемии. Утилизация же глюкозы тканями снижена как из-за дефицита инсулина, так и из-за инсулинорезистентности, развивающейся на фоне декомпенсации сахарного диабета.
Выраженная гипергликемия вызывает повышение осмоляр-
ности крови и внутриклеточную дегидратацию. А следствием усиления осмотического диуреза является внеклеточная дегид-
ратация, которая сопровождается тяжелыми электролитными нарушениями и может привести к гиповолемическому шоку и смерти пациента. Для ДКА характерно развитие гипертони-
ческого типа дегидратации.
Свободные жирные кислоты, образовавшиеся при активации липолиза, поступают в печень, где из них образуются кетоновые тела (кетогенез); в результате развивается кетонемия, которая еще больше нарастает из-за снижения утилизации кетоновых тел в тканях. Это приводит к кетонурии, которая сопровождается потерей катионов, т. е. усиленной экскрецией электролитов. Неконтролируемая продукция кетоновых тел обуславливает истощение щелочного резерва с падением уровня бикарбоната плазмы (НСО3-) и ростом дефицита оснований (BE), высоким анионным промежутком плазмы (АПП). Таким образом, накопление большого количества кетоновых тел является причиной развития метаболического ацидоза.
Дегидратация и гиповолемия приводят к снижению мозгового, почечного и периферического кровотока. Это приводит к гипоксии ЦНС и периферических тканей, развитию олиго- и анурии. Кетоацидотическая кома развивается, когда уровень бикарбонатов в сыворотке снижается до 10 ммоль/л. Гипоксия периферических тканей вызывает активацию в них анаэробного гликолиза и нарастание концентрации лактата (лактатацидоз), усиливающего тяжесть метаболических нарушений.
70
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
