
3 курс / Общая хирургия и оперативная хирургия / Хирургическая_анатомия_венечных_артерий
.pdfМы не будем здесь излагать усредненные данные по материалам литературы. На ша позиция в этом плане основана на сопоставлении эффективных коллатералей, функционирующих при тех или иных патологических состояниях, с материалами эм бриогенеза ВА. Согласно этим данным, наиболее постоянными и выраженными внутрисердечными анастомозами являются:
1)система сосудов Вьессена (в верхнем отделе передней стенки ПЖ) - межсистем ные анастомозы между передними желудочковыми ветвями правой ВА и ПМЖВ;
2)анастомозы между ветвью острого края (ВОК) правой ВА и ПМЖВ - по средней трети передней стенки ПЖ и правожелудочковой части верхушки сердца;
3)анастомозы в задней межжелудочковой борозде - межсистемные анастомозы между ОВ правой и левой ВА;
4)анастомозы на стенке предсердий - межсистемные анастомозы между длинны ми предсердными ветвями правой ВА и ОВ левой ВА;
5)анастомозы между ЗМЖВ и ПМЖВ в области верхушки сердца;
6)анастомозы между ЗМЖВ и ПМЖВ - септальные перфоранты в межжелудочко вой перегородке (межсистемные анастомозы - при правом типе доминантности кровообращения и внутрисистемные - при левовенечном типе доминантности).
Как свидетельствуют приведенные данные, большинство существующих анасто мозов представляют собой сохранившиеся межартериальные связи, формирующиеся еще при первоначальной закладке единого субэпикардиального сплетения. Исключе ние составляют только межсистемные связи, складывающиеся на поздних этапах формирования сердца (анастомозы между системами ЗМЖВ и ПМЖВ в области вер хушки сердца и межжелудочковой перегородки).
В норме, однако, анастомозы, представляющие собой остатки первично сложив шегося субэпикардиального сплетения, не функционируют. Широко развитая сеть разнообразных анастомозов (особенно этой последней группы) составляет тот мощ ный резерв, при помощи которого реализуется коллатеральное кровообращение при различных нарушениях кровоснабжения сердца. Это обнаруживается и при врож денном нарушении питания сердечной мышцы (при аномальном отхождении левой ВА от легочного ствола, например), и при приобретенной ее дисфункции (при ИБС, например), а также у больных с выраженной артериальной гипоксемией (при тетра де Фалло, например).
Несмотря на значительное количество работ, посвященных изучению различных сосудистых анастомозов в сердце (В.В.Огнев и др., 1954; С.П.Ильинский, 1962; С.В.Самойлова, 1970; И.Х.Рабкин и др., 1973; В.В. Кованое и Т.Н.Аникина, 1974; И.Х.Рабкин, 1974; Д. Г. Иоселиани, 1979; С.С.Михайлов, 1987), до настоящего вре мени отсутствуют точные данные об основных путях эффективного функционирова ния анастомозов. Между тем клиническое значение анастомозов определяется именно функциональными возможностями этих связей, в основе которых лежит их «адекват ность» (D. Lewin, 1974), эффективность (Д. Г. Иоселиани, 1979) или функциональная недостаточность (С. С. Михайлов, 1987).
Развитие функционально значимых коллатералей (от 200 до 300 мкм) при ИБС - достоверно установленный факт (И.Х.Рабкин и др., 1973; В.С.Савельев и др., 1975; Д.Г.Иоселиани, 1979; D.Lewin et al., 1983). Причем известно, что развитие конкрет ных путей коллатерального кровообращения в сердце определяется как локализацией стенозирующего процесса в ВА, так и расположением в сердце артериальных анасто мозов. Так, по данным Е. П. Мельмана и М. Г. Шевчука (1976), при стенозировании просвета ПМЖВ в верхней трети главную роль в коллатеральном кровообращении иг рают анастомозы на передней поверхности ЛЖ и верхушке сердца. При стенозе сред ней трети ПМЖВ значительного развития достигают анастомозы с ПВА на передней стенке ПЖ . При облитерации ОВ коллатеральное кровообращение осуществляется по расширенным анастомозам с ПМЖВ на переднебоковой стенке ЛЖ .
121
Исследованиями Д. Г. Иоселиани (1979) доказано, что существует связь между сис темами правой ВА и ПМЖВ. Автор констатирует и наличие внутрисистемных связей в пределах тех же ВА. О наличии связей между ветвями левой ВА сообщают также
И.X. Рабкин (1977) и С. С. Михайлов (1987).
Спрактической точки зрения, на наш взгляд, в основу оценки коллатерального рус ла должны быть положены признаки их «адекватности», основанные на должном пони мании механизмов их эффективного функционирования, поскольку простая констата ция наличия коллатералей не позволяет ответить на целый ряд важнейших вопросов.
Способны ли коллатерали защитить миокард при острой окклюзии сосуда? Их нали чие - признак достоверной защитимости миокарда или, наоборот, свидетельство тяже лых поражений? Каковы зоны распространения «адекватных» (коллатералей, обнару живаемых ангиокардиографически) коллатералей? Ответы на эти вопросы в литературе неоднозначны и нередко - взаимоисключающие. Мы полагаем, что ответы на эти вопро сы в первую очередь должны опираться на понимание механизмов формирования колла тералей между ВА. И если гемодинамические механизмы формирования коллатералей на сегодняшний день более или менее определены (давление в коллатералях, градиент давления, скорость кровотока и др.), то совершенно не конкретны данные, лежащие в ос нове понимания анатомического субстрата эффективных коллатералей и их эмбриональ ной обусловленности. Кроме того, тут, вероятно, следует вспомнить, что в стенке сердца анастомозы могут располагаться субэндокардиально, интрамиокардиально и субэпикардиально. По мнению Г. Г. Арабидзе и соавт. (1978), большая часть функционально зна чимых коллатералей расположена субэндокардиально и эндомурально (субэпикардиально). Недавно скрупулезными исследованиями М. Fujita и соавт. (1988) показано, что эф фективный кровоток осуществляется только анастомозами, расположенными субэпикардиально. Более того, в наиболее полной работе, посвященной коллатералям, показа но, что нативные коллатерали имеют в основном эпикардиальное происхождение (W. Schaper, 1971). Сейчас уже считается окончательно доказанным, что нативные кол латерали в ответ на острую и хроническую ишемию ремоделируются и обладают способ ностью к вазоконстрикции и вазодилатации (Т. Aversano et al., 1985; J. Schaper et al., 1993; M. Mansaray et al., 2000). Очень важно иметь в виду и такой факт, как различный потенциал коллатеральной защиты между отдельными субэпикардиальными стволами ВА. Как следует из наших данных, эмбриогенетически субэпикардиальные стволы ВА равнозначны и анатомически ответственны за равноценные участки миокарда. Отсюда равная ответственность каждого из них за адекватность кровоснабжения сердца. В осно ве наличия мощной коллатеральной защиты ПМЖВ или ветви острого края правой ВА лежит абсорбция исходно закладывающихся вокругартериальных, вокругбульбарных и бульбовентрикулярных колец первичного венечно-артериального сплетения, легко ре продуцируемых при возникновении необходимости в этом. Отсюда эффективность кол латералей между указанными сосудами. Исходя из нашего понимания того, что ряд вет вей, формирующихся из вокругжелудочковых колец и представляющих собой прокси мальные фрагменты веерообразно расходящихся дистально и поэтому несоединенных здесь колец, понятно, что ДВ, ОВ, ветвь тупого края и заднебоковая (левожелудочковая) ветвь такой защиты не имеют. Вернее, при богатейшей системе кровоснабжения сердца анастомозы между указанными сосудами, несомненно, существуют. Но они функцио нально недостаточны, и перечисление этих анастомозов вместе с эффективными анасто мозами является «лазейкой» для двусмысленности неверного толкования фактов. Пони мание этих данных важно не столько для понимания отсутствия эффективных коллате ралей между ДВ и ПМЖВ или ДВ и ВТК, сколько для того, чтобы знать, что обнаруже ние всех случаев со стенозированием ОВ, ДВ, ВТК или ствола левой ВА в силу анатоми ческого отсутствия адекватных коллатералей к ним является свидетельством необходи мости их васкуляризации. Поэтому понимание этого факта должно истолковываться как еще одно объективное анатомическое свидетельство в пользу обязательности полной реваскуляризации миокарда.
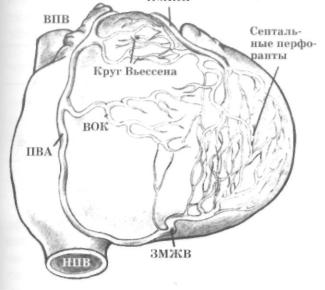
Приведенная нами система эмбриогенеза ВА объясняет существование эффек тивных коллатералей именно между ветвями правой ВА (через конусную артерию,
122
ПМЖВ |
артерию |
острого к р а я и другие ветви |
|||
|
п р а в о й |
ВА, |
о б р а з у ю щ и е |
ф е т а л ь н ы е |
|
|
круги Вьессена; рис . 68) и |
П М Ж В . В |
|||
|
первую очередь эти материал ы имеют |
||||
|
п е р в о с т е п е н н о е з н а ч е н и е |
при И Б С . |
|||
|
Эти |
данны е |
представляют |
интерес и |
|
|
д л я |
п о н и м а н и я анатомии |
и физиоло |
||
|
г и и |
а н о м а л ь н о г о о т х о ж д е н и я левой |
|||
ВА от ЛА . В этой связ и считаем умест н ы м подчеркнуть, что именно указан ные сосуды составляют основу вариа бельной анатомии ВА при пороках конотрункуса .
Сосуды у к а з а н н о й группы имеют объективную эмбриологическую базу для формирования соединения между П М Ж В и правой В А при тетраде Фалло. Более того, именно эти предбульбарные фрагменты фетального перитрункального кольца и составляют основу анатомии ВА при ОАЛА ПЖ или ТАЛА, выступая уже не в роли межкоронарных анасто мозов, а к а к полноценные ВА. Понима ние возможностей эффективного функ ционирования именно сосудов, образую щ и х фетальные венечно-артериальные круги, в этой связи трудно переоценить, поскольку здесь впервые акцентировано внимание на венечных сосудах, имею щ и х самостоятельное право на сущест
вование и играющих важную компенсирующую роль при целом ряде патологических состояний, требующих вспомогательной перфузии ишемизированных участков сердца.
Экстракардиалъные анастомозы
Экстракардиальные анастомозы делятся на анастомозы, соединяющие ВА с большим или малым кругом кровообращения, и анастомозы, расположенные по ходу магистраль ных сосудов (аорты, легочного ствола и полых вен), образующихся за счет vasa vasorum.
Среди э к с т р а к а р д и а л ь н ы х анастомозов наибольшее практическое значение имеют анастомозы, обеспечивающие связь с бронхиальными артериями . В 1966 г. L. Bjork при помощи посмертной ангиографии установил наличие коллатералей между ВА и легкими . К а к п о к а з а л и и с с л е д о в а н и я V. Bjork и L. Bjork (1965), F. I n t o n t i и С. Marchegiani (1965), бронхиальные коллатерали могут развиваться из системы ОВ
левой |
ВА, |
а т а к ж е из |
предсердных ветвей ВА (A. Moberg, |
1968). |
|
|
||
Важное |
п р а к т и ч е с к о е з н а ч е н и е э к с т р а к а р д и а л ь н ы е анастомозы приобретают в |
|||||||
группе |
ц и а н о т и ч е с к и х |
ВПС |
с о б е д н е н н ы м л е г о ч н ы м |
к р о в о т о к о м . Т а к , |
д о к а з а н о , |
|||
что бронхиально - венечные анастомоз ы существуют |
при |
тетраде |
Ф а л л о |
(R. Dabizzi |
||||
et al., |
1980; H.Zureikat, |
1980; |
S.Sharma et al., 1988). |
По |
д а н н ы м |
л и т е р а т у р ы , в |
||
среднем частота венечно - бронхиальны х анастомозов при тетраде Ф а л л о составляет 10% (табл. 4) . У ч и т ы в а я их к л и н и ч е с к о е значение , сегодня о ц е н к е коллатерально
го |
кровотока |
п р и |
ВПС |
п р и д а е т с я |
особое з н а ч е н и е |
(Е. Н. Рюмина |
и др., 1979; |
|||
Ю.Д.Волынский |
и др., |
1981; |
Ю.С.Петросян и |
др., 1990; |
A. La Porta et |
al., |
1979; |
|||
A. |
Bogers |
et al., |
1989; |
J. Kirklin et al., |
1981). |
|
|
|
|
|
|
Как |
известно, сосуды, |
осуществляющие |
окольное кровообращение |
при |
тетраде |
||||
Фалло и в ы п о л н я ю щ и е компенсаторные ф у н к ц и и до операции, могут оказаться источ-
123
|
|
|
|
Т а б л и ц а 4 |
|
Частота коронарно-бронхиальных коллатералей при тетраде Фалло |
|||||
|
|
|
|
||
Авторы |
Год публикации |
Число наблюдений |
|||
|
|
||||
абс. |
% |
||||
|
|
|
|||
|
|
|
|
|
|
L. Bjork |
1966 |
[57] |
5(60) |
8,3 |
|
R. Dabizzi et al. |
1980 |
[60] |
31(119) |
26,0 |
|
H. Zureikat |
1980 |
[131] |
4 (23) |
17,4 |
|
S. Sharma et al. |
1988 |
[118] |
11(330) |
3,3 |
|
|
|
|
|
|
|
В с е г о . . . |
|
|
51 (532) |
9,6 |
|
|
|
|
|
|
|
П р и м е ч а н и е . В скобках - общее число наблюдений.
ником серьезных интра- и послеоперационных осложнений (Ю.Д.Волынский и др., 1981; D.McGoon et al., 1975; J.Kirklin et al., 1981). Для предотвращения перегрузки сердца во время и после операции, а также для предупреждения большого артериовенозного сброса в области легочной артерии и, соответственно, развития «феномена ко ронарной кражи» с последующей ишемией миокарда (L. Bjork, 1966; S. Sharma etal., 1988), в случае принятия решения выполнить радикальную коррекцию порока, боль шие коллатеральные сосуды, впадающие в центральные отделы легочно-артериально го дерева (ЛАД) (при наличии таковых), должны быть перевязаны (D. McGoon et al., 1975). С другой стороны, поскольку терминальные ветви легочных артерий сообщают ся не со всеми бронхолегочными сегментами (S. Haworth and F. Macartney, 1979), пе ревязка коллатеральных сосудов, не соединенных с центральными отделами ЛАД, мо жет привести к гипоксии и инфаркту легкого (J.Kirklin et al., 1981). Остающиеся по сле операции крупные коллатеральные сосуды, не соединенные с центральными отде лами ЛАД, образуют обособленную систему кровоснабжения легких (участки легочной сосудистой секвестрации) (Ю.Д. Волынский и др., 1981), которые могут стать источни ком легочного кровотечения. Надежным способом борьбы с подобным осложнением яв ляется перевязка крупных коллатеральных сосудов во время операции (К. Sano et al., 1978) или их транскатетерная эмболизация (Ю.Д. Волынский и др., 1981). Предотвра щение указанных осложнений требует тщательного дооперативного выявления разме ра, количества, места отхождения и распределения этих сосудов.
В заключение представляется необходимым отметить, что важность приведенных материалов определяется не столько существующей компенсирующей функцией окольного кровообращения при тетраде Фалло, сколько необходимостью понимания того факта, что отсутствие должного внимания к коллатералям при данном пороке чревато фатальными осложнениями.
Сосуды Вьессена—Тебезия
Как уже отмечалось выше, сосуды Вьессена-Тебезия эмбриологически представ ляют собой сохранившиеся синусоиды, открывающиеся в полости сердца. Как извест но, по мере образования компактного миокарда большая часть синусоид подвергается редукции. Одновременно является доказанным фактом, что при сохранении губчатой структуры миокарда (например, при АЛА с ИМЖП) в миокарде сохраняется синусоидный тип кровоснабжения. Синусоиды в недифференцированном миокарде - один из путей компенсации при данном пороке (R. Freedom et al., 1983).
В 1706 г. Вьессен (R. Vieussens) описал отверстия в просвете ЛЖ . Введя в ВА гиафрановую краску, он обнаружил, что она выходит из указанных отверстий в полость ЛЖ. Спустя два года A. Thebesius (1708) также описал отверстия в стенке ЛЖ . По его данным, они имели сообщения с венечными венами. С тех пор все отверстия и каналы в стенках сердечных камер называют тебезиевыми каналами или сосудами Вьессена-Тебезия.
Сосуды Вьессена-Тебезия имеют весьма своеобразное строение, несколько отличное в разных отделах сердца. Располагаясь в толще миокарда, в предсердиях они напоминают
124
по строению венозные стволики, а в желудочках эти сосуды построены по синусоидному типу (С. П. Ильинский, 1958). Стенка их состоит из одного слоя эндотелия, подкреплен ного соединительнотканной основой, содержащей эластические волокна. По данным С. В. Самойловой (1970), сосуды Вьессена-Тебезия по своей морфологии занимают про межуточное место между обычными кровеносными сосудами и капиллярами.
В. Д. Арутюнов (1962) считает, что большинство этих сосудов располагается в облас ти верхушки сердца, по мнению С. П. Ильинского (1958), - их больше в предсердиях. Со суды Вьессена-Тебезия располагаются в толще миокарда, то есть являются интрамуральными сосудами, точечные отверстия которых открываются во всех полостях сердца
(СВ. Самойлова, 1970; С. П. Ильинский, 1971). Они анастомозируют как с артериальны ми, так и венозными стволами. Двусторонняя связь сосудов Тебезия (с артериями и вена ми сердца) обусловливает сложность циркуляции крови в миокарде. Соответственно фи зиологическим нуждам момента, синусоиды могут депонировать дополнительные массы крови, а в других случаях кровь из синусоид может быть отведена в систему артерий или вен сердца. М. Я. Арьев (1935) и Н. И. Лепорский (1939) отводят сосудам Тебезия опре деленную роль в кровоснабжении сердца. С П . Ильинский (1971) считает, что артериосинусоидные анастомозы являются анатомической основой компенсации коронарного кровотока, осуществляемой через сосуды Вьессена-Тебезия. А. И. Озарай (1958) считает их шлюзовой системой, сообщающейся с различными камерами сердца и дополнитель ными резервуарами для крови.
Таким образом, по мнению большинства авторов (С. П. Ильинский, 1962; В. И. Колесов, 1977; С.В.Самойлова, 1970; В. В. Кованое и Т.Н.Аникина, 1974; Б.И.Хубутия, 1974), сосуды Вьессена-Тебезия - активная сосудистая система миокарда, кото рой приписывают известное значение в компенсации кровоснабжения зон ишемии миокарда, рассматривая их как своеобразные коллатерали. Однако полной ясности в этом вопросе нет. Пути перемещения крови внутри миокарда при патологических ус ловиях нуждаются еще в дополнительном изучении.
Сегодня важность дальнейшего изучения морфофункциональных особенностей системы сосудов Вьессена-Тебезия и вен сердца определяется и прямыми запросами клиники, и в частности разработкой и внедрением в клиническую практику ретро градной кардиоплегии. Полагают, что эффективность чреспредсердного введения кардиоплегического раствора определяется возможностью достичь гомогенного охлажде ния сердца у больных с мультифокальными поражениями ВА (N. Silverman et al., 1978; J.Dietl et al., 1989). В основе такого подхода лежит поступление введенного чреспредсердно-кардиоплегического раствора через сосуды Вьессена-Тебезия и вены передней стенки правого желудочка в полость правого желудочка.
4. Ангиокардиографическая анатомия венечных артерий
Разработка методов прямой реваскуляризации миокарда немыслима без правиль ной интерпретации коронарограмм. При несомненных успехах в прижизненном изу чении коронарных артерий (Ю.С.Петросян и Л.С.Зингерман, 1974; G.Gensini and P. Esente, 1975; С. Ilsley et al., 1982; J. Dodge et al., 1988) реальные сопоставления ана томии ВА и ангиоградиографической анатомии ВА в литературе ограничены единич ными сообщениями (М. Raphael et al., 1980). Между тем такие сопоставления крайне актуальны, в частности для разработки программ обучения.
Первое описание прижизненного рентгенологического изображения ВА, полученно го с помощью коронарографии, принадлежит L. DiGuglielmo и М. Guttadauro (1952). По следующая детализация рентгеноанатомии ВА осуществлялась односторонне - путем са мостоятельного изучения и описания рентгеноанатомии ВА (W. Sewell, 1966; G. Gensini et al, 1967; M.Tsuzuki et al, 1968; R.Favaloro, 1970; Ю.С.Петросян и Л.С.Зингерман,
125
1974; Д. Лужа, 1973; С. Ilsley et al, 1982; D. Lewin and G. Gardiner, 1988). И хотя работы современных авторов характеризуются углубленными исследованиями рентгеноанато мии с трехмерной оценкой внутригрудного расположения ВА (D.Parker et al., 1987; J. Dodge et al., 1988) на сегментарном уровне (W.Austen et al., 1975; W. Vieweg et al., 1975; J. Dodge et al., 1988)y ясно, что первым этапом в исследовании ВА должны были бы стать работы по прижизненной идентификации анатомии ВА на основании сопоставления этих материалов с данными анатомии ВА. Поскольку даже существующие в этой области ра боты далеко не безупречны, с целью объективизации образовательных программ нами проведены анатомо-ангиокардиографические сопоставления строения ВА.
Мы сравнивали коронарограммы со слепками ВА сердец лиц, умерших от причин, не связанных с сердечно-сосудистыми заболеваниями, в проекциях, используемых при коронарной артериографии. Такой подход был продиктован тем, что рентгеноло гический образ ВА представляет собой двухмерное отображение трехмерной структу ры (венечно-артериального дерева). Учитывая трехмерную пространственную ориен тацию ВА, для объективной оценки ВА необходимо их контрастирование в несколь ких проекциях. Для этого обычно используют переднезаднюю, 1-ю и 2-ю косые проек ции, а изменения и особенности анатомии ВА определяются по данным многопроек ционного исследования. Первая (или правая передняя) косая (угол наклона объекта визуализации к сагиттальной плоскости составляет 20-35° вправо) и вторая (или ле вая передняя) косая (угол наклона - 60-70° влево) проекции отражают реальное косое положение сердца и его основных (атриовентрикулярных и межжелудочковых) бо розд в грудной клетке. Понятно, что крупные В А, располагающиеся в атриовентрику лярных и межжелудочковых бороздах, ориентированных вдоль короткой и длинной осей сердца, могут быть визуализированы в профиль именно в этих проекциях. По скольку идентификация рентгеноанатомии ВА не может опираться на одно только пространственное воображение исследователя, а в каждой из используемых проекций рентгенологическая картина венечно-артериального дерева различается, мы полага ем, что приводимые здесь анатомо-ангиокардиографические сопоставления могут представлять определенный практический интерес.
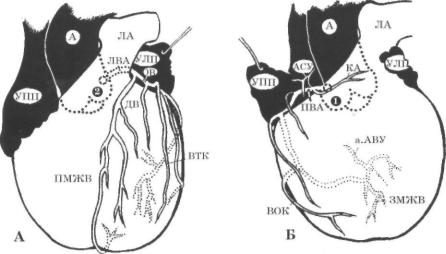
Одноплоскостная анатомическая схема строения венечно-артериального дерева и сердечного комплекса представлена на рис. 69. На рис. 70 представлена изолирован-
Рис. 69. Одноплоскостная анатомическая схема строения венечно-артериального дерева и сер дечного комплекса.
А- система левой венечной артерии (ЛВА), Б - система правой венечной артерии (ПВА). 1 — 1-й лицевой синус аорты, 2 - 2-й лицевой синус аорты.
А- аорта, ЛА - легочная артерия, УПП - ушко правого предсердия, УЛП - ушко левого предсердия, ПМЖВ - перед няя межжелудочковая ветвь, ОВ - огибающая ветвь, ДВ - диагональная ветвь, ВТК — ветвь тупого края, АСУ — арте рия синусного узла, КА - конусная артерия, BOK — ветвь острого края, а.АВУ - артерия атриовентрикулярного узла, ЗМЖВ - задняя межжелудочковая ветвь.
126
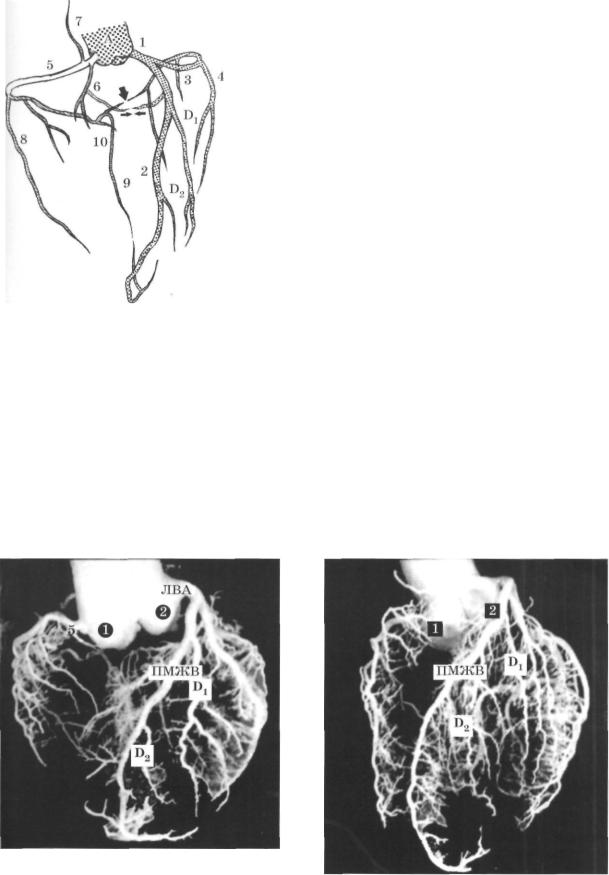
Рис. 70. Изолированная анатомическая схема венеч но-артериального дерева.
1 - левая венечная артерия, 2 - передняя межжелудочковая ветвь, 3 - огибающая ветвь, 4 - ветвь тупого края, Dj и D2 - 1-я и 2-я диа гональные артерии, 5 - правая венечная артерия, 6 - конусная ар терия, 7 - артерия синусного узла, 8 - ветвь острого края, 9 — зад няя межжелудочковая ветвь, 10 - артерия атриовентрикулярного узла.
А - аорта. Сохранение круга Вьессена показано двумя стрелками (ветви конусной артерии и правожелудочковые ветви передней межжелудочковой артерии). Сохранение первичного вокругпредсердного кольца показано большой стрелкой.
В дальнейшем в работе (иллюстрациях) использован указанный ци фровой код обозначений венечных артерий.
ная анатомическая схема строения венечно-артериального дерева. Как следует из представленных данных, а также из многопроекционного исследования коронарограмм и рисунков, воспроизводящих строение венечно-артериального дерева на кор розионных препаратах, в проекциях, соответствующих таковым, используемым в коронарографии, первые никак не отражают строения ВА в соответствующих проекци ях. Поэтому приводим описание анатомии ВА в соответствии с направленностью и определяемостью ВА на коррозионных препаратах в соответствующих проекциях.
Переднезадняя проекция
Как следует из рисунков 71-74, в переднезадней проекции четко определяется отхождение стволов правой и левой ВА. Это единственная проекция, позволяющая их визуализировать независимо от уровня отхождения от синусов Вальсальвы и степени
Рис. 71. Коррозионный препарат. Перед |
|
|
незадняя проекция. |
Рис. 72. Коррозионный препарат. Перед |
|
1 и 2 - 1-й и 2-й лицевые синусы аорты; Dp D2 - 1-я и |
||
незадняя проекция. |
||
2-я диагональные артерии; 5 - правая венечная |
||
артерия. |
1 и 2 — 1-й и 2-й лицевые синусы аорты. |
|
|
127
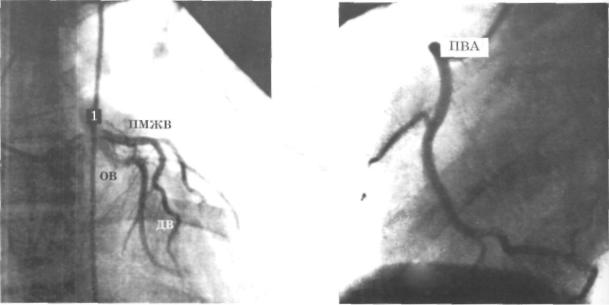
Рис. 73. Коронарограмма. Переднезадняя |
Рис. 74. Коронарограмма. Переднезадняя |
проекция. |
проекция. |
Левая коронарная артерия (1) и ее ветви: передняя |
ПВА - правая венечная артерия, |
межжелудочковая ветвь (ПМЖВ), диагональная |
|
(ДВ) и огибающая (OB). |
|
регургитации контраста. Идентификация отхождения КА и ОВ левой ВА в этой про екции затруднена.
Проекция позволяет визуализировать ряд дистальных диагональных ветвей ПМЖВ, а также оценить участие ПМЖВ в кровоснабжении диафрагмальной поверх ности сердца.
Особенности всех прочих ВА и их ветвей определяются только при сопоставлении данных многопроекционного исследования.
Левая венечная артерия
Анатомическая схема распределения основных стволов левой ВА (ПМЖВ и ОВ) и их взаимоотношений с отделами и структурами сердца, воспроизведенная с коррози онных препаратов в 1-й и 2-й передних косых проекциях, приведена на рис. 75.
1. Левая передняя косая проекция. В этой проекции ствол левой ВА находится в ор тогональной проекции и поэтому оценка его особенностей затруднена. Визуализация ствола левой ВА в этой проекции зависит и от уровня его отхождения от 2-го лицевого (левого в дефинитивном сердце) синуса аорты, и от степени рефлюкса контрастного ве щества в аорту (при резком стенозе или окклюзии ствола левой ВА, например).
С другой стороны, в этой проекции отчетливо визуализируется бифуркация (трифуркация) левой ВА (рис. 75,Б; 76, 77 и 78). В этой проекции ПМЖВ идет по правому контуру сердца, а ОВ и ее крупные ветви - по левому.
ПМЖВ, как правило, распознается по перегородочным артериям, отходящим от нее под прямым углом. Очень важна и идентификация промежуточной ветви левой ВА, по скольку в случае существования она ответственна за кровоснабжение значительного бас сейна, включающего в себя переднюю поверхность левого желудочка и верхушку сердца.
Недостатком проекции является суперпозиция проксимального участка ВТК с ОВ.
И хотя в этой проекции визуализация ВТК чаще не затруднена, обнаружение сужений
вее проксимальной трети в 1-й косой проекции сопровождается определенными слож ностями.
Таким образом, эта проекция позволяет идентифицировать тип ветвления левой ВА и особенности строения ПМЖВ, ОВ и их ветвей. И хотя она не позволяет оценить состо-
128
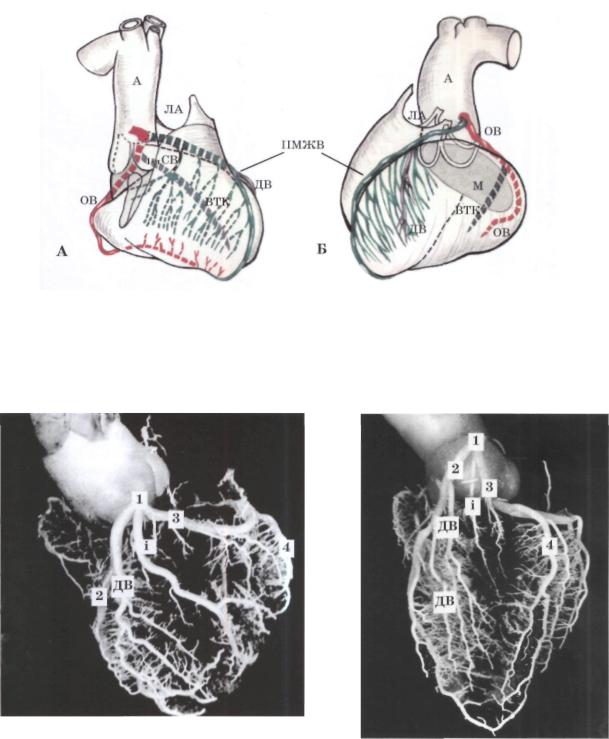
Рис. 75. Анатомическая схема распределения основных стволов левой венечной артерии и их взаимоотношений с отделами и структурами сердца, воспроизведенная с коррозионных препа ратов в 1-й (Б) и 2-й (А) передних косых проекциях.
Идентификация передней межжелудочковой ветви (ПМЖВ) легко осуществима по наличию септальных ветвей (СВ).
В 1-й передней косой проекции возможна суперпозиция огибающей ветви (ОВ) и ветви тупого края (ВТК), во 2-й перед ней косой проекции - ПМЖВ и диагональной ветви (ДВ).
А - аорта, ЛА - легочная артерия, М — митральный клапан.
Рис. 76. Коррозионный препарат. 1-я (левая |
|
|
передняя) косая проекция. |
Рис. 77. Коррозионный препарат. 1-я |
|
Левая венечная артерия (1) и ее ветви. |
||
(левая передняя) косая проекция. |
||
i - промежуточная артерия (a. intermedia). |
||
Левая венечная артерия (1) и ее ветви, |
||
Остальные обозначения те же, что и на рис. 70. |
||
i - промежуточная артерия (a. intermedia). |
||
|
||
|
Остальные обозначения те же, что и на рис. 70. |
яние ствола левой ВА и иногда проксимальных участков ПМЖВ (до 1-й септальной вет ви) и ОВ, она очень информативна для оценки крупных левожелудочковых ветвей ПМЖВ (диагональных, промежуточной, перегородочных) и ОВ (ВТК и, частично, - заднебоковой (ЗБ) левожелудочковой ветви).
2. Правая передняя косая проекция. В этой проекции ПМЖВ и ОВ также разведены, но она малоинформативна для оценки зоны бифуркации левой ВА. При отсутствии
129
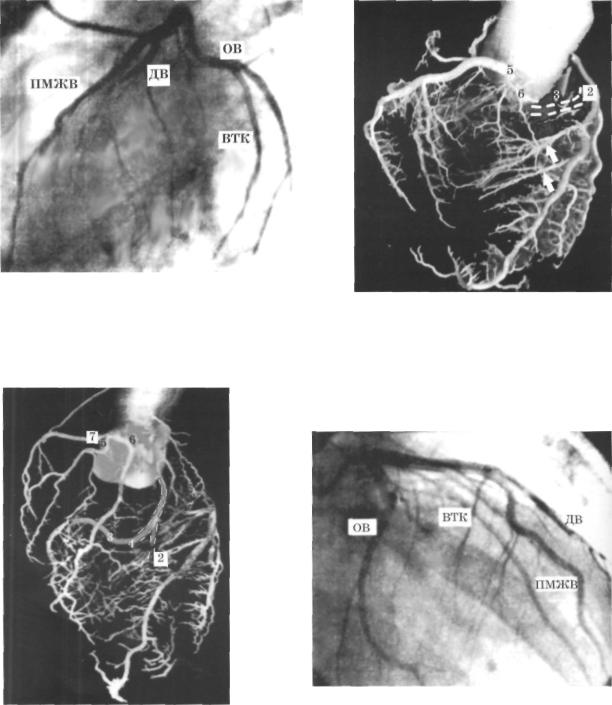
Рис. 78. Селективная коронарограмма левой |
|
коронарной артерии. |
Рис. 79. Коррозионный препарат. 2-я |
1-я (левая передняя) косая проекция. |
(правая передняя) косая проекция. |
ПМЖВ - передняя межжелудочковая ветвь, ДВ - диагональ |
Системы правой (5) и левой венечных артерий. |
ная ветвь, ОВ - огибающая ветвь, ВТК - ветвь тупого края. |
Септальные ветви передней межжелудочковой |
|
|
|
ветви (2) показаны стрелками, типичный ход оги |
|
бающей ветви (3) подчеркнут пунктиром. |
|
Остальные обозначения те же, что и на рис. 70. |
Рис. 80. Коррозионный препарат. 2-я |
Рис. 81. Селективная коронарограмма левой |
|
коронарной артерии. |
||
(правая передняя) косая проекция. |
2-я (правая передняя) косая проекция. |
|
Системы правой (5) и левой венечных арте |
ПМЖВ - передняя межжелудочковая ветвь, ДВ - диагональ |
|
рий. |
ная ветвь, ОВ - огибающая ветвь, ВТК — ветвь тупого края. |
|
Типичный ход огибающей ветви (3) и отхо |
|
|
дящей от нее ветви тупого края (4) подчерк |
заброса контрастного вещества в аорту эта проек |
|
нут пунктиром. |
||
ция очень информативна для оценки состояния |
||
Остальные обозначения те же, что и на рис. 70. |
||
проксимальных участков ПМЖВ и ОВ и прокси |
||
|
||
|
мальных септальных ветвей ПМЖВ. По ней мож |
но оценить и развитие правожелудочковых ветвей ПМЖВ. В этой проекции ПМЖВ ог раничивает левый контур сердца, а ОВ простирается правее от нее (рис. 75,А; 79-81).
Проекция оптимальна и для экспозиции ВТК и ее отхождения от ОВ. В этой проек ции зона расхождения ОВ и ВТК расположена в проекции, где указанные артериаль-
130
