
2 курс / Микробиология 1 кафедра / Доп. материалы / Общая медицинская микробиология
.pdfРоль сульфаниламидов в последнее время значительно снизилась в результате распространения резистентных к ним штаммов и появления мощных антибиотиков. Резистентность к сульфаниламидам связана с появлением в результате мутаций новых ферментов, нечувствительных к действию ингибиторов. Гены, кодирующие новые ферменты, локализуются на плазмидах или входят в состав транспозонов, что обеспечивает быстрое внутри- и межвидовое распространение резистентности. Между отдельными сульфаниламидами, как правило, отмечается практически полная перекрестная резистентность.
Комбинированным препаратом, который продолжает широко использоваться для лечения некоторых инфекций, является ко-тримоксазол (бисептол), в состав которого, помимо сульфаметоксазола, входит триметоприм (диаминопиримидин, аналог дигидрофолиевой кислоты). Триметоприм, являясь ингибитором фермента дигидрофолатредуктазы, блокирует превращения дигидрофолата в тетрагидрофолат. Триметоприм в 20–100 раз активнее сульфаметоксазола, а их совместное действие является синергидным.
Использование ко-тримоксазола дает хороший эффект при инфекциях мочевыводящих путей, бронхитах и пневмонии, вызванной Pneumocystis carinii. Его также применяют при шигеллезе, сальмонеллезе, брюшном тифе, менингококковой, стрептококковой, стафилококковой инфекциях.
Среди побочных эффектов сульфаниламидов отмечаются: аллергические реакции (эритема, синдромы Стивенса–Джонсона, Лайела), гематотоксичность (гематолитическая анемия, тромбоцитопения), гепатотоксичность.
2. Нитрофурановые препараты (нитрофурантоин (фурадонин), нифуроксазид, нифурател, фуразидин, фурацилин, фуразолидон, фурагин, фурамаг и др.).
Механизм действия: взаимодействие с НАДН2-дегидрогеназой мезосом бактерий. Являясь акцепторами кислорода, нитрофураны нарушают процесс клеточного дыхания бактерий, ингибируют биосинтез нуклеиновых кислот. В зависимости от концентрации оказывают бактериостатическое или бактерицидное действие.
Нитрофураны активны в отношении многих Грам+ и некоторых Грам– бактерий, а также грибов, простейших, риккетсий. Резистентны к нитрофуранам
Pseudomonas spp., Proteus spp., значительная часть штаммов Enterobacter spp. и Klebsiella spp. Частота приобретенной резистентности к нитрофуранам среди чувствительных микроорганизмов невысокая. Препараты данной группы нетоксичны, не раздражают слизистые оболочки, применяются в виде водных и спиртовых растворов для обработки ран, промывания полостей (фурацилин), в мазях и аэрозолях («Лифузоль»), в таблетках (фуразолидон, фурадонин, фурамаг) для лечения мочеполовых и кишечных инфекций. Фурамаг — комплексное соединение фурагина и карбоната магния, отличается высокой биодоступностью. По отношению к стафилококкам действует сильнее всех нитрофуранов, к некоторым Грам– бактериям — сильнее антибиотиков.
Среди побочных эффектов нитрофуранов отмечаются: гепатотоксичность, нейротоксичность, диспептические расстройства.
3. Производные 8-оксихинолина (хинозол, энтеросептол, мексаза, мексаформ, хлорхинальдол, интестопан, нитроксолин (5-НОК), налидиксовая (неграм,
238
невиграмон) кислота, пипемидиевая кислота (палин)) являются нефторированными хинолонами. Они обладают антибактериальной (умеренно активны в отношении Грам– бактерий при отсутствии значимой активности в отношении Грам+), противопаразитарной и противогpибковой активностью. Действуют цидно.
Механизм действия: образование комплексных соединений с ионами металлов и устранение их стимулирующего влияния на активность ферментов микроорганизмов.
При длительном применении эти препараты могут вызывать побочные явления: периферические невриты, миелопатии и поражения зрительного нерва, нарушения функций печени и почек. В связи с этим производные 8-оксихино- лина противопоказаны детям с поражениями периферической нервной системы, патологией глаз. Они не назначаются новорожденным и, особенно, недоношенным детям. Энтеросептол и мексаформ содержат йод, поэтому противопоказаны больным с повышенной чувствительностью к йодсодержащим лекарственным средствам.
8-Оксихинолины применяют для лечения мочеполовых и кишечных инфекций, вызванных Грам– бактериями, в большинстве случаев патогенной кишечной палочкой. Резистентность к 8-оксихинолинам формируется медленно.
4.Производные хиноксалин-1,4-диоксида (хиноксидин, диоксидин) —
противомикробные препараты «глубокого» резерва.
Механизм действия: вызывают структурные изменения в ЦП микроорганизмов и нарушают синтез бактериальной ДНК. Хиноксалины обладают широким спектром действия в отношении Грам+ и Грам– бактерий и оказывают бактерицидное действие. Они эффективны против штаммов бактерий, резистентных
кдействию других химиопрепаратов, но высокотоксичны, поэтомy используются для лечения тяжелых гнойно-воспалительных процессов только у взрослых. Активность хиноксалинов усиливается в анаэробной среде.
5.Производные парааминосалициловой кислоты (ПАСК) и гидразиди-
зоникотиновой кислоты (ГИНК) получены синтетическим путем.
Механизм действия: блокируют синтез миколовой кислоты. Активны в отношении некоторых штаммов микобактерий.
6.Препараты тяжелых металлов: мышьяка, висмута, сурьмы и рту-
ти (бийохинол, бисмоверол, моно- и дихлорид ртути и др.).
Механизм действия: образование нерастворимых соединений металлов с сульфгидрильными группами белков микроорганизмов, а также нарушение синтеза тимина и гуанина. Активны в отношении спирохет и простейших. Резистентность к препаратам тяжелых металлов формируется медленно.
7. Нитроимидазолы (производные ароматических соединений имидазо-
ла): метронидазол, трихопол, метрагил, тинидазол, орнидазол, секнидазол. Механизм действия: повреждение ДНК, вызываемое высокоактивными ра-
дикалами, высвобождающимися при восстановлении нитрогруппы препарата. Действие метронидазола зависит от ферментов анаэробного метаболизма, модифицирующих его структуру в активную форму. Аэробные микроорганизмы естественно резистентны к метронидазолу, т. к. не могут превратить его в активную форму.
239
Применяются для лечения протозойных инвазий (трихомониаза, лямблиоза, амебиаза) и инфекций, вызванных анаэробными бактериями, за исключением
Actinomyces spp. и Propionibacterium spp. Резистентность анаэробов к метронида-
золу встречается редко.
Метронидазол легко преодолевает ГЭБ и эффективен при лечении абсцессов мозга. Он является альтернативой ванкомицину при борьбе с C. difficile.
8.Противогрибковые препараты: антибиотики полиеновой группы
(нистатин, леворин, амфотерицин В), производные имидазола (клотримазол (канестен), миконазол, кетоконазол (низорал)) и других азолов (инраконазол (оругал), флуконазол (дифлюкан)).
Механизмы действия имидазолов:
– ингибируют биосинтез стеролов, что приводит к повреждению наружной клеточной мембраны грибов и повышению ее проницаемости;
– ингибируют синтез триглицеридов, фосфолипидов;
– уменьшают активность ферментов, тормозящих образование свободных радикалов, что приводит к внутриклеточному накоплению перекиси водорода и повреждению клеточных органелл;
– угнетают синтез нуклеиновых кислот в ядрах грибковых клеток. Имидазолы хорошо проникают во все биологические среды и ткани орга-
низма. Их используют системно при лечении кандидоза и глубоких микозов. При комбинации имидазолов с полиеновыми антибиотиками наблюдается аддитивный эффект.
9.Противовирусные препараты: аналоги нуклеозидов (ацикловир, ган-
цикловир, видарабин, идоксуридин, рибавирин, ламивудин, антиретровирусные препараты), озетальмивир, производные амантадина (амантадин, ремантадин), интерфероны и индукторы интерферонов (цилоферон, неовир, арбидол).
Механизмы действия аналогов нуклеозидов: ингибирование репликации вирусов путем блокирования ферментов, участвующих в биосинтезе вирусных нуклеиновых кислот. Для уменьшения токсического действия препаратов их используют в виде пролекарств (протоксинов), которые в вирусинфицированных клетках превращаются в токсины благодаря действию вирусспецифических ферментов.
Озетальмивир (тамифлю) — эффективный и селективный ингибитор нейраминидазы вирусов гриппа А и В — фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в клетки эпителия дыхательных путей и дальнейшего распространения по организму.
Механизмы действия производных амантадина: препятствуют депротеинизации вирионов и поступлению вирусной нуклеиновой кислоты в клеткумишень. Эффективны вначале заболевания при инфицировании некоторыми штаммами вирусов гриппа А.
Механизмы противовирусного действия интерферонов: подавление трансляции вирусных РНК в клетках. Действие интерферонов универсально либо за счет активации латентной рибонуклеазы, которая разрушает и-РНК, либо за счет запрета пролонгации полипептидной цепочки и ингибирования синтеза вирусных белков.
240
Механизмы противовирусного действия индукторов интерферонов: стимулируют в организме образование собственного эндогенного интерферона.
В связи с высокой токсичностью противовирусных препаратов этиотропная терапия при большинстве вирусных инфекций отсутствует. Противовирусные препараты применяются для лечения гриппа, герпеса, ВИЧ-инфекции, вирусных гепатитов.
10.Противоопухолевые препараты: антибиотики (антрациклины (дауно-
рубицин), флеомицины (блеомицин), актиномицины (дактиномицин)), алкилирующие агенты (митомицин, новэмбихин, хлорбутин, миелосан), антиметаболиты (метотрексат, фторурацил), растительные алкалоиды (винбластин, винкристин) ингибируют синтез нуклеиновых кислот и рост опухолевых клеток. Они обладают высокой антимитотической активностью при низкой избирательности действия, поэтому высокотоксичны, обладают иммуносупрессивным действием.
11.Противопаразитарные (антипротозойные и антигельминтные) пре-
параты блокируют различные этапы жизенного цикла паразитов.
Например, нитрогруппа метронидазола восстанавливается внутриклеточными транспортными протеинами последних, взаимодействует с ДНК простейших и ингибирует синтез нуклеиновых кислот. Метронидазол используют для лечения трихомониаза и амебиаза.
Мебендазол вызывает необратимое нарушение утилизации глюкозы, истощает запасы гликогена в тканях гельминтов, а также тормозит синтез АТФ. Мебендазол используют для лечения энтеробиоза.
12.Антибиотики.
АНТИБИОТИКИ
Антибиотики (от греч. anti — против, bios — жизнь) — химиопрепараты биологического (преимущественно микробного), полусинтетического или синтетического происхождения, которые в малых концентрациях подавляют развитие или вызывают гибель чувствительных к ним микроорганизмов и опухолевых клеток во внутренней среде животного организма.
Высокая специфичность антибиотиков и их отличие от антисептиков определяются мишенями действия. Мишени действия антибиотиков являются уникальными для прокариот и отсутствуют у эукариот. Благодаря этому препараты этой группы отличаются значительной терапевтической широтой — разницей между концентрациями, оказывающими антибактериальное действие, и концентрациями, проявляющими токсические эффекты на организм человека.
ТРЕБОВАНИЯ К АНТИБИОТИКАМ
К антибиотикам предъявляют следующие требования:
1.Высокая селективность действия (избирательное подавление микроорганизмов обеспечивается различием строения клеток прокариот и эукариот).
2.Высокая активность, т. е. действие в малых дозах.
3.Наличие спектра действия (перечня чувствительных к данному препарату видов микроорганизмов). При установленной этиологии заболевания и из-
241
вестной чувствительности штамма микроорганизма используются препараты узкого спектра действия. При эмпирической антибиотикотерапии предпочтение отдается антибиотикам широкого спектра действия.
4. Химиотерапевтический индекс больше 3. Он определяется по следующей формуле:
ХТИ = максимальная переносимая доза (Dmt-doses maxima toleranta)
минимальная лечебная доза (Dmc-doses minims curativa)
ХТИ определяет токсичность препарата: чем ХТИ выше, тем менее токсичен препарат.
5.Хорошая растворимость в нормальных и патологических жидкостях организма, хорошая всасываемость, действие в очаге воспаления при слабокислых значениях рН. Относительно медленное выведение из организма (период полужизни).
6.Отсутствие повреждающего, в т. ч. токсического действия на организм хозяина.
7.Отсутствие связывания с белками макроорганизма.
8.Отсутствие кумуляции в организме.
9.Медленная селекция резистентных к ним форм микроорганизмов.
10.Стабильность при хранении, невысокая стоимость препаратов.
КЛАССИФИКАЦИЯ
Выделяют следующие виды антибиотиков:
1.По антимикробному спектру действия:
– суперузкого спектра — на 1 вид бактерий;
– узкого — на 1–2 вида бактерий;
– широкого — на несколько видов бактерий;
– суперширокого — на бактерии, гельминты, грибы и простейших.
2.По происхождению:
–микробного происхождения: из бактерий — грамицидин, полимиксин; из грибов — пенициллин; из актиномицетов — стрептомицин;
–растительного происхождения: из высших растений — фитонциды, из семян редиса — рафанин, из чеснока — аллизин;
–животного происхождения — лизоцим, эритрин, эмолин;
–полусинтетические и синтетические.
Вначале использовались антибиотики биологического происхождения — продукты жизнедеятельности живых организмов. Путем химической модификации антибиотиков биологического происхождения были получены полусинтетические антибиотики, обладающие новыми ценными свойствами: кислото- и ферментоустойчивостью, расширенным спектром антимикробного действия, лучшим распределением в тканях и жидкостях организма, меньшим числом побочных эффектов. Когда была расшифрована химическая структура антибиотиков, некоторые из них выгоднее стало получать синтетическим путем.
3. По типу действия:
– бактериостатические (левомицетин, тетрациклины, линкозамиды, макролиды). Они ингибируют синтез белков и предотвращают размножение бакте-
242

рий, но не вызывают их гибели. Бактериостатические антибиотики неэффективны у иммунокомпроментированных организмов;
– бактерицидные (пенициллины, цефалоспорины, аминогликозиды, рифампицин, полипептиды). Они уничтожают микроорганизмы, нарушая проницаемость ЦПМ или ингибируя синтез РНК.
Для характеристики типа действия препарата определяют его минимальную ингибирующую концентрацию (МИК) и минимальную бактерицидную концентрацию (МБК). Препарат является бактерицидным, если МБК равна МИК или превышает ее.
4. По направленности действия:
–противобактериальные;
–противопротозойные;
–противоопухолевые.
Противобактериальные антибиотики по спектру противомикробного действия разделяются на следующие:
–действующие преимущественно на кокки (стафилококки, стрептококки, менингококки, гонококки) и некоторые Грам+ палочки (коринебактерии, клостридии): бензилпенициллин, бициллины, феноксиметилпенициллин, пенициллиназоустойчивые пенициллины (оксациллин, метициллин), цефалоспорины I поколения, макролиды, ванкомицин, линкомицин;
–широкого спектра действия, активные в отношении Грам+ и Грам– палочек: хлорамфеникол, тетрациклины, аминогликозиды, полусинтетические пенициллины широкого спектра действия (ампициллин, азлоциллин) и цефалоспорины II поколения;
–с преимущественной активностью в отношении Грам– палочек: полимиксины, цефалоспорины III поколения;
–противотуберкулезные (стрептомицин, рифампицин, флоримицин);
–противогрибковые (нистатин, леворин, гризеофульвин, амфотерицин В).
5. По химическому строению:
1. -Лактамные антибиотики ( -лактамы) — азотсодержащие гетероцик-
лические соединения с -лактамным кольцом. Они блокируют синтез пенициллинсвязывающих белков, входящих в состав КС бактерий. Действуют бактерицидно на размножающиеся бактерии. Между отдельными представителями группы -лактамов существуют значительные различия в уровне и спектре антибиотической активности.
Пенициллины — активной молекулой является 6-аминопенициллиновая кислота. Первым был получен бензилпеннициллин из гриба Penicillum natatum (продуцировал 20 ед/мл пенициллина). Сейчас отобраны штаммы грибов, продуцирующие более 25 000 ед/мл пенициллина.
В зависимости от спектра антимикробного действия выделяют 6 поколений пенициллинов (табл. 44).
Цефалоспорины — большая группа естественных (получены из грибка цефалоспорум) и полусинтетических антибиотиков, производных аминоцефалоспориновой кислоты. В зависимости от спектра антимикробного действия выделяют 4 поколения цефалоспоринов (табл. 45).
243
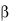
Монобактамы (азтреонам). Активны только в отношении аэробных Грам– бактерий (по уровню активности соответствует цефалоспоринам III поколения), резистентны к -лактамазам.
Карбапенемы (имипенем (тиенам), меропенем) обладают наиболее широким спектром антибактериальной активности из всех известных антибиотиков, в т. ч. в отношении штаммов, резистентных к пенициллинам, цефалоспоринам и аминогликозидам. Являются антибиотиками резерва при тяжелых полирезистентных нозокомиальных инфекциях, не поддающихся лечению препаратами других групп.
244

|
|
|
|
|
Таблица 44 |
|
|
Классификация и спектр активности пенициллинов |
|
||
|
|
|
|
|
|
|
Поколение |
Препараты |
Активны в отношении |
Неактивны |
Отношение к β-лактамазам |
|
в отношении |
и другие особенности |
|||
|
|
|
|
||
|
Природные |
Бензилпенициллин (пенициллин) |
Грам+ бактерий: стафилокок- |
Грам+ микобакте- |
Чувствительны к действию |
|
|
Феноксиметилпенициллин (кли- |
ков, стрептококков, пневмо- |
рий туберкулеза |
β-лактамаз Грам+ и Грам– |
|
|
ацил, оспен) |
кокков, возбудителей сибир- |
Грам– энтеробакте- |
бактерий |
|
|
Бензилпенициллина прокаин |
ской язвы, дифтерии, листе- |
рий, бордетеллы |
|
|
|
(бициллин V) |
риоза |
коклюша, сине- |
|
|
|
Бензатина бензилпенициллин |
Грам– бактерий: менингокок- |
гнойной палочки, |
|
|
|
(ретарпен, экстенциллин) |
ков, гонококков, протей, спи- |
клебсиелл, гемофи- |
|
|
|
|
рохет, лептоспир |
лов, легионелл |
|
|
Антистафилококковые: |
Оксациллин, клоксациллин, дик- |
Стафилококков и других |
Грам– бактерий |
Устойчивы к действию β-лак- |
|
метициллин и изоксазо- |
локсациллин, флуклоксациллин, |
Грам+ бактерий |
|
тамаз Грам– бактерий |
|
лилпенициллины |
нафциллин |
|
|
|
|
Комбинированные анти- |
Ампициллин/оксациллин (ампи- |
|
|
|
243 |
стафилококковые |
окс, оксамп) |
|
|
|
Расширенного спектра |
Ампициллин (пентрексил, рос- |
В отношении Грам+ бактерий |
Грам– бактерий |
Чувствительны к действию |
|
|
(аминопенициллины) |
циллин) |
их активность ниже, чем пе- |
(Haemophilus spp., |
большинства β-лактамаз. |
|
|
Амоксициллин (амоксикар, |
нициллинов II поколения, но |
Neisseria spp. и не- |
Амоксициллин по сравнению |
|
|
оспамокс, флемоксин солютаб, |
выше, чем I поколения |
которых представи- |
с ампициллином лучше вса- |
|
|
хиконцил) |
|
телей Enterobacteri- |
сывается, более биодоступен |
|
|
|
|
aceae (E. coli, Pro- |
и переносим (меньше побоч- |
|
|
|
|
teus spp.)) |
ных реакций со стороны |
|
|
|
|
|
ЖКТ) |
|
Ингибитор-защищенные |
Амоксициллин/клавуланат (ауг- |
Большинства Грам+ (стафи- |
Некоторых штам- |
Устойчивы к действию: |
|
|
ментин, амоксиклав) |
лококки, стрептококки, кори- |
мов |
– стафилококковых пеницил- |
|
|
Тикарциллин/клавуланат (ти- |
небактерии, пневмококки, не- |
|
линаз; |
|
|
ментин) |
которые клостридии) и Грам– |
|
– β-лактамаз широкого и |
|
|
Пиперациллин/тазобактам (та- |
(эшерихии, клебсиеллы, виб- |
|
расширенного спектра Грам– |
|
|
зоцин) |
рионы, сальмонеллы, шигел- |
|
бактерий; |
|
|
Пиперациллин/сульбактам (зо- |
лы, иерсинии, менингококки, |
|
– β-лактамаз анаэробных |
|
|
цин) |
гонококки) аэробных и анаэ- |
|
бактерий. |
|
|
Ампициллин/сульбактам (уна- |
робных бактерий |
|
Чувствительны к действию |
|
|
зин) |
|
|
хромосомных β-лактамаз |
245
|
|
|
|
|
Окончание табл. 44 |
|
|
|
|
|
|
|
Поколение |
Препараты |
Активны в отношении |
Неактивны |
Отношение к β-лактамазам |
|
в отношении |
и другие особенности |
|||
|
|
|
|
||
|
|
|
|
|
Грам– бактерий. Более ак- |
|
|
|
|
|
тивны в отношении микроор- |
|
|
|
|
|
ганизмов с приобретенной |
|
|
|
|
|
резистентностью к пеницил- |
|
|
|
|
|
линам |
|
Карбоксипенициллины |
Карбенициллин (геопен) |
Грам+ и Грам– бактерий, |
β-лактамазопроду- |
Чувствительны к действию |
|
(антисинегнойные) |
Тикарциллин |
включая большинство пред- |
цирующих штам- |
большинства β-лактамаз |
|
|
|
ставителей Enterobacteriaceae |
мов |
|
|
|
|
и Pseudomonas aeruginosa |
|
|
|
Уреидопенициллины |
Азлоциллин (секуропен) |
Пенициллины расширенного |
β-лактамазопроду- |
Чувствительны к действию |
|
(антипсевдомонадные) |
Мезлоциллин |
спектра действия более актив- |
цирующих штам- |
большинства β-лактамаз |
|
|
Пиперациллин (пипрацил, |
ны в отношении Грам– бакте- |
мов |
|
|
|
пиприл) |
рий (Pseudomonas, Serratia и |
|
|
244 |
|
|
Klebsiella) Грам+ бактерий, а |
|
|
|
|
также большинства анаэроб- |
|
|
|
|
|
|
ных бактерий |
|
|
|
Амидопенициллины |
Байпенициллин (байпен) |
Наиболее перспективные ан- |
Некоторых штам- |
|
|
|
|
тибиотики суперширокого |
мов |
|
|
|
|
спектра действия |
|
|
246
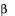
|
|
|
|
|
|
|
Таблица 45 |
|
|
|
|
|
Классификация и спектр активности цефалоспоринов |
|
|
||
|
|
|
|
|
|
|
|
|
|
Поколение |
|
Препараты |
Активны в отношении |
Неактивны |
Отношение к -лактамазам |
||
|
пероральные |
|
парентеральные |
в отношении |
и другие особенности |
|
||
|
|
|
|
|
||||
|
Первое |
Цефалексин |
|
Цефалотин |
Узкого спектра действия. Высо- |
Энтерококков |
Умеренно устойчивы к стафилокок- |
|
|
|
(кефлекс) |
|
Цефазолин (цефамезин, |
коактивны в отношении Грам+ |
|
ковым β-лактамазам. Чувствитель- |
|
|
|
Цефрадин |
|
кефзол) |
бактерий (кроме энтерококков и |
|
ны к хромосомным и плазмидным |
|
|
|
Цефадроксил |
|
Цефалоридин |
метициллинрезистентных стафи- |
|
β-лактамазам Грам– бактерий. Хо- |
|
|
|
(дурацеф) |
|
Цефапирин |
лококков). Умеренно эффективны |
|
рошо проникают в очаг воспаления |
|
|
|
|
|
Цефатон |
в отношении Грам– бактерий |
|
|
|
|
|
|
|
Цефзедон |
(Moraxella, Escherichia, Salmonel- |
|
|
|
|
|
|
|
|
la, Shigella, Klebsiella, Proteus). |
|
|
|
|
|
|
|
|
Мало активны в отношении анаэ- |
|
|
|
|
|
|
|
|
робов |
|
|
|
|
Второе |
Цефаклор |
|
Цефуроксим |
Широкого спектра действия. По |
Некоторых |
Устойчивы к стафилококковым |
|
|
|
(цеклор, тара- |
|
(зинацеф, кетоцеф) |
действию на Грам+ равноценны |
штаммов |
β-лактамазам, к плазмидным β-лак- |
|
245 |
|
цеф, альфацет, |
Цефамандол |
препаратам I поколения. Более |
|
тамазам Грам– бактерий. Чувстви- |
||
|
верцеф) |
|
Цефоницид |
активны в отношении Грам– бак- |
|
тельны к хромосомным и плазмид- |
||
|
|
Лоракарбеф |
|
Цефоранид |
терий (Haemophilus, Neisseria, |
|
ным β-лак-тамазам расширенного |
|
|
|
Цефуроксим |
|
Цефамицины (цефокси- |
Escherichia, Proteus, Klebsiella, |
|
спектра Грам– бактерий. Цефами- |
|
|
|
аксетил (зин- |
|
тин, цефотетан, цефмета- |
Serratia, Moraxella) и некоторых |
|
цины отличаются повышенной |
|
|
|
нат) |
|
зол) |
штаммов энтеробактерий |
|
устойчивостью к β-лактамазам и |
|
|
|
|
|
|
|
|
обладают выраженной антианаэ- |
|
|
|
|
|
|
|
|
робной активностью, особенно про- |
|
|
|
|
|
|
|
|
тив Bacteroides fragilis |
|
|
Третье |
Цефиксим |
|
Цефотаксим (клафоран, |
Более активны, чем I и II поколе- |
По действию |
Устойчивы к β-лактамазам (стафи- |
|
|
|
Цефтибутен |
|
тарцефоксим) |
ния, в отношении Грам– бакте- |
на стрептокок- |
лококковым, плазмидным широкого |
|
|
|
(цедекс) |
|
Цефтриаксон (роцефин, |
рий, в т. ч. мультирезистентных |
ков, стафило- |
спектра Грам– бактерий). Чувстви- |
|
|
|
Цефетамет |
|
лендацин, лонгацеф) |
энтеробактерий и синегнойной |
кокков, анаэ- |
тельны к хромосомным β-лактама- |
|
|
|
Цефдинир |
|
Цефтазидим (фортум, |
палочки |
робов уступа- |
зам Грам– бактерий. Хорошо про- |
|
|
|
Цефподоксим |
|
кефадим, тазицеф) |
|
ют препаратам |
никают в ткани и жидкости орга- |
|
|
|
Цефсулодин |
|
Цефоперазон (цефобид, |
|
I–II поколений |
низма, преодолевают ГЭБ, их кон- |
|
|
|
|
|
дардум) |
|
|
центрация в тканях в несколько раз |
|
|
|
|
|
Цефтибутен |
|
|
превышает МИК для большинства |
|
|
|
|
|
Цефсулодин |
|
|
патогенных возбудителей |
|
247
