
6 курс / Кардиология / Сумароков_А_В_,_Моисеев_В_С_,_Михайлов_А_А_Распознавание_болезней
.pdf
Р и с . 30. Схема истории заболевания больной К.
Конфигурация сердца при анемии в большинстве случаев приближается к митральной из-за раннего увеличения правого желудочка. Встречающееся иногда закругление дуг свидетельствует о миогенной дилатации. Гипертрофия миокарда при анемии обычно отсутствует, что подтверждают данные секции. В отличие от митрального порока при анемии редко увеличивается левое предсердие, а при увеличении последнего контрастированный пищевод отклоняется кзсди по пологой дуге, отсутствует мерцательная аритмия, симптом регургитации. При выраженной анемии бывают изменения в легких, которые при динамическом наблюдении и улучшении состояния больного могут исчезать (К- Э. Тавониус, 1964). Из 70 обследованных больных с анемией разной этиологии (гемоглобин 1,4—6,4 г%) у 52 выслушивался систолический шум на верхушке сердца и крупных сосудах, у 9 — на всех точках, что совпадало со значительной дилатацней сердца. Диастолический шум на аорте отмечен у 4 больных, причем в сочетании с большим пульсовым давлением, что позволило заподозрить аортальную недостаточность. У 2 больных обнаружен пресистолический шум на верхушке сердца и даже диастолическое дрожание, исчезнувшие при улучшении состава крови и общего состояния.
Одними из ранних компенсаторных механизмов при анемии является увеличение ударного объема и ускорение кровотока, способствующие усилению шумов. При тяжелой анемии с развитием сердечной недостаточности (анемическое сердце) шумы могут ослабнуть или исчезнуть.
Ошибочное распознавание порока сердца иногда может быть связано со сложной аускультативной картиной в поздних стадиях п е р в и ч н о й л е г о ч н о й г и п е р т о н и и .
.107
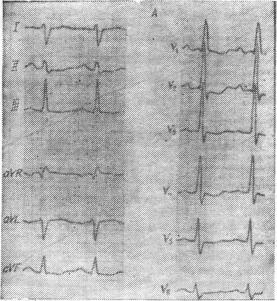
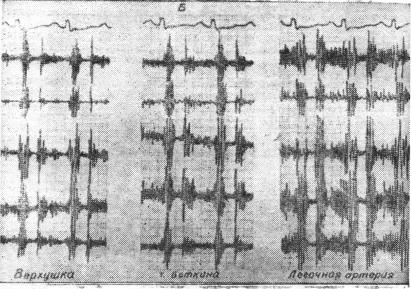
Р и с . 31. Электрокардиограмма (А) и фонокардиограммы с различных точек (Б)
той же больной.
На |
ФКГ: |
верхняя |
кри- |
||
в а я — Э К Г |
во |
II |
отведе- |
||
нии, |
последующие |
— |
|||
ФКГ |
в диапазонах |
аус- |
|||
культативных, |
низких |
||||
средних-1, |
средних-2 н |
||||
|
высоких |
частот. |
|
||
|
Больная К. (наблюдение 34-е), 31 года, находилась в клинике з мар- |
|||||
те—июне |
1971 г. В |
1964 г. перенесла |
нормальную |
беременность |
и роды, |
|
во |
время |
которых |
какой-либо патологии в сердце |
не обнаруживали. |
||
|
В 1967 г. больную впервые стали |
беспокоить сердцебиения |
(рис. 30). |
|||
С |
1968 г. присоединяется и нарастает |
одышка. В |
июне 1968 г. |
лечилась |
||
в 61-й больнице г. Москвы, выписана с диагнозом: ревматический митральный порок сердца. В этом же году обследована в Институте кардиологии, где диагностирован врожденный порок сердца — незаращение межпредсердной перегородки (зондирования не производилось). Терапия сердечными гликозидами дала некоторое улучшение. В связи с частыми простудными заболеваниями зимой 1970 г. усилилась одышка, стали появляться отеки ног, впервые отмечено увеличение печени. Вновь получила кардиотоническую терапию с временным эффектом.
В октябре 1970 г. впервые поступила в нашу клинику. При обследовании отмечена выраженная бледность кожных покровов, яркий «митральный» румянец щек, отчетливый акроцианоз. Пастозность голеней, число дыханий 22 в 1 мин. В легких: в нижних отделах дыхание жестковатое,
хрипы не |
определялись. Область |
сердца внешне не изменена, |
верхушеч- |
|||||||
1:ый толчок в V межреберье. Границы сердца: правая |
на |
1 |
см |
кнаружи |
||||||
от |
края |
грудины, |
верхняя — верхний |
край |
III ребра, |
левая — по левой |
||||
срединно-ключичной |
линии. Аускультативно |
(подтверждено |
на |
ФКГ) — |
||||||
I |
тон хлопающий, |
систолический |
шум |
по |
всему левому |
краю |
грудины, |
|||
диастолический шум в точке Боткина и на легочной артерии с пресистолическим усилением. Печень увеличена незначительно. Рентгенологически: корни легких широкие, плотные за счет расширенных центральных зетвей легочной артерии (выраженная артериальная гипертония в малом круге). Сердце с резко выступающей II дугой по левому контуру, поперечник его растянут влево за счет смещения небольшого левого желудочка увеличенным правым желудочком. Атриовазальный угол высоко расположен из-за гипертрофии правого желудочка и правого предсердия, в 1-й косой
108
проекции легочный конус значительно выступает, левые отделы сердца не изменены. Во 2-й косой проекции видно значительное расширение правого желудочка и еще более выраженное увеличение правого предсердия.
На ЭКГ (рис. 31): синусовый ритм, признаки гипертрофии правых предсердия и желудочка, нарушение внутрнпредсердной и внутрижелудочковой проводимости. Все лабораторные показатели, в том числе ревматические тесты, без особенностей. Больная консультирована в клинике госпитальной хирургии 1-го Московского медицинского института. Высказано предположение о наличии у больной синдрома Лютембаше, от зондирования сердца больная отказалась. После лечения сердечными гликозидами и мочегонными средствами выписана в относительно удовлетворительном состоянии.
Значительное ухудшение состояния наступило в марте 1971 г.: резко усилилась одышка, появились слабость, отеки ног, в области поясницы, асцит. При повторном поступлении в клинику состояние средней тяжести. Цианоз более выражен, число дыханий 30 в 1 мин. Со стороны сердца
обнаружены те же изменения, что |
и при |
предыдущей |
госпитализации. |
|||||
Пульс |
110 |
ударов в |
1 мин, |
ритмичный. |
Артериальное |
давление |
||
100/70 |
мм рт. |
ст. Печень |
выступала |
из-под |
края |
реберной |
дуги |
на S см. |
Симптом рефлюкса положительный, магнезиальное время 45 с. Анализы крови оставались нормальными. В моче появился белок (до 0,1°/оо; застойные почки). Больная консультирована кардиохирургом в Институте хирургии им. А. В. Вишневского. Обращено внимание на выраженную гипертонию в системе легочной артерии, которая была расценена как следствие дефекта межпредсердной перегородки со сбросом крови справа налево и выраженным нарушением кровообращения по большому кругу (застойная печень, асцит, отеки). Не исключался стеноз левого венозного отверстия, хотя отсутствие признаков перегрузи? левого предсердия про-
тиворечило этому. В связи с тяжестью состояния |
больной от зондирова- |
ния сердца и оперативного лечения решено было |
воздержаться. Прово- |
.109
димая терапия строфантином, мочегоннымн средствами, оротатом калия,
АТФ дала лишь временный эффект. При нарастающих явлениях |
сердеч- |
ной недостаточности больная скончалась 12. VI 1971 г. |
|
Клинический диагноз: дефект межпредсердной перегородки в |
сочета- |
нии с митральным стенозом (синдром Лютембаше). Выраженная гипертония малого круга. Нарушение кровообращения преимущественно по большому кругу.
Патологоанатомический диагноз: первичная легочная гнпертончч. Гипертрофия миокарда преимущественно правого желудочка с расширением его полости (тснцина стенки левого желудочка 1,2 см, правого 1,8 см).
Атеросклероз |
легочной артерии и ее ветвей. Тромбы в сегментарных вет- |
вях правой |
егочной артерии с развитием инфарктов. Венозное полнокро- |
вие внутренних органов. Мускатный цирроз печени. Асцит, гидроторакс, гидроперикардит.
Тзким образом, у молодой женщины имелась выраженная гипертония малого круга, о чем свидетельствовали рентгено-
логические |
признаки расширения ветвей легочной артерии |
:J явления |
перегрузки правых отделов сердца (рентгенологи- |
чески и электрокардиографически). Систолический и диастоли :еский шумы, выслушиваемые наиболее отчетливо у осно-
вания сердца и в |
III—IV межреберье слева, были расцене- |
ны как указание |
на врожденный порок сердца — дефект |
межпредсердной перегородки. Появление цианоза связывали со сбросом крови справа налево. Усиление I тона и, особен-
но, довольно громкий пресистолический шум (с |
максимумом |
|
в |
IV межреберье слева у грудины) создавали |
впечатление |
о |
наличии митрального стеноза. |
|
Некоторая нетипичность картины митрального стеноза, отсутствие увеличения левого предсердия, казалось, не противоречат диагнозу синдрома Лютембаше: у этих больных митральный стеноз длительное время дает менее заметные гемодинамические сдвиги в связи с разгрузкой левого предсердия через межпредсердный дефект. Однако секционные данные не подтвердили этих предположений: у больной установлена первичная гипертония легочной артерии с ее выраженным склерозом.
Очевидно, диастолический шум обусловлен относительной недостаточностью клапанов растянутой легочной артерии (шум Грэхема—Стила), а систолический — относительным стенозом ее устья. Труднее объяснить необычное для этой патологии пресистолическое усиление диастолического шума (приведшее к ошибочному распознаванию митрального стеноза). Мы предполагаем, что механизм его возникновения аналогичен таковому пресистолического шума Флинта при аортальной недостаточности: значительная диастолическая регургитация крови в правый желудочек (вследствие относительной недостаточности клапанов легочной артерии и резкой гипертонии малого круга) частично смещает створки
110
трикуспидального клапана, что приводит к относительному
трикуспкдальному стенозу. |
|
|
|
|
||
При дифференциальном |
диагнозе |
между |
ф у н к ц и о - |
|||
н а л ь н ы м и |
и |
о р г а н и ч е с к и м и |
д и а с т о л и ч е - |
|||
с к и м и ш у м а м и , |
которые, |
видимо, |
не |
так |
редки (Luisa- |
|
da, 1972), предлагается базироваться на следующих критериях:
—большой участок, на котором регистрируется шум, максимум его в II—III межреберье слева от грудины указывают на функциональный шум, скорее всего связанный со значительным увеличением желудочка;
—расщепление II тона с большим интервалом между его компонентами свидетельствует против митрального стеноза. Скорее следует думать о гипертензии малого круга, врожденном шунте или тяжелой правожелудочковой недостаточности;
—высокочастотный шум (мягкий, дующий шум при аус-
культации) не характерен для митрального стеноза, такой шум при этом пороке обнаруживается на ФКГ лишь в 12% случаев;
— отсутствие тона открытия митрального клапана свидетельствует против митрального стеноза, хотя в исключительных случаях он может отсутствовать при наличии выраженного стеноза с обызвествлением клапана и изредка встречает-
ся при чистой митральной |
недостаточности, при |
которой |
за |
|
ним иногда следует выраженный III |
тон; |
|
|
|
— диастолический шум |
большой |
амплитуды |
особенно |
с |
усилением в середине диастолы не характерен для стеноза;
— позднее начало диастолического шума свидетельствует в пользу его функциональной природы;
— диастолический шум без пресистолического усиления при наличии синусового ритма не патогномоничен для митрального порока;
—если пресистолический шум не носит характер creshendo, то наличие митрального стеноза при нормальной пред- сердно-желудочковой проводимости маловероятно;
—наличие на ФКГ выраженных III и IV тонов сердца обычно является признаком функциональной природы одновременно существующего диастолического шума;
—вдыхание амилнитрита обычно усиливает шум при митральном стенозе и чаще приводит к ослаблению функционального диастолического шума.
В некоторых случаях даже при использовании этих критериев возможны ошибки при решении вопроса о природе шума.
Определение этиологии порока сердца представляется важным во многих отношениях, ведь наряду с ревматиче-
111
ским и врожденными пороками сердца могут быть пороки и другой относительно редкой этиологии. Они могут возникать при первичном затяжном септическом эндокардите, сифилисе сердечно-сосудистой системы и других заболеваниях сердца. В последние годы обращено внимание на развитие пороков
сердца при |
р е в м а т о и д н о м а р т р и т е . |
|
||
Smyth, Graham (1959) из 519 обследованных с болезнью |
||||
Бехтерева у |
24 |
обнаружили |
этот порок. Schilder |
(1956) из |
100 больных |
с |
аортальной |
недостаточностью у 5 |
наблюдал |
ревматоидный артрит. По мнению Smyth, Graham (1959), аортальная недостаточность при анкилозирующем спондилите развивается тем чаще, чем больше длительность заболевания. Полагают, что аортит с аортальной недостаточностью встречается только при ревматоидном спондилите и не бывает при поражении только периферических суставов. При морфологическом исследовании обнаруживают утолщение и склероз интимы аорты, фиброз эластической ткани media с лимфэцитарной инфильтрацией, эндартериит vasa vasorum адвентиции, уплотнение клапанов аорты. Большинство авторов считают, что ревматоидные пороки протекают сравнительно доброкачественно и редко приводят к существенному нарушению кровообращения. Однако Zwaifler, Weintraub (1963) наблюдали у 5 больных аортальную недостаточность с выраженным нарушением гемодинамики, у них выслушивался даже ритм галопа. Вальвулит и аортит при ревматоидном артрите могут осложниться затяжным септическим эндокардитом.
В отечественной литературе имеются лишь единичные описания больных анкилозирующим спондилитом с аортальной недостаточностью (О. М. Буткевич, 1963; О. М. Виноградова, 1963; М. И. Теодори, 1972) . Приводим наше наблюдение.
Больной Я. (наблюдение 35-е), 65 лет, впервые обратился в клинику в 1966 г. с жалобами на деформацию и ограничение движений в позвоночнике, боли в мелких суставах кистей, лучезапястных, плечевых, коленгых, голеностопных, скованность по утрам, приступообразно сжимающие
боли в |
области сердца. |
|
|
|
С 1920 г. (в возрасте 20 лет) страдает полиартритом. В 1927 г. по- |
||||
явились |
боли в позвоночнике, |
а вскоре |
и признаки |
его деформации. |
В 1937 |
г. возникло выраженное |
обострение |
заболевания |
с резкими болями |
и припухлостью в мелких и крупных суставах рук и ног и высокой лихорадкой. С тех пор боли в суставах и позвоночнике стали постоянными, однако экссудативные явления в периферических суставах при обострении в последующие годы не наблюдались. С 1950 г. отмечает быстрое прогрессирование тугоподвижности и деформации позвоночника. В 1956 г. проводилось насильственное распрямление позвоночника. С 1960 г. РОЭ постоянно ускорена до 52 мм/ч. С 1963 г. вновь появились признаки воспаления в области лучезапястных суставов, а затем их деформация с
ульнарной девиацией. |
С того же времени отмечена тенденция к сниже- |
нию диастолического |
давления. |
С 1956 г. изредка стали беспокоить боли в области сердца типа сте-
112
иокардии. В 1957 г. перенес инфаркт миокарда с характерной динамикой ЭКГ. Боли в области сердца вновь появились в 1963 г., их учащение и усиление отчетливо совпадали с обострениями суставного процесса. Лечение преднизолоном приводило не только к стиханию полиартрита, по и к урежению приступов стенокардии. В связи с очередным обострением полиартрита обратился за консультацией в клинику.
Объективно: общее состояние относительно удовлетворительное. Питание значительно понижено. Кожа бледная. Характерная поза «просителя». Значительный кифоз грудного отдела позвоночника. Активные и пассивные движения во всех отделах позвоночника резко ограничены. Имеется умеренная деформация и припухлость суставов кистей, особенно пястнофаланговых справа, ульнарная девиация правой кисти. Мышцы развиты слабо. В легких возрастная эмфизема. Отчетливо выявляется капил-
лярный пульс. Левая |
граница |
сердца |
на 1 см |
кнаружи от |
срединно- |
|||
ключичной |
линии. |
Тоны |
сердца резко |
приглушены. Пульс |
типа celer |
|||
et altus, |
80—84 |
удара |
в |
1 |
мин, ритмичный. |
Артериальное |
давление |
|
140/20—110/0 м мрт. ст. Печень, селезенка, органы пищеварения, мочеполо-
вая система без отклонений |
от нормы. |
|
||
В крови: |
эр,—3 210 |
000, |
л.—7 400, эозин,—0,5%, |
п.—7,5%, с . - 5 8 % , |
лимф — 27%, |
мон.—7%, |
Р О Э — 4 8 мм/ч. Холестерин |
в сыворотке кро- |
|
ви—182 мг%. Реакция Вассермана положительная. Анализы мочи без особенностей. На ЭКГ синусовый ритм. Электрическая ось сердца отклонена влево. Признаки рубцовых изменений миокарда в области задней
стенки левого желудочка на фоне его увеличения. При |
рентгенологиче- |
ском исследовании грудной клетки обнаружены признаки |
эмфиземы лег- |
ких, увеличение сердца влево; аорта развернута, днффузно расширена и незначительно уплотнена. На рентгенограмме позвоночника определяются
основные |
признаки анкилозирующего спондилартрита, которые |
придают |
|
ему вид |
«бамбуковой |
палки». Диагностирован ревматоидный |
артрит |
с преимущественным |
поражением суставов позвоночника (анкилозиру- |
||
ющий спондилартрит Бехтерева—Штрюмпеля—Мари); ревматоидный аортит с развитием недостаточности аортальных клапанов; коронариит; атеросклеротический кардиосклероз.
Больной продолжал амбулаторно принимать предиизолон, что способствовало уменьшению воспалительных изменений в суставах. Однако дальнейшее течение болезни осложнилось присоединением амилоидоза почек с развитием нефротического синдрома, затем почечной недостаточности, от которой больной погиб в 1969 г.
На секции обнаружены амилоидоз почек и селезенки, распространенный атеросклероз с поражением аорты и коронарных артерий, склероз аортальных клапанов с их недостаточностью, значительная гипертрофия мышцы левого желудочка с его дилатацией, явления ревматоидного спондилартрита.
Таким образом, развитие недостаточности аортальных клапанов у больного болезнью Бехтерева на фоне ее прогрессирования с частыми обострениями позволяет отнести этот порок за счет основного заболевания. Одновременно, видимо, имелись явления коронариита (усиление синдрома стенокардии при обострении суставного процесса, отчетливое положительное влияние преднизолона на эти боли).
В последние годы описываются висцеральные поражения (например, ревматоидное легкое), обусловленные «ревматоидной болезнью», с поздним присоединением суставного синдрома или при его отсутствии. Истинный характер висцераль-
8—102 |
113 |

Р и с . 32. Схема истории заболевания больного Р.
ных поражений без суставного синдрома можно распознать лишь при гистологическом исследовании.
Legier (1966) описал больного с выраженной недостаточностью аортальных клапанов с развитием сердечной недостаточности и фатальным исходом. На секции гистологически выявлены изменения, специфичные для ревматоидного кардита, причем прижизненно отсутствовали признаки поражения суставов.
Не исключено развитие порока сердца и |
при |
с и с т е м н о й |
к р а с н о й в о л ч а н к е , с к л е р о д е р м и и |
и |
других кол- |
лагенозах, хотя окончательно высказаться об этиологии порока в таких случаях бывает очень трудно, особенно при развитии митрального стеноза.
Больной Р. (наблюдение 36-е), 29 лет, находился в клинике с июля 1964 г. по январь 1965 г. С 1959 г. (вскоре после возвращения из армии) стал отмечать небольшую одышку при физической нагрузке (рис. 32). В 1961 г. она заметно усилилась, после большого напряжения было кровохарканье. При обследовании в больнице обнаружен митральный порок сердца. Лечили аспирином и пенициллином. Осенью 1961 г. после охлаждения повышалась температура до 39°, было кровохарканье, появились колющие боли в сердце, усилились одышка, общая слабость. Лечили аспирином, валокордином. Продолжал работать в колхозе. В 1962 г. возник синдром Рейно. В 1963 г. состояние ухудшилось: усилилась одышка, появились боли в суставах. Повторно госпитализирован по поводу предполагавшегося обострения ревматического процесса и декомпенсированного порока сердца. Переведен на инвалидность II группы. В течение 1964 г. состояние было неудовлетворительным. Нарастала одышка (по временам появлялось удушье), беспокоили колющие боли в сердце, которые купи-
.114
ровались валокордином. Стал |
отмечать |
изменение |
кожи лица. Направлен |
|
на консультацию в |
Москву. |
|
|
|
Объективно: общее состояние относительно удовлетворительное. Лицо |
||||
маскообразно, кожа |
на нем |
натянута, |
несколько |
уплотнена. Припухлость |
и деформация проксимальных межфаланговых суставов. Положительный симптом Рейно. Кожа пальцев, особенно на кончиках, истончена. Увеличены все периферические лимфатические узлы. В легких хрипов нет, число дыханий 20 в 1 мин. Сердце увеличено во всех направлениях, при аускультации на верхушке I тон усилен, тон открытия митрального клапана, систолический и диастолический шумы, II тон раздвоен. Акцент II тона на легочной артерии. Пульс 88 ударов в 1 мин, ритмичный. Печень увеличена, выступает из-под края реберной дуги на 4 см. Пальпировался край селезенки. В крови: лейкоциты—13 700, формула без особенностей,
РОЭ — 2 |
мм/ч. Анализ мочи нормальный. В сыворотке крови: у-глобули- |
ны — 27%, общий белок — 7,2 г%. |
|
При |
рентгенографии: правый купол диафрагмы деформирован плев- |
ро-диафрагмальной спайкой, синусы свободны. Легочный рисунок в прикорневых зонах усилен, корни легких расширены. Сердце митральной конфигурации за счет выступления конуса легочной артерии, расширено во всех направлениях. В 1-м косом положении пищевод на уровне левого предсердия сужен и смещен кзади. Во 2-м косом положении ретростернальное пространство сужено левыми желудочком и предсердием. Тень аорты уплотнена. На рентгенокимограмме расширены зоны конуса легочной артерии, левого предсердия и желудочков, зубцы сниженной амплитуды, деформированы за счет систолического колена. На ЭКГ: ритм синусовый, правый тип, признаки перегрузки левого предсердия (Р mitrale; рис. 33). Титр анти-О-стрептолизина — 625 ед. При капилляроскопии отмечены атония и дегенерация капилляров.
Назначены преднизолон (максимальная суточная доза 20 мг с очень медленным снижением до поддерживающей дозы 10 мг в сутки), резохин, витамины, адонис. В результате лечения состояние больного значительно улучшилось: исчезли одышка, неприятные ощущения в области сердца, увеличились объем движений в кистях, подвижность и эластичность кожи. Показатели крови нормальные. Изменения со стороны сердца остались прежними, сохранилось небольшое увеличение печени, селезенки, лимфатических узлов. В течение года продолжал принимать преднизолон (10 мг в сутки), причем существенного прогрессирования процесса и явлений сердечной недостаточности не отмечено. Дальнейшая судьба больного неизвестна.
Диагноз: системная склеродермия с поражением сердца (с формированием митрального порока: стеноза и недостаточности митрального клапана), кожи, с гепатолиенальным синдромом, лимфаденопатией, синдромом Рейно.
Мы связываем развитие порока у данного больного со склеродермией, но полностью исключить ревматическую природу его невозможно.
Клапанные пороки сердца при системной склеродермии начали описывать лишь в последние годы. Е. М. Тареев и Н. Т. Гусева (1967) наблюдали 100 больных типичной системной склеродермией, из них у 17 на основании клинических и анатомических данных выявлен порок сердца. У всех этих
больных |
имелась недостаточность митрального |
клапана, у |
|||
3 — недостаточность в |
сочетании |
со стенозом |
митрального |
||
отверстия |
и у |
1, помимо этого, — недостаточность |
аортальных |
||
клапанов. |
У |
9 больных |
диагноз |
порока был поставлен при- |
|
8* |
|
|
115 |
|
|

Р и с. 33. Электрокардиограмма (А) и фонокардиограмма с области верхушки сердца (Б) той же больной:
На ФКГ: |
верхняя кривая — Э К Г во |
II отведении, последующие — ФКГ в диапа- |
зонах |
аускультативных, низких, |
средних-1, средних-2 и высоких частот. |
жизненно, из них 4 умерли и на секции диагноз был подтвержден. Из 16 секционных случаев системной склеродермии порок сердца выявлен в 8 (из них в 4 порок распознан прижизненно). При этом на вскрытии очаговый склероз клапанного и париетального эндокарда был обнаружен еще в 7 случаях. Следовательно, поражение эндокарда различной степени отмечалось в 15 из 16 секционных случаев. Диагно-
стика порока сердца при склеродермии |
затрудняется |
в |
связи |
с нередко преобладающим поражением |
миокарда, |
а |
также |
легких с элементами легочного сердца, что маскирует признаки порока. При этом следует учитывать, что недостаточность митрального клапана может быть относительной ввиду поражения миокарда и расширения полостей сердца.
Пороки сердца чаще наблюдались на фоне развернутой картины склеродермии. Однако у 3 больных порок был обнаружен в начале страдания и расценивался первоначально как проявление ревматизма. Двое из этих больных погибли. Патологоанатомические данные подтвердили склеродермический характер порока, который отличался от ревматического отсутствием резкой деформации клапана и экссудативно-кле- точного компонента даже при выраженной активности процесса.
l ie
