
6 курс / Кардиология / Джон_Кэмм_Болезни_сердца_и_сосудов_2011
.pdfСцинтиграфические исследования точнее, чем нагрузочные тесты, в диагностике многососудистого поражения коронарного русла и обнаружения местоположения и степени ишемии миокарда [102].
Фармакологические нагрузки могут быть использованы в качестве альтернативы у пациентов, которые не могут выполнить физическую нагрузку (например, пожилые или пациенты с заболеванием периферических сосудов или выраженной одышкой) [131]. Они включают в себя симпатомиметик добутамин, который вызывает увеличение потребления кислорода миокардом, моделируя, таким образом, физические упражнения, а также артериальные вазодилататоры - дипиридамол и аденозин, которые из-за феномена обкрадывания вызывают субэндокардиальную гипоперфузию регионов миокарда, ассоциированных со стенозированной венечной артерии.
Диагностическая точность тестов с фармакологическими пробами аналогична таковой при пробе с физической нагрузкой [132]. Последняя, однако, является предпочтительной из-за более очевидного соотношения уровня физической нагрузки с реальной физической активностью пациента, а также дополнительной диагностической и прогностической информации, получаемой по результатам физической нагрузки.
Радионуклидная ангиография использовалась в пре-дыдущие годы для диагностики обструктивной коронарной болезни сердца, но в настоящее время перестала быть популярной, поскольку не добавляет диагностической информации к предоставляемой другими неинвазивными тестами.
СТРЕСС-ЭХОКАРДИОГРАФИЯ
Стресс-ЭхоКГ является альтернативой перфузионной сцинтиграфии миокарда в качестве второго эшелона после стандартной нагрузочной пробы и имеет аналогичные показания и преимущества, включая более надежную диагностику многососудистого поражения и локализации ишемии миокарда [133]. Ее применение в качестве альтернативы нагрузочной пробы сомнительно (см.
табл. 17.6).
Диагностика ИБС по стресс-ЭхоКГ основана на обнаружении стресс-индуцированных обратимых нарушений движения стенки ЛЖ. По сравнению со сцинтиграфией, к неудобствам относятся низкое качество изображения примерно у 15% пациентов, более высокая зависимость интерпретации результов от оператора, более низкая чувствительность (в частности, для однососудистого поражения левой огибающей венечной артерии), необходимость специальной подготовки для правильной работы и интерпретации результатов, затруднения оценки ишемии в базальных отделах ЛЖ. Неспособность к изображению на пике нагрузки является незначительным недостатком, так как нарушения сократимости обычно не нормализуются сразу после прекращения нагрузки.
Стресс-ЭхоКГ, однако, имеет некоторые преимущества по сравнению с перфузионной сцинтиграфией, в том числе большую специфичность, возможность более широкой оценки сердечной анатомии и функции, большую доступность, меньшую стоимость и большую безопасность (отсутствие воздействия радиации).
Фармакологические нагрузки используются в стресс-ЭхоКГ чаще, чем физические. Показания к фармакологичесой стресс-ЭхоКГ такие же, как и для фармакологической сцинтиграфии. У пациентов с негативными результатами часто добавляют атропин либо добутамин (особенно у пациентов, принимающих β-адреноблокаторы) или дипиридамол, которые повышают ЧСС и чувствительность теста.
При сравнении различных стресс-тестов чувствительность стресс-ЭхоКГ с физической нагрузкой и с применением добутамина для диагностики обструктивной ИБС оказалась аналогичной, тогда как чувствительность стресс-ЭхоКГ с применением дипиридамола была ниже, а специфичность не отличались друг от друга [134].
СТРЕСС-МРТ
МРТ стресс-тестирование в сочетании с инфузией добутамина может определить отклонения движения стенок, индуцированные ишемией, и выгодно отличается от стресс-ЭХО с добутамином более высокоим качеством изображения [135] (глава 5). Сообщалось о низкой частоте случаев нормальной МРТ с добутамином [136]. Миокардиальная перфузия при МРТ охватывает весь желудочек с помощью мультиспирального изображения. Хотя этот метод еще находится в процессе разработки, результаты уже хороши по сравнению с другими методами визуализации [137]. Ограниченная доступность, высокая стоимость, а также некоторые трудности, связанные с необходимостью непрерывного контроля за пациентом во время стресс-теста, в настоящее время ограничивает использование данного метода для диагностики в клинической практике.

НЕИНВАЗИВНЫЕ МЕТОДЫ ОЦЕНКИ ВЕНЕЧНЫХ АРТЕРИЙ
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ
Последние значительные достижения в области технологий в большой степени преодолели проблему пространственного разрешения и артефакта движения, которые долгое время являлись сдерживающими факторами для этого типа изображения. Два метода визуализации такого рода включают сверхбыструю томографию, или ЭЛКТ, и МСКТ. Оба эти метода были утверждены для количественной оценки степени коронарной кальцификации, которая более тесно коррелирует с общей тяжестью поражения, чем с локализацией или степенью стеноза [138, 139]. Оценка коронарной кальцификации, однако, не рекомендована в качестве рутинного метода диагностики стабильной стенокардии [102].
Улучшение качества визуализации и разрешения позволяет выполнять коронарографию путем в/в инъекций контрастного вещества с МСКТ и является наиболее перспективной техникой для неинвазивной визуализации венечных артерий. МСКТ-ангиография точно определяет наличие и степень обструктивной ИБС для последующей реваскуляризации пациентов с симптомами. Однако негативное и позитивное прогностическое значение в самых последних сравнительных исследованиях свидетельствует, что КТ-ангиография не может заменить инвазивную коронарную ангиографию в диагностических целях, а кроме того, включает более высокие дозы облучения
[140].
МАГНИТНО-РЕЗОНАНСНАЯ АНГИОГРАФИЯ
Контрастная МРТ-коронарография также позволяет неинвазивно оценить просвет венечных артерий [141] и, кроме того, имеет потенциал для характеристики атеросклеротической бляшки [142] (глава 5). Дополнительным преимуществом методики является то, что она имеет значительный потенциал для оценки общей сердечной анатомии и функции. Однако в настоящее время она по-прежнему не рекомендована для исследований в клинической практике.
ИНВАЗИВНЫЕ МЕТОДЫ
Коронарография
По определению, обструктивная ИБС, являющася причиной стабильной стенокардии, диагноcтируется по наличию стеноза венечной артерии по данным ангиографии. Тем не менее с учетом небольшого, но определенного риска осложнений и ее стоимости, коронарная ангиография не может быть рекомендована как обычная диагностическая процедура для дифференциальной диагностики боли в грудной клетке. Частота осложнений, связанных с рутинной диагностической катетеризацией у больных, составляет 1-2%. Общая смертность от ИМ или инсульта составляет порядка 0,1-0,2%.
Коронарная ангиография (глава 8) в качестве диагностического метода должна проводиться у конкретных пациентов, в том числе:
•у пациентов, которые имеют высокую вероятность необходимости проведения реваскуляризации миокарда;
•у пациентов с высоким риском, перенесших реанимационные мероприятия в связи с развитием ВСС или угрожающих жизни желудочковых аритмий, у которых постановка окончательного диагноза о наличии или отсутствии ишемической болезни необходима для определения дальнейшей тактики ведения;
•у пациентов со стенокардией, у которых диагноз ИБС не подтвержден с помощью неинвазивных методов.
Коронарная ангиография для диагностических целей не должна выполняться:
•больным с ИБС, которые отказываются от реваскуляризации миокарда;
•больным с ИБС, у которых диагноз ИБС явно подтвержден результатами неинвазивного тестирования.
Рекомендации по диагностической коронарной ангиографии приведены в табл. 17.8 Таблица 17.8. Показания к проведению диагностической коронарной ангиографии
Доказательства и/или общее мнение, что диагностическая коронарная ангиография показана
Пациенты с тяжелой стабильной стенокардией (класс 3 или больше по классификации Канадского сердечно-сосудистого общества), несмотря на оптимальное лечение
Пережившие остановку сердца
Пациенты с опасными для жизни нарушениями желудочкового ритма
Пациенты, ранее перенесшие реваскуляризацию миокарда, у которых рано развивается рецидив средней или тяжелой стенокардии
Противоречивые данные и/или расхождение мнений о том, что диагностическая коронарная ангиография показана, но вес доказательств/ мнений в пользу ее необходимости несколько выше
Пациенты с умеренной или высокой претестовой вероятностью ИБС после клинического обследования и неубедительных данных неинвазивного тестирования, или противоречивых результатов различных неинвазивных исследований
Пациенты с высоким риском рестеноза по данным неинвазивных тестов после чрескожных коронарных вмешательств, выполненных в месте, имеющем решающее значение для определения прогноза
Доказательства или общее мнение, что диагностическая коронарография не показана
Пациенты, которым диагноз ИБС достоверно подтвержден с помощью неинвазивных тестов
Пациенты, отказывающиеся от реваскуляризации миокарда
ВНУТРИСОСУДИСТЫЕ ДИАГНОСТИЧЕСКИЕ МЕТОДЫ
УЛЬТРАЗВУКОВОЕ ВНУТРИСОСУДИСТОЕ ИССЛЕДОВАНИЕ
Внутрисосудистое УЗИ позволяет получать изображения венечных артерий при прохождении ультразвукового катетера в просвет венечной артерии (глава 8). Это позволяет точно измерить диаметр просвета венечных артерий, оценить повреждение и степень ремоделирования сосудов, а также оценить степень атероматозного поражения и отложения кальция. Оно также позволяет детально оценить поражение, являющееся мишенью для вмешательства, относительно места, установки и степени дилатации коронарных стентов, а также посттрансплантационную васкулопатию [143]. Эта техника играет важную роль в специализированных медицинских учреждениях, в частности, в качестве дополнения к ЧТА. Таким образом, правильнее было бы использовать ее в конкретных условиях и для исследовательских целей, чем для широкого практического использования в качестве первой линии для исследования ИБС (глава 8) [102].
ИНВАЗИВНЫЕ МЕТОДЫ ОЦЕНКИ ФУНКЦИОНАЛЬНОЙ ТЯЖЕСТИ ПОРАЖЕНИЯ КОРОНАРНЫХ АРТЕРИЙ
Функциональная тяжесть поражения венечных артерий после ангиографии может быть оценена либо путем измерения коронарного резерва с помощью внутрикоронарного допплеровского исследования [144], либо с помощью внутрикоронарного измерения давления кровотока [145,146]. Оба метода включают индукцию гиперемии посредством внутрикоронарной инъекции сосудорасширяющих агентов. Такие физиологические измерения могут облегчить диагностику в случаях промежуточной степени стеноза (визуальная оценка 30-70% в диаметре) и помочь более обоснованному решению относительно целесообразности реваскуляризации. Они не должны, однако, использоваться регулярно [102].
СТРАТИФИКАЦИЯ РИСКА СТАБИЛЬНОЙ СТЕНОКАРДИИ
Данные о прогнозе стабильной ИБС можно получить исходя из клинической картины заболевания и результатов неинвазивных методов обследования. При этом оцениваются два важнейших прогностических фактора, а именно функция ЛЖ, присутствие и степень тяжести ишемии миокарда. В некоторых случаях риск для пациента можно оценить с помощью инвазивного исследования анатомии венечных сосудов.
ОЦЕНКА КЛИНИЧЕСКИХ ДАННЫХ
Степень тяжести и частота приступов боли в грудной клетке имеют значение для оценки прогноза, как и следует из классификации Канадского сердечно-сосудистого общества. Действительно, низкий порог возникновения ангинозного приступа обычно говорит о выраженном снижении резервов коронарного кровотока [147]. Симптомы острой дисфункции ЛЖ в ходе приступа стенокардии, возможно свидетельствующие об обширном характере ишемии миокарда, также ухудшают прогноз. С другой стороны, зависимость между симптомами и степенью тяжести ИБС недостаточно четкая, что ограничивает значимость клинических симптомов для оценки прогноза. Данные физикального осмотра также помогут в оценке риска. Наличие поражения периферических сосудов (сонных артерий или артерий нижних конечностей) у пациентов со стабильной стенокардией повышает риск появления сердечно-сосудистых осложнений в будущем. Кроме того, признаки СН (отражающие функциональную активность ЛЖ) свидетельствуют о неблагоприятном прогнозе.
У всех пациентов с подозрением на ишемическую болезнь, включая стабильную стенокардию, необходимо определить уровень глюкозы крови натощак и также натощак оценить липидный профиль, в том числе общий ХС, ЛПВП, ЛПНП и триглицериды. Результаты анализа позволят определить степень риска для данного пациента и оценить необходимость лечения. Ожирение, и в особенности признаки метаболического синдрома, обычно говорят о неблагоприятном прогнозе как у пациентов с уже установленным диагнозом, так и тех, у которых заболевание протекает бессимптомно. Метаболический синдром может быть подтвержден с помощью измерения окружности талии, АД, уровней ЛПВП, триглицеридов и глюкозы натощак, что предоставляет дополнительные прогностические данные помимо тех, которые доступны при использовании стандартной Фремингемской шкалы риска, причем без значительного увеличения расходов на дополнительные лабораторные исследования. Дальнейшие лабораторные тесты, включая измерение уровней аполипопротеинов, гомоцистеина, липопротеинов, патологии гемостаза и маркеров воспаления, таких как С-реактивный белок, рассматриваются в качестве методов дальнейшего улучшения оценки риска. В последнее время получены данные, что уровень мозгового натрий-уретического пептида позволяет прогнозировать степень риска независимо от возраста, ФВ ЛЖ и обычных факторов риска. На данный момент, однако, дополнительная прогностическая информация, предоставляемая указанными биохимическими маркерами в случаях стабильной стенокардии, представляется достаточно ограниченной. Пока не получено данных о том, что использование этих маркеров сможет значительно улучшить существующие терапевтические стратегии, достаточно убедительных для того, чтобы рекомендовать их для всех пациентов, особенно с учетом высокой стоимости тестов и ограниченной возможности их выполнения.
Присутствие изменений на стандартной ЭКГ в 12 отведениях (в частности Q-волн, стойких изменений волны ST-T), а также признаки увеличения ЛЖ или застоя в малом круге кровообращения, выявляемые при рентгенографии грудной клетки, также относятся к числу прогностически неблагоприятных факторов [148].
Существует достаточно много общедоступных формул, учитывающих множественные факторы риска, для расчета общего риска развития заболевания венечных сосудов или ССЗ у пациентов с отсутствием указанных диагнозов. С другой стороны, эти формулы не подходят для той части популяции, у которой уже отмечаются симптомы. Несмотря на то что уже разработаны шкалы для прогнозирования развития заболевания венечных сосудов, использующие клинические данные, информацию, полученную в ходе нагрузочных проб или их комбинацию, число таких шкал относительно невелико и их применение ограничено группой пациентов, способных выполнять нагрузочные пробы. Существует переработанная версия Фремингемской формулы расчета риска, которая была адаптирована для использования у пациентов с уже существующими ССЗ, но она не позволяет провести четкое различие между первичными проявлениями заболевания венечных сосудов и уже имеющимися симптомами. Информация из баз данных медицинских учреждений (например, Duke database) также была использована для создания номограмм, позволяющих определить абсолютные уровни риска возникновения заболевания венечных сосудов и летальности, используя различные комбинации данных, полученных в ходе неинвазивных
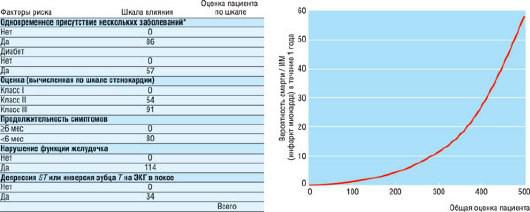
методов обследования и коронарной ангиографии. Однако эти методики оценки, разработанные на основе данных популяционного анализа, полученных около 30 лет назад, не являются специфичными для популяции со стабильной стенокардией и не могут широко использоваться. Сравнительно недавно была разработана Европейская шкала оценки стенокардии, которая представляет собой простой и объективный инструмент, позволяющий рассчитать риск летального исхода или возникновения ИМ, не приводящего к смерти, у пациентов со стабильной стенокардией. Для этого используются шесть прогностических факторов: сопутствующая патология, диабет, оценка стенокардии по шкале, продолжительность симптомов, функция ЛЖ и признаки нарушений реполяризации, выявляемые на ЭКГ в состоянии покоя [1]. Точность прогноза данной шкалы сопоставима с более старыми шкалами, однако она более четко соответствует современной популяции (рис. 17.21).
Рис. 17.21. Слева: оценочный лист расчета риска для пациентов со стабильной стенокардией на основе результатов Европейского исследования стабильной стенокардии (Euro heart survey of stable angina), обзора, проводившегося в 156 кардиологических поликлиниках. Справа: схема, определяющая предполагаемую вероятность смерти или нефатального ИМ в течение ближайшего года от момента обследования в зависимости от сочетания клинических данных и результатов обследования у больных со стабильной стенокардией.* Одно или более цереброваскулярных событий в анамнезе; заболевания печени, такие как хронический гепатит или цирроз печени, или другие заболевания с повышением уровня трансаминаз более чем в три раза от верхней границы нормы; заболевания периферических сосудов, определяющиеся как хромота в покое или при физической нагрузке, ампутация в связи с артериальной сосудистой недостаточностью, сосудистая хирургия (восстановление или шунтирование), или ангиопластика в конечностях, документально подтвержденная аневризма аорты, или признаки нарушения артериального кровотока, полученные неинвазивными методиками обследования; ХПН, требующая хронического диализа или трансплантации почки или приводящая к уровню сывороточного креатинина больше, чем 200 мкмоль/л; хронические заболевания дыхательных путей, определяемые как ранее диагностированные врачом или если пациент получает бронхолитики, или FEV1 ‹75%, PaO2 ‹60%, или PaCO2> 50% по данным предыдущих обследований; хронические воспалительные состояния, определяемые как ревматоидный артрит, системная красная волчанка или другие заболеваниями соединительной ткани, ревматические полимиалгии и так далее; злокачественные новообразования, определяется как диагноз злокачественного процесса в течение последнего года или активное злокачественное новообразование. Изменено (с
разрешения): Daly C.A., De Stavola B., Lopez Sendon J.L. et al. Predicting prognosis in stable angina results from the Euro heart survey of stable angina: prospective observational study // BMJ. - 2006. - Vol. 332. - P. 262-267.
ОЦЕНКА ФУНКЦИИ ЛЕВОГО ЖЕЛУДОЧКА
Наиболее мощным самостоятельным предиктором долговременной выживаемости пациентов со стабильной ИБС считают ФВ ЛЖ. У пациентов со стабильной стенокардией смертность нарастает с уменьшением ФВ. В ходе исследования CASS было установлено, что 12-летняя выживаемость у пациентов с ФВ >50%, 35-49 и ‹35% составляет 73, 45 и 21% соответственно [151]. Клиническая оценка, как отмечалось ранее, может выявить пациентов с симптомами СН, которые вследствие этого составляют группу с существенно более высоким риском сердечно-сосудистых осложнений в будущем. С другой стороны, бессимптомная желудочковая дисфункция встречается не так уж редко, но, как было продемонстрировано, является вдвое более значимым фактором риска, чем
СН с явными симптомами. Поэтому оценка функции ЛЖ крайне желательна для определения степени риска у пациентов со стабильной стенокардией. Наиболее простым способом оценки функции ЛЖ представляется 2D-ЭхоКГ. Однако, вследствие некоторых технических аспектов (неадекватное "эхо-окно"), ЭхоКГ может не позволить правильно оценить функцию ЛЖ примерно у 10% пациентов. В подобных случаях необходимо использование других визуализирующих методик обследования (например, сцинтиграфии или МРТ сердечно-сосудистой системы). В ряде случаев удобнее оценивать функцию ЛЖ с помощью других методов. Например, у пациентов, проходящих нагрузочный тест, визуализация при котором осуществляется с помощью сцинтиграфии или МРТ, функцию ЛЖ можно оценить непосредственно во время теста. Аналогично у пациентов, которым по каким-либо показаниям проводится коронарная ангиография, сократительную функцию ЛЖ можно оценить с помощью ЛЖ-ангиографии, проводимой непосредственно во время инвазивной процедуры.
ОЦЕНКА СТЕПЕНИ МИОКАРДИАЛЬНОЙ ИШЕМИИ
Стресс-ЭКГ служит ключевой методикой для оценки объема сердечной мышцы, который находится в состоянии повышенного риска ишемии. Высокая толерантность к нагрузке при отсутствии ишемии рассматривается как прогностически благоприятный признак [152]. Действительно, по данным исследования CASS, завершение 2-го этапа протокола Брюса в ходе проведения стресс-теста на беговой дорожке и отсутствие ишемии четко ассоциировались с показателем смертности в течение года ‹1% даже при отсутствии терапии антитромбоцитарными препаратами и статинами. Необходимо также отметить, что очень низкая смертность была отмечена у пациентов, которые смогли пройти дальше 4-го этапа протокола Брюса, несмотря на поражение трех сосудов [153].
Возникновение ишемии миокарда во время физических упражнений, в особенности, если она появляется при небольшом уровне нагрузки и сочетается с низкой ФВ, предполагает крайне неблагоприятный прогноз [129]. Особенности ЭКГ, относящиеся к прогностически неблагоприятными признакам, перечислены в табл. 17.9.
Таблица 17.9. Результаты основных неинвазивных стресс-тестов, указывающие на высокую степень риска
ЭКГ с физической нагрузкой |
Депрессия сегмента ST ≥1 мм на 1-й ступени стандартного |
|
протокола Брюса. |
|
Медленное восстановление депрессии ST (>5 мин) после |
|
нагрузки. |
|
Достижение рабочей нагрузки ‹4 MET. |
|
Аномальная реакция АД. |
|
Оценка по шкале Дьюка ≤-11 |
|
|
Сцинтиграфия миокарда с |
Многочисленные и/или крупные и/или серьезные обратимые |
физической нагрузкой |
дефекты перфузии. |
|
Стресс-индуцированная дилатация ЛЖ. |
|
Стресс-индуцированное повышенное поглощение Та201 |
|
легкими |
|
|
Стресс-ЭхоКГ |
Многочисленные и/или крупные и/или серьезные нарушения |
|
регионарной сократимости стенок. |
|
Стресс-индуцированная дилатация ЛЖ |
|
|
Были также предложены комплексные шкалы, принимающие во внимание симптомы, признаки ишемии на ЭКГ, а также другие параметры нагрузочного теста, которые могут применяться для улучшения прогностической стратификации пациентов со стабильной стенокардией. Шкала Дьюка для тредмил-теста [154] (рис. 17.22), разработанная в больших группах пациентов, учитывает толерантность к нагрузке (продолжительность нагрузки), тяжесть ишемии миокарда (максимальная депрессия сегмента ST) и появление приступа стенокардии, и использует следующую формулу для расчета результата:

продолжительность теста (протокол Bruce, в минутах) - (5 × депрессия сегмента ST в ходе нагрузки,
в миллиметрах) - (4 × оценка по шкале стенокардии),
где оценка по шкале стенокардии может принимать значение "0", если приступ во время упражнения не развивается вообще, "1" в том случае, если приступ, возникающий во время теста, не ограничивает его выполнение, и "2" в том случае, когда приступ служит причиной остановки теста.
Рис. 17.22. Номограмма, позволяющая провести примерную оценку прогноза у пациентов с ИБС, подвергшихся стресс-тесту на беговой дорожке по протоколу Брюса. Чтобы получить оценку 5-летней выживаемости или ежегодной смертности (линия "прогноза"), нужно соединить прямой линией значение максимальной депрессии сегмента ST, выявленной в ходе нагрузочного теста (линия "ST-сегмента"), с линией индуцированной нагрузкой "стенокардии", которая будет пересекать линию "ишемии" в определенной точке. Второй линией эту точку нужно соединить с точкой на линии "объем переносимой нагрузки", соответствующей продолжительности нагрузки или MET, достигнутой в ходе проведения теста. Вторая линия пересечет линию "прогноза" в точке, которая и будет соответствовать примерному прогнозу. Здесь же представлена формула расчета индекса теста Дьюка с беговой дорожкой для распределения пациентов в группы с низким, средним и высоким риском (см. подробное описание в тексте). Изменено: Mark D.B., Shaw L., Harrell F.E. Jr. et al. Prognostic value of a treadmill exercise score in outpatients with suspected coronary artery disease // N. Engl. J. Med. - 1991. - Vol. 325. - P. 849-853.
Среди пациентов с подозрением на ИБС две трети тех, у кого отмечалась оценка по шкале Дьюка >5, выживаемость в течение 4 лет составляла 99% (среднегодовой уровень смертности 0,25%). В то же время в "противоположной части спектра" у 4% пациентов с оценкой -11 и менее 4-летняя выживаемость равнялась 79% (среднегодовой уровень смертности 5%) [154].
У пациентов, которые могут выполнять нагрузочные тесты и чьи данные ЭКГ можно успешно интерпретировать, дополнительное прогностическое значение нагрузочных тестов с визуализацией по сравнению с ЭКГ стресс-тестом представляется достаточно ограниченным с клинической точки зрения [155]. Показателями неблагоприятного клинического течения у больных со стабильной стенокардией служат размеры дефекта перфузии и/или проявления дисфункции ЛЖ, обнаруживаемые при радионуклидной сцинтиграфии, а также степень патологического движения стенки ЛЖ, выявляемая при ЭхоКГ и индуцированная физической нагрузкой или фармакологическими "стрессорными факторами" (см. табл. 17.9) [156, 157].
Частые преходящие ишемические эпизоды в течение дня, фиксируемые при ХМ, также рассматриваются как критерии более неблагоприятного прогноза [158]. С другой стороны, то, насколько велика дополнительная информация, предоставляемая этими находками, представляется неясным. Однако амбулаторное ХМ поможет в оценке прогноза у пациентов, которые не могут выполнять нагрузочные тесты.

ОЦЕНКА КОРОНАРОГРАММЫ
Крайне важно понимать, что диагностические методики, позволяющие распознавать атеросклеротические бляшки, которые могут в будущем стать причиной острых коронарных заболеваний, пока отсутствуют [159] (глава 8). Таким образом, в настоящее время основные усилия при определении степени риска сфокусированы на использовании неинвазивных методик обследования. Логика состоит в том, чтобы выявить тех пациентов, у которых восстановление сосудистого кровотока сможет уменьшить уровень смертности.
Было предложено несколько прогностических показателей, связывающих степень тяжести заболевания и вероятность развития острых заболеваний сердца в дальнейшем. Наиболее простой и часто используемый из них предполагает деление пациентов на группы в зависимости от поражения одной, двух, трех или основного ствола левой венечной артерии. Недавно было установлено, что распространенность атеросклеротического поражения, оцениваемая по данным ангиографии, является лучшим прогностическим показателем, чем его тяжесть (т.е. число венечных артерий, имеющих критический стеноз) [160]. Таким образом, более высокая смертность в группе пациентов с множественным поражением артерий по сравнению с теми, у которых поражена лишь одна, по-видимому, является следствием большего количества бляшек, не приводящих к стенозированию вообще или вызывающих умеренный стеноз, однако являющихся потенциальным источником острых коронарных эпизодов. Клиническое применение шкал, основанных на степени выраженности коронарного атеросклероза, по-прежнему представляется ограниченным.
По данным исследования CASS, у пациентов, получавших медикаментозное лечение, уровень 12летней выживаемости составлял 91% при отсутствии поражения венечных артерий, по сравнению с 74% при поражении одной артерии, 59% при поражении двух и 50% при поражении трех артерий [151]. Пациенты с выраженным стенозом основного ствола левой венечной артерии (LM) имеют неблагоприятный прогноз при проведении лечения. Поражение левой передней нисходящей артерии также существенно уменьшает уровень выживаемости. Так, было продемонстрировано, что 5-летняя выживаемость при поражении трех сосудов в сочетании с более чем 95% стенозом левой передней нисходящей артерии составляет 54% по сравнению с 79% при поражении трех сосудов, но без проксимального стеноза левой передней нисходящей артерии [161].
При правильном использовании результаты клинического обследования и неинвазивных тестов предоставляют информацию, достаточную для адекватной оценки вероятности осложнений. Это наиболее соответствует действительности в тех случаях, когда вероятность тяжелого поражения венечных сосудов до проведения обследования представляется низкой. Если оцениваемый среднегодовой риск смертности в результате ССЗ составляет 1%, то эффективность использования коронарографии для выявления тех пациентов, чей прогноз заболевания можно улучшить, будет весьма невелика. С другой стороны, ангиография представляется оправданной для тех пациентов, риск смертности которых составляет более 2% в год. Решение о необходимости использования ангиографии в промежуточной группе пациентов, чей риск сердечно-сосудистой смертности составляет 1-2% в год, должно зависеть от большого количества различных факторов, таких как имеющиеся симптомы, функциональное состояние, образ жизни и род занятий пациента [102], а также сопутствующие заболевания и ответ на первоначальную терапию [162]. Коронарную ангиографию не следует проводить у пациентов, которые отказываются от инвазивных процедур, предпочитают избегать реваскуляризации или не находятся в группе, которой показана реваскуляризация миокарда [162] В табл. 17.10 приводятся рекомендации по использованию коронарной ангиографии для оценки риска.
Таблица 17.10. Рекомендации по стратификации риска по данным коронарной ангиографии
Пациенты, проходящие диагностическую коронарную ангиографию (см. табл. 17.8)
Пациенты с установленным высоким риском неблагоприятного исхода на основе неинвазивных тестов, включая клиническую оценку, оценку объема миокарда с риском возникновения ишемии, а также оценку функции ЛЖ
Пациенты, которым планируется проведение больших внесердечных хирургических вмешательств, особенно в сфере сосудистой хирургии (пластика аневризма аорты, бедренное шунтрование, каротидная эндартерэктомия), а также установлен риск неблагоприятных исходов на основании неинвазивных тестов, включая оценку объема миокарда с риском возникновения ишемии и функции ЛЖ, от среднего до высокого
ЛЕЧЕНИЕ СТАБИЛЬНОЙ СТЕНОКАРДИИ
Терапевтическая стратегия у пациентов со стабильной стенокардией преследует две основные цели. Первая цель состоит в улучшении прогноза путем предотвращения ИМ и смерти. Усилия по предотвращению ИМ и смерти фокусируются преимущественно на снижении частоты возникновения острых коронарных эпизодов и развития дисфункции ЛЖ. Медикаментозное лечение и изменение образа жизни пациента играют важнейшую роль в изменении течения атеросклеротического процесса и "стабилизации" коронарных бляшек, а также уменьшении активации тромбоцитов, фибринолитических и воспалительных изменений, которые способствуют развитию острых коронарных нарушений. Данные лечебные меры могут также замедлить прогрессирование или даже способствовать обратному развитию коронарного атеросклероза. У пациентов с высоким риском осложнений реваскуляризация миокарда предоставляет дополнительную возможность улучшения прогноза с помощью улучшения существующего уровня кровоснабжения.
Вторая цель заключается в уменьшении или ликвидации симптомов с помощью антиангинальных препаратов и использовании реваскуляризации у тех пациентов, у которых медикаментозная терапия оказывается неэффективной.
СПОСОБЫ УЛУЧШЕНИЯ ПРОГНОЗА: ИЗМЕНЕНИЕ ОБРАЗА ЖИЗНИ
Основные изменения образа жизни, которые способны привести к улучшению клинического прогноза ИБС, приведены в табл. 17.11.
Таблица 17.11. Рекомендации по изменению образа жизни
Прекращение курения
Оценка статуса курения и совет бросить курить и избегать пассивного курения
Бупропион, варениклин или никотин для лечения пациентов, которые бросают курить
Физическая активность
Физические аэробные упражнения умеренной интенсивности по крайней мере пять раз в неделю
Для больных высокого риска - программы реабилитации под медицинским наблюдением
Диета и снижение массы тела
Снижение массы тела, ИМТ ‹25 кг/м2 и окружности талии ‹102/88 см (мужчины/женщины)
Диета, основанная на низком потреблении соли и насыщенных жиров, а также регулярном употреблении фруктов, овощей и рыбы
Умеренное употребление алкогольных напитков не следует запрещать
КУРЕНИЕ
Существует множество доказательств негативного влияния курения на состояние здоровья. Курение уже сейчас убивает 1 из 10 взрослых, а к 2030 г. будет являться причиной смерти 10 млн человек в год [163]. Отрицательный эффект курения зависит от количества выкуриваемого в день табака и общего "стажа" курения [164]. Курение влияет на сердечно-сосудистую систему однонаправленно с другими факторами риска, такими как возраст, пол, артериальная гипертензия и диабет. Пассивное курение, как было обнаружено, также увеличивает риск ИБС. Курение в течение длительного времени приводит к нарушению эндотелий-зависимой способности венечных сосудов к расширению [165]. Усиливающаяся в связи с курением агрегация тромбоцитов и формирование тромбоцитарных тромбов могут являться причиной острых коронарных нарушений
