
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ 89
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •1.2.1 Радикало-функциональная номенклатура
- •1.2.2 Систематическая (заместительная) номенклатура
- •1.3 Вопросы и упражнения для самопроверки:
- •2. ИЗОМЕРИЯ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ
- •2.1 Структурная изомерия
- •2.2 Стереоизомерия
- •2.2.1.1 Геометрическая изомерия или цис-транс-изомерия один из видов стереоизомерии, возникающий при разном расположении одинаковых заместителей по одну или по разные стороны плоскости π связи или неароматического цикла (Рис.2.1).
- •2.2.1.2 Хиральность.
- •2.2.1.3 Оптическая изомерия. Энантиомеры и диастереомеры
- •2.2.1.4 Относительная и абсолютная конфигурации
- •2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
- •2.3 Вопросы и упражнения для самопроверки
- •3.1. Образование ковалентных связей
- •3.2.3 Ароматичность
- •3.3 Взаимное влияние атомов в молекуле
- •3.3.1 Индуктивный эффект
- •3.3.2 Мезомерный эффект
- •3.4. Вопросы и упражнения для самопроверки
- •4. КИСЛОТНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •4.1 Теория Бренстеда-Лоури, протолитическая
- •4.2. Вопросы и упражнения для самопроверки
- •5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- •5.1 Механизмы органических реакций
- •5.2.1 Гидратация алкенов. Роль кислотного катализатора
- •5.2.2 Реакции присоединения к асимметричным алкенам (правило Марковникова)
- •5.2.3 Реакция присоединения к α, β-ненасыщенным карбонильным соединениям
- •5.3.1 Галогенирование бензола
- •5.3.2 Ориентирующее действие заместителей в бензольном ядре. Ориентанты первого и второго рода
- •5.4 Нуклеофильное замещение у насыщенного атома углерода
- •5.5 Механизм и стереохимия реакций элиминирования (Е)
- •5.6 Окисление и восстановление органических соединений
- •5.6.1 Окисление гидроксильных и оксо-групп
- •5.6.2 Окисление непредельных и ароматических соединений
- •5.6.3 Реакции восстановления
- •5.6.4 Обратимые окислительно-восстановительныесистемы
- •5.7. Вопросы и упражнения для самопроверки
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- •6.1 Способы получения альдегидов и кетонов
- •6.2 Химические свойства альдегидов и кетонов (карбонильных соединений)
- •6.2.1 Реакция альдегидов с нуклеофилами
- •6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
- •6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
- •6.2.2 Реакции конденсации
- •6.2.2.1 Кето-енольная таутомерия альдегидов и кетонов. Альдольное присоединение
- •6.2.2.2 Кротоновая конденсация или альдольно - кротоновая конденсация
- •6.3 Окисление и восстановление альдегидов и кетонов
- •6.4 Вопросы и упражнения для самопроверки
- •7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- •7.1. Основные пути получения карбоновых кислот:
- •7.2. Малоновый синтез карбоновых кислот
- •7.3. Классификация карбоновых кислот
- •7.4 Химические свойства карбоновых кислот
- •7.4.2. Восстановление карбоновых кислот
- •7.4.3. Декарбоксилирование карбоновых кислот
- •7.5. Дикарбоновые кислоты
- •7.6. Угольная кислота и ее производные
- •7.7. Вопросы и упражнения для самопроверки
- •8. ПОЛИ- И ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ
- •8.1. Аминоспирты
- •8.2 Классификация одноосновных гидроксикислот
- •8.2.1 Получение гидроксикислот
- •8.2.2 Специфические реакции гидроксикислот
- •8.3. Многоосновные гидроксикислоты
- •8.4. Оксокислоты
- •8.5 Вопросы и упражнения для самопроверки
- •9. АМИНОКИСЛОТЫ
- •9.1. Изомерия аминокислот
- •9.2. Классификации аминокислот
- •9.2.1. Классификации аминокислот по биологической ценности
- •9.2.2. Классификации аминокислот на основе химического строения аминокислот
- •9.2.2.3. Современная классификация α-аминокислот
- •9.4. Кислотно-основные свойства аминокислот
- •9.5. Способы получения аминокислот
- •9.6. Химические свойства
- •9.7. Специфические реакции α, β, γ, δ-аминокислот
- •9.8. Качественные реакции на аминокислоты, пептиды, белки.
- •9.9. Методы количественного определения аминокислот
- •9.10. Редко встречающиеся аминокислоты
- •9.11.2 Вторичная структура полипептидной цепи
- •9.11.3 Третичная структура белков
- •9.12. Вопросы и упражнения для самопроверки
- •Классификация углеводов
- •10.1. Моносахариды, классификация
- •10.2. Циклическое строение моносахаридов
- •10.3. Химические свойства моносахаридов
- •10.3.1. Реакции полуацетального гидроксила
- •10.3.3. Окисление и восстановление моносахаридов
- •10.3.4. Изомеризация в щелочной среде
- •10.4. Качественные реакции моносахаридов. Отличительные реакции пентоз и гексоз
- •10.5. Производные моносахаридов
- •10.6. Олигосахариды
- •10.6.1. Химические свойства олигосахаридов
- •10.7. Полисахариды
- •10.7.1. Гомополисахариды
- •10.7.2. Гетерополисахариды
- •10.8. Гликопротеины
- •10.9. Вопросы и упражнения для самопроверки
- •11. БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •11.1. Пятичленные ароматические гетероциклы
- •11.2. Шестичленный ароматический гетероцикл
- •11. 3. Нуклеиновые кислоты (НК)
- •11.3.1 Нуклеозиды
- •11.3.2. Нуклеотиды
- •11.3.3. Нуклеозидциклофосфаты
- •11.3.4. Рибо- и дезокси-рибонуклеиновые кислоты
- •11.4. Вопросы и упражнения для самопроверки
- •12. ЛИПИДЫ
- •12.1. Высшие жирные кислоты
- •12.2. Классификация омыляемых липидов
- •12.2.1. Простые липиды
- •12.2.1.1.Химические свойства простых липидов
- •12.2.2 Сложные липиды
- •12.2.2.2. Гликолипиды
- •12.3. Неомыляемые липиды
- •12.3.1 Терпены (изопреноиды)
- •12.3.3. Стероиды
- •12.4. Вопросы и упражнения для самопроверки
- •13. Методы, используемые для изучения соединений в органической химии
- •Литература
При составлении названия пептида входящие в его состав аминокислотные остатки перечисляются последовательно, начиная с N-концевой, (несущей свободную α-аминогруппу) (табл. 9.1). С-концевой называется аминокислотный остаток, несущий свободную α-карбоксильную группу. При этом втривиальных названиях аминокислот окончание «ин» заменяется на «ил» за исключением C- концевого остатка. Нумерация аминокислотных остатков, входящих в пептиды, начинается с N-конца.
9.7. Специфические реакции α, β, γ, δ-аминокислот
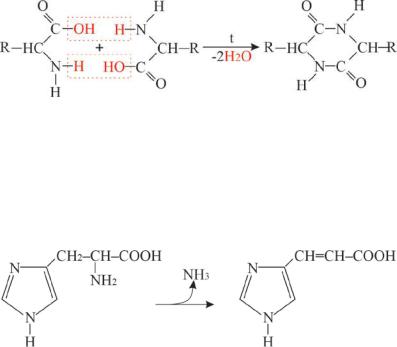
а) Специфические реакции α-аминокислот. α – аминокислоты при нагревании подвергаются межмолекулярной дегидратации с образованием дикетопиперазинов(циклический дипептид, диамид):
α – аминокислоты |
дикетопиперазин |
б) Внутримолекулярное дезаминирование
В животном организме под действием фермента гистидиндезаминазыпроисходитобразованиеаммиакаиуроканиновой кислоты из гистидина и в смывах с кожи человека можно обнаружить соли урокановой кислоты (уроканата):
гистидин |
уроканиновая кислота |
150
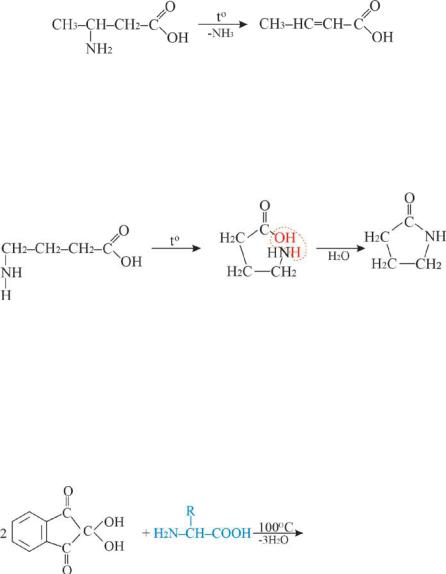
Внутримолекулярное дезаминирование β-аминокислот с образованием α,β -ненасыщенных кислот характерно для бактерий и растений:
β-аминомасляная кислота |
кротоновая кислота |
в) Специфические реакции γ, δ-аминокислот
γ, δ - аминокислоты при нагревании подвергаются внутримолекулярной дегидратации с образованием циклических амидов (лактамов). В случае γ – аминомасляной кислоты образуется γ –бутиролактам:
γ – аминомасляная |
γ –бутиролактам |
|
кислота |
||
|
9.8. Качественные реакции на аминокислоты, пептиды, белки.
Аминокислоты можно обнаружить с помощью цветных реакций. Общая качественная реакция α-аминокислот – это реакция со спир-
товым раствором нингидрина (нингидринная реакция). Продукт реакцииимеетсине-фиолетовое окрашивание, интенсивность которого зависит от концентрации аминокислот:
α-аминокислота
нингидрин
151
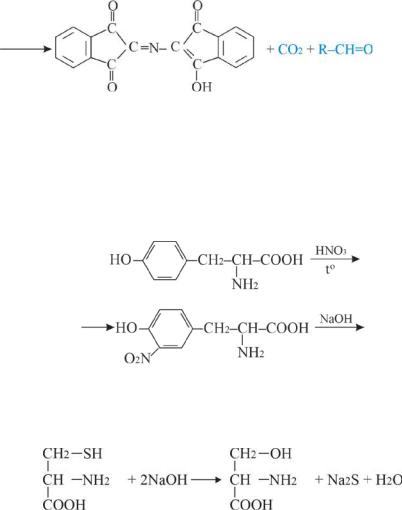
сине-фиолетовое окрашивание |
альдегид |
Ксантопротеиноваяреакцияслужитдляобнаружениянекоторых ароматических α-аминокислот (фенилаланин, тирозин). При действии концентрированной азотной кислотой на тирозин образуется нитросоединение, окрашенное в жёлтый цвет; при добавлении NаОН окраска становится оранжевой.
тирозин
продукт
оранжевого
цвета
нитротирозин
Реакция Фоля - реакция служит для определения α-аминокислот, содержащих SH-группы (цистеин).
(CH3COO)2Pb + 2NaOH → Pb(ONa)2 + 2CH3COOH Na2S + Pb(ONa)2 + 2H2O → PbS↓ + 4NaOH
черный осадок сульфида свинца
152
9.9. Методы количественного определения аминокислот
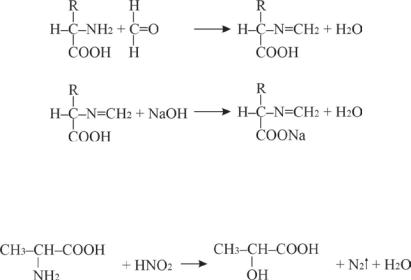
Метод Серенсена (формольное титрование) основан на связывании формальдегидом свободных аминогрупп и алкалиметрическомтитрованииэквивалентного количества карбоксильных групп:
Метод количественного определения аминокислот Ван Слайка позволяет определять небольшие количества аминокислот в крови и прочих биологических материалах по объему выделившегося азота:
При этом образуется α-гидроксикислота и выделяется газообразный азот, по объёму которого судят о количестве вступившей в реакцию α-аминокислоты.
Для разделения аминокислот, образовавшихся врезультате гидролиза полипептидов, с последующей количественной детекцией, Э. Фишер предложил использоватьфракционную вакуумнуюперегонку их эфиров, однако данный метод в настоящее время не имеет широкого применения.
153
