
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ 89
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •1.2.1 Радикало-функциональная номенклатура
- •1.2.2 Систематическая (заместительная) номенклатура
- •1.3 Вопросы и упражнения для самопроверки:
- •2. ИЗОМЕРИЯ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ
- •2.1 Структурная изомерия
- •2.2 Стереоизомерия
- •2.2.1.1 Геометрическая изомерия или цис-транс-изомерия один из видов стереоизомерии, возникающий при разном расположении одинаковых заместителей по одну или по разные стороны плоскости π связи или неароматического цикла (Рис.2.1).
- •2.2.1.2 Хиральность.
- •2.2.1.3 Оптическая изомерия. Энантиомеры и диастереомеры
- •2.2.1.4 Относительная и абсолютная конфигурации
- •2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
- •2.3 Вопросы и упражнения для самопроверки
- •3.1. Образование ковалентных связей
- •3.2.3 Ароматичность
- •3.3 Взаимное влияние атомов в молекуле
- •3.3.1 Индуктивный эффект
- •3.3.2 Мезомерный эффект
- •3.4. Вопросы и упражнения для самопроверки
- •4. КИСЛОТНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •4.1 Теория Бренстеда-Лоури, протолитическая
- •4.2. Вопросы и упражнения для самопроверки
- •5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- •5.1 Механизмы органических реакций
- •5.2.1 Гидратация алкенов. Роль кислотного катализатора
- •5.2.2 Реакции присоединения к асимметричным алкенам (правило Марковникова)
- •5.2.3 Реакция присоединения к α, β-ненасыщенным карбонильным соединениям
- •5.3.1 Галогенирование бензола
- •5.3.2 Ориентирующее действие заместителей в бензольном ядре. Ориентанты первого и второго рода
- •5.4 Нуклеофильное замещение у насыщенного атома углерода
- •5.5 Механизм и стереохимия реакций элиминирования (Е)
- •5.6 Окисление и восстановление органических соединений
- •5.6.1 Окисление гидроксильных и оксо-групп
- •5.6.2 Окисление непредельных и ароматических соединений
- •5.6.3 Реакции восстановления
- •5.6.4 Обратимые окислительно-восстановительныесистемы
- •5.7. Вопросы и упражнения для самопроверки
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- •6.1 Способы получения альдегидов и кетонов
- •6.2 Химические свойства альдегидов и кетонов (карбонильных соединений)
- •6.2.1 Реакция альдегидов с нуклеофилами
- •6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
- •6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
- •6.2.2 Реакции конденсации
- •6.2.2.1 Кето-енольная таутомерия альдегидов и кетонов. Альдольное присоединение
- •6.2.2.2 Кротоновая конденсация или альдольно - кротоновая конденсация
- •6.3 Окисление и восстановление альдегидов и кетонов
- •6.4 Вопросы и упражнения для самопроверки
- •7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- •7.1. Основные пути получения карбоновых кислот:
- •7.2. Малоновый синтез карбоновых кислот
- •7.3. Классификация карбоновых кислот
- •7.4 Химические свойства карбоновых кислот
- •7.4.2. Восстановление карбоновых кислот
- •7.4.3. Декарбоксилирование карбоновых кислот
- •7.5. Дикарбоновые кислоты
- •7.6. Угольная кислота и ее производные
- •7.7. Вопросы и упражнения для самопроверки
- •8. ПОЛИ- И ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ
- •8.1. Аминоспирты
- •8.2 Классификация одноосновных гидроксикислот
- •8.2.1 Получение гидроксикислот
- •8.2.2 Специфические реакции гидроксикислот
- •8.3. Многоосновные гидроксикислоты
- •8.4. Оксокислоты
- •8.5 Вопросы и упражнения для самопроверки
- •9. АМИНОКИСЛОТЫ
- •9.1. Изомерия аминокислот
- •9.2. Классификации аминокислот
- •9.2.1. Классификации аминокислот по биологической ценности
- •9.2.2. Классификации аминокислот на основе химического строения аминокислот
- •9.2.2.3. Современная классификация α-аминокислот
- •9.4. Кислотно-основные свойства аминокислот
- •9.5. Способы получения аминокислот
- •9.6. Химические свойства
- •9.7. Специфические реакции α, β, γ, δ-аминокислот
- •9.8. Качественные реакции на аминокислоты, пептиды, белки.
- •9.9. Методы количественного определения аминокислот
- •9.10. Редко встречающиеся аминокислоты
- •9.11.2 Вторичная структура полипептидной цепи
- •9.11.3 Третичная структура белков
- •9.12. Вопросы и упражнения для самопроверки
- •Классификация углеводов
- •10.1. Моносахариды, классификация
- •10.2. Циклическое строение моносахаридов
- •10.3. Химические свойства моносахаридов
- •10.3.1. Реакции полуацетального гидроксила
- •10.3.3. Окисление и восстановление моносахаридов
- •10.3.4. Изомеризация в щелочной среде
- •10.4. Качественные реакции моносахаридов. Отличительные реакции пентоз и гексоз
- •10.5. Производные моносахаридов
- •10.6. Олигосахариды
- •10.6.1. Химические свойства олигосахаридов
- •10.7. Полисахариды
- •10.7.1. Гомополисахариды
- •10.7.2. Гетерополисахариды
- •10.8. Гликопротеины
- •10.9. Вопросы и упражнения для самопроверки
- •11. БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •11.1. Пятичленные ароматические гетероциклы
- •11.2. Шестичленный ароматический гетероцикл
- •11. 3. Нуклеиновые кислоты (НК)
- •11.3.1 Нуклеозиды
- •11.3.2. Нуклеотиды
- •11.3.3. Нуклеозидциклофосфаты
- •11.3.4. Рибо- и дезокси-рибонуклеиновые кислоты
- •11.4. Вопросы и упражнения для самопроверки
- •12. ЛИПИДЫ
- •12.1. Высшие жирные кислоты
- •12.2. Классификация омыляемых липидов
- •12.2.1. Простые липиды
- •12.2.1.1.Химические свойства простых липидов
- •12.2.2 Сложные липиды
- •12.2.2.2. Гликолипиды
- •12.3. Неомыляемые липиды
- •12.3.1 Терпены (изопреноиды)
- •12.3.3. Стероиды
- •12.4. Вопросы и упражнения для самопроверки
- •13. Методы, используемые для изучения соединений в органической химии
- •Литература
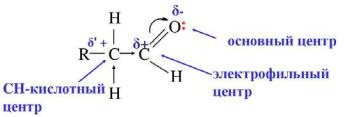
Рис. 6.1 Схема реакционных центров карбонильных соединений
Реакции альдегидов и кетонов можно подразделить на несколько типов в зависимости от характера реагента:
а) реакции альдегидов и кетонов с нуклеофилами (электронное строение карбонильной группы в альдегидах и кетонах обусловли-
вает реакции присоединения с атакой нуклеофила на атом углерода),
б) кето-енольная таутомерия и альдольное присоединение в основной среде, обусловленные подвижным α -водородом,
в) окисление альдегидов и кетонов.
6.2.1 Реакция альдегидов с нуклеофилами
При взаимодействии альдегидов с нуклеофильным реагентом может происходить реакция присоединения или реакция конденсации (тоестьсотщеплениемводыилиспирта).Обатипапревращенийимеют обшую начальную стадию процесса, которая заключается в нуклеофильной атаке на углерод карбонильной группы. Двойная связь между атомами углерода и кислорода поляризована в связи с большой разницей в электроотрицательности данных атомов. В результате поляризации карбонильной группы на атоме углерода возникает частичный положительный заряд.
91
6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
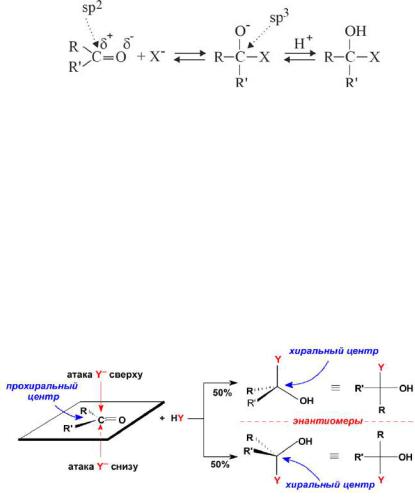
Рассмотрим механизм присоединения Н–X к карбонильным соединениям:
карбонильное нуклеофил соединение
Если соединение Н–X ионизировано на Н+ и X–, нуклеофильная группа X– передаёт свободную пару электронов карбонильному углероду, то есть происходит атака более эффективного нуклеофила X– на карбонильный углерод. Одновременно происходит перемещение π- связи к атому кислорода и миграция протона к отрицательно заряжённому кислороду.
Нуклеофильные агенты атакуют карбонильные соединения перпендикулярно плоскостидвойнойсвязи(Рис.6.2). Есливрезультате присоединения формируется хиральный центр, продуктами реакции будут энантиомеры:
Рис. 6.2 Схема реакции присоединения к альдегидам и асимметричным кетонам
92
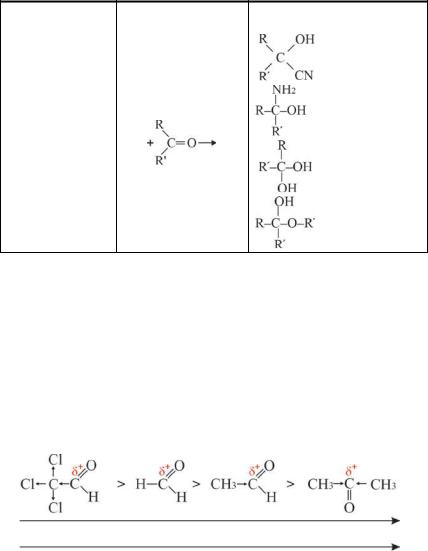
Таблица 6.1
Реакции присоединения альдегидов и кетонов
H – X |
Альдегид или |
Продукт реакции |
|
кетон |
|||
|
|
||
H – C ≡ N |
|
|
|
|
|
цианогидрин |
|
H –NH2 |
|
|
|
|
|
аминоспирт |
|
H – OH |
|
|
|
|
|
гем-диол |
|
H – O –R'' |
|
|
|
|
|
полуацеталь |
Примечание: R, R' = алкил или Н
По этому механизму протекают реакции присоединения с соединениями, представленными в табл. (Табл. 6.1).
Факторы, влияющие на реакционноспособность альдегидов и кетонов:
а) Увеличение частичного положительного заряда (δ+) на карбонильном атоме углерода в результате отрицательного индуктивного эффекта заместителей повышает активность альдегидов и кетонов и наоборот:
уменьшение δ+ на карбонильном углероде уменьшение реакционной способности
-I CCl3 IH=0 +IR(R=Alk) +I эффект двух групп R(R=Alk)
93
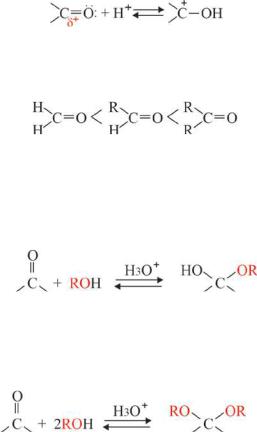
б) Влияние кислотного катализатора: в кислой среде активность карбонильной группы резко увеличивается, поскольку вследствие протонирования кислорода на атоме углерода возникает полный положительный заряд:
в) Увеличение пространственной затрудненности для нуклеофильнойатаки,наличиеобъемныхзаместителейукарбонильногоатома углерода:
6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
Полуацетали и ацетали образуютсявреакцииальдегидаиликетона с первичным спиртом (по механизму AN присоединения):
полуацеталь
В присутствии кислотного катализатора полуацетали реагируют со спиртом далее, давая ацетали – диалкиловые эфиры диола:
ацеталь
Реакция ацетализации идет в две стадии: на первом этапе ацетализации молекула спирта присоединяется к альдегиду или кетону с разрывом двойной связи при карбонильной группе с образованием неполного простого эфира – полуацеталя.
94
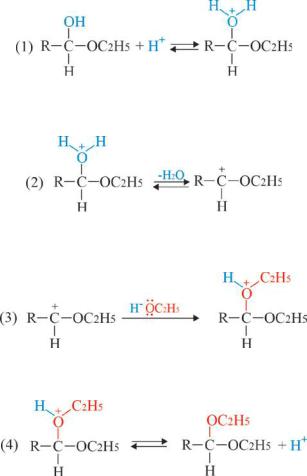
Механизм образования ацеталей
Процесс идет в несколько стадий. В присутствии кислотного катализатора происходит протонирование гидроксильной группы полуацеталя с образованием иона оксония (1):
В результате элиминации молекулы воды на атоме углерода образуется полный положительный заряд (карбкатион, (2)):
К карбкатиону присоединяется вторая молекула спирта по механизму нуклеофильного присоединения (3):
Процесс завершается отщеплением протона и образованием ацеталя – диалкилового эфира диола (4).
Возможно также образование циклических полуацеталей в том случае, когда молекулы содержат как карбонильную группу, так и
95
