
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ 89
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •1.2.1 Радикало-функциональная номенклатура
- •1.2.2 Систематическая (заместительная) номенклатура
- •1.3 Вопросы и упражнения для самопроверки:
- •2. ИЗОМЕРИЯ. ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ
- •2.1 Структурная изомерия
- •2.2 Стереоизомерия
- •2.2.1.1 Геометрическая изомерия или цис-транс-изомерия один из видов стереоизомерии, возникающий при разном расположении одинаковых заместителей по одну или по разные стороны плоскости π связи или неароматического цикла (Рис.2.1).
- •2.2.1.2 Хиральность.
- •2.2.1.3 Оптическая изомерия. Энантиомеры и диастереомеры
- •2.2.1.4 Относительная и абсолютная конфигурации
- •2.2.2.2 Конформации циклических алифатических соединений. Теория напряжения Байера
- •2.3 Вопросы и упражнения для самопроверки
- •3.1. Образование ковалентных связей
- •3.2.3 Ароматичность
- •3.3 Взаимное влияние атомов в молекуле
- •3.3.1 Индуктивный эффект
- •3.3.2 Мезомерный эффект
- •3.4. Вопросы и упражнения для самопроверки
- •4. КИСЛОТНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- •4.1 Теория Бренстеда-Лоури, протолитическая
- •4.2. Вопросы и упражнения для самопроверки
- •5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- •5.1 Механизмы органических реакций
- •5.2.1 Гидратация алкенов. Роль кислотного катализатора
- •5.2.2 Реакции присоединения к асимметричным алкенам (правило Марковникова)
- •5.2.3 Реакция присоединения к α, β-ненасыщенным карбонильным соединениям
- •5.3.1 Галогенирование бензола
- •5.3.2 Ориентирующее действие заместителей в бензольном ядре. Ориентанты первого и второго рода
- •5.4 Нуклеофильное замещение у насыщенного атома углерода
- •5.5 Механизм и стереохимия реакций элиминирования (Е)
- •5.6 Окисление и восстановление органических соединений
- •5.6.1 Окисление гидроксильных и оксо-групп
- •5.6.2 Окисление непредельных и ароматических соединений
- •5.6.3 Реакции восстановления
- •5.6.4 Обратимые окислительно-восстановительныесистемы
- •5.7. Вопросы и упражнения для самопроверки
- •6. ОСНОВНЫЕ КЛАССЫ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- •6.1 Способы получения альдегидов и кетонов
- •6.2 Химические свойства альдегидов и кетонов (карбонильных соединений)
- •6.2.1 Реакция альдегидов с нуклеофилами
- •6.2.1.1 Особенности реакций присоединения к альдегидам и асимметричным кетонам
- •6.2.1.2. Реакции присоединения спиртов. Образование полуацеталей и ацеталей
- •6.2.2 Реакции конденсации
- •6.2.2.1 Кето-енольная таутомерия альдегидов и кетонов. Альдольное присоединение
- •6.2.2.2 Кротоновая конденсация или альдольно - кротоновая конденсация
- •6.3 Окисление и восстановление альдегидов и кетонов
- •6.4 Вопросы и упражнения для самопроверки
- •7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- •7.1. Основные пути получения карбоновых кислот:
- •7.2. Малоновый синтез карбоновых кислот
- •7.3. Классификация карбоновых кислот
- •7.4 Химические свойства карбоновых кислот
- •7.4.2. Восстановление карбоновых кислот
- •7.4.3. Декарбоксилирование карбоновых кислот
- •7.5. Дикарбоновые кислоты
- •7.6. Угольная кислота и ее производные
- •7.7. Вопросы и упражнения для самопроверки
- •8. ПОЛИ- И ГЕТЕРОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ
- •8.1. Аминоспирты
- •8.2 Классификация одноосновных гидроксикислот
- •8.2.1 Получение гидроксикислот
- •8.2.2 Специфические реакции гидроксикислот
- •8.3. Многоосновные гидроксикислоты
- •8.4. Оксокислоты
- •8.5 Вопросы и упражнения для самопроверки
- •9. АМИНОКИСЛОТЫ
- •9.1. Изомерия аминокислот
- •9.2. Классификации аминокислот
- •9.2.1. Классификации аминокислот по биологической ценности
- •9.2.2. Классификации аминокислот на основе химического строения аминокислот
- •9.2.2.3. Современная классификация α-аминокислот
- •9.4. Кислотно-основные свойства аминокислот
- •9.5. Способы получения аминокислот
- •9.6. Химические свойства
- •9.7. Специфические реакции α, β, γ, δ-аминокислот
- •9.8. Качественные реакции на аминокислоты, пептиды, белки.
- •9.9. Методы количественного определения аминокислот
- •9.10. Редко встречающиеся аминокислоты
- •9.11.2 Вторичная структура полипептидной цепи
- •9.11.3 Третичная структура белков
- •9.12. Вопросы и упражнения для самопроверки
- •Классификация углеводов
- •10.1. Моносахариды, классификация
- •10.2. Циклическое строение моносахаридов
- •10.3. Химические свойства моносахаридов
- •10.3.1. Реакции полуацетального гидроксила
- •10.3.3. Окисление и восстановление моносахаридов
- •10.3.4. Изомеризация в щелочной среде
- •10.4. Качественные реакции моносахаридов. Отличительные реакции пентоз и гексоз
- •10.5. Производные моносахаридов
- •10.6. Олигосахариды
- •10.6.1. Химические свойства олигосахаридов
- •10.7. Полисахариды
- •10.7.1. Гомополисахариды
- •10.7.2. Гетерополисахариды
- •10.8. Гликопротеины
- •10.9. Вопросы и упражнения для самопроверки
- •11. БИОЛОГИЧЕСКИ АКТИВНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- •11.1. Пятичленные ароматические гетероциклы
- •11.2. Шестичленный ароматический гетероцикл
- •11. 3. Нуклеиновые кислоты (НК)
- •11.3.1 Нуклеозиды
- •11.3.2. Нуклеотиды
- •11.3.3. Нуклеозидциклофосфаты
- •11.3.4. Рибо- и дезокси-рибонуклеиновые кислоты
- •11.4. Вопросы и упражнения для самопроверки
- •12. ЛИПИДЫ
- •12.1. Высшие жирные кислоты
- •12.2. Классификация омыляемых липидов
- •12.2.1. Простые липиды
- •12.2.1.1.Химические свойства простых липидов
- •12.2.2 Сложные липиды
- •12.2.2.2. Гликолипиды
- •12.3. Неомыляемые липиды
- •12.3.1 Терпены (изопреноиды)
- •12.3.3. Стероиды
- •12.4. Вопросы и упражнения для самопроверки
- •13. Методы, используемые для изучения соединений в органической химии
- •Литература
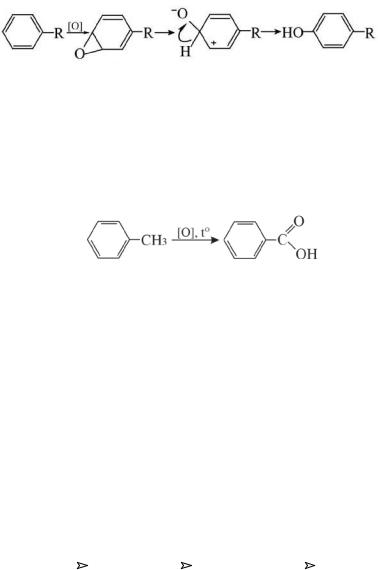
эпоксид σ-комплекс
В основном ароматическое кольцо довольно устойчиво к окислению.Усоединений,имеющихалифатическиебоковыецепи,окислению подвергается α-углеродный атом боковой цепи. Так, например, толуол обладает гораздо меньшей токсичностью, чем бензол, поскольку окисляется в организме в бензойную кислоту, которая ввиду высокой полярности сравнительно быстро выводится из организма:
толуол |
бензойная кислота |
5.6.3 Реакции восстановления
Реакции восстановления обратны тем, что мы рассмотрели выше. Например, при участии НАДН in vivo протекает реакция превращения альдегидов в спирты. В результате восстановления альдегидов образуются первичные спирты, а кетонов – вторичные. Кофермент НАДН поставляет гидрид ион (Н–), а протон берётся из среды и т.д.
Несколько другим путём происходит восстановление нитросоединений. Этот процесс характерен для лекарственных средств ряда нитрофурана, группы широкоиспользуемых антибактериальных средств,
в которых в результате биотрансформации происходит восстановление нитрогруппы до аминогруппы через нитрозо- и гидроксиламинное производные:
R |
|
NO |
2 |
[H] |
R |
|
N |
|
O |
[H] |
|
R |
|
NH |
|
OH |
[H] |
R |
|
NH |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|||
|
нитро- |
нитрозо- |
|
гидроксиламинное- |
амино- |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
производные |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
85 |
|
|
|
|
|
|
|
|
|
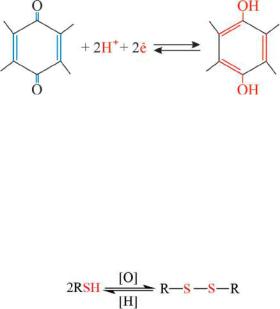
5.6.4 Обратимые окислительно-восстановительныесистемы
К обратимым окислительно-восстановительным системам относятся соединения, имеющие в своем составе гидрохинон-хинон и тиол-дисульфид, представленные окисленной и восстановленной формами глутатиона, которые участвуют в биологически важных процессах. Система хинон-гидрохинон в составе кофермента Q участвуетвпереносеэлектроноввмитохондриях(вдыхательнойцепи). При окислении гидрохинона (двухатомного фенола) образуется циклический ненасыщенный кетон – 1,4-бензохинон, который называют просто хиноном:
хинон |
гидрохинон |
|
(парахинон) |
||
|
||
окислитель |
восстановитель |
|
(окисленная форма) |
(восстановленная форма ) |
Вобратной реакции хинон принимает два электрона и два протона
ивосстанавливается в гидрохинон.
Важную роль в функционировании глутатиона-трипептида, содержащего цистеин, и формировании пространственной структуры белков играют обратимые окислительно-восстановительные системы тиолдисульфид:
тиол дисульфид
Тиолы легко подвергаются окислению с образованием дисульфидов. Так, из двух молекул α-аминокислоты цистеина получается α- аминокислота цистин:
86
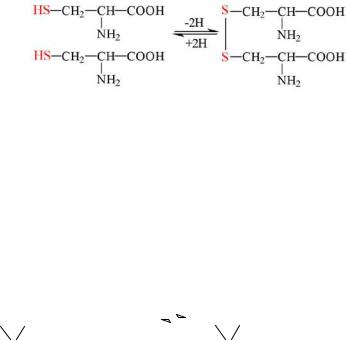
цистеин цистин
Особенно много цистеиновых звеньев, способных при окислении образовыватьдисульфидныесвязи, вбелкахволосишерсти – кератине. Дисульфидная связь встречается во многих пептидах и белках, участвует в создании третичной структуры белков.
В регулировании углеводного и липидного обмена важную роль играет окисление дигидролипоевой кислоты в липоевую:
HS |
SH |
( |
|
) |
|
COOH |
|
S |
|
S |
( CH |
) |
|
COOH |
||||||
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
CH |
|
|
H C |
|
CH |
|
|||||||||
H C |
CH |
|
|
|
||||||||||||||||
|
4 |
|
|
|
2 |
4 |
|
|
||||||||||||
2 |
|
|
|
|
|
2 |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|||||||
дигидролипоевая |
|
|
|
|
липоевая кислота |
|
|
|
||||||||||||
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
87
