
- •УСЛОВНЫЕ СОКРАЩЕНИЯ
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •1.1. Классификации возбудителей инфекционных болезней
- •1.2. Классификация инфекционных болезней
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 2. СИНДРОМЫ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- •2.1. Лихорадка
- •2.2. Экзантемы
- •2.3. Диарейный синдром
- •2.4. Поражения ротоглотки
- •2.5. Лимфопролиферативный синдром
- •2.6. Психоневрологические синдромы
- •2.7. Синдром острой сосудистой недостаточности (синдром шока)
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 3. ДИАГНОСТИКА ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ
- •3.2. Принципы терапии инфекционных больных
- •ВОПРОСЫ К ГЛАВЕ
- •Раздел 1. БАКТЕРИОЗЫ
- •Глава 4. КИШЕЧНЫЕ ИНФЕКЦИИ
- •4.1. Брюшной тиф и паратифы А и В
- •4.2. Сальмонеллез
- •4.3. Дизентерия
- •4.4. Кишечная коли-инфекция
- •4.5. Пищевые токсикоинфекции
- •4.6. Ботулизм
- •4.7. Холера
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 5. БАКТЕРИАЛЬНЫЕ ЗООНОЗЫ
- •5.1. Чума
- •5.2. Туляремия
- •5.3. Сибирская язва
- •5.4. Бруцеллез
- •5.5. Псевдотуберкулез
- •5.6. Иерсиниоз кишечный
- •5.8. Мелиоидоз
- •5.9. Эризипелоид
- •5.10. Кампилобактериоз
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 6. ДРУГИЕ БАКТЕРИАЛЬНЫЕ ИНФЕКЦИИ
- •6.1. Менингококковая инфекция
- •6.2. Лепра
- •6.3. Атипические микобактериозы
- •6.4. Столбняк
- •6.5. Стрептококковая инфекция
- •6.6. Дифтерия
- •6.7. Листериоз
- •6.8. Болезнь легионеров
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 7. БОЛЕЗНИ, ВЫЗВАННЫЕ СПИРОХЕТАМИ, РИККЕТСИЯМИ, ХЛАМИДИЯМИ И МИКОПЛАЗМАМИ
- •7.1. Тиф возвратный вшивый
- •7.2. Тиф возвратный эндемический
- •7.3. Иксодовый клещевой боррелиоз
- •7.4. Лептоспироз
- •7.5. Содоку (болезнь укуса крыс) и стрептобациллез
- •7.6. Хламидиозы
- •7.7. Микоплазмозы
- •7.8. Риккетсиозы
- •ВОПРОСЫ К ГЛАВЕ
- •Раздел 2. ВИРУСНЫЕ БОЛЕЗНИ
- •Глава 8. Вирусные инфекции дыхательных путей
- •8.1. Грипп
- •8.2. Парагрипп
- •8.3. Аденовирусная инфекция
- •8.4. Респираторно-синцитиальная вирусная инфекция
- •8.5. Риновирусная инфекция
- •8.6. Реовирусная инфекция
- •8.7. Коронавирусная инфекция
- •ВОПРОСЫ К ГЛАВЕ
- •9.1. Полиомиелит
- •9.2. Клещевой энцефалит
- •9.3. Энцефалит японский
- •9.4. Подострый склерозирующий панэнцефалит
- •9.5. Прогрессирующий краснушный панэнцефалит
- •9.6. Бешенство
- •9.7. Губкообразные энцефалопатии (прионные болезни)
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 10. ВИРУСНЫЕ ИНФЕКЦИИ, ХАРАКТЕРИЗУЮЩИЕСЯ ПОРАЖЕНИЕМ КОЖИ И СЛИЗИСТЫХ ОБОЛОЧЕК
- •10.1. Герпесвирусные инфекции
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 11. ВИРУСНЫЙ ГЕПАТИТ
- •11.1. Гепатит А
- •11.2. Гепатит В
- •11.3. Гепатит С
- •11.4. Гепатит D
- •11.5. Гепатит Е
- •11.6. Цирроз печени
- •11.7. Первичная гепатокарцинома
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 12. ВИЧ-ИНФЕКЦИЯ
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 13. ВИРУСНЫЕ ЛИХОРАДКИ, ПЕРЕДАЮЩИЕСЯ ЧЛЕНИСТОНОГИМИ, И ВИРУСНЫЕ ГЕМОРРАГИЧЕСКИЕ ЛИХОРАДКИ
- •13.1. Геморрагические лихорадки
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 14. ДИАРЕЯ ВИРУСНАЯ
- •14.1. Ротавирусная инфекция
- •14.2. Энтеровирусный гастроэнтерит
- •ВОПРОСЫ К ГЛАВЕ
- •Раздел 3. ПРОТОЗОЙНЫЕ ИНФЕКЦИИ И ГЕЛЬМИНТОЗЫ
- •Глава 15. ПРОТОЗОЙНЫЕ ИНФЕКЦИИ
- •15.1. Малярия
- •15.2. Лейшманиоз
- •15.3. Токсоплазмоз
- •15.4. Балантидиаз
- •15.5. Амебиаз
- •ВОПРОСЫ К ГЛАВЕ
- •Глава 16. ГЕЛЬМИНТОЗЫ
- •16.1. Кишечные гельминтозы
- •16.2. Внекишечные гельминтозы
- •16.3. Личиночные (ларвальные) гельминтозы
- •ВОПРОСЫ К ГЛАВЕ
- •Приложение
- •ЛИТЕРАТУРА
2 – 3 приема, после еды, на курс лечения (взрослому) 300 – 400 мг/кг.
Контроль эффективности лечения проводят через 2 – 3 мес. после окончания терапии трехкратным исследованием мокроты с 7-дневным интервалом.
Профилактика. Основой профилактики является соблюдение технологических приемов обработки и приготовления блюд из пресноводных раков и крабов. При купании в открытых водоемах следует остерегаться заглатывания воды, так как личинки парагонимусов могут сохраняться в фрагментах тел погибших раков и крабов и контаминировать воду. Также важно охранять водоемы от фекального загрязнения.
16.3. Личиночные (ларвальные) гельминтозы
Наиболее актуальными для нашей страны личиночными гельминтозами являются эхинококкоз, цистицеркоз и симптомокомплекс, вызываемый мигрирующими личинками зоонозных гельминтов (larva migrans).
16.3.1. Эхинококкоз
Различают два вида инвазии: гидатиозный (цистный) эхинококкоз, вызываемый личинками
Echinococcus granulosus, и альвеолярный эхи-
нококкоз, вызываемый личинками Echinococcus multilocularis.
16.3.1.1. Гидатиозный (цистный) эхинококкоз
Этиология. Возбудитель – в личиночной стадии E. granulosus – мелкая цестода, длиной 3,4 – 6,18 мм и шириной 0,47 – 0,98 мм, имеющая сколекс с 4 присосками и крючьями и 3 – 4 проглоттида, наполненных яйцами. Личинка представляет однокамерный пузырь
(Echinococcus unilocularis) диаметром 1 – 50 мм и бо-
лее. Стенка пузыря состоит из 2 слоев: наружного (кутикулярный) и внутреннего (герминативный), из клеток которого образуются мелкие пристеночные выпячивания (выводковые камеры), содержащие сколексы
– до сотни в одном пузыре. Полость пузыря заполнена жидкостью.
Эпидемиология. Эхинококкоз – пероральный биогельминтоз, зооноз. Окончательными хозяевами гельминта и источниками инвазии являются плотоядные животные – домашние собаки, волк, шакал, рысь, куница, хорь и др., у которых в кишечнике паразитирует зрелый червь; его членики, содержащие яйца, выделяются с калом во внешнюю среду. Заражение человека происходит в результате заглатывания инвазионных яиц эхинококка при тесном контакте с инва-
зированными собаками, овцами, на шерсти которых в изобилии находятся яйца гельминта, а также при употреблении в пищу продуктов, сырых овощей, ягод, обсемененных яйцами паразитов.
Восприимчивость к эхинококкозу всеобщая, иммунитет изучен недостаточно. Встречается инвазия повсеместно, в нашей стране регистрируется преимущественно в южных регионах, в Поволжье и Сибири.
Патогенез и патологоанатомическая картина.
Из заглоченных человеком яиц эхинококка в желудке и кишечнике высвобождаются онкосферы, которые через кишечную стенку проникают в кровь, затем в печень. Здесь большая часть онкосфер задерживается, а остальные заносятся кровью в различные органы (легкие, головной мозг, почки, сердце и др.), где медленно формируется личиночная стадия (эхинококк), достигающая через 5 – 6 мес. диаметра 2 – 40 мм. В легких эхинококковые пузыри могут приобретать наибольшие размеры – 20 – 25 см в диаметре. К 5 – 6 мес. вокруг личинки образуется фиброзная капсула. Растущий пузырь вызывает сдавление окружающих тканей, что проявляется симптомами объемного процесса в различных органах.
Гибель паразита и присоединение бактериальной инфекции приводят к формированию абсцессов.
В патогенезе инвазии большое значение имеет сен-
сибилизация организма к паразитарным метаболитам, обладающим антигенными свойствами. При нарушении целостности эхинококкового пузыря может развиться анафилактический шок, наблюдается диссеминация паразита с образованием большого числа новых паразитарных кист.
Клиническая картина. Эхинококкозу свойственно длительное течение с постепенным нарастанием симптомов. В большинстве случаев первые признаки болезни появляются через много лет после заражения. Лишь некоторые больные рано замечают слабость, снижение работоспособности, головные боли, появление крапивницы или других высыпаний, периодические повышения температуры тела.
Наиболее частый вариант инвазии — эхинококкоз печени (более 50 % всех случаев эхинококкоза). Различают 3 стадии болезни. Первая стадия – от момента инвазии печени до первых клинических проявлений болезни, в подавляющем большинстве случаев протекает латентно. Вторая стадия характеризуется появлением как общих признаков заболевания, так и различных симптомов поражения печени. Больные теряют аппетит и работоспособность, жалуются на слабость, головные боли, похудание, субфебрилитет; иногда возникают аллергические симптомы: высыпания, зуд, непереносимость лекарственных пре-
паратов и др. Для этой стадии характерны боли в животе различной интенсивности, ощущения давления и тяжести в правом подреберье или эпигастрии, тошнота, рвота, расстройство стула. Печень увеличена, на поздних сроках достигает огромных размеров, чаще за счет правой доли, плотна на ощупь, безболезненна. При локализации пузыря на передненижней поверхности печени его можно обнаружить в виде «опухоли» плотноэластической, а при начавшейся кальцификации стенки пузыря – деревянистой консистенции. Флюктуация встречается редко. Третья стадия – стадия осложнений. Самыми частыми из них являются нагноение эхинококковых пузырей и развитие абсцесса печени с возможным вскрытием его в брюшную или плевральную полость, забрюшинное пространство, в желудок, кишку, бронх; разрыв неинфицированного пузыря с появлением комплекса аллергических реакций (вплоть до шока) и диссеминацией эхинококкоза; сдавление кистой воротной или нижней полой вены с соответствующей симптоматикой, а также сдавление внутри- и внепеченочных желчных протоков с развитием обтурационной желтухи.
Вгемограмме часто обнаруживается эозинофилия
–от 4 – 6 до 60 – 70 %, увеличивается СОЭ. Выявляются нарушения функции печени, выраженность которых зависит от стадии патологического процесса.
Вторым по частоте вариантом эхинококкоза является эхинококкоз легких (более чем в 20 % случаев). Период клинической манифестации разделяют на 2 стадии. Первая – стадия невскрывшейся эхинококковой кисты. Основная симптоматика этой стадии обусловлена ростом пузыря и сдавлением ткани легкого, бронхов и сосудов, вовлечением в патологический процесс плевры. Больные жалуются на боли в грудной клетке различного характера и разной степени интенсивности, кашель, сначала сухой, а затем со слизисто-гнойной мокротой, кровохарканье, одышку. В случае нагноения эхинококкового пузыря развивается абсцесс легкого. Вторая – стадия вскрывшейся кисты характеризуется внезапным и резким изменением течения заболевания. При прорыве пузыря в бронх (20 – 40 % случаев) появляются сильный кашель, удушье, цианоз, в мокроте обнаруживается содержимое пузыря (в том числе и дочерние кисты), иногда примесь крови. Эти симптомы продолжаются несколько дней и даже недель и могут сопровождаться аспирационными пневмониями и тяжелыми аллергическими реакциями.
Прорыв эхинококкового пузыря в полость плевры или перикарда может проявляться шоком и немедленной смертью больного. В более благоприятном случае прорыва кисты в плевру наблюдается карти-
на, сходная с таковой при острейшем экссудативном плеврите. В случае сообщения пузыря с бронхиальным деревом развивается пневмоили пиопневмоторакс. При эхинококкозе легкого в гемограмме определяются такие же изменения, как при эхинококкозе печени.
Эхинококкоз другой локализации (головного мозга, селезенки, почек, костей, мышц и т. д.) встречается редко.
Прогноз. Всегда очень серьезный, а в запущенных случаях неблагоприятный. Диагностика. Для диагностики эхинококкоза разработаны сероиммунологические тесты: ИФА, РНГА, РСК, реакция латекс-агглю- тинации с антигеном из жидкости эхинококковых пузырей, кожная аллергическая реакция Каццони, более информативная при эхинококкозе печени. Важное значение имеют инструментальные методы диагностики (рентгенологическое исследование печени на фоне пневмоперитонеума, КТ, МРТ, ангиография, сканирование и УЗИ печени, лапароскопия) и диагностическая лапаротомия.
Лечение. Основной метод лечения больного цистным эхинококкозом – оперативный. Во время операции необходимо соблюдать все меры предосторожности, чтобы не нарушить целостность кисты. Для предотвращения обсеменения окружающих тканей
зародышевыми элементами эхинококка используют пункционную аспирацию содержимого кисты с заполнением ее гермицидом (80 – 100 % глицерином) с экспозицией на 10 мин с последующим хирургическим удалением кисты.
Албендазол назначают по 400 мг 2 раза в день (утро
–вечер) или, при массе тела менее 60 кг, по 15 мг/кг (в два приема). Максимальная суточная доза не должна превышать 800 мг. Проводят 3 – 4 и более циклов терапии албендазолом по 28 дней с 2-недельны- ми интервалами между ними. При длительном назначении терапии возможно развитие лейкопении. В случаях непереносимости албендазола можно использовать мебендазол по 500 мг 2 раза в день первые 3 дня, в последующие 3 дня – по 500 мг 3 раза в сутки, далее в максимальной дозировке – 25 – 30 мг/кг/сут в 3 – 4 приема на протяжении 30 дней с проведением 6
–12 циклов лечения с 30-дневным интервалом между ними. При длительном приеме этих препаратов, помимо гемограммы, также необходимо контролировать функцию печени и почек.
Окончательно выздоровевшими признаются пациенты, у которых после проведенного лечения отсутствуют клинические проявления эхинококкоза, а серологические исследования остаются негативными в течение 3 – 4 лет. Наблюдение за пролеченными паци-
ентами продолжается не менее 5 лет. Профилактика эхинококкоза у человека включает
соблюдение правил личной гигиены, периодическое гельминтологическое обследование собак и своевременную дегельминтизацию (в скотоводческих регионах каждые 45 сут), контроль бродячих животных. Фекалии собак рекомендуется обеззараживать хлорной известью. Не допускается скармливание собакам сырых внутренностей домашних животных.
16.3.1.2. Альвеолярный эхинококкоз
Болезнь вызывается личинками E. multilocularis, отличающимися экзофитным ростом вновь образующихся пузырей, инфильтрирующих окружающие ткани. Эпидемиологические и клинико-лабораторные черты инвазии сходны с таковыми при гидатиозном (цистном) эхинококкозе.
Болезнь регистрируется спорадически в Восточной и Западной Сибири, в Поволжье, некоторых южных регионах России.
Диагностическая тактика аналогична таковой при инвазии E. granulosus.
Лечение. Радикальным лечением больных альвеококкозом считается хирургическое вмешательство лишь при наличии одиночного узла без метастазирования, когда резекцию узла можно провести в пре-
делах здоровых тканей. Назначение албендазола в дозировке 10 – 15 мг/кг/сут в 2 приема после еды в течение 2 – 4 лет (непрерывно) приостанавливает развитие паразита и улучшает течение болезни. Длительные курсы албендазола требуют систематического контроля (1 раз в 7 – 10 дней) гемограммы и биохимических показателей крови на предмет гепатотоксичности. При наличии полости распада альвеолярного эхинококка показано назначение антибиотиков широкого спектра действия.
Диспансерное наблюдение за больными альвеококкозом проводится хирургами и/или инфекционистами пожизненно.
16.3.2. Синдром мигрирующих личинок (Larva migrans)
Симптомокомплекс Larva migrans – заболевание,
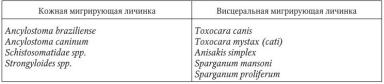
обусловленное паразитированием мигрирующих личинок зоогельминтов, для которых человек не является естественным хозяином. Дальнейшего созревания личинки в организме человека не происходит. Различают кожную и висцеральную формы болезни. В табл. 43 представлены некоторые представители гельминтов, личинки которых у человека могут вызывать развитие симптомокомплекса мигрирующей ли-
чинки (СМЛ).
Кожная форма (Cutaneous larva migrans – CLM).
Возбудителями являются нематоды ( Ancylostoma caninum, A. braziliense, A. ceylonicum), паразити-
рующие у собак и кошек, и трематоды (сем. Schistosomatidae), паразитирующие у водоплавающих птиц. Возбудители мигрирующей личинки из семейства анкилостомид чаще встречаются в регионах с тропическим и субтропическим климатом (Юго-Во- сточная Азия, Африка, Южная Америка, страны Карибского бассейна). Заражение может произойти на песчаных пляжах, в песочницах, при контакте открытой кожи с почвой и водой, контаминированными фекалиями животных. В группы риска входят туристы, дети, пловцы, строители. При благоприятных условиях во внешней среде из яиц быстро выходят личинки, которые проникают в кожу, располагаясь в зернистом слое эпидермиса или в более глубоких слоях, откуда они вновь мигрируют в эпидермис. В коже, по ходу продвижения личинки, развивается местная аллергическая реакция, сопровождающаяся по- лиморфно-ядерной инфильтрацией, отеком, расширением капилляров и нередко разрушением клеток под действием паразитарных протеаз. После гибели личинок обычно наступает полное выздоровление. A. caninum имеет менее продолжительную фазу мигра-
ции, но способна к проникновению в скелетные мышцы.
Таблица 43
Представители гельминтов, личинки которых могут вызывать развитие СМЛ
Клинические проявления развиваются через 2 – 3 дня, а иногда спустя месяцы после инвазии и характеризуются возникновением чувства жжения, покалывания или зуда в месте внедрения гельминта, чаще в области нижних конечностей, ягодиц или паховой области. На коже появляется аллергический линейный дерматит часто с извитыми ходами шириной до 3 мм, распространяющийся со скоростью продвижения личинки (1 – 5 см в сутки). Кожный зуд бывает интенсивным и может приводить к бессоннице.
Кожные проявления при стронгилоидозе отличаются развитием прямолинейного аллергического дерматита (larva currens – «бегущая личинка») со скоростью до 5 – 15 см/ч. Дифференциальный диагноз при кож-
ной мигрирующей личинке следует проводить с линейным мигрирующим миазом, вызываемым личин-
ками двукрылых Gastrophilus и Hypoderma.
Вслучае заражения шистосоматидами на коже соответственно внедрению церкариев через 20 – 30 мин появляются эритематозно-папулезные элементы, превращающиеся спустя 1 – 3 дня в корочки, часто наблюдается местная или распространенная крапивница (церкариоз, зуд купальщиков, шистосоматидный дерматит). При более интенсивной инвазии отмечаются кратковременная лихорадка, признаки общего недомогания, более выраженные при повторном заражении. Спустя 12 нед. (реже 5 – 6 нед.) наступает выздоровление. Аналогичная картина может наблюдаться в ранней стадии шистосомозов у человека.
Продолжительность патологических явлений при кожной мигрирующей личинке может достигать 4 – 6 мес. При расчесывании кожи и присоединении вторичной бактериальной флоры наблюдается затяжное течение.
Вгемограмме больных кожной формой larva migrans, несмотря на тканевую локализацию личинок, эозинофилия встречается относительно редко. В соскобах кожи можно найти остатки личинок.
Лечение. Препаратом выбора при кожной мигриру-
ющей личинке является ивермектин (Mectizan) в дозе 200 мкг/кг перорально один раз в сутки в течение 1 – 2 дней или албендазол (Zentel) по 400 мг/сут в течение 3 дней, а при обширном поражении кожи курс албендазола продлевают до 7 дней. Альтернативно используют мебендазол (Vermox) по 200 мг/сут в течение 7 – 10 дней с повторным курсом через 1 – 2 мес. Наружное применение крема тиабендазола 15 % в течение 5 дней вместе с антигистаминными препаратами помогает быстро купировать кожный зуд. Также известно, что личинки погибают при орошении пораженной области хлорэтилом. При присоединении вторичной бактериальной инфекции применяют антибиотикотерапию.
Висцеральная форма (Visceral larva migrans – VLM).
Возбудителями являются личинки цестод (Sparganum mansoni, Sparganum proliferum, Multiceps spp.) и
нематод (Тохосаra canis, Тохосаrа mystах, Тохаscaris leonina и др.) в имагинальной стадии паразитирующих у плотоядных животных. Человек заражается висцеральной мигрирующей личинкой в результате заглатывания яиц гельминтов с водой и пищевыми продуктами и становится промежуточным хозяином. Заболевание регистрируется преимущественно у детей 1 – 4 лет.
Спарганоз у человека вызывается личинками
плероцеркоидами цестод Sparganum mansoni и Sparganum proliferum, которые в половозрелой стадии обитают в тонкой кишке кошек и собак – окончательных хозяев гельминта. Первым промежуточным хозяином паразита является пресноводный рачок циклоп, в котором гельминт развивается до стадии процеркоида. Человек заболевает спарганозом при употреблении в пищу вторых промежуточных хозяев этого паразита (лягушек, змей, птиц и т. д.), а также при случайном употреблении воды, содержащей циклопов. Известны случаи заражения спарганозом при использовании лягушек и змей в народной медицине при непосредственном прикладывании их к воспаленной коже и ранам. Для данного паразита человек является биологическим тупиком. Для личинок Sparganum proliferum характерна диссеминация в различные органы и ткани. Личинки Sparganum mansoni вызывают образование подкожных фиброзных узлов диаметром до 2 см.
Клиническая картина при спарганозе зависит от локализации личинок, которые могут располагаться в подкожной клетчатке, мышцах, глазах, лимфатических узлах, брюшной полости. Поражение кожи характеризуется болезненным отечным дерматитом, глаз
– конъюнктивитом. Нередко у больных возникает лихорадка, крапивница, отеки. Гибель личинок обуслов-
ливает формирование очагов воспаления и некроза в тканях. В гемограмме определяется эозинофилия. Окончательный диагноз ставится морфологически после хирургического удаления личинок плероцеркоидов.
Ценуроз. В случае заражения цестодами в кишечнике человека из яиц гельминтов выходят личинки, проникающие через кишечную стенку в кровь и достигающие различных внутренних органов, где они трансформируются в пузыревидные личинки, достигающие 5 – 10 см в диаметре, которые сдавливают ткани и нарушают функцию соответствующих органов.
Клинические проявления болезни развиваются спустя 4 – 5 мес. после заражения и в начальной стадии характеризуются нерезко выраженными признаками интоксикации: наблюдается плохое самочувствие, возможна аллергическая экзантема. В дальнейшем присоединяются и нарастают симптомы, обусловленные локализацией паразита в органах.
Наиболее тяжелая клиническая картина наблюдается при поражении центральной нервной системы. Личиночные стадии цепней (ценуры, цистицерки) располагаются преимущественно в оболочках и веществе головного мозга, вызывая клиническую картину объемного процесса (цистицеркоз, ценуроз голов-
ного мозга). У больных наблюдаются головная боль, признаки церебральной гипертензии, очаговые симптомы, эпилептиформные судороги. Кроме головного мозга, личинки могут располагаться в спинном мозге, глазу, серозных оболочках, межмышечной соединительной ткани и т. д.
Токсокароз. Возбудителями токсокароза являются личинки нематод животных: Toxocara canis (в половозрелой стадии паразитирует у семейства псовых), Toxocara cati (гельминт семейства кошачьих). Токсокары являются геогельминтами. Созревание выделенных животными яиц происходит в окружающей среде в течение 3 нед. В организме собак и кошек токсокара проходит полный цикл развития до формирования половозрелых форм в тонкой кишке, у человека
– только до стадии личинки, которая совершает миграцию из кишечника с кровотоком в различные органы и ткани (висцеральная мигрирующая личинка). Отдельно рассматривают глазную форму мигрирующей личинки. Заболевание распространено повсеместно, но чаще встречается в регионах с тропическим климатом. Человек заражается при заглатывании зрелых яиц токсокар, попавших на кожу рук, пищевые продукты и в воду. Чаще заражаются дети 1 – 6 лет в связи с тесным контактом с животными, землей и песком в песочницах, контаминированных фекалиями собак и
реже кошек.
В основе патогенеза токсокароза лежит непосредственное повреждение тканей мигрирующей личинкой и формирование эозинофильных гранулем.
Токсокароз у человека характеризуется полиморфной клинической картиной и сопровождается тяжелой общей аллергической реакцией с лихорадкой неправильного типа, сухим кашлем, приступами бронхиальной астмы, аллергической экзантемой. При рентгенографии в легких выявляются летучие эозинофильные инфильтраты. Нередко наблюдается гепатомегалия с развитием желтухи и изменением функциональных проб печени; в биоптатах печени обнаруживаются эозинофильные гранулемы. Аналогичные изменения могут быть найдены в почках, кишечной стенке, миокарде и других тканях. Гемограмма таких больных характеризуется значительной эозинофилией (50
– 90 %); возможна лейкемоидная реакция, СОЭ повышена. Часто обнаруживается гипергаммаглобулинемия.
Личинки токсокар также способны поражать центральную нервную систему с формированием эозинофильного менингоэнцефалита, объемных образований головного мозга, миелита и церебрального васкулита.
Заболевание склонно к рецидивирующему тече-
нию, продолжительность его достигает 5 – 8 мес. (иногда 2 лет). Прогноз серьезный, при отсутствии лечения при висцеральной форме возможны летальные исходы.
Глазная форма токсокароза чаще встречается изолированно от висцеральной и характеризуется односторонним поражением органа зрения. Возрастная группа при глазной форме старше и в среднем состоит из детей школьного возраста (старше 8 лет). Эозинофилия при этой форме не характерна. Клинически отмечается снижение остроты зрения, выпадение части поля зрения. При офтальмоскопии можно обнаружить личинки токсокар в стекловидном теле, а также на глазном дне. Поражение сетчатки личинкой может вызывать мигрирующую скотому, отслоение сетчатки и одностороннюю слепоту, особенно при формировании гранулем в области зрительного нерва. Заболевание необходимо дифференцировать от ретинобластомы. Описаны случаи комбинированного токсокароза, при котором сначала поражается глаз, а затем внутренние органы.
Диагностика токсокароза проводится с учетом клинико-эпидемиологических данных. Диагноз подтверждается инструментальными (эндоскопия, рентгенография, КТ, МРТ) и сероиммунологическими (РСК, РПГА, ИФА, реакция микропреципитации и
др.) методами, применяют морфологическое изучение биоптатов органов. При ИФА титр специфических антител 1: 800 и выше свидетельствует о заболевании. При глазной форме токсокароза титр антител редко превышает 1: 200. Исследование фекалий у человека при токсокарозе не имеет диагностического значения, что объясняется особенностями жизненного цикла данного паразита.
Лечение. При среднетяжелом и тяжелом течении висцерального токсокароза назначают албендазол по 10 мг/кг/сут в два приема в течение 10 – 20 дней. При тяжелом течении с вовлечением в патологический процесс органов дыхания, сердечно-сосудистой или центральной нервной системы показано назначение глюкокортикостероидов (преднизолон по 0,5 – 1,0 мг/кг/сут). Альтернативными препаратами являются тиабендазол (минтезол) по 25 – 50 мг/кг/сут или мебендазол (вермокс) – взрослым по 200 мг/сут в течение 5 – 7 дней. Рекомендуется повторный курс спустя 1 – 2 мес. Контроль лечения проводится спустя 2 мес. Критериями эффективности терапии считается регресс клинических проявлений, снижение эозинофилии и титра специфических антител.
Эффективных схем лечения глазной формы токсокароза не разработано. Применяют албендазол по 800 мг два раза в сочетании с преднизолоном до
1,5 мг/кг/сут в течение 2 нед. Мебендазол при глазной форме, а также при поражении головного мозга неэффективен, так как не проникает через гематоэнцефалический барьер. Ивермектин при токсокарозе не используют.
Профилактика. Включает в себя комплекс сани- тарно-гигиенических и ветеринарных мероприятий с предупреждением контакта между детьми и зараженными животными, регулярной дегельминтизацией домашних животных и защитой пищевых продуктов от возможной контаминации почвой и фекалиями кошек и собак. При работе в водоемах рекомендуется ношение защитной одежды.
Анизакиоз. Разновидностью синдрома VLM является инвазия личинками нематод Anisakis simplex,
Anisakis schupakovi, Pseudoterranova decipiens, для которых окончательными хозяевами являются морские млекопитающие (китообразные и ластоногие), а также рыбоядные птицы и хищные рыбы. Промежуточными хозяевами анизакид чаще являются водные беспозвоночные (головоногие моллюски и ракообразные). Человек заражается анизакиозом, употребляя в пищу сырую или недостаточно термически обработанную морскую рыбу или ракообразных.
В месте внедрения личинок – слизистой оболочке желудка, кишечника, а в редких случаях миграции
