

БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
БИОЛОГИЧЕСКИЙ ФАКУЛЬТЕТ
Кафедра биохимии
БИОХИМИЯ В СХЕМАХ И ТАБЛИЦАХ
МИНСК
2010
УДК 571.1 ББК 28.072
(1)K 62
Рекомендовано Ученым советом биологического факультета
15 сентября 2010 г., протокол № 1
С о с т а в и т е л и:
О. И. Губич, Т.А. Кукулянская, Н.М. Орел, И. В. Семак
Рецензенты:
кандидат биологических наук, заведующий кафедрой биотехнологии и биоэкологии УО ”Белорусский государственный технологический университет” Леонтьев В.Н.
кандидат биологических наук, доцент кафедры генетики Белорусского государственного университета Храмцова Е.А.
Биохимия в схемах и таблицах/ авт.-сост.: О.И. Губич [и др.]. –
Б63 Минск.: БГУ, 2010. – 100 с.
Вучебном пособии в наглядной форме приводятся основные положения статической
идинамической биохимии. Рассмотрены основные классы биологических молекул, клеточные процессы с их участием, а также механизмы важнейших биохимических процессов в животной клетке.
Предназначено для студентов, магистрантов, аспирантов биологических специальностей ВУЗов, а также широкого круга читателей, интересующихся вопросами биохимии.
УДК 577.1
ББК
28.072
© БГУ, 2010
2
ПРЕДИСЛОВИЕ
Важнейшей составляющей эффективной подготовки современного специалиста-биолога в высшей школе является освоение ими ключевых положений биологической химии. Поскольку биохимия относится к числу наиболее динамично развивающихся областей знаний, чрезвычайно важно представить накопленную к настоящему времени информацию в легко доступной студентам, наглядной форме. Таким образом, данное пособие представляет собой справочник, позволяющий оперативно получать наглядную информацию по основным разделам биохимии в объеме университетского курса, но не заменяющий хороший учебник по этому предмету.
Пособие начинается с разделов, посвященных строению и классификации важнейших биомолекул: белков, углеводов, нуклеиновых кислот, липидов, витаминов и гормонов. Особое внимание уделяется вопросам энзимологии, кинетике ферментативных реакций и особенностям регуляции ферментативных процессов в клетке.
Во второй половине издания рассмотрены основные реакции превращения биологических молекул, матричные процессы, важнейшие положения биоэнергетики животной клетки.
Данное пособие будет стимулировать самостоятельную подготовку студентов и магистрантов, повышать уровень и качество подготовки современных специалистов-биологов.
Все замечания и пожелания, касающиеся улучшения представленного в пособии материала, будут приняты авторами с благодарностью.
3
СТРУКТУРНАЯ БИОХИМИЯ
АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
Таблица. Классификация -аминокислот
Группа |
Функциональные группы |
Аминокислоты |
||
аминокислот |
|
|
|
|
|
Гидрофильные, полярные |
|
||
Кислые |
Карбоксильная |
-СОО- |
Аспарагиновая |
Asp |
(отрицательно |
группа |
|
Глутаминовая |
Glu |
заряженные при |
|
|
|
|
рН≈7,4) |
|
|
|
|
|
|
|
|
|
Основные |
Аминогруппа |
-NH3+ |
Лизин |
Lys |
(положительно |
|
|
Аргинин |
Arg |
заряженные при |
|
|
Гистидин |
His |
рН≈7,4) |
|
|
|
|
|
|
|
|
|
Нейтральные |
Тиольная группа |
-SH |
Цистеин |
Cys |
|
|
|
|
|
|
Гидроксильная |
-ОН |
Серин |
Ser |
|
группа |
|
Треонин |
Thr |
|
|
|
Тирозин |
Tyr |
|
Амиды |
-CONH2 |
Аспарагин |
Asn |
|
|
|
Глутамин |
Gln |
|
Гидрофобные, неполярные |
|
||
Алифатические |
-CH2- |
|
Аланин |
Ala |
|
|
|
Валин |
Val |
|
|
|
Лейцин |
Leu |
|
|
|
Изолейцин |
Ile |
|
|
|
Метионин |
Met |
Ароматические |
-C6H5- |
|
Фенилаланин |
Phe |
|
|
|
Триптофан |
Trp |
|
|
|
*(Тирозин |
Tyr) |
Другие |
Иминокислота |
Пролин |
Pro |
|
|
|
|
Глицин |
Gly |
*Тирозин, или гидроксифенилаланин - ароматическая, гидрофильная,
полярная аминокислота.
4
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОКИСЛОТ
декарбоксилирование (образование аминов)
дезаминирование (образование карбоновых кислот)
этерификация карбоксильных групп (образование сложных эфиров)
образование амидов
переаминирование (замещение аминогруппы)
гидроксилирование
взаимодействие с альдегидами (образование шиффовых оснований)
образование N-гликозидов (при взаимодействии с углеводами)
образование О-гликозидов (при взаимодействии с углеводами)
окисление SH-групп (образование дисульфидных содеинений, например димера цистеина - цистина)
фосфорилирование гидроксиаминокислот (образование сложных фосфорных эфиров
окисление гуанидиновой группы аргинина
образование пептидной связи (полимеризация аминокислот с образованием пептидов)
пептидная связь
|
|
|
|
|
|
|
|
|
|
|
|
|
- H2O |
|
|
|
|
|
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H2N |
|
CH |
|
COOH + |
H2N |
|
CH |
|
COOH |
|
|
|
|
H2N |
|
CH |
|
C |
|
N |
|
CH |
|
COOH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH |
|
|
CH |
|
|
|
|
|
CH2 |
|
CH2 |
|||||||||||||||||
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
|
|
SH |
|
|
|
|
|
OH |
|
SH |
|||||||||||||||||
|
серин |
цистеин |
|
|
|
|
серилцистеин |
|||||||||||||||||||||||
Взаимодействие -аминокислот между собой
с образованием пептидной связи
5

СТЕРЕОИЗОМЕРИЯ -АМИНОКИСЛОТ
|
D - ряд |
|
|
L - ряд |
|
||||||||
|
|
COOH |
|
|
|
COOH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
|
NH2 |
H N |
|
C |
|
|
H |
||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
R |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
энантиомеры
АМФОТЕРНЫЕ (КИСЛОТНО-ОСНОВНЫЕ) СВОЙСТВА-АМИНОКИСЛОТ В РАСТВОРАХ
|
|
R |
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
C |
|
COOH |
|
|
H N |
|
C |
|
COO |
|||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
||||||||
биполярный (цвиттер-) ион
рI=(pK1+pK2)/2,
где pK1 – константа диссоциации карбоксильных групп; pK2 – константа диссоциации аминогрупп.
Заряд аминокислот при различных значениях рН среды
рН < pI |
рН = pI |
pH > pI |
|
|
|
Заряд > 0 |
Заряд = 0 |
Заряд < 0 |
(положительный) |
|
(отрицательный) |
6
КАЧЕСТВЕННАЯ РЕАКЦИЯ НА -АМИНОКИСЛОТЫ
|
O |
|
|
|
|
|
OH |
+ |
H2N |
CH COOH |
|
|
|
|
|||
|
OH |
|
|
|
|
|
O |
|
|
R |
|
|
|
|
|
|
|
Нингидрин |
|
|
α-Аминокислота |
||
окисленный |
O |
|
|
|
O |
|
H |
+ NH3 + CO2 + RCHO + |
OH |
||
|
|
|
|||
|
OH |
|
|
|
OH |
|
O |
|
|
|
O |
Нингидрин |
|
|
|
Нингидрин |
|
восстановленный |
|
O |
O |
окисленный |
|
|
|
|
|
||
|
|
|
|
N |
|
|
|
|
O |
O |
|
Пурпур Руэмана
БИУРЕТОВАЯ РЕАКЦИЯ - КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ПЕПТИДНУЮ СВЯЗЬ
|
|
|
|
|
H |
|
|
|
|
R2 |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R4 |
O |
|
|
H |
+2NaOH |
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
H2N |
|
|
C |
|
|
C |
|
|
|
|
N |
|
|
|
|
C |
|
|
|
|
|
|
C |
|
|
|
|
|
|
N |
|
|
|
|
|
|
C |
|
|
|
|
C |
|
|
|
|
N |
|
|
|
|
C |
|
|
C |
|
|
|
N |
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
+Cu(OH)2 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
R1 O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R3 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R5 |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Полипептид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
OH |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
R4 |
|
OH |
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
||||||||||||||
|
|
|
|
H2N |
|
|
|
|
|
C |
|
|
|
C |
|
|
|
|
N |
|
|
|
|
|
C |
|
|
|
|
|
C |
|
|
|
|
|
N |
|
|
|
C |
|
|
|
C |
|
|
N |
|
C |
|
C |
|
|
N |
|
C |
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R3 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R5 |
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Енольная форма полипептида |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|
|
C |
|
|
|
|
|
C |
|
|
|
|
|
|
N |
|
|
|
|
C |
|
|
|
|
C |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CHR3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cu |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
N |
|
|
|
|
|
C |
|
|
|
C |
|
|
|
N |
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
ONa R4 |
|
|
|
|
|
|
|
|
|
|
ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
Биуретовый медный комплекс (фиолетового цвета)
7
Таблица. Уровни структурной организации белков
Структурный |
Характеристика |
|
|
Типы связей |
|||
уровень |
структуры |
|
|
в структуре |
|
||
Первичная структура |
последовательность |
|
ковалентные |
связи |
|||
|
аминокислотных |
|
(пептидные) |
|
|||
|
остатков в поли- |
|
|
|
|
||
|
пептидной цепи |
|
|
|
|
||
|
|
|
|
|
|
||
Вторичная структура |
конфигурация |
|
|
водородные связи |
|
||
- -спираль |
полипептидной цепи |
|
|
|
|
||
- -структура |
|
|
|
|
|
|
|
Сверхвторичная |
упорядоченное |
рас- |
|
|
|
||
структура |
положение -спираль- |
|
|
|
|||
|
ных участков и/или |
- |
|
|
|
||
|
структур полипептид- |
|
|
|
|||
|
ной цепи |
|
|
|
|
|
|
|
|
|
|
|
|
||
Третичная структура |
пространственная |
|
|
гидрофобные |
|
||
|
организация |
|
|
взаимодействия |
|
||
|
(конформация) |
|
|
|
водородные связи |
||
|
полипептидной цепи |
|
|
ионные связи |
|
||
|
|
|
|
|
|
дисульфидные |
|
|
|
|
|
|
(ковалентные) связи |
||
|
|
|
|
|
|
|
|
Четвертичная |
способ |
организации |
в |
|
гидрофобные |
|
|
структура |
пространстве |
отдель- |
взаимодействия |
|
|||
|
ных |
полипептидных |
|
водородные связи |
|||
|
цепей, |
образование |
|
ионные связи |
|
||
|
макромолекулярных |
|
|
|
|
||
|
комплексов |
|
|
|
|
|
|
8
ФЕРМЕНТЫ
Таблица. Классификация ферментов
|
Класс ферментов |
Тип реакции |
1. |
Оксидоредуктазы |
Окислительно-восстановительные |
|
|
реакции всех типов |
2. |
Трансферазы |
Перенос отдельных атомов и групп |
|
|
атомов |
3. |
Гидролазы |
Гидролитическое расщепление |
|
|
химических связей |
4. |
Лиазы |
Негидролитическое расщепление |
|
|
двойных связей или их образование |
5. |
Изомеразы |
Взаимопревращение различных |
|
|
изомеров |
6. |
Лигазы |
Образование связей (синтез) с |
|
|
затратой энергии АТФ |
|
Единицы и формы выражения активности ферментов |
|
1 катал (каt) – количество фермента, которое катализирует превращение 1 моль субстрата за 1 сек при 25оС.
1 международная единица (МЕ) – количество фермента, которое катализирует превращение 1 мкмоль субстрата за 1 мин при 25оС.
Удельная активность - число единиц активности фермента, приходящихся на 1 мг белка.
9
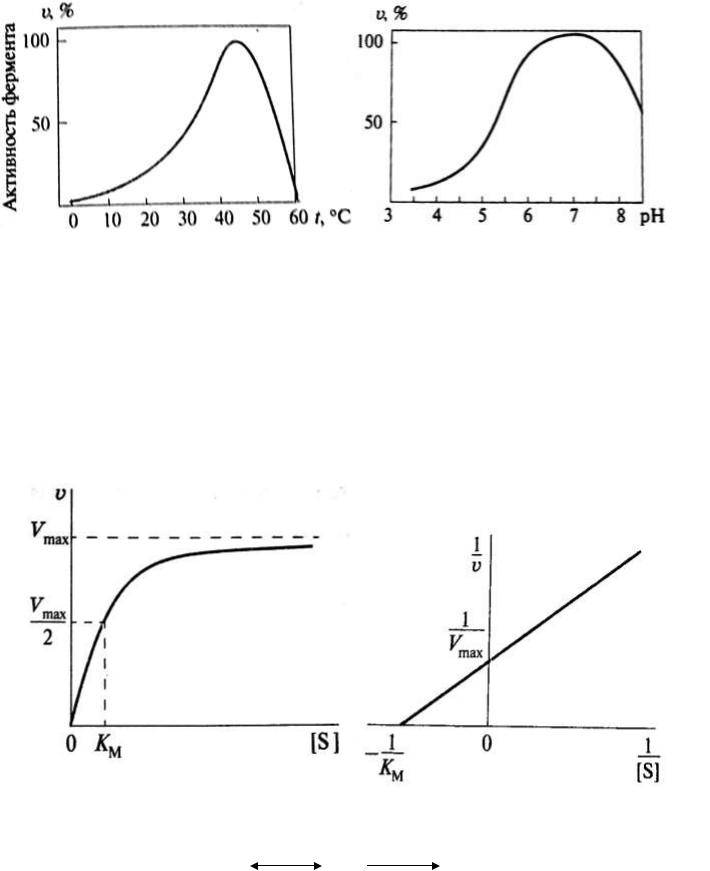
Зависимость активности ферментов от температуры (А) и рН среды (Б)
А |
Б |
КИНЕТИКА ФЕРМЕНТАТИВНЫХ ПРОЦЕССОВ
Зависимость скорости реакции от концентрации
K+1 |
K+2 |
K-1 |
10 |
