
Полезные материалы за все 6 курсов / Ответы к занятиям, экзаменам / 1. Морфология и ультраструктура
.pdfМЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЗАНЯТИЮ
1. Виды микроскопии, используемые в медицинской микробиологии.
Для диагностики инфекционных заболеваний используют световой,
темнополевой, фазово-контрастный, люминесцентный и электронный микро-
скопы.
Общее увеличение микроскопа определяют произведением увеличе-
ний объектива и окуляра.
Разрешающая способность микроскопа – это наименьшее расстояние между двумя точками, при котором они видны раздельно.
СВЕТОВОЙ МИКРОСКОП.
Разрешающая способность 0,2 мкм.
Предназначен для изучения формы, размеров и структуры окрашенных клеток.
При исследовании микроорганизмов применяют иммерсионный объек-
тив. Его преимущество - с помощью иммерсионного масла устанавливается оптически однородная среда с одинаковым показателем преломления между стеклом и линзой. Благодаря этому все лучи, не преломляясь и не изменяя направления, попадают в объектив, чем достигается более высокая разре-
шающая способность. В качестве иммерсионного масла обычно используют кедровое или касторовое, показатель преломления которых равен показателю преломления света в стекле.
ТЕМНОПОЛЕВОЙ МИКРОСКОП (ультрамикроскоп).
Разрешающая способность – 0,02-0,04 мкм.
Предназначен для изучения формы, размеров и подвижности живых, не-
окрашенных бактерий.
31
Темное поле создается с помощью специального конденсора, в котором затемнена центральная часть и таким образом создается боковое освещение.
Поэтому в объектив попадают лучи, отраженные от объекта. Увеличение разрешающей способности микроскопа связано с тем, что отраженный луч имеет более короткую длину волны.
ФАЗОВО-КОНТРАСТНЫЙ МИКРОСКОП.
Разрешающая способность – 0,2 мкм.
Предназначен для изучения формы, подвижности и структуры живых неокрашенных бактерий.
Имеет специальный набор фазовых объективов и соответствующих им кольцевых диафрагм конденсора. С помощью этого устройства достигается преобразование невидимых фазовых колебаний преломленного луча в види-
мые амплитудные колебания.
ЛЮМИНЕСЦЕНТНЫЙ МИКРОСКОП.
Разрешающая способность – 0,2 мкм.
Предназначен для экспресс-диагностики вирусных и бактериальных ин-
фекций.
Люминесцентная микроскопия основана на способности некоторых ве-
ществ светиться под действием коротковолновых ультрафиолетовых (УФ)
лучей. Препараты для люминесцентной микроскопии окрашивают специаль-
ными люминесцентными красителями – флуорохромами (акридиновый оранжевый, аурамин и др.). В качестве источника УФ-света обычно исполь-
зуют ртутно-кварцевую лампу. Под действием УФ-излучения окрашенные клетки начинают светиться красным или зеленым светом.
32
ЭЛЕКТРОННЫЙ МИКРОСКОП.
Разрешающая способность – менее 1Å (Å – ангстрем, 1Å = 0,1нм = 10-4
мкм, 1 мкм=0,01мм).
Предназначен для изучения строения вирусов, бактерий и отдельных макромолекул.
Высокая разрешающая способность достигается малой длиной волны электронов. В электронном микроскопе вместо света используют поток элек-
тронов в безвоздушной среде. Источником электронов является вольфрамо-
вая нить катода, разогреваемая до высокой (2500-29000С) температуры. Роль оптических линз выполняют электромагниты. Для исследования препаратов в электронном микроскопе применяют специальные пленки, проницаемые для электронов.
2.Техника приготовления и окрашивания бактериологического препа-
рата. Принцип простого и сложного методов окраски.
Этапы приготовления мазка:
1.Собственно приготовление мазка.
2.Высушивание.
3.Фиксация.
4.Окрашивание.
1.Собственно приготовление мазка:
из культуры бактерий, выращенной в жидкой питательной среде:
-обезжирить предметное стекло;
-нанести на стекло с помощью бактериологической петли каплю куль-
туры и распределить ее параллельными движениями;
из культуры бактерий, выращенной на плотной питательной среде:
33
- на обезжиренное стекло нанести каплю физиологического раствора, за-
тем внести в эту каплю петлей небольшое количество культуры бактерий с плотной питательной среды и распределить параллельными движениями.
2.Высушивание мазка на воздухе или высоко над пламенем спиртовки (в
струе теплого воздуха).
3.Фиксация мазка:
жаром, в пламени спиртовки – при изучении формы и расположения бак-
терий и дифференциации их при окраске сложным методом;
химическим методом – при изучении нативных (сохранивших естествен-
ную структуру) препаратов от больного (кровь, ликвор, гной и т.д.). В каче-
стве химических фиксаторов чаще используют этиловый и метиловый спирт,
а также смесь Никифорова (смесь этилового спирта и эфира в соотношении
1:1).
Цель фиксации:
-убить микроорганизмы;
-прикрепить их к предметному стеклу;
-улучшить их прокрашивание.
4.Окрашивание препарата простым и сложным методом.
Простой метод окраски позволяет изучать форму, размеры и взаимо-
расположение бактерий. Для окраски используют только один краситель,
чаще фуксин Пфейффера или метиленовый синий.
34

Принципиальный рецепт простого водно-спиртового красителя:
1 часть красителя
+
10 частей 96о этилового спирта
+
100 частей дистиллированной воды
Сложные методы окраски позволяют дифференцировать микроорга-
низмы (окраска по Граму, Цилю-Нильсену) или видеть отдельные структуры клеток (окраска по Бурри-Гинсу, Нейссеру, Романовскому-Гимзе). Для окра-
ски используют более одного красителя.
3. Окраска по Граму. Примеры грамположительных и грамотрицатель-
ных бактерий. Механизм окраски.
Окраска по Граму (в модификации Синѐва):
-на фиксированный мазок накладывают фильтровальную бумагу, пропи-
танную генциан-фиолетовым, смачивают водой, окрашивают 2 минуты;
-снимают бумагу и наносят на мазок раствор Люголя на 1 минуту, затем краситель сливают;
-обесцвечивают мазок 96о спиртом 10-15 секунд;
-промывают мазок водой;
-докрашивают мазок фуксином Пфейффера 30 секунд;
-промывают мазок водой, высушивают фильтровальной бумагой и микро-
скопируют.
Механизм окраски по Граму.
Дифференцировка на грамположительные и грамотрицательные бакте-
рии зависит от строения клеточной стенки, основой которой является пепти-
35
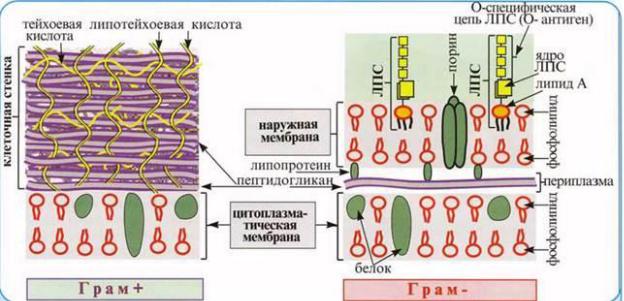
догликан. У грамположительных бактерий толщина пептидогликана 50 нм, у
грамотрицательных – не более 120 нм.
При окрашивании препарата генциан-фиолетовым, а затем раствором Люголя, образуется комплекс генциан-фиолетовый + йод. Все клетки окра-
шиваются в сине-фиолетовый цвет. При обработке спиртом у грамположи-
тельных бактерий образовавшийся комплекс не обесцвечивается. Поэтому при окрашивании фуксином Пфейффера они сохраняют сине-фиолетовый цвет. У грамотрицательных бактерий комплекс генциан-фиолетовый + йод обесцвечивается спиртом и при окраске фуксином Пфейффера они приобре-
тают розово-красный цвет.
В результате окраски бактерии дифференцируют на грамположительные
(сине-фиолетовые) или грамотрицательные (розово-красные).
К грамположительным относят все кокки (кроме нейссерий) и спорооб-
разующие бактерии. К грамотрицательным – нейссерии, неспорообразующие бактерии, спириллы.
Строение клеточной стенки грамположительных и грамотрицательных
бактерий
36
ПРАКТИЧЕСКАЯ РАБОТА
1. С помощью преподавателя освоить технику приготовления мазка культур бактерий из жидкой и с плотной питательных сред.
Этапы приготовления мазка:
1.Собственно приготовление мазка.
-обезжирить предметное стекло сухим мылом и обвести снизу границы мазка карандашом по стеклу;
-приготовление мазка из жидкой питательной среды: прокалить петлю,
над спиртовкой открыть пробку пробирки, обжечь края пробирки, на-
брать каплю культуры петлей. Снова обжечь края пробирки и закрыть пробкой. Пробирку поставить в штатив, нанести каплю культуры на предметное стекло и распределить петлей параллельными движениями
(диаметр мазка – 0,5-1см). Прокалить петлю;
-приготовление мазка с плотной питательной среды: прокалить петлю,
над спиртовкой открыть пробирку с физиологическим раствором, обжечь края пробирки и набрать петлей каплю физиологического раствора. Сно-
ва обжечь края пробирки и закрыть пробкой. Нанести каплю на предмет-
ное стекло. Затем прокалить петлю, над спиртовкой открыть пробирку с плотной питательной средой, обжечь края пробирки. С поверхности плотной среды взять петлей немного культуры бактерий, снова обжечь края пробирки и закрыть пробкой. Внести культуру в каплю физ. раство-
ра, распределить микробную взвесь параллельными движениями (диа-
метр мазка – 0,5-1см). Прокалить петлю.
2.Высушить мазок высоко над пламенем спиртовки.
3.Фиксировать мазок жаром. Для этого стекло 3 раза внести в среднюю треть пламени спиртовки на 1-2 секунды. Приступить к окрашиванию мазка.
37

2.Самостоятельно приготовить мазки из культур стафилококков (плотная питательная среда) и кишечных палочек (жидкая питательная среда).
Окрасить мазок стафилококков метиленовым синим – 3 минуты, а мазок кишечных палочек фуксином Пфейффера – 1 минуту. Промыть мазки водой и высушить фильтровальной бумагой.
3.Приготовить мазки из смесей культур: S.epidermidis + E.сoli и
B.anthracoides + E.coli. Окрасить мазки по Граму.
4.Микроскопировать приготовленные препараты.
5.Зарисовать препараты.
Staphylococcus epidermidis |
Bacillus anthracoides |
+ |
+ |
Escherichia coli |
Escherichia coli |
6. Убрать рабочее место. |
|
38
Занятие №3
Тема. Строение бактериальной клетки. Кислотоустойчивые бактерии. Окра-
ска по Цилю-Нильсену. Спорообразование у бактерий и его значение.
Цель занятия. Изучить строение бактериальной клетки, процесс спорообра-
зования у бактерий. Освоить методику окраски препаратов по методу Циля-
Нильсена.
I.Теоретические знания:
1.Оболочечные структуры бактериальной клетки: капсула (капсульный слой), клеточная стенка, цитоплазматическая мембрана. Особенности кле-
точной стенки кислотоустойчивых бактерий. Окраска по Цилю-Нильсену.
Механизм окраски. L-формы бактерий, их медицинское значение. Мико-
плазмы.
2. Цитоплазма, ее составные: нуклеоид (генофор), плазмиды, рибосомы, ме-
зосомы, включения.
3.Поверхностные структуры бактериальной клетки: жгутики, пили.
4.Спорообразование у бактерий.
II.Практические навыки:
1.Приготовление мазка кислотоустойчивых (вакцинные туберкулезные бак-
терии – BCG) и кислотоподатливых (стафилококки) бактерий.
2. Окраска мазка по Цилю-Нильсену.
39
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЗАНЯТИЮ
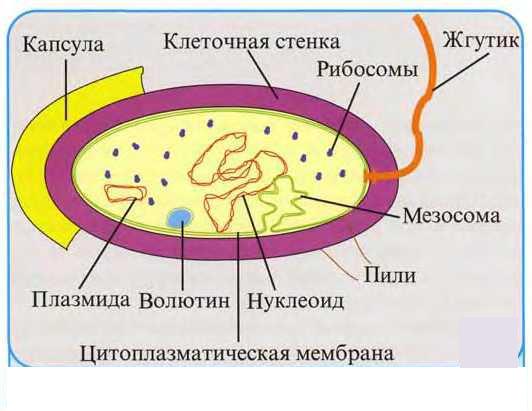
К основным структурам бактериальной клетки относят оболочечные
структуры, цитоплазму и органеллы.
Строение бактериальной клетки
1.Оболочечные структуры бактериальной клетки.
Коболочечным структурам бактериальной клетки относят капсульный слой, клеточную стенку и цитоплазматическую мембрану.
Снаружи многие бактерии имеют КАПСУЛЬНЫЙ СЛОЙ (МИКРО-
КАПСУЛУ). Это слизистое образование, не превышающее диаметр бактери-
альной клетки. У некоторых бактерий имеется ИСТИННАЯ КАПСУЛА –
слизистый слой, превышающий диаметр бактериальной клетки. Капсула не является обязательной структурой. У большинства бактерий она имеет поли-
сахаридную природу. У некоторых (Bacillus anthracis) – состоит из белка.
40
