
- •Предмет, задачи общей и неорганической химии. Роль химии в естественных науках.
- •Основные понятия химии
- •Основные понятия химии.
- •Основные стехиометрические законы.
- •Газовые законы: г. Люссака, Авогадро, объединенный газовый закон.
- •Строение атома; развитие учения о строении атома; модели Томсона, Резерфорда, Бора.
- •Характеристика основных квантовых чисел.
- •Важнейшие классы и номенклатура неорганических веществ.
- •Периодический закон и периодическая система элементов.
- •Ковалентная химическая связь. Способы образования ковалентной связи. Основные характеристики.
- •Геометрия структур с ковалентным типом связи (гибридизация sp, sp2, sp3)
- •Метод валентных связей и метод молекулярных орбиталей.
- •Ионная и металлическая связь.
- •Межмолекулярное взаимодействие. Водородная связь.
- •Кристаллическое, жидкое и аморфное состояние веществ.
- •Скорость химических реакций. Константа скорости и ее физические свойства
- •Влияние температуры на скорость химических реакций. Основные положения теории активации Аррениуса.
- •Катализ. Влияние катализаторов на скорость химических реакций.
- •Необратимые и обратимые реакции. Принцип Ле Шателье.
- •Дисперсные системы и их характеристика.
- •3. По агрегатному состоянию дисперсионной среды и дисперсной фазы.
- •Способы выражения концентрации растворов.
- •Энергетика химических связей. Характеристика систем. Функции состояния.
- •Внутренняя энергия. Энтальпия и энтропия.
- •Энергия Гиббса.
- •Закон Генри. Законы Рауля.
- •Осмотическое давление. Закон Ван-Гоффа.
- •Особенности растворов электролитов. Основные положения электролитической диссоциации.
- •Буферные растворы и их характеристика. Уравнение Гендерсона-Хассельбаха.
- •Ионное произведение воды. Водородный показатель.
- •Произведение растворимости. Реакции обмена в растворах электролитов.
- •Гидролиз солей. Количественные характеристики гидролиза.
- •Теория овр. Важнейшие окислители и восстановители. Метод электронного баланса.
- •Ионно-электронный метод (метод полуреакций).
- •Классификация овр.
- •Электрохимические процессы. Электронный потенциал. Водородный электрод.
- •Электрохимический ряд напряжения металлов. Уравнение Нернста.
- •Гальванический элемент и его влияние на протекание овр.
- •Электролиз растворов и расплавов.
- •Комплексные соединения. Номенклатура и классификация.
- •Константа устойчивости и константа неустойчивости (характеристика кс)
Особенности растворов электролитов. Основные положения электролитической диссоциации.
Электролиты – вещества, проводящие электрический ток.
Законы Аррениуса:
Молекулы веществ, проводящих в растворе электрический ток, при растворении в воде диссоциируют на ионы.
Образовавшиеся при электрической диссоциации ионы имеют заряд и отличаются по свойствам от нейтральных атомов и молекул.
При пропускании электрического тока через раствор электролита положительно заряженные ионы направляются к катоду(-), а отрицательно заряженные – к аноду(+).
Буферные растворы и их характеристика. Уравнение Гендерсона-Хассельбаха.
Буферные растворы — растворы, сохраняющие неизменными значения рН при разбавлении или добавлении небольшого количества сильной кислоты или основания.
Буфер состоит из слабой кислоты и ее соли, или слабого основания и его соли.
Эффективным буфером является буфер, который отличается по значению рН в диапазоне рН от -1 до +1.
Каждая из буферных систем характеризуется определенной присущей ей концентрацией ионов Н+ (активной кислотностью), которую система и стремится сохранить на неизменном уровне при добавлении к ней сильной кислоты либо щелочи.
Уравнение Гендерсона-Хассельбаха:
![]()
Значение рК для слабого электролита является величиной постоянной, не зависит от концентрации этого электролита в растворе и приводится в соответствующих справочниках.
В водных растворах рН и рОН являются сопряженными величинами. Их сумма всегда равна 14, т.е.:
рН + рОН = 14
Зная концентрацию ионов Н+или рН можно вычислить концентрацию гидроксильных ионов или рОН.
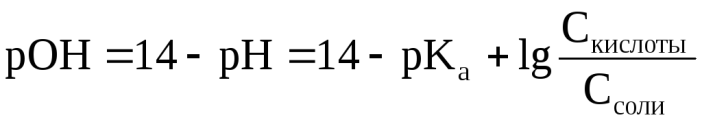
Уравнения Гендерсона-Гассельбаха для расчета рОН и рН в оснóвных буферных системах выглядят следующим образом:
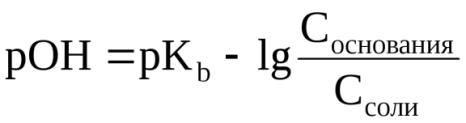
![]()
- где pKb = –lg Kb (основания), Соснования и Ссоли – исходные молярные концентрации компонентов данных буферных систем, т.е. слабого основания и его соли с сильной кислотой.
Уравнение Гендерсона-Гассельбаха является приближенным и его не рекомендуется использовать в следующих случаях:
1) если кислота либо основание буферной системы не является достаточно слабым электролитом (например, для кислоты pKa < 3). Тогда нельзя пренебрегать их диссоциацией в присутствии собственной соли;
2) если кислота либо основание буферной системы являются, наоборот, слишком слабыми электролитами (например, для кислоты pKa > 11). Тогда нельзя пренебрегать гидролизом их солей.
Ионное произведение воды. Водородный показатель.
Вода - слабый электролит - диссоциирует, образуя ионы H+ и OH-. Эти ионы гидратированы, то есть, соединены с несколькими молекулами воды, но для простоты мы записывали их в негидратированной форме
H2O = H+ + OH−
Запишем выражение для константы равновесия, опираясь на закон действия масс:
K = [H+]·[OH—]/[H2O]
Концентрацию воды, принято исключать из данного выражения, вследствие ее практически постоянного значения в разбавленных растворах. Получаем новую константу равновесия KН2О, которая называется ионным произведением воды:
KН2О = [H+]·[OH—]
При температуре 25ºС KН2О = 1·10-14 и остается постоянным в водных растворах кислот, щелочей, солей или других соединений.
KН2О = [H+]·[OH—] = 1·10-14
При повышении температуры ионное произведение воды сильно возрастает.
Полученное выражение применимо не только к чистой воде, но и к растворам.
Если осуществляется условие [H+] = [OH—], то раствор называется нейтральным, но обычно эти величины не совпадают, тогда при увеличении одного показателя, другой должен уменьшаться, так, чтобы их произведение оставалось постоянным (1·10-14).
Кислотно-основные свойства растворов определяются величиной концентрации ионов водорода или гидроксила. Мы уже знаем, что ионное произведение воды при определенной температуре постоянно, а [H+] и [OH—] — переменные, то по их величинам можно говорить о кислотности или щелочности раствора. При нейтральном характере раствора, т.е. [H+] = [OH—], получаем следующее:
[H+] = [OH—] = (KН2О)1/2 = (1·10-14)*1/2 = 10-7 М
Соотношение между количеством ионов [H+] и [OH-] определяет характер среды:
[H+] =10-7= [OH-] - нейтральная среда
[H+] >10-7> [OH-] - кислая среда
[H+] <10-7< [OH-] - щелочная среда.
Водородный показатель рН - это отрицательный десятичный логарифм концентрации ионов водорода рН = - lg[H+].
Аналогично рOН = - lg[OH-].
Логарифмируя ионное произведение воды, получаем pH + pOH = 14.
Примеры.
Если [H+] = 10-2M, то рН = 2, а [ОH-]= 10-12M.
Если [ОH-] = 10-4M, то [H+]= 10-10M, а рН = 10.
Если рН = 8, то [H+]= 10-8M, а [ОH-] = 10-6M
Если рОН = 5, то рН = 9, а [H+]= 10-9M.
