
- •Учреждение образования
- •Управляемая самостоятельная работа № 7
- •Сердечная и гладкая мышечные ткани
- •Глава 1. Гистогенез и регенерация мышечной ткани
- •Глава 2. Сердечная поперечно-полосатая мышечная ткань
- •Глава 3. Гладкая мышечная ткань
- •Глава 4. Специальные гладкомышечные ткани
- •Список используемой литературы
Глава 2. Сердечная поперечно-полосатая мышечная ткань
Структурно-функциональной единицей сердечной поперечно-полосатой мышечной ткани является клетка - кардиомиоцит.
По строению и функциям кардиомиоциты подразделяются на две основные группы:
типичные или сократительные кардиомиоциты, образующие своей совокупностью миокард;
атипичные кардиомиоциты, составляющие проводящую систему сердца и подразделяющиеся в свою очередь на три разновидности.
Сократительный кардиомиоцит представляет собой почти прямоугольную клетку 50-120 мкм в длину, шириной 15-20 мкм, в центре которой локализуется обычно одно ядро. Покрыт снаружи базальной пластинкой. В саркоплазме кардиомиоцита по периферии от ядра располагаются миофибриллы, а между ними и около ядра локализуются в большом количестве митохондрии. В отличие от скелетной мышечной ткани, миофибриллы кардиомиоцитов представляют собой не отдельные цилиндрические образования, а по существу сеть, состоящую из анастомозирующих миофибрилл, так как некоторые миофиламенты как бы отщепляются от одной миофибриллы и наискось продолжаются в другую. Кроме того, темные и светлые диски соседних миофибрилл не всегда располагаются на одном уровне, и потому поперечная исчерченность в кардиомиоцитах выражена не столь отчетливо, как в скелетных мышечных волокнах. Саркоплазматическая сеть, охватывающая миофибриллы, представлена расширенными анастомозирующими канальцами. Терминальные цистерны и триады отсутствуют. Т-канальцы имеются, но они короткие, широкие и образованы не только углублением плазмолеммы, но и базальной пластинки. Механизм сокращения в кардиомиоцитах практически не отличается от такового в скелетных мышечных волокнах.
Сократительные кардиомиоциты, соединяясь встык друг с другом, образуют функциональные мышечные волокна, между которыми имеются многочисленные анастомозы. Благодаря этому из отдельных кардиомиоцитов формируется сеть - функциональный синтиций. Наличие щелевидных контактов между кардиомиоцитами обеспечивает одновременное и содружественное их сокращение вначале в предсердиях, а затем и в желудочках.
Области контактов соседних кардиомиоцитов носят название вставочных дисков. Фактически, никаких дополнительных структур (дисков) между кардиомиоцитами нет. Вставочные диски - это места контактов цитолеммы соседних кардиомиоцитов, включающие в себя простые, десмосомные и щелевидные контакты. Обычно во вставочных дисках различают поперечный и продольный фрагменты. В области поперечных фрагментов имеются расширенные десмосомные соединения. В этих же местах с внутренней стороны плазмолемм прикрепляются актиновые филаменты саркомеров. В области продольных фрагментов локализуются щелевидные контакты. Посредством вставочных дисков обеспечивается как механическая, так и метаболическая (прежде всего ионная) связь кардиомиоцитов.
Сократительные кардиомиоциты предсердий и желудочков несколько отличаются между собой по морфологии и функциям. Так, кардиомиоциты предсердий в саркоплазме содержат меньше миофибрилл и митохондрий, в них почти не выражены Т-канальцы, а вместо них под плазмолеммой выявляются в большом числе везикулы и кавеолы - аналоги Т-канальцев. Кроме того, в саркоплазме предсердных кардиомиоцитов у полюсов ядер локализуются специфические предсердные гранулы, состоящие из гликопротеиновых комплексов. Выделяясь из кардиомиоцитов в кровь предсердий, эти вещества влияют на уровень давления крови в сердце и сосудах, а также препятствуют образованию тромбов в предсердиях. Следовательно, предсердные кардиомиоциты, кроме сократительной, обладают и секреторной функцией. В желудочковых кардиомиоцитах более выражены сократительные элементы, а секреторные гранулы отсутствуют.
Вторая разновидность кардиомиоцитов - атипичные кардиомиоциты образуют проводящую систему сердца, состоящую из:
синусо-предсердный узел;
предсердно-желудочковый узел;
предсердно-желудочковый пучок (пучок Гиса), ствол, правую и левую ножки;
концевые разветвления ножек - волокна Пуркинье.
Атипичные кардиомиоциты обеспечивают генерирование биопотенциалов, их проведение и передачу на сократительные кардиомиоциты.
По своей морфологии атипичные кардиомиоциты отличаются от типичных рядом особенностей:
они крупнее (длина 100 мкм, толщина 50 мкм);
в цитоплазме содержимся мало миофибрилл, которые расположены неупорядочено и потому атипичные кардиомиоциты не имеют поперечной исчерченности;
плазмолемма не образует Т-канальцев;
во вставочных дисках между этими клетками отсутствуют десмосомы и щелевидные контакты.
Атипичные кардиомиоциты различных отделов проводящей системы отличаются между собой по структуре и функциям и подразделяются на три основные разновидности:
Р-клетки (пейсмекеры) - водители ритма (I типа);
переходные клетки (II типа);
клетки пучка Гиса и волокон Пуркинье (III тип).
Клетки I типа (Р-клетки) составляют основу синусо-предсердного узла, а также в небольшом количестве содержатся в атриовентрикулярном узле. Эти клетки способны самостоятельно генерировать с определенной частотой биопотенциалы и передавать их на переходные клетки (II типа), а последние передают импульсы на клетки III типа, от которых биопотенциалы передаются на сократительные кардиомиоциты.
Источники развития кардиомиоцитов - миоэпителиальные пластинки, представляющие собой определенные участки висцеральных листков спланхнотома, а конкретнее из целомического эпителия этих участков.
Биопотенциалы сократительные кардиомиоциты получают из двух источников:
из проводящей системы сердца (прежде всего из синусо-предсердного узла);
из вегетативной нервной системы (из ее симпатической и парасимпатической части).
Регенерация сердечной мышечной ткани
Кардиомиоциты регенерируют только по внутриклеточному типу. Пролиферации кардиомиоцитов не наблюдается. Камбиальные элементы в сердечной мышечной ткани отсутствуют. При поражении значительных участков миокарда (в частности, при инфаркте миокарда) восстановление дефекта происходит за счет разрастания соединительной ткани и образования рубцов (пластическая регенерация). Естественно, что сократительная функция в этих участках отсутствует. Поражение проводящей системы сопровождается нарушением ритма сердечных сокращений.
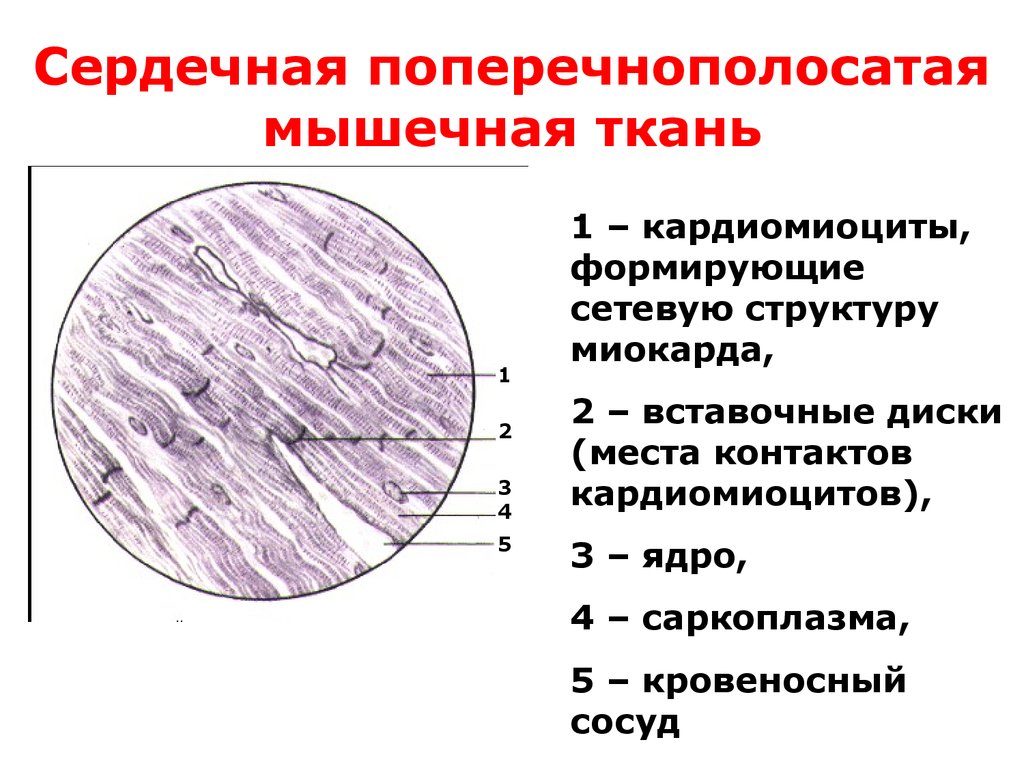
Рис. 2 – Сердечная поперечно-полосатая мышечная ткань
