
- •Міністерство охорони здоров'я України
- •Модуль 2. Кількісний хімічний аналіз цілі модуля:
- •Заняття 14
- •Актуальність теми
- •Цілі навчання
- •Орієнтовна основа дій
- •1. Послідовність аналітичних операцій в гравіметричному методі осадження
- •2. Правила роботи з аналітичними терезами
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталони рішення типових розрахункових задач
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №15
- •Актуальність теми
- •Зміст навчання
- •Орієнтовна основа дій
- •1. Метод відгонки. Схема визначення вологи в лікарських сполуках
- •2. Алгоритм визначення масової частки вологи методом непрямої відгонки
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №16
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Короткі методичні вказівки до роботи на практичному занятті
- •Граф логічної структури теми: Титриметричні методи аналізу. Титранти, їх приготування, розрахунки в титриметрії. Приготування розчинів 0,1м NaOh та 0,1м нСl
- •Заняття № 17
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм стандартизації розчину hCl за розчином натрію тетраборату
- •2. Алгоритм стандартизації розчину NaOh за оксалатною кислотою
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №18
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії Алгоритм визначення масової відсоткової частки натрію гідроксиду та натрію карбонату в суміші
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №19
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 20
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм визначення загальної твердості води
- •2. Схема зворотного комлеконометричнеого визначення свинцю
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №21
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії Алгоритм приготування та стандартизації 0,1 м розчину AgNo3
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталон рішення завдання №7.
- •Короткі методичні вказівки до роботи на практичному занятті
- •Граф логічної структури теми: Осаджувальне титрування. Аргентометрія, меркурометрія. Визначення масової частки галогенідів в препараті осаджувальним
- •Заняття № 22
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм стандартизації розчину йоду за тіосульфатом натрію
- •2.Алгоритм стандартизації розчину калію перманганату за розчином натрію оксалату
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталон рішення завдання №7
- •Еталон рішення завдання №8
- •Заняття № 23
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 27
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа діяльності Цифрові значення крітерія стьюдента
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 25
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Приклади завдань колоквіуму:
- •Заняття № 26
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Питання до підсумкового модульного контролю за темою «Кількісний хімічний аналіз»
- •Приклади ситуаційних завдань до підсумкового модульного контролю:
- •Модуль 3. Кількісний інструментальний аналіз Цілі модуля:
- •Заняття № 27
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм кількісних фотометричних визначень методом градуювального графіка
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №28
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Реєстрація спектру поглинання кофеїну
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №30
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм вимірювання показника заломлення на рефрактометрі
- •Фактори показників заломлення f розчинів лікарських речовин
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 30
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм вимірювання інтенсивності флуоресценції
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 31
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм потенціометричного визначення рН розчину
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Граф логічної структури теми:Електрохімічні методи аналізу. Потенціометрія
- •Заняття № 33
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №33
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм полярографічних визначень
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №34
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм проведення висхідної паперової або тонкошарової хроматографії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Граф логічної структури теми: Хроматографічні методи. Паперова та тонкошарова хроматографія
- •Заняття № 35
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 37
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа діяльності Класифікація методів спектрального аналізу
- •Приклади питань колоквіуму:
- •Заняття № 36
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 38
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Приклади ситуаційних завдань для підсумкового модульного контролю
Еталони рішення типових розрахункових задач
10. Розчин препарату Nа3РО4 ( mн = 0,7030 г) осадили у вигляді MgNН4РО4∙ 6Н2О. Після фільтруваання та промивання осад прокалили при 1000°С. Маса отриманого осаду Mg2P2О7 склала 0, 4320 г. Розрахуйте масову відсоткову частку фосфора в наважці.
Рішення
mгр.ф (Mg2P2О7) = 0,4320 г;
F = 2М(Р) / М(Mg2P2О7) = 0,2782; mн = 0,7030 г;
W,% = mгр.ф ∙ F ∙ 100 / mн
w, %(Р) = 0,4320 ∙ 0,2782 ∙ 100 / 0,7030 = 17,10 %.
Приклад 3. При прожарюванні забрудненного препарату натрію оксалату mн = 1,3906 г отримали залишок масою mгр.ф = 1,1436 г. Визначити ступінь чистоти зразку.
Рішення.
Слід допустити, що різниця між вихідною та кінцевою масами відповідає втраті вуглецю оксиду при прожарюванні. Аналіз базується на вимірюванні цієї величини:
t
Na2C2О4 → Nа2СО3 + СО↑
ν(СО) = ν (Na2C2O4),
таким чином, w, %(Na2C2O4) = (mн - mгр.ф) ∙ F ∙ 100 / mн ;
F = M(Na2C2O4) / M(CO) = 4,784;
w, %(Na2C2O4) = (1,3906 – 1,1436) ∙ 4,784 ∙ 100 / 1,3906 = 84,97 %.
Короткі методичні вказівки до роботи на практичному занятті
На початку заняття перевіряється підготовленність студентів до заняття шляхом усного опитування, проводиться інструктаж з техніки безпеки з хімічними реактивами. Далі студенти знайомляться з методиками експериментальної роботи . Черговим пропонується організувати робоче місце для групи. Студенти працюють самостійно у відповідності до ООД, викладених у методичних вказівках. По закінченні роботи студенти записують свої спостереження, рівняння відповідних хімічних реакцій, проводять необхідні розрахунки. Далі проводиться підсумковий контроль за темою (набори тестів). Потім розглядаються результати самостійної роботи, аналізуються помилки, підводяться підсумки заняття.
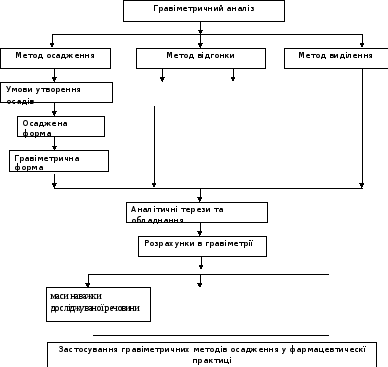
Граф логічної структури теми: Гравіметричний метод аналізу. Визначення масової частки магнію у солях магнію методом осадження. Розрахунки в гравіметрії
Прямий
Непрямий

об'єму
розчину осадника
Результатів
визначень




Заняття №15
Тема: Гравіметричний метод аналізу, метод відгонки. Визначення вологи у препаратах
Актуальність теми
Метод відгонки дозволяє визначати масу залишку після виділення певного компоненту. Непрямий метод відгонки найчастіше застосовують при визначенні вологи у лікарських препаратах, іноді для визначення вмісту карбонатів, сульфідів та сульфітів після обробки проб кислотою і проводять способом висушування з подальшим прожарюванням. Наприклад, так визначають вмісту кристалізаційної води у натрію тетрабораті. Найчастіше непрямий метод відгонки використовують у контрольно-аналітичній практиці при визначенні доброякісності лікарських субстанцій, які мають у складі молекули води (кристалогідрати), які при порушенні умов зберігання можуть втрачати воду.
Загальна мета. Вміти використовувати методи відгонки у гравіметричному аналізі для кількісного визначення вмісту лікарських речовин, домішок та вологи у лікарських речовинах.
Конкретні цілі. Вміти:
Класифікувати гравіметричні методи відгонки.
Визначати масову частку вологи методом непрямої відгонки.
Розраховувати масову частку компонента у методах відгонки.
