
4 и 5
.docxЗАДАЧИ К КОНТРОЛЬНОЙ РАБОТЕ №10
Вариант 1
|
1. |
Среди нижеперечисленных металлов найти те, которые могут восстановить катион железа Fe2+: Mn, Zn, Pb, Cu. |
Выпишем значения стандартных электродных потенциалов данных металлов:
φ0(Fe2+/Fe0)= - 0,473В φ0(Zn2+/Zn0) =-0,76 В
φ0(Mn2+/Mn0)= -1,18 В φ0(Pb2+/Pb0) =−0,126 В
φ0(Cu2+/Cu0) = +0,337 В
Так как Mn и Zn имеют более низкие электродные потенциалы, чем Fe, то поэтому они являются более сильными восстановителями по сравнению с железом:
Zn0 + Fe2+ → Zn2+ + Fe0
Mn0 + Fe2+ → Mn2+ + Fe0
Pb0 + Fe2+ ↛
Cu0 + Fe2+ ↛
|
2. |
Среди нижеперечисленных катионов металлов найти те, которые могут окислить свинец: Mg+2, Zn+2, Hg+2, Ag+. |
Согласно ряду напряжений металлов
φ0(Hg2+/Hg0)= 0,79 В φ0(Zn2+/Zn0) =-0,76 В
φ0(Mg2+/Mg0) = -2,36 В φ0(Pb2+/Pb0) = −0,126 В
φ0(Ag+/Ag0) = 0,799 В
Серебро и ртуть имеют стандартные электродные потенциалы выше, чем свинец.
Таким образом, катион серебра и катион ртути являются окислителями более сильными, чем катион свинца, и будут окислять Pb0 до Pb2+:
Hg2+ + Pb0 → Hg0 + Pb2+; 2Ag++ Pb0 → 2Ag0 + Pb2+;
Mg+2 + Pb0↛ ; Zn2+ + Pb0↛
|
3. |
Рассчитать Э.Д.С. гальванического элемента (−)
Zn если концентрация cульфата цинка ZnSO4 в растворе равна 0,01М, а концентрация серной кислоты H2SO4 – 0,0001М и полагая, что электролиты полностью дисссоциированы. В каком направлении будут перемещаться электроны во внешней цепи при работе этого элемента? |
|
Дано: |
Решение |
|
C(ZnSO4) = 0,01 моль/л C(H2SO4) = 0,0001 моль/л E0(Zn2+/Zn0) =-0,76 В E0(H+/H2) = 0 В |
Для решения задачи воспользуемся формулой Нерста. E = E0 + 0.0591 *lg ([Ox]/[Red])/n E(Zn2+/Zn0) = E0(Zn2+/Zn0) + 0.0591 *lg ([Zn2+]/[ Zn0])/2 E(Zn2+/Zn0) = -0,76 + 0.0591 *lg (0,01/1)/2 = -0,8191 В
E(H+/H2) == -E0(H+/H2) + 0.0591 *lg ([H+]/[ H2]) E(H+/H2) = -0,2364 В
ЭДС гальванического элемента вычисляется как: E = E1 – E2 Причём, при вычислении ЭДС меньший (в алгебраическом смысле) электродный потенциал вычитается из большего. E = E(H+/H2) - E(Zn2+/Zn0) E = -0,2364 – (-0,8191) = 0.5827 В
E(H+/H2) > E(Zn2+/Zn0) Значит, электроны будут двигаться от цинкового электрода к водородному электроду. При этом цинк будет растворяться. |
|
E -? |
Ответ: E = 0.5827 В; электроны будут двигаться от цинкового электрода к водородному электроду
|
4. |
В гальваническом элементе протекает токообразующая реакция: Fe + NiCl2 = FeCl2 + Ni Составьте электронное уравнение реакции, если:
Какова схема работы этого элемента? |
Ni2+ + 2e → Ni 2 1 катод
2
Fe - 2e → Fe2+ 2 1 анод
Fe + Ni2+ → Ni↓+ Fe2+
![]()
![]() >
>
![]()
![]() ,
значит,
электроны будут двигаться от железа к
никелю.
,
значит,
электроны будут двигаться от железа к
никелю.
Схема элемента имеет вид:
(−)
Fe
FeCl2
![]() NiCl2
Ni
(+),
NiCl2
Ni
(+),
|
5. |
Составьте схему работы двух гальванических элементов, в одном из которых хром является анодом, в другом – катодом. Составьте уравнения электронных реакций, происходящих на электродах. |
Хром является анодом:
3Cr + Fe(NO3)2 → Cr(NO3)2 + 2Fe↓
Fe2+ + 2e → Fe 2 1 катод E0(Fe2+/Fe)= -0,441 В
2
Cr - 2e → Cr2+ 2 1 анод E0(Cr2+/Cr)= -0,9 В
Cr + Fe2+ → Fe ↓+ Cr2+
E0(Fe2+/Fe)>E0(Cr2+/Cr) значит, электроны будут двигаться от хрома к железу
Схема элемента имеет вид:
(−)Cr Cr(NO3)2 Fe(NO3)2 Fe (+),
Хром является катодом:
Mn + Cr(NO3)2→ Mn(NO3)2 + Cr
Mn + 2e → Mn2+ 2 1 анод E0(Mn2+/Mn)= -1,18 В
2
Cr - 2e → Cr2+ 2 1 катод E0(Cr2+/Cr)= -0,9 В
Mn + Cr2+ → Cr ↓+ Mn2+
E0(Cr2+/Cr) > E0(Mn2+/Mn), значит, электроны будут двигаться от марганца к хрому.
Схема элемента имеет вид:
(−)
Mn
Mn(NO3)2
![]() Cr(NO3)2
Cr
(+),
Cr(NO3)2
Cr
(+),
Вариант 4(коррозия)
|
1. |
Написать уравнения процессов, протекающих при электролизе расплава гидроксида лития на инертных электродах. |
На инертных электродах протекают следующие процессы:
K(–):Li+ + e =Li0 A(+): 4OH− −4e =2H2O + O2
Электролиз расплава нитрата калия имеет вид:
4LiOH → 4Li + H2O↑ + О2↑
|
2. |
Напишите уравнения процессов, проходящих на электродах при электролизе водного раствора нитрата свинца с инертным анодом. |
Нитрат свинца диссоциирует согласно уравнению:
Pb(NO3)2 = Pb2+ + 2NO3-
.
K(–): Pb2+ + 2е → Pb0 2 1
2H2О + 2е- = H2 + 2ОН- 2 4
А(+): 2H2O – 4e = 4H+ + O2↑ 4 1
Pb2+ +2H2О + 2H2О → Pb0 + H2 + 2ОН- + O2 + 4H+
Pb(NO3)2 + 2H2O → Pb + H2 + 2HNO3 + O2
|
3. |
Железное изделие покрыли медью. Какое это покрытие – анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и хлорводородной (соляной) кислоте. Какие продукты коррозии образуется в первом и во втором случаях? |
Если железо покрыть медью мы получим катодное покрытие.
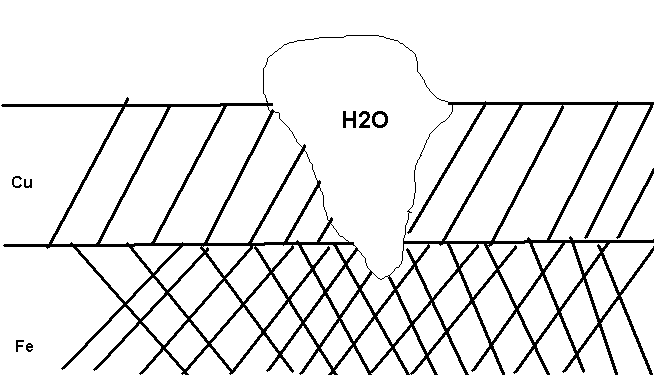
Процесс в нейтральной среде:
Катод(-):2H2О + 2е- = H2 + 2ОН-
Анод(+): Fe -2e → Fe2+
Fe + 2H2О → Fe(OH)2 + H2
Затем Fe(OH)2 окисляется до Fe(OH)3
4 Fe(OH)2 + 2H2O + O2 →4 Fe(OH)3
Процесс в кислой среде:
Катод(-):2H+ + 2е- = H2
Анод(+): Fe -2e → Fe2+
Fe + 2HCl → FeCl2 + H2
Анодное покрытие
Для него мы можем использовать цинк
Процесс в нейтральной среде:
Катод(-):2H2О + 2е- = H2 + 2ОН-
Анод(+): Zn -2e → Zn2+
Zn + 2H2О →Zn(OH)2 + H2
Процесс в кислой среде:
Катод(-):2H+ + 2е- = H2
Анод(+): Zn -2e → Zn2+
Zn + 2HCl → ZnCl2 + H2
Вывод: При анодном покрытии разрушается анодный слой, а при катодном покрытии разрушается сама железное изделие, если нарушена защита (царапина)
|
4. |
Напишите уравнения реакций, протекающих при электролизе водного раствора сульфата марганца (II) на марганцевом аноде. Как изменится рН среды около электродов? |
При проведении электролиза с использованием активного (расходуемого) анода процесс усложняется и конкурирующими реакциями на электродах являются следующие:
на аноде — окисление анионов и гидроксид-ионов, анодное растворение металла — материала анода;
на катоде — восстановление катиона соли и ионов водорода, восстановление катионов металла, полученных при растворении анода.
На аноде возможны процессы:
2H2O – 4e = 4H+ + O2↑ φ01 = 1,23 В
Mn -2e → Mn2+ φ02 = -1,18 В
Т.к φ02<φ01 , то будет происходить окисление марганца
На катоде:
2H2O + 2e = 2OH- + H2↑ φ03 = -0,41 В
Mn2++ 2e → Mn φ02 = -1,18 В
Т.к φ02<φ03 , то будет происходить выделение водорода.
Около анода рН будет кислый из-за гидролиза: Mn2+ + H2O → MnOH+ +H+
Около катода рН будет щелочной
|
5. |
При электролизе водного раствора ZnSO4 током 2А за 10 часов на катоде выделилось 1,25 л Н2. Рассчитать массу выделившегося цинка. |
Сульфат цинка диссоциирует согласно уравнению:
ZnSO4 = Zn2+ + SO42-
.
K(–): Zn2+ + 2е → Zn0 2 1
2H2О + 2е- = H2 + 2ОН- 2 4
А(+): 2H2O – 4e = 4H+ + O2↑ 4 1
Zn2+ +2H2О + 2H2О → Zn0 + H2 + 2ОН- + O2 + 4H+
ZnSO4+ 2H2O → Zn + H2 ↑+ H2SO4 + O2↑
Для того чтобы найти массу выделившегося цинка, воспользуемся уравнением закона Фарадея:
m = Мэ*I*t/F , где m – масса образовавшегося вещества, г; Мэ – его эквивалентная масса, п/моль; F – постоянная Фарадея (96500 Кл/моль)
m = 32,5*2*36000/96500 = 24,25 г
ν(H2) = 1,25/22,4= 0,0558 моль
ν(Zn) =24,25/65 = 0,373 моль
выход цинка по току равен:
ω = 0,0558 моль/0,373 моль ≈ 0,15 или 15%
m(Zn)практ. =24,25 * 0,15 = 3.6375 г
Ответ: m(Zn)практ. = 3.6375 г
