
Молекулярная физика III
.pdf
находится в тепловом равновесии с катодом, так что из уравнения (5) определяется и температура катода.
Зная зависимость анодного тока J от скорости электронов, нетрудно найти функцию распределения термоэлектронов по скоростям. Для этого нужно воспользоваться известным соотношением
|
|
|
|
|
n(V ) n0 |
|
|
, |
(6) |
f (V )dV |
|
V
где f (V ) - функция распределения термоэлектронов по скоростям; n(V ) – число частиц, имеющих скорость больше заданного значения V . Дифференцируя (6) по V получаем
|
|
|
f (V ) |
1 |
|
d n(V ) |
. |
(7) |
|||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
n0 |
|
|
dV |
|
||
В нашем случае |
n(V ) |
|
J |
, поэтому имеем |
|
||||||||
|
|
|
|||||||||||
|
n0 |
J0 |
|
|
|
|
|
|
|
|
|||
|
|
|
f (V ) |
1 |
|
|
d i |
. |
(8) |
||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
i0 |
|
|
dV |
|
||||
Таким образом, для нахождения функции распределения по скоростям нужно осуществить графическое дифференцирова-
ние кривой зависимости J J0 от V .
Описание установки.
31
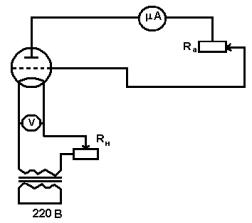
Рис.1.
В настоящей работе для изучения распределения Максвелла используется следующая установка (см. рис.1).
Напряжение в цепи накала лампы подается через понижающий трансформатор. Величина тока в цепи накала регулируется низкоомным реостатом Rн . Величина задерживающего
потенциала устанавливается с помощью магазина сопротивлений Rа , включенного в цепь лампы.
Задание 1. Изучение зависимости логарифма анодного тока от задерживающего потенциала и проверка распределения
32
Максвелла.
1. Установить на магазине сопротивления Rа 0 и с помощью реостата Rн подобрать такое напряжение накала, при
котором ток достаточно велик, но не превышает пределы токоизмерительного прибора.
2.При установленном напряжении накала снять зависимость тока от задерживающего потенциала. Величина задержи-
вающего |
потенциала |
U з определиться выражением |
|
Uз J (Rа |
R ) , где |
R |
– сопротивление микроампермет- |
ра. |
|
|
|
3.Повторить измерения для нескольких напряжений накала.
4.Построить графики зависимости логарифма анодного тока от задерживающего напряжения U з для каждого напряже-
ния накала.
5. Определить угловые коэффициенты зависимостей ln J от
Uи вычислить температуру катода.
6.Используя соотношение (8), построить функции распределения термоэлектронов по скоростям, при различных токах накала.
7.Найти наивероятнейшую скорость термоэлектронов и сравнить ее со скоростью электронов на уровне Ферми (для вольфрама 10 эВ).
Распределение Больцмана.
Для изучения распределения числа частиц в зависимости от потенциальной энергии воспользуемся системой «жидкостьпар». В условии термодинамического равновесия пар насыщен. Такое равновесие устанавливается в закрытом сосуде с жидкостью. Молекулы пограничного слоя между жидкостью и паром находятся в поле сил притяжения молекул, находящихся в объеме жидкости. Для того чтобы покинуть этот слой, молекуле
33
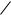
необходимо совершить работу против сил притяжения. При нагревании молекулы жидкости приобретают добавочную энергию, достаточную для преодоления сил притяжения и переходят в пар.
Число молекул в единице объема насыщенного пара определяется законом Больцмана
n n e |
E |
(1) |
kT , |
||
0 |
|
|
где T – температура системы в градусах |
Кельвина; |
|
k 1.38 10 23 Дж/К – постоянная Больцмана; E энергия, необходимая для преодоления потенциального барьера на грани-
це раздела двух фаз; n0 |
– концентрация молекул жидкости при |
|||||||
температуре кипения; |
E |
|
, где |
N |
|
6.02 1026 |
кмоль-1 |
– |
|
a |
|||||||
|
|
Na |
|
|
|
|
||
|
|
|
|
|
|
|
||
число Авогадро; – молярная теплота перехода. Молярная теплота перехода численно равна работе, которую нужно совершить, чтобы перевести 1 кмоль вещества из жидкого в газообразное состояние при температуре перехода. Так как E имеет смысл работы выхода, то формула Больцмана представляется в виде
|
|
|
|
|
|
|
n n0 e |
N a kT |
. |
(2) |
|||
|
|
|||||
Согласно основному закону молекулярно-кинетической |
||||||
теории газа |
|
|
|
|
||
n |
Pн |
|
, |
|
|
(3) |
kT |
|
|
||||
|
|
|
|
|
||
где Pн – давление насыщенного пара.
В состоянии термодинамического равновесия температура в различных точках объема газа постоянна, поэтому вместо n можно измерять Pн .
P P e |
|
|
P P e |
E |
|
|
N a kT |
|
|
. |
|
||
или |
kT |
(4) |
||||
н 0 |
|
н 0 |
|
|||
34
Описание установки.
Схема установки приведена на рисунке 2. Она состоит из двух сообщающихся сосудов 1 и 2, наполненных водой. В сосуде 2 находится кипятильник 3, термометр 4, краны 5 и 6 соединяют сосуды с атмосферой. Манометр 7 измеряет давление в сосуде 1. По линейке 8 определяется разность уровней воды в сосудах. Напряжение на кипятильнике регулируется через ЛАТР.
35

Рис. 2.
Задание 2. Изучение распределения Больцмана и определение работы выхода молекул из жидкости в пар.
1. Открыть краны 5 и 6 для установления в сосудах атмосферного давления.
2. Включить кипятильник* в сеть, установив на ЛАТРе напряжение 24В.
3. Довести воду в сосуде 2 до кипения (до парообразования).
4. Отключить кипятильник и перекрыть кран 5. Как известно, давление насыщенных паров зависит от температуры, поэтому после понижения температуры в сосуде 2 (в результате остывания), давление паров жидкости также понизиться. Для поддержания одинакового давления в обоих сосудах, во второй сосуд будет втягиваться вода из первого. Если в сосуде 1 было атмосферное давление Pa , то после пе-
рекрытия крана 5 давление в сосуде 1 будет меньше |
|
атмосферного на величину P , определяемую по ма- |
|
|
1 |
нометру. Давление P P в сосуде 1 уравновешива- |
|
0 |
1 |
ется давлением насыщенных паров и избыточным
давлением столба жидкости P2 в сосуде 2. |
|
|||
P P P P , |
(5) |
|||
0 |
1 |
н |
2 |
|
отсюда давление насыщенного пара |
|
|||
P P P P , |
(6) |
|||
н |
0 |
1 |
2 |
|
Давление избыточного столба жидкости |
P2 gh , |
|||
где g – ускорение свободного падения; |
– плот- |
|||
ность жидкости; |
h |
– разность уровней жидкости, |
||
определяемая по линейке.
* Кипятильник должен быть полностью погружен в воду.
36
5.Через каждые 5-10° градусов записывать температу-
ру, показания манометра и разность уровней жидкости h . Манометр проградуирован в кг/см2 (1 кг/см2
= 9.8 *104 Па).
6.Подсчитать по формуле (6) давление насыщенных паров.
7.Линеаризовать формулу (4) и построить график в
координатах ln н , |
1 . |
|
|
|
|
T |
|
|
|
|
|
ln н |
|
|
8. Из графика определить |
tg |
1 |
|
и вычислить |
|
|
|||
|
|
T |
|
|
работу выхода молекул в пар.
Контрольные вопросы
1.Сущность метода задерживающего потенциала.
2.Физический смысл энергии Ферми.
3.Как определить минимальную скорость электронов , преодолевающих задерживающий потенциал.
4.Что такое теплота парообразования, удельная теплоемкость?
5.Какой пар называется насыщенным? Зависит ли давление насыщенного пара от давления и температуры?
6.Чему равно давление насыщенного пара при кипении жидкости?
7.Что общего и в чем различие в распределении Больцмана и Максвелла?
Литература
1.Сивухин Д.В. Курс общей физики. М.: Наука, 1975.
Т.2,3.
2.Епифанов Г.И. Физика твердого тела. М. 1965.
37

3.Кикоин И.К., Кикоин А.К. Молекулярная физика. М.:
Наука, 1976.
Приложение
Хорошо известно, что свободные электроны в металле вследствие принципа Паули подчиняются квантовой статистике Ферми-Дирака. При этом распределение по скоростям имеет вид:
|
|
2m3dV dV |
dV |
|
|
|||
dnV |
|
|
x |
y |
|
z |
. |
(1) |
|
|
|
|
|||||
3 |
|
|
||||||
|
h |
exp |
|
|
1 |
|
|
|
|
|
|
|
kT |
|
|
|
|
Распределение электронов по энергиям описывается выражением:
dn |
|
|
|
4 (2m3 ) 12 |
|
. |
(2) |
|
|
|
|
|
|
|
|||
|
h |
3 |
|
|
|
|
|
|
|
|
exp |
|
1 |
|
|||
|
|
|
|
|
kT |
|
|
|
В выражениях (1) и (2) величина d nV означает число электронов в единице объема металла с компонентами скоростей
Vx (Vx dVx ); Vy (Vy dVy ); Vz (Vz dVz ). |
- энергия элек- |
трона; m - масса электрона; h - постоянная Планка; d n - число электронов с энергией от до d . Параметр при аб-
солютном нуле соответствует наибольшей энергии электронов и называется энергией Ферми. Его численное значение определяется из условия нормировки
|
4 (2m)3 / 2 |
|
1/ 2d |
|
|
|
|
|
n dn |
|
|
|
|
|
|
. |
(3) |
h |
3 |
|
|
|
||||
|
|
|
1 |
|
||||
0 |
|
|
0 |
exp |
|
|
||
|
|
|
|
kT |
|
|
|
|
38
Известно, что при определенных условиях (см. ниже) распределение Ферми-Дирака приближается к распределению Мак- свелла-Больцмана. Из выражений (1) и (2) видно, что для этого необходимо выполнение неравенства
|
|
|
|
kT 1 |
(4) |
||
для всех значений . Вследствие положительности |
неравен- |
||
ство (4) можно заменить более сильным условием |
|
||
|
|
|
|
kT |
1. |
(5) |
|
найдем выражение для kT . Для этого подставим (4) в (3), пренебрегая единицей в знаменателе по сравнению с величи-
ной |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
kT , и выполним интегрирование. Тогда получим: |
||||||||||||||
|
|
|
|
n 2(2 mkT) |
3 / 2 |
|
e |
|
kT , |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
h3 |
|
|
|
|
|
отсюда находим, что |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
e kT |
2(2 mkT) |
3 / 2 |
|
|||||||
|
|
|
|
|
. |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
nh3 |
|
|
|
||
Подставляя (7) в (1) получаем: |
|
|
|
|
|
|||||||||
|
|
2 3 / 2 |
|
|
|
|
|
|
|
|
||||
|
dnV |
|
|
exp |
|
|
|
dVxdVydVz . |
||||||
|
|
|
|
|
||||||||||
|
|
2 kT |
|
|
kT |
|
|
|
|
|
||||
(6)
(7)
(8)
Уравнение (8) является распределением Максвелла-Больцмана. Таким образом, как видно из (7), большая масса частиц, соответствует более точному выполнению классического приближения.
При термоэлектронной эмиссии за пределы металла выходят только более быстрые электроны. При этом их концен-
трация в 1010 1012 раз меньше концентрации свободных электронов в металле. В этих условиях неравенство (5) заведомо выполняется. Поэтому получаемое нами распределение термо-
39
электронов по скоростям должно совпадать с распределением Максвелла-Больцмана (8).
40
