
Молекулярная физика III
.pdfЛабораторная работа № 12 Определение удельной теплоемкости жидкости
Цель работы: определение удельной теплоемкости жидкости методом графического учета потерь тепла вследствие теплообмена с окружающей средой.
Приборы и принадлежности: калориметр, источник питания, амперметр, вольтметр, потенциометр ПП-63, реостат, секундомер.
Удельная теплоемкость вещества характеризует количество теплоты, необходимое для нагревания 1 кг данного вещества на 1 К:
c |
dQ |
(1) |
|
mdT |
|||
|
|
где c – удельная теплоемкость; dQ – количество теплоты, не-
обходимое для нагревания тела массой m на dT градусов. Удельная теплоемкость меняется с температурой, однако для узкого интервала температур эту величину для каждого вещества можно считать постоянной.
Точное определение c вызывает затруднения вследствие неизбежного теплообмена калориметра с окружавшей средой. Термостатирование калориметра снижает теплообмен, но не может свести его к нуле. Для учета теплообмена с окружающей средой в уравнение теплового баланса вводятся поправки, учитывающие потери тепла в окружающую среду, а такие тепло, идущее на нагревание калориметра. Наименьшие; эти потери будут для опытов, проведенных в интервале температур от Tн
(ниже температура окружающей среды) до Tв (выше темпера-
тура окружающей среды), однако это не всегда удобно для эксперимента. Расчет поправок проще, если теплообмен идет в
21
одном направлении. Если температура калориметра выше температуры окружающей среды (что легко осуществить, немного подогрев исследуемую жидкость), то в течение всего опыта калориметр только отдает тепло. Расчетная формула для определения удельной теплоемкости может быть получена из уравнения баланса для этого случая:
|
|
Q T mc Э |
(2) |
|
Q – |
количество |
теплоты, |
отданное |
нагревателем; |
T T2 |
T1 , измеренное повышение температуры калори- |
|||
метра с жидкостью ( T1 – начальная температура в коксит |
||||
включения нагревателя, T2 – конечная максимальная темпе- |
||||
ратура опыта); – |
поправка, |
учитывающая теплообмен |
||
(знак (+) соответствует выбранному ранее направление теплообмена); m – масса исследуемой в калориметре жидкости; c – ее удельная теплоемкость; Э – тепловой эквивалент калориметра, т.е. количество теплоты, которое надо сообщить калориметру, чтобы нагреть его на один градус (для калориметра из однородного материала тепловой эквивалент равен массе калориметра, умноженной на удельную теплоемкость, в данной работе калориметр стеклянный).
22

Описание установки.
В настоящей работе для определения удельной теплоемкости жидкости используется калориметр, представляющий собой стеклянный сосуд К (рис.1), внутри которого находится нагреватель Н (омическое сопротивление).
Калориметр установлен в большой сосуд А, являющийся термостатом и играющим роль внешней среды.
T1 T2
mA
24В 

 V
V
н
К
А
Рис. 1.
Температура в калориметре измеряется с помощью термометра 1, а температура окружающей среды - термометром 2. Нагреватель Н включается в цепь постоянного тока через реостат.
23
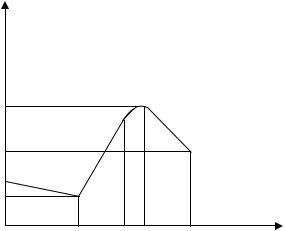
Количество теплоты, отданное нагревателем, рассчитывается по формуле Q IUt , где I и U – ток и напряжение на нагревателе; t – время нагревания. Для правильного определения Q , T и Э следует воспользоваться графиком изменения температуры калориметра от времени. Из-за теплооб-
T
T2 |
|
|
|
|
T3 |
|
|
|
|
T0 |
|
|
|
|
T1 |
|
|
|
|
0 |
t1 |
t2 t′2 |
t3 |
t, c |
|
Рис.2
мена температура калориметра представляет сложную функцию времени.
От t 0 до t , идет так называемый начальный период изменения температуры – охлаждение в результате теплообмена от начальной температура в калориметре T0 (начало опыта,
момент включения секундомера) до T1 – температуры через время t1 (момент включения нагревателя).
В интервале от t1 , до t2 идет главный период - калориметр получает от нагревателя больше тепла, чем отдает вследствие теплообмена, t2 – момент выключения нагревателя, но из-за тепловой инерции максимальная температура T2 , достигается
24
позднее - в момент времени t '2 . В интервале от t '2 до t3 (вы-
ключение секундомера, конец опыта) идет конечный период - охлаждение в результате теплообмена от максимальной температура T2 до конечной T0 (в момент времени t3 ).
Задание. Расчет удельной теплоемкости спирта.
1.Налить в калориметр 70-80 см3 воды.
2.Взвесить калориметр с водой. Определить массу воды.
3.Установить калориметр со спиртом в термостат и, включив нагреватель, подогреть систему на 15-20°С при напряжении
U≈12 В.
4.Выключить нагреватель и, дождавшись начала охлаждения, включить секундомер, записывая через каждые 5 минут показания термометров. Снять 10-12 показаний.
5.Одновременно со снятием последнего показания снова включить нагреватель (U≈12 В) и, отмечая показания потенциометра через каждую минуту, подогреть систему на
10-15°С.
6.Выключить нагреватель, продолжая вести наблюдения (снимать показания через каждую минуту) до начала охлаждения, после чего отсчеты производить через 5 минут, делая 10-12 измерений. Таким образом, все три периода температурного хода снимаются непрерывно, друг за другом, не выключая секундомера.
7.По полученным данным построить график T f (t) . Рас-
считать температурную поправку (см. прил.1). Тепловой эквивалент калориметра 41,638 Дж/(кгК).
8.Рассчитать удельную теплоѐмкость спирта по формуле (9).
Контрольные вопросы
25
1.Существуют ли понятия удельных теплоемкостей при постоянном давлении и объеме для жидкости? Если да, то какую из них определяет в данной работе?
2.Почему холодный спай термопара находится в термостате, а не при нулевой температуре?
3.Каким еще способом можно определить удельную теплоемкость жидкости?
Литература
1.Сивухин Д.В. Общий курс физики, М., Наука, 1979, Т.2.
2.Матвеев А. Н. Молекулярная физика. М. Наука, 1982.
3.Савельев И.В. Курс общей физики. М. Наука, 1978 Т.1.
4.Кикоин А.К, Кикоин И.К. Молекулярная физика. М., Нау-
ка, 1976.
Приложение 1. Расчет температурной поправки.
При точных калориметрических измерениях вводится ряд различных поправок, но в данной работе можно ограничиться только температурной поправкой, обусловленной теплообменом. Все тепло, полученное системой "жидкость - калориметр" от нагревателя делится на две части: Q - тепло, идущее на
нагревание системы от T1 до T2 и q - тепло, отдаваемое системой окружающей среде (термостату). Без этой потери система нагрелась бы на T1 T , где T T2 T1 .
Количество тепла, отдаваемое системой в течение периода (главного) вследствие теплообмена с окружающей средой, можно определить по закону Ньютона
t ' |
|
|
q 2 T T0 |
dt |
(3) |
t1 |
|
|
26
где - коэффициент теплоотдачи калориметра; T0 тура термостата. Величина поправки связана с q ем
|
|
|
q |
|
|
|
|
|
|
|
|
mc Э |
|
||||
Подставляя q , получим |
|
||||
|
|
|
t ' |
|
|
|
|
k 2 T T0 |
dt |
||
|
|
|
t1 |
|
|
где |
|
|
|||
|
. |
|
|||
mc Э |
|
||||
- темперауравнени-
(4)
|
|
|
Пусть за малое время dt температурная поправка со- |
ставляет d , т.е. dq (mc Э)d T T0 dt . |
|||
Будем считать и T0 постоянными величинами. Выражение |
|||
d |
k T T0 |
||
|
|
|
|
|
|||
dt |
T |
|
|
характеризует скорость охлаждения системы вблизи температуры T ,
тогда
d |
k T T и |
d |
k T T |
||||||||
|
|
|
|
|
|
||||||
|
1 |
0 |
|
2 0 |
|||||||
dt |
T |
|
|
|
|
dt |
T |
|
|||
|
|
1 |
|
|
|
|
|
|
2 |
|
|
скорости охлаждения вблизи температур T1 и T2 . |
|||||||||||
Равенство |
d |
|
dT |
справедливо в том случае, когда нагрева- |
|||||||
dt |
dt |
||||||||||
|
|
|
|
|
|
|
|
|
|||
тель выключен и тепло в систему не поступает, т.е. в начальные и конечные периоды, когда сказывается тепловая инерция нагревателя. Так как T T1 и T2 T3 невелики, то изменение
температуры в начальный и конечный периоды можно считать
27
линейными. Заменим |
d |
величиной |
|
T |
, найденной |
|||
|
|
|
|
t |
|
|||
|
||||||||
|
|
dt |
T |
|
|
T |
|
|
из графика температурного хода охлаждения:
T
t T1
T
t T2
-из линейной части начального периода;
-из линейной части конечного периода.
Будем считать, что скорость нагревания калориметра в течение главного периода значительно больше скорости охлаждения, играются роль небольшой поправки к основному процессу нагревания.
Тогда временную зависимость температура в течение главного периода можно считать линейной
T |
T2 T1 |
t |
t1T2 t '2 |
T1 |
(7) |
||
|
|
|
|||||
|
t ' |
t |
|
t ' |
t |
|
|
2 |
1 |
2 |
1 |
|
|
||
Подставив выражение (7) в соотношение (5), проинтегрируем последнее выражение и, используя значения
Tt T1
|
T |
, получим окончательно |
|
|||||||
и |
|
|
||||||||
|
t T |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
T |
|
T |
|
t '2 |
t1 (8) |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
||||||||
|
|
2 |
|
t T |
|
t T |
|
|
|
|
|
|
|
|
|
1 |
|
2 |
|
|
|
Количество теплоты, отданное нагревателем, рассчитывается по формуле Q IUt , где I - сила тока в амперах; U - на-
пряжение в вольтах; t - время действия нагревателя в секундах.
Тогда |
|
|
|
|
|
c |
I U t |
|
Э |
. |
(9) |
m ( T ) |
|
||||
|
|
m |
|
||
28
Лабораторная работа № 13 Распределение Максвелла.
Цель работы: изучить статистические распределения Максвелла и Больцмана на примере распределения термоэлектронов по скоростям и распределение числа частиц в зависимости от потенциальной энергии.
Приборы и принадлежности: электронная лампа,
вольтметр, микроамперметр, магазины сопротивлений, реостат, понижающий трансформатор, сообщающиеся сосуды, кипятильник, термометр, манометр.
Распределение Максвелла.
В состоянии термодинамического равновесия молекулы идеального газа равномерно распределяются по всему пространству, а скорости равномерно распределяются по всем направлениям. При этом, если движение молекулы подчиняется законам классической механики, то распределение молекул по скоростям описывается распределением Максвелла:
|
|
m 3 / 2 |
|
dp(Vx ,Vy |
,Vz ) |
|
|
|
|||
|
|
2 kT |
|
|
|
mV 2 |
|
|
|
|
|
|
|
, |
(1) |
|
|||||
exp |
2kT |
dVxdVydVz |
|||
|
|
|
|
|
где dp(Vx ,Vy ,Vz ) – вероятность того, что молекула имеет ско-
рость в интервале Vx (Vx dVx ); Vy (Vy dVy ); Vz (Vz dVz ); m, V - масса и скорость молекулы, соответственно; k – постоянная Больцмана; T – абсолютная температура; dVx , dVy , dVz -
дифференциалы проекций вектора скорости по осям декартовой системы координат.
29

В настоящей работе распределение Максвелла изучается на примере электронного газа. В электронной лампе вследствие термоэмиссии образуется облако электронов, которое по своим свойствам близко к идеальному газу (см. приложение). В этих условиях движение электронов подчиняется законам классической механики и описывается распределением (1). Если анод и катод лампы рассматривать как плоскости, то плотность тока на аноде, в отсутствие ускоряющего потенциала
|
|
m |
3 / 2 |
|
|
|
|
|
|
|
|
mV |
2 |
|
|
|
|||||
|
|
dVx dVy dVz |
|
|
|
|
|
|
|
|
|||||||||||
J0 |
|
|
|
|
Vx |
|
|
|
|
|
|
(2) |
|||||||||
|
|
exp |
|
|
|
|
|
ne, |
|||||||||||||
|
|
2 kT |
|
0 |
|
|
|
|
|
|
|
2kT |
|
|
|||||||
где |
n – плотность электронов, |
e – заряд электрона. Выполнив |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
интегрирование в (2), получаем выражение J |
|
|
ne |
|
kT |
. |
|
||||||||||||||
0 |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 m |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Если на анод подавать отрицательный потенциал, то достичь анода сумеют только те электроны кинетическая энергия кото-
|
mV 2 |
|
||
рых |
|
превышает величину |
eU , где U - задерживающий |
|
2 |
||||
|
|
|
||
потенциал. Выражение анодного тока в этом случае имеет вид:
|
1/ 2 |
|
|
|
|
2 |
|
|
|
|
|
|
|
eU |
|
|||
m |
dVx |
|
|
|
mVx |
|
|
|
|
|
2 |
|
|
|||||
J |
|
|
Vx |
exp |
|
|
|
|
J0 exp |
|
|
|
|
, |
(3) |
|||
|
|
|
|
|
||||||||||||||
|
2 kT |
eU |
|
|
|
2kT |
|
|
|
|
|
|
|
kT |
|
|||
логарифмируя (3), получаем |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
ln J ln J |
|
|
eU |
. |
|
|
|
|
|
(4) |
|||
|
|
|
|
|
0 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
kT |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
таким образом, если распределение электронов по скоростям подчиняется распределению Максвелла, то зависимость логарифма тока от задерживающего напряжения линейна.
Определив угловой коэффициент этой прямой
e |
|
ln J |
, |
(5) |
|
kT |
U |
||||
|
|
|
можно рассчитать температуру электронного газа. Опыт показывает, что при термоэлектронной эмиссии электронный газ
30
