
Методичка по биохимии. 1 курс - 1 модуль
.pdf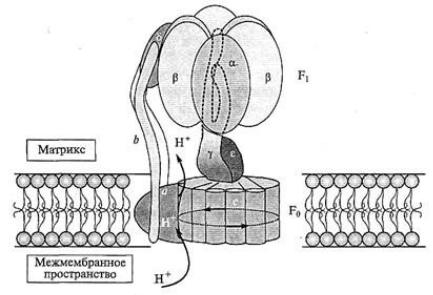
каталитическую «головку»; между α- и β-субъединицами располагаются 3 активных центра, в которые поступают молекулы АДФ и неорганического фосфата и происходит синтез АТФ. γ-, ε-, δ- субъединицы связывают комплекс
F1 с Fо.
Рис. 6 Строение Н+-АТФ-синтазы
Повышение концентрации протонов в межмембранном пространстве активирует АТФ-синтазу. Электрохимический потенциал ΔμН+ заставляет протоны двигаться по каналу АТФ-синтазы в матрикс. Под действием потока протонов по каналу каталитическая часть АТФ синтазы (F1) вращается вокруг устья канала. Синтез АТФ проходит три стадии:
поступление АДФ и неорганического фосфата (Pi) в каталитический центр,
поворот на 120о и сжимающая деформация каталитического центра, сближающая отталкивающиеся группы остатков фосфорной кислоты; на этой стадии происходит образование АТФ и молекулы воды,
поворот на 120о и освобождение из активного центра молекулы АТФ. В освободившийся каталитический центр поступают новые молекулы АДФ и Pi (неорганического фосфата)
Таким образом, при каждом переносе протонов через канал Fo энергия электрохимического потенциала расходуется на поворот стержня, в результате
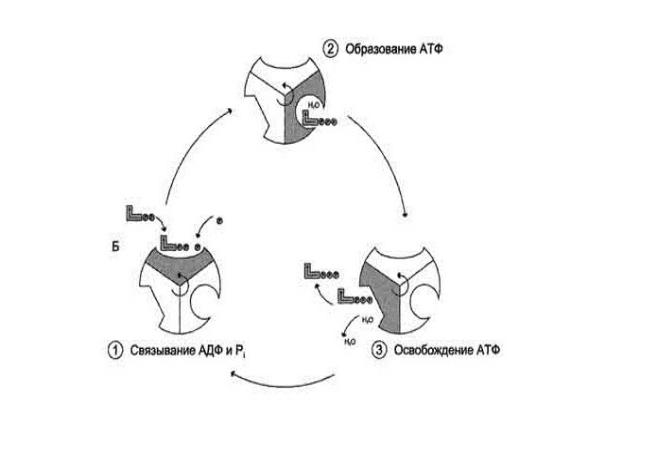
которого циклически изменяется конформация α - и β-субъединиц и все 3 активных центра катализируют очередную фазу цикла (рис 7):
Рис. 7 Механизм действия Н+-АТФ-синтазы
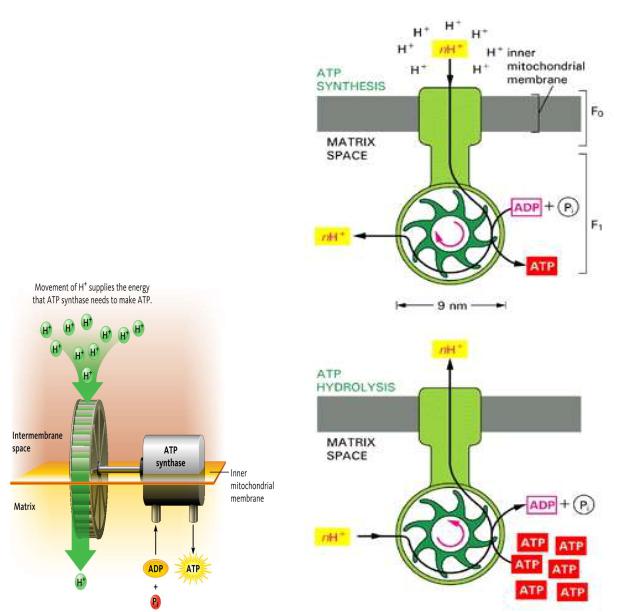
а)
Рис.8. Принцип работы Н+-АТФ-синтазы
Механизм сопряжения реакций окисления и синтеза АТФ
Процесс переноса электронов по ЦПЭ и синтез АТФ энергетически сопряжены.
Первый процесс - перенос электронов от восстановленных коферментов NADH и FADH2 через ЦПЭ на кислород - экзергонический.
NADH + H+ + 1/2 O2 → NAD+ + H2O + 52 ккал/моль(=220 кДж/моль).
Второй процесс - фосфорилирование AДФ, или синтез АТФ, - эндергонический:
АДФ + Н3РО4+7,3 ккал/моль (30,5 кДж/моль) = АТФ + Н2О.
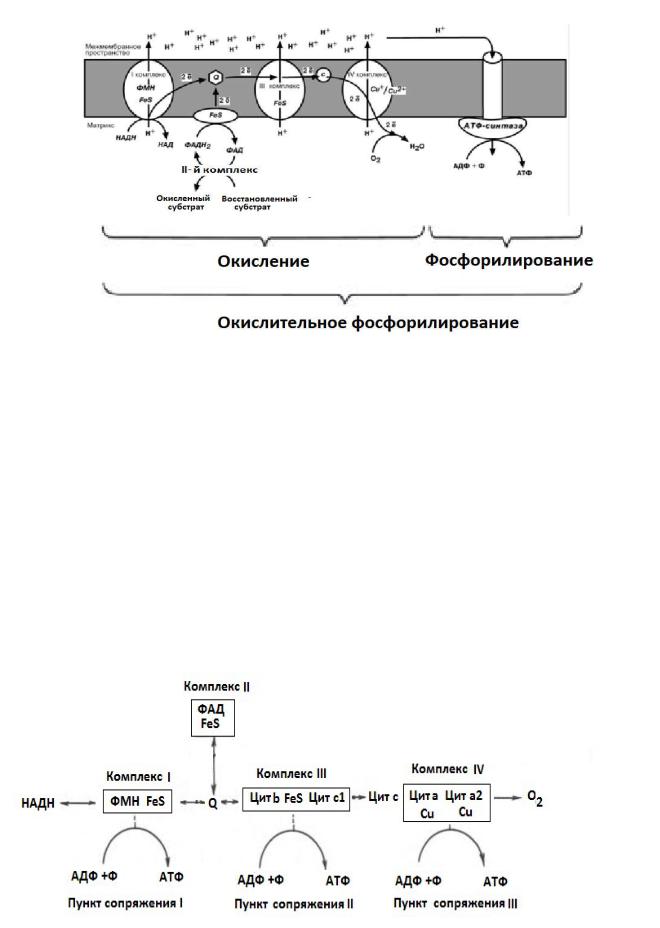
Рис. 9. Сопряжение реакций окисления и синтеза АТФ.
Перенос Н+ через мембрану происходит в строго определенных участках мембраны. Эти участки называются участки сопряжения (или, не совсем точно, пункты фосфорилирования). Они представлены I, III, IV комплексами дыхательных ферментов. В результате работы этих комплексов создается трансмембранный электрохимический потенциал не менее 0,2 в, необходимый для синтеза АТФ. Таким образом, электрохимический потенциал, генерируемый в каждом из 3 пунктов сопряжения дыхания и фосфорилирования, является движущей силой синтеза АТФ.
Рис. 10. Локализация пунктов сопряжения окисления и фосфорилирования.
Коэффициентом окислительного фосфорилирования (Р/О) называют отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания. Окисление молекулы НАДН2 в ЦПЭ сопровождается образова-нием 3 молекул АТФ, следовательно, для НАДН2 Р/О = 3. Электроны от ФАДзависимых дегидрогеназ поступают в ЦПЭ на KoQ, минуя первый пункт сопряжения. Поэтому образуются только 2 молекулы АТФ (Р/О = 2).
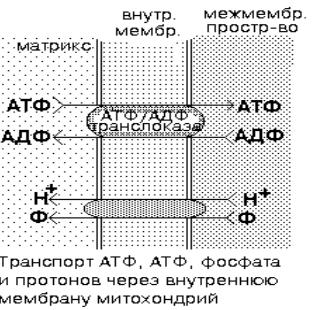
После синтеза АТФ переносится в цитоплазму путем облегчённой диффузии по градиенту концентраций, поскольку основные процессы, в которых АТФ потребляется, протекают в цитоплазме.
Как происходит транспорт АТФ из митохондрий в цитоплазму?
Для этого используется специфический для АТФ транспортный белок - АТФ/АДФ-транслоказа. Это интегральный белок, локализован во внутренней мембране митохондрий.
Во внутренней мембране митохондрий есть белокпереносчик - АТФ/АТФтранслоказа, который имеет 2 центра связывания: со стороны матрикса для АТФ, снаружи - для АДФ. При изменении конформации АТФ/АДФтранслоказы АДФ переносится в матрикс, а АТФ - в межмембранное пространство, а
затем - в цитоплазму, где используется.
Для образования АТФ в матрикс всё время должен поступать неорганический фосфат (Ф). Для этого во внутренней мембране митохондрий есть транспортная система, которая обеспечивает перенос фосфата в матрикс сопряженно с переносом Н+. Это белок-переносчик, который имеет 2 центра
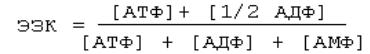
связывания: для Ф и Н+. Ф и Н+ вместе переносятся из межмембранного пространства в матрикс.
8. Регуляция биоэнергетических процессов в клетке. Дыхательный контроль.
Если клетка организма находится в условиях покоя, то АТФ мало используется и накапливается. Поэтому снижается концентрация АДФ и Ф. В этих условиях АТФ-синтетаза уже не получает из цитоплазмы достаточно фосфата и АДФ для синтеза АТФ. Её активность понижается, и скорость движения протонов из межмембранного пространства в матрикс по протонному каналу этого фермента тоже падает. Поэтому сохраняется высокий градиент концентраций протонов на внутренней мембране митохондрий. В этих условиях энергии переноса водорода по цепи митохондриального окисления уже не хватает для выталкивания Н+ из матрикса в межмембранное пространство. Перенос водорода по цепи тормозится и прекращается окисление субстратов.
Метаболизм в клетке регулируется отношением АТФ/АДФ. Это отношение характеризует ЭНЕРГЕТИЧЕСКИЙ ЗАРЯД КЛЕТКИ (ЭЗК).
В норме ЭЗК = 0.85-0.90. Может изменяться от 0 до 1. Высокий ЭЗК тормозит синтез АТФ, и активирует использование АТФ (АТФ-> АДФ + Ф)
Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается.
9. Разобщение окисления и фосфорилирования.
Механизмы разобщения окисления и фосфорилирования
Разобщение дыхания и фосфорилирования называют явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ.
Так как электрохимический градиент состоит из двух компонентов (электрического и химического), то существуют два принципиальных способа его уменьшить – нивелировать разность зарядов или разность концентрации ионов водорода.
Разобщители – это вещества, которые могут переносить протоны (протонофоры) или другие ионы (ионофоры) через мембрану минуя каналы АТФ-синтазы. Они снижают величину электрохимического градиента, что приводит к увеличению скорости движения электронов по ферментам дыхательной цепи. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О2, окисления НАДН2, ФАДН2, снижается коэффициент Р/О, энергия выделяется в виде теплоты.
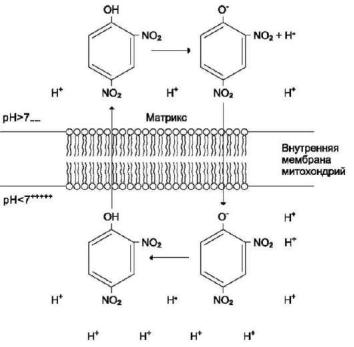
Классическим протонофором является 2,4-динитрофенол. Динитрофенол протонируется в межмембранном пространстве, где концентрация протонов выше, и диффундирует через внутреннюю мембрану митохондрий в матрикс. В матриксе, где концентрация протонов ниже, 2,4- динитрофенол теряет протон, переходит в ионизированную форму и может возвращаться в межмембранное пространство.
Рис. 11. Разобщающее действие 2,4-динитрофенола
Подобным образом действуют ионофоры, увеличивающие проницаемость мембраны для ионов Na+ и К+, например, антибиотики - валиномицин и грамицидин
Физиологическим протонофором является белок "термогенин", в
изобилии имеющийся в клетках бурой жировой ткани (до 15% от всех белков митохондрий). Существенным отличием бурой жировой ткани от белой является большое количество митохондрий, которые придают клеткам бурокрасный цвет. При охлаждении организма эти клетки получают сигналы по симпатическим нервам, и в них активируется расщепление жира – липолиз. Окисление жиров приводит к получению НАДН и ФАДН2, активизации работы дыхательной цепи и возрастанию электрохимического градиента. Однако АТФсинтазы в мембранах митохондрий этих клеток мало, зато много термогенина. Благодаря ему, большая часть энергии ионов водорода рассеивается в виде тепла, обеспечивая поддержание температуры тела при охлаждении.
Примерами разобщителей могут быть также некоторые лекарства, например дикумарол - антикоагулянт или метаболиты, которые образуются в организме, билирубин - продукт катаболизма тема, тироксин - гормон щитовидной железы. Все эти вещества проявляют разобщающее действие только при их высокой концентрации.
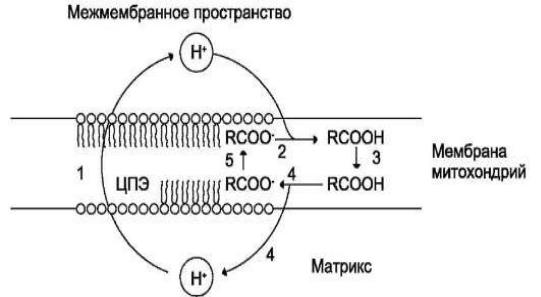
Рис.12. Механизм разобщающего действия жирных кислот.
1- выкачивание протонов дыхательной цепью; 2 - протонирование аниона жирной кислоты; 3 - диффузия протонированной жирной кислоты к внутренней
поверхности мембраны; 4 - диссоциация RCOOH с образованием RCOO- и иона Н+; 5 - перенос RCOOпосредством АТФ/АДФ-антипортера или разобщающего белка к наружной поверхности митохондриальной мембраны. Образующиеся свободные жирные кислоты служат не только «топливом», но и важнейшим регулятором разобщения дыхания и фосфорилирования.
Ингибирование ферментов дыхательной цепи.
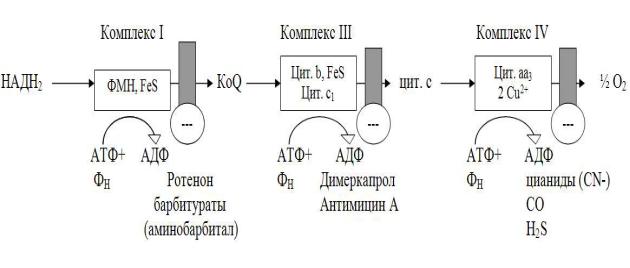
Ингибиторы NADH-дегидрогеназы: ротенон - высокотоксичное
вещество, содержащееся в некоторых водорослях и являющееся ядом для рыб; амитал - лекарственный препарат из группы барбитуратов.
Ингибитор QH2-дегидрогеназы - антимицин А, токсичный антибиотик, продуцируемый одним из штаммов Streptomyces.
Ингибиторы цитохромоксидазы - цианид, СО, H2S. Цианид наиболее токсичен для человека; он присоединяется к Fe3+ цитохромоксидазы и блокирует перенос электронов к кислороду (рис. ).
Рис. 13. Участки ингибирования дыхательной цепи специфическими лекарственными веществами.
