
- •Симптоматические артериальные гипертензии. Клинические проявления. Критерии диагностики. Принципы лечения.
- •Клинические проявления: При симптоматической гипертонии жалобы обусловлены основным заболеванием:
- •Патогенез:
- •Лечение
- •Трепетание и фибрилляция предсердий. Причины, диагностические (экг) критерии, формы, влияния на гемодинамику. Классификация фибрилляций предсердий.
- •Критерии установления диагноза/состояния:
- •Влияние на гемодинамику
- •Классификация фп и тп
- •Диагностические критерии (клинические и экг) желудочковой пароксизмальной тахикардии. Неотложная помощь.
- •1 Этап:
- •2 Этап:
- •3 Этап:
- •Дифференциальный диагноз болевого синдрома при стабильной стенокардии с другими причинами болей в грудной клетке.
- •Принципы лечения экстрасистолии, основные группы антиаритмических препаратов, механизмы их действия.
- •Основные группы препаратов (из файла):
- •Антиангинальные средства: классификация механизмы действия, побочные эффекты.
- •I. Средства, понижающие потребность миокарда в кислороде и повышающие доставку кислорода.
- •II. Средства, понижающие потребность миокарда в кислороде.
- •III. Средства, повышающие доставку кислорода к миокарду.
- •Антитромботические средства: классификация механизмы действия, показания, противопоказания, побочные эффекты.
- •Антикоагулянты прямого действия
- •Антикоагулянты непрямого действия
- •Фибринолитические средства
- •Средства, препятствующие агрегации трц- тромбоциты аск
- •Атеросклероз и гиперлипидемии. Классификация. Стандарты лечения и принципы первичной и вторичной профилактики.
- •Классификация гиперлипидемии:
- •Стабильное течение ибс. Основные формы согласно мкб 10. Принципы постановки диагноза. Препараты для улучшения прогноза.
- •Инфаркт миокарда с подъемом st. Критерии постановки диагноза. Неотложная помощь. Вопросы маршрутизации пациентов.
- •Жалобы, анамнез.
- •Лабораторная диагностика.
- •Неотложная помощь
- •Острый коронарный синдром без подъема сегмента st. Основные клинические формы. Критерии постановки диагноза. Вопросы маршрутизации. Принципы лечения.
- •Лечение
- •Инфаркт миокарда без подъема сегмента st. Критерии постановки диагноза. Неотложная и ранняя инвазивная стратегия. Вопросы маршрутизации пациентов. Оказание помощи на догоспитальном этапе.
- •Кардиомиопатии. Классификация. Вопросы дифференциальной диагностик. Принципы лечения.
- •2. Гипертрофическая кардиомиопатия (гкмп)
- •3. Рестриктивная кардиомиопатия (ркмп)
- •14. Гипертоническая болезнь. Уровни ад. Стратификация риска. Целевые уровни ад в зависимости от клинической ситуации.
- •Целевые ад
- •15. Острая сердечная недостаточность. Этиология. Дифференциальная диагностика. Неотложная помощь.
- •Лечение догоспитальное
- •Стратификация риска:
- •Тактика ведения пациентов высокого и очень высокого риска.
- •17. Резистентная артериальная гипертония. Вопросы диагностики. Тактика ведения. Вопросы корректировки сопутствующих факторов риска.
- •Тактика ведения:
- •Жалобы, анамнез.
- •Лабораторная диагностика.
- •Показания для тромболизиса.
- •Противопоказания для тромболизиса.
- •19. Острая сердечная недостаточность. Этиология. Критерии диагностики на догоспитальном этапе. Вопросы неотложной помощи.
- •20. Острая сердечная недостаточность при инфаркте миокарда. Классификация. Критерии диагностики. Неотложная помощь. Показания к инвазивным вмешательствам.
- •Неотложная помощь (при отеке легких)
- •Кардиогенный шок
- •Лечение истинного кардиогенного шока гипокинетический вариант:
- •21. Классификация гипертонической болезни. Представление о факторах риска. Поражения органов мишеней. Сердечно-сосудистые заболевания, связанные с аг. Критерии стратификации риска.
- •Выделяются 3 стадии гипертонической болезни.
- •Факторы сс риска у пациентов с аг:
- •22. Диагностические критерии с-а блокады. Причины, прогноз, тактика ведения.
- •23. Гипертонические кризы. Причины. Критерии диагностики. Осложнения. Тактика ведения. Профилактика.
- •Причины
- •Критерии диагностики:
- •Типичные проявления гипертонических кризов:
- •Тактика ведения
- •24. Основные группы антигипертензивных препаратов, механизмы действия, показания и противопоказания к назначению, разовые и суточные дозы препаратов.
- •Показания
- •Рассовые предпочтения:
- •Фракция выброса
- •Критерии постановки диагноза
- •Клинические симптомы и признаки
- •Лабораторные признаки:
- •Инструментальная диагностика:
- •В связи с этим выделяют стадии и функциональные классы:
- •Стадии хсн
- •Функционаяльные классы (фк):
- •26. Кардиомиопатия. Классификация. Критерии постановки диагноза. Принципы лечения.
- •27. Реноваскулярная артериальная гипертензия. Клинико-инструментальная диагностика. Врачебная тактика.
- •28. Симптоматические артериальные гипертензии эндокринного генеза. Диагностические критерии феохромоцитомы. Врачебная тактика.
- •1) Феохромоцитома и феохромобластома; альдостерома (первичный альдостеронизм, или синдром Конна); кортикостерома; болезнь и синдром Иценко—Кушинга; акромегалия; диффузный токсический зоб.
- •29. Хроническая сердечная недостаточность с низкой фракцией выброса лж. Критерии постановки диагноза. Объем инструментальной и лабораторной диагностики. Смотри вопрос 25.
- •30. Нарушения проводимости: av блокады. Клинические проявления. Врачебная тактика.
- •31. Наджелудочковые нарушения ритма. Врачебная тактика. Стандарты диагностики и лечения.
- •32. Вопросы стратификации сердечно сосудистого риска. Популяционный и индивидуальный подход. Шкалы оценки.
- •33. Инфаркт миокарда с подъемом сегмента st. Принципы диагностики. Оказание помощи на догоспитальном этапе и госпитальном этапе.
- •Лабораторная диагностика.
- •Инструментальные методы:
- •Неотложная помощь
- •Госпитальный этап:
- •34. Желудочковые нарушения ритма. Причины, диагностические (экг) критерии. Прогноз. Принципы лечения.
- •Основными механизмами жта являются:
- •Классификация желудочковых нарушений ритма сердца основана на нескольких ключевых положениях.
- •Критерии установки диагноза:
- •Лечение
- •35. Фибрилляция предсердий. Диагностика. Восстановление синусового ритма.
- •Критерии установления диагноза/состояния:
- •Классификация фп
- •Восстановление синусового ритма.
- •36. Хроническая сердечная недостаточность с сохранной и умерено-сохранной фракцией выброса. Диагностические критерии. Вопросы лечения.
- •Фракция выброса
- •Критерии постановки диагноза
- •Клинические симптомы и признаки
- •Лабораторные признаки:
- •Инструментальная диагностика:
- •В связи с этим выделяют стадии и функциональные классы:
- •Стадии хсн
- •Функционаяльные классы (фк):
- •Лечение
- •С промежуточной фракций выброса
- •С сохранной фракций выброса
- •41.Диагностические критерии острой левожелудочковой (отек легких) и острой правожелудочковой недостаточности, прогноз неотложная помощь.
- •Неотложная помощь (при отеке легких)
- •42.Восполительные заболевания миокарда и перикарда. Дифференциальная диагностика. Стандарты ведения пациентов.
- •I. Инфекционные или инфекционно-аллергические перикардиты
- •II. Асептические перикардиты: при ревматических заболеваниях, при инфаркте миокарда
- •43.Гипертоническая болезнь. Классификация. Дифференциальная диагностика. Основные группы антигипертензивных препаратов.
- •Выделяются 3 стадии гипертонической болезни.
- •Факторы сс риска у пациентов с аг:
- •Показания
- •Рассовые предпочтения:
- •44. Фибрилляция предсердий. Формы. Выбор тактики лечения. Принципы удержания синусового ритма.
- •Критерии установления диагноза/состояния:
- •Классификация фп и тп
- •45. Гипертоническая болезнь. Факторы риска, поражение органов мишеней, наличие сердечно сосудистых заболеваний, обусловленных аг. Стратификация риска.
- •46. Инфекционный эндокардит. Критерии постановки диагноза. Вопросы первичной и вторичной профилактики. Принципы лечения.
- •Критерии Дюка
- •Клиническая картина
- •51. Легочная гипертензия. Критерии постановки диагноза. Классификация. Показания к лаг- терапии.
- •Критерии постановки диагноза.
- •Лечение.
- •Пульмонология
- •1. Обострение бронхиальной астмы. Вопросы дифференциальной диагностики. Критерии жизнеугрожающего обострения астмы. Дифференциальная диагностика хобл и ба
- •2. Дифференциальный диагноз легочного инфильтративного синдрома.
- •2. Инфильтративный туберкулёз
- •3. Легочной эозинофильный инфильтрат
- •4. Интерстициальные заболевания легких. Основные нозологии. Вопросы диагностики. Принципы лечения.
- •5. Хобл. Роль спирометрии в постановке диагноза. Шкалы клинической оценки течения хобл и риска обострений. Принципы лечения в зависимости от градации a,b,c,d.
- •6. Бронхиальная астма. Фенотипы заболевания. Стандарты диагностики и лечения
- •7. Фенотипы бронхиальной астмы. Неконтролируемая и тяжелая бронхиальная астма. Вопросы дифференциальной диагностики и тактики ведения.
- •Внебольничные пневмонии тяжелого течения. Диагностические критерии, течение, критерии высокого риска летального исхода. Неотложная терапия.
- •9. Понятие контроля при бронхиальной астме. Терапевтические опции для достижения контроля над течением заболевания. Организация step up и step down терапии.
- •10. Дыхательная недостаточность. Классификация. Клинические проявления. Критерии диагностики. Неотложная помощь. Профилактика.
- •11. Бронхиальная астма. Определение. Фенотипы. Критерии постановки диагноза. Роль спирометрии. Понятие о вариабельности и обратимости бронхиальной обструкции.
- •12. Тэла. Причины. Критерии постановки диагноза. Неотложная помощь. Принципы лечения.
- •13. Обострение хобл. Клинические проявления. Критерии тяжелого обострения. Вопросы неотложной помощи. Тактика ведения. Профилактика.
- •14. Заболевания плевры. Вопросы дифференциальной диагностики. Тактика ведения.
- •15. Дифференциальная диагностика и принципы лечения интерстициальных заболеваний легких.
- •1. С установленной этиологией:
- •16.Вопросы диагностики легочной артериальной гипертонии, связанной с хроническими заболеваниями легких. Принципы леченияя.
- •17. Бронхиальная астма. Фенотипы заболевания. Диагностические и лечебные алгоритмы.
- •18. Хобл. Этиология. Критерии постановки диагноза. Алгоритмы лечения.
- •19. Антибактериальная терапия внебольничной пневмонии. Выбор на амбулаторном этапе, при лечении в стационаре и отделении интенсивной терапии.
- •20. Пневмония тяжелого течения. Критерии постановки диагноза. Врачебная тактика.
- •20. Дыхательная недостаточность. Диагностические критерии. Врачебная тактика.
- •22. Саркоидоз. Клинические проявления. Диагностика. Врачебная тактика.
- •23. Внебольничная пневмония. Этиология. Клинические проявления. Принципы диагностики. Лечебная тактика.
- •24. Диагностика, дифференциальная диагностика и лечебная тактика при ба
- •25. Вирусно-бактериальные пневмонии. Вопросы диагностики и врачебной тактики. Профилактика
- •26. Дыхательная недостаточность. Клиническая, лабораторная и инструментальная диагностика. Принципы лечения.
- •27. Бронхолитики – β2-агонисты, м3-холинолитики, комбинированные препараты. Формы доставки, продолжительность действия, возможности использования в клинике внутренних болезней.
- •28. Хронический бронхит. Диагностические критерии. Вопросы дифференциальной диагностики. Принципы лечения.
- •29. Интерстициальные заболевания легких. Принципы диагностики. Основные нозологические формы. Критерии обычной интерстициальной пневмонии.
- •30. Диагностика, дифференциальная диагностика и лечебная тактика при хронической обструктивной болезни легких.
- •31. Экссудативный плеврит. Этиология. Диагностика. Принципы лечения.
- •32. Дыхательная недостаточность. Клиническая, лабораторная и инструментальная диагностика. Принципы лечения.
- •33. Вопросы классификации пневмонии. Стандарты лечения в зависимости от тяжести течения и этиологии. Вопросы профилактики
- •34. Диагностика, дифференциальная диагностика и лечебная тактика при хронической обструктивной болезни легких.
- •35. Хронический бронхит. Вопросы дифференциальной диагностики. Тактика ведения.
- •36. Идиопатический легочный фиброз. Критерии постановки диагноза. Дифференциальная диагностика кт-патерна обычной интерстициальной пневмонии. Возможности улучшения течения болезни
- •Гастроэнторология
- •1. Редкие болезни кишечника. Глютеновая энтеропатия. Болезнь Уиппла. Методы диагностики. Тактика ведения и лечения
- •1. Медикаментозная терапия:
- •9. Хронический панкреатит. Классификации. Основные клинические синдромы. Методы диагностики. Осложнения хронического панкреатита.
- •10. Псевдомембранозный колит
- •14. Дифференциальная диагностика заболеваний, сопровождающихся гепатомегалией. Алгоритм обследования.
- •15. Хронический панкреатит. Классификации. Основные клинические синдромы. Методы диагностики. Принципы лечения.
- •21. Основные виды и причины желтух. Принципы лабораторной и инструментальной диагностики.
- •23. Дифференциальный диагноз при диарее. Стандарт обследования. Принципы лечения.
- •25. Гэрб. Внепищеводные проявления. Современные стандарты диагностики и лечения.
- •30. Гепатомегалия. Цирроз печени. Ранняя диагностика синдрома портальной гипертензии. Лечение и профилактика кровотечений из расширенных вен пищевода
- •32.Желчнокаменная болезнь. Определение. Классификация. Стандарты диагностики и лечения. Показания к холецистэктомии.
- •33. Биохимические синдромы при заболеваниях печени. Диагностика и принципы лечения хронического гепатита с учетом этиологии (вирусной, аутоиммунной, лекарственно-индуцированной).
- •34. Дифференциальная диагностика и врачебная тактика при заболеваниях поджелудочной железы. Стандарты лечения.
- •35. Клинические и лабораторные синдромы при заболеваниях печени
- •40. Функциональные билиарные расстройства. Стандарты диагностики и лечения.
- •41. Язвенная болезнь желудка и дпк. Базисная терапия. Показания к эрадикации Helicobacter pylori. Современные схемы.
- •Ревматология
- •5. Диагностика и лечение лекарственной болезни. Анафилактический шок.
- •8. Современные принципы базисной терапии ревматоидного артрита
- •18. Синдром старческой хрупкости. Критерии диагностики. Врачебная тактика.
- •20. Скв. Показатели активности воспалительного процесса. Принципы интенсивной терапии.
- •21. Ревматоидный артрит. Критерии постановки диагноза и оценки воспалительного процесса. Принципы базисной терапии. Показания к назначению генно-инженерной биологической терапии
- •23. Антифосфолипидный синдром. Этиология. Клинические проявления. Методы диагностики. Принципы лечения.
- •Нефрология
- •3. Вопросы кардио-ренального континуума в практике врача-терапевта. Дифференциальная диагностики при снижении функции почек. Тактика. Принципы лечения.
- •7. Хроническая болезнь почек. Тактика врача терапевта.
- •Гематология
- •Дифференциальный диагноз гипохромных анемий:
- •Дифференциальный диагноз гиперхромных анемий:
На основании имеющихся данных молодым пациентам с изолированной систолической АГ 1-й степени следует рекомендовать мероприятия по изменению образа жизни (особенно прекращение курения); необходимость назначения АГТ на настоящий момент не доказана; показано длительное наблюдение, поскольку у многих из них в дальнейшем возможно развитие стойкой АГ
50. Клинические проявления острого коронарного синдрома. Вопросы дифференциальной диагностики с другими причинами болей в грудной клетке (с расслаивающейся аневризмой аорты, спонтанным пневмотораксом, тромбоэмболией легочной артерии и др.).
Острый коронарный синдром (ОКС) – термин, обозначающий любую группу клинических признаков или симптомов, позволяющих подозревать острый инфаркт миокарда (ИМ) или нестабильную стенокардию (НС). Термин “ОКС” используется, когда диагностической информации еще недостаточно для окончательного суждения о наличии или отсутствии очагов некроза в миокарде и, следовательно, представляет собой предварительный диагноз в первые часы и сутки заболевания, в то время как термины “ИМ” и “нестабильная стенокардия” используются при формулировании заключительного диагноза. Соответственно, термин “ОКС” может использоваться на догоспитальном или раннем госпитальном этапах и в дальнейшем трансформируется в диагноз “острый ИМ”, “НС”, либо, по результатам дифференциальной диагностики – в любой другой диагноз, в том числе не кардиологический.
Острый коронарный синдром со стойкими подъемами сегмента ST на ЭКГ (ОКСпST) — недавно возникшие клинические признаки или симптомы ишемии миокарда в сочетании с наличием стойких (длительностью более 20 минут) подъемов сегмента ST как минимум в двух смежных отведениях ЭКГ.
Острый коронарный синдром без стойкого подъема сегмента ST на ЭКГ (ОКСбпST) – остро возникшие клинические признаки или симптомы ишемии миокарда, когда на ЭКГ отсутствует стойкий (длительностью более 20 минут) подъем сегмента ST как минимум в двух смежных отведениях и нет остро возникшей блокады левой ножки пучка Гиса. Может закончиться без развития очагов некроза миокарда (НС) или с развитием очагов некроза (ИМ, с формированием или без формирования патологических зубцов Q на ЭКГ).
Формы ОКС без ST:
Основным в ведении пациентов с ОКСбпST на всех этапах оказания помощи является наряду с диагностикой постоянная стратификация риска развития кардиальных осложнений. В итоге в исходе ОКСбпST дифференцируются две клинические формы:
Нестабильная стенокардия - острая ишемия миокарда, тяжесть и продолжительность которой недостаточны для развития некроза миокарда (нет диагностически значимых повышений уровней тропонина).
Инфаркт миокарда без подъема сегмента ST – острая ишемия миокарда, тяжесть и продолжительность которой приводит к некрозу миокарда.
Клиническая картина
жалобы на боль в области сердца или за грудиной, одышку смешанного характера при физической нагрузке или в покое, тошноту, головокружение, потливость, сердцебиение.
боль за грудиной или в левой половине грудной клетки различной интенсивности, иррадиирующая в левую руку, шею, челюсть, межлопаточное пространство, возникшая при физической нагрузке или психоэмоциональном перенапряжении, часто сопровождающаяся страхом смерти. Боль не может купироваться после прекращения физической нагрузки или после приема нитратов.
возбуждены или могут быть заторможены, кожный покров бледный, часто повышенной влажности, акроцианоз.
При тромбоэмболии легочной артерии - внезапно возникает выраженная одышка, которая не усиливается в горизонтальном положении. Боль локализуется в боковых отделах грудной клетки, имеет связь с дыханием и может сопровождаться кровохарканьем.
Острое расслоение аорты - упорный болевой синдром продолжается несколько часов и не купируется нитратами и анальгетиками. Боль локализуется по центру грудной клетки, в спине; может быть иррадиация боли вниз по позвоночнику.
При пневмотораксе возникает острая боль в боковых отделах грудной клетки.
51. Легочная гипертензия. Критерии постановки диагноза. Классификация. Показания к лаг- терапии.
Легочная гипертензия – гемодинамическое и патофизиологическое состояние, которое характеризуется повышением среднего давления в легочной артерии (ДЛА) ≥ 25 мм рт. ст. в покое, измеренного при чрезвенозной катетеризации сердца.
Различают первичную (идиопатическую) и вторичную легочную гипертензию. Последняя осложняет течение различных форм патологии.
ЛГ встречается при самых разнообразных заболеваниях и состояниях и крайне редко является самостоятельным заболеванием – например, таким, как идиопатическая. Классификация легочных гипертензий, принятая Европейским обществом кардиологов и Европейским респираторным обществом в 2015 г., выделяет 5 основных групп, объединенных общностью клинических, гемодинамических, патоморфологических характеристик и подходов к лечению. В 2018 году на 6-м Всемирном конгрессе по ЛГ в Ницце внесены изменения в клиническую классификацию ЛГ 2015 г.
Таблица 1. Клиническая классификация легочных гипертензий [6, 11]
I. Легочная артериальная гипертензия: 1.1. Идиопатическая легочная артериальная гипертензия 1.2. Наследственная: 1.2.1. Мутации гена BMPR2 1.2.2. Другие мутации кандидатных генов 1.3. Индуцированная лекарственными препаратами и токсинами 1.4. Ассоциированная с: 1.4.1. Системными заболеваниями соединительной ткани 1.4.2. ВИЧ-инфекцией 1.4.3. Портальной гипертензией 1.4.4. Врожденными пороками сердца 1.4.5. Шистосомозом 1.5. ЛАГ с длительным ответом на БКК 1.6. ЛАГ с явными чертами веноокклюзионной болезни / гемангиоматоза легочных капилляров 1.7. Персистирующая ЛГ новорожденных |
III. Легочная гипертензия, связанная с патологией легких и/или гипоксией: 3.1. ХОБЛ 3.2. Рестриктивные заболевания легких 3.3. Другие заболевания легких с рестриктивно-обструктивным паттерном 3.4. Гипоксия без заболеваний легких 3.5. Аномалии развития легких |
IV. ЛГ из-за обструкции легочной артерии: 4.1. Хроническая тромбоэмболическая ЛГ 4.2. Другие причины обструкции легочной артерии |
|
V. Легочная гипертензия с неясными и/или многофакторными механизмами заболевания: 5.1. Гематологические заболевания 5.2. Системные и метаболические нарушения 5.3. Другие 5.4. Сложные врожденные пороки сердца
|
|
II. Легочная гипертензия, связанная с патологией левых камер сердца: 2.1. ЛГ вследствие СНнФВ 2.2. ЛГ вследствие СНсФВ 2.3. Клапанная патология 2.4. Врожденная/приобретенная сердечно-сосудистая патология, приводящая к посткапиллярной ЛГ |
Гемодинамическая классификация легочной гипертензии [6]
Определение |
Характеристики |
Клинические группы |
Легочная гипертензия |
Среднее ДЛА ≥25 мм рт.ст. |
Все варианты легочной гипертензии |
Прекапиллярная легочная гипертензия |
Среднее ДЛА ≥25 мм рт.ст., ДЗЛА ≤ 15 мм рт.ст. ЛСС ≥ 3 ед Вуд |
1. Легочная артериальная гипертензия. 3. Легочная гипертензия вследствие патологии легких. 4. Хроническая тромбоэмболическая легочная гипертензия. 5. Легочная гипертензия с неясными и/или множественными механизмами
|
Изолированная посткапиллярная легочная гипертензия
Комбинированная пре- и посткапиллярная легочная гипертензия |
Среднее ДЛА ≥25 мм рт.ст., ДЗЛА >15 мм рт.ст. ЛСС<3 ед. Вуда
Среднее ДЛА ≥25 мм рт.ст., ДЗЛА>15 мм рт.ст. ЛСС<3 ед. Вуда
|
1. Легочная гипертензия вследствие патологии левых камер сердца. 2. Легочная гипертензия с неясными и/или множественными механизмами |
Функциональная классификация легочной гипертензии (ВОЗ) [16]
Класс |
Описание
|
IФК |
Нет ограничений обычной физической активности, она не вызывает повышенной одышки, усталости, болей в груди или предсинкопальных состояний. |
IIФК |
Легкое ограничение физической активности. Дискомфорт в покое отсутствует, но обычная физическая активность вызывает повышенную одышку, слабость, боль в грудной клетке или пресинкопальные состояния. |
IIIФК |
Значительное ограничение физической активности. В состоянии покоя дискомфорта нет, но физическая активность меньше обычной вызывает повышенную одышку, усталость, боль в груди или пресинкопальные состояния. |
IVФК |
Одышка и/или усталость в состоянии покоя, усиливающиеся практически при минимальной физической активности. Могут быть признаки правожелудочковой недостаточности. |
Классификация:
МКБ-10:
Другие формы сердечно-легочной недостаточности (I27):
I27.0 – Первичная легочная гипертензия
I27.2 – Другая вторичная легочная гипертензия
I27.8 – Другие уточненные формы легочно-сердечной недостаточности
Критерии постановки диагноза.
Критерии постановки диагноза легочной гипертензии: повышение среднего ДЛА ≥25 мм. рт. ст., измеренного в покое при чрезвенозной катетеризации сердца [11].
Диагностика ЛГ включает следующие этапы:
Скрининг, включающий в себя сбор жалоб, оценку принадлежности пациента к группам риска развития ЛАГ, определение вероятности ЛГ при помощи трансторакальной эхокардиографии (ЭхоКГ).
Последовательное исключение наиболее частых причин ЛГ, в первую очередь заболеваний левых отделов сердца (группа 2), патологии легких (группа 3) и ХТЭЛГ.
Верификация диагноза ЛГ при ЧВКС- чрезвенозная катетеризация сердца, уточнение нозологической принадлежности.
Оценка функционального класса и стратификация риска ЛАГ.
Лечение.
В принятой в настоящее время стратегии ведения пациентов с ЛАГ можно выделить три основные составляющие: общие рекомендации, поддерживающую терапию и специфическую терапию ЛАГ [6, 116]. Применение препаратов поддерживающей терапии не оказывает влияния на выживаемость пациентов с ЛАГ, тогда как использование специфических препаратов приводит к увеличению продолжительности жизни пациентов, уменьшению количества госпитализаций и увеличению времени до клинического ухудшения и трансплантации.
общие рекомендации: Что-то вроде бесед и психологической помощи.
поддерживающая терапия (антикоагулянты непрямые (антагонисты витамина К), диуретики, сердечные гликозиды (дигоксин), оксигенотерапия)
специфическую терапию ЛАГ:
основана на представлении о роли эндотелиальной дисфункции в ремоделировании легочной артерии. Действие таргетной терапии связано с блокадой рецепторов вазоконстрикторных субстанций и стимуляцией основных путей, опосредованных мощными вазодилататорами, такими как NO и простациклин. В настоящее время специфическая терапия включает 6 основных классов лекарственных препаратов, доказавших свою эффективность у пациентов с ЛАГ и одобренных к применению.
включающая блокаторы «медленных» кальциевых каналов (амлодипин, нифедипин),
Антигипертензивные средства для лечения легочной артериальной гипертензии C02KX, относящиеся к ЭРА (бозентан**, мацитентан**, амбризентан**)
ингаляционный илопрост,
фосфодиэстеразы ингибиторы (ИФДЭ-5),
риоцигуат
селексипаг
Показания:
Рекомендована своевременная замена терапии БКК на другие классы специфических препаратов в случае утраты ее эффективности у пациентов с ИЛАГ, наследственной ЛАГ и ЛАГ, ассоциированной с приемом лекарственных препаратов [6, 9, 10, 147].
ЕОК IC (УДД5 УУРС)
Рекомендуется продолжить терапию высокими дозами БКК пациентам с ИЛАГ, наследственной ЛАГ и ЛАГ, ассоциированной с приемом лекарственных препаратов, имеющим показатели гемодинамики, по данным ЧВКС, близкие к нормальным значениям при достижении I-II ФК (ВОЗ) [9, 10, 147].
EОК IC (УДД5 УУРС)
Рекомендуется начать специфическую терапию препаратами других классов пациентам III-IV ФК (ВОЗ) или пациентам, не имеющих значимого улучшения гемодинамики (т. е при недостижении гемодинамических показателей, близких к норме) на фоне терапии высокими дозами БКК.
Пульмонология
1. Обострение бронхиальной астмы. Вопросы дифференциальной диагностики. Критерии жизнеугрожающего обострения астмы. Дифференциальная диагностика хобл и ба
Признаки |
ХОБЛ |
БА |
Анамнез |
Курение, возраст > 35 лет. медленное нарастание респираторных симптомов |
Отягощенная наследственность по материнской или отцовской линии, начало часто в детстве |
Кашель |
Постоянное или интермитирующее покашливание днём |
Приступообразный, ночью или утром |
Выделение мокроты |
Скудная вязкая, при обострении зелёная или жёлтая |
Скудная стекловидная |
Одышка |
Постоянная, медленно прогрессирующая |
Приступообразная, прекращающаяся под влиянием бронхолитиков, реже спонтанно |
Переносимость физической нагрузки |
Снижена и постепенно необратимо ухудшается |
Снижается при обострении и восстанавливается в ремиссии |
Внелёгочные проявления |
Цианоз, похудание, признаки правожелудочковой недостаточности |
При атопической форме - риниты, кожные проявления аллергии, пищевая аллергия |
Эозинофилия крови |
Может быть, но не связана с патогенезом ХОБЛ |
Нередко, так как связана с патогенезом заболевания |
Эозинофилия мокроты |
Редко, не связана с патогенезом заболевания |
Часто, особенно при терапии без ГКС |
Эритроциоз |
Характерен при хронической гипоксии |
Не характерен |
Увеличение Ig E |
Может быть, но не связано с патогенезом заболевания |
Часто при атопической форме |
Сенсибилизация к стандартным аллергенам |
Не характерна |
Характерна |
ОФВ1 и ОФВ1/ФЖЕЛ |
Нарастающее снижение в соответствии со стадией болезни |
Снижается и восстанавливается в соответствии с тяжестью БА |
Изменение ОФВ1 после пробы с β2-агонистами |
Прирост ОФВ1< 15% |
Прирост ОФВ1> 15 % |
Суточные колебания ПСВ |
Менее 15% |
20 % и более в зависимости от тяжести БА |
Формирование лёгочного сердца |
Обязательный признак |
Не характерно |
Эффективность ГКС |
Низкая |
Высокая |
Клиническая оценка больного с обострением БА, нарастающей одышкой и ухудшением газообмена должна быть проведена очень быстро, при этом сохраняя достаточную тщательность. Оценка пациента должна включать историю заболевания, определение его тяжести, потенциальные провоцирующие факторы, оценка осложнений и ответ на терапию.
Под астматическим статусом понимают эпизод острой дыхательной недостаточности (ОДН) вследствие обострения БА. В современных классификациях астматический статус эквивалентен понятиям "жизнеугрожающая астма" и "астма, близкая к фатальной"
Жизнеугрожающая астма
Один из следующих критериев:
ПСВ < 33% от лучших значений
SрO2 < 92%
PaO2 < 60 мм рт.ст.
Нормокапния (РаСО2 35-45 мм рт.ст.)
"Немое" легкое
Цианоз
Слабые дыхательные усилия
Брадикардия
Гипотензия
Утомление
Оглушение
Кома
Астма, близкая к фатальной
Гиперкапния (РаСО2 > 45 мм рт.ст.) и/или
Потребность в проведении механической вентиляции легких
2. Дифференциальный диагноз легочного инфильтративного синдрома.
Вопросы врачебной тактики при организации дифференциальной диагностики ведущих нозологий (пневмония, рак, туберкулез).
Инфильтрат в лёгком – это участок лёгочной ткани, характеризующийся скоплением обычно не свойственных ему клеточных элементов, увеличенным объёмом и повышенной плотностью.
По данным рентгенологического исследования:
1) Ограниченные затемнения и очаги (наиболее часто)
2) Округлая тень – одиночная или множественная
3) Легочная диссеминация
4) Усиление легочного рисунка
Субъективные симптомы:
-Неспецифичны
-Могут указывать на поражение дыхательной системы
-Более часто встречается одышка, кашель, боли в грудной клетке, выделение мокроты, кровохарканье
-Возможно наличие только неспецифических симптомов: утомляемость, снижение работоспособности, головная боль, снижение массы тела
-Возможно полное отсутствие субъективных жалоб
Данные физикального обследования:
- Отставание больной половины грудной клетки в дыхании
- Усиление голосового дрожания в проекции уплотнения
- Тупой или притуплённый перкуторный звук
- Бронхиальное дыхание (крупные очаги) или ослабленное везикулярное (мелкие)
- Дополнительные дыхательные шумы: крепитация, различные хрипы, шум трения плевры
. ПНЕВМОНИЯ
Пневмония – острое инфекционное воспаление лёгочной ткани с обязательным вовлечением в процесс респираторных отделов лёгких
По объёму легочного инфильтрата
-Долевая (ранее крупозная)
-Очаговая (=бронхопневмония, однако термин признан устаревшим)
-Полисегментарная (термин используется в рентгенлогии, в клинической практике не применяется)
-Интерстициальная (не является истинной пневмонией, так как отсутствует поражение альвеол, в настоящее время термин заменн на «пульмонит»)
Подозрение на пневмонию:
1. Анамнез
** связь с перенесённой ОРВИ
** контакт с больным
** недомогание, симптомы общей интоксикации в течение нескольких дней
** гипертермия (субфебрилитет) в течение нескольких дней
** возможно острое начало или бессимптомное течение – анамнез отсутствует
2. Жалобы:
** характерные для интоксикационного синдрома
** гипертермия
** кашель
** боль в грудной клетке
** ДН
** возможно полное отсутствие жалоб
2. Инфильтративный туберкулёз
Подозрение на туберкулёз:
- Постепенное начало
- Предшествовал период немотивированного недомогания
- Субфебрилитет, кашель
- Физикальные симптомы выражены слабо
- Синдром легочной инфильтрации выявлен в области верхушки или верхней доли
- Затемнение обычно однородное, но в прилегочной ткани есть свежие очаги
- «Дорожка» к корню
- В корнях встречаются обызвествленные лимфоузлы
3. Легочной эозинофильный инфильтрат
1. Локальный легочный эозинофилит
· простой легочной эозинофилит (синдром Леффлера), причины – растительные аллергены, плесневые грибы, гальминты, лекарства, пищевые продукты, никель
· хроническая эозинофильная пневмония (длительный легочной эозинофилит, синдром Лера-Киндберга), причины – плесневые грибы, гельминты, лекарства, пищевые продукты, опухоли внутренних органов (почек, простаты), гемобластозы
2. Легочной эозинофилит с астматическим синдромом, причины – лекарства, гельминты, плесневые грибы, пищевые продукты, отмена поддерживающей терапии (ГКС), аспергиллы
3. Легочной эозинофилит с системными проявлениями (гиперэозинофильный миелопролиферативный синдром), причина не известна
Клиника
- Чаще отсутствует
- Возможны проявления, характерные для пневмонии
- Инфильтраты в лёгких гомогенные, без четких контуров и «дорожки» к корню
- Локализуются в различных отделах лёгкого
- Характерна «летучесть»
- Быстрый эффект ГКС
. ЗАТЕМНЕНИЕ ПРИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЯХ
- центральный рак легкого
- периферический рак легкого, особенно пневмоническая форма бронхиолоальвеолярного рака
- метастаз в легкие – единичный и множественные, в то числе эндобронхиальный
- лимфомы легкого
- саркомы легкого
Периферический рак:
o бугристые, неровные контуры тени
o структура тени однородная или с полостями распада
o окружающая легочная ткань интактна (м.б. периканкрозная пневмония)
o отводящей дорожки к корню нет
o часто увеличены лимфоузлы средостения
Анамнез
o пожилой возраст
o курение
o повторные пневмонии одной локализации
o длительные эпизоды кашля, в т.ч. непродуктивного
Метастатические поражения:
- множественные круглые тени
- необходим поиск первичной опухоли
- чаще метастазирует опухоль почек, хорионэпителиома, меланома, рак матки, молочной железы, ЖКТ
. АНОМАЛИИ РАЗВИТИЯ ЛЁГКИХ
- Киста лёгкого с аномальным кровоснабжением ( внутридолевая секвестрация лёгкого)
- Гипоплазия лёгких простая, кистозная, нагноившиеся легочные кисты
- Артериовенозные аневризмы в легких
- Лимфангиэктазия и прочие аномалии лимфатической системы
. НАГНОИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ ЛЁГКИХ
Это группа острых воспалительных процессов в лгких, протекающих с нагноением, некрозом и деструкцией
Термины:
Абсцесс – отграниченный гнойник, «множественные абсцессы»
Гангрена
Классификация:
1. Острая гнойно-некротическая деструкция лёгкого
- ограниченная ГНДЛ (с хорошим бронхиальным дренажом; с недостаточным бронхиальным дренажом; с полным нарушением бронхиального дренажа))
- распространённая ГНДЛ (бронхогенная – легочная, легочно-плевральная; гематогенная - легочная, легочно-плевральная)
- ограниченная гангрена (регрессирующая, прогрессирующая)
- распространенная гангрена (прогрессирующая)
2. Хроническая гнойная деструкция лёгких
ДИАФРАГМАЛЬНАЯ ГРЫЖ
АСПИРАЦИЯ ИНОРОДНОГО ТЕЛА
- обтурация бронха с развитием ателектаза и пневмонии дистальнее места обструкции
- диф.диагностика с опухолевым ателектазом
- в случае аспирации рентген-контрастного тела оно визуализируется на фоне инфильтрата
Вопросы врачебной тактики при организации дифференциальной диагностики ведущих нозологий.Тут просто необходимо доп обследование и сбор анамнеза.
3. Дифференциальная диагностика плеврального выпота. Этиология, клинические проявления, показания к проведению плевральной пункции и исследованию плевральной жидкости. Различие между транссудатом и экссудатом.
Синдромом плеврального выпота называют, прежде всего, клинический симптомокомплекс, характеризующийся накоплением жидкости в плевральной полости.
— постепенно или относительно быстро нарастающая одышка, которая сначала проявляется при физических нагрузках, а потом — в состоянии покоя;— цианоз видимых слизистых оболочек, в тяжелых случаях — акроцианоз; —боль в грудной клетке на стороне поражения не является постоянным симптомом; чаще всего она беспокоит в начале накопления жидкости и при её рассасывании; — при односторонней локализации процесса определятся отставание пораженной половины грудной клетки в акте дыхания, реже — небольшое выбухание пораженной стороны; в горизонтальном положении больному легче лежать на пораженной стороне;
—на стороне патологического процесса отсутствует или определяется значительно ослабленное голосовое дрожание; там же методом перкуссии определяется тупой звук, зона которого очерчивается характерной линией Дамуазо; —аускультацией над пораженной областью легкого
определяется значительно ослабленное везикулярное дыхание, часто дыхание не выслушивается.
Плевральная пункция должна проводиться при любом, даже очень малом, количестве плевральной жидкости.
Плевральный транссудат — это, как правило, прозрачная соломенно-жёлтая жидкость небольшой относительной плотности, с низким содержанием белка и без склонности к осаждению при длительном отстаивании. Содержание клеток в ней не превышает 1,0×109/л.
Характерным свойством является также низкая активность в такой жидкости лактатдегидрогеназы (ЛДГ). Наиболее частыми причинами накопления транссудата в плевральной полости является застойная сердечная недостаточность (кардиогенный гидроторакс), цирроз печени, нефротический синдром, тяжелая форма микседемы
Плевральный экссудат — это жидкость желтого или оранжевого цвета с более высокой плотностью, высоким содержанием белка и фибриногена. Экссудат часто имеет свойство образовывать осадок при длительном отстаивании. Содержание клеток в нем часто превышает 1,0×109/л. Высокой активностью отличается ЛДГ. Наиболее частыми причинами накопления экссудата в плевральной полости являются воспалительные процессы легких.
Из документа другого!!!
Плеврит - это воспаление плевральных листков, сопровождающееся выпотеванием в плевральную полость экссудата того или иного характера.
ЭТИОЛОГИЯ.
Инфекционные
туберкулез (20-50%)
бактериальный
пневмококк. Паралелльно с пневмонией могут развиваться парапневмонические (развиваются вместе с пневмонией) и метапневмонические (после пневмонии) плевриты.
стафилококк. В основном является причиной эмпием плевры.
микоплазмы
синегнойная палочка, кишечная палочка
грибковые
аспергиллез
кандидомикоз
бластомикоз
паразитарные
Асептические:
карциноматозный (40%)
метастатический (рак легкого сопровождается плевритом в 43%, рак молочной железы 23%, лимфомы 8%).
мезотелиома - первичная опухоль плевры. Частота встречаемости 2:1000. Наиболее часто заболевают мужчины 20-40 лет имевшие контакт с асбестом. Характеризуется появлением геморрагичекого экссудата, в среднем живут после постановки диагноза прогноз 1-2 года.
ферментативный - острый панкреатит
аллергические
лекарственная аллергия
постинфарктный аллергический синдром. Проявляется тремя П - плеврит, перикардит, пневмонит. Четвертое П - симптом плеча.
эмболия легочной артерии
системные васкулиты
гранулематоз Вегенера
узелковый периартериит
системные заболевания соединительной ткани
ревматоидный артрит
системная красная волчанка
посттравматические
при элетроожогах
саркоидоз Бека
уремия
лучевая терапия
Различают 4 синдрома:
синдром сухого плеврита
синдром выпотного плеврита
синдром эмпиемы плевры
синдром основного заболевания
Клиника фибринозного плеврита:
жалобы на боли при дыхании, кашле, при наклоне в противоположную сторону. Длительная субфебрильная лихорадка особенно по вечерам; потливость. Объективно: дыхание поверхностное, учащенное, положение больных вынужденное (больной лежит на больном боку, чтобы уменьшить боль). При физикальном исследовании наряду с симптомами основного заболевания будет прослушиваться локализованный или обширный шум трения плевры.
При экссудативном плеврите болевые ощущения могут ослабевать, но у больного появляется чувство тяжести в той или иной половине грудной клетки, одышка, сухой или со скудной мокротой кашель (рефлекторный характер). Больной принимает вынужденное положение. При осмотре выявляется цианоз, акроцианоз, набухшие вены шеи. При осмотре грудной клетки: выбухание межреберий, пораженная половина отстает при дыхании. При пальпации ограничена экскурсия, голосовое дрожание не проводится. При перкуссии бедренная тупость легочного звука. При аскультации дыхание не проводится (если количество жидкости небольшое, то дыхание может проводиться, при наличии гноя дыхание может стать жестким или бронхиальным. При горизонтальном положении будет ослабление везикулярного дыхания).
Клиника эмпиемы плевры - гектический характер лихорадки, выраженные признаки интоксикации, изменения аскультативных данных.
Достоверным признаком диагностики плеврита является рентгенография органов грудной клетки: классические признаки выпотного плеврита - гомогенное затемнение легочной ткани с косым верхним уровнем жидкости. Классические признаки появляются в случае диффузного плеврита, если количество жидкости превышает 1 литр. Если жидкости меньше литра, то жидкость скапливается в синусах, и сглаживает нижнебоковой синус. Сложно бывает поставить диагноз, если имеется тотальное затемнение той или иной половины грудной клетки (тотальная острая пневмония, ателектазы легкого прямое противопоказание в торакоцентезу). Если это жидкость, то наблюдается контралатеральное смещение органов средостения. При гидропневмотораксе уровень жидкости горизонтальный. При междолевом плеврите то обычно, это представляется в виде двояковыпуклой линзы.
В диагностике плевритов большое значение придают плевральной пункции. Торакоцентез проводится в 7-8 межреберье по заднеакссилярной или лопаточной линии. Полученную жидкость осматривают, определяют ее цвет, консистенцию. Необходимо определить транссудат или экссудат: нужно определить количества белка, произвести пробу Ривольта, исследовать ЛДГ. Транссудат: количество белка меньше 32 г/л, уровень ЛДГ меньше 1.3 ммоль/л, проба Ривольта отрицательная.
Содержание белка в транссудате меньше, чем в экссудате, и составляет не более 3% (обычно 0,5—2,5%), в экссудате — 3—8%.
Относительная плотность транссудата меньше 1,015, чаще в пределах 1,006—1,012, экссудата — выше 1,015, преимущественно 1,018—1,022.
4. Интерстициальные заболевания легких. Основные нозологии. Вопросы диагностики. Принципы лечения.
это гетерогенная группа заболеваний известной и неизвестной природы, характеризующиеся распространенным, как правило, двусторонним поражением респираторных отделов легких (альвеол, респираторных бронхиол) с развитием необратимого фиброза при хроническом течении.
ИБЛ известной природы: Пневмокониоз, гиперсенситивный пневмонит, поражения легких при системных заболеваниях соединительной ткани, идиопатический легочный фиброз, саркоидоз.
Методы диагностики:
Рентгенологические (являются двусторонние изменения ретикулярного характера, более выраженные в нижних отделах легких. При прогрессировании заболевания ретикулярный паттерн становится более грубым, тяжистым; появляются округлые кистозные просветления, отражающие формирование сотового легкого”
спирометрия
пульсоксиметрия
диффузионная способность легких(снижение легочного комплаенса и статических легочных объемов (общей емкости легких , функциональной остаточной емкости, остаточного объема)
исследование газов крови
биопсия легких
Современное лечение ИЛФ построена в основном на применении ГКС и цитостатиков
монотерапия ГКС, комбинация ГКС с азатиоприном и комбинация ГКС
с циклофосфамидом.
ГКС 0,25 мг/кг в сутки в течение 8 недель;
+ азатиоприн • начальная доза – 25–50 мг/сут; дозу повышают на 25 мг каждые 1–2 недели до достижения максимальной дозы – 150 мг/сут
5. Хобл. Роль спирометрии в постановке диагноза. Шкалы клинической оценки течения хобл и риска обострений. Принципы лечения в зависимости от градации a,b,c,d.
Хроническая обструктивная болезнь легких (ХОБЛ) – заболевание, характеризующееся персистирующим ограничением воздушного потока, которое обычно прогрессирует и является следствием хронического воспалительного ответа дыхательных путей и легочной ткани на воздействие ингалируемых повреждающих частиц или газов
Спирометрическая (функциональная) классификация ХОБЛ
I стадия ХОБЛ Легкая < 0,7 (70%) ОФВ1 ≥ 80%
II Среднетяжелая < 0,7 (70%) 50%≤ОФВ1< 80%
III Тяжелая < 0,7 (70%) 30%≤ОФВ1< 50%
IV Крайне тяжелая < 0,7 (70%) ОФВ1 < 30% или < 50% в сочетании с хронической дыхательной недостаточностью
Классификация ХОБЛ согласно GOLD
A группа пациентов -Низкий риск обострений Симптомы не выражены- спиромтр.классификация GOLD 1–2 число обострений за 1 год. ≤1 шкала mMRC 0–1 CAT-тест <10
B Низкий риск обострений Симптомы выражены GOLD 1–2 ≤1 >2 ≥10
C Высокий риск обострений Симптомы не выражены GOLD 3–4 >2 0–1 <10
D Высокий риск обострений Симптомы выражены GOLD 3–4 >2 >2 ≥10
Всем пациентам с ХОБЛ рекомендуется отказ от курения
-Стартовая монотерапия одним бронхолитиком длительного действия (ДДАХ или ДДБА) рекомендуется пациентам с невыраженными симптомами (mMRC<10
-При наличии у пациента выраженных симптомов (mMRC ≥2 или САТ≥10) рекомендуется назначение комбинации ДДАХ/ДДБА сразу после установления диагноза ХОБЛ
-Для лечения ХОБЛ рекомендуется использовать следующие длительннодействующие антихолинергики (ДДАХ): тиотропия бромид
-Пациентам с ХОБЛ и частыми обострениями (2 и более среднетяжелых обострений в течение 1 года или хотя бы 1 тяжелое обострение, потребовавшее госпитализации) также рекомендуется назначение ИГКС в дополнение к ДДБД
-У больных ХОБЛ без повторных обострений и с сохранной функцией легких (ОФВ1 > 50% от должного) рекомендуется полная отмена ИГКС при условии назначения ДДБД
6. Бронхиальная астма. Фенотипы заболевания. Стандарты диагностики и лечения
Бронхиальная астма (БА) является гетерогенным заболеванием, характеризующимся хроническим воспалением дыхательных путей, наличием респираторных симптомов, таких как свистящие хрипы, одышка, заложенность в груди и кашель, которые варьируют по времени и интенсивности, и проявляются вместе с вариабельной обструкцией дыхательных путей
Аллергическая БА: наиболее легко распознаваемый фенотип, при котором БА обычно начинается в детстве, связана с наличием других аллергических заболеваний (атопический дерматит, аллергический ринит, пищевая аллергия) у пациента или родственников. Для этого фенотипа характерно эозинофильное воспаление дыхательных путей. Пациенты с аллергической БА обычно хорошо отвечают на терапию ингаляционными глюкокортикостероидами ИГКС.
Неаллергическая БА: встречается у взрослых, не связана с аллергией. Профиль воспаления дыхательных путей у больных с данным фенотипом может быть эозинофильным, нейтрофильным, смешанным или малогранулоцитарным. В зависимости от характера воспаления пациенты с неаллергической астмой могут не отвечать на терапию ИГКС.
БА с поздним дебютом: у некоторых пациентов, особенно женщин, астма развивается впервые уже во взрослом возрасте. Эти больные чаще не имеют аллергии и, как правило, являются относительно рефрактерными к терапии стероидами или им требуются более высокиее дозы ИГКС.
БА с фиксированной обструкцией дыхательных путей: у некоторых пациентов с длительным анамнезом БА, по-видимому, вследствие ремоделирования бронхиальной стенки развивается фиксированная обструкция дыхательных путей.
БА у больных с ожирением: пациенты с ожирением и БА часто имеют выраженные респираторные симптомы, не связанные с эозинофильным воспалением.
Стандарты диагностики и лечения: сбор анамнеза у пациента с БА причины возникновения, продолжительность клинических проявлений и разрешения симптомов, наличие аллергических реакций у пациента и его кровных родственников, причинно-следственные особенности возникновения признаков болезни и ее обострений.( тест по контродю над астмой)
-Наиболее часто при БА выявляют свистящие хрипы, которые у ряда пациентов выслушиваются только во время форсированного выдох
Инструментальная диагностика Спирометрия Бронходилатационный тест считается +, если после ингаляции бронходилататора коэффициент бронходилатации по (ОФВ1) составляет не менее 12%,
-У пациентов с нормальными показателями спирометрии и отрицательным бронходилатационным тестом для подтверждения диагноза БА рекомендуется использовать тесты на выявление бронхиальной гиперреактивности
- В качестве маркеров аллергического воспаления при БА рекомендуется исследовать уровень эозинофилов в мокроте
Ступенчатая терапия БА.
Ступень 1 Короткодействующие β2–агонисты (КДБА)
Ступень 2 низких доз ИГКС в качестве базисной терапии и КДБА для купирования симптомов
Ступень 3 комбинация низких доз ИГКС и (ДДБА)
Ступень 4 комбинации низких доз ИГКС (будесонид или беклометазон/формотерол в режиме единого ингалятора или комбинации средних доз ИГКС/ДДБА и КДБА
Ступень 5 рекомендуется направлять к специалисту, занимающемуся экспертизой и лечением тяжелой БА, В качестве дополнительной терапии к максимальной дозе ИГКС ≥ 1000 мкг в эквиваленте беклометазона дипропионата рекомендуются тиотропия бромид, омализумаб**, меполизумаб, реслизумаб, минимально возможная доза пероральных ГКС.
7. Фенотипы бронхиальной астмы. Неконтролируемая и тяжелая бронхиальная астма. Вопросы дифференциальной диагностики и тактики ведения.
Аллергическая БА: наиболее легко распознаваемый фенотип, при котором БА обычно начинается в детстве, связана с наличием других аллергических заболеваний (атопический дерматит, аллергический ринит, пищевая аллергия) у пациента или родственников. Для этого фенотипа характерно эозинофильное воспаление дыхательных путей. Пациенты с аллергической БА обычно хорошо отвечают на терапию ингаляционными глюкокортикостероидами ИГКС.
Неаллергическая БА: встречается у взрослых, не связана с аллергией. Профиль воспаления дыхательных путей у больных с данным фенотипом может быть эозинофильным, нейтрофильным, смешанным или малогранулоцитарным. В зависимости от характера воспаления пациенты с неаллергической астмой могут не отвечать на терапию ИГКС.
БА с поздним дебютом: у некоторых пациентов, особенно женщин, астма развивается впервые уже во взрослом возрасте. Эти больные чаще не имеют аллергии и, как правило, являются относительно рефрактерными к терапии стероидами или им требуются более высокиее дозы ИГКС.
БА с фиксированной обструкцией дыхательных путей: у некоторых пациентов с длительным анамнезом БА, по-видимому, вследствие ремоделирования бронхиальной стенки развивается фиксированная обструкция дыхательных путей.
БА у больных с ожирением: пациенты с ожирением и БА часто имеют выраженные респираторные симптомы, не связанные с эозинофильным воспалением.
Неконтр. Бр.астма: за последние 4 недели у пациента отмечались дневные симптомы чаще 2-х раз в неделю, ночные пробуждения из-за БА, потребность в препарате для купирования симптомов чаще 2-х раз в неделю, любое ограничение активности из-за БА
Тяжелая БА: астма, требующая терапии ступени 4 и 5, для того чтобы сохранить контроль, или БА, которая остается неконтролируемой, несмотря на эту терапию (ступень 5) Высокие дозы ИГКС/ДДБА, тиотропия бромид, таргетная терапия и/или СГКС
Дифференциальная диагностика бронхиальной обструкции, определяемой как ОФВ1/ФЖЕЛ
При отсутствии бронхиальной обструкции(Синдром хронического кашля Гипервентиляционный синдром Синдром дисфункции голосовых связок ГЭРБ Риниты Заболевания сердца Легочный фиброз)
При наличии бронхиальной обструкции(ХОБЛ Бронхоэктазы Инородное тело Облитерирующий бронхиолит Стеноз крупных дыхательных путей Рак легких Саркоидоз)
Внебольничные пневмонии тяжелого течения. Диагностические критерии, течение, критерии высокого риска летального исхода. Неотложная терапия.
Тяжелая внебольничная пневмония – это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризующаяся плохим прогнозом и требующая проведения интенсивной терапии.
Для принятия решения относительно места лечения пациента используйте шкалу CRB-65 спутанность сознания, ЧДД >30 вдохов/мин САД <90 мм.рт.ст. ДАД <=60 мм.рт.ст. возраст >65 л –пнев.тяж.течения
Оценка тяжести внебольничной пневмонии у пациентов в больнице – шкала CURB-65 спутанность сознания, ЧДД >30 вдохов/мин САД <90 мм.рт.ст. ДАД <=60 мм.рт.ст. возраст >65 л, концентрация в сыворотке мочевины >7 ммоль/л –пнев.тяж.течения Риск смерти 15-40%
Признаки тяжёлой формы внебольничной пневмонии:А. Большие – острая дыхательная недостаточность с частотой дыхания свыше 40 за одну минуту; септический шок с показанием назначения вазопрессоров (больше 4-х часов).Б. Малые – разрушение лёгочной ткани; быстрое увеличение инфильтрации, определяемой при рентгенографии; респираторные и гемодинамические нарушения; снижение сатурации кислорода до 90 % и ниже; нарушения сознания; осложнения; лица старше 64 лет; тяжёлые сопутствующие заболевания.
Лечение: Всем пациентам с ВП при РаО2 < 60 мм рт.ст. или SрO2 < 90% (при дыхании воздухом) рекомендуется респираторная поддержка
Всем пациентам с ВП при РаО2 < 60 мм рт.ст. или SрO2 < 90% (при дыхании воздухом) рекомендуется респираторная поддержка
Антибактериальная терапия Препараты выбора:
Амоксициллин/клавуланат в/в + макролид в/в
Цефотаксим в/в+ макролид в/в
Цефтриаксон в/в+ макролид в/в
ЦЕФТАРОЛИН (ЗИНФОРО) 600 мг в/в капельно + макролид в/в
Респираторные фторхинолоны (левофлоксацин, моксифлоксацин) в/в
+ ЦЕФТАРОЛИН (ЗИНФОРО) 600 мг в/в капельно
Всем пациентам с ТВП рекомендуется эмпирическое назначение противовирусных препаратов при наличии клинических/эпидемиологических данных, предполагающих вероятное инфицирование вирусами гриппа
Больным с внебольничной пневмонией легкого течения антибактериальную терапию можно проводить в амбулаторных условиях. Оптимальными являются препараты, которые можно применять 1–2 раза в сутки. Пациент с внебольничной пневмонии тяжелого течения подлежит госпитализации; обычно назначают бета-лактамные антибиотики (амоксициллин/клавуланат, карбапенемы, цефалоспорины III-IV поколений) в сочетании с макролидами или любым фторхинолоном (офлоксацин, ципрофлоксацин). При тяжелом течении пневмонии антибактериальные препараты следует применять внутривенно, по крайней мере, до получения клинического эффекта.
При нетяжелой внебольничной пневмонии антибактериальная терапия может быть завершена по достижении стойкой нормализации температуры тела (в течение 3–4 дней). При таком подходе длительность лечения обычно составляет 7–10 дней. При тяжелой внебольничной пневмонии неуточненной этиологии рекомендован 10-дневный курс антибактериальной терапии. В эти же сроки обычно наблюдается исчезновение лейкоцитоза. В случае наличия клинических и/или эпидемиологических данных о микоплазменной или хламидийной этиологии внебольничной пневмонии продолжительность терапии должна составлять 14 дней. Более длительные курсы антибактериальной терапии показаны при внебольничной пневмонии стафилококковой этиологии или внебольничной пневмонии, вызванной грамотрицательными энтеробактериями, – от 14 до 21 дня. При указании на легионеллезную пневмонию длительность антибактериальной терапии составляет 21 день.
9. Понятие контроля при бронхиальной астме. Терапевтические опции для достижения контроля над течением заболевания. Организация step up и step down терапии.
Понятие «контроль астмы» включает в себя не только отсутствие клинических проявлений болезни, потребности в «спасательной» терапии, снижения функции легких, но также и предотвращение отдаленных рисков, таких как обострение болезни и побочные эффекты приема лекарственных препаратов.
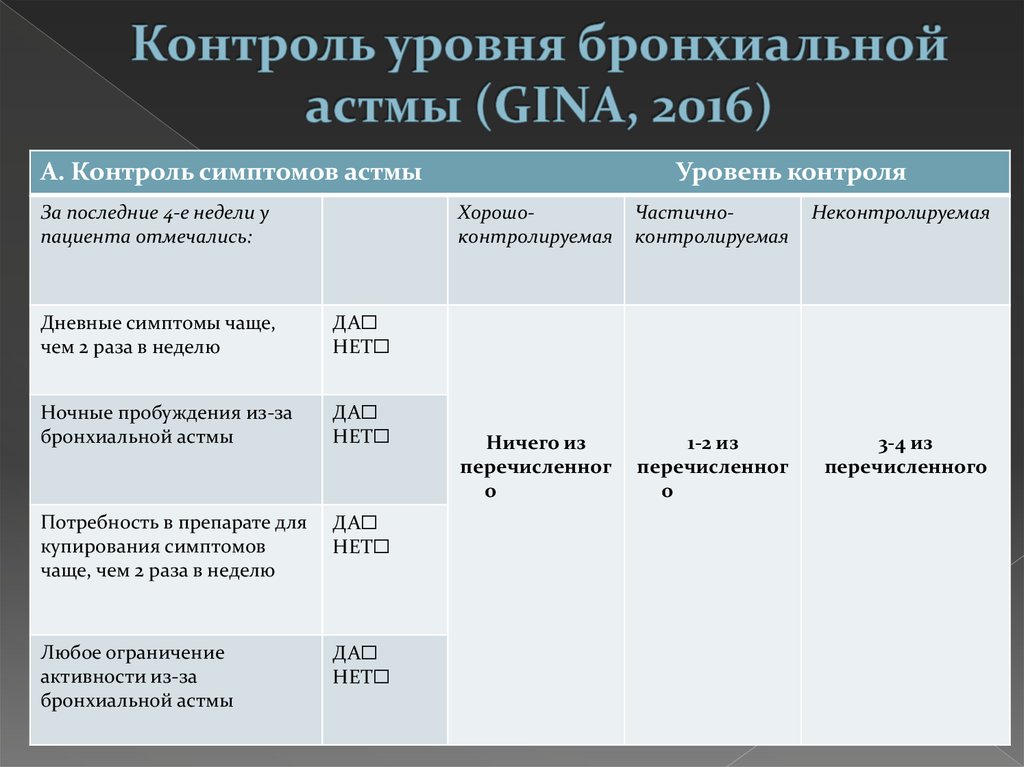
Терапевтические опции для достижения контроля над течением заболевания
Каждая ступень включает варианты терапии, которые могут служить альтернативами при выборе поддерживающей терапии БА, хотя и не являются одинаковыми по эффективности. Первоначальный выбор ступени терапии зависит от выраженности клинических проявлений БА.
Увеличение объема терапии (переход на ступень вверх) показано при отсутствии контроля и/или наличии факторов риска обострений. Снижение объема терапии показано при достижении и сохранении стабильного контроля ≥ 3 месяцев и отсутствии факторов риска с целью установления минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля.
10. Дыхательная недостаточность. Классификация. Клинические проявления. Критерии диагностики. Неотложная помощь. Профилактика.
J 96. Острая дыхательная недостаточность – быстро нарастающее (время развития несколько минут/дней) тяжелое патологическое состояние больного, обусловленное несоответствием системы внешнего дыхания метаболическим потребностям организма для поддержания нормального парциального напряжения кислорода и углекислого газа в артериальной крови, или оно достигается за счет усиленной работы систем дыхания и кровообращения, что приводит к снижению и последующему истощению функциональных возможностей организма.
Этиологическая классификация ОДН: первичная ОДН, вторичная ОДН, смешанная форма ОДН.
Первичная ОДН характеризуется нарушением доставки кислорода в альвеолы из-за повреждения системы внешнего дыхания.
При вторичной ОДН страдает транспорт кислорода из альвеол к тканям, так как происходит развитие патологических процессов в системах, которые не относятся непосредственно к органам дыхания, в первую очередь развивается декомпенсация кровообращения.
Смешанная ОДН сопровождается сочетанием артериальной гипоксемии и гиперкапнии.
Патогенетическая классификация ОДН: гипоксемическая, вентиляционная, смешанная.
Гипоксемическая дыхательная недостаточность (паренхиматозная, легочная, ДН 1-го типа) характеризуется артериальной гипоксемией, развивающейся главным образом в результате нарушения регионарного вентиляционно-перфузионного баланса или внутрилегочного шунтирования крови.
Вентиляционная дыхательная недостаточность (гиперкапническая, «насосная», ДН 2-го типа) обусловлена первичным уменьшением эффективности легочной вентиляции (альвеолярная гиповентиляция), что нарушает выведение СО2 и нередко приводит к нарушениям кислотно-основного состояния (КОС), т.е. характерным признаком является гиперкапния (PaCO2≥ 45 мм рт.ст.), гипоксемия также присутствует, но хорошо поддается терапии кислородом. Уровень гиперкапнии прямо пропорционален степени уменьшения альвеолярной вентиляции.
Смешанная дыхательная недостаточность. Нарушено как распределение газа в легких (вентиляционно-перфузионные отношения, так и вентиляционная (насосная) функция легких. Компенсаторно возникает одышка – ранний и надежный симптом ОДН, субъективно проявляющаяся чувством нехватки воздуха или затруднения дыхания. При этом изменяются частота, ритм и глубина дыхания, сопровождающееся повышением работы дыхательных мышц.
Степени тяжести синдрома ОДН.
Вентиляционная ОДН:
Норма: paСO2 = 35-45 мм рт.ст.
I степень (умеренная) - paСO2 < 50 мм рт.ст.
II степень (выраженная) - paСO2 = 51-69 мм рт.ст.
III степень (тяжелая) - paСO2 >70 мм рт.ст.
Гиперкапническая кома – 90-140 мм рт.ст.
Паренхиматозная ОДН:
Норма: paO2 = 80-100 мм рт.ст. (SpO2 ≥ 95 мм рт.ст.)
I степень (умеренная) - paO2 = 60-79 мм рт.ст. (SpO2 =90-94%)
II степень (выраженная) - paO2 = 40–59 мм рт.ст. (SpO2=76-89%)
III степень (тяжелая) - paO2 <40 мм рт.ст. (SpO2 ≤ 75%)
Гипоксемическая кома – 39-30 мм рт.ст.
Клинические проявления гипоксемической
со стороны органов дыхания: диспноэ, тахипноэ, гиперпноэ – углубление дыхания;
со стороны органов кровообращения: тахи- или брадипноэ, аритмиии, артериальная гипер- или гипотензия, цианоз слизистых оболочек, легочная гипертензия, правожелудочковая сердечная недостаточность.
Клинические проявления вентиляционной
со стороны ЦНС обусловлены ее поражением: головная боль, беспокойство, тремор конечностей, судороги, отек диска зрительного нерва, спутанная речь, нарушение сознания (оглушение, сопор, кома);
другие признаки: покраснение кожных покровов (багрово-синюшнее лицо), экзофтальм с гиперемией сосудов конъюнктивы; повышенная потливость, артериальная гипертензия и тахикардия, одутловатость лица.
I стадия ОДН. Пациент находится в сознании, жалуется на чувство нехватки воздуха, беспокоен, астеничен. Кожные покровы бледные, влажные, небольшой акроцианоз видимых слизистых. ЧД до 30 в 1 мин, ЧСС до 110 в 1 мин, АД в норме или несколько повышено, paO2 снижается до 70 мм рт.ст., paСO2 снижено из-за компенсаторной одышки.
II стадия ОДН. Больной жалуется на выраженное удушье, возможно развитие психомоторного возбуждения, нарушение сознания, бреда, галлюцинаций. Кожные покровы влажные, цианотичные, нередко в сочетании с гиперемией. ЧД 30-40 в 1 мин, ЧСС 120-140 в 1 мин нередко аритмия, регистрируется гипертензия, paO2 снижается до 60 мм рт.ст., paСO2 повышается до 50 мм рт.ст.
III стадия ОДН. Сознание помрачено или отсутствует, возможно развитие судорожного синдрома из-за гипоксии мозга, наблюдается пятнистый цианоз, гипоксическое расширение зрачка с отсутствием реакции на свет. При прогрессировании процесса тахипное (ЧД > 40 в 1 мин) переходит в брадипное (ЧД < 8 в 1 мин). Наблюдается гипотензия, тахиаритмии, paO2 уменьшается до 50 мм рт.ст. и ниже, paСO2 повышается до 90 мм рт.ст. и выше.
Диагностика
Диагностическими критериями ОДН служат показатели парциального давления кислорода в артериальной крови (рО2) менее 75 мм рт. ст., показатели парциального давления углекислого газа в крови (рО2) более 45 мм рт. ст.
Неотложная помощь
После обеспечения проходимости дыхательных путей убедитесь в генезе острой дыхательной недостаточности: с этой целью выведите нижнюю челюсть вперед и установите воздуховод в ротовую полость для устранения западения языка. Если после вышеуказанных мероприятий у больного нормализуется дыхание, следует думать, что ОДН возникла на фоне обструкции верхних дыхательных путей. Если же после проведения вышеуказанного пособия признаки ОДН не купируются, вероятнее всего центральный или смешанный генез нарушения дыхания.
Для купирования острой дыхательной недостаточности I ст. бывает достаточным проведение больному оксигенотерапии увлажненным кислородом. Оптимальным является 35—40% содержание кислорода во вдыхаемой смеси. Вышеуказанная концентрация во вдыхаемом воздухе достигается при подаче кислорода через дозиметр наркозного или дыхательного аппарата в объеме 3—5 л/мин. Непосредственную подачу кислорода больному можно осуществлять через носовые катетеры или через маску наркозного аппарата.
При острой дыхательной недостаточности I ст. на фоне устраненной обструкции дыхательных путей и при отсутствии воздуховода для предупреждения западения языка больному нужно придать устойчивое боковое положение.
Наличие острой дыхательной недостаточности II—III ст. является показанием для перевода больного на ИВЛ. В экстремальной ситуации, при быстром нарастании признаков ОДН, показано проведение коникотомии, или прокалывание трахеи толстыми иглами. Выполнение трахеотомии в экстренной ситуации не проводится из-за длительности самого оперативного вмешательства. Данную операцию следует рассматривать как плановую при разможжении лица, переломах перстневидного хряща, длительном (более 2—3 суток) нахождении больного на ИВЛ.
При бронхообструктивном синдроме – бронходилататоры (сальбутамол ингаляционно 1-2 дозы/100—200 мкг аэрозоля или 2,5-5 мг через небулайзер). При выраженной бронхообструкции необходимо рассмотреть целесообразность системного введения глюкокортикоидов.
Дезинтоксикационная терапия (изотонический раствор, 5% раствор глюкозы, гемодез-Н, объём однократного введения 200 – 400 мл).
При артериальной гипотензии (АД < 90/60 мм рт. ст.) - начать восполнение потери жидкости, учитывая, что при повышении температуры на 1 °С количество жидкости в организме уменьшается на 500 мл/сут (0,9% р-р натрия хлорида — 400 мл в/в, 5% р-р декстрозы - 400 мл в/в, быстрая инфузия, гидроксиэтилкрахмал 500 мл).
Профилактика
Первичная профилактика включает в себя проведение мероприятий, направленных на устранение факторов риска развития заболевания. В задачи первичной профилактики входит выявление лиц с отягощенной наследственностью по БА и другим аллергическим заболеваниям. Предоставление при трудоустройстве на производство с высоким содержанием аллергенов и других раздражающих веществ.
К мерам вторичной профилактики относятся мероприятия, проводимые для лечения пациентов в межприступный период, направленные на предупреждение обострений БА:
■ Исключить контакт с причинно-значимыми аллергенами.
■ Исключить (или максимально ограничить) влияние неспецифических раздражителей: курения, профессиональных вредностей, поллютантов, резких запахов и других. При необходимости лимитировать физическую и психоэмоциональную нагрузку.
■ Не принимать β-адреноблокаторы
■ Амбулаторная консультация лечащего врача (пульмонолога, аллерголога-иммунолога) для определения дальнейшей тактики (обследования, лечения обострения бронхиальной астмы, подбора базисной терапии).
■ Обучение в астма-школе. Всем пациентам с немотивированным кашлем (легочные причины были исключены) показана гастродуоденофиброскопия с целью выявления гастроэзофагеальной рефлюксной болезни или обследование на предмет синдрома обструктивного апноэ сна.
11. Бронхиальная астма. Определение. Фенотипы. Критерии постановки диагноза. Роль спирометрии. Понятие о вариабельности и обратимости бронхиальной обструкции.
J 45. Бронхиальная астма (БА) является гетерогенным заболеванием, характеризующимся хроническим воспалением дыхательных путей, наличием респираторных симптомов, таких как свистящие хрипы, одышка, заложенность в груди и кашель, которые варьируют по времени и интенсивности, и проявляются вместе с вариабельной обструкцией дыхательных путей.
Классификация БА по фенотипам
Аллергическая БА: наиболее легко распознаваемый фенотип, при котором БА обычно начинается в детстве, связана с наличием других аллергических заболеваний (атопический дерматит, аллергический ринит, пищевая аллергия) у пациента или родственников. Для этого фенотипа характерно эозинофильное воспаление дыхательных путей. Пациенты с аллергической БА обычно хорошо отвечают на терапию ингаляционными глюкокортикостероидами ИГКС.
Неаллергическая БА: встречается у взрослых, не связана с аллергией. Профиль воспаления дыхательных путей у больных с данным фенотипом может быть эозинофильным, нейтрофильным, смешанным или малогранулоцитарным. В зависимости от характера воспаления пациенты с неаллергической астмой могут не отвечать на терапию ИГКС.
БА с поздним дебютом: у некоторых пациентов, особенно женщин, астма развивается впервые уже во взрослом возрасте. Эти больные чаще не имеют аллергии и, как правило, являются относительно рефрактерными к терапии стероидами или им требуются более высокие дозы ИГКС.
БА с фиксированной обструкцией дыхательных путей: у некоторых пациентов с длительным анамнезом БА, по-видимому, вследствие ремоделирования бронхиальной стенки развивается фиксированная обструкция дыхательных путей.
БА у больных с ожирением: пациенты с ожирением и БА часто имеют выраженные респираторные симптомы, не связанные с эозинофильным воспалением.
Трудная для лечения БА это астма, которая не контролируется, несмотря на лечение на ступени 4 или 5 по GINA (например, ИГКС в средней или высокой дозе со вторым контроллером (ДДБА или АЛТР); поддерживающая терапия ОКС)), или для которой требуется такое лечение для поддержания хорошего контроля симптомов и уменьшения риска обострений. Во многих случаях БА может быть трудной для лечения из-за модифицируемых факторов, таких как: неправильная техника ингаляции, плохая приверженность лечению, курение или сопутствующие заболевания, или из-за неправильного диагноза.
Тяжелая астма является подгруппой трудно поддающейся лечению астмы и означает астму, которая остается неконтролируемой, несмотря на приверженность максимально оптимизированной терапии и лечению сопутствующих заболеваний, или ухудшается когда высокие дозы ГКС уменьшаются.
Критерии постановки диагноза
1. Анамнез и оценка симптомов. Наиболее распространенными симптомами заболевания являются эпизодические приступы удушья, одышки, появление свистящих хрипов, ощущение тяжести в грудной клетке, а также кашель. Однако сами по себе эти симптомы еще не являются диагнозом. Важный клинический маркер бронхиальной астмы - исчезновение симптомов спонтанно или после применения бронходилататоров и противовоспалительных препаратов. При оценке и сборе анамнеза значение придается следующим фактам: повторные обострения, чаще всего провоцируемые аллергенами или неспецифическими стимулами - холодным и влажным воздухом, физической нагрузкой, различными запахами, плачем, смехом или вирусной инфекцией, а также сезонная вариабельность симптомов и наличие атопических заболеваний у больного или его родственников.
2 Клиническое обследование. Поскольку симптомы астмы меняются в течение дня, при физикальном обследовании врач может и не выявить характерных признаков болезни. При обострении бронхиальной астмы вероятность клинических проявлений, таких, как одышка, раздутие крыльев носа при вдохе, прерывистая речь, возбуждение, включение вспомогательной дыхательной мускулатуры, положение ортопноэ, постоянный или прерывающийся кашель, достаточно высока. Аускультативно врач чаще всего выслушивает сухие хрипы. Однако необходимо помнить, что у некоторых больных даже в период обострения при аускультации хрипы могут не выслушиваться, в то время как с помощью объективных исследований будет зарегистрирована значительная бронхообструкция, вероятно, за счет преобладающего вовлечения в процесс мелких дыхательных путей.
3. Исследование функции внешнего дыхания значительно облегчает постановку диагноза. Измерение функции внешнего дыхания обеспечивает объективную оценку бронхообструкции, а измерение ее колебаний -непрямую оценку гиперреактивности дыхательных путей. Существует широкий диапазон различных методов для оценки степени бронхиальной обструкции, но наиболее широкое применение получили измерение объема форсированного выдоха за 1 секунду (ОФВ1) и связанное с ним измерение форсированной жизненной емкости легких (ФЖЕЛ), а также измерение форсированной (пиковой) скорости выдоха (ПСВ). Важным диагностическим критерием является значительное увеличение офв) (более 12%) и ПСВ (более 15%) после ингаляции бета-2-агонистов короткого действия.
Пикфлоуметрия - наиболее важное нововведение в диагностике и контроле бронхиальной астмы.
4. Оценка аллергологического статуса. Наряду с оценкой симптомов, анамнеза, физикальных данных и показателей функции внешнего дыхания для постановки диагноза имеет большое значение изучение аллергологического статуса. Наиболее часто используются скарификационные, внутрикожные и уколочные (прик-тест) тесты. Однако в ряде случаев кожные тесты приводят к ложнонегативным или ложнопозитивным результатам. Поэтому часто проводится исследование специфических IgE-антител в сыворотке крови.
5. С целью дифференциальной диагностики необходимы: рентгенография легких, ЭКГ, клинический анализ крови, мокроты.
Вариабельность – это колебания выраженности симптомов и показателей функции легких в течение определенного времени (одних суток, нескольких дней, месяцев или в зависимости от сезона).
Обратимость – это быстрое увеличение ОФВ1 (или ПСВ), выявляемое через несколько минут после ингаляции бронходилататора быстрого действия (например, 200-400 мкг сальбутамола).
12. Тэла. Причины. Критерии постановки диагноза. Неотложная помощь. Принципы лечения.
I 26
ТЭЛА — окклюзия ствола или ветвей легочной артерии частичками тромба, сформировавшимися в венах большого круга кровообращения или правых камерах сердца и занесенными в легочную артерию с током крови.
Причины
тромбоз глубоких вен голени (в 70 – 90% случаев), часто сопровождающийся тромбофлебитом.
тромбоз нижней полой вены и ее притоков
сердечно-сосудистые заболевания, предрасполагающие к появлению тромбов и эмболий в легочной артерии (ИБС, активная фаза ревматизма с наличием митрального стеноза и мерцательной аритмии, гипертоническая болезнь, инфекционный эндокардит, кардиомиопатии и неревматические миокардиты)
септический генерализованный процесс
онкологические заболевания (чаще рак поджелудочной железы, желудка, легких)
тромбофилия (повышенное внутрисосудистое тромбообразование при нарушении системы регуляции гемостаза)
антифосфолипидный синдром — образование антител к фосфолипидам тромбоцитов, клеток эндотелия и нервной ткани (аутоиммунные реакции); проявляется повышенной склонностью к тромбозам различных локализаций.
Критерии постановки диагноза
Признак |
Количество баллов |
Клинические симптомы тромбоза глубоких вен нижних конечностей (как минимум, их отечность и болезненность при пальпации по ходу глубоких вен) |
3 |
При проведении дифференциального диагноза ТЭЛА наиболее вероятна |
3 |
Тахикардия |
1,5 |
Иммобилизация или хирургическое вмешательство на протяжении последних 3-х дней |
1,5 |
Тромбоз глубоких вен нижних конечностей или ТЭЛА в анамнезе |
1,5 |
Кровохарканье |
1 |
Онкопроцесс в настоящее время или давностью до 6 месяцев |
1 |
Если сумма не превышает 2 балла вероятность ТЭЛА низкая; при сумме баллов 2-6 – умеренная; при сумме более 6 баллов – высокая.
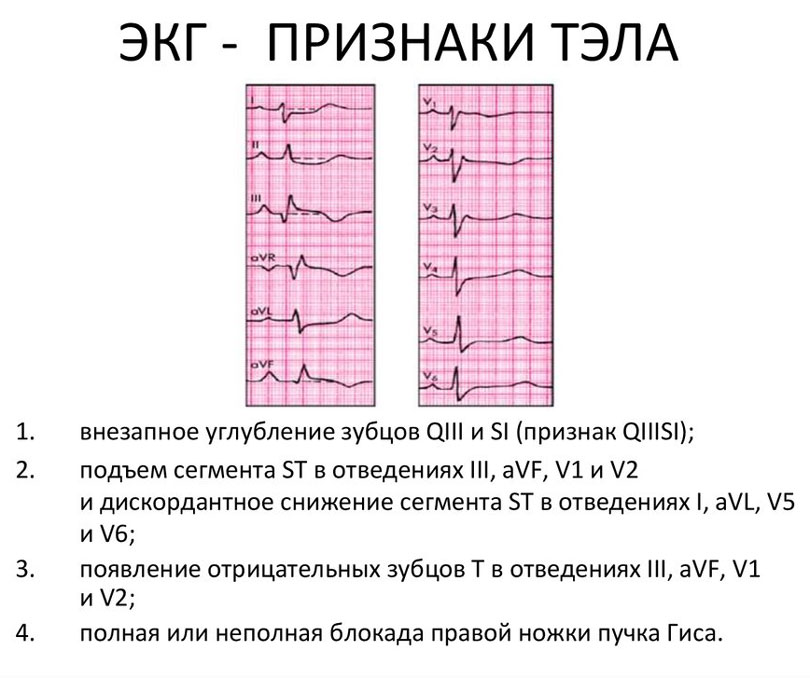
Неотложная помощь
■ При потере сознания, остановке кровообращения и/или дыхания проводят сердечно-лёгочную реанимацию.
■ Коррекция гипоксии — оксигенотерапия.
■ Купирование болевого синдрома.
При выраженном болевом синдроме показаны наркотические анальгетики, которые также снижают давление в малом круге кровообращения и уменьшают одышку:
■ морфин 1% — 1 мл развести раствором 0,9% натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводить в/в дробно по 4—10 мл (или 2—5 мг) каждые 5—15 мин до устранения болевого синдрома и одышки, либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты).
При инфарктной пневмонии, когда боль в грудной клетке связана с дыханием, кашлем, положением тела, применяют ненаркотические анальгетики:
■ кеторолак в/в 30 мг (1 мл), дозу необходимо вводить не менее чем за 15 с (при в/м введении анальгетический эффект развивается через 30 мин).
При подозрении на ТЭЛА во всех случаях начинают антикоагулянтную терапию:
■ гепарин натрия в/в болюсом 5000 ME. Гепарин натрия не растворяет тромб, но приостанавливает тромботический процесс и препятствует нарастанию тромба дистальнее и проксимальнее эмбола.
■ Допамин вводят только в/в капельно 100—250 мкг/мин (1,5—3,5 мкг/кг/мин).
Приготовление раствора непосредственно перед инфузией: 400 мг допамина добавляют к 250 мл 0,9% р-ра хлорида натрия (образуется прозрачный и бесцветный раствор с концентрацией 1600 мкг/мл). Начало терапевтического эффекта при в/в введении в течение 5 мин, продолжительность — 10 мин.
■ Инфузионную терапию не проводят в связи с опасностью нарастания дилатации правого желудочка и снижения сердечного выброса.
При развитии бронхоспазма:
■ Сальбутамол 2,5 мг через небулайзер в течение 5—10 мин. При неудовлетворенном эффекте через 20 мин ингаляцию повторить
■ Аминофиллин (эуфиллин*) 2,4% — 5 мл в/в медленно. Снижает общее периферическое сосудистое сопротивление и давление в малом круге кровообращения, повышает чувствительность дыхательного центра к стимулирующему влиянию углекислого газа.
Принципы лечения
Основой лечения пациента с высоким риском является тромболизис или эмболэктомия в сочетании с антикоагулянтной терапией. Пациентам без высокого риска реперфузию не проводят, важнейшим элементом терапии являются антикоагулянты.
Пациенту, поступающему в состоянии гипотензии/шока, обеспечивается адекватная инотропная и респираторная поддержка.
При подозрении на ТЭЛА, еще до получения окончательного подтверждения диагноза, пациенту назначают антикоагулянтную терапию. Препарат выбора при массивной ТЭЛА – нефракционированный гепарин (НФГ). Вводится болюс 80 ЕД/кг (или 10 000 ЕД), а затем проводится инфузия 18 ЕД/кг/ч (800–1250 ЕД/ч) до целевого значения активированного частичного тромбопластинового времени (АЧТВ) 1,5–2,3 от верхней границы нормы (46–70 с) с коррекцией инфузии по соответствующим таблицам. Варфарин назначают с первых суток лечения. Длительность терапии НФГ – не менее 5 сут, его отменяют, когда целевое международное нормализованное отношение (МНО) сохраняется в течение 2 дней на уровне > 2,0.
Одновременно в отсутствие противопоказаний (табл. 6) начинают процедуру тромболизиса, которая приводит к клиническому и/или эхокардиографическому улучшению у 92% пациентов.
Временное «окно» для проведения тромболизиса при ТЭЛА значительно больше, чем при инфаркте миокарда: оптимальные сроки – до 48 ч, а целесообразность тромболизиса сохраняется до 5 суток от развития заболевания.
При ТЭЛА высокого риска и абсолютных противопоказаниях к тромболизису, при неудаче тромболизиса (гипотензия без эффекта от терапии > 1 ч), шоке и риске смерти до наступления эффекта тромболитической терапии рекомендуют чрескожную катетерную или хирургическую эмболэктомию.
13. Обострение хобл. Клинические проявления. Критерии тяжелого обострения. Вопросы неотложной помощи. Тактика ведения. Профилактика.
J 44. Обострение ХОБЛ — это острое событие, характеризующееся ухудшением респираторных симптомов, которое выходит за рамки их обычных ежедневных колебаний и приводит к изменению режима используемой терапии.
Клиника
- появление или усиление одышки;
- увеличение объема отделяемой мокроты;
- увеличение гнойности мокроты.
При наличии всех трех признаков (усиление одышки, увеличение объема мокроты, появление гнойной мокроты) диагностируется обострение I типа, каких-либо двух признаков — II типа, если имеется только один — III типа.
Спустя несколько часов или дней на первый план выходят клинические признаки обострения ХОБЛ: пациента начинает беспокоить стеснение в грудной клетке, резко усиливается кашель, появляется свистящее дыхание, отходит желтая либо желто-зеленая мокрота, нарастает одышка, слабость.
При тяжелом обострении могут развиваться выраженные гипоксемия и гиперкапния (как проявления острой дыхательной недостаточности), нарастает тахипноэ, появляется диффузный цианоз, спутанность сознания. При сопутствующем поражении сердца (ИБС, хроническое легочное сердце) может нарушаться сердечный ритм, появляются или усугубляются симптомы правожелудочковой недостаточности (боли в правом подреберье вследствие увеличения печени, отеки на нижних конечностях, асцит).
Классификация тяжести обострений ХОБЛ
Легкая – пациенту необходимо увеличение объема проводимой терапии, которое может быть осуществлено собственными силами больного.
Средняя - пациенту необходимо увеличение объема проводимой терапии (назначение антибиотиков и/или системных глюкокортикостеродов), которое требует консультации больного врачом.
Тяжелая - пациент/врач отмечают явное и/или быстрое ухудшение состояния больного, требуется госпитализация больного.
Неотложная помощь
Препаратами выбора являются ДАИ – дозированные аэрозольные ингаляторы. 2-4 дозы Сальбутамола или Беродуала. В зависимости от тяжести состояния ингаляции повторяют через каждые 20-30 мин или переходят на поддерживающую терапию по 1-2 ингалации 2-3 раза в сутки.
Применение глюкокортикоидов. Преднизолон 20мг — перорально или дексаметазон 4-20мг (1-5мл) в/в медленно или в/м.
Эуфилин 2% 5-10мл + 10-20мл изотонический р-р медленно внутривенно или капельно.
Килородотерапия и неинвазивная вентиляция легких.
При бактериальной этиологии болезни назначается антибиотикотерапия.
Тактика ведения
1. Бронходилататоры короткого действия, желательно через небулайзер (сальбутамол 200 мкг 4 р/сут или беротек 200 мкг 4 р/сут). Возможно добавление к схеме лечения антихолинергических препаратов (атровент 80 мкг 4 р/сут).
2. Глюкокортикостероиды. При нетяжелом обострении и амбулаторном лечении могут быть назначены как ингаляционно (будесонид 6–8 мг/сут через небулайзер), так и per os (преднизолон 40 мг/сут в течение 5 дней).
3. Антибактериальные препараты. При нетяжелом обострении без признаков бронхиальной инфекции не всегда показаны. Если есть признаки бактериального воспаления бронхиального дерева, но состояние пациента стабильно, данные препараты можно назначать внутрь. У пациентов в тяжелом состоянии антибактериальная терапия проводится только парентерально. Могут использоваться препараты разных групп:
1) защищенные пенициллины — амоксициллин + клавулановая кислота (амоксиклав и др.) 1,2 г 2 р/сут внутрь или в/венно;
2) макролиды — азитромицин по 0,5 г 1 р/сут, кларитромицин по 0,5 г 2 р/сут;
3) цефалоспорины — цефуроксим 0,5 — 1,5 г 3 р/сут в/мышечно или в/венно; 4) респираторные фторхинолоны — моксифлоксацин 0,4 г 1 р/сут, левофлоксацин 0,25–0,5 г 2 р/сут, внутрь или в/венно.
4. Респираторная поддержка. При тяжелой одышке, участии в акте дыхания вспомогательной дыхательной мускулатуры, тахипноэ свыше 25 дыхательных движений в минуту, нарастающем ацидозе, гипоксии, гиперкапнии пациентам может потребоваться неинвазивная вентиляция легких. Она проводится при помощи маски. При недостаточной эффективности проводится искусственная вентиляция легких.
Профилактика
Цель вторичной профилактики — предотвращение обострений у пациентов с ХОБЛ. Отказ от курения жизненно необходим пациентам, так как скорость снижения функции легких напрямую зависит от статуса курения. Вакцинация противогриппозной и поливалентной пневмококковой вакциной снижает частоту обострений, связанных с сезонным подъемом заболеваемости респираторными инфекциями.
14. Заболевания плевры. Вопросы дифференциальной диагностики. Тактика ведения.
Плевральный выпот
Плевральные выпоты традиционно подразделяются на транссудаты (общий белок < 30 г/л) и экссудаты (общий белок > 30 г/л). В промежуточных случаях (а именно, когда содержание протеина составляет 25–35 г/л) разграничить экссудат и транссудат помогает определение содержания в плевральной жидкости лактатдегидрогеназы (ЛДГ) и градиента альбумина между сывороткой и плевральной жидкостью.
Их дифференциация важна потому, что «низкобелковые» выпоты (транссудаты) не требуют дальнейших диагностических мероприятий; необходимо лишь лечение вызвавшей их патологии, в то время как при обнаружении плеврального экссудата, безусловно, нужна дополнительная диагностика.
При физикальном обследовании обнаруживается ограничение дыхательных движений грудной клетки, «каменная» тупость при перкуссии, приглушение дыхания при аускультации и часто — зона бронхиального дыхания сверху от уровня жидкости.
Плеврит
Воспаление париетальной и висцеральной плевры, сопровождающееся накоплением серозного или гнойного экссудата в плевральной полости, принято называть экссудативным плевритом. Плеврит следует рассматривать как патологическое состояние плевры, осложняющее процессы в легком (инфаркт легкого, пневмония, кровоизлияние в плевральную полость в результате травмы, карциноматоз плевры при раке легких, мезотелиомы плевры, метастазов из других органов) и в поддиафрагмальном пространстве (при остром панкреатите в результате проникновения в плевральную полость агрессивных ферментов поджелудочной железы, а также при гнойных процессах в поддиафрагмальном пространстве).
Эмпиема плевры
Эмпиема плевры и различные формы экссудативных плевритов фактически являются осложнением других заболеваний (гнойные заболевания легких и органов брюшной полости). Почти у 90 % больных эмпиема плевры возникает в связи с воспалительными процессами в легких (на фоне острой пневмонии 5 %, абсцесса легкого 9— 11 %, при гангрене легкого 80—95 %). Бурное развитие эмпиемы наблюдается при прорыве в плевральную полость абсцесса или гангрены легкого.
Опухоли плевры
Доброкачественные и злокачественные опухоли исходят либо из соединительнотканной пластинки плевры (мезенхимомы), из мезотелия (мезотелиомы) или из тканей грудной стенки (фибромы, хондромы, остеомы, нейриномы, ангиомы, саркомы и др.). Опухоли, исходящие из тканей грудной клетки, не отличаются от аналогичных опухолей, возникающих в других областях тела. В процессе роста они распространяются в плевральную полость.
Дифференциальная диагностика
Весьма полезным в дифференциальной диагностике плевритов является исследование глюкозы плеврального содержимого. Низкое содержание (менее 3,33 ммоль/л) характерно для туберкулеза, опухолевого поражения, ревматического и парапневмонического плеврита.
При других вариантах плевритов содержание глюкозы в экссудате обычно равно таковому в сыворотке крови. При уровне глюкозы менее 2,22 ммоль/л у больных с парапневмоническим плевритом весьма высока вероятность формирования эмпиемы, а при эмпиеме глюкоза в плевральном содержимом обычно отсутствует.
Интенсивность воспаления в плевральной полости обычно коррелирует с повышением лактатдегидрогеназы (ЛДГ). Наряду с ЛДГ по специальным показаниям в экссудате можно определять и другие маркеры воспаления: металлопротеазы, интерлейкины. Иммунологическое исследование плеврального содержимого направлено на обнаружение либо этиологически значимых агентов (антигены), либо следов их пребывания (антитела). Для этой цели используются иммуноферментный анализ и ПЦР. Бактериологическое исследование плеврального содержимого дает максимальную информацию при инфекционной природе плевритов.
Тактика ведения
Верхняя граница выпота определяется перкуторно, при рентгенографии легких или при помощи УЗИ плевральной полости.
При проведении плевральной пункции получают жидкость, характер и объем которой зависит от причины плеврита. Цитологическое и бактериологическое исследование плеврального экссудата позволяет выяснить этиологию плеврита. Плевральный выпот характеризуется относительной плотностью выше 1018-1020, многообразием клеточных элементов, положительной реакцией Ривольта.
В крови определяются повышение СОЭ, нейтрофильный лейкоцитоз, увеличение значений серомукоидов, сиаловых кислот, фибрина. Для уточнения причины плеврита проводится торакоскопия с биопсией плевры.
Врачебные мероприятия при плеврите направлены на устранение этиологического фактора и облегчение симптоматики. При плевритах, вызванных пневмонией, назначается антибиотикотерапия. Ревматические плевриты лечатся нестероидными противовоспалительными препаратами, глюкокортикостероидами. При туберкулезных плевритах лечение проводится фтизиатром и заключается в специфической терапии рифампицином, изониазидом и стрептомицином на протяжении нескольких месяцев.
С симптоматической целью показано назначение анальгетиков, мочегонных, сердечно-сосудистых средств, после рассасывания выпота - физиотерапии и лечебной физкультуры.
При экссудативном плеврите с большим количеством выпота прибегают к его эвакуации путем проведения плевральной пункции или дренирования. Одномоментно рекомендуется эвакуировать не более 1-1,5 л экссудата во избежание сердечно-сосудистых осложнений (вследствие резкого расправления легкого и обратного смещения средостения). При гнойных плевритах проводится промывание плевральной полости антисептическими растворами. По показаниям внутриплеврально вводятся антибиотики, ферменты, гидрокортизон и т. д.
С целью лечения рецидивирующих экссудативных плевритов проводят плевродез (введение в плевральную полость талька или химиопрепаратов для склеивания листков плевры). Для лечения хронического гнойного плеврита прибегают к хирургическому вмешательству – плеврэктомии с декорткацией легкого. При развитии плеврита в результате неоперабельного поражения плевры или легкого злокачественной опухолью по показаниям проводят паллиативную плеврэктомию.
15. Дифференциальная диагностика и принципы лечения интерстициальных заболеваний легких.
Интерстициальные заболевания легких (ИЗЛ) или диффузные паренхиматозные заболевания легких (ДПЗЛ) – гетерогенная группа заболеваний и патологических состояний известной и неизвестной природы, характеризующаяся распространенным, как правило, двусторонним поражением респираторных отделов легких (альвеол, респираторных бронхиол)
1. С установленной этиологией:
лекарственные, лучевые, токсические ИБЛ
пневмомикозы, ассоциированные с ВИЧ-инфекций
ИБЛ на фоне коллагенозов (склеродермии, дерматомиозита, ревматоидного артрита, СКВ) и пневмокониозов (асбестоза, силикоза, бериллиоза)
ИБЛ на фоне инфекций (атипичной пневмонии, диссеминированного туберкулеза легких, пневмоцистной пневмонии и пр.)
ИБЛ на фоне экзогенного аллергического альвеолита
2. Идиопатические интерстициальные пневмонии:
неспецифическая, десвамативная, острая, лимфоидная, криптогенная организующаяся
идиопатический легочный фиброз
3. Гранулематозные:
ИБЛ на фоне саркоидоза, гранулематоза Вегенера, гемосидероза легких, экзогенного аллергического альвеолита
4. Ассоциированные с другими заболеваниями:
патологией печени (хроническим гепатитом, первичным билиарным циррозом печени), кишечника (НЯК, болезнь Крона), ХПН
наследственными заболеваниями (нейрофиброматозом)
злокачественными опухолями
5. Прочие:
ассоциированные с гистиоцитозом Х, лимфангиолейомиоматозом, легочным протеинозом, первичным амилоидозом легких.
Общая симптоматика может включать лихорадку, недомогание и быструю утомляемость, потерю массы тела. Одышка: вначале она возникает или усиливается только при нагрузке, затем становится постоянной и прогрессирующей. Одышка обычно носит инспираторный характер и сопровождается свистящими хрипами, что может быть ошибочно принято за бронхиальную астму. Непродуктивный кашель – сухой или со скудной слизистой мокротой. К более поздним признакам ИБЛ относятся цианоз и формирование «пальцев Гиппократа». С большой частотой встречаются деформации грудной клетки. При тяжелых формах развивается легочно-сердечная недостаточность.
Диагностика интерстициальных болезней легких
При осмотре - тахипноэ, несоответствие выраженности одышки физикальным изменениям в легких. аускультация - на вдохе прослушиваются крепитирующие хрипы различной локализации. В крови – умеренный лейкоцитоз и повышение СОЭ; по данным ИФА – отрицательные серологические тесты на наличие Ат к микоплазме, легионеллам, риккетсиям. Проводится анализ газового состава крови и КЩС (артериальная гипоксемия на ранних этапах сменяется гиперкапнией в терминальной стадии).
Рентгенологические методы (рентгенография и КТ легких). На ранних стадиях на рентгено- и томограммах можно увидеть деформацию и усиление легочного рисунка, мелкоочаговые тени, снижение прозрачности легочных полей ( феномен «матового стекла»); в дальнейшем развивается рентгенологическая картина интерстициального фиброза и картина «сотового легкого».
По данным спирометрии чаще обнаруживается рестриктивный тип нарушений легочной вентиляции, снижение легочных объемов. При развитии легочной гипертензии на ЭКГ обнаруживается гипертрофия миокарда правых отделов сердца. Диагностическая бронхоскопия позволяет провести бронхоальвеолярный лаваж; при ИБЛ в промывных вод бронхов преобладают нейтрофилы. Кроме этого, в ходе эндоскопического исследования может быть выполнена трансбронхиальная биопсия легких. Также в отдельных случаях прибегают к открытой или трансторакальной биопсии легочной ткани.
Л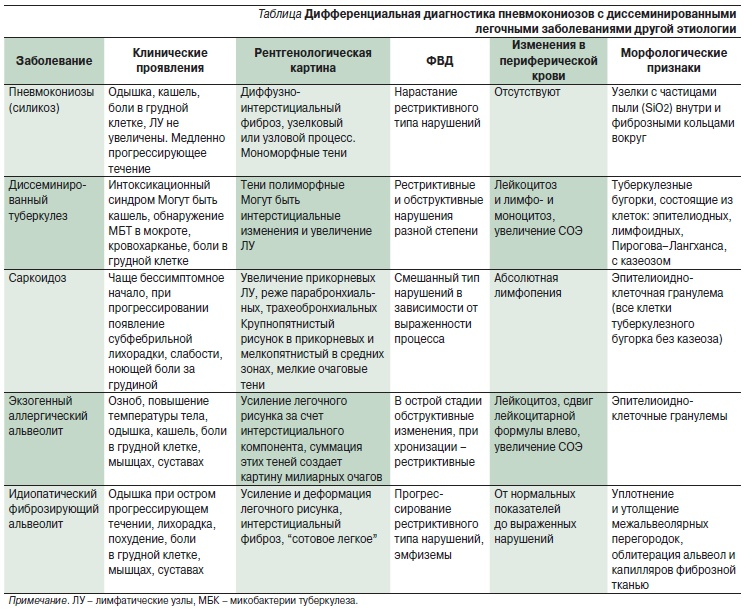 ечение
и прогноз интерстициальных болезней
легких
ечение
и прогноз интерстициальных болезней
легких
Первым шагом в лечении ИБЛ должен стать отказ от курения, взаимодействия с вредными производственными факторами, токсическими лекарственными препаратами. Вся последующая терапия проводится параллельно с лечением основного заболевания.
В большинстве случаев препаратами первой линии при интерстициальных болезнях легких являются кортикостероиды (преднизолон), которые в течение 1–3 мес. назначаются в высоких дозировках с последующим переходом на поддерживающую дозу. При отсутствии положительной динамики в течение года назначаются цитостатики (циклофосфамид, азатиоприн, хлорамбуцил). Из других фармпрепаратов используются бронходилататоры (внутрь и в виде ингаляций), однако они эффективны только на стадии обратимой бронхиальной обструкции. При артериальной гипоксемии (РаО2 кислородотерапия. В случае тяжелого течения интерстициальной болезни легких единственно эффективным методом может стать пересадка легкого.
Исходами ИБЛ могут быть улучшение, стабилизация состояния, прогрессирование легочного фиброза, летальный исход, реже – спонтанный регресс изменений (например, при неспецифической интерстициальной пневмонии). Средняя продолжительность жизни пациентов колеблется от 1 года при болезни Хаммана-Рича до 10 и более лет при респираторном бронхиолите. Профилактика интерстициальных болезней легких возможна только в случае известной этиологии.
16.Вопросы диагностики легочной артериальной гипертонии, связанной с хроническими заболеваниями легких. Принципы леченияя.
это группа заболеваний, характеризующихся прогрессирующим повышением легочного сосудистого сопротивления и давления в легочной артерии (ДЛА), которое приводит к развитию правожелудочковой сердечной недостаточности и преждевременной гибели пациентов
Клиническая классификация легочной гипертензии
1. Легочная артериальная гипертензия: 1.1.Идиопатическая (ИЛГ) 1.2.Наследуемая (мутации BMPR2, другие) 1.3.Индуцированная приемом лекарств и токсинов 1.4.Ассоциированная с: системными заболеваниями соединительной ткани, ВИЧ-инфекцией, портальной гипертензией, врожденными пороками сердца (системно-легочные шунты), шистосомозом 1". Легочная вено-окклюзионная болезнь/ легочный капиллярный гемангиоматоз (спорадическая, наследуемая (мутация EIF2AK4), индуцированная приемом лекарств/токсинов, ассоциированная (СЗСТ, ВИЧ-инфекцией) |
2. Легочная гипертензия вследствие патологии левых отделов сердца: 2.1. Систолическая дисфункция 2.2. Диастолическая дисфункция 2.3. Клапанные пороки 2.4. Врожденная/ приобретенная обструкция приносящего/выносящего тракта левого желудочка 2.5. Врожденный или приобретенный стеноз легочных вен |
3. Легочная гипертензия вследствие заболеваний легких и/или гипоксемии: 3.1. Хроническая обструктивная болезнь легких 3.2. Интерстициальные заболевания легких 3.3.Другие заболевания легких со смешанными рестриктивными и обструктивными нарушениями 3.4. Нарушения дыхания во время сна 3.5. Синдром альвеолярной гиповентиляции 3.6. Высокогорная ЛГ 3.7. Аномалии развития легких |
4. Хроническая тромбоэмболическая легочная гипертензия: 4.1. Хроническая тромбоэмболия в систему легочной артерии 4.2. Другие обструкции легочной артерии (ангиосаркома, другие внутрисосудистые опухоли, артериит, врожденные аномалии, паразитарные заболевания) |
5. ЛГ неизвестного или смешанного генеза: 5.1. Гематологические заболевания (хроническая гемолитическая анемия, миелопролиферативные заболевания, спленэктомия) 5.2. Системные нарушения (саркоидоз, легочный гистиоцитоз, лимфангиолейомиоматоз, нейрофиброматоз, васкулиты) 5.3. Метаболические нарушения (гликогенозы, болезнь Гоше, дисфункция щитовидной железы) 5.4. Другие (опухолевая обструкция, фиброзирующий медиастинит, хроническая почечная недостаточность, сегментарная ЛГ) |
Диагностика
Обычно пациенты, не знающие о своем заболевании, обращаются к врачу с жалобами на одышку. При осмотре пациента выявляется цианоз, а при длительном течении легочной гипертензии – деформация дистальных фаланг пальцев в форме «барабанных палочек», а ногтей — в виде «часовых стеклышек». При аускультации сердца определяется акцент II тона и его расщепление в проекции легочной артерии, при перкуссии - расширение границ легочной артерии.
ЭКГ - для выявления гипертрофии правых отделов сердца.
Эхокардиографию – для осмотра сосудов и полостей сердца, определения скорости кровотока в системе легочной артерии.
Компьютерную томографию – послойные снимки органов грудной клетки показывают увеличенные легочные артерии, а также сопутствующие легочной гипертензии заболевания сердца и легких.
Рентгенографию легких - определяет выбухание главного ствола легочной артерии, расширение ее главных ветвей и сужение более мелких сосудов, позволяет косвенно подтвердить наличие легочной гипертензии при выявлении других заболеваний легких и сердца.
Катетеризацию легочной артерии и правых отделов сердца – проводится с целью определения кровяного давления в легочной артерии. Является самым достоверным методом диагностики легочной гипертензии. Через прокол в яремной вене зонд подводится к правым отделам сердца и с помощью монитора давления на зонде определяется кровяное давление в правом желудочке и легочных артериях. Катетеризация сердца является малоинвазивной методикой, практически не сопряженной с риском осложнений.
Ангиопульмонографию – рентгенконтрастное исследование сосудов легких с целью определения сосудистого рисунка в системе легочной артерии и сосудистого кровотока. Проводится в условиях специально оснащенной рентгеноперационной с соблюдением мер предосторожности, т. к. введение контрастного вещества может спровоцировать легочно-гипертонический криз.
Лечение легочной гипертензии
Основными целями в лечении легочной гипертензии являются: устранение ее причины, понижение кровяного давления в легочной артерии и предотвращение тромбообразования в легочных сосудах. В комплекс лечения пациентов с легочной гипертензией входит:
Прием вазодилатирующих средств, расслабляющих гладкомышечный слой сосудов (празозин, гидралазин, нифедипин). Вазодилататоры эффективны на ранних стадиях развития легочной гипертензии до возникновения выраженных изменений артериол, их окклюзий и облитераций. В этой связи важное значение приобретает ранняя диагностика заболевания и установление этиологии легочной гипертензии.
Прием дезагрегантов и антикоагулянтов непрямого действия, снижающих вязкость крови (ацетил-салициловой кислоты, дипиридамола и др.). При выраженном сгущении крови прибегают к кровопусканию. Оптимальным у пациентов с легочной гипертензий считается уровень гемоглобина крови до 170 г/л.
Ингаляции кислорода как симптоматическую терапию при выраженной одышке и гипоксии.
Прием мочегонных препаратов при легочной гипертензии, осложненной правожелудочковой недостаточностью.
Трансплантация сердца и легких в крайне тяжелых случаях легочной гипертензии. Опыт подобных операций пока невелик, но свидетельствует об эффективности данной методики.
17. Бронхиальная астма. Фенотипы заболевания. Диагностические и лечебные алгоритмы.
Смотри вопрос 6,11
18. Хобл. Этиология. Критерии постановки диагноза. Алгоритмы лечения.
Смотри вопрос 5
19. Антибактериальная терапия внебольничной пневмонии. Выбор на амбулаторном этапе, при лечении в стационаре и отделении интенсивной терапии.
Антибактериальная терапия Препараты выбора:
Амоксициллин/клавуланат в/в + макролид в/в
Цефотаксим в/в+ макролид в/в
Цефтриаксон в/в+ макролид в/в
ЦЕФТАРОЛИН (ЗИНФОРО) 600 мг в/в капельно + макролид в/в
Респираторные фторхинолоны (левофлоксацин, моксифлоксацин) в/в
+ ЦЕФТАРОЛИН (ЗИНФОРО) 600 мг в/в капельно
Всем пациентам с ТВП рекомендуется эмпирическое назначение противовирусных препаратов при наличии клинических/эпидемиологических данных, предполагающих вероятное инфицирование вирусами гриппа
Больным с внебольничной пневмонией легкого течения антибактериальную терапию можно проводить в амбулаторных условиях. Оптимальными являются препараты, которые можно применять 1–2 раза в сутки. Пациент с внебольничной пневмонии тяжелого течения подлежит госпитализации; обычно назначают бета-лактамные антибиотики (амоксициллин/клавуланат, карбапенемы, цефалоспорины III-IV поколений) в сочетании с макролидами или любым фторхинолоном (офлоксацин, ципрофлоксацин). При тяжелом течении пневмонии антибактериальные препараты следует применять внутривенно, по крайней мере, до получения клинического эффекта.
При нетяжелой внебольничной пневмонии антибактериальная терапия может быть завершена по достижении стойкой нормализации температуры тела (в течение 3–4 дней). При таком подходе длительность лечения обычно составляет 7–10 дней. При тяжелой внебольничной пневмонии неуточненной этиологии рекомендован 10-дневный курс антибактериальной терапии. В эти же сроки обычно наблюдается исчезновение лейкоцитоза. В случае наличия клинических и/или эпидемиологических данных о микоплазменной или хламидийной этиологии внебольничной пневмонии продолжительность терапии должна составлять 14 дней. Более длительные курсы антибактериальной терапии показаны при внебольничной пневмонии стафилококковой этиологии или внебольничной пневмонии, вызванной грамотрицательными энтеробактериями, – от 14 до 21 дня. При указании на легионеллезную пневмонию длительность антибактериальной терапии составляет 21 день.
20. Пневмония тяжелого течения. Критерии постановки диагноза. Врачебная тактика.
Смотри вопрос 19
Критерии тяжелого течения пневмонии
1. Общее состояние больного:
- цианоз,
- спутанное сознание, бред,
- температура тела выше 39.
2. Дыхательная недостаточность:
- выраженная одышка (более 30/мин и более),
- парциальное давление кислорода менее 60 мм.рт.ст., при спонтанном дыхании ( насыщение менее 90%).
3. Сердечно-сосудистая недостаточность:
- тахикардия, не соответствующая степени выраженности лихорадки,
- артериальная гипотензия (АД систолическое ниже 100 мм.рт.ст., диастолическое ниже 60 мм рт.ст.).
4. Результаты инструментальных и лабораторных исследований:
- гиперлейкоцитоз свыше 25х109 или лейкопения менее 4х109,
- рентгенография: двусторонняя или многодолевая пневмония, плевральный выпот,
- повышения уровня креатинина и трансаминаз в несколько раз по отношению к норме.
При поступлении больного пневмонией в стационар необходимо прежде всего оценить тяжесть состояния пациента и решить вопрос о месте его лечения (терапевтическое отделение или отделение реанимации, интенсивной терапии).
Тяжелая внебольничная пневмония – это особая форма заболевания различной этиологии, проявляющаяся выраженной дыхательной недостаточностью и/или признаками тяжелого сепсиса или септического шока, характеризующаяся плохим прогнозом и требующая проведения интенсивной терапии.
Выделение больных с тяжелым течением пневмонии в отдельную группу представляется крайне важным, учитывая высокий уровень летальности, нередко наличие у пациентов тяжелой сопутствующей патологии, особенности этиологии заболевания и особые требования к антибактериальной терапии. При наличии клинических или лабораторных признаков тяжелого течения или симптомов тяжелого сепсиса целесообразно проводить лечение пациента в отделении реанимации и интенсивной терапии.
20. Дыхательная недостаточность. Диагностические критерии. Врачебная тактика.
Острая дыхательная недостаточность (ОДН) – синдром, в основе которого лежат нарушения в системе внешнего дыхания, при которых не обеспечивается нормальный газовый состав артериальной крови или его поддержание на нормальном уровне достигается за счет чрезмерного функционального напряжения этой системы.
Этиология.
Различают легочные и внелегочные причины развития ОДН.
Внелегочные причины:
Нарушение центральной регуляции дыхания: а) острые сосудистые расстройства (острые нарушения мозгового кровообращения, отек головного мозга); б) травмы головного мозга; в) интоксикации лекарственными препаратами, действующими на дыхательный центр (наркотические препараты, барбитураты); г) инфекционные, воспалительные и опухолевые процессы, приводящие к поражению ствола головного мозга; д) коматозные состояния.
Поражение костно–мышечного аппарата грудной клетки и повреждение плевры: а) периферические и центральные параличи дыхательной мускулатуры; б) спонтанный пневмоторакс; в) дегенеративно-дистрофические изменения дыхательных мышц; г) полиомиелит, столбняк; д) травмы спинного мозга; е) последствия действия фосфорорганических соединений и миорелаксантов.
ОДН при нарушении транспорта кислорода при больших кровопотерях, острой недостаточности кровообращения и отравлениях (окисью углерода).
Легочные причины:
Обструктивные расстройства: а) закупорка дыхательных путей инородным телом, мокротой, рвотными массами; б) механическое препятствие доступу воздуха при сдавлении извне (повешение, удушение); в) аллергический ларинго - и бронхоспазм; г) опухолевые процессы дыхательных путей; д) нарушение акта глотания, паралич языка с его западением; е) отечно-воспалительные заболевания бронхиального дерева.
Рестриктивные расстройства: а) инфильтрация, деструкция, дистрофия легочной ткани; б) пневмосклероз.
Уменьшение функционирующей легочной паренхимы: а) недоразвитие легких; б) сдавление и ателектаз легкого; в) большое количество жидкости в плевральной полости; г) тромбоэмболия легочной артерии (ТЭЛА).
В клинике выделяют три стадии ОДН.
I стадия. Больной в сознании, беспокоен, может быть эйфоричен. Жалобы на ощущение нехватки воздуха. Кожные покровы бледные, влажные, легкий акроцианоз. Число дыханий (ЧД) – 25-30 в мин., число сердечных сокращений (ЧСС) - 100-110 уд/мин, АД в пределах нормы или немного повышено, Ра О2 70 мм рт ст., Ра СО2 35 мм рт ст. (гипокапния носит компенсаторный характер, как следствие одышки).
II стадия. Жалобы на сильнейшее удушье. Психомоторное возбуждение. Возможны бред, галлюцинации, потеря сознания. Кожные покровы цианотичные, иногда в сочетании с гиперемией, профузный пот. ЧД – 30 - 40 в мин., ЧСС - 120-140 уд/мин, артериальная гипертензия. Ра О2 уменьшается до 60 мм рт ст., Ра СО2 увеличивается до 50 мм рт ст.
III стадия. Сознание отсутствует. Судороги. Расширение зрачков с отсутствием их реакции на свет, пятнистый цианоз. Брадипное (ЧД – 8-10 в мин). Падение АД. ЧСС более 140уд/мин, аритмии. Ра О2 уменьшается до 50 мм рт ст., Ра СО2 увеличивается до 80 - 90 мм рт ст. и более.
Принципы интенсивной терапии ОДН.
Неотложная помощь:
Восстановление проходимости дыхательных путей: тройной прием (запрокидывание головы, открывание рта, выдвижение нижней челюсти), применение воздуховодов, интубация трахеи, коникотомия, трахеостомия.
Оксигенотерапия: кислородотерапию проводят с помощью носовых катетеров и масок, создающих определенную концентрацию кислорода во вдыхаемом воздухе. При использовании носовых канюль или катетеров поток кислорода от 1 до 6л/мин создает во вдыхаемом воздухе его концентрацию, равную 24 - 44% (в атмосферном воздухе – 21%). Кислородотерапия должна быть безопасной, контролируемой, легко управляемой. Кислород токсичен: дыхание чистым кислородом в течение 3-5 дней может привести к гибели. Высокие концентрации кислорода могут быть причиной РДСВ. Только при терминальных состояниях, апноэ, гипоксической коме, отравлениях окисью углерода (СО) применяют 100% кислород.
Если выбранный метод кислородотерапии неэффективен, то показана искусственная вентиляция легких (ИВЛ).
Абсолютные показания для проведения ИВЛ:
Ра О2 менее 50 мм рт ст.;
Ра СО2 более 60 мм рт ст.;
неэффективность дыхания (при нормальном или несколько повышенном Ра СО2 не достигается адекватное достижение артериальной крови кислородом).
Относительные показания для проведения ИВЛ:
черепно-мозговая травма с признаками ОДН;
отравления снотворными или седативными препаратами;
травмы грудной клетки;
астматический статус;
нарушения нейромышечной передачи;
патологические состояния, требующие мышечной релаксации (судорожный синдром, эпистатус, столбняк).
Комплексная интенсивная терапии:
Дренирование мокроты: постуральный дренаж, перкуссионный массаж, санационная бронхоскопия.
ИВЛ; гипербарическая оксигенация.
Терапия основного заболевания.
Гепаринотерапия: гепарин 10000тыс Ед. в/в болюсно, с последующей непрерывной инфузией 10-15 Ед./кг/час.
Снижение давления в малом круге кровообращения (спазмолитики, эуфиллин, нитроглицерин).
Симптоматическая терапия: коррекция кислотно-щелочного равновесия, обезболивание, инфузионная терапия, купирование коллапса.
22. Саркоидоз. Клинические проявления. Диагностика. Врачебная тактика.
Саркоидоз (болезнь Бенье-Бека-Шаумана) – системное доброкачественное заболевание не уточненной этиологии, характеризующееся развитием тканевых реакций продуктивного типа с формированием эпителиоидно-клеточных гранулем без казеоза с исходом в рассасывание или в интерстициальный фиброз.
Этиология: достоверно не определена, выявлена генетическая предрасположенность (HLA-А1, В8, В13) к болезни.
Патогенез: воздействие неизвестного этиологического фактора --> накопление в альвеолах и интерстиции легких активных альвеолярных макрофагов --> гиперпродукция ИЛ-1, активатора плазминогена, фибронектина и др. --> скопление лимфоцитов, моноцитов, фибробластов и их активация --> лимфоидно-макрофагальная инфильтрация легких --> альвеолит --> эпителиоидно-клеточные гранулемы (центральная часть – из эпителиодных и гигантских многоядерных клеток Пирогова-Лангханса, по периферии – лимфоциты, макрофаги, плазматические клетки, фибробласты) --> фиброзирование гранулем с развитием диффузного интерстициального фиброза легких.
Основные рентгенологические формы саркоидоза:
1. Саркоидоз внутригрудных л.у.
2. Саркоидоз внутригрудных л.у. и легких
3. Саркоидоз легких
4. Саркокидоз органов дыхания, комбинированный с поражением других органов
5. Генерализованный саркоидоз с поражением органов дыхания
Международная классификация саркоидоза:
стадия I – медиастинальная (лимфожелезистая) форма – двустороннее увеличение бронхопульмональных л.у., реже – л.у. других групп (трахеобронхиальных, паратрахеальных) до 3-5 см в диаметре с четкими полициклическими контурами; периаденит, изменения в легочной ткани, сдавление органов средостения отсутствуют
стадия II – медиастинально-легочная форма – сочетанное поражение внутригрудных л.у. и легочной ткани диффузно-интерстициального или очагового характера
стадия III – легочная форма – выраженные изменения в легочной ткани в виде густой диссеминации в средних отделах на фоне пневмосклероза и эмфиземы; при прогрессировании процесса эти изменения выявляются на всем протяжении легочной ткани
стадия IV – легочной фиброз с признаками «сотового легкого»
Клиническая картина саркоидоза:
- заболевают преимущественно женщины в возрасте 20-40 лет
- начало заболевания может быть бессимптомное (саркоидоз выявляется случайно при флюорографии), постепенное (жалобы на общую слабость, потливость ночью, сухой кашель, боли в межлопаточной области, прогрессирующая одышка), острое (кратковременное повышение температуры тела в течение 4-6 дней, мигрирующие боли в крупных суставах, одышка, боль в грудной клетке, сухой кашель, увеличенные, безболезненные, не спаянные с кожей периферические л.у., лимфаденопатия средостения, узловатая эритема в области бедер, голеней, разгибательной поверхности предплечья).
Острое начало может протекать в виде синдромов: 1) Лефгрена – лимфаденопатия средостения, повышение температуры тела, узловатая эритема, артралгия, увеличение СОЭ и 2) Хеерфордта-Вальденстрема – лимфаденопатия средостения, повышение температуры тела, паротит, передний увеит, парез лицевого нерва.
- наиболее характерно первично-хроническое течение заболевания (вначале поражаются легкие, затем другие органы; у ½ больных спонтанное выздоровление), реже – вторично-хроническое течение (развивается вследствие трансформации острого течения; прогноз неблагоприятный).
- поражение внутригрудных л.у. (увеличиваются чаще прикорневые бронхопульмональные, трахеобронхиальные, паратрахеальные л.у. > 1,5 см - лимфаденопатия средостения); увеличение периферических л.у. (чаще шейных и надключичных) – безболезненны, не спаяны между собой и с подлежащими тканями, плотноэластические, никогда не изъязвляются, не нагнаиваются, не распадаются и не образуют свищей
- поражение бронхопульмональной системы:
а) поражение легких - сухой или малопродуктивный с небольшим выделением слизистой мокроты кашель, боли в грудной клетке, прогрессирующая одышка; при развитии фиброза и эмфиземы легких значительно ослабевает везикулярное дыхание
б) поражение бронхов – малопродуктивный кашель, рассеянные сухие, реже мелкопузырчатые хрипы; при бронхоскопии – эктазии сосудов (патогномично для саркоидоза)
в) поражение плевры в виде сухого или экссудативного с большим количеством лимфоцитов в экссудате плеврита
- поражение органов пищеварения: увеличение и болезненность околоушной железы; поражение печени (ощущение тяжести в правом подреберье, сухость и горечь во рту, печень увеличена, плотная, поверхность гладкая)
- поражение селезенки вплоть до гиперспленизма с лейкопенией, тромбоцитопенией, гемолитической анемией
- поражения сердца - саркоидозная инфильтрация, гранулематоз и фиброз миокарда: одышка, боли в области сердца при физической нагрузке, сердцебиения, перебои, аритмии, расширение границы сердца влево, глухость тонов, систолический шум в области верхушки, признаки сердечной недостаточности
- поражение костно-суставной системы: неинтенсивные боли в костях (из-за остеопороза), обратимые асептические артриты крупных суставов, проявляющиеся преимущественно болями
- поражение нервной системы – периферическая нейропатия: снижение чувствительности в области голеней и стоп, снижение мышечной силы; саркоидозный менингит; поражение спинного мозга с развитием периферических параличей
- поражение кожи – узловатая эритема (болезненные красноватые узлы в подкожной клетчатке бедер, голеней, разгибательной поверхности предплечий с изменениями цвета кожи над ними от красного до желтовато-зеленого), гранулематозный саркоидоз кожи (мелко- или крупноочаговые эритематозные бляшки на коже тыльных поверхностей кистей, стоп, лица, в области старых рубцов), саркоид Дарье-Руссо (плотные безболезненные узлы 1-3 см в диаметре шарообразной формы в подкожной клетчатке, не сопровождающиеся изменениями кожи)
- поражения глаз в виде переднего и заднего увеитов, конъюнктивита, помутнения роговицы, катаракты, глаукомы и др.
Диагностика саркоидоза органов дыхания:
1. Лучевая диагностика (обзорная рентгенография и томография средостения в прямой и боковой проекциях):
а) внутригрудная аденопатия – двустороннее расширение средостения и корней легких за счет увеличения л.у., удлинение тени корней; на томограмме внутригрудные л.у. в виде крупных конгломератов с четкими контурами, округлой или овальной формы
б) диссеминация – наличие в легочной ткани рассеянных теней гранулем от милиарных до 0,7-1,0 см, более тесно расположенных у междолевой плевры, аксиллярных зонах
в) инфильтрация (пневмоническое поражение) – инфильтративные изменения за счет альвеолита, которые могут перекрывать тени легочного поля и гранулем
г) интерстициальные изменения – мелкосетчатая ситовидная деформация легочного рисунка с дальнейшим развитием в диффузный фиброз и эмфизему
2. Радиоизотопное сканирование легких с цитратом Ga-67 – накапливается в пораженных л.у., легких, др. пораженных органах
3. Фибробронхоскопия с биопсией – позволяет обнаружить специфические гранулемы без казеоза
4. Медиастиноскопия, торакоскопия или открытая биопсия легких – проводятся в случае, когда другими методами диагноз поставить не удалось
5. Лабораторные исследования и пробы:
а) ОАК: иногда эозинофилия, абсолютная лимфопения
б) БАК: определяется поражением внутренних органов; повышено содержание АПФ (уровень коррелирует с активностью процесса), лизоцима
в) иммунограмма: колебания активности натуральных киллеров, снижение фагоцитарной функции лейкоцитов, увеличение абсолютного количества В-лимфоцитов с гиперпродукцией ряда иммуноглобулинов, ЦИК.
г) проба Квейма: 0,15-0,2 мл стандартного саркоидозного АГ вводят в/к в область предплечья, через 3-4 недели место введения АГ иссекается (обязательно с подкожной клетчаткой) и исследуется гистологически; реакция положительна при развитии типичной саркоидозной гранулемы
д) проба Манту с 2 ТЕ ППД-Л: отрицательная
Дифференциальный диагноз: медиастинальная форма – с ТБ внутригрудных л.у., медиастинальной формой лимфогранулематоза, различными видами лимфом, лимфомой Кастлемана (ангиофолликулярной гиперплазией л.у.), иерсиниозом, фелинозом; легочно-медиастинальная форма – с диссеминированным ТБ острого и подострого течения, бронхоальвеолярных раком, легочно-медиастинальной формой лимфогранулематоза, гемосидерозом, гистиоцитозом Х, кониозом, экзогенным аллергическим альвеолитом, лимфогенным карциноматозом, лимфоматоидным гранулематозом; легочная форма – с идиопатическим фиброзирующим альвеолитом, поражением легких при системных заболеваниях соединительной ткани, васкулитах, микозами и др.
Лечение саркоидоза:
1. ГКС – показаны при: а) наличии внелегочных проявлений; б) ухудшении зрения; в) поражении миокарда; г) поражении ЦНС; д) прогрессирующем течении заболевания; е) рецидивах болезни с выраженными клиническими проявлениями и нарушениями функции внешнего дыхания; ж) гиперкальциемии, гиперкальциурии: начальная доза преднизолона 15-20 мг/сут, со 2-ого месяца терапии – снижение дозы до поддерживающей 5-10 мг/сут в течение 6-36 мес; возможна интермиттирующая терапия – 25-30 мг/сут преднизолона внутрь через день с постепенным снижением дозы на ¼ таблетки каждые 7 дней до 7,5 мг/сут к 6 мес. терапии; при поражении слизистой бронхов, бронхообструкции – ингаляционные ГКС (флутикозон, будесонид).
2. При неэффективности ГКС – цитостатики: метотрексат 10-25 мг/неделю, азатиоприн 100-150 мг/сут, циклофосфамид 50-150 мг/сут
3. При поражении кожных покровов, слизистой носа - «малые иммунодепрессанты»: делагил 750 мг/сут, плаквенил 200-400 мг/сут 5-6 мес
4. При неэффективности ГКС и наличии интерстициального фиброза – антифибротическая терапия: интерферон гамма 1 100 мг п/к ежедневно 6 мес.
5. Антицитокиновая терапия пентоксифиллином 25 мг/кг в течение 6 мес. (ингибирует выработку альвеолярными макрофагами ФНО), антиоксидантными комплексами в течение 2 мес.
23. Внебольничная пневмония. Этиология. Клинические проявления. Принципы диагностики. Лечебная тактика.
ВП – острое заболевание, возникшее во внебольничных условиях – то есть вне стационара или диагностированное впервые 48 ч от момента госпитализации, сопровождающиеся симптомами инфекции нижних отделов дыхательных путей (лихорадка, кашель, выделение мокроты) и рентгенологическими признаками инфильтративных изменений в легких.
Патогенез
Противоинфекционная защита нижних отделов дыхательных путей включает следующие механизмы:
Механические факторы - фильтрация, кашель, чихание, колебательные движения ресничек мерцательного эпителия
Механизмы неспецифического иммунитета
Механизмы специфического иммунитета
Можно выделить четыре патогенетических механизма обуславливающих развитие пневмонии:
Аспирация секрета ротоглотки;
Аспирация нестерильного содержимого пищевода/желудка
Вдыхание аэрозоля, содержащего микроорганизмы;
Гематогенное распространение микроорганизмов из внелегочного очага инфекции
Распространение инфекции из соседних пораженных органов
Факторы риска:
Алкоголизм, курение
ХОБЛ
Декомпенсированный сахарный диабет
Пребывание в домах престарелых
Несанированная полость рта
Эпидемия гриппа или ОРВИ
Бронхоэктазы
Наркомания
Локальная бронхиальная обструкция
Контакт с системами охлаждения воздуха и воды
Этиология ВП непосредственно связана с нормальной микрофлорой, колонизующие верхние отделы дыхательных путей, лишь некоторые обладают способностью при попадании в нижние отделы дыхательных путей вызывать воспалительную реакцию (таблица 2).
Таким возбудителем является чаще всего Streptococcus pneumoniae(30-50%). Существенное значение в этиологии имеют так называемые атипичные микроорганизмы, на долю которых приходится 8-30%:Mycoplasma pneumoniae,Chlamydia pneumoniae,Legionella pneumophila.М. pneumoniaeиС. Pneumoniaeчасто вызывают ВП у лиц молодого и среднего возраста (≥20 – 30% случаев), однако их этиологическая роль у пациентов старшего возраста менее значительна (1 – 3% случаев).
К редким возбудителям (3 – 5%) относится Haemophilus influenzae,Staphylococcus aureus,Klebsiella pneumoniae, реже другие энтеробактерии. Очень редко могут бытьРseudomonas аеruginosa(у больных муковисцидозом, бронхоэктазами). Вирусные респираторные инфекции рассматриваются как факторы рискавоспаления легких, являясь «проводником» бактериальной инфекции. ВП может быть связана с новым, ранее неизвестными возбудителями, вызывающими вспышки заболевания. К таким можно отнести ТОРС – ассоциированный коронавирус, вирус птичьего гриппа. Выделение таких микроорганизмов (Streptococcus viridans, Staphylococcus epidermidis, Enterococcus spp., Neisseria spp., Candida spp.) свидетельствует о контаминации материала флорой верхних отделов дыхательных путей, а не об этиологической значимости этих микробов.
Диагностика
Подозрение на пневмонию должно возникать при наличии у больного лихорадки, в сочетании с жалобами на кашель, одышку, отделение мокроты и /или боли в грудной клетке.
Лихорадка. У 25% пациентов старше 60 лет отсутствует лихорадка, а клинические симптомы представлены слабостью, утомляемостью, тошнотой, болями в животе, нередко на первый план выходят симптомы декомпенсации сопутствующих заболеваний.
Кашель. В начальном периоде болезни кашель может быть сухим, мучительным. Через несколько дней появляется мокрота.
Характер мокроты может быть разнообразным от слизистой до гнойной, иногда содержит прожилки крови или имеет «ржавый» характер. Гнойная мокрота в большом количестве характеризует формирование абсцесса легкого.
Выраженная одышкаи частота дыхания более 30 в минуту является одним из критериев тяжелого состояния больного.
Боли при дыхании могут быть связаны с поражением плевры при пневмонии с развитием сухого плеврита. Поражение диафрагмальной плевры может вызвать боль в брюшной полости.
Внелегочные проявления пневмонии:
Ознобы и потливость.
Миалгии.
Головная боль.
Цианоз.
Тахикардия
Herpes labialis
Кожная сыпь. Поражение слизистых.
Спутанность сознания
Диарея
Желтуха
Наличие или отсутствие того или иного признака, его выраженность определяются, с одной стороны, характером возбудителя, а с другой – особенностей иммунной системы организма. Наличие тяжелых соматических заболеваний, пожилой возраст, выраженный иммунодефицит способствуютатипичному течению пневмонии, особенностью которых может быть отсутствие или малая выраженность физикальных признаков легочного воспаления, отсутствие лихорадки, преобладание внелегочных симптомов.
Результатыобъективного обследованиязависят от многих факторов, включая степень тяжести, распространенность пневмонической инфильтрации, возраста, наличия сопутствующей патологии, наличие осложнений пневмонии. У 20% пациентов данные признаки отличаются или вообще отсутствуют.
Перкуссия– характерно укорочение перкуторного звука над пораженным участком легкого. При развитии экссудативного плеврита обнаруживается притупление перкуторного звука вплоть до тупого. При сухом плеврите перкуторные данные чаще не меняются.
Аускультация – локально выслушивается бронхиальное дыхание, фокус звучных мелкопузырчатых хрипов или крепитации. Усилена бронхофония и голосовое дрожание. При сухом плеврите шум трения плевры, при плевральном выпоте резко ослабленное дыхание.
Лабораторная диагностика и дополнительные методы исследования
Диагностический минимум обследования, у амбулаторных пациентов, должен включать исследования, позволяющие установить диагноз ВП и решить вопрос о тяжести течения. К ним относят:
Анализ крови– лейкоцитоз со сдвигом лейкоцитарной формулы влево или лейкопения, при тяжелой пневмонии возможно появление токсической зернистости лейкоцитов, снижение Нb, повышение СОЭ.
ЛЕЧЕНИЕ: пенициллины (амоксиклав, цефтриаксон и др), + макролиды (азитромицин), либо респираторный фторхинолон (левофлоксацин, моксифлоксацин).
24. Диагностика, дифференциальная диагностика и лечебная тактика при ба
Бронхиальная астма (БА) — хроническое воспалительное заболевание дыхательных путей с участием клеток (тучных, эозинофилов, Т-лимфоцитов), медиаторов аллергии и воспаления, сопровождающееся у предрасположенных лиц гиперреактивностью и вариабельной обструкцией бронхов, что проявляется приступом удушья, появлением хрипов, кашля или затруднения дыхания, особенно ночью и/или ранним утром.
ДИАГНОСТИКА
Диагностика БА облегчается при использовании следующих диагностических критериев:
приступы удушья с затруднением выдоха, сопровождающиеся сухими хрипами над всей поверхностью легких, которые слышны даже на расстоянии (дистанционные сухие хрипы);
эквиваленты типичного приступа бронхиальной астмы: приступообразный кашель в ночное время, нарушающий сон; повторно возникающее свистящее дыхание; затруднение дыхания или чувство стеснения в грудной клетке; появление кашля, одышки или свистящего дыхания в определенное время года, при контакте с определенными агентами (животные, табачный дым, парфюмерные изделия, выхлопные газы и т.д.) или после физической нагрузки;
выявление обструктивного типа дыхательной недостаточности при исследовании параметров функции внешнего дыхания;
исчезновение или значительное облегчение дыхания и прирост показателей ОФВ на 20% и более после применения бронходилататоров;
наличие биологического маркера бронхиальной астмы — высокий уровень азота оксида (N0) в выдыхаемом воздухе.
Лечение бронхиальной астмы.
Все препараты, применяемые при лечении бронхиальной астмы, делятся на две группы:
Средства для профилактики приступов заболевания (не купируют приступ удушья!) составляют базисную терапию - стабилизаторы мембран тучных клеток, глюкокортикоиды, антагонисты лейкотриеновых рецепторов.
Бронхорасширяющие препараты, используемые для купирования приступов астмы, дают симптоматический эффект и частота их применения служит индикатором эффективности базисной терапии - β2-адреномиметические средства, М-холиноблокаторы, препараты теофиллина.
Механизм действия стабилизаторов мембран тучных клеток состоит в снижении чувствительности тучных клеток к дегранулирующим агентам: специфическим при действии аллергена на сенсибилизированную клетку и неспецифическим – при прямом дегранулирующем эффекте химических и физических факторов, за счет уменьшения концентрации внутриклеточного кальция, включающего механизмы дегрануляции. Предварительное введение препаратов этой группы предотвращает или уменьшает выраженность бронхоспазма в ответ на последующее поступление аллергена. При этом снижается уровень гистамина, стимулирующего бронхоспазм по немедленному типу, и факторов хемотаксиса, привлекающих эозинофилы и нейтрофилы в очаг воспаления бронхов. Кроме того, установлено непосредственное действие стабилизаторов мембран тучных клеток на активность эозинофилов, нейтрофилов, моноцитов. Таким образом, подавляется не только ранняя, но и поздняя фаза астматической реакции, спустя 3-4 часа после провоцирующего действия. Данная группа препаратов эффективно предупреждают приступы удушья, провоцируемые физической нагрузкой, а также при атопической астме, связанной с прогнозируемым повышением содержания аллергена в воздухе (в первую очередь при пыльцевой астме).
Кетотифен (кетостерил, задитен) 1мг×2 р, per os;
кромоглициевая кислота (ифирал, кромогексал) – 20 мг×4р, ингаляционно;
недокромил натрия 4 мг×2-4р, ингаляционно;
кромогликат натрия (интал, кромоген) 1-2 мг×3-4р, ингаляционно. Комбинированные препараты (стабилизаторы мембран тучных клеток + β2-адреномиметики) интал+, дитек.
Глюкокортикоиды обладают широким спектром иммуномодулирующего и противовоспалительного действия: блокируют синтез простагландинов и лейкотриенов, подавляют синтез и эффекты цитокинов, стимулируют созревание β-адренергических рецепторов клеток и, тем самым, восстанавливают чувствительность клеток к действию адренергического стимула, влияют на систему иммунитета, преимущественно на Т-лимфоциты, уменьшая иммунологическое воспаление в ткани бронхов, подавляют дегрануляция тучных клеток и базофилов, угнетают активность слизеобразования, как базального, так и индуцированного медиаторами воспаления.
Будесонид (бупранал, транстек, эднок),
беклометазон (альдецин, бекотид, беклазон Эко),
флутиказон (флексотид),
флутиказон+салметерол (серетид, серетид мультидиск),
будесонид+формотерол (симбикорт).
Антагонисты лейкотриеновых рецепторов - фармакологическая активность препаратов проявляется на основных клетках мишенях, участвующих в патогенезе астмы (эозинофилах, нейтрофилах, моноцитах, тучных клетках): длительное использование снижает активность немедленной и замедленной фазы астматической реакции, уменьшает гиперреактивность бронхов. Эта группа препаратов является терапией выбора при аспириновой бронхиальной астме.
Зафирлукаст 20 мг×2р, per os;
монтелукаст 10 мг×1 р, per os (на ночь),
пранлукаст.
25. Вирусно-бактериальные пневмонии. Вопросы диагностики и врачебной тактики. Профилактика
Пневмонии – группа различных по этиологии, патогенезу, морфологической характеристике острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации.
Диагностика ТВП включает:
cбор эпидемиологического анамнеза;
идентификацию пневмонии;
выявление сепсиса и ПОН;
выявление острой ДН;
оценку сопутствующей патологии (исключение обострения или декомпенсации сопутствующих заболеваний).
Лабараторная диагностика. Биохимический анализ крови (мочевина, креатинин, электролиты, печеночные ферменты, билирубин, глюкоза, альбумин), Исследование уровня С-реактивного белка (СРБ) в сыворотке крови, Исследование плевральной жидкости (определение рН, активности ЛДГ, содержания белка, цитологическое исследование). Исследование газов артериальной крови с определением PaO2, PaCO2, pH, бикарбонатов, лактата. Бактериоскопия и культуральное исследование респираторного образца - мокрота или ТА (у пациентов, находящихся на ИВЛ)
Инструментальная диагностика при ВП включает лучевые методы исследования (рентгенография, компьютерная томография органов грудной полости), пульсоксиметрию, ультразвуковые исследования, фибробронхоскопию, электрокардиографическое исследование (ЭКГ).
Наиболее эффективными средствами профилактики ВП в настоящее время являются пневмококковые и гриппозные вакцины. С целью специфической профилактики пневмококковых инфекций, в том числе пневмококковой ВП у взрослых используютя вакцины двух типов: 23-валентная пневмококковая полисахаридная вакцина (ППСВ23) и 13-валентная пневмококковая конъюгированная вакцина (ПКВ13). Вакцинация против пневмококковой инфекции проводится круглогодично. Иммунизация пневмококковыми вакцинами рекомендуется всем пациентам с высоким риском развития пневмококковых инфекций.
26. Дыхательная недостаточность. Клиническая, лабораторная и инструментальная диагностика. Принципы лечения.
Дыхательная недостаточность — патологическое состояние организма, при котором нарушено поддержание нормального газового состава крови или оно достигается за счёт напряжения компенсаторных механизмов внешнего дыхания. Синдром дыхательной в досгаточности — один из самых важных пульмонологических синдромов, поскольку его возникновение свидетельствует о нарушении основной функции органов дыхания — газообмена.
ДН PaO2 мм рт.ст.
Компенсированная > 90
I ст. 80–89
II ст. 60–79
III ст. < 60
IV ст. < 40
По уровню декомпенсации систем дыхания и кровообращения, сознания, содержанию кислорода и углекислоты в крови различают III стадии ОДН.
I стадия ОДН. Пациент находится в сознании, жалуется на чувство нехватки воздуха, беспокоен, астеничен. Кожные покровы бледные, влажные, небольшой акроцианоз видимых слизистых. ЧД до 30 в 1 мин, ЧСС до 110 в 1 мин, АД в норме или несколько повышено, paO2 снижается до 70 мм рт.ст., paСO2 снижено из-за компенсаторной одышки.
II стадия ОДН. Больной жалуется на выраженное удушье, возможно развитие психомоторного возбуждения, нарушение сознания, бреда, галлюцинаций. Кожные покровы влажные, цианотичные, нередко в сочетании с гиперемией. ЧД 30-40 в 1 мин, ЧСС 120-140 в 1 мин нередко аритмия, регистрируется гипертензия, paO2 снижается до 60 мм рт.ст., paСO2 повышается до 50 мм рт.ст.
III стадия ОДН. Сознание помрачено или отсутствует, возможно развитие судорожного синдрома из-за гипоксии мозга, наблюдается пятнистый цианоз, гипоксическое расширение зрачка с отсутствием реакции на свет. При прогрессировании процесса тахипное (ЧД > 40 в 1 мин) переходит в брадипное (ЧД < 8 в 1 мин). Наблюдается гипотензия, тахиаритмии, paO2 уменьшается до 50 мм рт.ст. и ниже, paСO2 повышается до 90 мм рт.ст. и выше.
Для ранней диагностики данного заболевания проводятся функциональные пробы для исследования функций внешнего дыхания (спирометрия, пикфлоуметрия), лабораторный анализ газового состава крови, рентгенография легких, КТ, пульсоксиметрия.
27. Бронхолитики – β2-агонисты, м3-холинолитики, комбинированные препараты. Формы доставки, продолжительность действия, возможности использования в клинике внутренних болезней.
Бронхолитики
b2-адреномиметики, которые по продолжительности действия могут быть: короткодействующими и пролонгированными, а по способу введения: ингаляционными, парентеральными и пероральными.
Антихолинергические (м-холинолитики) препараты, которые по продолжительности действия представлены: короткодействующими и пролонгированными формами, а по способу введения только ингаляционными.
Селективные стимуляторы b2-адренорецепторов: 1. Короткодействующими препаратами являются сальбутамол, тербуталин и фенотерол. Преимущественно назначаются в виде аэрозольных ингаляций и являются наиболее щадящими и высокоэффективными b2-агонистами при БА. Они могут быть рекомендованы вместо ранее использовавшихся неселективных b2- агонистов, таких как орципреналин (алупент, астмопент). Предназначены для купирования приступов астмы и назначаются в режиме «по требованию». Фенотерол обладает частичной b2- селективностью. Характеризуется более мощным, в сравнении с сальбутамолом, бронхолитическим действием, но и большим риском побочных эффектов. 2. Пролонгированные b2-агонисты (сальметерол, формотерол и сальтос). С учетом быстрого наступления бронхолитического эффекта после применения форадила (формотерол) (1-3 мин) препарат может оказаться эффективным при купировании имеющегося бронхоспазма.
Показания: астма и другие состояния, ассоциированные с обратимой обструкцией дыхательных путей. Противопоказания: - гипертиреоидизм, - сердечная недостаточность, - аритмии, - удлинение Q-T интервала, - гипертензия, - беременность, - диабет (парентеральное применение)
М-ХОЛИНОЛИТИКИ Препараты блокируют действие ацетилхолина на М-холинергические рецепторы, которые представлены преимущественно в крупных воздухоносных путях. Соответственно, эффект препаратов более выражен при бронхитах, чем при астме, которая характеризуется преимущественным вовлечением периферических бронхов. В связи с этим традиционно признаны как более эффективные в лечении бронхоконстрикции, связанной с хроническим бронхитом у пациентов, не отвечающих на терапию b2- агонистами. Тиопропия бромид. Ипратропиума бромид.
Общие показания для преимущественного применения холинолитиков при БА:
- являются средством выбора при преобладании признаков бронхита, служащего клиническим эквивалентом астмы, в первую очередь, у пожилых людей, в т.ч. «поздняя астма» (важно использовать препараты совместно с муколитическими и отхаркивающими средствами);
- при «кашлевой астме» (кашель как эквивалент приступа астмы), при бронхиальной обструкции, провоцируемой физической нагрузкой, холодом, вдыханием пыли, газов;
- при бронхообструктивном синдроме с выраженной бронхореей («влажная астма»);
Показания к назначению: - Базисная терапия ХОБ и ХОБЛ.
- Симптоматическая терапия БА (при противопоказаниях к применению БДА и метилксантинов или их непереносимости, а также для потенцированиях терапевтических эффектов).
- Функциональные пробы на обратимость бронхиальной обструкции.
Режим дозирования: взрослым по 2 дозы 3-4 раза в сутки. Побочные эффекты: возможны: кашель, сухость во рту, боль в горле.
(β2-агонист и М-холинолитик) – беродуал (бронхолитик)
28. Хронический бронхит. Диагностические критерии. Вопросы дифференциальной диагностики. Принципы лечения.
- хр диффузное прогрессирующее воспаление бронхов, проявляющееся продуктивным кашлем, продолжающемся не менее 3 месяцев в году в течение 2 лет подряд, при исключении других заболеваний ВДП, бронхов и легких, которые могли бы вызвать эти симптомы. В анамнезе факторами риска развития и обострения хронического бронхита могут быть: • наличие вредных привычек (курение), • воздействие физ и хим факторов (вдыхание пыли, дыма, окиси углерода), • климатические факторы (сырой и холодный климат) • сезонность (осень, зима, ранняя весна) • аллергические заболевания и иммунодефицитные состояния, • вирусная инфекция • генетические факторы, конституциональная предрасположенность. Основные жалобы: • начало хр бронхита постепенное: утренний кашель с отделением слизистой мокроты, который постепенно начинает беспокоить в течение суток, усиливаясь в холодную и сырую погоду, с годами становится постоянным; • мокрота слизистая, в периоды обострения – слизисто-гнойная или гнойная; • в периоды обострения появляется и прогрессирует одышка; • в периоды обострения могут возникать озноб, субфебрильная температура; • общая слабость, недомогание. Физикальное обследование: • при обострении температура тела субфебрильная или нормальная; • при аускультации – жесткое дыхание, рассеянные сухие хрипы (в период обострения). Лаб-ные исследования • в ОАК – лейкоцитоз, ускоренное СОЭ; • при наличии мокроты (бк ислл-е) обязательно 3-х кратное исследование на бациллу Коха для исключения тбк легких. Инструментальные исследования • рентген ОГК при наличии кашля более 3-х недель, отсутствии эффекта от проводимой терапии обострения, у лиц пожилого возраста; • спирография (умеренные обструктивные нарушения вентиляции легких (ОФВ1 > 50-60 % от должной)); • по показаниям бронхоскопия. Принципы лечения: нет курению, обильное питье, ЛФК. При бронх обструкции – бронходилататоры (короткодействующие бета-2-агонисты (сальбутамол, фенотерол) и холинолитики (ипратропия бромид), а также комбинированные препараты (фенотерол+ипратропия бромид) в виде раствора для ингаляций через небулайзер или аэрозоля до 4-6 раз/сутки). При наличии вязкой мокроты –муколитики (амброксол, ацетилцистеин). При сохранении затяжного кашля и появлении признаков гиперреактивности дыхательных путей - противовоспалительных нестероидных препаратов (фенспирид), при неэффективности их – ингаляционные глюкокортикостероидные препараты (будесонид, беклометазон, флютиказон). При наличии бактериального обострения – АТБ 5-10 дней. Амоксициллины (в т.ч «защищенные» амоксициллин/клавуланат) макролиды (спирамицин, азитромицин, кларитромицин), «респираторные» фторхинолоны (левофлоксацин, моксифлоксацин), цефалоспорины 3 покол. Иммунокорригирующие препараты (левамизол, тималин).
Диагноз |
Диагностические критерии |
Туберкулез бронхов |
- характерны симптомы туберкулезной интоксикации (ночные поты, анорексия, слабость, субфебрильная температура тела), кровохарканье, отсутствие «гнойности» мокроты, - наличие бацилл Коха в мокроте и промывных водах бронхов, - туберкулезный семейный анамнез, положительные туберкулиновые пробы - локальный эндобронхит с рубцами и свищами при фибробронхоскопии, - положительный эффект от лечения туберкулостатическими препаратами |
Внебольничная пневмония |
- Фебрильная лихорадка свыше ≥ 38,0 - Озноб, боль в груди - Кашель с отделением гнойной мокроты - Тахикардия - Дыхательная недостаточность - Укорочение перкуторного звука, бронхиальное дыхание, крепитация, влажные хрипы - Рентгенологически – инфильтрация легочной ткани |
Бронхиальная астма |
- Аллергоанамнез - Приступообразный кашель в ночное время и/или утренние часы, при контакте с аллергеном - Хрипы, свисты в груди - Наличие сопутствующих аллергических заболеваний (атопический дерматит, аллергический ринит, проявления пищевой и лекарственной аллергии). - Эозинофилия в крови. - Повышение уровня IgE в крови. - Наличие в крови специфических IgE к различным аллергенам. |
Рак бронха |
- чаще у курящих мужчин и характеризуется надсадным кашлем с примесью крови, - атипичные клетки в мокроте, - в поздних стадиях — боли в грудной клетке, геморрагический экссудативный плеврит. - решающую роль в диагностики рака бронха играют фибробронхоскопия и биопсия слизистой оболочки бронха |
Застойная сердечная недостаточность |
- Хрипы в базальных отделах легких - Ортопноэ - Кардиомегалия - Признаки скопления жидкости в интерстициальной ткани или альвеолах на рентгенограмме - Протодиастолический ритм галопа, тахикардия - Ухудшение кашля, одышки и свистящих хрипов в ночное время |
29. Интерстициальные заболевания легких. Принципы диагностики. Основные нозологические формы. Критерии обычной интерстициальной пневмонии.
- гетерогенная группа болезней, объединенная рентгенологическим синдромом двусторонней диссеминации. Одним из наиболее распространенных и прогностически неблагоприятных заболеваний из группы ИЛБ является идиопатический фиброзирующий альвеолит (далее-ИФА - воспалением и фиброзом легочного интерстиция и воздухоносных пространств, дезорганизацией структурно-функциональных единиц паренхимы). Нозоологические формы: обычная интерстициальная пневмония, десквамативная интерстициальная пневмония, острая интерстициальная пневмония – синдром Хаммена–Рича, неспецифическая интерстициальная пневмония. Саркоидоз. Силикоз. Склеродермия. СКВ. Ревматоидный артрит. Ковид -19, Тбк.
Диагностика: При осмотре больного обращаем внимание тахипноэ, несоответствие выраженности одышки физикальным изменениям в легких. Во время аускультации на вдохе прослушиваются крепитирующие хрипы различной локализации. В крови – умеренный лейкоцитоз и повышение СОЭ; по данным ИФА – отрицательные серологические тесты на наличие Ат к микоплазме, легионеллам, риккетсиям. Проводится анализ газового состава крови и КЩС (артериальная гипоксемия на ранних этапах сменяется гиперкапнией в терминальной стадии).
Большую информационную ценность в диагностики интерстициальных болезней легких представляют рентгенологические методы (рентгенография и КТ легких). На ранних стадиях на рентгено- и томограммах можно увидеть деформацию и усиление легочного рисунка, мелкоочаговые тени, снижение прозрачности легочных полей (феномен «матового стекла»); в дальнейшем развивается рентгенологическая картина интерстициального фиброза и картина «сотового легкого».
По данным спирометрии чаще обнаруживается рестриктивный тип нарушений легочной вентиляции, снижение легочных объемов. При развитии легочной гипертензии на ЭКГ обнаруживается гипертрофия миокарда правых отделов сердца.
Критерии обычной интерстициальной пневмонии: Клиническая картина не обладает специфичностью и может совпадать с другими сущностями, что может затруднять постановку диагноза. У большинства имеется прогрессирующая одышка при физической нагрузке и хр сухой кашель. Физикальное исследование выявляет мелкопузырчатые хрипы в конце выдоха, пальцы в форме “барабанных палочек”, слабость, боли в грудной клетке. Типичный Паттерн ОИП (Сочетание четырех условий):
преобладание в субплевральных, базальных отделах
ретикулярные изменения (утолщения внутридольковых перегородок)
сотовое легкое +/- тракционные бронхо- бронхиолоэктазы
отсутствие других КТ признаков перечисленных в секции “противоречащие ОИП признаки”
Паттерн возможной ОИП (Сочетание трех условий):
преобладание в субплевральных, базальных отделах
ретикулярные изменения
отсутствие других КТ признаков перечисленных в секции “противоречащие ОИП признаки”
Паттерн противоречащих ОИП признаков (Наличие любого из семи следующих признаков):
преобладание в верхних или средних отделах
перибронховаскулярные изменения
выраженные изменения по типу матового стекла (т.е. более выраженные, чем ретикулярные изменения)
многочисленные микроузелки (двусторонние, преимущественно в верхних долях)
дискретные кисты (двусторонние, множественные, не относящиеся к сотовому легкому)
диффузное мозаичное уплотнение/ воздушные ловушки (в ≥3 долях с обеих сторон)
консолидация бронхолегочного сегмента (-ов) или доли (-ей)
30. Диагностика, дифференциальная диагностика и лечебная тактика при хронической обструктивной болезни легких.
Хроническая обструктивная болезнь легких - хроническое воспалительное заболевание, возникающее под воздействием различных факторов, главным из которых является табакокурение. Протекает с преимущественным поражением дистальных отделов дыхательных путей и паренхимы легких, формированием эмфиземы.
одышка при физической нагрузке, снижение переносимости физических нагрузок и
хронический кашель.
Шкала CAT.
Спирометрия
Пульсоксиметрия.
теста 6-минутной ходьбы
Рентгенография грудной клетки
Пикфлоуметрия - Определение объема пиковой скорости выдоха
Бронхография, бронхоскопия
Анализ мокроты
Лечение
Отказ от курения
короткодействующие β2-агонисты – сальбутамол
короткодействующие антихолинергетики – ипратропия бромид
длительнодействующие β2-агонисты – формотерол
муколитики и отхаркивающие
ингаляционных глюкокортикостероидов;
антибиотикотерапии во время обострений;
оксигенации
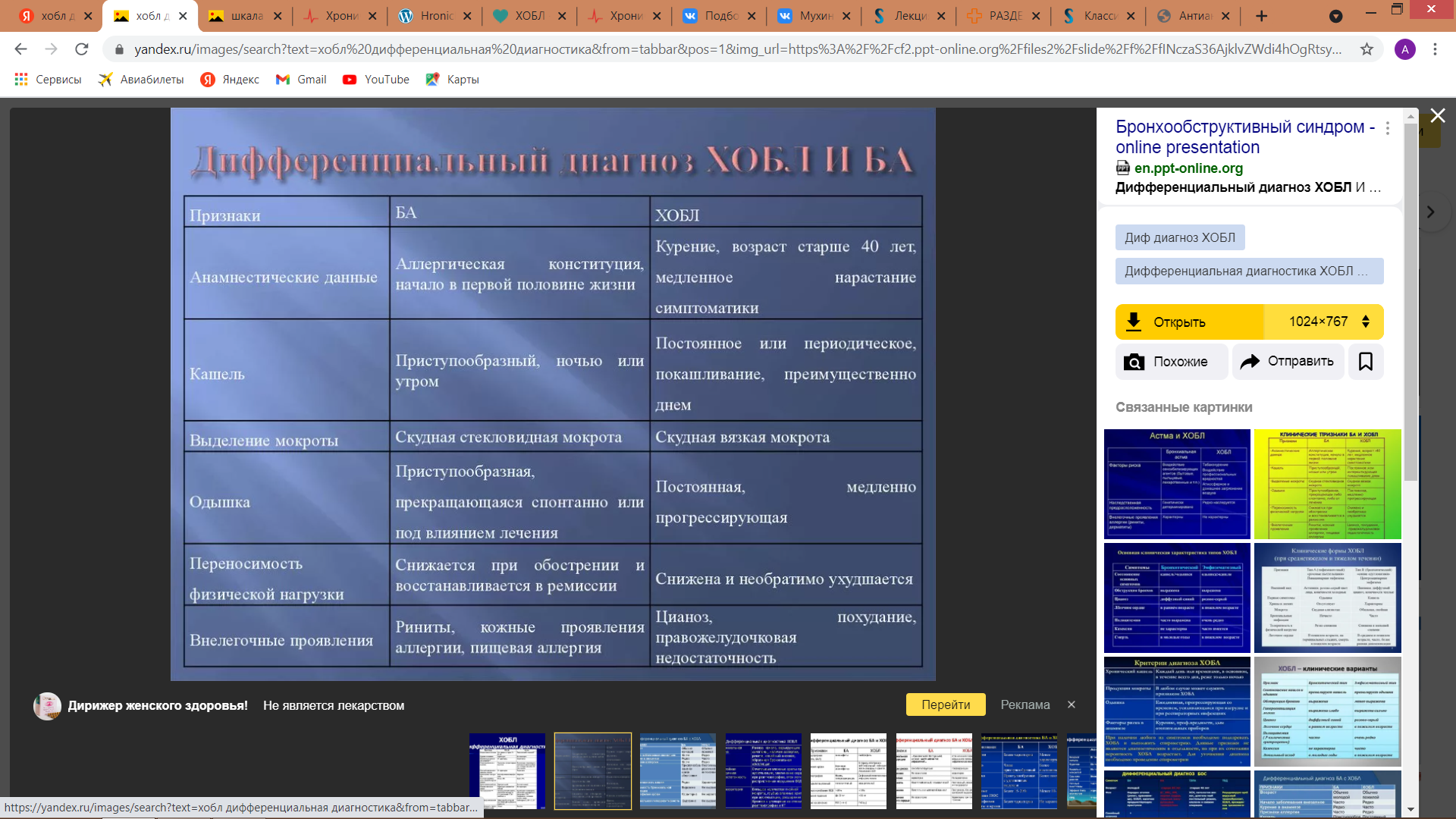
31. Экссудативный плеврит. Этиология. Диагностика. Принципы лечения.
Экссудативный плеврит - это поражение плевры инфекционного, опухолевого или иного характера, протекающее с явлениями экссудации – образованием и накоплением выпота в плевральной полости.
Причины
как осложнения острых пневмоний, абсцессов и гангрены лёгких или как проявление туберкулёза, травмы грудной клетки.
вызывают следующие возбудители: Стафилококки, Пневмококки; Микобактерии туберкулёза; Бледная трепонема; Легионелла; Кишечная палочка; Грибы; Вирусы.
Диагностика
По мере накопления выпота плевральные листки разобщаются, что сопровождается стиханием болей. На смену болям приходят тяжесть в соответствующей половине грудной клетки, кашель, одышка, заставляющая больного принимать вынужденное положение на больном боку.
Симптомы усиливаются при глубоком дыхании, кашле, движениях. Нарастающая дыхательная недостаточность проявляется бледностью кожных покровов, цианозом слизистых оболочек, акроцианозом. тахикардии, гипотония.
потливостью, слабостью. лихорадка, озноб, интоксикация, головная боль, отсутствие аппетита.
При осмотре - отставание пораженной половины грудной клетки (она увеличена в объеме, межреберные промежутки выбухают) в акте дыхания.
Пальпаторно - ослабление голосового дрожания. При перкуссии - определяется тупой звук.
Аускультативно над зоной экссудата дыхательные шумы не определяются.
рентгенографии или рентгеноскопии легких - интенсивное гомогенное затемнение, смещение сердца в здоровую сторону.
УЗИ плевральной полости.
плевральная пункция
Лечение
дренирование плевральной полости
С учетом основного диагноза назначается медикаментозная терапия
анальгетиков, противовоспалительных, противокашлевых, десенсибилизирующих, мочегонных средств, кислородотерапии, переливание плазмозамещающих растворов
32. Дыхательная недостаточность. Клиническая, лабораторная и инструментальная диагностика. Принципы лечения.
Дыхательная недостаточность — это патологическое состояние организма, характеризующееся недостаточным обеспечением газового состава крови, или оно может достигаться при помощи компенсаторных механизмов внешнего дыхания.
Клиника:
одышка; симптомы гипоксемии; признаки гиперкапнии, признаки утомления и слабости дыхательной мускулатуры.
признаком гипоксемии является цианоз. Тахикардия, гипотония. нарушения памяти на текущие события, потеря сознания.
проявления гиперкапнии: тахикардия; повышение сердечного выброса, системная вазодилатация; бессонница; частые пробуждения ночью и сонливость в дневное время; утренние головные боли; тошнота. гиперкапнической комы.
Симптомы утомления и слабости дыхательных мышц: Изменение частоты дыхания. ЧД> 25/мин. Вовлечение в дыхание вспомогательных групп мышц. Парадоксальное дыхание.
Диагностическим критерием ДН считается:
развитие артериальной гипоксемии – снижение парциального давления кислорода <60 мм рт. ст. (сатурация кислорода SpO2<90%)
развитие артериальной гиперкапнии – повышение парциального давления углекислого газа в артериальной крови > 45 мм рт. ст.
КОС крови
Пульсоксиметрия.
Капнография – метод непрерывной графической регистрации концентрации СО2 в выдыхаемом воздухе
теста 6-минутной ходьбы
Рентгенография грудной клетки
Принцип лечения:
создание микроклимата (проветривание помещений, увлажнение);
поддержание свободной проходимости дыхательных путей (отсасывание слизи, бронхолитические, отхаркивающие средства);
оксигенотерапия (ИВЛ);
спонтанное дыхание под постоянным положительным давлением (СДППД);
нормализация легочного кровотока (эуфиллин -бронхолитик, пентамин);
коррекция КОС;
лечение основного заболевания и сопутствующих патологических состояний.
33. Вопросы классификации пневмонии. Стандарты лечения в зависимости от тяжести течения и этиологии. Вопросы профилактики
Пневмонии – группа острых инфекционных (преимущественно бактериальных) заболеваний, характеризующихся очаговым поражением респираторных отделов легких с обязательным наличием внутриальвеолярной экссудации.
Форма:
1) очаговая бронхопневмония;
2) сегментарная пневмония;
3) интерстициальная пневмония;
4) крупозная пневмония.
внебольничная - внебольничной считают пневмонию, развившуюся вне стационара, либо диагностированную в первые
больничная (нозокомиальная)-
Аспирационная
Пневмонии у лиц с иммунодефицитными состояниями.
В зависимости от возбудителя:
- пневмококковые;
- стрептококковые;
- стафилококковые;
- хламидиазные;
- микоплазменные;
- фридлендеровские.
Лечение
ингаляции кислорода.
Антибиотикотерапия.
При внегоспитальной пневмонии - пенициллины (амоксициллин с клавулановой к-той, ампициллин), макролиды, цефалоспорины.
Для лечения внутрибольничных пневмоний - пенициллины, цефалоспорины, фторхинолоны (ципрофлоксацин, офлоксацин), карбапенемы, аминогликозиды.
При неизвестном возбудителе назначают комбинированную антибиотикотерапию. Курс лечения может продолжаться от 7 до 14 дней, возможна смена антибиотика.
Симптоматическая терапия. проведение дезинтоксикационной терапии, иммуностимуляции, назначения жаропонижающих, отхаркивающих и муколитических, антигистаминных средств.
Профилактика
Меры предупреждения развития пневмонии заключаются в закаливании организма, поддержании иммунитета, исключении фактора переохлаждения, санации хронических инфекционных очагов носоглотки, прекращении курения и злоупотребления алкоголем. У ослабленных лежачих пациентов с целью профилактики пневмонии целесообразно проведение дыхательной и лечебной гимнастики, массажа, назначение антиагрегантов (пентоксифиллина, гепарина).
34. Диагностика, дифференциальная диагностика и лечебная тактика при хронической обструктивной болезни легких.
Хроническая обструктивная болезнь легких - хроническое воспалительное заболевание, возникающее под воздействием различных факторов, главным из которых является табакокурение. Протекает с преимущественным поражением дистальных отделов дыхательных путей и паренхимы легких, формированием эмфиземы.
одышка при физической нагрузке, снижение переносимости физических нагрузок и
хронический кашель.
Шкала CAT.
Спирометрия
Пульсоксиметрия.
теста 6-минутной ходьбы
Рентгенография грудной клетки
Пикфлоуметрия - Определение объема пиковой скорости выдоха
Бронхография, бронхоскопия
Анализ мокроты
Лечение
Отказ от курения
короткодействующие β2-агонисты – сальбутамол
короткодействующие антихолинергетики – ипратропия бромид
длительнодействующие β2-агонисты – формотерол
муколитики и отхаркивающие
ингаляционных глюкокортикостероидов;
антибиотикотерапии во время обострений;
оксигенации
35. Хронический бронхит. Вопросы дифференциальной диагностики. Тактика ведения.
хроническое диффузное прогрессирующее воспаление бронхов, проявляющееся продуктивным кашлем, продолжающемся не менее 3 месяцев в году в течение 2 лет подряд, при исключении других заболеваний верхних дыхательных путей, бронхов и легких, которые могли бы вызвать эти симптомы.
Дифф.диагност.: Туберкулез бронхов − характерны симптомы туберкулезной интоксикации (ночные поты, анорексия, слабость, субфебрильная температура тела), кровохарканье, отсутствие «гнойности» мокроты, − наличие бацилл Коха в мокроте и промывных водах бронхов, − туберкулезный семейный анамнез, положительные туберкулиновые пробы − локальный эндобронхит с рубцами и свищами при фибробронхоскопии, − положительный эффект от лечения туберкулостатическими препаратами
Внебольничная пневмония− Фебрильная лихорадка свыше ≥ 38,0 − Озноб, боль в груди − Кашель с отделением гнойной мокроты − Тахикардия − Дыхательная недостаточность − Укорочение перкуторного звука, бронхиальное дыхание, крепитация, влажные хрипы − Рентгенологически – инфильтрация легочной ткани
Бронхиальная астма − Аллергоанамнез − Приступообразный кашель в ночное время и/или утренние часы, при контакте с аллергеном − Хрипы, свисты в груди − Наличие сопутствующих аллергических заболеваний (атопический дерматит, аллергический ринит, проявления пищевой и лекарственной аллергии). − Эозинофилия в крови. − Повышение уровня IgE в крови. − Наличие в крови специфических IgE к различным аллергенам.
Рак бронха − чаще у курящих мужчин и характеризуется надсадным кашлем с примесью крови, − атипичные клетки в мокроте, − в поздних стадиях — боли в грудной клетке, геморрагический экссудативный плеврит. − решающую роль в диагностики рака бронха играют фибробронхоскопия и биопсия слизистой оболочки бронха
Застойная сердечная недостаточность − Хрипы в базальных отделах легких − Ортопноэ − Кардиомегалия − Признаки скопления жидкости в интерстициальной ткани или альвеолах на рентгенограмме − Протодиастолический ритм галопа, тахикардия − Ухудшение кашля, одышки и свистящих хрипов в ночное время
Тактика лечения: Немедикаментозное лечение • устранить внешние причинные факторы (курение, вдыхание вредных веществ и другое); • для облегчения выделения мокроты - поддержание адекватной гидратации (обильное питье воды, морсов до 2-3 л/сутки); • увлажнение воздуха в помещении• устранение воздействия на больного факторов окружающей среды, вызывающих кашель (дыма, пыли, резких запахов, холодного воздуха); • ЛФК, массаж грудной клетки, физиотерапия Медикаментозное лечение бронходилататоры. Наилучшим эффектом обладают короткодействующие бета-2-агонисты (сальбутамол, фенотерол) и холинолитики (ипратропия бромид), а также комбинированные препараты (фенотерол+ипратропия бромид) в виде раствора для ингаляций через небулайзер или аэрозоля до 4-6 раз/сутки.
При наличии вязкой мокроты показаны мукоактивные препараты различного механизма действия (амброксол, бизолвон, ацетилцистеин, карбоцистеин, эрдостеин) внутрь, инъекционно или в виде ингаляций через небулайзер.
При сохранении затяжного кашля и появлении признаков гиперреактивности дыхательных путей возможно применение НПВС(фенспирид), при неэффективности их – ингаляционные глюкокортикостероидные препараты (будесонид, беклометазон, флютиказон, циклесонид и др.),
При наличии бактериального обострения хронического бронхита назначаются антибактериальные препараты. П
36. Идиопатический легочный фиброз. Критерии постановки диагноза. Дифференциальная диагностика кт-патерна обычной интерстициальной пневмонии. Возможности улучшения течения болезни
Интерстициальные заболевания легких – гетерогенная группа заболеваний и патологических состояний известной и неизвестной природы, характеризующаяся распространенным, как правило, двусторонним поражением респираторных отделов легких (альвеол, респираторных бронхиол).
Идиопатический легочный фиброз – особая форма хронической прогрессирующей фиброзирующей интерстициальной пневмонии неизвестной этиологии; возникает преимущественно у людей старшего возраста, поражает только легкие и связана с гистологическим и/или компьютерно-томографическим паттерном обычной интерстициальной пневмонии.
Критерии установления диагноза/состояния:
1) жалобы на одышку при отсутствии очевидных причин, клинически значимых внешнесредовых или лекарственных воздействий; отсутствие признаков СЗСТ;
2) двухсторонней инспираторной крепитацией в базальных отделах легких при аускультации;
4) выявление паттерна обычной интерстициальной пневмонии (ОИП) при ВРКТ органов грудной клетки и/или при патолого-анатомическом исследовании биоптатов легочной ткани.
Основными признаками ОИП при КТ органов грудной клетки являются:
- преобладание изменений в кортикальных и базальных отделах легких;
- диффузные двухсторонние ретикулярные изменения;
- мелкие субплевральные воздушные кисты («сотовое легкое») и/или
- периферические тракционные бронхо- или бронхиолоэктазы [42] (Рис. 1-3).
«Матовое стекло» может присутствовать на фоне ретикулярных изменений и «сотового легкого», но не должно превалировать над другими изменениями. Такое "матовое стекло" является признаком фиброза.
Дифференциальная диагностика

Всем больным ИЛФ рекомендуется лечение противоопухолевыми препаратами и другими иммунодепрессантами (антифибротическими препаратами) – нинтеданибом** или пирфенидоном

Гастроэнторология
1. Редкие болезни кишечника. Глютеновая энтеропатия. Болезнь Уиппла. Методы диагностики. Тактика ведения и лечения
К редко встречаемым болезням кишечника можно отнести целиакию (глютеновая энтеропатия) и болезнь Уиппла. Особенностями редко встречаемых заболеваний являются не специфические клинические проявления, трудности в диагностике, возможные осложнения и снижение качества жизни, сложности в лечении.
Целиакия (глютеновая энтеропатия) – хроническое генетически обусловленное иммуно-опосредованное заболевание, с характерной стойкой непереносимостью белка глютена (содержится в пшенице, ржи, ячмене) с формированием при этом атрофии слизистой оболочки тонкой кишки (в первую очередь постбульбарного отдела двенадцатиперстной кишки), полным восстановлением структуры слизистой оболочки тонкой кишки при соблюдении характера питания не содержащего глютен.
В тонкой кишке при иммунно – опосредованном воспалении формируются морфологические изменения, проявляемые атрофией ворсинок (гиперрегенераторная атрофия), гипертрофией крипт. Может развиваться синдром мальабсорбции.
Диагностика целиакии (глютеновой энтеропатии): Жалобы: - хроническая диарея со зловонным запахом - боли в животе (рецидивирующие) - вздутие живота - снижение массы тела - боли в костях и суставах - раздражительность - утомляемость - нарушение менструального цикла
*Семейный анамнез (выявление непереносимости злаковых у близких родственников) Данные объективного исследования: - бледность кожи лица - афтозные язвы десен и повреждения эмали - болезненность при пальпации околопупочной области
Инструментальные методы диагностики: - ЭФГДС (эндоскопия с биопсией слизистой оболочки постлуковичного отдела двенадцатиперстной кишки) - эндоскопия видиокапсульная - УЗИ органов брюшной полости и щитовидной железы - колоноскопия
Гистологическое изучение биопсийного материала слизистой оболочки постлуковичного отдела двенадцатиперстной кишки. Рентгенологические методы диагностики: - КРТ тонкой кишки - рентгенография тонкой кишки Денситометрия костей для диагностики остеопороза
Лабораторные методы диагностики: - в анализе крови серологическое определение антител: антиглиадиновых ( IgA ) глиадин, (IgG) глиадин, антиэндомизиальных, антител к тканевой трансглютаминазе ( IgA) - анализ крови (общий, глюкоза, гликозилированный гемоглобин, общий белок, белковые фракции, электролиты, микроэлементы) - анализы кала (фекальная эластаза 1)
Лечение лиц с выявленной целиакией: - строгая пожизненная аглютеновая диета (запрещается употреблять пищу, которая содержит рожь, пшеницу, ячмень в любом количестве) - при лактазной недостаточноти ограничить прием молочных продуктов и исключить молоко - исключение хлебных и кондитерских изделий из муки - рацион питания может включать: рис, гречку, картофель, кукурузу, соевые бобы, а овес и продукты из него ограничить в употреблении - симптоматическая терапия - применение преднизолона (при несоблюдении диеты) (приводит к улучшению морфологической структуры слизистой оболочки тонкой кишки)
Болезнь Уиппла - заболевание тонкой кишки, вызванное грамположительной бациллой Tropheryma whippelii, характеризующееся закупоркой лимфатических сосудов тонкой кишки и других органов глюкозамино-гликановыми (мукополисахаридными) комплексами бактериального происхождения, что приводит к формированию полисистемных поражений - экссудативной энтеропатии, синдрому мальабсорбции, артралгиям, полисерозитам и неврологическим нарушениям.
Cимптомы, течение
Болезнь Уиппла является системным заболеванием, поэтому клиническая картина складывается из симптомов поражения тонкой кишки, мезентериальных лимфатических узлов, синовиальных оболочек суставов, сердца, легких, головного мозга, глаз.
(мигрирующие боли в суставах, припухлость суставов, миалгии, миозит, диарея, стеаторея, приступообразные боли в животе после еды, потеря массы тела, лимфаденопатия, лихорадка, кашель, боль в грудной клетке, расстройства психики)
Алгоритм диагностики Для установления диагноза достаточно наличия одного из указанных признаков:
- синхронные сокращения жевательных мышц или лицевых мышц; - выявление возбудителя Tropheryma whippelii в биоптатах тонкого кишечника; - обнаружение ДНК возбудителя методом ПЦР.
Инструментальная диагностика
1. Рентгенография кишечника.
2. Эндоскопическое исследование
3. УЗИ органов грудной клетки и брюшной полости. Выявляются увеличенные лимфоузлы, визуализирующиеся как очаги повышенной эхогенности. Возможно обнаружение асцита, гепатоспленомегалии, плеврального или перикардиального выпота.
4. Компьютерная томография органов грудной клетки и брюшной полости. Выявляются увеличенные лимфоузлы, визуализирующиеся как очаги пониженной плотности. Могут обнаруживаться асцит, гепатоспленомегалия, плевральный или перикардиальный выпот.
5. Биопсия кишечника. При световой микроскопии выявляются внутриклеточные и внеклеточные включения жира в слизистой оболочке тонкой кишки и в брыжеечных лимфатических сосудах. Возможно обнаружение инфильтрации слизистой оболочки тонкой кишки "пенистыми" макрофагами, которые содержат гранулы с PAS-положительной реакцией (свидетельствуют о грамположительных микроорганизмах в слизистой оболочке).
6. МРТ головного мозга - выполняется при наличии симптомов со стороны центральной нервной системы. Могут обнаруживаться очаги пониженной плотности в коре головного мозга (неспецифичный для болезни Уиппла признак), диффузные изменения в полушариях мозжечка, в области гипоталамуса, базальных ганглиев, гиппокампа.
7. ЭхоКГ - выполняется при наличии признаков поражения сердечно-сосудистой системы.
Лабораторная диагностика
1. Общий анализ крови: - гипохромная микроцитарная анемия (у 90% больных); при дефиците фолиевой кислоты анемия приобретает смешанный характер; - снижен уровень гемоглобина; - возможно повышение количества лейкоцитов и тромбоцитов, СОЭ.
2. Коагулограмма: повышение показателя протромбинового времени свыше 15-20 секунд.
3. Биохимический анализ крови: - могут выявляться гипопротеинемия, гипохолестеринемия, гипоальбуминемия (обусловлена нарушением синтеза альбуминов и потерей больших количеств сывороточного альбумина через сосуды пищеварительного тракта); - в сыворотке крови снижено содержание калия, кальция, магния, железа.
4. ПЦР позволяет выявить наличие возбудителя заболевания, даже если в пробе присутствует всего несколько молекул ДНК возбудителя.
5. Тест с D-ксилозой (оценка абсорбционной функции тонкой кишки): после приема 25 г D-ксилозы пациент в течение 5 часов собирает мочу. При ненарушенных процессах всасывания в тонкой кишке количество выделенной за это время D-ксилозы должно быть не менее 5 г.
6. Тест Шиллинга (оценка всасывания витамина В 12) . Пациент принимает меченый витамин В 12, в норме показатели его экскреции с мочой в течение суток составляют не менее 10%. Если данные показатели ниже 5%, всасывание витамина B 12 в тонкой кишке нарушено.
7. Исследование кала. В 90% случаев выявляется стеаторея.
Методы лечения. Диета с ограничением жиров, повышенным содержанием белка и витаминов. Лечебное питание должно способствовать борьбе с диареей и восполнять нутритивные дефициты. Целесообразно использовать специальные смеси для энтерального питания с коротко- и среднецепочечными триглицеридами, которые всасываются не в лимфатических, а в кровеносных сосудах. Медикаментозное лечение: глюкокортикостероиды, антибиотики, ферменты. Осуществляется коррекция поливитаминной недостаточности. В ряде случаев показана симптоматическая терапия.
2. Кислотозависимые заболевания. Стандарты диагностики+
Кислотозависмые заболевания – группа заболеваний верхних отделов ЖКТ, обусловленных избыточной продукцией соляной кислоты париетальными клетками слизистой оболочки желудка.
Она включает в себя следующие заболевания: ГЭРБ, язвенную болезнь желудка и двенадцатиперстной кишки, функциональную диспепсию; гастропатию, индуцированную приемом НПВП; а также синдром Золлингера —Эллисона.
МЕТОДЫ ДИАГНОСТИКИ ГЭРБ
• Клинический. рефлюксный синдром (эндоскопически негативная форма ГЭРБ), проявляющийся исключительно симптомами (наличие изжоги и / или регургитации, беспокоящих больного).
• Терапевтический тест с одним из ингибиторов протонной помпы в стандартных дозировках в течение 5 - 10 дней.
• Эндоскопическое исследование позволяет выявить и оценить изменения в дистальном отделе пищевода, прежде всего рефлюкс - эзофагит. При подозрении на метаплазию пищевода (пищевод Баррета) и злокачественное поражение проводятся множественная биопсия и морфологическое исследование.
• Суточный рефлюкс - мониторинг пищевода (pH - мониторинг, комбинированный многоканальный импеданс - pH - мониторинг) для выявления и количественной оценки патологического гастроэзофагиального рефлюкса, определения его связи с симптомами болезни, а также для оценки эффективности терапии. Суточный pH - мониторинг позволяет выявить патологический кислый рефлюкс (pH < 4,0). Импеданс - pH - мониторинг наряду с кислыми даёт возможность выявлять слабокислые, щелочные и газовые рефлюксы.
• Манометрия пищевода - для оценки моторики пищевода (перистальтика тела, давление покоя и расслабление нижнего и верхнего пищеводных сфинктеров), дифференциальной диагностики с первичными (ахалазия) и вторичными (склеродермия) поражениями пищевода. Манометрия помогает правильно расположить зонд при pH - мониторинге пищевода (на 5 см выше проксимального края нижнего пищеводного сфинктера).
• По показаниям проводится: рентгенологическое исследование верхних отделов желудочно-кишечного тракта - для диагностики и дифференциальной диагностики пептических язв и / или пептической стриктуры пищевода.
- оценка нарушений эвакуаторной функции желудка (электрогастрография и другие методы).
• При выявлении внепищеводных синдромов и при определении показаний к хирургическому лечению ГЭРБ - консультации специалистов (кардиолог, пульмонолог, лор, стоматолог, психиатр и др.).
МЕТОДЫ ДИАГНОСТИКИ ЯЗВЕННОЙ БОЛЕЗНИ:
• Клинический.
• Эндоскопический, при язве желудка в обязательном порядке для исключения малигнизации - прицельная биопсия (5 - 7 фрагментов) дна и краёв язвы.
• Рентгенологический для выявления осложнений (пенетрация, малигнизация). Определение осложнений функции желудка (pH - метрия).
Методы диагностики Helicobacter pylori
1. Биохимические методы
1.1. быстрый уреазный тест;
1.2. уреазный дыхательный тест с 13С-мочевиной;
1.3. аммонийный дыхательный тест;
2. Морфологические методы:
- гистологический метод - выявление Hp в биоптатах слизистой оболочки антрального отдела и тела желудка; в слое пристеночной слизи желудка.
3. Бактериологический метод с выделением чистой культуры и определением чувствительности к антибиотикам.
4. Иммунологические методы:
4.1. выявление антигена H. pylori в кале (слюне, зубном налёте, моче);
4.2. выявление антител к H. pylori в крови с помощью иммуноферментного анализа.
5. Молекулярно - генетические методы: (ПЦР) для изучения биоптатов слизистой оболочки желудка. ПЦР проводится не столько для выявления H. pylori, сколько для верификации штаммов H. pylori (генотипирование), в том числе молекулярно - генетических особенностей, определяющих степень их вирулентности и чувствительности к кларитромицину.
МЕТОДЫ ДИАГНОСТИКИ ГАСТРИТА
• клинический;
• эндоскопический с морфологической оценкой биопатов;
• диагностика Hp (см. выше)
• определение кислотообразующей функции желудка (pH - метрия);
• рентгенологический.
МЕТОДЫ ДИАГНОСТИКИ НПВП ГАСТРОПАТИИ
• клинический (изучение жалоб, сбор анмнеза заболевания, выявление факта длительности приёма приёма НПВП, аспирина, оценка факторов риска развития НПВП - гастропатии);
• общий анализ крови (концетрация гемоглобина, число эритроцитов, гематокрит), биохимический анализ крови (показатели обмена железа), анализ кала на скрытую кровь для выявления кровотечения;
• эндоскопический и / или рентгенологический.
МЕТОДЫ ДИАГНОСТИКИ СИНДРОМА ЗОЛЛИНГЕРА-ЭЛЛИСОНА
Лабораторные исследования:
- Гастрин. Повышенный уровень гастрина может указывать на опухоль в поджелудочной железе или двенадцатиперстной кишки. Перед исследованием следует прекратить прием лекарств, уменьшающих выработку желудочного сока. Уровень гастрина может колебаться, поэтому для получения более точных результатов исследование может проводиться несколько раз в разные дни. Уровень гастрина также может повышаться при хроническом гастрите, В12-дефицитной анемии и других заболеваниях.
- Измерение уровня кислотности желудочного сока. Методика заключается во введении в желудок зонда с последующим забором желудочного сока. Т Для синдрома Золлингера – Элиссона характерно значительное повышение кислотности желудочного сока.
- Провокационный тест с секретином (гормоном, участвующим в регуляции работы поджелудочной железой). Исследование состоит во внутривенном введении раствора секретина. В норме уровень гастрина в крови понижается, при синдроме Золлингера – Эллисона же уровень гастрина парадоксальным образом значительно повышается.
Другие методы исследования:
- Эндоскопия. Во время эндоскопии может быть проведена биопсия – забор образца ткани для последующего изучения под микроскопом.
- Ультразвуковое исследование (УЗИ) брюшной полости, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) брюшной полости. Данные исследования проводятся для визуализации опухоли и установления ее расположения и размеров.
3. Хронический холецистит: классификация, этиология, патогенез, диагностика. Лечение.+
Хронический холецистит – хроническое рецидивирующее заболевание желчного пузыря, характеризующееся нарушением его моторно-эвакуаторной функции, изменением физико-химических свойств желчи и достаточно частым образованием внутрипузырных конкрементов, что клинически наиболее часто проявляется желчной коликой.
Клиническая классификация
Общепринятой классификации хронического холецистита нет. Наиболее полной является классификация Я. С. Циммермана. По этиологии и патогенезу: Бактериальный, Вирусный, Паразитарный, Немикробный («асептический», иммуногенный), Аллергический, «Ферментативный», Невыясненной этиологии. По клиническим формам
1. Хронический бескаменный холецистит
2. С преобладанием воспалительного процесса
3. С преобладанием дискинетичеких явлений
4. Хронический калькулезный холецистит
По типу дискинезий
1. Нарушение сократительной функции желчного пузыря: Гиперкинез желчного пузыря; Гипокинез желчного пузыря (гипотония)
2. Нарушение тонуса сфинктерного аппарата желчевыводящих путей:
- Гипертонус сфинктера Одди
- Гипертонус сфинктера Люткенса
- Гипертонус обоих сфинктеров По характеру течения
1. Редко рецидивирующий (благоприятного течения)
2. Часто рецидивирующий (упорного течения)
3. Постоянного (монотонного) течения
4. Маскировочный (атипичного течения) По фазам заболевания: Фаза обострения (декомпенсация); Фаза затухающего обострения (субкомпенсация); Фаза ремиссии (компенсация - стойкая, нестойкая)
ЭТИОЛОГИЯ
Основную роль играет условно-патогенная микрофлора (эшерихии, стрептококки, стафилококки, реже протеи, синегнойная палочка, энтерококк), иногда патогенная микрофлора (шигеллы, сальмонеллы), вирусная и протозойная инфекция.
Предрасполагающие факторы: застой желчи в желчном пузыре, сдавления и перегибы желчевыводящих протоков, дискинезии желчного пузыря и желчевыводящих путей, нарушения тонуса и двигательной функции желчных путей под влиянием различных эмоциональных стрессов, эндокринных и вегетативных расстройств, патологических рефлексов измененных органов пищеварительной системы.
Общепризнанным является «правило 5F»: женский пол (female), возраст старше 40 лет (forty), ожирение при индексе массы тела более 30 (fat), множественные беременности (fertile), диспепсия с метеоризмом (flatulent). Дополнительно: наследственность; перенесенные вирусный гепатит и инфекционный мононуклеоз, сепсис, кишечные инфекции с затяжным течением; лямблиоз кишечника; панкреатит; синдром нарушенного всасывания.
ПАТОГЕНЕЗ
Функциональные нарушения нервно-мышечного аппарата способствуют гипо- или атонии желчного пузыря. Внедрение микробной флоры вызывает воспаление его слизистой. При дальнейшем прогрессировании процесса воспаление распространяется на подслизистый и мышечный слои стенки желчного пузыря, образуются инфильтраты, соединительнотканные разрастания. При переходе процесса на серозную оболочку формируются спайки с глиссоновой капсулой печени и соседними органами (желудок, 12-перстная кишка, кишечник), развивается перихолецистит. Помимо катарального, может возникнуть флегмонозный или гангренозный процесс. В тяжелых случаях в стенке желчного пузыря появляются мелкие абсцессы, очаги некроза, изъязвления, что приводит к перфорации или развитию эмпиемы. Хронический холецистит может возникнуть после острого воспаления, но чаще развивается самостоятельно и постепенно, на фоне желчнокаменной болезни, гастрита с секреторной недостаточностью, хронического панкреатита и других заболеваний органов пищеварения, ожирения.
Диагностические критерии
Жалобы и анамнез
Боль:
1) периодическая разной продолжительности или постоянная тупая, ноющая, неинтенсивная, чувство тяжести, дискомфорта в правом подреберье, не связанные с приемом пищи;
2) боль и ощущение дискомфорта в правом подреберье, различной интенсивности и продолжительности, связанные с приемом пищи;
3) приступ желчной колики:
- острая, интенсивная, нетерпимая, жгучая, распирающая, сжимающая, схваткообразная боль в эпигастрии и правом подреберье, заставляющая больного метаться в кровати, продолжительностью от 15 мин до 5 ч, достигая максимума в течение 20–30 мин;
- иррадиирует в правое плечо, надплечье, правую половину шеи, правую лопатку, спину, правую половину грудной клетки, иногда носит опоясывающий характер;
- появляется внезапно, поздно вечером или ночью, после погрешности в диете, физического и эмоционального напряжения, у женщин часто связана с менструальным циклом;
- вначале при движении больного интенсивность боли не меняется, но если приступ не купируется в течение 10–12 ч, развивается острое воспаление стенки желчного пузыря, клиника острого холецистита, боль приобретает постоянный характер, усиливается при изменении положения тела;
- боли рецидивируют.
Лихорадка с повышением температуры тела не выше 38 °C, носит нервнорефлекторный характер, после окончания приступа нормализуется, сопровождается ознобом, холодным липким потом. Сохранение температуры выше 38 °C свидетельствует о развитии осложнений.
Рвота. Обильная, не приносящая облегчения, вначале пищей, затем содержимым с примесью желчи, сопровождается тошнотой.
Желтуха. Иктеричность склер, кратковременное обесцвечивание кала, потемнение мочи.
Диспептические явления часто предшествуют развитию приступа и сохраняются в межприступный период: постоянное или периодическое ощущение горечи во рту; тошнота; изжога; постоянное или периодическое ощущение сухости во рту; отрыжка воздухом или пищей; снижение аппетита;- неустойчивый стул.
Физикальное обследование:
- объективно во время желчной колики пациент нередко беспокоен, напряжен, старается выбрать положение тела, при котором интенсивность боли минимальна;
- пальпаторно в правом подреберье, эпигастрии отмечается болезненность, также болезненность в точке Маккензи (место пересечения наружного края правой прямой мышцы живота с правой реберной дугой); Мюсси (в правая надключичная область между ножками грудинно-ключично-сосцевидной мышцы);
- симптомы: Мерфи - болезненность при пальпации в правом подреберье на вдохе; Кера - боль в правом подреберье во время глубокого вдоха;
- симптомы раздражения брюшины отсутствуют;
- пальпация и перкуссия позволяют выявить у некоторых больных участки гиперестезии и локальной болезненности, чаще в правой половине живота. Иногда может определяться и симптом локальной мышечной защиты;
- у лиц пожилого возраста в случае выраженной боли могут наблюдаться гемодинамические нарушения: цианоз, падение АД, нарушения сердечного ритма;
- иногда выявляется субиктеричность склер, мягкого неба и кожных покровов;
- при закупорке камнем общего желчного протока или его ущемлении в ампуле большого дуоденального сосочка развивается механическая желтуха (кожный зуд, моча «цвета пива», ахоличный кал);
- возможно повышение температуры, слабый или умеренный озноб.
Инструментальные исследования - УЗИ – утолщение стенки желчного пузыря (при обострении процесса – более 3 мм), увеличение его объема, в просвете пузыря — густой секрет, конкременты. Иногда выявляют сморщенный, уменьшенный в размерах желчный пузырь, заполненный конкрементами и практически не содержащий желчи;
- Эндоскопическая ретроградная холангиография применяется для оценки состояния желчных протоков, наличия в них конкрементов.
- Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) – позволяют выявить расширение желчных протоков, увеличение забрюшинных лимфатических узлов, заболевания головки поджелудочной железы и печени;
- Рентгеноконтрастные методы исследования желчного пузыря: пероральная холецистография, внутривенная холецистохолангиография. На снимках определяются дефекты наполнения в желчном пузыре за счет наличия в нем камней.
- Обзорная рентгенография правого подреберья как метод диагностики ЖКБ не имеет в настоящее время самостоятельного значения. Она позволяет выявить лишь рентгенпозитивные конкременты (чаще всего известковые). Лабораторные исследования:
- общий анализ крови - лейкоцитоз с нейтрофилезом, сдвиг лейкоформулы влево, незначительное увеличения СОЭ;
- общий анализ мочи чаще всего в норме, можно выявить положительную реакцию на билирубин (при осложнении хронического холецистита обтурационной желтухой);
- биохимические показатели – гипербилирубинемия, преимущественно за счет конъюгированной фракции, гиперхолестеринемия, повышение других маркеров холестаза.
- иммуноферментный анализ на выявление гельминтов: описторхоз, лямблиоз, токсакароз, аскаридоз;
- копрологическое исследование.
Тактика лечения Стол N 5 по Певзнеру. частый дробный прием пищи (до 5-6 раз в день), снижение в пищевом рационе доли животных жиров и увеличение растительных; обогащение блюд пищевыми волокнами Антибактериальные препараты при хроническом некалькулѐзном холецистите назначаются в случае бактериальной этиологии:
- ампициллин 4-6 г/сут / цефазолин 2-4 г/сут / гентамицин 3-5 мг/кг/сут-не менее 8-10 дней. Миотропные спазмолитики:
1. Антихолинергические средства: - атропин 0,1% - 1 мл; - платифиллин 0,2% - 2 мл;
2. Спазмолитические средства: - дротаверин 2% 2-4 мл внутримышечно или внутривенно;
- папаверин 2% - 2 мл под кожу;
Подавление рвоты и тошноты при хроническом холецистите - Метоклопрамид 2 мл × 2 раза внутримышечно или внутривенно; Холелитолитические средства перорально Урсодезоксихолевая кислота по 8-15 мг/кг/сут в 2-3 приѐма внутрь в течение длительного времени (до 2 лет).
Хирургическое вмешательство:
Хронический калькулезный холецистит подлежит плановому оперативному вмешательству.
4. Воспалительные заболевания кишечника. Этиология, механизмы развития, клинические проявления. Диагностика. Дифференциальный диагноз с другими поражениями кишечника.+
Воспалительные заболевания кишечника представлены идиопатическими хроническими поражениями кишечника со сходной во многом клинической картиной.
В группу хронических ВЗК входят: ЯК, БК, микроскопический колит (коллагенозный и лимфоцитарный).
Язвенный колит — хроническое заболевание, характеризующееся непрерывным воспалением слизистой оболочки толстого кишечника при отсутствии гранулем в биопсийном материале с поражением прямой кишки и различным по протяженности поражением толстой кишки, имеющее рецидивное и ремиттирующее течение.
Болезнь Крона — гранулематозное воспаление кишки, характеризующееся развитием ее стеноза, образованием свищей и внекишечными проявлениями. Регионарные поражения могут возникать в любых отделах ЖКТ.
Коллагенозный и лимфоцитарный колиты представляют собой заболевания, при которых поражается мембрана слизистой оболочки кишечника. Эти две нозологические формы объединены в одну группу под общим названием «микроскопический колит».

+ генетические факторы (Выявлены гены и их мутации, ассоциированные с ВЗК)
Патогенез ВЗК – процесс сложного и комплексного взаимодействия различных патофизиологических механизмов аутоиммунного воспаления, развивающихся на фоне генетической предрасположенности к неадекватному иммунному ответу как со стороны иммунной системы организма в целом, так и со стороны локальной иммунной системы и пищеварительного тракта в частности.
Клиническая картина язвенного колита
Отмечается хроническая диарея, почти всегда ассоциированная с ректальным кровотечением или хотя бы с наличием видимой крови в стуле, ректальные императивные позывы, тенезмы, отхождение слизисто-гнойного экссудата, ночные дефекации и спастическую боль в животе, как правило, в левой подвздошной области, усиливающуюся перед дефекацией и стихающую после нее, иногда тяжелый запор. Системные проявления: снижение массы тела, лихорадка, тахикардия, иногда тошнота и рвота.
Клиническая картина болезни Крона
• Хроническая диарея, Длительность – более 6 недель , Примесь слизи или крови в стуле
• Боль в животе частая продолжительная в правой подвздошной области
- Необъяснимая анемия,интоксикация
• Необъяснимая лихорадка
• Снижение массы тела
• Наружные свищи, кишечная непроходимость (стриктуры)
• Длительно незаживающие анальные трещины, свищи прямой кишки
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ КОЛЛАГЕНОЗНОГО И ЛИМФОЦИТАРНОГО КОЛИТА
Водянистая диарея — патогномоничный симптом коллагенозного колита, наблюдающийся почти у всех пациентов. потеря массы тела, боли в животе, метеоризм, общая слабость, частота стула до 20 раз в сутки, объем стула до 5 л в сутки, стеаторея, лейкоциты в кале, редко примесь слизи и крови в кале, внекишечные проявления в виде артрита (не более чем у 5–10 % пациентов). Характерно длительное доброкачественное течение заболевания. Коллагенозный колит может сочетаться с другими заболеваниями аутоиммунной природы: синдромом Рейно, ревматоидным артритом, псориазом, спру, гипер- и гипотиреозом.
ИНСТРУМЕНТАЛЬНЫЕ И ЛАБОРАТОРНЫЕ МЕТОДЫ ДИАГНОСТИКИ
Обязательные инструментальные исследования следующие:
- пальцевое исследование прямой кишки;
- колоноскопия с биопсией;
- ирригоскопия;
- фиброгастродуоденоскопия с биопсией;
- ультразвуковое исследование органов брюшной полости; органов малого таза;
- обзорная рентгенография органов брюшной полости.
Дополнительные инструментальные исследования:
- дуодено-еюнальная биопсия для оценки виллиозной атрофии;
- энтерография;
- компьютерная томография органов брюшной полости; мрт
- радионуклидные исследования;
- хромоэндоскопия;
- капсульная эндоскопия.
Обязательные лабораторные исследования:
- общий анализ крови; мочи;
- альфа-амилаза мочи;
- анализ кала на скрытую кровь; на паразиты;на микрофлору;
- биохимическое исследование крови: глюкоза, аланинаминотрансфераза, аспартатаминотрансфераза, общий белок, альбумин, СРП, сывороточное железо;
- исследование иммунного статуса (классы сублимфоцитов, циркулирующие иммунные комплексы, уровни иммуноглобулинов, фагоцитарная активность);
- анализ крови на антиглиадиновые антитела;
- копрограмма.
Дополнительные лабораторные исследования:
- определение калия, натрия, кальция и хлоридов в сыворотке крови.
Дифференциальный диагноз БК чаще проводят с кишечным туберкулезом, болезнью Бехчета, нестероидиндуцированной энтеропатией, язвенным колитом, синдромом раздраженного кишечника, целакией. Реже БК приходится дифференцировать с ишемическим, микроскопическим, радиационным колитами; дивертикулитом\дивертикулезом; лимфомой или толстокишечным раком.
 Дифференциальный
диагноз.
При ЯК дифференциальный спектр чаще
представлен следующими заболеваниями:
инфекционный колит; БК; рак кишечника,
синдром раздраженного кишечника,
кишечный туберкулез, нестероидиндуцированная
энтеропатия. Более редкими заболеваниями
для дифференциального диагноза с ЯК
являются ишемический, микроскопический,
радиационный колиты; геморрагический
васкулит; болезнь Бехчета; колит при
ВИЧ-инфекции.
Дифференциальный
диагноз.
При ЯК дифференциальный спектр чаще
представлен следующими заболеваниями:
инфекционный колит; БК; рак кишечника,
синдром раздраженного кишечника,
кишечный туберкулез, нестероидиндуцированная
энтеропатия. Более редкими заболеваниями
для дифференциального диагноза с ЯК
являются ишемический, микроскопический,
радиационный колиты; геморрагический
васкулит; болезнь Бехчета; колит при
ВИЧ-инфекции.
5. Цирроз печени. Этиология. Критерии постановки диагноза. Осложнения. Тактика ведения.+
Цирроз печени – это диффузный процесс, характеризующийся фиброзом и трансформацией нормальной структуры печени с образованием узлов регенерации. Представляет собой финальную стадию ряда хронических заболеваний печени.
Этиология
– злоупотребление алкоголем (свыше 50%);
– вирусные гепатиты (чаще – хронический гепатит C, реже – гепатиты B, D).
Метаболические нарушения:
– перегрузка железом при наследственном гемохроматозе;
– перегрузка медью при болезни Вильсона;
– недостаточность α1-антитрипсина;
– кистозный фиброз;
– галактоземия и гликогенозы;
– наследственные тирозинемия и телеангиэктазия, порфирии.
Заболевания желчных путей:
– внепеченочная обструкция желчных путей;
– врутрипеченочная обструкция желчных путей (первичный билиарный цирроз, первичный склерозирующий холангит);
– холангиопатии у детей (прогрессирующий детский холестаз, артериопеченочная дисплазия, холестаз с лимфедемой, синдром Зельвегера);
– затруднение венозного оттока из печени (синдром Бадда – Киари, веноокклюзионная болезнь, выраженная правожелудочковая недостаточность);
– токсическое воздействие фармпрепаратов и токсинов также может спровоцировать возникновение цирроза.
Причиной цирроза могут стать иммунные изменения (аутоиммунный гепатит, болезнь «трансплантат против хозяина»), иные болезненные состояния (саркоидоз, неалкогольный стеатогепатит, гипервитаминоз A, криптогенный цирроз).
Диагностика цирроза печени базируется на трех группах критериев:
1. Оценка состояния функции печени (т.е. стадия печеночноклеточной недостаточности).
2. Оценка тяжести потальной гипертензии.
3. Оценка психического статуса пациента (стадия печеночной энцефалопатии).
Оценка состояния функции печени осуществляется по тем же клиническим данным и функциональным пробам печени, что и при хроническом гепатите (синдром цитолиза и холестаза, геморрагический синдром, нарушение белковообразовательной функции
Синдром портальной гипертензии: повышение давления в бассейне воротниковой вены. является следствием редукции кровотока (сдавление мелких почечных вен узлами регенерирующих гепатоцитов, редукция ветвей портальной вены и печночной артерии и сужение просвета синусоидов в результате воспалительного процесса в печени), что приводит к повышению портального давления и развитию анастомозов между портальной веной и полыми венами.
Синдром печеночной энцефалопатии
Печеночная энцефалопатия —является результатом токсического влияния на ЦНС продуктов метаболизма азотистых соединений, у здоровых людей, инактивируемых печенью.
ЛАБОРАТОРНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Клинический анализ крови. уменьшение количества тромбоцитов, анемия, панцитопения,
Коагулограмма. снижение протромбированного индекса
Анализы мочи.
Биохимический анализ крови. (АлАТ), (АсАТ), (ЩФ), (ГГТП), билирубин, альбумин, калий, натрий, креатинин.
Определение антител к вирусам хронического гепатита.
Определение концентрации IgA, IgM, IgG в сыворотке крови.
Определение содержания альфа-фетопротеина (АФП).
ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Ультразвуковое исследование брюшной полости.
Радионуклидное сканирование печени.
Компьютерная томография брюшной полости.
Биопсия печени.
Дополнительные методы обследования. Можно диагностировать наследственные заболевания (гемохроматоз, дефицит альфа1-антитрипсина, болезнь ВильсонаКоновалова, муковисцидоз) которые могут быть причиной развития цирроза печени.
Исследование показателей метаболизма железа.
Десфераловый тест. Десфераловый тест позволяет подтвердить наличие перегрузки железом: после внутримышечного 0,5 г дефероксамина (Десферал) суточная экскреция железа с мочой значительно превышает нормальный уровень (0–5 ммоль/сутки).
Определение активности альфа1-антитрипсина
Определение содержания галактозо-1-фосфатурилтрансферазы.
Осложнения ЦП: асцит; спонтанный бактериальный перитонит (СБП); печеночная энцефалопатия (ПЭ); варикозное расширение вен пищевода (ВРВП); гепаторенальный синдром (ГРС); синдром гиперспленизма; тромбоз портальной (ТВВ) и селезеночной (ТСВ) вен; гепатоцеллюлярная карцинома (ГЦК) (может быть условно отнесена к осложнениям ЦП, так как в большинстве случаев возникает на его фоне).
лечение: Режим: запрет на курение; ограничение физической нагрузки у пациентов с декомпенсированным заболеванием печени и при наличии варикозного расширения вен ЖКТ. Диета: Запрет на потребление алкоголя; Принципы рационального питания; Ограничение поваренной соли · Рекомендации, специфические для конкретной этиологии ЦП (например, исключение продуктов, содержащих медь при болезни Вильсона-Коновалова) · Рекомендации, специфичные для конкретного осложнения ЦП (например, бессолевая диета при асците, ограничение жидкости при гипонатриемии ниже 120 ммоль/л на фоне отечно-асцитического синдрома) Медикаментозное лечение предусматривает: ·Отмена гепатотоксичных препаратов; ·Этиотропная терапия (например, противовирусную терапию при вирусной этиологии ЦП или абстиненцию при алкогольной этиологии, что во многих случаях способствует замедлению прогрессирования и даже регрессу заболевания) ·Базисную патогенетическую терапию (например, преднизолон и азатиопринпри ЦП в исходе аутоиммунного гепатита, D-пеницилламин при ЦП в исходе болезни Вильсона-Коновалова, урсодезоксихолевая кислота при первичном билиарном циррозе, aдeмeтиоинин при алкогольном ЦП, флеботомии и десферал при гемохроматозе, что во многих случаях способствует замедлению прогрессирования заболевания и повышению выживаемости пациентов) ·Терапию осложнений ЦП, а также их первичную и вторичную профилактику; ·Профилактика инфекций: вирусных гепатитов, бактериальных инфекций (сепсиса, менингита, пневмонии и других) ОРВИ путем вакцинации, а также своевременной антибактериальной терапии.
6. Синдром дисфагии. Дифференциальная диагностика заболеваний, сопровождающихся дисфагией и одинофагией. Эзофагиты. Тактика ведения и лечения больных с эзофагитами+
Дисфагия - нарушение глотания и прохождения пищи по пищеводу.
Основные заболевания и патологические состояния, при которых наблюдается дисфагия
1. Органические заболевания пищевода:Стеноз пищевода; Доброкачественные опухоли пищевода; Рак пищевода; зофагит острый, хронический, рефлюкс-эзофагит; Дивертикулы пищевода; Язва пищевода
2. Сужения пищевода, вызванные патологическими изменениями в соседних органах: Опухоли и кисты средостения; Задний медиастинит; Плевропульмональный фиброз; Митральный порок; Аневризма аорты; Увеличение щитовидной железы; Шейный остеохондроз и инородные тела
3. Заболевания центральной и периферической нервной и мышечной системы: Эзофагоспазм; Ахалазия кардии; Атония пищевода; Желудочно-пищеводный рефлюкс
4. Лекарственные, психогенные воздействия, психические заболевания
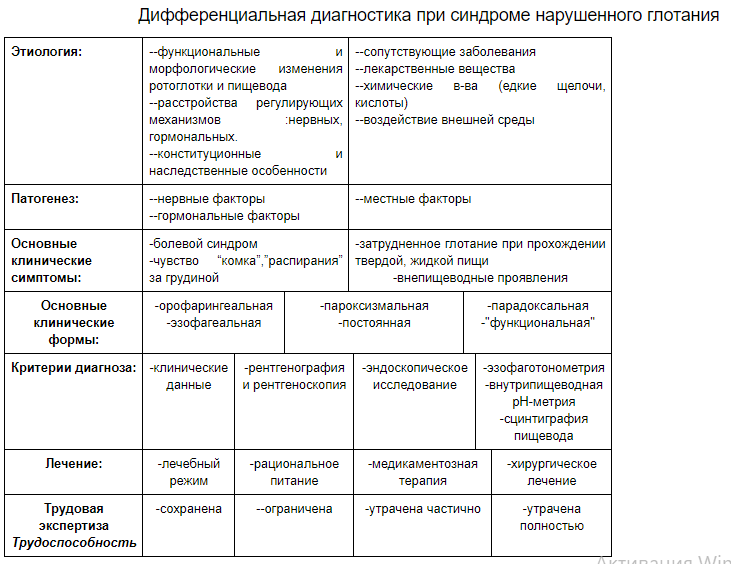
Эзофагит - заболевание пищевода, сопровождающееся воспалением его слизистой оболочки вследствие различных причин.
Эзофагит по течению может быть острым, подострым и хроническим. По характеру воспалительного процесса и его выраженности различают катаральный, отечный, эрозивный, псевдомембранозный, геморрагический, эксфолиативный, некротический и флегмонозный эзофагиты. Катаральный и отечный эзофагит (наиболее часто встречающиеся формы) ограничиваются гиперемией слизистой и ее отеком. При остром инфекционном процессе, а также химических и тепловых ожогах пищевода возможно развитие эрозий слизистой оболочки (эрозивный эзофагит). При тяжелом течении инфекции нередко происходит развитие некротической формы. Геморрагический эзофагит сопровождается кровоизлияниями в стенку пищевода. При псевдомембранозной форме фиброзный экссудат не сращен с подслизистой тканью в отличие от эксфолиативного эзофагита. Флегмона пищевода, как правило, развивается при повреждении стенки пищевода инородным телом.
Симптомы : затруднения и/или болезненные ощущения при глотании, изжога, боли во рту, ощущение чего-то застрявшего в горле, тошнота, рвота,
при остром возможно повышение температуры тела, наблюдается общее недомогание,
Хронический сопровождается болями за грудиной и в подложечной области
Инструментальная диагностика: - рентгенологическое исследование;
- эзофагоскопия;
- эзофагоманометрия (фиксирует различные по характеру нарушения моторики пищевода);
- мониторная рН-метрия пищевода; - эндоскопическое исследование желудочно-кишечного тракта.
Обязательные исследования: - общий анализ крови с определением ретикулоцитов, тромбоцитов; - общий анализ мочи. Дополнительные исследования: биохимический анализ крови (общий белок, альбумин, С-реактивный белок, сиаловые кислоты, глюкоза, АлАТ, АсАТ, билирубин, амилаза, ЩФ, мочевина, креатинин, электролиты). При остром эзофагите: бактериологический анализ мазков со стенок пищевода, ПЦР с биоптатами слизистой оболочки пищевода для этиологической верификации острого эзофагита.
Дифференциальный диагноз при эзофагите проводится в первую очередь с ГЭРБ (отсутствие эффекта от антирефлюксной терапии). Также с врожденными мембранами пищевода, стриктурами пищевода, неврогенной анорексией, поражениями пищевода при склеродермии, опухолями пищевода, термическими, химическими, лучевыми поражениями и т.д.
1. Медикаментозная терапия:
- прием антацидов;
- антисекреторные препараты;
- прокинетики; - анальгетики, седативные средства; - при подтверждении соответствующей этиологии назначаются антибактериальные, противовирусные, противогрибковые, противотуберкулезные средства. 2. Немедикаментозные методы. Общие рекомендации:
- после принятия пищи избегать наклонов вперед, не ложиться в течение 1,5 часов;
- спать с приподнятым не менее чем на 15 см головным концом кровати;
- не носить тесную одежду и тугие пояса;
- ограничить потребление продуктов, которые агрессивно действуют на слизистую оболочку пищевода (жиры, алкоголь, кофе, шоколад, цитрусовые); - селективная диета при эозинофильном эзофагите;
- отказаться от курения. Хирургическое лечение
Показания:
- безуспешность консервативного лечения;
- осложнения эзофагита (стриктуры, повторные или массивные кровотечения);
- частые аспирационные пневмонии;
- пищевод Барретта (из-за опасности малигнизации).
Хроническое прогрессирующее течение делает необходимым наблюдение у специалиста-гастроэнтеролога с проведением ЭГДС и биопсии минимум 1 раз в год.
7. Аутоиммунный гепатит. Патогенез. Клиническая картина. Диагностические критерии. Классификация. Особенности ведения и лечения больных.+
- характеризуется наличием тканевых антител, отсутствием других причин, вызывающих хронический гепатит. В зависимости от антител выделяют 3 типа аутоиммунного гепатита: I тип - антитела к гладкой мускулатуре, антинуклеарные антитела, антиактиновые антитела; II тип - антитела к печеночно-почечным микросомам, антимикросомальные антитела, антитиреоидные антитела, антиостровковые антитела (чаще наблюдается в возрасте 2-14 лет); III тип - антитела к печеночному растворимому антигену (чаще наблюдается у женщин в возрасте 20-70 лет). Клиника: 1) чаще наблюдается у женщин; 2) начальная стадия: лихорадка; картина, характерная для острого вирусного гепатита; 3) развернутая стадия: лихорадка, артралгии, кожная сыпь, желтуха; малая печеночная недостаточность: телеангиоэктазии, пальмарная эритема, миалгии; эндокринные нарушения: аменоррея, стрии, гирсутизм; системность проявлений: полисерозит, миокардит, гломерулонефрит, язвенный колит, синдром Шегрена, гемолитическая анемия, поражение щитовидной железы, лимфоаденопатия. Лабораторные критерии: 1) повышение уровня билирубина и трансаминаз более, чем в 10 раз; 2) гаммаглобулинемия; 3) ЛЕ-феномен, наличие антинуклеарного фактора; 4) антитела к гладкой мускулатуре, клеткам почечных канальцев, паренхиме печени. Лечение: иммуносупрессорная терапия - показания: а) клинические критерии тяжелое течение - желтуха, системные проявления, прекома; б) биохимические критерии: гаммаглобулинемия более 30-40%, повышение активности трансаминаз более, чем в 5 раз, повышение тимоловой пробы в 3 и более раз; в) иммунологические критерии: повышение IgG более 2000 мг/100 мл, высокие титры антител к гладкой мускулатуре, нарушение иммунорегуляции (повышенная активность, дефект суппрессорной активности); г) морфологические критерии: ступенчатые, мостовые или мультиформные некрозы. С целью иммуносупрессии применяют: 1) кортикостероиды - преднизолон 30-40 мг в день в течение 4-10 недель с последующим снижением до поддерживающей дозы 10-20 мг; 2) азатиоприн - 50-100 мг в день; 3) делагил - при нерезко выраженной активности - 0,25-0,5 г.
8. Дифференциальный диагноз и врачебная тактика при заболеваниях желчевыводящих путей и поджелудочной железы.+
Клинические стадии (фазы) острого панкреатита
I стадия – шока, гемодинамических нарушений 1-3 суток.
II стадия – функциональной недостаточности паренхиматозных органов (5-7 сутки).
III стадия – постнекротических и гнойных осложнений (2-4 недели).
Клиника зависит от морфологических изменений и фазы процесса.
1. Выраженная боль в эпигастрии с иррадиацией в поясницу или опоясывающего характера.
2. Тошнота.
3. Рвота (неукротимая, не приносящая облегчения)
4. Бледность кожных покровоч иногда с наличием цианоза (с-м Мондора), холодного липкого пота.
5. Субиктеричность или желтуха кожи и слизистых оболочек.
6. Брадикардия, сменяющаяся тахикардией.
7. Артериальная гипертензия.
8. Коллапс (при деструктивном панкреатите).
9. Резкая болезненность в эпигастрии при мягком животе.
10. Вздутие живота в подчревной области (с-м Боде).
11. Ригидность брюшной стенки в проекции поджелудочной железы (с-м Керте), "резиновый живот" по Мондору.
12. Болезненность при надавливании в левом реберно-позвоночном углу (с-м Мейо-Робсона).
13. Исчезновение пульсации в надчревной области (с-м Воскресенского).
14. Болезненность при перкуссии над поджелудочной железой (с-м Раздольского, Менделя).
15. Симптом Грей-Турнера – цианоз кожи на боковых областях живота.
16. Симптом Кулена – цианоз кожи вокруг пупка.
17. Симптом Грюнвальда – кровоизлияния вокруг пупка.
Диагностика
1. Ультразвуковая диагностика: увеличение размеров, снижение эхогенности, "размытости" контуров, скопление жидкости вблизи железы, сопутствующий холедохолитиаз и др.
2. Лабораторные методы:
общий анализ крови (нейтрофильный лейкоцитоз со сдвигом формулы влево, ускоренное РОЭ)
биохимический анализ крови (повышение активности амилазы, липазы, трипсина), снижение активности ингибиторов трипсина, повышение уровня билирубина, гипергликемия, снижение кальция);
анализ свертывающей системы крови (гиперкоагуляция при отечной форме и жировом панкреонекрозе, гиперкоагуляция - при геморрагическом панкреонекрозе, гиперфибриногенемия);
изменение калликреин-кининовой системы (снижение уровня кининогена, прекалликреина, ингибитора калликреина);
анализ мочи (амилазурия, резкое снижение суточного и часового диуреза вплоть до анурии, протеинурия, микрогематурия, цилиндрурия);
соотношение клиренса амилазы и клиренса криатенина более 5.
3. Рентгенодиагностика;
обзорная рентгеноскопия (высокое стояние левой половины диафрагмы, ограничение ее подвижности, выпот в левом плевральном синусе, парез кишечника);
контрастное исследование желудка и 12-перстной кишки (смещение желудка кпереди, расширение петли 12-перстной кишки);
компьютерная томография.
4. Специальные методы исследования:
гастро- и дуоденоскопия (огтеснение задней стенки желудка и привратника, гиперемия, отек и эрозии в области оттеснения, разворот петли 12-перстной кишки, дуоденит);
лапароскопия (бляшки очаговых некрозов жировой ткани, выпот в брюшной полости с высокой активностью ферментов).
Дифференциальный диагнозпроводится со следующими заболеваниями: 1. Острый холецистит. 2. Прободная язва желудка и 12-перстной кишки. 3. Острый аппендицит. 4. Острая кишечная непроходимость. 5. Острый гастрит. 6. Пищевая токсикоинфекция. 7. Инфаркт миокарда.
9. Хронический панкреатит. Классификации. Основные клинические синдромы. Методы диагностики. Осложнения хронического панкреатита.
Хронический панкреатит (ХП) – хроническое полиэтиологическое воспаление поджелудочной железы, продолжающееся более 6 месяцев, характеризующееся постепенным замещением паренхиматозной ткани соединительной и нарушением экзо- и эндокринной функции органа.
Эпидемиология: чаще страдают мужчины среднего и пожилого возраста; частота у взрослых 0,2-0,6%
Основные этиологические факторы:
1) алкоголь – основной этиологический фактор (особенно при сочетании с курением)
2) заболевания желчного пузыря и желчевыводящих путей (хронический калькулезный и бескаменный холецистит, дискинезии желчевыводящих путей)
3) злоупотребление жирной, острой, соленой, перченой, копченой пищей
4) лекарственная интоксикация (в первую очередь эстрогены и ГКС)
5) вирусы и бактерии, попадающие в проток поджелудочной железы из ДПК через фатеров сосочек
6) травмы поджелудочной железы (при этом возможно склерозирование протоков с повышением внутрипротокового давления)
7) генетическая предрасположенность (часто сочетание ХП с группой крови О(I)
8) беременность на поздних сроках (приводит к сдавления поджелудочной железы и повышению внутрипротокового давления)
Патогенез хронического панкреатита: В развитии хронического панкреатита основную роль играют 2 механизма: 1) чрезмерная активация собственных ферментов поджелудочной железы (трипсиногена, химотрипсиногена, проэластазы, липазы). 2) повышение внутрипротокового давления и затруднение оттока поджелудочного сока с ферментами из железы
В результате наступает аутолиз (самопереваривание) ткани поджелудочной железы; участки некроза постепенно замещается фиброзной тканью.
Алкоголь является как хорошим стимулятором секреции соляной кислоты (а она уже активируют панкреатические ферменты), так и приводит к дуоденостазу, повышая внутрипротоковое давление.
Классификация хронического панкреатита:
I. По морфологическим признакам: интерстициально-отечный, паренхиматозный, фиброзно-склеротический (индуративный), гиперпластический (псевдотуморозный), кистозный
II. По клиническим проявлениям: болевой вариант, гипосекреторный, астеноневротический (ипохондрический), латентный, сочетанный, псевдотуморозный
III. По характеру клинического течения: редко рецидивирующий (одно обострение в 1-2 года), часто рецидивирующий (2-3 и более обострений в год), персистирующий
IV. По этиологии: билиарнозависимый, алкогольный, дисметаболический, инфекционный, лекарственный
Клиника хронического панкреатита: 1) боль – может быть внезапной, острой или постоянной, тупой, давящей, возникает через 40-60 мин после еды (особенно обильной, острой, жареной, жирной), усиливается в положении лежа на спине и ослабевает в положении сидя при небольшом наклоне вперед, локализована при поражении головки - справа от срединной линии, ближе к правому подреберью, при поражении тела - по срединной линии на 6-7 см выше пупка, при поражении хвоста - в левом подреберье, ближе к срединной линии; в 30% случаев боль носит опоясывающий характер, еще в 30% - не имеет определенной локализации; половина больных ограничивают себя в приеме пищи из-за боязни болей
2) диспепсический синдром (отрыжка, изжога, тошнота, рвота); рвота у части больных сопровождают болевой синдром, многократная, не приносит никакого облегчения
3) синдром экзокринной недостаточности поджелудочной железы: «панкреатогенная диарея» (связана с недостаточным содержанием в выделенном панкреатическом соке ферментов, при этом характерно большое количество каловых масс, содержащих много нейтрального жира, непереваренных мышечных волокон), синдром мальабсорбции, проявляющийся рядом трофических нарушений (снижение массы тела, анемия, гиповитаминоз: сухость кожи, ломкость ногтей и выпадение волос, разрушение эпидермиса кожи)
4) синдром эндокринной недостаточности (вторичный сахарный диабет).
Диагностика хронического панкреатита:
1. Сонография поджелудочной железы: определение ее размеров, эхогенности структуры
2. ФГДС (в норме ДПК, как «корона», огибает поджелудочную железу; при воспалении эта «корона» начинает расправляться – косвенный признак хронического панкреатита)
3. Рентгенография ЖКТ с пассажем бария: контуры ДПК изменены, симптом «кулис» (ДПК выпрямляется и раздвигается, как кулисы на сцене, при значительном увеличении pancreas)
4. КТ – в основном используется для дифференциальной диагностики ХП и рака поджелудочной железы, т.к. их симптомы схожи
5. Ретроградная эндоскопическая холангиодуоденопанкреатография - через эндоскоп специальной канюлей входят в фатеров сосочек и вводят контраст, а затем делают серию рентгенограмм (позволяет диагностировать причины внутрипротоковой гипертензии)
6. Лабораторные исследования: а) ОАК: при обострении - лейкоцитоз, ускорение СОЭ. б) ОАМ: при обострении - увеличение диастазы. в) БАК: при обострении - повышение уровня амилазы, липазы, трипсина. в) копрограмма: нейтральный жир, жирные кислоты, непереваренные мышечные и коллагеновые волокна
Лечение хронического панкреатита.
1. При обострении - стол № 0 в течение 1-3 дней, затем стол № 5п (панкреатический: ограничение жирной, острой, жареной, пряной, перченой, соленой, копченой пищи); вся пища вареная; питание 4-5 раз/сутки малыми порциями; отказ от употребления алкоголя
2. Купирование боли: спазмолитики (миолитики: папаверин 2% – 2 мл 3 раза/сут в/м или 2% – 4 мл на физрастворе в/в, дротаверин / но-шпа 40 мг 3 раза/сут, М-холиноблокаторы: платифиллин, атропин), анальгетики (ненаркотические: анальгин 50% – 2 мл в/м, в тяжелых случаях – наркотические: трамадол внутрь 800 мг/сут).
3. Антисекреторные препараты: антациды, блокаторы протонной помпы (омепразол по 20 мг утром и вечером), блокаторы Н2-рецепторов (фамотидин по 20 мг 2 раза/сут, ранитидин) – снижают секрецию желудочного сока, который является естественным стимулятором секреции поджелудочной железы
4. Ингибиторы протеаз (особенно при интенсивном болевом синдроме): гордокс, контрикал, трасилол, аминокапроновая кислота в/в капельно, медленно, на физрастворе или 5% растворе глюкозы, октреотид / сандостатин 100 мкг 3 раза/сут п/к
5. Заместительная терапия (при недостаточности экзокринной функции): панкреатин 0,5 г 3 раза/сут во время или после еды, креон, панцитрат, мезим, мезим-форте.
6. Витаминотерапия – для предупреждения трофических нарушений как результата синдрома мальабсорбции
7. Физиотерапия: ультразвук, синусомоделированные токи различной частоты, лазер, магнитотерапия (при обострении), тепловые процедуры: озокерит, парафин, грязевые аппликации (в фазе ремиссии)
Диспансерное наблюдение: 2 раза/год на уровне поликлиники (осмотр, основные лабораторные тесты, УЗИ).
10. Псевдомембранозный колит
Псевдомембранозный колит — болезнь, обусловленная чрезмерным размножением Clostridium difficile, характеризуется острым началом, тяжелой диареей, гиповолемическим шоком, токсическим расширением толстой кишки, перфорацией слепой кишки, тромбогеморрагическим синдромом и без лечения приводит к гибели больного.
Этиология. Возбудители —Clostridium difficileобладают свойствами, общими и для других видов клостридий. Паразитируют в кишечнике человека. На искусственных питательных средах образуют большое количество газа и споры. Токсигенные штаммы возбудителя образуют токсин А (летальный энтеротоксин) и токсин В (цитотоксин). Около 5% здоровых людей являются носителями токсигенных клостридий. Заболевание возникает в результате бурного размноженияCl. difficile, что наблюдается при дисбактериозе, обусловленном применением антибиотиков широкого спектра действия. Клостридии чувствительны к метронидазолу и ванкомицину. Заболевание чаще развивается после применения клиндамицина, ампициллина, цефалоспоринов и аминогиликозидов. Реже возникновение заболевания связано с другими антибиотиками (исключением является ванкомицин и стрептомицин).
Эпидемиология. Заболевание чаще возникает как результат активизации эндогенной инфекции. Носителями клостридий являются здоровые люди, у 5% здоровых людей отмечается носительство токсигенных штаммов клостридий. Дети значительно чаще являются носителями токсигенных штаммов, но заболевание у них развивается реже, что связывают с наличием протективных антител, полученных от матери. Нормальная микрофлора тормозит размножение клостридий. У носителей (здоровых) при бактериологическом исследовании обнаруживаются лишь единичные колонии в расчете на 1 г испражнений, тогда как у больных псевдомембранозным колитом в 1 г испражнений содержится 104–105микроорганизмов. Споры клостридий устойчивы во внешней среде, и в некоторых случаях споры могут разноситься и руками медицинского персонала. В этих случаях можно говорить об экзогенной внутрибольничной инфекции. Заболевание может возникнуть иногда даже после кратковременного курса применения антибиотиков. Болезнь может возникнуть и при длительном (6 нед) применении химиопрепаратов, например, при лечении больных новообразованиями метатрексатом.
Патогенез. Псевдомембранозный колит развивается в результате воздействия токсинов, продуцируемыхCl. difficile. Выделенные от больных микробы продуцируют два токсина: токсин А — летальный энтеротоксин, обусловливающий кровоизлияния и секрецию жидкости в кишечнике, и токсин В — цитотоксин, обладающий цитопатическим эффектом в культуре ткани. В патогенезе болезни играют роль оба токсина, однако в начальный период заболевания большая роль принадлежит токсину А. Оба токсина разрушают клеточные мембраны, микрофилярии и синтез протеина. Бурное размножение клостридий и продукция ими токсинов является результатом дисбактериоза, когда антибиотики подавляют конкурентов клостридий в нормальной микрофлоре кишечника.
Симптомы и течение. Инкубационный период при эндогенной инфекции определить трудно. Однако если считать от начала антибиотикотерапии, то болезнь может развиться как после кратковременного курса (5–7 сут), так и после длительных (до 6 нед) курсов химиотерапии. Заболевание начинается остро. Появляется обильный, жидкий, водянистый, зеленоватого цвета стул с резким гнилостным запахом, с примесью крови. Появляются сильные схваткообразные боли в животе. Температура тела повышается до 39,5°С и выше. При пальпации отмечается спазм и болезненность кишечника. Развиваются и нарастают признаки обезвоживания (уменьшение массы тела, сухость кожи и слизистых оболочек, тахикардия, снижение АД, осиплость голоса, цианоз, судороги и др.), может развиться гиповолемический шок. В крови значительный лейкоцитоз, снижение количества альбуминов. Иногда псевдомембранозный колит протекает без поноса, что приводит к запоздалой диагностике и развитию тяжелых осложнений, таких как токсическая мегаколон и перфорация слепой кишки, что приводит к разлитому перитониту и гибели больных. В некоторых случаях в самом начале болезни, когда на фоне антибиотикотерапии появляется диарея, отмена антибиотиков может быстро привести к обратному развитию без появления характерной симптоматики.
Диагноз и дифференциальный диагноз. При распознавании псевдомембранозного колита учитывается прежде всего то, что болезнь появилась после использования антибиотиков. Клиническими особенностями является высокая лихорадка, появление водянистого стула с гнилостным запахом, развитие дегидратации, высокий лейкоцитоз. Доброкачественная неспецифическая диарея, которая может наблюдаться при антибиотикотерапии, не сопровождается лихорадкой и лейкоцитозом, самочувствие больного остается удовлетворительным.
В настоящее время хорошо отработаны диагностические критерии, позволяющие достоверно распознавать псевдомембранозный колит [R. Fekety, А. В.Shah, 1993]. Большое диагностическое значение имеет эндоскопия. В 90% случаев достаточно провести ректороманоскопию и лишь у 10% больных возникает необходимость использовать фиброколоноскопию. При ректороманоскопии выявляется гиперемия, отечность, легкая ранимость слизистой оболочки кишки. Поверхность зернистая, отмечаются геморрагии, слизистые псевдомембраны, моторика кишки повышена. Эндоскопический диагноз псевдомембранозного колита почти всегда (в 95%) удается подтвердить выделением Cl. difficile. При отсутствии псевдомембран делается биопсия слизистой оболочки кишки и при гистологическом исследовании можно обнаружить характерные изменения. При компьютерной томографии обнаруживается утолщение или диффузный отек стенки толстой кишки с явлениями периколита.
Для выделения культуры возбудителя используются селективные среды. Если данные эндоскопии не дают достаточных оснований для диагностики псевдомембранозного колита, то используется метод обнаружения в испражнениях токсина А (энтеротоксин) или токсина В (цитотоксин), продуцируемых Cl. difficile. Диагностическое значение имеет изменение течения болезни (улучшение) после отмены антибиотиков.
Дифференциальный диагноз необходимо проводить от стафилококкового энтероколита, который также может возникать при проведении антибиотикотерапии. Он также протекает тяжело и по клиническим проявлениям может напоминать клостридиозный колит. Диагноз базируется на отрицательных результатах исследований на клостридиоз и обнаружение в стуле грамположительных кокков.
Лечение. Прежде всего необходимо прекратить антибиотикотерапию, с которой связано развитие псевдомембранозного колита, а также восстановление потерь жидкости и электролитов. У 25% больных только это мероприятие через несколько дней дает хороший результат. Если этого недостаточно, переходят к противоклостридиозной химиотерапии. Препараты назначают преимущественно пероральным путем, так какCl. difficileредко внедряются в слизистую оболочку толстой кишки. Терапевтический эффект обусловлен созданием в просвете кишки большой концентрации химиопрепарата, что прекращает продукцию токсинов и повреждения им слизистой оболочки кишки. Все штаммы возбудителя высоко чувствительны к ванкомицину и почти все — к метронидазолу.
При пероральном применении метронидазол активен как против Cl. difficile, так и по отношению к некоторым другим возбудителям острых энтероколитов. При внутривенном введении метронидазол неэффективен. Метронидазол частично всасывается в тонком кишечнике, однако и в просвете толстой кишки создается ингибирующая концентрация. Лечение легких и среднетяжелых форм начинают с назначения метронидазола (учитывают и то, что ванкомицин имеет очень неприятный вкус и в 50 раз дороже метронидазола). Метронидазол не оказывает терапевтического эффекта при стафилококковых энтероколитах.
Ванкомицин является предпочтительным пероральным антибиотиком для лечения тяжелых форм псевдомембранозного колита. Он является антибиотиком выбора и для лечения стафилококковых энтероколитов. Ванкомицин назначают перорально, так как при внутривенном введении он не обусловливает достаточной концентрации в просвете кишки.Сl. difficileвесьма чувствительна к ванкомицину в концентрации 16 мг/л и менее. Так как ванкомицин не всасывается в желудочно-кишечном тракте, то при пероральном назначении в дозах 0,5–2 г/сут (разделить на 3–4 приема) создается концентрация в испражнениях 500–2000 мг/л. Даже относительно небольшие дозы ванкомицина (125–250 мг 4 раза в день) дают достаточно высокую концентрацию в стуле даже при наличии у больного профузного поноса. При назначении ванкомицина выраженное улучшение отмечается уже через 3–4 дня. Для подавления возбудителя и прекращения продукции токсинов достаточно 10-дневного курса лечения. После курса лечения могут некоторое время сохраняться повышение температуры тела и понос как результат еще незакончившегося воспалительного процесса в толстой кишке. Очень неприятный (горький) вкус ванкомицина может быть преодолен при использовании капсул, введения ванкомицина через назогастральный зонд или в клизме (через длинную трубку).
У 10–20 % больных через 1–4 нед после окончания лечения наступают рецидивы псевдомембранозного колита за счет сохранившихся в кишечнике спор или в результате нового заражения. Рецидивы хорошо поддаются терапии метронидазолом и ванкомицином, если лечение начать рано. При многократных рецидивах применяют длительный курс лечения ванкомицином (4–6 нед) или несколько 5–7-дневных курсов с перерывами между ними. Используют бактериальные препараты для восстановления нормальной микрофлоры кишечника.
11. Дифференциальная диагностика и врачебная тактика при болях в правом подреберье в практике врача-терапевта.+
- заболевания 12пк, желчевыводящих путей, печени, а также при внеабдоминальных заболеваниях (правосторонней пневмонии, правостороннем пиелонефрите, пузырно-мочеточниковом рефлюксе, уролитиазе) +боли в правом подреберье.
- Печеночная колика характеризуется острой, схваткообразного характера болью в эпигастральной области или в правом подреберье, быстро купирующейся спазмолитическими препаратами.
Тактика:сбор анамнеза,объектив данные, лаб диаг-ка(КАК,ОАМ,БХ), исслед на H.pylori, инструмент обслед (ФГДС, рентген,колоноскопия,рентген с барием),УЗИ орг брюш полости, ЭКГ, ФЛГ+консульт хирурга.
12. Маркеры цитолитического синдрома. Дифференциальный диагноз заболеваний печени, сопровождающихся синдромом цитолиза+
- повреждение клеток печени. Неспецифическая реакция клеток печени на действие повреждающих факторов. В основе цитолитического синдрома лежит изменение проницаемости мембран клеток и их органел, что приводит к выходу составных частей клеток в межклеточное пространство и в кровь. Эти нарушения могут быть обратимыми и необратимыми.
Опорные признаки:
1. В крови: гиперферментемия - АлАТ, АсАТ, ГлДГ, ЛДГ, альдолаза, гипербилирубинемия (преимущественно за счет прямого билирубина), повышение уровня сывороточного железа и витамина В12, гипоальбуминемия, уменьшение содержания факторов свертывания крови: фибриногена, протромбина, акцелерина, проконвертина, антигемофильных глобулинов.
2. Снижение толерантности к алкоголю.
3. Астенический синдром.
4. Диспептический синдром.
5. Нервно-психические расстройства.
6. Геморрагический диатез.
7. Эндокринные нарушения.
8. Кожные нарушения.
9. Отечно-асцитический синдром.
10. Печеночный запах.
Субъективные и объективные клинические симптомы, наблюдающиеся при цитолитическом синдроме, сводятся, по сути, к клиническим признакам печеночно-клеточной недостаточности.
13. Синдром холестаза. Дифференциальная диагностика заболеваний печени, сопровождающихся холестазом. Тактика ведения.+
 Холестаз
представляет собой нарушение синтеза,
секреции и оттока желчи. Клинические
признаки холестаза – слабость, кожный
зуд и в ряде случаев желтуха. Биохимические
маркеры холестатического синдрома: -
Щелочная фосфатаза (ЩФ);
Гаммаглютамилтранспептидаза (ГГТП);
-Лейцинаминопептидаза; - 5-нуклеотидаза.
Внепеченочный
холестаз обусловлен
нарушением оттока за счет желчемеханических
факторов (камень, опухоль). Внутрипеченочный
холестаз подразделяется:
1) внутридольковый (или печеночно-канальный);
2) междольковый (или протоковый).
Внутридольковый холестаз обусловлен
недостаточной секрецией желчи клетками
печени или желчными канальцами из-за
повреждения клеточных органелл.
Междольковый холестаз связан с
обструктивно-воспалительным процессом
в портальных полях.
Холестаз
представляет собой нарушение синтеза,
секреции и оттока желчи. Клинические
признаки холестаза – слабость, кожный
зуд и в ряде случаев желтуха. Биохимические
маркеры холестатического синдрома: -
Щелочная фосфатаза (ЩФ);
Гаммаглютамилтранспептидаза (ГГТП);
-Лейцинаминопептидаза; - 5-нуклеотидаза.
Внепеченочный
холестаз обусловлен
нарушением оттока за счет желчемеханических
факторов (камень, опухоль). Внутрипеченочный
холестаз подразделяется:
1) внутридольковый (или печеночно-канальный);
2) междольковый (или протоковый).
Внутридольковый холестаз обусловлен
недостаточной секрецией желчи клетками
печени или желчными канальцами из-за
повреждения клеточных органелл.
Междольковый холестаз связан с
обструктивно-воспалительным процессом
в портальных полях.
Лечение: Консервативная терапия начинается с диеты с ограничением нейтральных жиров и добавлением в рацион жиров растительного происхождения. Это объясняется тем, что всасывание таких жиров происходит без использования желчных кислот. Лекарственная терапия включает назначение препаратов урсодезоксихолевой кислоты, гепатопротекторов (адеметионина), цитостатиков (метотрексата). Дополнительно применяется симптоматическая терапия: антигистаминные препараты, витаминотерапия, антиоксиданты. Лечение синдрома холестаза: Диетические рекомендации (нейтр. жиры – при стеаторее не более 40 г/сут, триглицериды со средней длиной цепи – 40 г/сут (кокосовое масло); Витамин А 100000 МЕ в/м 1 р. в месяц; Витамин Е 10 – 50 мг в/м в сутки; Витамин К – 10 мг в/м в сутки (5 – 10 дней); Витамин D2 (эргокальциферол) 100000 МЕ в месяц в/м, Витамин D3 – альфа D3 ТЭВА 1 мкг в сутки; Кальций – 1,5 г per os (карбонат кальция), глюконат Ca в/в капельно 15 мг/кг 7 дней – при сильных болях в костях; Комбинированные препараты (витрум – кальций D, кальций D3 – Никомед);
Лечение кожного зуда: Холестирамин 4 – 16 г в сутки (при достижении эффекта можно снизить дозу) – препарат выбора (эффект наступает минимум через 1 неделю, полный эффект – не менее чем через 2 месяца) Билигнин 5 – 10 г в сутки, активированный уголь 10 – 20 г в сутки; Урсодезоксихолевая кислота (урсофальк, урсосан) 10 – 15 мг/кг в сутки – кожный зуд ослабевает через несколько месяцев; При рефрактерном зуде: гептрал 800 мг в/в 7-21 день, затем 800 мг * 2р. в день per os, фототерапия, плазмаферез; Индукторы микросомальных ферментов (при неэффективности холестирамина в максимальных дозах): фенобарбитал 30 – 180 мг, зиксорин 300 – 400 мг, рифампицин 300 – 600 мг; Антагонисты опиоидных рецепторов: налоксон 0,4 – 2 мг в/в, налмефен 5 – 80 мг; Ондансетрон (осетрон, зофран) 8 – 16 мг в сутки; Эстрогены, анаболики, ГКС, метронидазол (небольшое число наблюдений);
14. Дифференциальная диагностика заболеваний, сопровождающихся гепатомегалией. Алгоритм обследования.
Расспрос. Сведения о профессии и образе жизни больного помогают выявить длительный контакт с промышленными ядами или инсектицидами и заподозрить такие инфекции и инвазии, как лептоспироз, эхинококкоз, наиболее частые у людей, занятых в сельском хозяйстве. Важны указания на периоды голодания больного, в частности недостаток белка в пищевом рационе и длительные заболевания желудочно-кишечного тракта, ведущие к белково-витаминному дефициту. Употребление алкоголя + лекарства. Семейный анамнез позволяет заподозрить наследственные заболевания - доброкачественные гипербилирубинемии, гемолитическую анемию. Неврологические расстройства и патология печени у ближайших родственников.
Эпидемиологический анамнез. Важно установить были ли контакты с больными вирусным гепатитом, предшествовавшие данному заболеванию, а также инфекции, переливания крови, стоматологические вмешательства, операции, иньекционная или инфузионная терапия, хронический гемодиализ и другие манипуляции с повреждением кожи и слизистых оболочек, а также наличие наркомании, беспорядочной половой жизни, половых извращений.
Диспепсический синдром наблюдается при многих болезнях печени и желчных путей, особенно при острых гепатитах, ЦП, холелититазе. Плохой аппетит, тошнота, иногда рвота, тяжесть в эпигастрии, отрыжка, непереносимость жирной пищи, упорное вздутие живота, иногда запоры, дегтеобразный стул могут быть обусловлены печеночно-клеточной недостаточностью, портальной гипертензией. Похудание возможно при активном гепатите, ЦП, опухолях. Чувство тяжести, давления и ноющая боль в правом подреберье исходят из капсулы печени (серозной оболочки, висцеральной брюшины). К интенсивной боли приводит острое растяжение капсулы печени при остром вирусном гепатите (ОВГ), застойной сердечной недостаточности. При ХГ и ЦП болевые ощущения незначительны или вовсе отсутствуют. Воспалительное поражение капсулы печени (перигепатит) и спаечный процесс между фиброзной оболочкой и париетальной брюшиной также приводят к боли в правом подреберье и наблюдаются при раке, абсцессе, сифилисе печени. Печеночная и желчная колики возникают при желчнокаменной болезни и гипермоторной дискинезии желчных путей. Лихорадка обычно свойственна холангиту, абсцессу печени. Но возможна и в преджелтушной стадии ОВГ, при токсических поражениях печени, хронических гепатитах, активной стадии ЦП и раке печени.
Увеличение печени – наиболее частый симптом болезней печени, ее уменьшение наблюдается значительно реже. Патоморфологически увеличение печени может быть обусловлено: дистрофией гепатоцитов (например при гепатозах и тезаурисмозах); лимфо-макрофагальной инфильтрацией при острых и хронических гепатитах; развитием регенераторных узлов и фиброза при ЦП; застоем крови при сердечной недостаточности, эндофлебите печеночных вен, констриктивном перикардите; холестазом внутрипеченочным при первичном билиарном циррозе печени (ПБЦ) и внепеченочным при болезнях, ведущих к нарушению оттока желчи и формированию вторичного билиарного ЦП; очаговыми поражениями при опухолях, кистах, абсцессах. Перкуссия органа дает весьма приблизительные результаты. Определяют размеры печени по Курлову. Пальпация дает более определенные результаты.
Исследования: ОАК: - Hb↓ злокачественное новообразование, миелопролиферативные нарушения. - Л ↑ воспалительный процесс, лейкемия. - СОЭ ↑ воспалительный процесс и злокачественное образование.
Биохимия: - Креатинин. Изменение уровня в крови часто отмечается у больных с печеночной недостаточностью, у больных с амилоидозом и развившейся почечной недостаточностью. - Билирубин (общий, свободный, связанный) - Общий белок, протеинограмма.
Функциональные печёночные пробы: - Выраженные нарушения ферментов (АсАт↑, АлАт↑) наблюдаются у больных с гепатитом. - Резкое увеличение уровня ЩФ отмечается у больных с нарушением проходимости желчных путей. - Характер изменений ФПП варьирует в зависимости от причины гепатомегалии. –
Посев крови, мочи, ЦСЖ (положительный при лептоспирозе).
Альфа-фетопротени (↑ при гепатоцеллюлярной карциноме).
Аспирационная биопсия костного мозга (миелофиброз, лейкемия).
УЗИ (цирроз, метастазы, амебный абсцесс, эхинококковая киста, доля Риделя).
КТ (поражения поджелудочной железы, цирроз, кисты печени).
Биопсия печени
Специальные исследования: Серологические исследования при вирусном гепатите Anti-HCV, HBsAg, HBeAg, anti-HBeAg, anti-HBcore IgM, anti-HBcore IgG, anti-HDV, anti-HAV, anti-HEV Исследование методом ПЦР при вирусном гепатите HCV РНК- качественно, количественно, генотипирование, HBV ДНКкачественно, количественно
15. Хронический панкреатит. Классификации. Основные клинические синдромы. Методы диагностики. Принципы лечения.
- длительное воспалительное заболевание ПЖ, проявляющееся необратимыми морфологическими изменениями паренхимы и протоков органа, которые вызывают боль и/или стойкое снижение функции.
1. По этиологии: - Билиарнозависимый – Алкогольный – Дисметаболический – Инфекционный – Лекарственный – Аутоиммунный - Идиопатический
2. По клиническим проявлениям: - Болевой – Диспептический – Сочетанный - Латентный
3. По морфологическим признакам: - Интерстиционально-отечный – Паренхиматозный - Фиброзно-склеротический – Гиперпластический - Кистозный
4. По характеру клинического течения: - Редко-рецидивирующий - Часто-рецидивирующий - С постоянно присутствующей симптоматикой ХП
5. Осложнения: - Нарушение оттока желчи и пассажа дуоденального содержимого - Портальная гипертензия (подпеченочная) – Псевдоаневризма - Эндокринные нарушения: панкреатогенный сахарный диабет, гипогликемические состояния и др. - Воспалительные изменения: абсцесс, киста, парапанкреатит, "ферментативный" холецистит, пневмония, экссудативный плеврит, паранефрит и пр.
Клиника: Боль в животе, локализуется в эпигастрии с иррадиацией в спину, усиливаясь после приема пищи и уменьшаясь в положении сидя или наклоне вперед. Недостаточность внешнесекреторной функции ПЖ, проявляющаяся клинически, возникает только при снижении функциональной активности железы более чем на 90%. Клиническими проявлениями нарушения всасывания жиров являются стеаторея и метеоризм, потеря массы тела. Эндокринная панкреатическая недостаточность со временем развивается у 70% пациентов с ХП в виде нарушения толерантности к глюкозе. Сахарный диабет возникает при длительном течении ХП. Болевой синдром может сопровождаться диспепсией (тошнота, рвота, изжога, вздутие живота, метеоризм). Рвота при обострении хронического панкреатита может быть частой, изнуряющей, не приносящей облегчения. Физикально: болезненность мышц брюшной стенки при пальпации в зоне проекции ПЖ.
Диагн-ка: активность ферментов ПЖ в крови (амилаза, липаза), определение активности панкреатической эластазы-1 в кале. С целью оценки эндокринной недостаточности ПЖ рекомендуется регулярное (не реже 1 раза в год) исследование уровня гликозилированного гемоглобина в крови, уровня глюкозы крови натощак или проведение глюкозотолерантного теста. Инструментально: Обзорная рентгенография брюшной полости позволяет выявить только выраженную кальцификацию в проекции ПЖ. Трансабдоминальное УЗИ (свободную жидкость в брюшной полости, оценить состояние печени, билиарного тракта, почек, патология которых может имитировать ХП или сопутствовать ему).Эндосонографии панкреатобилиарной зоны (ЭСПБЗ) и КТ органов брюшной полости с внутривенным болюсным контрастированием, магнитнорезонансная панкреатохолангиография, РХПГ (не рекомендовано).
Лечение: диета, отказ от курения, анальгетиков (напр. парацетамол** 1000 мг x 3 р/день, прегабалин), или НПВС. При неэффективности следует отдавать предпочтение трамадолу** (не более 400 мг/сут). Заместительная ферментная терапия (панкреатин 25 тыс ЕД, пангрол). Антидепрессанты (амитриптилин) уменьшают проявления сопутствующей депрессии и могут уменьшить выраженность болей и потенцировать эффект анальгетиков. Гипосекреторные препараты: ингибиторы H+, К+-АТФазы (оме-празол), блокаторы Н2-рецепторов гистамина (ранитидин, фамо-тидин), селективные м-холиноблокаторы (пирензепин). Если есть непереносимость и/или противопоказания к вышеперечисленным препаратам назначаются алюминий-магнийсодержащие антациды (алмагель, фосфолюгель). Препараты, снижающие давление в протоковой системе поджелудочной железы: холиноблокаторы (бускопан*) и миотропные спазмолитики (дротаверин, мебеверин). При диспепсических проявлениях (изжога, отрыжка, тошнота) применят препараты, устраняющие нарушения гастродуоденальной моторики: метоклопрамид по 10 мг 2-3 р/сут.
Хир лечение при следующих состояниях: - интенсивная некупируемая абдоминальная боль, ведущая к снижению или утрате трудоспособности; - отсутствие эффекта от консервативного лечения в течение 3 мес.; - риск развития зависимости от анальгетиков и/или психотропных препаратов; - возникновение осложнений ХП, требующих инвазивного устранения (кровотечения, непроходимость ДПК, симптоматические псевдокисты и др.); - подозрение на рак ПЖ
16. Цирроз печени. Профилактика и методы консервативной терапии при печеночной энцефалопатии, печеночной коме.+
Цирроз печени - это диффузный процесс, характеризующийся фиброзом и трансформацией нормальной структуры органа с образованием узлов.
Печеночная энцефалопатия - симптомокомплекс психических и нервно-мышечных нарушений, обусловленных печеночно-клеточной недостаточностью и/или портосистемным шунтированием крови. Кома последняя стадия
Принципы лечения: 1. Инфузионная терапия – в/в капельное введение под контролем ЦВД, суточного диуреза и клинико-лабораторных данных глюкозо-калий-инсулиновой смеси (250 мл 5% глюкозы + 10 ЕД инсулина + 1 г хлорида калия), р-ров низкомолекулярных декстранов, свежезамороженной плазмы (до 1 л/сут), криопреципитата и др.
2. Длительные ингаляции смеси 30-50% кислорода с воздухом, при необходимости - ИВЛ
3. Коррекция КЩС – при метаболическом ацидозе: 4% р-р натрия гидрокарбоната 400-600 мл/сут в/в капельно, при метаболическом алкалозе: хлорид калия до 10 г/сут в 5% глюкозе
4. Связывание циркулирующего в крови аммиака: в условиях ацидоза - препараты глутаминовой кислоты 100-150 мл 10% р-ра в/в капельно каждые 8 часов, орницетил / гепа-Мерц 5-25 г/сут в 5% р-ре глюкозы в/в капельно, в условиях алкалоза – р-ры малата (яблочной кислоты) 7-15 мг/сут в 5% р-ре глюкозы в/в капельно.
Общее количество введенной за сутки жидкости должно быть 1,5-2 л и равняться суточному диурезу + непочечные потери воды (500 мл при нормальной температуре тела).
а. Уменьшение образования аммиаки в кишечнике (лактулоза (дюфалак) – 30-120 мл/с внутрь или в клизмах – до 300-600 мл/с; антибиотики – рифаксимин, реже – ципрофлоксацин, метронидазол, ванкомицин, неомицин.).
б. Усиление обезвреживания аммиака в печени (орнитин-аспартат (Гепа-Мерц) в/в 20-40 г/с, затем внутрь 18 г/с, орнитин-α-кетоглутарат (орницетел – в/в 15-25 г/с), липоливая кислота, эссенциальные фосфолипиды). в. Увеличение связывания аммиака в крови (бензоат натрия, фенилацетат натрия).
5. Витамины: аскорбиновая кислота по 5-10 мл 5% р-ра в/в, никотиновая кислота по 2-3 мл 1% р-ра в/в или в/м, пиридоксин по 2-4 мл 5% р-ра в/м, токоферол по 1-2 мл 5% масляного р-ра в/м, кокарбоксилаза по 100-200 мг/сут в/м, витамин В12 300-600 мкг в/м
6. Гепатопротекторы: липоевая кислота 4-10 мл 2% р-р в/в, эссенциале 10 мл в 5% р-ре глюкозы
7. Стабилизаторы энергетического обмена в гепатоцитах: холинхлорид 10 мл 10% р-ра в 250 мл 5% р-ра глюкозы 2 раза/сут
8. ГКС: преднизолон 250-500 мг в/в капельно (предупреждает отек мозга на фоне массивных инфузий, оказывает противовоспалительное и иммунодепрессивное действие)
9. Профилактика инфекционных осложнений: АБ, тормозящие бактериальную флору кишечника (канамицин 2-3 г/сут, ампициллин 3-6 г/сут, тетрациклины 2 г/сут), лактулоза по 50-100 мл внутрь до 5 раз в сутки (для создания кислой среды в толстой кишке, связывания токсических продуктов) + высокие сифонные клизмы
10. Плазмаферез, обменные замещения крови в условиях гипотермии, гемодиализ и перитонеальный диализ, гемофильтрация и др. методы экстракорпоральной детоксикации
11. Лечение ДВС-синдрома, сердечной сосудистых нарушений, острой дыхательной недостаточности и др.
12. Трансплантация печени
13. Выявление и устранение провоцирующих факторов (Кровотечение, инфекции, алкоголь, массивная мочегонная терапия, прием седативных и транквилизаторов, употребление в пищу большого количества животных белков)
17. Тактика ведения и медикаментозное лечение больного с циррозом печени со стойким асцитом. Показания к лапароцентезу.+
Асцит – скопление свободной жидкости в брюшной полости
Лечение:
1. Постельный режим, бессолевая диета, ограничение жидкости
2. Если нет эффекта (увеличения диуреза): 1. + спиронолактон 50-100 мг/с; при необходимости каждые 3-5 дней постепенное повышение до 200 мг (редко до 400мг/с)
3. Если нет эффекта (увеличения диуреза): 1. + 2. + фуросемид (внутрь или парентерально) 20-80 мг/с, при необходимости – до 120 мг/с
4. Если нет эффекта (увеличения диуреза): 1. + 2. + 3. + тиазидные диуретики
5. Если нет эффекта (увеличения диуреза): с целью устранения гиповолемии внутривенно вводится р-р альбумина или коллоидного кровезаменителя
6. Если нет эффекта от применения консервативной терапии: использование альтернативных методов (парацентез, оперативные методы, трансплантация печени) Примечание: в процессе лечения обязателен контроль и коррекция уровня калия крови.
Показания к лапароцентезу (суть заключается в проколе передней брюшной стенки с последующим забором скопившейся в брюшной полости жидкости и ее дальнейшим направлением на цитологическое и бактериологическое исследование): • факт госпитализации больного; • признаки перитонита или инфекции; • печеночная энцефалопатия; • ухудшение функции почек; • желудочно-кишечное кровотечение (перед назначением антибиотиков); неэффективность консервативной терапии.
18. Функциональные кишечные расстройства. Синдром раздраженного кишечника. Критерии диагноза. Лечебная тактика.+
Синдром раздраженного кишечника - - это функциональное кишечное расстройство, при котором абдоминальная боль или дискомфорт ассоциируются с дефекацией или изменением поведения кишечника и особенностями расстройства дефекации.
Диагностические критерии синдрома раздраженного кишечника (Римский консенсу):
Рецидивирующая абдоминальная боль или дискомфорт по крайней мере 3 дня в месяц за последние 3 месяца, ассоциирующаяся с 2 или более признаками из следующих:
1)улучшение после акта дефекации
2)начало, ассоциирующееся с изменением частоты стула; и/или
3)начало, ассоциирующееся с изменением формы (внешнего вида) стула
Подтверждающие критерии СРК (Римский консенсус III, 2006 г.)
Не являются частью диагностических критериев, включают:
1.Ненормальную частоту стула:
1.1.Частота стула менее чем 3 раза в неделю.
1.2.Частота стула более чем 3 раза в день.
2.Ненормальную форму стула:
2.1.шероховатый/твердый стул или
2.2.расслабленный/ водянистый стул
3.Натуживание при дефекации
4.Безотлагательность или чувство неполного опорожнения, выделение слизи и вздутие
Симптомы, исключающие СРК – «симптомы тревоги»
1.Потеря массы тела
2.Начало заболевания в пожилом возрасте
3.Сохранение симптомов в ночные часы (в период сна)
4.Постоянные интенсивные боли в животе, как единственный и ведущий симптом
5.Лихорадка
6.Наличие патологии органов брюшной полости при физикальном исследовании (исключая болезненность при пальпации кишечника и признаки метеоризма)
7.Изменение лабораторных показателей (анемия, лейкоцитоз, увеличение СОЭ, отклонения в биохимических тестах и др.)
Лечение: 1. Диета: не пропускать приемы пищи и не допускать длительных перерывов между приемами пищи. При диарейном и смешанном варианте СРК возможно назначение аглютеновой диеты, а также диеты с низким содержанием олиго-ди-моносахаридов (лактозы, фруктозы, фруктанов, галактанов) и полиолов (сорбитола, ксилитола, маннитола). При недостаточной эффективности диеты – возможно назначениеальфа-галактозидазы.
2. Купирование боли: Холиноблокаторы (Гиосцин бутилбромид). Спазмолитики (Дротоверин; Мебеверин; Отилония бромид Папаверин; Пинаверия бромид). Действующие на опиоидные рецепторы: Тримебутин малеат.
3. Купирование диареии: лоперамида гидрохлорид, диоктаэдрический смектит, невсасывающийся антибиотик рифаксимин и пробиотики.
4. Для запора: Слабительные набухающего действия: Псилиум (семена подорожника). Слабительные осмотического действия: Макрогол; Лактулоза; Полиэтиленгликоль; Соли магния; Сорбитол; Фосфаты. Размягчающие слабительные: Вазелиновое масло. Контактные слабительные: Производные дифенилметана - бисакодил, пикосульфат натрия. Рацинолевая кислота. Антрахиноны: Сенна, алое, ревень. Прокинетики: Метокопрамид; Домперидон.
5. Комбинированные препараты: Альверин + Симетикон
6. Вздутие: Симетикон. Диосмектит.
7. Психотропные препараты: антидепресанты (Парексетин), нейролептики.
19. Классификация и патогенез симптоматических язв. НПВП-гастропатии.+
К симптоматическим язвам желудка относятся: язвы «лекарственные» , «гипоксические язвы», , «гормоногенные язвы» при гиперпаратиреоидизме, ульцерогенных опухолях поджелудочной железы (синдром Золлингера-Эллисона - гастринома) и др.;
острые стрессовые язвы при инфаркте миокарда, ожоговой болезни, инсульте и т.д.; в этих случаях стрессовыми ситуациями для организма считаются шок, коллапс (резкое падение артериального давления), кислородное голодание тканей организма, острая недостаточность функции печени или почек (при воздействии нескольких из этих факторов совместно риск возникновения язвы резко возрастает);
язвы при гепатитах и при циррозах печени, где ключевым фактором является развитие портальной гипертензии с нарушением венозного оттока от желудка.
Лекарственные (медикаментозные) язвы. Механизм развития лекарственных язв может быть различным. Некоторые препараты подавляют образование защитных гормонов (простагландинов) в слизистой оболочке желудка и снижают выработку желудочной слизи (аспирин, диклофенак, ибупрофен, индометацин и др.). Другие препараты непосредственно повреждают слизистую оболочку желудка – сульфаниламиды, нестероидные противовоспалительные препараты салицилаты. Глюкокортикостероиды стимулируют усиленное образование соляной кислоты обкладочными клетками желудка, секрецию гастрина и пепсина, что еще больше повышает агрессивность желудочного содержимого. Образованию язв способствуют антикоагулянты, препараты наперстянки, нитрофурановые препараты.
Методика ранней диагностики НПВП-индуцированных поражений следующая: - анализ факторов риска (язвенный анамнез, Н.pilori-инфекция и т.д.);
- назначение НПВП одновременно с гастропротекторами;
- контроль за терапией на 7, 14-й дни – определение уровня аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы, γ-глутамилтранспептидазы, анализ кала на скрытую кровь);
- ЭГДС в случае появления симптоматики, положительной пробы на скрытую кровь;
- отмена НПВП при повышении АЛТ, АСТ, общего билирубина.
Лечение НПВП-гастропатии включает следующие меры:
- Прекращение приема НПВП у большинства больных не приводит к рубцеванию НПВП-индуцированных язв, хотя может повышать эффективность противоязвенного лечения. Длительность курсовой терапии должна быть не менее 4 недель, а при больших размерах и локализации язв в желудке – 8–12 недель.
- Препаратами выбора для лечения НПВП-гастропатии являются ИПП – омепразол, лансопразол, пантопразол, рабепразол, эзомепразол.
- Эффективность ИПП может быть повышена путем их комбинации с препаратами висмута.
+Эрадикация Н.pylori не ускоряет процесс заживления НПВП-индуцированных язв.
Основную роль в возникновении язв при ИБС играют следующие факторы: нарушение микроциркуляции в слизистой оболочке желудка, снижение скорости кровотока в сосудах стенки желудка, повышение показателей свертывающей системы крови, дислипидемия.
При гиперпаратиреозе в паращитовидных железах происходит избыточная продукция паратгормона или паратирина, регулирующего обмен кальция в организме. При этом сам гормон паращитовидных желез приводит к повышению продукции соляной кислоты в желудке. Кроме того, избыточное количество кальция в крови так же стимулирует секрецию соляной кислоты и гастрина.
Синдром Золлингера-Эллисона возникает в результате опухоли, располагающейся в области головки или хвоста поджелудочной железы (85 % случаев). В 15 % случаев опухоль локализуется в желудке или является проявлением множественного эндокринного аденоматоза (множественной эндокринной неоплазии). Развитие пептических язв, устойчивых к лечению, связано с повышенной выработкой желудочного сока и, соответственно, соляной кислоты и ферментов. Поскольку содержащаяся в желудке соляная кислота не успевает нейтрализоваться, она поступает в двенадцатиперстную кишку и тонкий кишечник, при этом нормальная кислотность содержимого кишечника повышается.
Механизмом развития стрессовой язвы считается нарушение взаимодействия факторов агрессии и факторов защиты слизистой оболочки желудка (и двенадцатиперстной кишки). Факторы агрессии начинают преобладать над факторами защиты. Механизм развития язв включает в себя выброс в кровь стрессовых гормонов глюкокортикостероидов и катехоламинов, которые стимулируют выброс соляной кислоты, уменьшают продукцию желудочной слизи, способствуют нарушению микроциркуляции крови в стенке желудка и двенадцатиперстной кишки. Как следствие нарушения микроциркуляции происходят кровоизлияния в слизистую оболочку. Затем в месте кровоизлияния в условиях сниженной защиты слизистой оболочки происходит разрушение поверхностного слоя слизистой - образуется эрозия. Эрозия постепенно углубляется и, достигая мышечного слоя желудка или двенадцатиперстной кишки, превращается в язву. Чаще всего такие стрессовые язвы образуются на слизистой оболочке дна и тела желудка, реже в двенадцатиперстной кишке. Гастродуоденальные язвы, возникшие при стрессовых ситуациях, наблюдаются почти у 80% больных.
20. Осложнения язвенной болезни. Ранняя диагностика стеноза привратника и желудочного кровотечения. Врачебная тактика. (2)+
Кровотечение является наиболее частым осложнением язвенной болезни. Различают скрытые и явные кровотечения.
Существует индекс Альговера = пульс/систолическое АД, в норме = 0,5 (60/120 = 0,5). При увеличении индекса до 1 объем кровопотери равен примерно 20%, при увеличении до 1,5 = 30%, при 2,0 = 50%. При массивных кровопотерях развивается коллапс или гиповолемический шок. Нередки присоединение признаков острой почечной и печеночной недостаточности.
Клиническая картина и диагностика. Ранними признаками острой массивной кровопотери являются внезапная слабость, головокружение, тахикардия, гипотония, иногда обморок. Позже возникает кровавая рвота (при переполнении желудка кровью), а затем мелена. Характер рвотных масс (алая кровь, сгустки темно-вишневого цвета или желудочное содержимое цвета "кофейной гущи") зависит от превращения гемоглобина под влиянием соляной кислоты в солянокислый гематин. Многократная кровавая рвота и появление впоследствии мелены наблюдаются при массивном кровотечении. Рвота, повторяющаяся через короткие промежутки времени, свидетельствует о продолжающемся кровотечении; повторная рвота кровью через длительный промежуток времени — признак возобновления кровотечения. При обильном кровотечении кровь способствует быстрому раскрытию привратника, ускорению перистальтики кишечника и выделению испражнений в виде "вишневого желе" или примеси малоизмененной крови.
По поводу тактики.Обострения ЯЖБ.Кровотечение является экстренным показанием для госпитализации в хирургический стационар.
Остановка кровотечения (одним из множества методов(клипирование,обкалывание и тд.).Лучше всего,если получится остановить кровотечение на ФГДС.
Обязательно используем дегидратационную терапию (чтобы компенсировать потерю жидкости)
Можно использовать компоненты крови и плазму.
Системные ГКС (преднизалон 30-60 мл в\в)
Перфорация встречается примерно в 5 - 20% случаев и требует немедленного оперативного вмешательства. Клиника перфорации представлена острой "кинжальной" болью в эпигастральной области, напряжением мышц передней брюшной стенки, признаками пневмоперитонеума - отсутствием печеночной тупости перкуторно, серповидной полоской воздуха под диафрагмой рентгенологически и в последующие сутки - перитонитом и резким ухудшением самочувствия больного.
Пенетрация - распространение язвы за пределы стенки желудка или 12-перстной кишки в окружающие ткани и органы. Диагностируется по изменению клиники - изменению характера болей, диспепсических расстройств, появлению поносов, сухости во рту, механической желтухи и т.д. Болевой синдром изменяет свой суточный ритм, больному перестают помогать антациды.
Стеноз осложняет течение язвенной болезни в 6 - 15% случаев и наиболее часто встречается стеноз привратника и постбульбарного отдела. Выделяют функциональный и органический стенозы. Стенозу характерно нарушение эвакуаторной деятельности желудка и 12-перстной кишки. При компенсированном стенозе общее состояние больных не меняется, но нередко больные отмечают чувство тяжести в эпигастрии после приема пищи, отрыжку кислым, рвоту, приносящую облегчение. Субкомпенсированный стеноз проявляется выраженной интенсивной болью в подложечной области, чувством распирания живота после приема небольшого количества пищи, отрыжкой тухлым, обильной рвотой, приносящей облегчение, наличием в рвотных массах пищи, съеденной накануне. Учащение рвоты приводит к развитию прогрессирующего истощения и обезвоживанию больного, что свидетельствует о декомпенсации стенозирования. В отличие от органического, клиническая картина функционального стеноза менее выражена и его признаки исчезают в фазу ремиссии.
Лечение. Больным с признаками обострения язвенной болезни при компенсированном и субкомпенсированном стенозе проводят курс консервативного противоязвенного лечения в течение 2—3 нед. В результате исчезает отек слизистой оболочки привратника и начальной части двенадцатиперстной кишки, уменьшается периульцерозный инфильтрат, улучшается проходимость привратника. В то же время корригируют водно-электролитные и белковые нарушения. Риск операции снижается.
+Больные с компенсированным стенозом могут быть оперированы после короткого (5—7 дней) периода интенсивного противоязвенного лечения.
Медикаментозное лечение:
Нормализация водно-электролитных нарушений
Парентеральное или зондовое энтеральное питание, обеспечивающее энергетические потребности организма за счет введения растворов глюкозы, аминокислот, жировой эмульсии и др.
Противоязвенное лечение по полной программе.(ИПП (ОМЕПРАЗОЛ.Можно в сочетании с препаратами висмута)
Систематическая декомпрессия желудка (аспирация желудочного содержимого через зонд).
+Малигнизация. Считается, что 8 - 10% язв в последующем трансформируются в рак, однако дифференциальная диагностика данных состояний с первично-язвенной формой рака крайне затруднена.
21. Основные виды и причины желтух. Принципы лабораторной и инструментальной диагностики.
Желтуха — синдром, возникающий при увеличении содержания в крови билирубина и характеризующийся желтой окраской кожи, слизистых оболочек, склер в результате отложения в них желчных пигментов при нарушении желчеобразования и желчевыделения.
Классификация. В зависимости от первичной локализации патологического процесса, приводящего к развитию желтухи, и механизма возникновения выделяют такие виды желтухи:
1) надпеченочную, вызванную повышенной продукцией билирубина, главным образом в связи с усилением распада эритроцитов (гемолитическая желтуха) и реже при нарушении плазменного транспорта билирубина;
Причина: Возникает в результате усиленного разрушения эритроцитов.(Анемия,например)
2) печеночную желтуху, обусловленную нарушением захвата, конъюгации и экскреции билирубина гепатоцитами вследствие их повреждения при различных патологических процессах, а также приобретенных и наследственных дефектах структуры гепатоцитов и ферментов, участвующих в метаболизме и транспорте билирубина в клетках печени;
Причиной возникновения печеночной желтухи является прежде всего действие этиологических факторов, вызывающих повреждение гепатоцитов (инфекция, токсические, в том числе лекарственные, вещества, внутрипеченочный холестаз), а также наследственный дефект захвата, конъюгации и выведения билирубина из гепатоцита.
3) подпеченочную желтуху (механическую), возникающую при затруднении оттока желчи по внепеченочным желчевыводящим путям.
Причина: рак головки поджелудочной железы, метастазы рака в лимфатические узлы ворот печени,холестаз(вроде как)
Для решения вопроса о надпеченочном характере желтухи используют комплекс клинических и лабораторных данных
Желтушность кожи и склер умеренная, кожа, как правило, бледная
Печень и селезенка могут быть увеличенными, но функция печени существенно не нарушена.
В общем анализе крови:
- анемия.
- увеличение числа ретикулоцитов. Ретикулоцитоз отражает активацию костномозговой продукции эритроцитов в ответ на их разрушение на периферии.
- ускоренный выброс из костного мозга недозрелых эритроцитов, содержащих РНК, обуславливает феномен полихроматофилии эритроцитов в фиксированных окрашенных азур-эозином мазках крови.
Биохимический анализ крови:
- уровень общего билирубина в сыворотке крови повышен;
- уровень непрямого билирубина повышен, уровень его повышения зависит от активности гемолиза и способности гепатоцитов к образованию прямого билирубина и его экскреции.
- уровень прямого билирубина (связанного) в сыворотке крови нормальный или слегка увеличен;
В моче:
- в моче повышается содержание стеркобилиногена (стеркобилинурия!), уробилиногена.
- билирубинурия отсутствует, так как через неповрежденный почечный фильтр проходит только прямой билирубин.
Кал:
- приобретает более интенсивное окрашивание.
- повышение стеркобилиногена (темная окраска).
Для решения вопроса о печеночном характере желтухи используют комплекс клинических и лабораторных данных :
Общее состояние нарушено, симптомы интоксикации.
Желтушность кожи и склер умеренно выраженная, с оранжевым оттенком или с серым колоритом.
Печень и селезенка увеличены.
Наличие геморрагического синдрома.
Тяжесть и боль в области правого подреберья.
Неустойчивый кожный зуд.
В общем анализе крови: при вирусных гепатитах возможны лейкопения, нейтропения, относительный лимфо- и моноцитоз.
Биохимический анализ крови:
- уровень общего билирубина в сыворотке крови повышен за счет повышения прямого билирубина (связанного) и относительного повышения непрямого билирубина.
- повышение индикаторов цитолитического синдрома (повреждение гепатоцитов) – повышение АЛТ, АСТ, особенно АлАТ, коэффициент де Ритиса менее 1,33.
- увеличены показатели тимоловой пробы.(очень важно)
- нарушение синтетической функции печени: снижение альбуминов, фибриногена, ПТИ < 80%;
В моче:
- появляются желчные пигменты — билирубин и уробилиноген
- цвет мочи темный.
Кал:
- содержание стеркобилиногена понижается (стул обесцвечивается).
Для решения вопроса о подпеченочном характере желтухи используют комплекс клинических и лабораторных данных
Желтуха с зеленоватым или зеленовато-сероватым оттенком;
Увеличение и уплотнение печени, реже – селезенки;
Устойчивый кожный зуд.
Биохимический анализ крови:
высокий уровень прямого билирубина (> 20 % от нормы);
повышение маркеров холестаза - ГГТ (гаммаглютаминтрансферазы), щелочной фосфатазы, холестерина, холестерола, желчных кислот, нуклеотидазы, β-ЛП;
отсроченное, умеренное повышение АЛТ, АСТ; АСТ/АЛТ < 1,33.
отсутствие нарушений синтетической функции печени;
В моче:
- определяется конъюгированный билирубин
- цвет мочи темный (холурия).
Кал:
- резкое снижение уровня стеркобилиногена вплоть до полного отсутствия (ахоличный стул).
Проявления обтурационной и паренхиматозной желтухи очень сходны. Критерием для дифференциального диагноза является наличие уробилиногена в моче при печеночной желтухе и отсутствие при обтурационной.
22. Неалкогольная жировая болезнь печени. Диагностические критерии. Принципы лечения.+
Неалкогольная жировая болезнь печени представляет собой спектр поражений печени, включающий жировую дистрофию (стеатоз печени) и жировую дистрофию с воспалением и повреждением гепатоцитов (неалкогольный стеатогепатит) и фиброзом печени с возможностью прогрессирования с исходом в цирроз.
Критерии установления диагноза:
a) Наличие избыточного количества жировых отложений в печени (определенное гистологическим исследованием или визуализирующими методами);
b) Отрицание в анамнезе хронического употребления алкоголя в токсичных дозах;
c) Исключение других причин жировой инфильтрации печени (гепатотропные вирусы, генетически детерминированные заболевания, лекарственное поражение печени).
Основные принципы лечения НАЖБП:
1. снижение массы тела (диета и физические нагрузки);
2. обязательная отмена потенциально гепатотоксичных препаратов, кроме случаев, когда польза от их назначения превышает риск;
3. коррекция метаболических нарушений: a) повышение чувствительности клеточных рецепторов к инсулину (метформин, тиазолидиндионы); b) коррекция нарушений липидного обмена (при субклиническом атеросклерозе УДХК(уродезоксихолиевая кислота 15 мг/кг массы тела / сутки в течении 24-х недель), при клиническом атеросклерозе – УДХК+статины); c) гипотензивная терапия;
4. лечение окислительного стресса (УДХК, антиоксиданты, ЭФЛ).
Медикаментозная терапия НАЖБП: Витамин Е (токоферол) (800 МЕ \сутки),УДХК.
23. Дифференциальный диагноз при диарее. Стандарт обследования. Принципы лечения.
Секреторная диарея характеризуется безболезненной обильной водной диареей (обычно более 1 л). Гиперсекрецию воды и электролитов вызывают бактериальные токсины, энтеропатогенные вирусы, желчные кислоты, простагландины и ряд других биологически активных веществ (вазоактивный интестинальный пептид, гастрин, кальцитонин). Секреторная диарея возникает независимо от диеты и не уменьшается при голодании.
Осмолярная диарея развивается при нарушении кишечного пищеварения и всасывания, в результате накопления в просвете кишки осмотически активных веществ, вызывающих активный приток натрия и воды. У пациентов с нарушенным всасыванием пищевых веществ преобладает полифекалия — обильный стул, содержащий большое количество остатков непереваренной пищи. Может развиться при приеме некоторых слабительных (например, лактулоза), или вследствие нарушения переваривания некоторых продуктов питания (например, молока). Этот тип диареи прекращается после голодания.
Экссудативная диарея возникает вследствие поступления воды и электролитов в просвет кишки при эрозивно-язвенных поражениях слизистой оболочки или при повышении гидростатического давления в лимфатических сосудах. При экссудативной диарее стул жидкий, часто с примесью крови и гноя. Этот тип диареи характерен для воспалительных заболеваний кишечника (язвенный колит, болезнь Крона) и ряда кишечных инфекций (дизентерия, сальмонеллез, кампилобактериоз).
Гипер — и гипокинетическая диарея. Гиперкинетическая диарея развивается при ускорении пропульсивной моторики кишечника. Повышение скорости транзита в первую очередь вызывают нейрогенные факторы, секретин, панкреозимин, гастрин, серотонин, простагландины, желчные кислоты. Этот тип диареи характерен для пациентов с синдромом раздраженного кишечника. При гиперкинетической диарее стул жидкий или кашицеобразный, частый, но суточное количество его не превышает 200–300 г.
Также стоит отметить Классификация диареи
По этиологии:
инфекционная
неинфекционная
По длительности:
острая (до 2-3 недель)
хроническая (свыше 3-х недель или при установленных частых эпизодах диареи в анамнезе)
Острая неинфекционная диарея
+Основными причинами острой неинфекционной диареи являются алиментарные погрешности в питании, прием некоторых лекарственных препаратов.
Острая инфекционная диарея
Круг этиологических факторов, обусловливающих развитие острой инфекционной диареи, очень широк. Это:
Бактерии
сальмонеллы;
шигеллы;
компилобактер;
клостридии; И ТД.
Лечение
Целесообразность проведения антимикробной терапии и ее характер полностью зависят от этиологии диареи и, соответственно, от особенностей диарейного синдрома.
В любом случае
Детоксикационная терапия
Дегидратационная терапия
Клизмы(Если речь идет об инфекционной природе возбудителя)
Можно промывание желудка (если эндотоксин в верхних отделах ЖКТ)
При "водянистой" диарее, вызванной бактериями, продуцирующими энтеротоксины, а также вирусами и простейшими, антибактериальная терапия не показана. В этом случае основу лечения составляет патогенетическая терапия, направленная на поддержание водно-электролитного баланса (пероральная или парентеральная регидратация).
+Диарея с выраженными признаками воспаления (присутствие крови, гноя, слизи и лейкоцитов в фекалиях), сопровождающаяся лихорадкой, скорее всего, вызвана патогенами , в отношении которых назначение этиотропных препаратов может обеспечить клинический и бактериологический эффект. (Ципрофлоксацин 0,5 2р\сутки 5-7 дней)
Обследование: КАК, Копрограмма, ОАМ,Б\Х, сбор анамнеза,Поиск возбудителя (ИФА,БАКТЕРИОСКОПИЯ И ТД.)Сильно расписывать не буду.Смысла нет.
24. Синдром нарушения всасывания (мальабсорбция). Этиология. Методы диагностики. Принципы лечения.+
Синдром мальабсорбции — нарушение всасывания из тонкой кишки пищевых веществ, приводящее к выраженному расстройству питания пациента. Выделяют мальдигестию (нарушение переваривания пищи до необходимых для всасывания составных частей, вследствие чего нарушается всасывание в кишечнике) и собственно мальабсорбцию — нарушение самого механизма всасывания в тонкой кишке. В выраженных случаях мальдигестия и мальабсорбция обычно сочетаются.
Этиологическая классификация синдрома мальабсорбции
I. Нарушение переваривания (мальдигестия):
1. Дефицит энзимов и частично бикарбонатов поджелудочной железы (хронический панкреатит в фазе развития фиброза, кисты поджелудочной железы).
2. Дефицит солей желчных кислот — недостаточное эмульгирование жиров (длительная закупорка желчных путей, гепатоцеллюлярная недостаточность, преципитация желчных кислот в тонкой кишке из-за низкого pH).
3. Недостаточное смешивание пищи с желчью и соком поджелудочной железы (гастроеюностомия).
Нарушение всасывания (мальабсорбция в узком смысле слова).
1. Повреждение всасывательной поверхности тонкой кишки (глютеноваяэнтеропатия, хронические атрофические энтериты, лучевое поражение тонкой кишки, стронгилоидоз и др.).
2. Уменьшение всасывательной поверхности тонкой кишки (резекция, анастомоз между желудком и толстой кишкой).
3. Болезни стенок тонкой кишки (болезнь Крона, амилоидоз, туберкулез кишок, кишечная липодистрофия — болезнь Уиппла). При болезни Уиппла поражаются мезентериальные лимфатические узлы, а также слизистая оболочка тонкой кишки, что приводит к нарушению всасывания белков, жиров, углеводов. Лимфоузлы инфильтрированы макрофагами и подвержены кистозной дегенерации. В кистах содержатся суданофильныелипогранулемы. Прижизненная диагностика возможна лишь с помощью биопсии тонкой кишки.
4. Расстройства кровоснабжения тонкой кишки (недостаточность мезентериального кровоснабжения, слипчивый перикардит, узелковый периартериит).
5. Дефицит энзимов тонкой кишки или расстройства биохимического механизма транспорта питательных веществ (дефицит дисахаридаз, пернициозная анемия, цистинурия, нарушение образования хиломикронов).
6. Расстройства моторики тонкой кишки (склеродермия, тиреотоксикоз, диабетическая висцеральная невропатия, карциноидный синдром, синдром Золлингера — Эллисона). При последнем синдроме не только ускоряется кишечная моторика, но в просвете тонкой кишки вследствие низкой pH инактивируется липаза поджелудочной железы и концентрация желчных кислот в тонкой кишке снижается, в результате чего нарушается гидролиз и всасывание жиров.
7. Дисбактериоз кишечника — вследствие длительного лечения антибиотиками, синдром приводящей петли, дивертикулы тонкой кишки, стриктуры кишок с задержкой содержимого.
Клинические симптомы
+Ведущий и ранний симптом — поносы.
Один из наиболее ранних и частых симптомов — стеаторея
Характерны также флатуленция — обильное скопление газа в желудке и кишечнике и метеоризм
Лабораторные данные
1. ОАК: признаки анемии.
2. БАК: снижение содержания общего белка, альбумина, холестерина, железа, кальция, натрия, хлоридов, глюкозы.
3. Проба с α-ксилозой, меченым витамином В12 и железом, проба на толерантность к глюкозе (плоская сахарная кривая), йод-калиевая проба — уменьшение всасывательной функции тонкой кишки.
4. Копроцитограмма: стеаторея, креаторея, при бродильной диспепсии — пузырьки газа, кислая реакция, при гнилостной диспепсии — щелочная реакция.
5. Снижение содержания энтерокиназы в кишечном соке.
Инструментальные исследования
+Рентгенологическое исследование тонкой кишки — неравномерный диаметр просвета тонкой кишки, беспорядочное утолщение поперечных складок, сегментация контрастного вещества, ускоренный его пассаж. Исследование лучше производить по методу Пансдорфа: желудок быстро наполняется 250 мл контрастного вещества, через 15 мин пациент получает вторую порцию контрастного вещества в течение 30 мин. Через 2 ч после принятия первой порции контрастного вещества начинают делать снимки. Аспирационная биопсия тонкой кишки — атрофия ворсинок.
Лечение синдрома мальабсорбции
.1. Лечение основного заболевания
2. Лечебное питание
3. Улучшение пищеварения и всасывания в тонкой кишке (заместительная ферментная терапия и коррекция всасывательной функции)
4. Лечение диареи и нормализация моторной функции кишки
5. Лечение СИБР и восстановление эубиоза кишки
6. Улучшение состояния слизистой оболочки тонкой кишки (применение вяжущих, адсорбирующих, обволакивающих препаратов)
7. Коррекция метаболических, электролитных нарушений, анемии, гиповитаминозов, эндокринных нарушений
Сложно что-то сказать по поводу конкретных препаратов. Все зависит от основного заболевания. Но тут как и у всех. Коррекция водно-электролитного баланса в обяззательном порядке)
Хирургическое лечение
+Хирургическое лечение проводится с учетом заболевания, которое привело к развитию синдрома мальабсорбции. Так, хирургические вмешательства выполняются пациентам с болезнями Крона , Гиршпрунга , кишечной лимфангиэктазией , осложнениями язвенного колита , заболеваниями печени.
25. Гэрб. Внепищеводные проявления. Современные стандарты диагностики и лечения.
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) – хроническое рецидивирующее заболевание, обусловленное нарушением моторноэвакуаторной функции органов гастроэзофагеальной зоны и характеризующееся регулярно повторяющимся забросом в пищевод содержимого желудка, а иногда и ДПК, что приводит к появлению клинических симптомов, ухудшающих качество жизни пациентов, повреждению слизистой оболочки дистального отдела пищевода с развитием в нем дистрофических изменений неороговевающего многослойного плоского эпителия, катарального или эрозивно-язвенного эзофагита (рефлюкс-эзофагита), а у части больных – цилиндроклеточной метаплазии.
Внепищеводные проявления ГЭРБ включают бронхолегочный, оториноларингологический, стоматологический синдромы.
Рефлюкс-индуцированный хронический кашель. ГЭРБ – причина хронического кашля в 40 % случаев, продуктивного кашля с мокротой в 15 % случаев.
Патогенез кашля, индуцированного ГЭРБ: 1) стимуляция эзофаготрахеобронхиального рефлекса при воздействии желудочного содержимого на вагусные рецепторы дистальной части пищевода; 2) активация кашлевого рефлекса с рецепторов гортани и трахеобронхиального дерева при микро- или макроаспирации содержимого пищевода.
Кашель, вызванный ГЭРБ, обычно сухой, у большинства пациентов обостряется после инфекции верхних дыхательных путей, возникает преимущественно при изменении положении тела, особенно при наклонах, в дневное время суток, реже ночью, что, вероятно, обусловлено активизацией механизмов защиты, которые препятствуют ПРНПС в горизонтальном положении тела.
Рефлюкс-индуцированная бронхиальная астма. Микроаспирация – основной механизм развития рефлюкс-индуцированной астмы. Патологический ГЭР рассматривается в качестве триггера приступов астмы, преимущественно в ночной период, преимущественно с 0 до 4 часов утра, что обусловлено уменьшением частоты глотательных движений и, следовательно, увеличением воздействие кислоты на слизистую оболочку пищевода. Эзофагеальные рецепторы, реагируя на заброс желудочного содержимого, активируют рефлекторную дугу: вагусные афферентные волокна, ядро вагуса, эфферентные волокна. Влияние на бронхиальное дерево проявляется в виде рефлекторного кашля или бронхоспазма.
Отоларингологические симптомы ГЭРБ наиболее многочисленны и разнообразны. К ним относят ощущение боли, кома, инородного тела в глотке, першение, желание «прочистить горло», охриплость, приступообразный кашель.
Ларингофарингеальный рефлюкс (ЛФР) является достаточно частым внепищеводным проявлением ГЭРБ и характеризуется ретроградным поступлением желудочного содержимого в гортань и глотку, приводя к рецидивирующему течению отоларингологической симптоматики.
ЛФР является инициирующим фактором многих заболеваний гортаноглотки, таких как рефлюкс-ларингит, узелковый ларингит, подскладочный стеноз, рак гортани, гранулёмы и язвы.
К клиническим признакам ЛФР принято относить: 1) осиплость; 2) дисфонию; 3) першение, боль или жжение в горле; 4) частое покашливание; 5) хронический кашель; 6) чувство кома в горле; 7) апноэ; 8) ларингоспазм; 9) дисфагию; 10) отечность слизистой (эдема) гортаноглотки; 11) постназальный затек.
Стоматологический синдром
Слюна является регулятором общего количества микроорганизмов. Изменения её физико-химических свойств в результате ГЭР могут способствовать дисбиозу в полости рта. При ГЭРБ выявлен микробиологический дисбаланс с превалированием микроорганизмов, продуцирующих различные ферменты патогенности: гемолизин (S. Intermedins, S. sanguis, Staphylococcus saprophyticus, S. warneri, Bacteroides spp.), лецитиназу (Staphylococcus xylosus), казеиназу, РНКазу, каталазу, а также установлено наличие грибов рода Candida albicans с патогенными свойствами, выражающимися в способности образовывать ростковые трубки, и повышенной адгезией к эпителиальным клеткам.
К числу наиболее характерных стоматологических поражений при ГЭРБ относятся: поражение мягких тканей (афтозный стоматит, изменения сосочков языка, жжение языка), некариозные поражения твёрдых тканей зубов (эрозии эмали), кариес, галитоз. Частота заболеваний полости рта при ГЭРБ колеблется от 5 до 69,4 %, их частота и выраженность зависят от возраста пациентов.
У взрослых пациентов с тяжёлым течением ГЭРБ наряду с типичными жалобами отмечены ощущение сухости, чувство жжения, боль в языке, «ошпаренность» языка, изменение вкусовой чувствительности языка. У пациентов с ГЭРБ стадии В и С (в соответствии с Лос-Анджелесской классификацией) отмечено достоверное повышение порога вкусовой чувствительности на сладкое, снижение – на кислое незначительное повышение – на горькое.
Диагностика
Опросник GERD-Q (чувствительность – 65,4 %, cпецифичность – 91,7 %) – стандартизированный опросник, состоящий из 6 вопросов, самостоятельно заполняется пациентом и удобен для интерпретации лечащим врачом. Оцениваемый в опроснике период – предыдущие 7 дней. По опроснику GERD-Q ГЭРБ диагностируется при сумме баллов ≥8, при 3–7 баллах диагноз ГЭРБ сомнителен.
Терапевтический тест с одним из ингибиторов протонной помпы в стандартной дозе в течение 7–10 дней (чувствительность 80 %, специфичность 57 %). Устранение симптомов подтверждает связь с рефлюксом и является критерием диагноза. Однако сохранение симптома не позволяет отказаться от диагноза ГЭРБ.
Альгинатный тест – оценка эффекта однократного приёма разовой дозы альгината при изжоге (чувствительность – до 97 %, специфичность – до 88 %). Купирование изжоги при однократном приёме альгината является дополнительным критерием диагноза ГЭРБ.
Тест Берштейна (пищевод орошают 0,1 н. раствором соляной кислоты (15 мл), считается положительным, если вызывает у больного ощущение изжоги и другие симптомы, характерные для ГЭРБ.
Гистологическое исследование биоптатов СО пищевода проводят для исключения ПБ, АКП, эозинофильного эзофагита. Расширение межклеточных пространств обнаруживается у всех пациентов с ГЭРБ независимо от наличия эрозий в пищеводе. В отличие от больных ГЭРБ у пациентов с функциональной изжогой межклеточные пространства не расширены.
Суточная рН-метрия в нижней трети пищевода признана «золотым стандартом» диагностики ГЭРБ (чувствительность 88–96 %, специфичность 85–100 %). рН-метрия – это процесс измерения концентрации водородных ионов непосредственно в желудочно-кишечном тракте с помощью рН-зонда и соответствующего регистрирующего прибора. Она позволяет выявить наличие и частоту кислых ГЭР, их взаимосвязь с симптомами, зависимость их появления от различных факторов, оценить эффективность антисекреторной терапии у пациентов как с типичными, так и с внепищеводными проявлениями ГЭРБ. (14,72).
Многоканальная внутриполостная импедансометрия пищевода – метод регистрации жидких и газовых рефлюксов, основанный на измерении сопротивления (импеданса), которое оказывает переменному электрическому току содержимое, попадающее в просвет пищевода.
Время закисления пищевода (AET) – это процент времени, в течение которого в нижней части пищевода на уровне 5 см выше верхней границы НПС рН < 4. Уровень 5 см выбран из такого расчёта, чтобы датчик рН на зонде, зафиксированным относительно носового отверстия, гарантировано не проваливался в желудок при глотках, когда пищевод из-за перистальтики укорачивается (рис. 8).
Манометрия высокого разрешения – исследование двигательной функции пищевода. Метод позволяет, используя многоканальный зонд, получать количественные показатели совокупной перистальтической активности, давления в сфинктерах пищевода, тонуса стенки органа, а также с помощью многоцветного объёмного изображения видеть продвижение по нему перистальтической волны. При ГЭРБ с её помощью выявляют снижение давления НПС, наличие ГПОД, увеличение количества ПРНПС, количественные показатели совокупной перистальтической активности стенки органа, эзофагоспазм, атипичные случаи ахалазии кардии, диагностируют синдромы руминации и супрагастральной отрыжки. Исследование позволяет верифицировать положение НПС для проведения рН-метрии. Оно является необходимым атрибутом обследования пациента, которое проводят для решения вопроса о хирургическом лечении ГЭРБ.
Критерии диагностики ГЭРБ (Лионское соглашение, 2017 г.):
1) эрозивный эзофагит (степени C и D Лос-Анжелесской классификации);
2) длинный сегмент ПБ;
3) пептические стриктуры в пищеводе;
4) длительное закисление пищевода (AET>6 %).
Лечение
Изменение образа жизни:
после приёма пищи избегать наклонов, горизонтального положения (в течение 1,5 часа); спать на кровати с приподнятым не менее чем на 15 см головным концом;
не носить тесную одежду и тугие пояса, корсеты, бандажи;
избегать работ, приводящих к повышению внутрибрюшного давления;
отказаться от курения и приёма алкоголя.
Изменение режима питания:
избегать обильного приёма пищи, не употреблять слишком горячей пиши, не есть на ночь (за 3–4 часа до сна);
ограничить потребление жиров, алкоголя, кофе, шоколада, цитрусовых, зелёного лука, чеснока, избегать употребления кислых фруктовых соков, продуктов, усиливающих газообразование (оказывают раздражающее действие на слизистую оболочку);
избегать повышения массы тела, снизить массу тела при ожирении.
Ограничение приёма лекарственных средств:
избегать приёма лекарственных средств, вызывающих рефлюкс: нитраты, антихолинергические, спазмолитики, седативные, снотворные, транквилизаторы, антагонисты кальция, бета-блокаторы, теофиллин, а также препаратов, повреждающих пищевод – аспирин, нестероидные противовоспалительные препараты.
Медикаментозное лечение.
Альгинаты. Патогенетически обосновано их назначение для уменьшения «кислотного кармана» и нейтрализации кислоты в области пищеводно-желудочного перехода у больных с ГЭРБ. Эти препараты способны значительно и длительно уменьшать количество как патологических кислых ГЭР, так и слабощелочных дуоденогастроэзофагеальных рефлюксов, создавая тем самым оптимальные физиологические условия для СО пищевода. Альгинаты оказывают цитопротективное и сорбционное действие. Альгинаты принимают по 10 мл 3–4 раза в день через 30–40 минут после еды и 1 раз на ночь до стойкого купирования симптомов заболевания, а затем – в режиме «по требованию».
Антациды. Антацидные средства (алюминия фосфат 2,08 г, комбинированные препараты – алюминия гидроксид 3,5 г и магния гидроксид 4,0 г в виде суспензии, алюминия гидроксид 400 мг и магния гидроксид 400 мг, а также кальция карбонат 680 мг и магния гидроксикарбонат 80 мг в виде таблеток) применяют для устранения умеренно выраженных и редко возникающих симптомов, особенно тех, которые связаны с несоблюдением рекомендованного образа. Антациды самостоятельной роли в лечении ГЭРБ не играют и могут применяться только в качестве средства кратковременного контроля симптомов.
Адсорбенты (диоктаэдрический смектит) оказывают комплексное действие: нейтрализуют соляную кислоту желудочного сока, дают выраженный адсорбирующий эффект, связывая компоненты содержимого ДПК (желчные кислоты, лизолецитин) и пепсин. Диоктаэдрический смектит повышает устойчивость СО пищевода к повреждающему действию рефлюктата. Адсорбенты можно применять как в качестве монотерапии при клинических проявлениях НЭРБ, так и в составе комплексной терапии ГЭРБ, особенно при смешанном (кислотный+желчный) рефлюксе. Диоктаэдрический смектит назначают по 1 пакетику (3 г) 3 раза в день.
Прокинетики способствуют восстановлению физиологического состояния пищевода, воздействуя на патогенетические механизмы ГЭРБ, уменьшая количество ПРНПС и улучшая пищеводный клиренс путём стимуляции двигательной функции нижележащих отделов пищеварительного тракта. Прокинетики можно применять в составе комплексной терапии ГЭРБ вместе с ИПП. Прокинетический препарат итоприда гидрохлорид (50 мг 3 раза в день) относится к средствам патогенетического лечения ГЭРБ, поскольку нормализует двигательную функцию верхних отделов пищеварительного тракта.
Ингибиторы протонной помпы (ИПП) эффективны при наличии как пищеводных, так и внепищеводных проявлений ГЭРБ. ИПП – это препараты, подавляющие активность фермента Н+, К+ -АТФазы, находящегося на апикальной мембране париетальной клетки и осуществляющего последний этап синтеза соляной кислоты. ИПП считают наиболее эффективными и безопасными препаратами для лечения ГЭРБ. Снижение продукции кислоты считают основным фактором, способствующим заживлению эрозивноязвенных поражений.
Основными принципами лечения ГЭРБ являются назначение ИПП и проведение длительной основной (не менее 4–8 недель) и поддерживающей (16–24 недели) терапии. При несоблюдении этих условий вероятность рецидива заболевания очень высока.
При наличии единичных эрозий пищевода (стадия А/1) продолжительность основного курса может составлять 4 недели с 43 использованием стандартной дозы ИПП: рабепразол по 20 мг в день, или омепразол по 20 мг 2 раза в день, или декслансопразол по 60 мг в день, или пантопразол по 40 мг в день, или эзомепразол по 40 мг в день, желательно с проведением контрольного эндоскопического исследования.
При множественных эрозиях пищевода (стадия В-С/2-4), осложнениях ГЭРБ продолжительность курса лечения любым препаратом из группы ИПП должна составлять не менее 8 недель. Продолжительность поддерживающей терапии после заживления эрозий должна составлять как минимум 16–24 недели. При возникновении осложнений ГЭРБ поддерживающую терапию следует проводить ИПП также в полной дозе.
В отсутствие эрозий пищевода для лечения НЭРБ можно назначить ИПП в половинной дозе.
Существует несколько вариантов поддерживающего лечения: 1) регулярный (систематический) приём ИПП в половинной дозе; 2) терапия «по мере необходимости» (pro re nata), которую проводят при рецидиве типичных для ГЭРБ клинических симптомов (изжога, кислая регургитация, дисфагия) длительностью более 5 дней; 3) «терапия выходного дня» (по субботам и воскресеньям); 4) терапия «по требованию» (on demand), когда наряду с рецидивом клинических симптомов ГЭРБ появляются признаки рефлюкс-эзофагита.
Эрадикации H. pylori при ГЭРБ. В связи с тем, что не установлена связь между выявлением H. pylori и развитием ГЭРБ и АКП, эрадикационная терапия инфекции H. pylori не входит в программу ведения пациентов с ГЭРБ. Однако при наличии показаний к эрадикации H. pylori (язвенная болезнь, хронический хеликобактерный гастрит, длительный прием ИПП), такая терапия может быть проведена при ГЭРБ, поскольку она не провоцирует ухудшение её течения и не оказывает влияния на эффективность лечения.
Антирефлюксное хирургическое лечение ГЭРБ показано при осложненном течении заболевания (повторные кровотечения, пептические стриктуры пищевода, развитие ПБ с дисплазией эпителия высокой степени, доказанной двумя морфологами, частые аспирационные пневмонии). В настоящее время доступны несколько хирургических методик, которые могут применяться в лечении ГЭРБ.
Медикаментозная терапия ПБ подразумевает снижение повреждающих свойств рефлюктата; контроль над секрецией соляной кислоты в желудке; купирование симптомов улучшение качества жизни; эпителизация повреждений слизистой оболочки; предотвращение формирования на фоне ПБ дисплазии эпителия и АКП.
Всем больным ПБ рекомендуется постоянная антисекреторная терапия ИПП. Основные принципы консервативного лечения ПБ: назначения стандартных доз ИПП, достаточных для стабилизации эндоскопической и морфологической картины в пищеводе и купирования симптомов; разделение дозы ИПП на 2 приёма: перед завтраком и перед ужином; проведение длительной (не менее 8–12 месяцев) основной терапии и постоянной поддерживающей терапии; 45 при дуоденогастральном рефлюксе больным с ПБ могут быть назначены в различных комбинациях антациды, прокинетики, урсодезоксихолевая кислота, холестирамин, сукральфат.
26. Болезнь Крона. Клинические проявления в зависимости от локализации заболевания. Стандарты лечения. Показания к биологической терапии. +
К 50. Болезнь Крона (БК) - хроническое, рецидивирующее заболевание желудочно-кишечного тракта неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений.
Монреальская классификация болезни Крона по локализации поражения: Терминальный илеит, Колит, Илеоколит.
± Поражение верхних отделов желудочно-кишечного тракта
± Поражение аноректальной зоны
Тонкокишечная локализация
Общие симптомы обусловлены интоксикацией и синдромом мальабсорбции и включают: слабость, недомогание, снижение работоспособности, повышение температуры тела до субфебрильной, похудание, отеки (за счет потери белка), гиповитаминоз (кровоточивость десен, трещины в углах рта, пеллагрозный дерматит, ухудшение сумеречного зрения), боли в костях и суставах (обеднение солями кальция), трофические нарушения (сухость кожи, выпадение волос, ломкость ногтей), недостаточность надпочечников (пигментация кожи, гипотония), щитовидной железы (заторможенность, одутловатость лица), половых желез (нарушение менструации, импотенция), паращитовидных желез (тетания, остеомаляция, переломы костей), гипофиза (полиурия с низкой плотностью мочи, жажда).
Местные симптомы:
Периодические, а позже постоянные тупые боли (при поражении 12-перстной кишки - в правой эпигастральной области, тощей кишки - в левой верхней и средней части живота, подвздошной кишки - в правом нижнем квадранте живота).
Стул полужидкий, жидкий, пенистый, иногда с примесью слизи, крови.
При стенозировании кишки - признаки частичной кишечной непроходимости (схваткообразные боли, тошнота, рвота, задержка газов, стула).
При пальпации живота - болезненность и опухолевидное образование в терминальном отделе подвздошной кишки, при поражении остальных отделов - боли в околопупочной области.
Формирование свищей внутренних, открывающихся в брюшную полость (межпетлевых, между подвздошной и слепой кишкой, желчным и мочевым пузырем), и наружных, открывающихся в поясничную и паховую области.
Возможны кишечные кровотечения (мелена).
Локализация в толстой кишке (гранулематозный колит)
Основные клинические симптомы:
Боли в животе схваткообразного характера, возникающие после еды и перед дефекацией. Возможны также постоянные боли при движениях, наклонах туловища (обусловлены развитием спаечного процесса). Боли локализуются по ходу толстого кишечника (в боковых и нижних отделах живота).
Выраженная диарея (жидкий или кашицеобразный стул до 10-12 раз в сутки с примесью крови). У некоторых больных бывают выраженные позывы к дефекации ночью или под утро.
Бледность, сухость кожи, снижение ее тургора и эластичности.
При осмотре живота выявляется снижение тонуса мышц передней брюшной стенки, пальпация по ходу толстой кишки сопровождается значительной болезненностью. Сигмовидная кишка чаще всего определяется в виде жгута, что объясняется инфильтрацией ее стенки.
У 80% больных отмечаются анальные трещины. Особенности, отличающие их от обычных трещин: различная локализация, часто множественный характер, значительно меньшая болезненность, вялость грануляций, отсутствие ригидных рубцовых краев, спазма сфинктера.
При пальцевом исследовании в случае вовлечения в процесс стенок анального канала пальпируются отечные ткани, часто можно определить снижение тонуса сфинктера. После извлечения пальца наблюдается зияние ануса и подтекание кишечного содержимого, обычно гнойно-кровянистого характера.
Важный диагностический признак - свищи, связанные с кишечником, и инфильтраты брюшной полости. Свищи прямой кишки при болезни Крона даже при длительном существовании редко сопровождаются рубцеванием и чаще всего бывают окружены инфильтрированными тканями с полиповидно измененной, инфильтрированной слизистой оболочкой в области внутреннего отверстия и вялыми «губовидно-выступающими» наружу грануляциями вокруг наружного отверстия.
Сочетанное поражение тонкой и толстой кишки
При локализации патологического процесса в подвздошной кишке и правых отделах толстой кишки преобладают боли в правой половине живота и субфебрильная температура тела; у части больных наблюдаются симптомы мальабсорбции. При диффузном поражении толстой кишки в сочетании с поражением терминального отдела подвздошной кишки в клинической картине доминирует симптоматика тотального колита.
Локализация в верхних отделах желудочно-кишечного тракта
Клиническая картина болезни Крона с локализацией патологического процесса в пищеводе, желудке, 12-перстной кишке на начальных этапах напоминает клинику, соответственно, хронического эзофагита, хронического гастрита, дуоденита. При поражении желудка и 12-перстной кишки клинические проявления могут быть сходны с клиникой язвенной болезни желудка и 12-перстной кишки (язвенно-подобный синдром), причем в рвотных массах часто бывает примесь крови. По мере прогрессирования заболевания присоединяются слабость, субфебрильная температура тела, похудание, анемия.
Лечение
Целями терапии БК являются индукция ремиссии и ее поддержание без постоянного приема ГКС, профилактика осложнений, предупреждение операции, а при прогрессировании процесса и развитии опасных для жизни осложнений – своевременное назначение хирургического лечения. Поскольку хирургическое лечение не приводит к полному излечению пациентов с БК, даже при радикальном удалении всех пораженных сегментов кишечника необходимо проведение противорецидивной терапии, которую следует начать не позднее 2 недель после перенесенного оперативного вмешательства.
Лекарственные препараты, назначаемые пациентам с БК, условно подразделяются на:
1. Средства для индукции ремиссии: системные ГКС (преднизолон и метилпреднизолон) и топические (будесонид), иммуносупрессоры (азатиоприн, 6- меркаптопурин, метотрексат), биологические генно-инженерные препараты: моноклональные антитела к ФНО-альфа (инфликсимаб, адалимумаб и цертолизумаба пэгол) и моноклональные антитела к интегринам, селективно действующие только в ЖКТ (ведолизумаб), а также антибиотики и салицилаты.
2. Средства для поддержания ремиссии (противорецидивные средства): иммуносупрессоры (азатиоприн, 6-меркаптопурин), биологические препараты (инфликсимаб, адалимумаб, цертолизумаба пэгол и ведолизумаб) и 5-аминосалициловая кислота и ее производные.
3. Вспомогательные симптоматические средства: парентеральные препараты железа для коррекции анемии, препараты для коррекции белково-электролитных нарушений, средства для профилактики остеопороза (препараты кальция) и др.
Тяжелая атака БК любой локализации требует проведения интенсивной противовоспалительной терапии в специализированном стационаре.
• При первой атаке лечение следует начинать с системных ГКС в комбинации с иммуносупрессорами (АЗА (2-2,5 мг/кг), 6-МП (1,5 мг/кг, а при непереносимости тиопуринов – метотрексат 25 мг/нед. п/к или в/м) или без них.Внутривенно вводят ГКС (преднизолон 75 мг/сут. или метилпреднизолон 60 мг/сут.) в течение 7-10 дней с последующим переходом на пероральный прием ГКС. Снижение дозы ГКС осуществляется по схеме.
• Для некоторых пациентов с редким рецидивированием заболевания допустимы повторные курсы ГКС терапии в сочетании с иммуносупрессорами.
• При отсутствии эффекта от ГКС, развитии стероидорезистентности, стероидозависимости или при неэфективности иммуносупрессоров (рецидив через 3-6 месяцев после отмены системных ГКС на фоне тиопуринов) показаны биологические препараты разных групп (анти-ФНО: инфликсимаб, адалимумаб, цертолизумаба пэгол или анти-интегриновые антитела: ведолизумаб).
• При рецидиве заболевания лечение рекомендуется сразу начинать с биологических препаратов в комбинации с иммуносупрессорами или без них. ГКС назначают только при невозможности применения биологических препаратов.
• Антибактериальная терапия: o 1 линия - метронидазол 1,5 г/сутки + фторхинолоны (ципрофлоксацин, офлоксацин) в/в 10-14 дней; o 2 линия - цефалоспорины в/в 7-10 дней; o 3 линия - рифаксимин в дозе 800-1200 мг в течение 14 дней. Данные, полученные при проведении систематических обзоров и мета-анализов диктуют необходимость дальнейших исследований для оценки целесообразности применения антибиотиков в лечении БК .
• Инфузионная терапия: регидратация, коррекция белково-электролитных нарушений.
• Коррекция анемии: гемотрансфузии (эритромасса) при анемии ниже 80 г/л, далее – терапия препаратами железа парентерально (железа(III) гидрооксид сахарозный комплекс, железа(III) гидрооксид декстрана, железо карбоксимальтозат).
• Энтеральное питание (зондовое) у истощённых пациентов.
• При достижении клинической ремиссии ГКС в комбинации с тиопуринами дальнейшее лечение (поддерживающая терапия) проводится АЗА/6-МП. В случае ремиссии, достигнутой любым из биологических препаратов, поддерживающее лечение проводится тем же препаратом строго в соответствии с инструкцией к препарату. Инфликсимаб можно комбинировать с АЗА. При невозможности проведения длительной терапии биологическими препаратами профилактика рецидива проводится тиопуринами.
Для больных с активной БК со стероидорезистентностью, стероидозависимостью или при неэфективности иммуносупрессоров (рецидив через 3-6 месяцев после отмены кортикостероидов на фоне АЗА/6-МП) показана биологическая терапия в виде индукционного курса (инфликсимаб, адалимумаб, цертолизумаба пэгол или ведолизумаба), с последующим переходом на длительное (многолетнее) поддерживающее лечение. Дозы биологических препаратов назначают в соответствии с инструкцией по применению. Отсутствие ответа на биологическую терапию определяется в течение 12 недель.
После достижения ремиссии любым из биологических препаратов следует перейти к поддерживающей терапии (с иммуносупрессорами или без них) по схеме, указанной в инструкции по применению. Для повышения эффективности лечения инфликсимабом рекомендуется комбинировать с иммуносупрессорами. Для адалимумаба и цертолизумаба пэгола целесообразность такой комбинации не доказана. Анти-ФНО препараты демонстрируют сходную эффективность и профиль безопасности, в связи с чем выбор препарата определяется лечащим врачом.
Потеря ответа на анти-ФНО терапию может привести к нарастанию активности заболевания, осложнениям и обсуждению вопроса о хирургическом лечении. При рецидиве заболевания лечение рекомендуется сразу начинать с биологических препаратов в комбинации с иммуносупрессорами или без них.
Биологическую терапию (особенно при назначении инфликсимаба) для большей эффективности необходимо сочетать с иммуносупрессивной (азатиоприн) терапией. Проведение хирургического вмешательства на фоне терапии иммуносупрессорами и биологическими препаратами, как правило, не требует изменения противорецидивной терапии.
27. Хронический гастрит. Определение. Современная классификация. Значение морфологического исследования слизистой оболочки желудка.+
К 29. ХГ - группа хронических заболеваний, которые морфологически характеризуются воспалительными и дистрофическими процессами в слизистой оболочке желудка, прогрессирующей атрофией с функциональной и структурной перестройкой и разнообразными клиническими признаками.
Классификация
Тип гастрита |
Этиологические факторы |
Неатрофический |
Helicobacter pylori |
Атрофический аутоиммунный |
Иммунные механизмы |
Атрофический мультифокальный |
Helicobacter pylori Нарушения питания Факторы среды |
Химический |
Химические раздражители Желчь (ДГР) Приём НПВС |
Радиационный |
Лучевое поражение |
Лимфоцитарный |
Идиопатический Иммунные механизмы Глютен Helicobacter pylori |
Гранулематозный |
Болезнь Крона Саркоидоз Гранулематоз Вегенера Инородные тела Идиопатический |
Эозинофильный |
Пищевая аллергия |
Гигантский гипертрофический |
Болезнь Менетрие |
Рабочая классификация хронических гастритов
По типу гастритов:
Неатрофический (поверхностный) гастрит.
Атрофический гастрит (аутоиммунный атрофический и мультифокальный атрофический).
Особые формы гастритов (реактивный, радиационный, лимфоцитарный, гранулематозный, эозинофильный, гигантский гипертрофический и др.).
По локализации:
Антральный отдел желудка.
Тело желудка.
Пангастрит.
По этиологическому фактору:
Инфекционные факторы (Нр, другие бактерии, кроме Нр, грибы, паразиты).
Неинфекционные факторы (аутоиммунные, алкогольный, постгастро-резекционный, воздействие желчи вследствие дуодено-гастральных рефлюксов, воздействие нестероидных противовоспалительных препаратов, воздействие химических агентов, воздействие радиации, нарушение питания, пищевая аллергия и др.).
Неизвестные факторы.
По эндоскопической картине:
Поверхностный (эриматозный/экссудативный) гастрит.
Эрозии.
Атрофии.
Метаплазия эпителия.
Геморрагии.
Гиперплазия слизистой.
Наличие ДГР и др.
По морфологии:
Степень воспаления.
Активность воспаления.
Наличие атрофии желудочных желез.
Наличие и тип кишечной метаплазии.
Степень обсеменения слизистой Нр.
По функциональному признаку:
Нормальная секреция.
Повышенная секреция.
Секреторная недостаточность (умеренная или выраженная).
По клиническим признакам:
Фаза обострения.
Фаза ремиссии.
Осложнения:
Кровотечения.
Малигнизация.
Значение морфологического исследования слизистой оболочки желудка
Гистология процесса представлена следующим образом: полиморфноядерные лейкоциты инфильтрируют собственную пластину, железы и фовеолярный эпителий, образуя небольшие микроабсцессы. Наблюдаются лимфоидные агрегаты и лимфоидные фолликулы, расширяющие собственную пластинку СО, иногда лимфоциты проникают в эпителий. Инфекция H. pylori – основная причина вторичной атрофии СО желудка. Атрофические изменения (как метапластические, так и неметапластические) в образце биопсии из угла и антрального отдела в первую очередь следует рассматривать как доказательства хеликобактерного гастрита.
На поздних стадиях атрофии, связанной с хронической инфекцией H. pylori, как в теле, так и в антральном отделе наблюдается обширное замещение КМ, связанной с развитием гипохлоргидрии. По мере распространения КМ количество бактерий H. pylori, обнаруживаемых в желудке, уменьшается, так как H. pylori исчезает из участков метапластического эпителия. Особое значение этой проблеме придает то, что атрофический гастрит является начальной ступенью каскада изменений СО, приводящего к злокачественному новообразованию желудка (каскад Корреа).
Типичные гистологические паттерны
Хронический антральный гастрит: инфильтрация собственной пластинки плазматическими клетками, лимфоцитами и небольшим количеством эозинофилов.
Активный хронический антральный гастрит: когда вышеперечисленные признаки связаны с нейтрофилами.
Лимфоидные фолликулы в СО антрального отдела встречаются часто, но неспецифичны.
28. Кислотозависимые заболевания. Дифференциальная диагностика при функциональной диспепсии и хроническом гастрите. Роль инфицирования Н.pylori. Стандарты диагностики и лечения. +
Кислотозависмые заболевания – группа заболеваний верхних отделов ЖКТ, обусловленных избыточной продукцией соляной кислоты париетальными клетками слизистой оболочки желудка.
Кислотозависимые заболевания желудочно-кишечного тракта:
Гастроэзофагеальная рефлюксная болезнь.
Хронический гастрит.
Язвенная болезнь желудка и 12- перстной кишки.
Функциональная желудочная диспепсия.
ГЭРБ - хроническое рецидивирующее заболевание, обусловленное спонтанным, регулярно повторяющимся забросом в пищевод желудочного и/или дуоденального содержимого, приводящему к поражению нижнего отдела пищевода.
ХГ - группа хронических заболеваний, которые морфологически характеризуются наличием воспалительных и дистрофических процессов в слизистой оболочке желудка, прогрессирующей атрофией, функциональной и структурной перестройкой с разнообразными клиническими признаками или бессимптомным течением.
Язвенная болезнь - хроническое рецидивирующее заболевание, протекающее с чередованием периодов обострения и ремиссии, ведущим проявлением служит образование дефекта (язвы) в стенке желудка или двенадцатиперстной кишки
Диспепсия – это боль или дискомфорт (чувство тяжести, переполнения, неопределенное неприятное ощущение) в верхней части живота, преимущественно по срединной линии. Иногда может присутствовать также чувство тошноты.
Дифф. диагностика
ХГ несет информацию о морфологических процессах в слизистой оболочке желудка с позиций их значения как предраковых изменений.
Диагноз «хронический гастрит» не несет никакой информации о наличии у больного каких-либо жалоб, поскольку, в большинстве случаев хронический гастрит протекает бессимптомно. Попытка выйти из положения в таких случаях с помощью формулировки диагноза как «хронический гастрит в стадии обострения» (при наличии симптомов диспепсии) или «хронический гастрит в стадии ремиссии» (при их отсутствии) не решает проблему, поскольку обострение и ремиссия хронического гастрита - это понятия сугубо морфологические и не коррелируют с наличием или отсутствием клинических симптомов (можно иметь хронический гастрит с выраженной морфологической активностью и отсутствием каких-либо клинических симптомов и, наоборот, гистологически неактивный поверхностный хронический гастрит с выраженными диспепсическими жалобами).
Диагноз «хронический гастрит» не способен объяснить механизм возникновения имеющихся у больного симптомов диспепсии и, соответственно, не может помочь в выборе лекарственных препаратов, способствующих их устранению. Указанные пробелы восполняет диагноз «функциональная диспепсия».
Диагноз «функциональная диспепсия» позволяет правильно понять патогенез диспепсических симптомов, которые могут отмечаться у больных хроническим гастритом. Позволяет оптимизировать лечение больных, определяя выбор тех или иных групп лекарственных препаратов.
Хронический гастрит, обнаруженный у больного при эндоскопическом исследовании (желательно, чтобы он был подтвержден при гистологическом исследовании), и клинический симптомокомплекс, свойственный функциональной диспепсии, могут и должны комбинироваться при постановке общего диагноза и шифроваться в МКБ-10 с использованием рубрики как «хронический гастрит», так и рубрики «функциональное расстройство желудка».
Роль инфицирования Н.pylori
Преобладание инфекции в антральном отделе желудка приводит к повышению секреции гастрина, скорее всего из-за локального снижения синтеза соматостатина. Возникающая гиперсекреция соляной кислоты предрасполагает к развитию препилорической и дуоденальной язвы. Инфекция, преобладающая в теле, приводит к атрофии слизистой желудка и снижению продукции кислоты, возможно из-за увеличения локальной секреции интерлейкина 1b. Пациенты с преобладанием инфекции в теле предрасположены к язве желудка и аденокарциноме.
Аммиак, вырабатываемый Helicobacter pylori, позволяет организму выжить в окружающей его кислой среде желудка и разрушить слизистый барьер. Цитотоксины и муколитические ферменты, вырабатываемые Helicobacter pylori, могут играть роль в повреждении слизистой оболочки и последующем ульцерогенезе.
Диагностика
Клинический анализ крови (изменения характерны только для атрофического гастрита в сочетании с В12-дефицитной анемией: снижение содержания гемоглобина, увеличение ЦП, появление мегакариоцитов).
Клинический анализ мочи, кала, кал на скрытую кровь (изменения не характерны). Биохимическое исследование крови (изменения не характерны).
Инвазивные методы: быстрый уреазный тест, морфологические методы.
Неинвазивные методы: дыхательный тест с мочевиной, меченной 13С, и определение антигена H. pylori в кале.
Серологические методы: определение АТ к Н. Pylori в крови.
Лечение
Антисекреторная терапия основывается на применении ингибиторов протонной помпы (ИПП) и блокаторов Н2-гистаминорецепторов. ИПП используют в стандартной дозе (омепразол 20 мг, лансопразол 30 мг, пантопразол 40 мг, рабепразол 20 мг, эзомепразол 20 мг) 1 раз в день утром натощак за 30-60 мин до еды, длительность лечения – до 4 нед. В качестве блокатора Н2-гистамино-рецепторов применяют фамотидин в дозе 20 мг 2 раза в день (утром и вечером), длительность лечения – до 4 нед.
Антацидные средства (невсасывающиеся антациды) – гефал, альмагель, маалокс, фосфалюгель и подобные применяют по стандартной дозе короткими курсами по несколько дней или «по требованию» во время болей или перед их обычным возникновением.
При наличии инфекции H.pylori у пациентов с функциональной диспепсией эрадикационная терапия осуществляется по правилам, описанным в разделе «Хронический гастрит».
Гастропрокинетические препараты (прокинетики) являются терапией выбора постпрандиального дистресс-синдрома. Прокинетики усиливают и нормализуют гастродуоденальную перистальтику и эвакуацию, оказывают противорвотный эффект, повышают тонус нижнего пищеводного сфинктера. Общее противопоказание для приема прокинетиков: желудочно-кишечное кровотечение, механическая непроходимость, перфорация.
К прокинетикам, используемым в клинической практике, относятся: антагонисты допаминергических D2 -рецепторов (центральных и периферических) – метоклопрамид и домперидон; антагонист дофаминовых D2-рецепторов и блокатор ацетилхолинестеразы – итоприд.
Метоклопрамид является прокинетиком первого поколения, применяется в таблетках по 10 мг 3-4 раза в день до еды, курс лечения 2-4 нед. Имеется парентеральная форма в ампулах по 2 мл (10 мг), вводят внутримышечно или внутривенно по 1–2 мл до 4 раз в сутки.
Домперидон оказывает умеренный прокинетический эффект на кишечник. Домперидон назначают по 10 мг (1 табл) 3 раза в день за 10–30 мин до еды и, при необходимости, на ночь. При нарушении функции почек дозу препарата необходимо уменьшить.
Итоприда гидрохлорид применяют по 1 табл. (50 мг) 3 раза в день. Регулирующим влиянием на желудочно-кишечную моторику обладает тримебутин (дебридат, трибукс) – периферический антагонист опиатных рецепторов; ингибирует освобождение ацетилхолина, возможно действие на высвобождение норадреналина. Применяют по 100–200 мг 3 раза в день в течение 2 нед.
29. Дисфагия. Определение. Алгоритм диагностического поиска при ахалазии и раке пищевода. Тактика ведения и лечения.+
Дисфагия — это патологическое состояние, при котором нарушается акт глотания. Проявляется затруднением проглатывания твердой пищи, жидкостей, слюны, их попаданием в органы дыхания, усиленным образованием слюны, болевыми ощущениями за грудиной, осиплостью голоса, першением в горле.
Ахалазия кардии – хроническое нервно-мышечное заболевание пищевода, при котором нарушается прохождение пищевых масс по пищеводу и из пищевода в желудок вследствие патологических изменений пищеводной перистальтики и отсутствия рефлекторного расслабления нижнего пищеводного сфинктера (кардии) во время глотания.
Диагностика
При рентгенологическом исследовании отмечается наличие натощак в пищеводе большого количества содержимого, а также замедление прохождения взвеси сульфата бария из пищевода в желудок. Важным диагностическим симптомом служит отсутствие газового пузыря желудка. Дистальный отдел пищевода сужен. Это ровное сужение, переходящее в супрастенотическое (веретенообразное или S-образное) расширение пищевода, дает рентгенологический симптом «мышиного хвоста».
При эндоскопии выявляются расширение пищевода (часто с атонией его стенки), признаки застойного эзофагита (отек и гиперемия слизистой оболочки), иногда с участками метаплазии эпителия (лейкоплакия). Вход в кардию закрыт, однако эндоскоп (в отличие от сужения, обусловленного злокачественной опухолью) проводится в желудок без большого сопротивления.
Диагноз ахалазии кардии подтверждается и с помощью эзофаготономанометрического исследования. При этом обнаруживаются отсутствие рефлекса раскрытия кардии при глотании, повышение тонуса НПС, различные нарушения перистальтики грудного отдела пищевода.
Важную роль в распознавании злокачественных новообразований пищевода принадлежит рентгенологическому исследованию. При экзофитном росте опухоли с распадом и изъязвлением выявляется дефект наполнения с неровными «изъеденными» краями. При эндофитном и инфильтративном росте отмечается плоский дефект наполнения, циркулярно суживающий просвет пищевода; стенка пищевода в этом участке становится ригидной.
Достаточно точным методом дооперационной диагностики, позволяющим определить распространенность опухолевого процесса (особенно при его локализации в средней трети пищевода) является компьютерная томография. В распознавании поражения средостения и метастазов в печени может помочь также магнитно-резонансная томография.
Достаточно надежным методом дооперационной диагностики стадии рака пищевода (с точностью, составляющей 80-90%) в настоящее время становится эндосонография. Она позволяет выявить опухоли, размеры которых не превышают 3 мм, а также дает возможность оценить (на глубину до 5 см) состояние тканей, окружающих пищевод (в первую очередь, региональных лимфатических узлов).
Наиболее точным методом диагностики рака пищевода является ЭГДС. При этом при экзофитном росте определяется бугристая опухоль, выступающая в просвет пищевода, легко кровоточащая при контакте с эндоскопом. При эндофитном росте обмечается ригидность стенки пищевода в месте поражения, при изъязвлении опухоли образуются язвы неправильной формы с бугристыми неровными краями.
При локализации злокачественной опухоли в верхней трети пищевода для исключения прорастания в трахеобронхиальное дерево, которое наблюдается почти в 30% случаях, дополнительно проводится бронхоскопия.
Лечение
Основным методом лечения ахалазии кардии, который оказывается эффективным у 60-90% больных, является пневмокардиодилатация. При ее проведении используются баллоны, имеющие диаметр до 50 мм, устанавливаемые пищевод под рентгенологическим контролем, в которых при поэтапном расширении кардии последовательно повышается давление (со 180- 200 мм рт. ст. до 340-360 мм рт. ст.). Пневмокардиодилатация приводит к исчезновению у больных дисфагии, причем у значительной части пациентов эффект сохраняется в течение многих лет.
Вспомогательную роль в лечении больных ахалазией кардии играют лекарственные препараты. При сопутствующей гипермоторной дискинезии грудного отдела пищевода применяют нитраты (например, изосорбит динитрат в дозе 0,005-0,01 г 3 раза в день перед едой) или блокаторы кальциевых каналов (нифедипин по 0,01-0,02 г 3 раза в день). Для лечения сопутствующего эзофагита назначают соответствующую диету, обволакивающие и вяжущие средства.
В последние годы предпринимаются попытки применения для лечения больных ахалазией кардии токсина ботулизма, который вводится инъекционно (в дозе 80 единиц) при эзофагогастроскопии в область НПС.
При неэффективности пневмокардиодилатации, а также при осложненном течении заболевания, проводится хирургическое лечение (операция миотомии по Геллеру). В настоящее время все чаще используются лапароскопические модификации этой операции, дающие лучшие функциональные результаты.
Излечение больных раком пищевода достигается только при применении хирургического метода. Проведение радикальной операции оказывается возможным только в тех случаях, когда отсутствует прорастание опухоли в органы средостения и нет метастазов в отдаленных лимфатических узлах, доступных для оперативного удаления, а также других органах (печени, легких). В настоящее время проводятся в основном два вида радикальных операций при раке пищевода: трансторакальная эзофагэктомия «единым блоком», при которой наряду с пищеводом удаляются медиастинальные, перикардиальные и супрапанкреатические лимфатические узлы вместе с непарной веной и грудным лимфатическим протоком, и так называемая стандартная эзофагэктомия.
Лучевая терапия чаще всего применяется с паллиативной целью при неоперабельном раке пищевода. У большинства больных (70%) она способствует уменьшению размеров опухоли и исчезновению дисфагии.
Широкое распространение в лечении рака пищевода получили в последние годы эндоскопические методы. К ним носятся эндоскопическая резекция опухоли (при раннем раке пищевода), эндоскопическое бужирование пищевода в сочетании с лазеротерапией и установкой саморасширяющихя металлических эндопротезов (стентов) с целью восстановления проходимости пищевода в неоперабельных случаях рака.
30. Гепатомегалия. Цирроз печени. Ранняя диагностика синдрома портальной гипертензии. Лечение и профилактика кровотечений из расширенных вен пищевода
Гепатомегалия – синдром, характеризующийся патологическим истинным увеличением печени в размерах. О гепатомегалии говорят, когда размер печени превышает 12 сантиметров по правой среднеключичной линии, а край левой доли пальпируется в эпигастральной области.
Цирроз печени – это диффузный процесс, характеризующийся фиброзом и трансформацией нормальной структуры печени с образованием узлов регенерации. Цирроз печени представляет собой финальную стадию ряда хронических заболеваний печени.
Синдром портальной гипертензия – клинический синдром, обусловленный повышенным давлением в системе воротной вены, вследствие затруднения кровотока в портальной вене/ печеночных венах /нижней полой вене.
Диагностика
Диагностики заболеваний, которые привели к циррозу печени, являющемуся наиболее часто причиной развития портальной гипертензии:
а. антитела к вирусам хронического гепатита
б. онкомаркеры
Оценка функции печени:
а. коагулограмма (снижение протромбинового индекса)
б. биохимический анализ крови (АСТ, АЛТ, билирубин, ГГТП, ЩФ, калий, натрий, креатинин, альбумин, мочевина)
Оценка наличия гиперспленизма:
а. клинический анализ крови (анемия, лейкопения, тромбоцитопения)
Контрастная рентгенография пищевода указывает на наличие варикозного расширения вен пищевода и кардиального отдела желудка.
Эзофагогастродуоденоскопия позволяет диагностировать варикозные вены пищевода, портальную гипертензионную гастропатию.
Трансабдоминальное УЗИ органов брюшной полости позволяет определить увеличение печени и селезенки, наличие асцитической жидкости в брюшной полости, диаметр воротной вены, печеночных вен и нижней полой вены; выявить места сдавления воротной и нижней полой вены Увеличение диаметра селезеночной вены более 10 мм, воротной - более 15 мм достоверно свидетельствует о наличии портальной гипертензии.
Ультразвуковая допплерография печеночных и портальных вен позволяет получить информацию о гемодинамике в портальной системе и развивающихся коллатералях; установить изменения направления кровотока (он может отсутствовать, быть обратным или турбулентным).
КТ-ангиография позволяет получить информацию о величине, форме, состоянии сосудов печени, плотности паренхимы органа.
Магниторезонансная томография позволяет определить уровень блокады портального кровообращения и степень выраженности коллатерального кровотока; состояние отводящих вен печени и наличие асцита.
Гепатосцинтиграфия позволяет определять (по распределению радиофармпрепарата) поглотительно-экскреторную функцию печени; можно оценить выраженность цирротических изменений в печени.
Транскавальная печеночная венография определение проходимости печеночных вен и печеночного сегмента нижней полой вены (при подозрении на синдром Бадда-Киари); оценка эффективности хирургической терапии.
Портография позволяет судить о состоянии спленопортального русла, с помощью серийных снимков, полученных в ходе ангиографии, можно изучить все фазы кровотока в печени - артериальную, паренхиматозную и венозную, изучение снимков венозной фазы дает возможность оценить состояние портальной системы.
Спленоманометрия установление формы портальной гипертензии, определение величины давления в портальной системе и оценки состояния сосудистого русла измерение уровня заклиненного печеночно-венозного давления в системе воротной вены и ее ветвей . Повышение давления свыше 300-350 мм вод.ст. является фактором риска возникновения кровотечений из варикозно-расширенных вен пищевода.
Биопсия печени могут быть получены различные гистологические результаты, которые определяются тем заболеванием, которое привело к нарушению кровообращения в системе портальной вены.
Фибросканирование (эластометрия печени) - инновация в сфере диагностики цирроза. Неинвазивный (ультразвуковой) метод оценки состояния тканей печени имеющий высокий уровень корреляции с данными биопсии печени:
• F0- фиброзные изменения отсутствуют.
• F1- начальные изменения; единичные очаги фиброза.
• F2- умеренно выраженный фиброз.
• F3- выраженный фиброз, очаги цирроза.
• F4- сформированный цирроз.
Лечение и профилактика кровотечений из расширенных вен пищевода
Восполнение ОЦК.
ИТТ при легкой степени кровопотери:
· Кровопотеря 10-15% ОЦК (500-700 мл): внутривенное переливание кристаллоидов (декстроза, натрия ацетат, натрия лактат, натрия хлорида 0,9%) в объеме 200% от объема кровопотери (1-1,4 л).
ИТТ при средней степени кровопотери:
· Кровопотеря 15-30% ОЦК (750-1500 мл): в/в кристаллоиды (раствор глюкозы, натрия хлорида 0,9%, натрия ацетат, натрия лактат) и коллоиды (желатин), в соотношении 3:1 с общим объемом 300% от объема кровопотери (2,5-4,5 литров); ИТТ при тяжелой степени кровопотери:
· При кровопотере 30-40% ОЦК (1500-2000 мл): в/в кристаллоидов (декстроза, натрия хлорида 0,9%, натрия ацетат, натрия лактат) и коллоидов (гелофузин) в соотношении 2:1 с общим объемом 300% от объема кровопотери (3-6 литров). Показано переливание компонентов крови (эритроцитарная масса, СЗП 30% от перелитого объема, тромбоконцентрата при уровне содержания тромбоцитов < 50х109) и препарата крови - раствор альбумина при гипопротеинемии (общий белок < 60 г/л) и гипоальбуминемии (альбумин < 35 г/л).
Препараты витамина К:
Менадиона натрия бисульфит по 2 мл 3 раза в/внутривенно.
Ингибиторы протеолиза (апротинин/аналоги: контрикал, апротинин) снижают потребность в проведении заместительной терапии и уменьшают кровопотерю. Рекомендовано применение 50 000 ЕД контрикала, затем 10 000-20 000 через каждые 4-6 часов. Начальная доза апротинина при геморрагическом шоке 500 тыс. КИЕ. Скорость введения не более 5 мл/мин, затем в/в капельно 50 тыс КИЕ в час.
Фармакологическая терапия для снижения портального давления: Применение вазоактивных препаратов способствуют остановке кровотечения в 75-80%. Из сосудосуживающих препаратов (для снижения ПД), используемых в лечении кровотечения из ВРВ, имеют преимущество меропенем и его аналоги: октреотид и вапреотид, так как они имеют низкий побочный эффект.
Октреотид: вводится болюсно внутривенно 50 мкг/ч с последующим непрерывным в/в введением через дозатор 50 мкг/ч в течение 5 дней или капельно в/в 5 дней (УД-5D). Или вводится 0,025 мг/ч.
Соматостатин: болюсно в/в 250 мкг в течение 5 минут и можно повторить 3 раза в течение 1 часа. Далее непрерываное введение 6 мг (=250 мкг) в течение 24 часов. Доза может быть повышена до 500 мкг/ч.
Терапия первой линии комбинированная терапия:
· применение неселективных β-блокаторов для снижения портального давления: пропранолол в дозе 20 мг 2 раза в сутки или надолол 20-40 мг 1-2 раза в сутки. Коррекция дозы по урежению ЧСС (довести 55-60 в 1 мин); · + лигирование ВРВ (EVL). Накладываются до 6 колец на вены каждые 1-2 недели. Первая контрольная ЭФГДС через 1-3 месяцев и в последующем каждые 6-12 месяцев для контроля за рецидивом ВРВ.
Терапия второй линии:
· если NSBB+ EVL была не эффективной, тогда показана операция TIPS или шунтирующие, но лишь пациентам класса А по тяжести течения ЦП. Класса В и С эти операции не показаны, так как приводят к развитию энцефалопатии
Для вторичной профилактики кровотечения из ВРВ не показано: · NSBB+склеротерапия;
· EVL+склеротерапия.
31.Воспалительные заболевания кишечника. Язвенный колит. Диагностика. Дифференциальный диагноз с колитами инфекционной этиологии, псевдомембранозным колитом.+
Язвенный колит – хроническое воспалительно-язвенное заболевание слизистой оболочки толстой кишки, чаще всего проявляющееся кровянистой диареей.
Диагностика.
Кровь — характерны: анемия (как правило, смешанного генеза: анемия хронических заболеваний с дефицитом железа), лейкоцитоз, тромбоцитоз, ускорение СОЭ и повышение С-реактивного белка. Возможно снижение железа, сывороточного ферритина, витамина B12 (в случае поражение проксимальных отделов кишечника и желдука), диспротеинемия с гипоальбуминемией (как результат нарушения всасывания в кишечнике). В иммунограмме: часто — повышение гипергаммаглобулениемия (IgG), иногда отмечается селективный дефицит IgA.
Определение ASCA (антител к Saccharomyces cerevisae), для диагностически сложных случаев, помогает подтвердить, может служить дополнительным серологическим маркером в диагностике болезни Крона;
Анализы кала— с целью исключения инфекционной причины энтерита и колита. Включают бактериологические тесты на определение шигел, сальмонел, иерсиний, кампилобактера, клостридий (Cl. Difficile), туберкулезной палочки, дизентерийной амебы, различных гельминтов и паразитов.
Кальпротектин — белок, продуцируемый нейтрофилами слизистой оболочки кишечника. Его уровень повышен при болезни Крона и язвенном колите, кроме того этот показатель повышен при инфекционных поражениях кишечника, онкологических заболеваниях. Проведение посевов крови и кала обязательно в случае септических состояний
Диагностические критерии
1) эндоскопия — макроскопическая картина и результат гистологического исследования биоптата слизистой оболочки толстой кишки;
2) выделение из кала штамма C. difficile, продуцирующего токсины и/или обнаружение токсинов C. difficile в кале. Лихорадка и лейкоцитоз свидетельствуют о более тяжелом течении
Дифференциальная диагностика
Диарея другой этиологии — на основе анамнеза и микробиологических исследований; язвенный колит — отличается постоянной примесью свежей крови в стуле, другой микроскопической картиной изменений слизистой оболочки, а также неэффективностью лечения метронидазолом.
Псевдомембранозный колит - это заболевание, характеризующееся повреждением слизистой оболочки толстой кишки с очаговыми или диффузными фибринозными наложениями, возникающими в результате воздействия факторов патогенности Clostridium difficile
32.Желчнокаменная болезнь. Определение. Классификация. Стандарты диагностики и лечения. Показания к холецистэктомии.
Жёлчнокаменная болезнь (ЖКБ, син.: холелитиаз) — хроническое заболевание с генетической предрасположенностью, при котором наблюдается образование камней в жёлчных путях. При образовании камней в жёлчном пузыре (ЖП) говорят о «холецистолитиазе», в общем жёлчном протоке — о «холедохолитиазе», во внутрипеченочных протоках — о «внутрипеченочном холелитиазе».
Различают камни двух основных видов — холестериновые и пигментные.
Камни размером до 1 см условно обозначают как мелкие, 1–2 см — средние и более 2 см — крупные, хотя при проведении инструментальной диагностики возможны ошибки в оценке размера камней
I стадия – начальная (предкаменная):
а) густая неоднородная желчь;
б) формирование билиарного сладжа (с наличием микролитов,
замазкообразной желчи, сочетание замазкообразной желчи с микролитами).
II стадия – формирование желчных камней:
а) по локализации (в желчном пузыре, в общем желчном протоке,
печёночных протоках);
б) по количеству конкрементов (одиночные, множественные);
в) по составу (холестериновые, пигментные, смешанные);
г) по клиническому течению (латентное, болевая форма, диспепсическая
форма, под маской других заболеваний).
III стадия – хронический рецидивирующий калькулёзный холецистит.
IV стадия – осложнения.
Выделяют также клинические формы калькулёзного холецистита:
- латентная форма;
- диспепсическая форма;
- хроническая болевая форма;
- желчная колика; желтушная форма;
- атипичная форма (стенокардитическая и др.).
Диагностика.
УЗИ печени и жёлчных путей
Обзорная рентгенография брюшной полости
Эндоскопическая ретроградная холангиография (ЭРХГ)
Магнитно-резонансная холангиопанкреатография (МР-ХПГ)
Эндоскопическое ультразвуковое исследование (эндоУЗИ)
Лечение
Образ жизни, питание
Поддержание нормальной массы тела и рациональное питание помогают предотвращать развитие острого холецистита. Калорийность рациона должна быть умеренной, прием пищи — дробным (5–6 раз в день с перерывами не более 4–5 ч, за исключением ночи).
Тактика лечения:
- хенодезоксихолевая кислота (ХДХК) 15мг/кг/сут, одноразово вечером (у 30% больных возникает диарея и транзиторно повышается активность АСТ, АЛТ);
- урсодезоксихолевая кислота (урсохол) 10мг/кг/сут. Одноразово вечером (у 2% больных возникает диарея);
- ХДХК 7-8мг/кг/сут + УДХК 7-8мг/кг/сут. Одноразово вечером (у 5% больных диарея, редко транзиторное повышение уровня сывороточных трансаминаз);
- продолжительность лечения 18-24 дня.
Показания к холецистэктомии
острый холецистит (воспаление желчного пузыря);
хронический холецистит с повторяющимися обострениями;
закупорка (обструкция) желчного протока – как правило, вызывается попаданием камня в желчный проток
33. Биохимические синдромы при заболеваниях печени. Диагностика и принципы лечения хронического гепатита с учетом этиологии (вирусной, аутоиммунной, лекарственно-индуцированной).
1. цитолиз
2. холестаз
3. мезенхимально-воспалительный
4. печеночно-клеточная недостаточность
(гиперазотемия)
5. портальная гипертензия
6. гиперспленизм
7. синдром патологической регенерации
и опухолевого роста
8. геморрагический
9. астенический
10. диспептический
Диагностика
(1) Оценка тяжести поражения печени должна включать контроль биохимических показателей, в т. ч. аспартатаминотрансферазы (АСТ), АЛТ, гамма-глутамилтранспептидазы (ГГТ), щелочной фосфатазы, уровень билирубина, альбумина плазмы и глобулинов, общий анализ крови, протромбиновое время и УЗИ печени (A1). Обычно активность АЛТ выше, чем АСТ. Однако при прогрессировании заболевания и развитии цирроза печени может наблюдаться обратное соотношение. Характерные признаки цирроза — прогрессирующее снижение уровня альбумина плазмы и/или повышение уровня гамма-глобулинов и удлинение протромбинового времени, что часто сопровождается снижением числа тромбоцитов.
(2) Выявление ДНК HBV и определение ее концентрации чрезвычайно важны для диагностики, решения вопроса о проведении терапии и дальнейшего наблюдения пациентов (A1). Настоятельно рекомендуется использование количественных методов определения уровня ДНК HBV на основе полимеразной цепной реакции (ПЦР) в режиме реального времени, что обусловлено их высокой чувствительностью, специфичностью, точностью и широким динамическим диапазоном [38–41] (A1). Всемирная организация здравоохранения (ВОЗ) определила международный стандарт для унификации описания концентраций ДНК HBV [42]. Концентрацию HBV-ДНК в сыворотке следует выражать в МЕ/мл, чтобы обеспечить возможность сравнения результатов.
(3) Необходимо также проводить систематический поиск других возможных причин хронического заболевания печени, включая коинфекцию HDV, HCV и/или ВИЧ (A1). У пациентов с хронической HBV-инфекцией требуется также определять антитела к вирусу гепатита А (анти-HAV), а при их отсутствии следует рекомендовать вакцинацию против HAV. Необходимо также принимать во внимание наличие сопутствующих заболеваний, таких как алкогольные, аутоиммунные и метаболические поражения печени, сопровождающиеся стеатозом или стеатогепатитом (A1).
Лечение
1. Патогенетическая терапия:
инфузионная, дезинтоксикационная
сорбенты
нормализация функций ЖКТ (пробиотики, ферменты)
нормализия функций ЖВП
улучшение тканевого обмена (атигипоксанты, гепатопротекторы)
2. Симптоматическая терапия
3. Этиотропная противовирусная терапия - ламивудин 4. Иммуномодулирующая и иммунокорригирующая терапия
тенофовира алафенамид 25 мг 1 раз в день внутрь,
тенофовира дизопроксила фумарат 300 мг 1 раз в день внутрь и энтекавир 0.5 мг 1
раз в день внутрь в качестве монотерапии,
не рекомендованные режимы: ламивудин и телбивудин,
длительность терапии- пожизненно, не менее 5-лет
34. Дифференциальная диагностика и врачебная тактика при заболеваниях поджелудочной железы. Стандарты лечения.
Классификация+
I. Пороки развития:
Аномалия положения
Добавочная железа
Кольцевидная железа
II. Повреждения:
Закрытые
Открытые
Ш.Панкреатиты:
Острые
Хронические
IV. Опухоли:
Доброкачественные
Злокачественные
V. Кисты:
1.Ложные
Истинные
VI. Свищи:
Наружные
Внутренние
Острый панкреатит – воспалительно-некротическое поражение поджелудочной железы, развивающееся в результате ферментативного аутолиза или самопереваривания.
Лабораторные методы:
общий анализ крови (нейтрофильный лейкоцитоз со сдвигом формулы влево, ускоренное РОЭ)
биохимический анализ крови (повышение активности амилазы, липазы, трипсина), снижение активности ингибиторов трипсина, повышение уровня билирубина, гипергликемия, снижение кальция);
анализ свертывающей системы крови (гиперкоагуляция при отечной форме и жировом панкреонекрозе, гиперкоагуляция - при геморрагическом панкреонекрозе, гиперфибриногенемия);
изменение калликреин-кининовой системы (снижение уровня кининогена, прекалликреина, ингибитора калликреина);
анализ мочи (амилазурия, резкое снижение суточного и часового диуреза вплоть до анурии, протеинурия, микрогематурия, цилиндрурия);
соотношение клиренса амилазы и клиренса криатенина более 5.
3. Рентгенодиагностика;
обзорная рентгеноскопия (высокое стояние левой половины диафрагмы, ограничение ее подвижности, выпот в левом плевральном синусе, парез кишечника);
контрастное исследование желудка и 12-перстной кишки (смещение желудка кпереди, расширение петли 12-перстной кишки);
компьютерная томография.
4. Специальные методы исследования:
гастро- и дуоденоскопия (огтеснение задней стенки желудка и привратника, гиперемия, отек и эрозии в области оттеснения, разворот петли 12-перстной кишки, дуоденит);
лапароскопия (бляшки очаговых некрозов жировой ткани, выпот в брюшной полости с высокой активностью ферментов).
Течение острого панкреатита считается легким, если определяются благоприятные прогностические признаки и отсутствуют системные осложнения. Лечение заключается в проведении поддерживающей терапии. Необходимо осуществлять адекватную компенсацию потерь циркулирующей жидкости в результате рвоты и диафореза. Возникновение гиповолемии может привести к трансформации заболевания в некротизирующий панкреатит. Для купирования боли можно использовать наркотические анальгетики (меперидин 50 - 100 мг внутримышечно каждые 3 - 4 ч или гидроморфон), включая морфин. При развитии инфекции дыхательной системы, желчевыводящих или мочевых путей проводится соответствующая антибактериальная терапия. Прием пищи возобновляют на 3-7-й день пребывания в больнице после исчезновения резистентности живота, значительного стихания болей, при восстановлении перистальтических шумов и появлении у больного чувства голода. Желательно начинать с дробного приема пищи, состоящей прежде всего из углеводов, которые в меньшей степени, чем жиры и белки, стимулируют секрецию поджелудочной железы.
35. Клинические и лабораторные синдромы при заболеваниях печени
Коэффициент де Ритиса (известное также как АсАТ/АлАТ и АСТ/АЛТ) — соотношение активности сывороточных АСТ (аспартатаминотрансфераза) и АЛТ (аланинаминотрансфераза). Значение коэффициента в норме составляет 1,33±0,42 или 0,91-1,75. Коэффициент де Ритиса в пределах нормальных значений (0,91-1,75) обычно характерен для здоровых людей. Однако, повышение АСТ при одновременном росте отношения АСТ/АЛТ (коэффициент де Ритиса больше 2) свидетельствует о поражении сердца, и можно с уверенностью говорить об инфаркте миокарда или ином процессе, связанным с разрушением кардиомиоцитов. Коэффициенте де Ритиса меньше 1 говорит о поражении печени.
В клинической картине заболевания гепатобилиарной системы выделяют следующие синдромы:
синдром гепатомегалии;
синдром желтухи;
синдром холестаза;
синдром печеночно-клеточной недостаточности;
синдром портальной гипертензии;
отечно-асцитический синдром;
синдром спленомегалии;
синдром гиперспленизма(лабораторный);
цитолитический синдром;
мезенхимально-воспалительный синдром;
синдром малых признаков;
астено-вегетативный синдром;
гепаторенальный синдром;
геморрагический синдром;
анемический синдром
Синдром цитолиза
(цитолитический синдром или синдром нарушения целостности гепатоцитов) ↑ АсАТ, АлАТ, ЛДГ и ее изоферментов – ЛДГ4 и ЛДГ3, фруктозо-1-фосфатальдолазы, сорбит-дегидрогеназы, а концентрации ферритина, сывороточного железа, витамина В12 и билирубина за счет повышения прямой фракции
Синдром холестаза
(экскреторно-билиарный синдром, холестатический синдром ↑ ЩФ, ЛАП, ГГТФ, холестерина, Р-липопротеинов, конъюгированной фракции билирубина, желчных кислот, фосфолипидов
Синдром печеночно-клеточной недостаточности
(синдром синтетической недостаточности) ↓ общего белка (особенно альбумина), трансферрина, холестерина, II, V, VII факторов свертывания крови, холинэстеразы, альфа-липопротеинов
↑ билирубина за счет неконъюгированной фракции
Мезенхимально-воспалительный синдром ↑ СОЭ, появление в крови С-реактивного белка, ревматоидного фактора, антител к субклеточным фракциям гепатоцита, антимитохондриальных и антиядерных антител, изменение количества и функциональной активности Т - и В-лимфоцитов, повышение уровня иммуноглобулинов. 36. Дифференциальный диагноз при болях в эпигастральной области. Стандарты диагностики и лечения болевого синдрома при хроническом панкреатите.+

Основные методы купирования боли при хроническом панкреатите:
Анальгетики
Подавление воспаления ткани поджелудочной железы
Прекращение приема алкоголя
Воздействие на иннервацию
медикаментозное (амитриптилин, доксепин)
чрескожная электрическая стимуляция нервов
оперативное (двустороннее пересечение внутренностных нервов, интраплевральная анальгезия, блокада чревного сплетения введением алкоголя, стероидов)
Антиоксиданты, аллопуринол
Снижение интрапанкреатического давления
подавление секреции - омепразол, Н2-блокаторы - панкреатические ферменты - соматостатин
устранение обструкции - стенты - удаление камней - хирургическое лечение Основные причины развития синдрома ОЖ:
1. Острые воспалительные заболевания органов пищеварения.
2. Перфорации полого органа, возникающие вследствие различных заболеваний или повреждений органов брюшной полости.
3. Механическая кишечная непроходимость.
4. Острые нарушения мезентериального артериального и венозного кровообращения.
5. Внутренние кровотечения в брюшную полость и забрюшинное пространство.
6. Острые воспалительные процессы и нарушение кровообращения в придатках матки.
37. Дифференциальная диагностика и врачебная тактика при болях в правом подреберье. Тактика ведения и консервативная терапия при печеночной колике.+
Правый верхний отдел живота (правое подреберье)
Билиарная боль Постоянная, быстро усиливается с достижением «плато», длится до 4–6 ч, может отдавать в надлопаточную область
Острый холецистит более продолжительная (более 6 ч) билиарная боль с появлением локальной болезненности, защитного напряжения мышц, лихорадки и/или лейкоцитоза
Диспепсия вздутие живота, тошнота, отрыжка, плохая переносимость жирной пищи
Язва двенадцатиперстной кишки Боль, возникающая через 2 ч после приема пищи, стихающая после приема пищи или антацидов
Абсцесс печени Боль, ассоциированная с лихорадкой и ознобом, пальпируемая печень, болезненность и напряжение мышц в правом подреберье
Инфаркт миокарда Боль/дискомфорт в правом верхнем квадранте живота или эпигастральной области, может иметь сходство с билиарной болью
Принципы лечения При бессимптомном течении наиболее целесообразно придерживаться тактики наблюдения пациента без активного лечения.Образ жизни, питание поддержание нормальной массы тела и рациональное. Калорийность рациона должна быть умеренной, прием пищи — дробным (5–6 раз в день с перерывами не более 4–5 ч, за исключением ночи). Целесообразно употреблять продукты, обогащенные пищевыми волокнами (свежие фрукты и овощи), злаками (зерновой хлеб, овес, коричневый рис, продукты с отрубями), полезны фасоль и чечевица, из мясных продуктов следует отдавать предпочтение содержащим меньшее количество жира
38. Дифференциальный диагноз и лечение при внепеченочном и внутрипеченочном холестазе. +
Внепеченочный холестаз развивается при механической обструкции магистральных внепеченочных или внутрипеченочных протоков. Наиболее частой причиной внепеченочного холестаза являются камни общего желчного протока
Внутрипеченочный холестаз развивается при отсутствии обструкции магистральных желчных протоков и является следствием нарушения метаболизма желчных кислот при таких заболеваниях, как гепатит, первичный билиарный цирроз.
Дифференциальная диагностика холестаза. Обструктивный холестаз: Внепеченочная обструкция • Холелитиаз • Холангиокарцинома • Сдавление желчных путей (лимфатические узлы, опухоли поджелудочной железы) • Холангит, перихолангит,• Панкреатит, кисты поджелудочной железы • Паразитарные инфекции • Кисты общего желчного протока •
Внутрипеченочная обструкция • Внутрипеченочные опухоли или метастазы • Гепатолитиаз
Необструктивный холестаз Первичные холестатические поражения • Вирусные гепатиты • Лекарственные гепатиты Вторичные холестатические поражения • Первичный билиарный цирроз • Другие формы цирроза
Симптоматическое лечение холестаза, в особенности внепеченочного, заключается в ускорении выведения больших количеств билирубина из организма, уменьшении симптомов интоксикации и снижении кожного зуда. Как правило, в зависимости от выраженности симптоматики используется пероральная или инфузионная детоксикационная терапия
Препаратом выбора для неспецифического лечения больных с холестазом может являться урсодезоксихолевая кислота (УДХК
39. ГЭРБ. Стандарты диагностики. Тактика лечения больных в зависимости от тяжести эзофагита.+
Диагноз ГЭРБ устанавливается на основании: 1) анамнестических данных (характерные жалобы, выявление ГЭРБ прежде); 2) инструментального обследования (обнаружение рефлюкс-эзофагита при эндоскопическом исследовании пищевода, выявление патологического желудочно-пищеводного рефлюкса при рН- метрии и рН-импедансометрии).
Лечение. Всем пациентам с ГЭРБ рекомендуется изменение образа жизни (снижение массы тела при ее избытке, прекращение курения, избегание ситуаций, повышающих внутрибрюшное давление) и диетотерапия
Антациды и алгинаты могут применяться эффективны в быстром устранении симптомов Антацидные средства — алюминия фосфат 2,08 г, комбинированные препараты — магалдрат 400 или 800 мг и симетикон 20 или 40 мг, алюминия гидроксид 400 мг и магния гидроксид 400 мг применяют в лечении умеренно выраженных и нечасто возникающих симптомов, особенно тех, которые связаны с несоблюдением рекомендованного образа жизни
Эзофагопротекторы — новая фармакологическая группа, представителем которой является биоадгезивная формула на основе гиалуроновой кислоты и хондроитина сульфата для защиты слизистой оболочки
Прокинетики. Возможности применения прокинетиков при лечении ГЭРБ обусловливаются их способностью влиять на важные звенья патогенеза заболевания. Они способствуют восстановлению нормального физиологического состояния пищевода, уменьшая количество ПРНПС, улучшая пищеводный клиренс за счет стимуляции двигательной функции нижележащих отделов пищеварительного тракта
Ингибиторы протонной помпы (ИПП) — это препараты, подавляющие активность фермента Н+, К+-АТФазы, находящегося на апикальной мембране париетальной клетки и осуществляющего последний этап синтеза соляной кислоты. На сегодняшний день ИПП считаются наиболее эффективными препаратами для лечения ГЭРБ.
40. Функциональные билиарные расстройства. Стандарты диагностики и лечения.
Дисфункции билиарного тракта, в зависимости от вызвавшей их причины, разделяют на первичные и вторичные. Первичные дисфункции желчного пузыря и сфинктера Одди (СО) Вторичные функциональные расстройства билиарного тракта либо являются следствием органической патологии билиарной системы, например, ЖКБ, либо обусловлены заболеваниями других органов пищеварения: поджелудочной железы, желудка и двенадцатиперстной кишки или кишечника.
Общими признаками функциональных расстройств желчного пузыря и сфинктера Одди
1. болевой синдром, свойственный ФРЖП и СО;
2. нормальные показатели печеночных ферментов, конъюгированного билирубина и амилазы/липазы;
3. нарушение функции желчного пузыря;
4. отсутствие камней или органических изменений в желчном пузыре.
Оптимизация образа жизни, регулярная физическая активность, диетотерапия, выявление нарушений психовегетативного статуса и их коррекция.
Медикаментозная терапия включает препараты, влияющие на моторную функцию желудочно-кишечного тракта. При нарушении моторики желчного пузыря и сфинктера Одди (спазм сфинктера пузырного протока и сфинктера Одди) показано назначение спазмолитиков. Всасывающиеся спазмолитики (тримебутин, М-холиноблокаторы, дротаверин и др.) назначаются при функциональном расстройстве ЖП.
При дисфункции желчного пузыря, обусловленного гипомоторной дискинезией, для повышения сократительной функции применяют прокинетики: домперидон, метоклопрамид, итоприда гидрохлорид
Для улучшения реологических свойств желчи, уменьшения в желчи количества микролитов, предупреждения камнеобразования и возможного растворения имеющихся мелких конкрементов применяется урсодезоксихолевая кислота.
41. Язвенная болезнь желудка и дпк. Базисная терапия. Показания к эрадикации Helicobacter pylori. Современные схемы.
Всем пациентам с ЯБ с целью ускорения заживления язв рекомендуется диетотерапия
Пациентам с обострением ЯБ с целью достижения заживления язв рекомендуется проведение антисекреторной терапии ингибиторами протонного насоса в течение 4–6 недель
При неэффективности ИПН или наличии противопоказаний к их применению пациентам с обострением ЯБ с целью достижения заживления язв рекомендуется назначение в течение 4–6 недель блокаторов Н2 -гистаминовых рецепторов (ранитидин**, фамотидин**)
Всем пациентам с ЯБ с положительными результатами тестирования на инфекцию H. рylori с целью профилактики последующих рецидивов ЯБ рекомендуется проведение эрадикационной терапии
схемой первой линии является стандартная тройная схема эрадикационной терапии, включающая в себя ИПН (в стандартной дозе 2 раза в сутки), кларитромицин** (по 500 мг 2 раза в сутки) и амоксициллин** (по 1000 мг 2 раза в сутки)
Схемы эрадикац. Терапии. 1. Назначение дважды в день повышенной дозы ИПН (удвоенной по сравнению со стандартной). 2. Увеличение продолжительности тройной терапии с ИПН и кларитромицином** до 14 дней.
3) может быть назначена классическая четырехкомпонентная схема на основе висмута трикалия дицитрата** (120 мг 4 раза в сутки) в комбинации с ИПН (в стандартной дозе 2 раза в сутки), тетрациклином (500 мг 4 раза в сутки), метронидазолом** (по 500 мг 3 раза в сутки) в течение 10–14 дней
42. Диагностические критерии и лечебная тактика при синдроме раздраженного кишечника с преобладанием запора.+
Боль в животе Больной может характеризовать боль как неопределённую, жгучую, тупую, ноющую, постоянную, кинжальную, выкручивающую. Боль локализована преимущественно в подвздошных областях, чаще слева. Обычно боль усиливается после приёма пищи, а после дефекации, отхождения газов, приёма спазмолитических препаратов выраженность ее уменьшается.синдрома при СРК считается отсутствие боли в ночные часы.
Ощущение вздутия живота Менее выражено в утренние часы, нарастает в течение дня, усиливается после приёма пищи.
Нарушения функции кишечника в виде запора возможно выделение «овечьего» кала, каловых масс в виде «карандаша», а также пробкообразного кала.
Лабораторная диагностика Диагностическим минимумом при наличии симптоматики, соответствующей СРК, является проведение общего анализа крови с определением СОЭ и уровня С-реактивного белка, общий анализ кала и тест на скрытую кровь, определение антител IgA или IgG к тканевой трансглутаминазе, общий анализ мочи
Лечение больных с СРК заключается в коррекции диеты и образа жизни, приеме фармакологических средств, применении психотерапевтических методов воздействия
Для лечения больных с СРК-З применяют слабительные средства следующих групп: слабительные средства, увеличивающие объем каловых масс (пустые оболочки семян подорожника); осмотические слабительные средства (макрогол 4000, лактулоза); слабительные средства, стимулирующие моторику кишки (бисакодил).
Слабительные средства, увеличивающие объем каловых масс прием псиллиума в дозе 10 г/сут приводил к достоверному уменьшению выраженности симптомов заболевания уже в течение 1-го месяца лечения, в то время
Осмотические слабительные средства полиэти‑ ленгликоль (ПЭГ, макрогол) и лактулоза, способствующие замедлению всасывания воды и увеличению объема кишечного содержимого
Слабительные средства, стимулирующие моторику кишкиа бисакодил
Энтерокинетики (1 мг у лиц старше 65 лет или 2 мг у лиц моложе 65 лет 1 раз в сутки
Язвенная болезнь желудка и 12-перстной кишки. Базисная терапия. Показания к эрадикации Helicobacter pylori. Современные схемы.+
Показания для эрадикационной терапии HР первой линии:
Абсолютные:
все пациенты с HР-ассоциированной язвой желудка и двенадцатиперстной кишки, вне зависимости от стадии течении болезни;
MALT-лимфома желудочно-кишечного тракта;
состояние после эндоскопической резекции ранней стадии рака желудка;
необследованная диспепсия у лиц моложе 55 лет, некупируемая 4-недельным курсом ингибиторов протонной помпы и 4-недельным курсом антацидов.
Относительные:
ГЭРБ;
НПВС-ассоциированная диспепсия;
высокий популяционный риск рака желудка;
железодефицитная анемия неясной этиологии.
Эрадикационная терапия HР 1-й линии:
Категории пациентов |
Препараты и дозы |
Пациент без аллергии к пенициллинам и не применявший ранее макролиды |
Омепразол 20 мг 2 раза в день Кларитромицин 500 мг 2 раза в день Амоксициллин 1000 мг 2 раза в день В течение 10-14 дней |
Пациент с аллергией к пенициллинам, не применявший ранее макролиды, с наличием противопоказаний к проведению квадротерапии |
Омепразол 20 мг 2 раза в день Кларитромицин 500 мг 2 раза в день Метронидазол 500 мг 2 раза в день В течение 10-14 дней |
Эрадикационная терапия H.pylori 2-й линии – квадротерапия, используется как терапия спасения при резистентном течении:
Препарат висмута 525 мг 4 раза в день
Метронидазол 250 мг 4 раза в день
Тетрациклин 500 мг 4 раза в день
Омепразол 20 мг 2 раза в день
В течение 10-14 дней
Третий вариант терапии первой линии Один из РРI в стандартной дозе в сочетании с амоксициллином по 1000 мг висмута трикалия дицитрата по 240 мг соответственно два раза в день в течение 10 дней. При отсутствии заживления язвы, по данным ЭГДС, лечение продолжить одним из РРI или висмута трикалием дицитратом еще в течение трёх недель. Антихеликобактерная терапия третьей линии Терапия проводится при отсутствии эрадикации НР после проведения терапии второй линии по следующей схеме: один из РРI в стандартной дозе, висмута трикалия дицитрат по 240 мг, фуразолидон по 200 мг (соответственно все препараты принимаются два раза в день в течение 7 дней). При выборе изложенного выше порядка использования медикаментозных схем лечения больных язвенной болезнью, ассоциируемой с НР, исходили из следующего:
• у большей части пациентов тройная антихеликобактерная терапия дает возможность добиться эрадикации НР (следовательно, уменьшить количество препаратов, что позволяет снизить вероятность появления осложнений и побочных действий у большего числа больных, а также уменьшить финансовую составляющую лечения); • фуразолидон дает больше побочных эффектов и осложнений, чем метронидазол (Маастрихтские соглашения подтвердили эффективность и целесообразность применения метронидазола в эрадикационной НР-терапии язвенной болезни).
Ревматология
1. Остеопороз. Этиология. Клинические проявления. Методы диагностики. Принципы лечения.+
Остеопороз — системное заболевание скелета, характеризующееся снижением массы кости в единице объема и нарушением микроархитектоники костной ткани, приводящим к увеличению хрупкости костей и высокому риску их переломов. Наряду с термином остеопороз используется термин остеопения, имеющий двоякий смысл. Во-первых, так обозначается любое снижение минеральной плотности кости, во-вторых, ситуация, при которой по данным костной денситометрии критерий «Т» оказывается в пределах от —1 до —2,5.
Этиология. По этиологии остеопороз может быть первичным, который подразделяется на постменопаузальный, сенильный, ювенильный, идиопатический, и вторичным, или симптоматическим, т.е. обусловленным каким-то конкретным заболеванием.
Патогенез. При остеопорозе с высоким костным обменом резорбция кости не компенсируется нормальным или повышенным костеобразованием, а при остеопорозе с низким костным обменом скорость резорбции кости нормальна или снижена, а темп костеобразования замедлен. Обе формы могут проявляться как различные стадии остеопоротического процесса у одного больного. В патогенезе постменопаузального остеопороза пусковым фактором является эстрогенная недостаточность, резко ускоряющая потери костной массы. На остеобластах имеются рецепторы эстрогенов, а дефицит последних способствует продукции остеобластами фактора, стимулирующего дифференцировку, и активность остеокластов, что обусловливает повышенную резорбцию кости. В патогенезе сенильного остеопороза наряду с дефицитом половых стероидов и кальцитонина большое значение придают отрицательному кальциевому балансу, обусловленному дефицитом витамина D и сниженной абсорбции кальция в кишечнике, что в итоге приводит к развитию вторичного гиперпаратиреоза и повышенной резорбции костной ткани, Нарушение обмена витамина D вызывается как уменьшением инсоляции вследствие снижения пребывания на улице, так и нарушением образования его активных форм из-за дефицита половых гормонов. Избыточная или недостаточная секреция большинства гормонов в любом возрасте ведет к остеопорозу (гиперпаратиреоз, тиреотоксикоз, синдром Кушинга). Избыток глюкокортикоидов подавляет костеобразование, при этом снижается всасывание кальция в кишечнике и повышается экскреция его почками, что создает отрицательный кальциевый баланс, приводит к вторичному гиперпаратиреозу и повышенной костной резорбции. Механизм развития остеопороза при гипогонадизме у женщин в репродуктивном периоде сходен с таковым при постменопаузе.
Для постменопаузального, стероидного и гипогонадного остеопороза характерны преимущественные потери трабекулярной костной ткани (переломы тел позвонков, ребер, лучевой кости в типичном месте). Преимущественное поражение кортикальной костной ткани свойственно сенильному остеопорозу, гиперпаратиреозу и тиреотоксикозу (переломы трубчатых костей, шейки бедра).
Клинические проявления
♦ Более чем в 50 % случаев протекает бессимптомно или малосимптомно и выявляется лишь при наличии переломов костей, которые могут иметь любую локализацию.
♦ Переломы проксимальных отделов бедра и дистальных отделов костей предплечья.
♦ Переломы тел позвонков, боли в спине, нарушение функции и деформация позвоночника (уменьшение роста, горб, нарушение походки).
Диагностика
Основным методом диагностики остеопороза и оценки минеральной плотности костной ткани является костная денситометрия, меньшее значение имеет традиционная рентгенография. Если критерий «Т» по данным денситометрии оказывается меньше —2,5, устанавливается диагноз остеопороза; в том случае если критерий «Т» меньше —1,0, но больше —2,5 — речь идет об остеопении. Костная денситометрия показана:
— Женщинам в постменопаузе после 65 лет независимо от наличия дополнительных факторов риска.
— Женщинам в постменопаузе моложе 65 лет при наличии дополнительных факторов риска.
— Мужчинам в возрасте 70 лет и старше.
— Взрослым с переломами при минимальной травме в анамнезе.
— Взрослым с заболеваниями и состояниями, приводящими к снижению костной массы, особенно женщинам старше 45 лет и мужчинам старше 65 лет.
— Взрослым, принимающим препараты, снижающие костную массу.
— С целью мониторинга эффективности лечения остеопороза.
Для оценки уровня костного метаболизма с целью выбора и оценки эффективности терапии остеопороза могут использоваться маркеры костной резорбции и костеобразования.
Дифференциальная диагностика
Ее целью является исключение вторичного остеопороза, при котором помимо симптоматического возможно этиотропное лечение приведшего к нему основного заболевания. Большинству пациентов с остеопорозом необходимо проведение исследований: общего и биохимического анализа крови, функции почек и печени, уровня ионизированного кальция и фосфора, ТТГ, тестостерона (только у мужчин). В зависимости отданных клинической картины проводятся другие необходимые исследования.
Лечение. При остеопорозе применяют препараты нескольких групп:
1. Бисфосфонаты (алендронат, ибандроновая кислота) существенно снижают риск переломов позвоночника, бедренной кости и костей запястья. Механизм их действия заключается в подавлении активности остеокластов, уменьшении опосредованной остеокластами резорбции костной ткани.
2. Кальцитонин лосося (миакальцик) помимо антирезорбтивной активности, связанной с воздействием на специфические рецепторы остеокластов, обладает анальгетическим эффектом и способствует уменьшению болей при переломах костей.
3. Заместительная терапия эстрогенами у женщин в постменопаузе может использоваться как для профилактики, так и для лечения остеопороза.
4. Селективные модуляторы эстрогеновых рецепторов (ралоксифсн) в одних тканях проявляют себя как агонисты эстрогенов (костная ткань), в других — как антагонисты (эндометрий, молочная железа); используются для лечения остеопороза у женщин в постменопаузе.
5. Терипаратид— N-терминальный фрагмент паратгормона человека, усиливает костеобразование за счет влияния на активность остеобластов.
6. Препараты кальция (преимущественно карбонат), витамина D и активные метаболиты витамина D (а-кальцидиол, кальцитриол) используются в комбинации с перечисленными выше препаратами в комплексной терапии остеопороза.
2. Врачебная тактика и дифференциальный диагноз суставного синдрома при ревматоидном артрите. +
Суставной синдром - характерный симптомокомплекс, проявляющийся болями в суставах, их дефигурацией и деформацией, ограничением движений в суставах, изменениями сухожильно-связочного аппарата суставов окружающих мышц. В основе патогенеза суставного синдрома лежат воспалительные или дистрофические изменения в суставах и околосвязочном аппарате, в легких случаях синдром проявляется только артралгиями.
Суставной синдром может быть проявлением преимущественного поражения самих суставов, отражением системных поражений организма при диффузных заболеваниях соединительной ткани, системных васкулитах. Суставной синдром - наиболее яркое проявление большой группы т.н. ревматических заболеваний (см. общую схему)
Признаки поражения суставов
Боли в суставах, дефигурация и деформация суставов, гипертермия кожи над пораженными суставами, ограничение движений в суставах, изменения в сухожильно-связочном аппарате суставов, изменения мышц
Признаки полисистемного поражения
Поражения кожи и слизистых - эритема в виде бабочки, кольцевидная эритема, многоформная экссудативная эритема, узловатая эритема, пурпура васкулитного типа, крапивница, узелки (ревматические, ревматоидные, геберденовские), подагрические тофусы, ксантомы
Поражения глаз - ирит, иридоциклит, увеит, конъюнктивит, эписклерит, склерит
Поражения сердца и сосудов - миокардит, эндокардит, перикардит, васкулиты
Поражения легких - пневмонит, плеврит
Поражения мочевыделительной системы - гломерулонефрит, гломерулит, амилоидоз, «истинная склеродермическая почка», уретрит, простатит
Поражения желудочно-кишечного тракта - дисфагия, абдоминальные кризы, гепатолиенальный синдром
Клиника суставного синдрома. В клинической картине суставного синдрома можно выделить субъективные и объективные признаки.
Боли в суставах являются постоянным симптомом при ревматических заболеваниях. В возникновении болей, их инициации играют роль механические факторы - перегрузка сустава, растяжение сухожильно-связочного аппарата, раздражение синовиальной оболочки; микроциркуляторные расстройства; обменные нарушения в костном скелете, развитие в суставе воспалительных и дегенеративных изменений. Вследствие этих процессов в тканях суставов накапливаются вещества-алгетики (тканевые протеазы, кинины, простагландины, гистамин, серотонин), которые раздражают болевые рецепторы и дают начало дуге болевого рефлекса. Ноцицепторы находятся в адвентиции микрососудов, фиброзной капсуле суставов, периосте костей, связках и сухожилиях. Их нет в синовиальной оболочке, хряще и менисках. Обязательно выясняются параметры суставных болей - точная локализация, характер, длительность, интенсивность, время появления в течение суток.
Второй субъективный симптом - ограничение движений в суставах. Степень выраженности этого признака обычно прямо пропорциональна тяжести органических и функциональных изменений в суставах.
К объективным признакам поражения суставов относят дефигурацию и деформацию суставов, припухлость, покраснение кожи над суставами, нарушение функции суставов. Дефигурация сустава (или суставов) - это изменение формы сустава за счет воспалительного отека синовиальной оболочки и периартикулярных тканей, выпота в полость сустава, гипертрофии синовиальной оболочки и фиброзно-склеротических изменений околосуставных тканей. Деформация суставов - это стойкое изменение формы суставов за счет костных изменений, развития анкилозов, подвывихов. Припухлость в области сустава может быть при обеих указанных состояниях. Покраснение кожи над пораженными суставами обусловлено локальным повышением кожной температуры и свидетельствует об активном воспалительном процессе в суставе.
При осмотре и пальпации пораженных суставов ориентировочно устанавливается ограничение объема движений, свойственных данному суставу. Оценивается ограничение активных и пассивных движений в суставах.
Если поражен один сустав, говорят о моноартрите; два-три сустава - олигоартрите, более трех - полиартрите.
Имеются особенности суставного синдрома при основных нозологических формах суставной патологии.
Ревматоидный артрит. Утренняя скованность в суставах более 30 минут. Полиартрит. Реже олиго- и моноартрит. Поражаются мелкие суставы кистей и стоп - пястно-фаланговые, проксимальные межфаланговые. В период обострения и по мере прогрессирования заболевания выраженная деформация суставов, нарушение их функции. Как правило, отсутствие связи с инфекцией. Ревматический полиартрит. Суставные проявления появляются через 2,5 - 3 недели после ангины, фарингита. Поражаются крупные суставы, характерны летучесть, симметричность поражения, поразительно быстрый эффект аспирина и других НПВС. Нет суставной инвалидизации.
Реактивный артрит. Прослеживается четкая связь с инфекцией - урогенной, энтерогенной, тонзилогенной. Поражение суставов по типу моно- или олигоартрита, часто признаки сакроилеита. Выраженной деформации суставов нет. Отмечается выраженной благоприятный эффект антибиотиков и НПВС.
Синдром Рейтера. Триада признаков - поли-олигоартрит, конъюнктивит, уретрит.
Анкилозирующий спондилоартрит. Прогрессирующее поражение позвоночника - спондилоартрит, могут поражаться крупные суставы, но без их суставной инвалидизации.
Подагра. Рецидивирующие артриты, особенно поражение 1 плюснефалангового сустава
Инфекционные специфические артриты. В анамнезе указания на туберкулез, гонорею. Преимущественно асимметричные моно- олигоартриты. Псориаз. Поражение межфаланговых в основном дистальных суставов кистей (пальцы в виде сардельки или редиски). Есть признаки сакроилеита
Деформирующий остеоартроз. Поражаются в основном крупные суставы, боли усиливаются при нагрузке. Может быть выраженная деформация суставов, вторично - признаки синовита.
При констатации признаков суставного синдрома в качестве первичных диагностическх гипотез (ПДГ) могут быть выдвинуты предположения о трех группах заболеваний: 1) собственно заболевания суставов, когда в клинической картине имеются признаки только суставного синдрома; 2) диффузные заболевания соединительной ткани, когда наряду с суставными проявлениями имеются признаки полисистемного поражения; 3) системные васкулиты.
Дополнительные методы исследования методы исследования при суставном синдроме включают функциональные методы - гониометрию, индикаторные методы, визуализирующие и гистоморфологические методы.
Гониометрия - это объективная оценка двигательной функции суставов, которая производится с помощью измерения углов тех или иных направлений движений в данном суставе. Проводится специальными приборами - гониометрами. Гониометр представляет собой градуированный полукруг, к основанию которого прикреплены подвижная и неподвижная бранши. Их устанавливают по проекции осей конечностей, и при движении бранш синхронно с движениями в суставах образуются углы, величина которых измеряется в градусах.
К индикаторным можно отнести методы исследования активности воспалительного процесса, нарушений иммунного статуса, объективной оценки болевого синдрома, исследование синовиальной жидкости.
В большинстве случаев при ревматических болезнях имеет место воспалительный процесс. В этой связи методы оценки его активности широко применяются в ревматологии. Количество их достаточно велико, но существует чаще всего применяемый комплекс исследований активности воспалительного процесса. Это определение лейкоцитоза, лейкоцитарной формулы и СОЭ в клиническом анализе крови. При активном воспалении отмечается умеренный лейкоцитоз, нейтрофилез, сдвиг лейкоцитарной формулы влево, ускорение СОЭ. “Показатели острой фазы” или “острофазовые показатели” - С-реактивный белок, фибриноген, сиаловые кислоты, протеинограмма. У больных с активным воспалительным процессом в крови обнаруживается С-реактивный белок (в норме он отсутствует), повышается свыше 0,4 г/л содержание фибиногена, свыше 200 усл.ед. содержание сиаловых кислот, отмечается диспротеинемия, гипер -1- и 2, -глобулинемия. Довольно информативно определение в крови серомукоида.
Для клинической оценки иммунитета при ревматических заболеваниях необходимо исследование четырех главных компонентов иммунной системы, принимающих участие в защите организма и патогенезе аутоиммунных заболеваний: гуморальный иммунитет (В-клетки); клеточно-опосредованный иммунитет (Т-клетки, моноциты); фагоцитарные клетки ретикуло-эндотелиальной системы (нейтрофилы, макрофаги); комплемент.
Боли доминируют в клинике большинства заболеваний опорно-двигательного аппарата. Количественная оценка болей и выраженность противоболевого эффекта лечения чаще всего проводится клинически, а также с помощью визуально-аналоговых или вербально-аналоговых шкал. Однако, эти шкалы измеряют боль только по одному параметру - интенсивности. Боль же, согласно современным представлениям, относится к категории сложных восприятий, охватывающих разнообразные качества. Для ее оценки целесообразно использовать клинико-психологические методики, в частности, отечественный вариант Мак-Гиловского болевого опросника, разработанного Мелзак в университете Мак-Гила. Опросник составлен в виде анкеты, на вопросы которой отвечает больной. Состоит из трех шкал: сенсорной, аффективной и эвалюативной (оценочной). Сенсорная шкала, в свою очередь, включает 13 подшкал (1-13), в каждой из которых имеются слова-определители - дескрипторы. Ими больной характеризует свою боль. При этом каждому дескриптору в шкале присвоен свой ранг, и чем он выше, тем “выразительней” в плане соответствия интенсивности боли. Аффективная шкала состоит из 6 подшкал (14-19), построенных по такому же принципу. Здесь больной отвечает на вопрос, какие чувства и переживания вызывает у него боль. Эвалюативная шкала состоит из одной подшкалы (20). Больной оценивает свою от “слабой” до “ сильнейшей”. После заполнения анкеты рассчитывается ряд показателей, из которых главный - индекс рангов общий (ИРО). Составляется также графический болевой профиль больного. Опросник используется также для оценки противоболевого эффекта проводимой терапии. Есть возможность с его помощью выделять градации противоболевого эффекта, что клинически иногда бывает оценить очень трудно.
Исследование синовиальной жидкости позволяет дифференцировать дистрофические и воспалительные заболевания суставов, выделять в ряде случаев определенные нозологические формы. Синовиальная жидкость получается путем пункции сустава. Она оценивается по ряду параметров: цвет, вязкость, прозрачность, характер муцинового сгустка и цитологический состав.
Рентгенологическое исследование суставов - один из наиболее информативных методов визуализирующего исследования у больных суставной патологией. При этом надо учитывать стадии развития процесса. Наиболее важные и типичные рентгенологические изменения при суставных синдромах представлены в таблице.
Рентгенологические признаки Заболевание
Краевые костные эрозии эпифизов. Ревматоидный артрит
Остеолиз дистальных фаланг пальцев. Псориатическая артропатия
Подхрящевой остеосклероз,.остеофиты. Деформирующий артроз
Деструктивный артроз,.“пробойники” Подагра
Сакроилеит, кальцификация, связок позвоночника Болезнь Бехтерева
3. Врачебная тактика и дифференциальный диагноз при остеоартрозе с явлениями вторичного синовита.+
Остеоартроз (ОА) (в зарубежной литературе называется остеоартрит) – хроническое заболевание суставов, в основе которого лежит дегенеративно-дистрофическое поражение суставного хряща. Вторично поражаются субхондральная кость, синовиальная оболочка (синовит), связки, капсула, околосуставные мышцы. Таким образом, при остеоартрозе первичным является дистрофия хряща, вторично развивается умеренный артрит (синовит) – воспаление сустава. ОА является наиболее частой причиной эндопротезирования тазобедренных и коленных суставов.
Диагноз ДОА в большинстве случаев нетруден и основывается на клинико-рентгенологических признаках болезни (табл. 2). К ним отнесены:
1) боли механического типа - при нагрузке, усиливающиеся к вечеру, исчезающие в покое;
2) жалобы на периодическое заклинивание сустава с формированием его блокады;
3) наличие в анамнезе механической перегрузки сустава;
4) медленное незаметное начало болезни, часто без видимых причин;
5) преимущественное поражение наиболее «нагруженных» суставов - нижних конечностей и дистальных межфаланговых;
6) стойкая деформация суставов, обусловленная изменениями кости, но не мягких тканей;
7) сравнительно небольшое ограничение подвижности суставов, за исключением случаев коксартроза;
+8) характерные рентгенологические признаки, которые включают: сужение суставной щели, субхондральный остеосклероз, кисты, выраженный краевой остеофитоз, деформация суставных поверхностей;
9) отсутствие изменений показателей анализа крови;
10) синовиальная жидкость невоспалительного типа с хорошей вязкостью и небольшим числом клеток - до 5000 в 1 мм3.
Дифференциальный диагноз проводится, в первую очередь, с ревматоидным артритом, особенно в случаях множественного поражения суставов, в том числе, при наличии реактивных синовитов и небольшого увеличения СОЭ. Следует помнить, что и воспалительные и метаболические артриты могут служить причиной развития вторичного ДОА с характерными клиническими симптомами.
Лечение ДОА должно решать следующие задачи: 1) предотвращать прогрессирование дегенеративного процесса в суставном хряще; 2) уменьшать боли и явления реактивного синовита; 3) улучшать функции пораженных суставов.
Немедикаментозная терапия весьма разнообразна и включает мероприятия по коррекции биомеханики тела. Следует подчеркнуть, что самое обоснованное и эффективное лечение не принесет успеха, если не будет соблюден двигательный режим больного, а именно, разгрузка пораженных суставов до минимума движений.
При нарушениях осанки и движений помогают гимнастика или специальные ортопедические приспособления, например ношение поддерживающего пояса или корсета при поясничном лордозе, использование шин или ортезов для профилактики деформации при ДОА I пястно-фалангового сустава. При ДОА суставов нижних конечностей нельзя подолгу стоять, сидеть на корточках, стоять на коленях. При ожирении необходимо приложить максимум усилий для снижения массы тела.
ЛФК показана только при отсутствии явлений реактивного синовита, должна проводиться в облегченном положении сустава, вне его статических нагрузок с постепенным увеличением объема движений и сочетаться с массажем региональных мышц.
Базисная терапия, направленная на предотвращение прогрессирования дегенеративного процесса, основывается на способности пораженного хряща восстанавливать содержание протеогликанов при введении препаратов, содержащих мукополисахариды. Именно на этом основано действие препаратов-хондропротекторов (румалон, артепарон, хондролон, хондроитин сульфат, глюкозамин сульфат, алфлутоп, хондроксин и др.). Они обладают свойством стимулировать восстановительные процессы в поврежденном хряще, увеличивать синтез гликозаминогликанов и гиалуроновой кислоты, улучшают вязкость синовиальной жидкости. Препараты предназначены для курсового применения 1-2 раза в год.
Для стимуляции обменных процессов в хряще традиционно применяют биостимуляторы - экстракт алоэ, стекловидное тело, АТФ, однако их эффективность невелика и не доказана. Показанием для назначения этих препаратов являются начальные стадии ДОА, когда еще возможно активировать восстановительные процессы в хряще.
Для улучшения общего и местного кровообращения применяют вазоактивные препараты, такие как но-шпа, препараты никотиновой кислоты. С этой же целью назначается физиотерапевтическое лечение - серные, радоновые, сероводородные ванны.
Назначение разнообразных нестероидных противовоспалительных препаратов (ацеклофенак, диклофенак, ибупрофен, напросин, мелоксикам, нимесулид, целекоксиб и др.) способствует уменьшению болевых ощущений и явлений реактивного синовита.
Особенно хороший противовоспалительный эффект оказывает внутрисуставное назначение лекарственных препаратов (кроме тазобедренного сустава). Это могут быть растворимые формы глюкокортикоидов (гидрокортизон, кеналог), а также ингибиторы лизосомальных ферментов (трасилол, контрикал, гордокс). Последние оказывают противовоспалительный эффект за счет торможения выброса кининов и подавления расщепления мукополисахаридов. Показан также эффект от внутрисуставного введения поливинилпирролидона, который не только оказывает противовоспалительное действие, но и выполняет роль заместителя синовиальной жидкости, что особенно ценно на развернутых этапах болезни.
4. Дифференциальная диагностика и врачебная тактика при метаболических и дегенеративных заболеваниях суставов (диабетическая артропатия, подагра, первичный остеоартроз).+
Остеоартроз.
Остеоартроз (деформирующий остеоартроз) - локальное дегенеративное заболевание суставов с разрушением хряща (его исчезновением), изменением суставных поверхностей и вторичной реакцией костной ткани и отсутствием системных изменений. При остеоартрозе развивается субхондральный остеосклероз, краевые разрастания кости - остеофиты. Заболевание развивается в среднем и пожилом возрасте, соотношение женщин и мужчин 3:1.
Различают остеортрозы первичные (генуинные) и вторичные (на фоне поврежденных травмой, при аномалии развития суставов или на фоне других артритов). Первичный остеоартроз протекает: в виде локальной формы (олиго-моноартрит): преимущественно поражаются кисти, первый плюснефаланговый сустав, коленный и тазобедренный сустав (отсутствует симметричность поражения), редко поражается лучезапястный сустав или в виде генерализованной формы (полиостеоартроз) с вовлечением в процесс 4-х и более суставов.
Диагностические критерии остеоартроза:
Боль в суставах при движении и физической нагрузке.
Изменение формы суставов вследствие костных разрастаний.
Ограничение функции сустава из-за боли и костных разрастаний.
Подагрический артрит.
Подагра - нарушения пуринового обмена. Характерны: повышение содержания мочевой кислоты в крови (гиперурикемия) и отложения уратов в суставах и/или околосуставных тканях. Гиперурикемия - основной фактор, предрасполагающий к образованию кристаллов в организме (нормальные показатели мочевой кислоты в крови: 420 мкмоль/л - для мужчин, 360 мкмоль/л - для женщин). Основные причины повышенного образования мочевой кислоты (конечного продукта распада пуринов): дефект ферментной системы синтеза мочевой кислоты (наследственный), повышенный распад клеток (алкоголизм, заболевания крови, хронический гемолиз, протиоопухолевая терапия), при замедлении выведения мочевой кислоты (хроническая почечная недостаточность, свинцовая нефропатия, голодание). Неблагоприятные факторы нарушения пуринового обмена: ожирение, сахарный диабет, артериальная гипертония, гиперлипидемия, атеросклероз. Главными органами-мишенями являются суставы и почки. Заболеваемость подагрой составляет от 0,1 до 2 % (в старших возрастных группах достигает 4-6 %). Соотношение мужчин и женщин составляет 9:1 (даже 20:1).
Диагностические критерии подагры:+
Наличие в анамнезе и наблюдение повторных атак острого артрита.
Развитие максимума воспаления в течение 1-х суток.
Моноартикулярный характер артрита.
Гиперемия кожи над воспаленным суставом.
Болезненность и припухлость I плюснефарангового сустава.
Одностороннее поражение I плюснефарангового сустава.
Одностороннее поражение 2-х плюсневых суставов.
Диабетическая артропатия — боли в суставах, «хруст», ограничение подвижности, уменьшение количества синовиальной жидкости и повышение её вязкости.Идет чаще как осложнение Диабета. Все, что нашел.
5. Диагностика и лечение лекарственной болезни. Анафилактический шок.
ЛБ – это своеобразная, стойкая неспецифическая реакция организма, возникающая при применении терапевтических или разрешающих (малых) доз медикаментов и проявляющаяся разнообразными клиническими синдромами.
Анафилактический шок – это вид лекарственной аллергии немедленного типа, возникшей на повторное введении медикамента в организм больного.
Лекарственный анафилактический шок возникает через 3-30 мин после введения лекарственного препарата. Клинические признаки разнообразны. В зависимости от тяжести различают 3 степени анафилактического шока. Тяжесть шока обусловлена степенью нарушения кровообращения и функции внешнего дыхания. При легком течении анафилактического шока наблюдается короткий продромальный период 5-10 мин, который характеризуется появлением зуда, уртикальной сыпи, гиперемии кожи, отека Квинке, отека гортани с осиплостью голоса вплоть до афонии. Больные успевают пожаловаться на боль в грудной клетке, головокружение, нехватку воздуха, ухудшение зрения, онемение пальцев, языка, губ, болей в животе, поясничной области.
Объективно: бледность кожных покровов, цианоз, пульс нитевидный, бронхоспазм с дистанционными свистящими хрипами, рвота, жидкий стул. АД 60\30 - 50\0 мм рт ст тоны сердца едва прослушиваются, экстрасистолы.
Рекомендуется проведение следующих мероприятий при анафилактическом шоке.
п\к ввести 0,5 - 1 мл 0.1% р-ра адреналина
уложить больного лучше в положение Тренделенбурга для предупреждения аспирации рвотных масс
в\в ввести 10.0 - 10% р-ра Са хлор или 10%-10.0 глюконата Са в\к
в\в-струйно, затем капельно 300-500 мл 5% р-ра глюкозы или физ р-ра + 0.5-1 0.1% р-ра адреналина или мезатона 1%-1.0 с глюкокортикоидами (гидрокартизон 100-250 мг, преднизолон 50-100 мг). Гормональная терапия продолжается 3-5 дней после снятия острых явлений анафилактического шока.
при бронхоспазме – эуфиллин 2.4% - 10 , вазоспастическая новокаиновая блокада
при отеке гортани – трахеостомия, увлажненный кислород
антигистаминные средства (супрастин 2%-2.0, тавегил 0.1%-1.0, димедрол 1%-1.0)
сердечные гликозиды
при анафилактическом шоке пенициллиновой этиологии после принятия послешоковых мер – 800 тыс ЕД (или 1 млн) пеницилменазы, которая разрушает пенициллин , через 6-8 часов введение пенициллиназы повторяется
реанимационные мероприятия (искусственная вентиляция легких, закрытый массаж сердца при остановке дыхания и сердечной деятельности).
6. Дифференциальный диагноз и врачебная тактика суставного синдрома при подагре+
Дифференциальный диагноз суставного синдрома
Суставной синдром - характерный симптомокомплекс, проявляющийся болями в суставах, их дефигурацией и деформацией, ограничением движений в суставах, изменениями сухожильно-связочного аппарата суставов окружающих мышц. В основе патогенеза суставного синдрома лежат воспалительные или дистрофические изменения в суставах и околосвязочном аппарате, в легких случаях синдром проявляется только артралгиями.
+Суставной синдром может быть проявлением преимущественного поражения самих суставов, отражением системных поражений организма при диффузных заболеваниях соединительной ткани, системных васкулитах. Суставной синдром - наиболее яркое проявление большой группы т.н. ревматических заболеваний.
Имеются особенности суставного синдрома при основных нозологических формах суставной патологии.
Ревматоидный артрит. Утренняя скованность в суставах более 30 минут. Полиартрит. Реже олиго- и моноартрит. Поражаются мелкие суставы кистей и стоп - пястно-фаланговые, проксимальные межфаланговые. В период обострения и по мере прогрессирования заболевания выраженная деформация суставов, нарушение их функции. Как правило, отсутствие связи с инфекцией. Ревматический полиартрит. Суставные проявления появляются через 2,5 - 3 недели после ангины, фарингита. Поражаются крупные суставы, характерны летучесть, симметричность поражения, поразительно быстрый эффект аспирина и других НПВС. Нет суставной инвалидизации.
Реактивный артрит. Прослеживается четкая связь с инфекцией - урогенной, энтерогенной, тонзилогенной. Поражение суставов по типу моно- или олигоартрита, часто признаки сакроилеита. Выраженной деформации суставов нет. Отмечается выраженной благоприятный эффект антибиотиков и НПВС.
Рентгенологическое исследование суставов. Деструктивный артроз,.“пробойники”при падагре
Краевые костные эрозии эпифизов. Ревматоидный артрит
Остеолиз дистальных фаланг пальцев. Псориатическая артропатия
Подхрящевой остеосклероз,.остеофиты. Деформирующий артроз
Подагра
Подагра рассматривается как системное, ферменто-метаболическое заболевание, обусловленное нарушением пуринового обмена, развитием гиперурикемии, гиперурикозурии. Проявляется поражением суставов и внесуставными признаками.
Можно выделить две основные формы суставных проявлений подагры - типичную и атипичную. При типичной форме первым поражается I плюснефаланговый сустав одной из ног. Начало острое, внезапное. Характерны очень сильные боли в суставе, его припухлость, гиперемия и практически полное нарушение функции. Повышается температура, иногда до очень высоких цифр, резко ухудшается общее состояние. Через 5-6 дней боли стихают, уменьшаются местные проявления артрита, коже вокруг сустава шелушится. В последующем острые приступы повторяются, но уже захватывается все большее количество суставов конечностей.
Атипичные формы в целом встречаются достаточно часто. Может быть ревматоидноподобная форма, когда отмечается затяжное течение приступа и процесс сразу локализуется в мелких суставах кистей или 1-2 крупных суставах. Подагра может начинаться в виде моноартрита одного из крупных суставов, характерно при этом острое начало, выраженные боли и местные проявления - припухлость, гиперемия сустава, нарушение его функции.
Диагностические критерии. Приводим диагностические критерии подагры
1. Повышение содержания мочевой кислоты в сыворотке крови более 0,42 ммоль/л у мужчин и 0,36 ммоль/л у женщин.
2. Тофусы.
3. Кристаллы мочевой кислоты в синовиальной жидкости или в тканях, выявленные химически или морфологически.
4. Острые приступы артрита, возникающие внезапно, с полной клинической ремиссией в течение 1-2 недель.
Диагноз подагры устанавливается при наличии двух критериев.
Лечение подагры должно проводиться с учетом:
А) специфических факторов риска (уровень мочевой кислоты в крови, количество предыдущих атак, наличие R-логических изменений);
Б) клинической фазы подагры (острая атака/рецидивирующие атаки, хроническая тофусная подагра, подагра вне обострения);
В) общих факторов риска (возраст, пол, ожирение, употребление алкоголя, наличие коморбидных состояний, взаимодействие принимаемых лекарственных препаратов).
2. Модификация образа жизни, снижение веса, соблюдение диеты, исключение употребления алкоголя (особенно пива), информированность пациента о его заболевании.
3. Неотъемлемой частью терапии подагры является коррекция таких значительных факторов риска, как гиперлипидемия, артериальная гипертензия, гипергликемия, ожирение, курение.
Медикаментозное лечение
Нестероидные противовоспалительные препараты
Кетопрофен 100-400 мг/сут в 3-4 приема. (Неселективный НПВС)
Мелоксикам 7,5-15 мг/сут в 1 прием. (Селективный НПВС)\
Ингибиторы протонной помпы (КОНТРОЛОК (пантопрозол) 20 мг - 1 раз в сутки.)
Аллопуринол применяется длительно, начиная с низких доз (100 мг/сут), с постепенной эскалацией дозы на 100 мг каждые 2-4 недели (если это необходимо). Для пациентов с поражением почек доза аллопуринола должна быть ниже.
В качестве профилактики подагрических атак в первые месяцы титрации дозы урикоингибитора применяется колхицин в дозе 0,5-1 мг/сут и/или НПВП+ингибиторы протонной помпы
7. Системная склеродермия. Критерии постановки диагноза. Принципы лечения.+
Системная склеродермия (СС) или системный склероз - диффузное заболевание соединительной ткани с фиброзно-склеротическими изменениями кожи и внутренних органов, васкулитом мелких сосудов в форме облитерирующего эндартериита.
Клинические критерии Американской ревматологической ассоциации для распознавания системной склеродермии:
«Большие» критерии:
Проксимальная склеродерма – двустороннее, симметричное утолщение, уплотнение, индурация, склероз дермы пальцев, кожи конечностей проксимально от пястно-фаланговых и плюсне-фаланговых суставов, вовлечение в патологический процесс кожных покровов лица, шеи, грудной клетки, живота.
«Малые» критерии:
Склеродактилия – индурация, склероз, остеолиз концевых фаланг, деформация пальцев кистей рук;
Рубцы, дефекты тканей на подушечках пальцев кистей рук;
Базальный легочный фиброз с двух сторон.
Для диагноза СС у больного должны присутствовать либо «большой», либо, по меньшей мере, два «малых» критерия.
Тактика лечения подразумевает выполнение следующих воздействий на организм больного:
Торможение активности облитерирующего эндартериита мелких сосудов, склерозирования кожи, фиброза внутренних органов.
Симптоматическое лечение болевого (артралгии, миалгии) и других синдромов, нарушенных функций внутренних органов.
Для подавления избыточного коллагенообразования у больных с активным воспалительным процессом, подостром течении СС назначается:
D-пенициламин (купренил) перорально по 0,15-0,2 в сутки 2 недели. Затем дозировку повышают на 0,3 каждую неделю до достижения максимальной - 1,5-1,8 г/сутки. Если прием D-пенициламина сопровождается появлением кожных высыпаний, его дозу уменьшают и добавляют к лечению преднизолон – 10-15 мг/сутки внутрь. Появление на фоне такого лечения нарастающей протеинурии является основанием для полной отмены D-пенициламина.
Для снижения активности механизмов синтеза коллагена, особенно при неэффективности или возникновении противопоказаний для D-пенициламина, можно применить:
колхицин – 0,5 мг/сутки (3,5 мг в неделю) с постепенным повышением дозы до 1-1,5 мг/сутки (около 10 мг в неделю). Препарат можно принимать в течение полутора-четырех лет подряд.
При диффузной форме СС с выраженными и тяжелыми системными проявлениями целесообразно применить иммуносупрессивные дозы глюкокортикоидов и цитостатиков.
преднизолон перорально по 20-30 мг/сутки до достижения клинического эффекта. Затем дозировку препарата медленно уменьшают до поддерживающей – 5-7,5 мг/сутки, которую рекомендуют принимать в течение 1 года.
При отсутствии эффекта, возникновении побочных реакций на прием больших доз глюкокортикоидов, используют цитостатики:
Азатиоприн перорально 150-200 мг/сутки в сочетании с пероральным приемом 15-20 мг/сутки преднизолона в течение 2-3 месяцев.
При хроническом течении СС с преимущественно кожными проявлениями, минимальной активности фиброзирующего процесса, следует назначать аминохинолиновые препараты:
Плаквенил 0,2 – 1-2 таблетки в день в течение 6-12 месяцев.
Делагил 0,25 – 1-2 таблетки в день в течение 6-12 месяцев.
Симптоматические средства предназначены в первую очередь для компенсации вазоспастической реактивности, лечения синдрома Рейно, других сосудистых нарушений. С этой целью применяются блокаторы кальциевых каналов, ингибиторы АПФ, антиагреганты:
Нифедипин – до 100 мг/сутки.
Верапапил - до 200-240 мг/сутки.
Каптоприл – до 100-150 мг/сутк
8. Современные принципы базисной терапии ревматоидного артрита
Общие принципы Т2Т сформулированы следующим образом.+ А. Лечение ревматоидного артрита следует проводить на основании совместного решения пациента и врача-ревматолога.
B. Основная цель при лечении больного ревматоидным артритом – обеспечить максимально продолжительное сохранение высокого качества жизни, связанного с состоянием здоровья, путем контроля над симптоматикой, предотвращения структурного поражения суставов, нормализации функции и социальных возможностей пациента. C. Подавление воспаления – важнейший способ достижения этой цели. D. Лечение до достижения цели с помощью оценки активности заболевания и соответствующего подбора терапии способствует оптимизации исходов при РА.
Целью лечения является достижение стойкой клинической ремиссии или (альтернативная цель) как минимум стойко низкой активности болезни, что обеспечивает стабилизацию функциональных возможностей пациента, сохранение качества жизни и трудоспособности. Современная стратегия лечения РА строится по принципам «Лечения до достижения цели»(“ Treat to target”) и подразумевает активное назначение противовоспалительной терапии с момента установления диагноза, частый (как минимум каждые 3 мес. до достижения ремиссии, каждые 6 мес. после достижения ремиссии) и объективный (с применением количественных методов) контроль над состоянием пациента, изменение схемы лечения при отсутствии достаточного ответа на терапию вплоть до достижения целей лечения, после чего постоянное динамическое наблюдение
Основное место в лечении РА занимает медикаментозная терапия, при которой применяются следующие группы лекарственных средств: нестероидные противовоспалительные
препараты (НПВП), глюкокортикоиды (ГК) и базисные противовоспалительные препараты (БПВП)
9. Митральные пороки ревматической и неревматической этиологии. Вопросы клинической и инструментальной диагностики в практике врача-терапевта. Принципы организации лечения+
Митральный стеноз: Ревматический I05.0 Неревматический (с уточнением этиологии) Митральная недостаточность: Ревматическая Неревматическая (с уточнением этиологии)
Комбинированный ревматический митральный порок (ревматический митральный стеноз с недостаточностью):
С преобладанием стеноза
С преобладанием недостаточности
Без явного преобладания
Пролапс митрального клапана I34.1
Аортальный стеноз:
Ревматический
Неревматический (с уточнением этиологии)
Аортальная недостаточность: Ревматическая I06.1 Неревматическая I35.1 (с уточнением этиологии)
Комбинированный аортальный порок:
Ревматический аортальный стеноз с недостаточностью I06.2
Неревматический аортальный (клапанный) стеноз с недостаточностью I35.2 (с уточнением этиологии)
С преобладанием стеноза
С преобладанием недостаточности
Без явного преобладания
Трикуспидальный стеноз: Ревматический I07.0 Неревматический I36.0 (с уточнением этиологии)
Трикуспидальная недостаточность: Ревматическая I07.1 Неревматическая I36.1 (с уточнением этиологии)
Комбинированный трикуспидальный порок: Ревматический трикуспидальный стеноз с недостаточностью I07.2 Неревматический трикуспидальный стеноз с недостаточностью I36.2 (с уточнением этиологии)
Клапанный стеноз ЛА I37.0 Недостаточность клапана ЛА I37.1 Комбинированный порок клапана ЛА (стеноз ЛА с недостаточностью клапана I37.2)
Сочетанные пороки сердца: Митрально-аортальный I08.0 Митрально-трикуспидальный I08.1 Аортально-трикуспидальный I08.2
Сочетанное поражение митрального, аортального и трехстворчатого клапанов I08.3
ЭхоКГ является стандартным методом диагностики для оценки структуры и функции клапана.
На ЭКГ по мере прогрессирования порока появляются признаки перегрузки левого предсердия (P mitrale), гипертрофии ПЖ: увеличенная амплитуда зубцов комплекса QRS в сочетании с измененной конечной частью желудочкового комплекса (уплощение, инверсия зубца Т, снижение сегмента ST) в соответствующих отведениях. Часто регистрируют нарушения ритма сердца (фибрилляция, трепетание предсердий). На рентгенограмме определяется увеличение левого предсердия и ПЖ, кальцификация митрального клапана, перераспределение легочного сосудистого кровотока к верхним отделам легких, расширение ЛА.
Медикаментозная терапия направлена на лечение и предотвращение осложнений. Необходимо профилактическое назначение антибиотиков перед стоматологическими и другими вмешательствами для снижения риска развития инфекционного эндокардита. У пациентов молодого возраста с острой ревматической лихорадкой в анамнезе высок риск развития рецидива, поэтому профилактическую антибиотикотерапию им проводят постоянно до достижения взрослого возраста. Применение диуретиков или органических нитратов пролонгированного действия позволяет временно уменьшать выраженность одышки. Блокаторы β-адренорецепторов или блокаторы кальциевых каналов, снижающие ЧСС, способны значительно повысить толерантность к физическим нагрузкам за счет удлинения диастолы и времени наполнения ЛЖ. Показанием для назначения антикоагулянтов является фибрилляция предсердий, у пациентов с синусовым ритмом они показаны в случае больших размеров левого предсердия (>50 мм), наличия спонтанного эхо-контрастирования при проведении трансэзофагеальной эхоКГ, тромбоэмболий в анамнезе и наличии тромба в левом предсердии.
10. Системная красная волчанка. Классификация, критерии активности, клиника.+
Системная красная волчанка (СКВ) - системное аутоиммунное заболевание неизвестной этиологии, характеризующееся гиперпродукцией органоспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов.
Выделяют следующие варианты течения заболевания.
• Острое течение характеризуется внезапным началом с резким повышением температуры тела (часто до фебрильных значений), быстрым поражением многих внутренних органов, включая почки, и значительной иммунологической активностью (высокие титры антиядерного фактора и АТ к ДНК).
• Подострое течение проявляется периодически возникающими обострениями заболевания, не столь выраженными как при остром течении, и развитием поражения почек в течение первого года болезни.
• Хроническое течение характеризуется длительным преобладанием одного или нескольких симптомов, таких как дискоидное поражение кожи, полиартрит, гематологические нарушения (тромбоцитопения и др.), феномен Рейно, небольшая протеинурия, эпилептиформные припадки. Особенно характерно хроническое течение при сочетании СКВ с АФС.
• Активность - выраженность потенциально обратимого иммуновоспалительного повреждения внутренних органов, определяющая характер терапии у конкретного больного. Активность следует отличать от тяжести - совокупности необратимых изменений, потенциально опасных для жизни больного.
Выделяют 3 степени активности СКВ.
При высокой активности (III степени) отмечают высокую лихорадку, выраженные изменения со стороны внутренних органов (нефрит с НС, эндомиокар- дит, перикардит с выпотом и/или экссудативный плеврит), тяжёлое поражение ЦНС, кожи (дерматит), опорно-двигательного аппарата (острый полиартрит и/или полимиозит) и другие, сопровождающиеся выраженными изменениями лабораторных показателей, в том числе значительным повышением СОЭ (более 45 мм/ч) и иммунологических показателей (повышение титров АНФ и AT к ДНК, значительное снижение общей гемолитической активности комплемента и его компонентов СЗ, С4).
Волчаночный криз констатируют у больных в критических состояниях, характеризующихся развитием функциональной недостаточности какого-либо органа на фоне чрезмерно высокой активности патологического процесса.
При умеренной активности (II степени) лихорадка обычно субфебрильная, признаки поражения различных органов выражены умеренно. У больных могут отмечать полиартралгии или полиартрит, дерматит, умеренную реакцию со стороны серозных оболочек, нефрит без НС и нарушения почечных функций, миокардит и др. СОЭ повышена в пределах 25-45 мм/ч, отмечают повышение титров АНФ, AT к ДНК, циркулирующих иммунных комплексов.
При низкой активности (I степени) общее состояние больных обычно не нарушено, лабораторные показатели изменены мало, признаки поражения внутренних органов определяют только при комплексном инструментальном исследовании. Клинически отмечают неяркие признаки кожного и суставного синдромов.
Оценка степени активности патологического процесса имеет решающее значение для определения тактики лечения больного на каждом этапе болезни.
Состояние ремиссии констатируют при отсутствии у больного клинических и лабораторных признаков активности процесса.
КЛИНИЧЕСКАЯ КАРТИНА. ОБЩИЕ ПРОЯВЛЕНИЯ
• При остром течении или при обострении СКВ, как правило, наблюдают общие симптомы заболевания (слабость, похудание, лихорадку, анорексию и др.).
ПОРАЖЕНИЕ КОЖИ
• Эритематозный дерматит локализуется на лице (фигура бабочки), шее, груди (зона "декольте"), в области крупных суставов.
• Фотосенсибилизация - повышение чувствительности кожи к действию солнечного излучения, выражающееся обычно появлением характерных для СКВ высыпаний на подвергшихся воздействию солнечного света участках.
• Алопеция. Выпадение волос может быть генерализованным или очаговым.
ПОРАЖЕНИЕ СЛИЗИСТЫХ ОБОЛОЧЕК
• Поражение слизистых оболочек представлено при СКВ хейлитом (застойной гиперемией губ с плотными сухими чешуйками, иногда - с корочками или эрозиями, с исходом в атрофию) и безболезненными эрозиями на слизистой оболочке полости рта (чаще на нёбе).
ПОРАЖЕНИЕ СУСТАВОВ И СУХОЖИЛИЙ
• Артралгии.
• Волчаночный артрит - симметричный (реже асимметричный) неэрозивный полиартрит, чаще всего локализующийся в мелких суставах кистей, лучезапястных и коленных суставах.
• Хронический волчаночный артрит (синдром Жакку), сопровождающийся развитием стойких деформаций и контрактур, напоминающих таковые при ревматоидном артрите, связан с поражением связок и сухожилий.
• Асептический некроз (омертвение участка органа или ткани) чаще плечевой или бедренной кости
ПОРАЖЕНИЕ МЫШЦ
• Поражение мышц протекает в форме миалгий и/или проксимальной мышечной слабости (как при полимиозите), реже в виде синдрома миастении.
ПОРАЖЕНИЕ ЛЁГКИХ
• Плеврит, сухой или выпотной
• Волчановный пневмонит
ПОРАЖЕНИЕ СЕРДЦА
• Перикардит
• Миокардит
• Эндокардит
ПОРАЖЕНИЕ ПОЧЕК
• Клиническая картина волчаночного нефрита крайне разнообразна. Она варьирует от персистирующей невыраженной протеинурии до быстропрогрессирующего гломерулонефрита.
ПОРАЖЕНИЕ ЖКТ
• Возможно развитие дилатации пищевода и нарушения его моторики, гастропатии (связанной с приёмом НПВП), гепатомегалии, очень редко васкулита (на фоне обострения) или тромбоза мезентериальных сосудов, острого панкреатита.
ПОРАЖЕНИЕ НЕРВНОЙ СИСТЕМЫ
• Головная боль, чаще мигренозного характера, резистентная к ненаркотическим и даже наркотическим анальгетикам; нередко сочетается с другими неврологическими и психическими нарушениями.
• Эпилептиформные припадки.
• Поражение черепных нервов (в том числе и зрительных нервов с развитием нарушений зрения).
• Острые нарушения мозгового кровообращения (в том числе и инсульты), поперечный миелит (редко
• Полиневропатии
• Органический мозговой синдром характеризуется эмоциональной лабильностью, эпизодами депрессии, нарушением памяти, слабоумием.
СИНДРОМ ШЁГРЕНА-снижение секреции слезных и слюнных желез, сопровождающиеся жжением в глазах и сухостью носоглотки
ФЕНОМЕН РЕЙНО- значительно выраженная реакция мелких кровеносных сосудов кончиков пальцев на воздействие холода или психоэмоциональное потрясение
11. Системная красная волчанка. Критерии постановки диагноза. Тактика ведения.+
Системная красная волчанка (СКВ) - системное аутоиммунное заболевание неизвестной этиологии, характеризующееся гиперпродукцией органоспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов.
ДИАГНОСТИКА- критерии Американской ревматологической ассоциации
1. Сыпь на скулах: фиксированная эритема на скуловых выступах, имеющая тенденцию к распространению к носогубной зоне.
2. Дискоидная сыпь: эритематозные приподнимающиеся бляшки с прилипающими кожными чешуйками и фолликулярными пробками; на старых очагах могут быть атрофические рубцы.
3. Фотосенсибилизация: кожная сыпь, возникающая в результате необычной реакции на солнечный свет.
4. Язвы в ротовой полости: изъязвление полости рта или носоглотки; обычно безболезненное.
5. Артрит: неэрозивный артрит, поражающий 2 или более периферических сустава, проявляющийся болезненностью, отёком и выпотом.
6. Серозит: плеврит (плевральные боли, или шум трения плевры, или наличие плеврального выпота) или перикардит (подтвержденный с помощью ЭхоКГ или выслушиванием шума трения перикарда).
7. Поражения почек: персистирующая протеинурия > 0,5 г/сутки или цилиндрурия (эритроцитарная, гемоглобиновая, зернистая или смешанная).
8. Поражение ЦНС: судороги или психоз (в отсутствие приёма ЛС или метаболических нарушений).
9. Гематологические нарушения: гемолитическая анемия с ретикулоцитозом, или лейкопения <4,0*109/л (зарегистрированная 2 и более раза), или тромбоцитопения <100*109/л (в отсутствие приема ЛС).
10. Иммунологические нарушения анти-ДНК, анти-Sm, аФЛ: увеличение уровня IgG или IgM (АТ к кардиолипину); положительный тест на волчаночный антикоагулянт при использовании стандартных методов; ложноположительная реакция Вассермана в течение как минимум 6 мес. при подтвержденном отсутствии сифилиса с помощью реакции иммобилизации бледной трепонемы и теста флуоресцентной адсорбции трепонемных АТ
11. АНФ: повышение титров АНФ (при отсутствии приема ЛС, вызывающих волчаночноподобный синдром).
Диагноз устанавливают при обнаружении 4 и более вышеперечисленных критериев.
Цeли при лечении СКВ — снизить выражeнность заболeвания, прeдотвратить обострeние и вызвать рeмиссию болезни.
Глюкокортикоиды (ГК) — препараты первого ряда при СКВ. Наиболее эффективны препараты короткого действия, минимально влияющие на минеральный обмен:
преднизолон;
метилпреднизолон ("Урбазон", "Медрол", "Солу-Медрол")
Дозировка зависит от активности заболевания:
низкая активность < 10-20 мг/сутки;
умеренная — 20-40 мг/сутки в течение 2-4 недель с постепенным снижением до поддерживающих доз;
высокая активность > 1 мг/кг/сутки (но не больше 60 мг/сутки), длительность зависит от клинического эффекта.
Цитостатики (метотрексат).
НПВП при лихорадке и для уменьшения болей в суставах и мышцах.
Противомалярийные препараты. при невыраженных формах СКВ. гидроксихлорохин — по 200 мг в сутки, доза может быть увеличена до 400 мг в сутки. Улучшение проявляется через 4-6 месяцев.
Больным СКВ необходимо снижать уровень липидов и сахара, уменьшать риск образования тромбов
Генно-инженерные биологические препараты (ГИБП) — ритуксимаб и белимумаб.
Все больные СКВ подлежaт диспансерному нaблюдению.
Пациентом с СКВ необходимо:
Посещать ревматолога не реже двух раз в три месяца.
Каждые три месяца сдавать анализы: ОАК, ОАМ, б/х крови
Ежегодно:
сдавать анализ на липидный профиль для профилактики атеросклероза;
проходить денситометрию (диагностика плотности и вероятности переломов костной ткани) для предотвращения остеопороза;
делать Rg-графию костей таза, чтобы избежать асептического некроза головки бедренной кости;
проходить офтальмологическое исследование для предотвращения риска ретинопатии при приёме гидроксихлорохина;
определять титры антител к фосфолипидам (при наличии вторичного антифосфолипидного синдрома);
12. Аортальные пороки. Этиология. Клинико-инструментальная диагностика. Тактика врача-терапевта.+
Основными вариантами аортальных пороков являются стеноз устья аорты (аортальный стеноз) и/или недостаточность аортального клапана - НАК.
Стеноз устья аорты (аортальный стеноз) — это сужение выносящего тракта ЛЖ в области АК (аортального клапана), ведущее к затруднению оттока крови и резкому возрастанию градиента давления между ЛЖ и аортой
Этиология
Наиболее частыми причинами клапанного АС являются:
– дегенеративный кальцифицирующий (идиопатический) процесс на створках АК;
– врожденные аномалии АК (чаще встречается бикуспидальный АК);
– ревматическое поражение створок клапана (хроническая ревматическая болезнь сердца — ХРБС)
Клинические признаки: головокружения и обмороки при физической нагрузке; «стенокардические» боли в области сердца; одышка, сердечная астма. бледность кожных покровов;
• при значительном сужении аортального клапана пульс становится малым, низким и редким (pulsusparvus, tardus et rarus); АД нормальное или снижение систолического АД; разлитой высокий и резистентный верхушечный толчок, расширение границ относительной тупости сердца влево; • систолическое дрожание, определяемое пальпаторно во втором межреберье справа от грудины;
• при аускультации во втором межреберье справа от грудины определяется ослабление I тона, и II тона из-за плохой подвижности деформированных створок аортального клапана.
Инструментальные исследования
ЭКГ: горизонтальное положение ЭОС; признаки гипертрофии левого желудочка; признаки ишемии миокарда при суточном мониторировании;
• аритмии: синусовая бради- и тахикардия, экстрасистолия, ФП на стадии кардиомегалии.
ЭхоКГ:
• признаки гипертрофии левого желудочка;
• изменение структуры створок аортального клапана, кальцификация створок;
• уменьшение амплитуды раскрытия створок аортального клапана:
МРТ выявляет те же признаки аортального стеноза, что и ЭхоКГ.
Рентгенологическое исследование: обызвествление аортального клапана, увеличение тени сердца влево, в частности, удлинение нижней дуги левого контура, более подчеркнутая «талия» сердца, пост-стенотическая дилатация аорты, на поздних стадиях - застойные явления в легких.
Принципы лечения:
1. При значительном стенозе – ограничение тяжелой физической нагрузки.
2. Медикаментозная терапия в легких случаях не требуется, в тяжелых случаях – малоэффективна, проводится профилактика инфекционного эндокардита и лечение сердечной недостаточности (ингибиторы АПФ назначаются очень осторожно, что лимитируется наличием гипотензии).
3. Хирургическое лечение показано при градиенте систолического давления на клапане свыше 50 мм рт.ст. при нормальном МОС (оперативная вальвулотомия, чрезкожная балонная аортальная вальвулопластика, протезирование аортального клапана).
Недостаточность аортального клапана - патологическое состояние, при котором в период диастолы створки клапана не закрывают полностью просвет аорты и вследствие этого происходит обратный ток крови из аорты в левый желудочек (аортальная регургитация).
Этиология
• Органическая недостаточность, связанная с поражением створок клапана: хроническая ревматическая болезнь; инфекционный эндокадит; склероз; травматический отрыв створок.
• Относительная недостаточность, связанная с дилатацией аорты при следующих заболеваниях: атеросклероз, атерокальциноз аорты; сифилис; синдром Марфана; диффузные заболевания соединительной ткани.
• Врожденная аномалия: неполное смыкание створок или пролапс аортального клапана (врожденный двустворчатый клапан аорты).
Симптомы.
1. Бледность кожных покровов и слизистых оболочек, цианоз губ, акроцианоз.
2. Симптом Мюссе - покачивание головы вперед и назад в такт пульсу, усиленная пульсация периферических артерий: сонных («пляска каротид»), подмышечных, радиальных. Пульсация сосудов ногтевого ложа, определяющаяся при легком прижатии кончика ногтя (капиллярный пульс Квинке).
3. Определяется пульсация зрачков, иногда - пульсация язычка мягкого нёба.
4. Пульс скорый и высокий, вследствие большой разницы между систолическим и диастолическим АД (celer et altus).
5. Повышение систолического и снижение диастолического (иногда ниже 20 мм рт.ст.) АД, высокое пульсовое давление.
6. Верхушечный толчок разлитой, усиленный, приподнимающий, куполообразный, смещенный влево и вниз.
7. Границы относительной тупости сердца расширены влево вследствие гипертрофии и дилатации левого желудочка, сердце приобретает аортальную конфигурацию с подчеркнутой талией.
8. При аускультации сердца: тоны сердца ослаблены, II тон над аортой тоже ослаблен, при разрушении створок может вообще не выслушиваться, а при атеросклеротическом поражении клапана, наоборот, может оставаться достаточно звучным.
9. При выслушивании бедренной артерии выслушивается двойной тон Траубе и двойной шум Виноградова-Дюрозье.
Инструментальные исследования
ЭКГ - признаки гипертрофии левого желудочка:
ЭхоКГ:
• гипертрофия и дилатация левого желудочка;
• усиленное систолическое движение стенки левого желудочка;
• утолщение, нередко кальцификация, отсутствие фазы смыкания створок аортального клапана в диастолу;
• расширение корня аорты;
• на поздних стадиях - дилатация левого предсердия, повышение давления в легочной артерии;
Рентгенологическое исследование - тень сердца с подчеркнутой талией, увеличенным левым желудочком, закругленной верхушкой, напоминает «сидящую утку или башмак». Признаки венозного полнокровия и застоя в малом круге кровообращения.
Принципы лечения приобретенных пороков сердца.
1. Ограничение тяжелых физических нагрузок во избежание усугубления дилатации левого желудочка.
2. Медикаментозная терапия проводится по поводу застойной сердечной недостаточности (при этом особенно эффективны ингибиторы АПФ, уменьшающие регургитацию); рекомендуется профилактика инфекционного эндокардита.
3. Хирургическое лечение (чаще протезирование биологическим или механическим протезом) показано при:
- появлении клинических признаков порока (ангинозной боли, признаков левожелудочковой сердечной недостаточности)
- при наличии выраженной регургитации и прогрессирующей дилатации левого желудочка, увеличении конечно-систолического объема и уменьшении фракции выброса даже без клинических проявлений порока
- при значительном снижении физической работоспособности по данным нагрузочного тестирования.
13. Дифференциальная диагностика системных васкулитов. Классификация. Критерии постановки диагноза. Принципы лечения.+
Дифференциальный диагноз: •Клинические признаки, наблюдаемые при системных васкулитах, встречаются при системных заболеваниях соединительной ткани (включая антифосфолипидный синдром), инфекциях (инфекционный эндокардит, сифилис, другие системные инфекции) и опухолях(предсердная миксома, лимфопролиферативные опухоли), тяжѐлом атеросклеротическом поражении сосудов, больные с лихорадкой, похуданием и признаками полиорганного поражения (сосудистая пурпура, множественный мононеврит, мочевой синдром).
Системные васкулиты (СВ)- гетерогенная группа заболеваний, основным морфологическим признаком которых является воспаление сосудистой стенки, а клинические проявления зависят от типа, калибра, локализации пораженных сосудов и активности системного воспаления.
-Васкулит с поражением сосудов крупного калибра
Васкулит с поражением сосудов среднего калибра
Васкулиты с поражением сосудов мелкого калибра
Васкулиты ассоциированные с антинейтрофильными цитоплазматическими антителами
Васкулит с поражением сосудов единственного органа
Васкулит ассоциированный с системными заболеваниями
Васкулит, ассоциированный с определенными этиологичесими факторами
Критерии диагностики: Конституциональные симптомы, недеструктивный олигоартрит, Поражение кожи •Множественный мононеври Поражение почек - ишемическое поражение, О. гломерулонефрит, поражение ЛОР-органов
Лабораторные исследования ОБЩИЙ АНАЛИЗ КРОВИ •Наблюдается нормохромная анемия, тромбоцитоз, нейтрофильный лейкоцитоз, повышение СОЭ и СРБ. ИММУНОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ • Антиген цитоплазматических нейтрофилов (ANCA) •Криоглобулины: маркер криоглобулинемического васкулита. Биохимический анализ крови (креатинин, КФК, общий белок и белковые фракции, электролиты, печеночные пробы, липидный спектр, СРБ, глюкоза) Антитела к фосфолипидам волчаночный антикоагулянт, АТ к кардиолипину
Коагулограмма: фибриноген, МНО, АЧТВ Бактериологическое обследование крови: исключение инфекции ОАМ Суточная протеинурия ЭКГ
Тактика ведения:. Медикаментозное лечение: НПВС, ГЛЮКОКОРТИКОИДЫ( Гидрокортизон, 1 мг/кг/сут, ГК составляет 3—4 нед.,после достижения эффекта дозу препаратов постепенно уменьшают по 5 мг в 2 нед до поддерживающей (0,15-0,2 мг/кг/сут), которая назначается от одного года до 3—5 лет)
ИММУНОСУПРЕССИВНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА . Циклофосфамид - 1-2 мг/кг/сут (перорально) в течение 10-14 дней, МЕТОТРЕКСАТ •Доза препарата 12,5-17,5 мг в неделю. АЗАТИОПРИН •Оптимальная доза 1-3 мг/кг/сут; поддерживающая доза - 50 мг в день.
ВНУТРИВЕННЫЕ ИММУНОГЛОБУЛИНЫ • в дозе 2 мг/кг (ежемесячно в течение 6 мес)
14. Остеоартроз. Современные представления об этиологии. Клинические проявления. Стандарты лечения.+
гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц.
Остеоартроз является мультифакториальным полиэтиологическим заболеванием. Три основные причины развития дегенеративно-дистрофического процесса в суставе: травма, дисплазия и воспаление.
Травма сустава — самая частая причина артроза. На втором месте стоит дисплазия сустава — врождённые особенности, которые сопровождаются плохой биомеханикой сустава.
Воспаление также достаточно часто приводит к повреждениям тканей сустава и развитию вторичного артроза. Чаще всего это является результатом аутоиммунных заболеваний (например, ревматоидный артрит)
Клин.прояления: боль в области пораженного сустава усиление боли в положении стоя или при нагрузке боль появляется при нагрузке или в покое; К концу дня после физической нагрузки, боли усиливаются, после отдыха боли уменьшаются наличие «стартовых болей»; утренняя скованность и тугоподвижность, ограничение функции сустава. Физикальное обследование: крепитация увеличение объѐма сустава чаще происходит за счѐт пролиферативных изменений (остеофитов), но может быть и следствием отѐка околосуставных тканей. образование узелков в области дистальных (узелки Гебердена) и проксимальных (узелки Бушара) межфаланговых суставов кистей. выраженная припухлость и локальное повышение температуры над суставами возникает редко, но может появляться при развитии вторичного синовита. варусная деформация коленных суставов, «квадратная» кисть, узелки Гебердена и Бушара соответственно в дистальных и проксимальных межфаланговых суставах кистей
Рентгенологическая стадия: 0 – изменения отсутствуют. I – сомнительные рентгенологические признаки. II – минимальные изменения (небольшое сужение суставной щели, единичные остеофиты). III – умеренные проявления (умеренное сужение суставной щели, множественные остеофиты). IV – выраженные изменения (суставная щель почти не прослеживается, грубые остеофиты).
Тактика лечения : все пациенты с остеоартрозом получают лечение амбулаторно. − Немедикаментозное лечение: Режим: II,свободный; Стол №15. − Медикаментозное лечение: Рентгенологическая стадия I немедикаментозное лечение и НПВП, хондропротекторы(Хондроитин сульфат внутрь 250-500 мг 2 раза в сутки сутки, Курсами 2 раза в год); Рентгенологическая стадия II немедикаментозное лечение, НПВП, хондропротекторы и в/с введение препаратов исскуственной синовиальной жидкости курсами; Рентгенологическая стадия III немедикаментозное лечение, НПВП, хондропротекторы, антидепресанты и в/с введение препаратов исскуственной синовиальной жидкости курсами; Рентгенологическая стадия IV эндопротезирование пораженного сустава.
15. Анкилозирующий спондилоартрит. Методы диагностики. Стандарты лечения. Б.Бехтерева.+
Анкилозирующий спондилит (АС) – хроническое, прогрессирующее воспалительное ревматическое заболевание, преимущественно поражающее осевой скелет с частым вовлечением в патологический процесс энтезисов и периферических суставов, а также других органов и систем.
Клинические критерии: 1. Боли и скованность в нижней части спины, длительностью не менее 3 мес, уменьшающиеся после физических упражнений и не стихающие в покое. 2. Ограничение движений в поясничном отделе позвоночника в сагиттальной и фронтальной плоскостях. 3. Уменьшение дыхательной экскурсии грудной клетки в сравнении с нормальными значениями (для пола и возраста). Рентгенологический критерий: Cакроилиит двусторонний/одностор.
Тактика лечения Немедикаментозное лечение: поддержание оптимальной массы тела; сбалансированная диет; ЛФК
Медикаментозное лечение: препаратами первой линии =НПВС(Диклофенак 75 мг 1 раз в сутки 5 дней, Эторикоксиб внутрь по 60- 120 мг в сутки 1-2 раза в сутки) Базисные противовоспалительные препараты (БПВП)- Сульфасалазин внутрь 500- 2000 мг 2-3 раза в сутки длительно) Глюкокортикостероидные препараты (ГК)- Бетаметазон = внутрисуставно 2мг + 5мг) Генно-инженерные биологические препараты- Адалимумаб рекомбинантные человеческие моноклональные антитела к ФНО п/к 40 мг п/к 1 раз в 2 недели длительно
16. Дифференциальный диагноз ревматоидного артрита с артритами при системных болезнях соединительной ткани (системная красная волчанка, системная склеродермия).+
Признаки |
Признаки СКВ |
Признаки РА |
Характер поражения суставов |
Мигрирующий |
Прогрессирующий |
Утренняя скованность |
Нехарактерна |
Выражена |
Преходящие сгибательные контрактуры |
Характерны |
Нехарактерны |
Деформация суставов |
Минимальная поздняя |
Значительная |
Механизм развития деформаций |
Преимущественное поражение сухожильно-связочного аппарата и мышц |
Деструкция суставных поверхностей |
Нарушение функции |
Незначительное |
Значительное |
Эрозии костей |
Нехарактерны |
Типичны |
Анкилозы |
Несвойственны |
Характерны |
Морфологическая картина |
Подострый синовит с ядерной патологией |
Хронический гиперпластический синовит с образованием паннуса |
Ревматоидный фактор |
Непостоянен, в низких титрах у 5—25% больных |
Стойкий, в высоких титрах у 80% больных |
Положительный LE-клеточный тест |
У 86% больных |
У 5—15% больных |
Признак |
Реактивный артрит |
Ревматоидный артрит |
Другие спондилоартропатии |
Поражение суставов |
Асимметричный моно-олигоартрит суставов нижних конечностей |
Артрит суставов кисти |
Псориатический артрит –дистальный межфаланговый артрит кистей и стоп, анкилозирующий спондилит - сакроилеиит |
Утренняя скованность |
Не характерна |
Выражена |
Скованность в поясничной области |
Предшествующяя артриту инфекции (диареи или уретрита) |
Характерны |
Не характерны |
Не характерны |
Подвижность суставов |
Ограничена незначительно |
Выражена |
Ограничение движений поясничного отдела позвоночника |
Рентгенография суставов |
Энтезопатия в виде очагов деструкции в местах прикрепления связок к костям |
Остеопороз, сужение суставной щели, узуры |
Сакроилеиит и признаки энтезопатии |
СОЭ |
Повышена |
Повышена |
Повышена |
Ревматоидный фактор |
Отрицательный |
Положительный при серопозитивном варианте РА |
Отрицательный |
Эффект от применения |
НПВП и антибактериальной терапии |
Базисных протиовоспалительных препаратов |
Сульфасалазина |
Системная склеродермия. Феномен Рейно и уплотнение кожи; редко может выявляться артрит, обычно артралгии; ограничение объёма движений, связанное с прикреплением кожи к подлежащей фасции.
17. Дифференциальная диагностика и врачебная тактика при серонегативных спондилоартритах (спондилоартриты, ассоциированные с неспецифическим язвенным колитом, терминальным илеитом, псориазом).+
Врачебная тактика
Немедикаментозное лечение: При затяжном или хроническом течении РеА избегать факторов, которые потенциально могут провоцировать обострение болезни (интеркуррентные инфекции, стресс, курение и приёма алкоголя); сбалансированная диета, включающая продукты с высоким содержанием полиненасыщенных жирных кислот (рыбий жир, оливковое масло и др.), фрукты, овощи; обучение пациентов (изменение стереотипа двигательной активности и др.); лечебная физкультура (1-2 раза в неделю); физиотерапия: тепловые или холодовые процедуры, ультразвук, лазеротерапия (при умеренной активности РеА); санаторно-курортное лечение (в стадии ремиссии).
Медикаментозное лечение
Антимикробная терапия: Лечение триггерной инфекции антибиотиками, чувствительными к соответствующим микроорганизмам, до эрадикации инфекции (около 4 недель). При выявлении хламидийной инфекции у больного РеА, необходимо обследование и лечение полового партнёра в течение 2 недель антибактериальными препаратами под микробиологическим контролем. Антибактериальную терапию хламидийного артрита проводят макролидами, тетрациклинами и фторхинолонами в оптимальных суточных дозах: азитромицин 0,5 -1,0 г, рокситромицин 0,3 г, кларитромицин 0,5 г. (макролиды);доксициклин 0,3 г. (тетрациклины); ципрофлоксацин 1,5 г, офлоксацин 0,6 г., ломефлоксацин 0,8 г., пефлоксацин 0,8 г. (фторхинолоны).
Нестероидные противовоспалительные препараты для подавления воспалительного процесса в суставах, энтезисах и позвоночнике. Выбор отдельных ЛС осуществляется в зависимости от индивидуальной эффективности и переносимости.
Рекомендуемые дозы НПВП: диклофенак 25 мг. 75 – 150 мг/сут в 2 приема; ибупрофен 1200 – 2400 мг/сут в 3-4 приема; индометацин 25 мг. 50 –200 мг/сут в 2-4 приема (макс. 200 мг); кетопрофен 100 – 400 мг/сут в 3-4 приема; этодолак 600 – 1200 мг/сут в 3 – 4 приема;ацеклофенак 200 мг в 2 приема; лорноксикам 8 – 16 мг в 2 приема; мелоксикам 7,5 –15 мг/сут в 1 прием; эторикоксиб 120 – 240 мг/сут в 1-2 приема.
Глюкокортикоиды: Локальная терапия ГК (бетаметазон): внутрисуставное введение в дозе 0,8-4 мг 1 раз в 3 нед., введение в область воспалённых энтезисов. В случае ярких, прогностически неблагоприятных системных проявлений (кардит, нефрит и др.) может быть эффективна кратковременная терапия ГК (преднизолон 5 мг, метилпреднизолон) для приёма внутрь не более 10 мг/сут. При конъюнктивите применяют глазные капли, содержащие ГК. В большинстве случаев иридоциклита достаточно локальной терапии ГК (дексаметазонкапли глазные 0,1%, мазь глазная) (инстилляции, субконъюнктивальные инъекции) в сочетании со средствами, расширяющими зрачок.
Сульфасалазин 500 мг применяется в дозе (2 г/сут) при затяжном или хроническом течении (отсутствие эффекта от симптоматической терапии в течение 3 мес. и более): снижает признаки воспаления периферических суставов; не влияет на прогрессирование артрита. Метотрексат 2,5 мг, азатиоприн, применяют по тем же показаниям, как и сульфасалазин.
18. Синдром старческой хрупкости. Критерии диагностики. Врачебная тактика.
R 54. Старческая астения (СА) – ключевой гериатрический синдром (ГС), характеризующийся возраст-ассоциированным снижением физиологического резерва и функций многих систем организма, приводящий к повышенной уязвимости организма пожилого человека к воздействию эндо- и экзогенных факторов, с высоким риском развития неблагоприятных исходов для здоровья, потери автономности и смерти. Синдром СА тесно связан с другими ГС и с полиморбидностью, может быть потенциально обратим и влияет на тактику ведения пациента.
Диагностика синдрома СА состоит из двух этапов:
1. скрининг старческой астении (выполняется любым медицинским работником, контактирующим с пациентом 60 лет и старше, в первую очередь - врачом общей практики, врачом терапевтом-участковым, семейным врачом);
2. комплексная гериатрическая оценка (выполняется врачом-гериатром, медицинской сестрой и другими участниками мультидисциплинарной команды).
Комплексная гериатрическая оценка (КГО) – многомерный междисциплинарный диагностический процесс, включающий оценку физического и психоэмоционального статуса, функциональных возможностей и социальных проблем пожилого человека, с целью разработки плана лечения и наблюдения, направленного на восстановление или поддержание уровня его функциональной активности.
Основными задачами КГО являются:
1) определение основных проблем, ухудшающих функциональный статус и качество жизни пациента;
2) определение степени тяжести СА.
3) разработка плана мероприятий, направленных на разрешение/устранение этих проблем.
Длительность КГО составляет 1,5 - 2 часа. В виду достаточно большой продолжительности КГО и потенциальной возможности утомления пациента, визиты к медицинской сестре и к врачу-гериатру могут быть запланированы в разные дни с разумным интервалом (например, 2-3 дня). В ходе КГО важно уточнить ожидания и предпочтения самого пациента и членов его семьи.
Кому проводится КГО? Только пациентам в стабильном состоянии, отобранным на основании скрининга. КГО не проводится на фоне острых заболеваний / декомпенсации хронических состояний.
Где проводится КГО? В гериатрическом кабинете, в гериатрическом отделении, на 16 дому. В период госпитализации КГО проводится однократно. Некоторые шкалы могут быть использованы для оценки динамика состояния.
Кто проводит КГО? Мультидисциплинарная команда: врач – гериатр, медицинская сестра, имеющая подготовку по гериатрии, специалист по социальной работе, при необходимости – инструктор-методист по лечебной физкультуре, другие специалисты (например, врачдиетолог, врач-невролог, психолог). До осмотра врачом-гериатром ряд тестов, измерений и оценок по шкалам выполняется подготовленной медицинской сестрой.
Какие домены оценивают при КГО Домены КГО физическое здоровье (жалобы и анамнез, включая лекарственный, физическое исследование и исследование по органам и системам) функциональный статус (физическое функционирование, риск падений, инструментальная и базовая функциональная активность) когнитивные функции и эмоциональное состояния (выполняется в первую очередь, так как утомление пациента может повлиять на их результаты), социальный статус и потребность в социальной помощи Учитываются результаты лабораторных и инструментальных исследований.
Присутствие членов семьи/опекунов при КГО Рекомендуется присутствие члена семьи/опекуна или человека, ухаживающего за пациентом с целью получения необходимых данных анамнеза, более достоверной оценки проблем и функциональных возможностей пациента, а также обсуждения дальнейшего плана ведения.
Врачебная тактика
Наличие множества заболеваний и ГС у ослабленных и зависимых пациентов с синдромом СА не позволяет одновременно проводить их диагностику и коррекцию в полном объеме. Выбор приоритетного направления лечения в данный момент должен основываться на результатах КГО с учетом следующей последовательности:
1. Лечение потенциально жизнеугрожающих заболеваний и состояний.
2. Коррекция заболеваний и ГС, ухудшающих функциональную активность и влияющих на качество жизни в данный момент.
3. Коррекция заболеваний и ГС, ухудшающих функциональную активность и влияющих на качество жизни в долгосрочной перспективе с учетом ожидаемой продолжительности жизни пациента.
При выборе метода лечения следует учитывать:
подтверждение его эффективности в клинических исследованиях по данному заболеванию,
в какой популяции его эффективность продемонстрирована,
в каких дозах и как долго использовались назначаемые препараты.
При составлении индивидуального плана ведения пациента с синдромом СА важно оценить, насколько положения существующих клинических рекомендаций по тем или иным нозологиям применимы для данного пациента с учетом выявленных ГС, результатов оценки функционального статуса, когнитивных и эмоциональных нарушений, а также социальных проблем и ожидаемой продолжительности жизни.
Немедикаментозные методы лечения старческой астении
Рекомендуется регулярная физическая активность в объеме и интенсивности, зависящей от индивидуальных функциональных возможностей, всем пациентам с синдромом старческой астении или риском ее развития с целью улучшения/поддержания физического, функционального и когнитивного статусов.
Рекомендованы следующие виды физической активности пациентам со старческой астенией или риском ее развития: упражнения на сопротивление; силовые упражнения; аэробные тренировки (ходьба с изменением темпа и направления, ходьба на беговой дорожке, подъем по ступенькам); упражнения на поддержание равновесия.
Рекомендовано проводить консультирование по вопросам рационального питания всем пациентам с синдромом старческой астении с целью профилактики синдромов недостаточности питания и саркопении с акцентом на достаточное потребление белка с пищей и водно-питьевой режим.
Рекомендуется увеличение потребления белка до 1,0-1,5 г / кг массы тела в сутки пациентам с синдромом старческой астении с целью лечения и профилактики саркопении [78-85].
Рекомендовано использовать нутриционную поддержку у пациентов с синдромом старческой астении и недостаточностью питания с целью поддержания массы тела, коррекции саркопении и сохранения функционального статуса.
Не рекомендуется снижение веса пациентам старческого возраста с избыточной массой тела и ожирением I степени (индекс массы тела 25-35,9 кг/м2 ) в виду увеличения риска развития гериатрических синдромов и неблагоприятных исходов.
Рекомендуется консультировать по вопросам организации безопасных условий проживания всех пациентов пожилого и старческого возраста, а также пациентов со старческой астенией, с повторными падениями или с высоким риском падений с целью снижения риска падений.
Рекомендуется консультирование по вопросам подбора обуви всех пациентов пожилого и старческого возраста, с синдромом старческой астении, с повторными падениями или с высоким риском падений с целью снижения этого риска.
Рекомендуется проведение когнитивного тренинга всем пациентам пожилого и старческого возраста с синдромом старческой астении с целью профилактики когнитивного снижения и замедления прогрессирования старческой астении.
Рекомендуется направлять пациентов пожилого и старческого возраста на консультацию к специалистам по социальной помощи с целью выявления потенциально корригируемых проблем социального характера, а также рекомендовать обращаться в центры социального обслуживания для повышения социальной активности.
Медикаментозная терапия
Рекомендуется при выборе тактики лекарственной терапии у пациентов пожилого и старческого возраста принимать во внимание не только наличие хронических и/ или острых заболеваний, но и гериатрических синдромов (особенно старческой астении), результаты оценки функционального статуса, наличие когнитивных и эмоциональных нарушений, а также социальных проблем у пациентов с синдромом старческой астении.
Рекомендуется мониторировать появление/усугубление ГС при назначении лекарственной терапии у пациентов пожилого и старческого возраста с синдромом старческой астении или риском ее развития с целью оценки безопасности лечения.
Рекомендуется прием препаратов витамина D или его аналогов пациентам с синдромом старческой астении и дефицитом/недостатком витамина D с целью коррекции его уровня, профилактики падений и переломов и улучшения прогноза жизни.
Рекомендовано назначение комбинации витамина D или его аналогов и препарата кальция всем пациентам с синдромом старческой астении и остеопорозом.
Рекомендовано назначение антиостеопоротической антирезорбтивной терапии (алендроновой кислотой, золедроновой кислотой, деносумабом) пациентам с синдромом старческой астении и остеопорозом с целью профилактики переломов.
Рекомендуется назначение костно-анаболической терапии терипаратидом сроком на 24 мес с последующим переходом н антирезорбтивную терапию пациентам с анамнезом переломов вследствие остеопороза (особенно тел позвонков или проксимального отдела бедренной кости), не получавшим ранее антирезорбтивную терапию, с целью профилактики последующих переломов.
Рекомендуется назначение костно-анаболической терапии терипаратидом пациентам с синдромом старческой астении и тяжелым остеопорозом с неэффективностью антирезорбтивной терапии и наличием предшествующих низкоэнергетических переломов вследствие остеопороза.
Рекомендуется назначать терапию алендроновой кислотой, золедроновой кислотой, деносумабом, терипаратидом в сочетании с комбинацией витамина D или его аналогов и препарата кальция пациентам со старческой астенией и остеопорозом с целью обеспечения оптимальной эффективности лечения.
19. Дифференциальная диагностика и врачебная тактика при воспалительных заболеваниях суставов.+
Классификация заболеваний суставов:
Воспалительные заболевания суставов (могут вызвать все 5 классов известных возбудителей: бактерии, вирусы, грибки, простейшие, глисты). Инфекционные воспаления суставов, вызванные бактериями, могут быть неспецифической этиологии (ревматический полиартрит, палиндромный ревматизм, ревматоидный полиартрит, реактивные артриты и др.) и специфической этиологии (туберкулезный, сифилитический, гонорейный, бруцеллезный, дизентерийный, токсоплазмозный, менингококковый и др.). Вирусные артропатии наблюдаются при сывороточном гепатите, краснухе, оспе, ветряной оспе, инфекционном мононуклеозе и др. Кандидозные полиартриты наблюдаются при споротрихозе (артрит “садовника”), кандидозе и др.
Дегенеративно-дистрофические поражения суставов: деформирующий остеоартроз, болезнь Бехтерева, остеохондропатии (врожденная - болезнь Пертеса).
Метаболические поражения суставов: подагра, псевдоподагра.
Вторичные артропатии: при заболевании крови (гемофилия, лейкозы, капилляротоксикоз и др.), при онкозаболеваниях (как паранеопластический процесс), при заболеваниях соединительной ткани (коллагенозы), при эндокринных заболеваниях (сахарный диабет, синдром или болезнь Иценко-Кушинга), при заболеваниях кожи (псориаз), при заболеваниях печени (агрессивный гепатит), вибрационной болезни, нарушении обмена витамина С (скорбут), при психических заболеваниях
Травматические и посттравматические артриты.
Сочетанные формы.
РА - хроническое воспалительное заболевание неизвестной этиологии с характерным симметричным поражением суставов и внесуставными проявлениями, в крови больных часто определяется ревматоидный фактор. Для диагностики РА используют Критерии Американской коллегии ревматологов (1987): Диагноз ревматоидного артрита ставится при наличии 4 из 7 критериев. Критерии с 1 по 4 должны присутствовать не менее 6 недель.
• утренняя скованность - возникающая по утрам скованность в области суставов или околосуставных тканей, сохраняющаяся не менее 1 часа;
• артрит 3 или более суставов - подтвержденное врачом наличие припухлости или выпота, по крайней мере в 3 суставах; возможно поражение до 14 суставов (с 2 сторон): пястнофаланговых, проксимальных межфаланговых, суставов запястья, локтевых, голеностопных;
• артрит суставов кистей - припухлость, по крайней мере одной из следующих групп суставов: суставов запястья, пястнофаланговых и проксимальных межфаланговых;
• симметричный артрит - сходное, однако без абсолютной симметрии, двустороннее поражение суставов (пястнофаланговых, проксимальных межфаланговых, плюснефаланговых);
• ревматоидные узелки - подтвержденное врачом наличие подкожных узелков, локализующихся преимущественно на выступающих участках тела, разгибательных поверхностях или в околосуставных областях;
• РФ - обнаружение (любым методом) повышенных титров РФ в сыворотке крови;
• рентгенологические изменения, типичные для РА: эрозии или околосуставной остеопороз, локализующиеся в суставах кистей и стоп и наиболее выраженные в клинически пораженных суставах.
Псориатический артрит развивается у 6-7% больных псориазом через 6-7 лет после кожных проявлений, иногда предшествует кожным проявлениям заболевания. Диагн-ие критерии псориатического артрита: 1. Поражение дистальных межфаланговых суставов пальцев. 2. Одновременное поражение пястно-фалангового (плюстне-фалангового), проксимального и дистального межфаланговых суставов (“осевое поражение”). 3. Раннее поражение суставов стоп, в том числе большого пальца. 4. Боли в пятках (подпяточный бурсит). 5. Наличие псориатических бляшек на коже или типичное для псориаза изменение ногтей (подтверждается дерматологом). Дифф диагноз псориатического артрита: 1. Ревматоидный артрит (формы псориатического артрита, протекаюшей с поражением 1 или 2-х крупных суставов и отсутствием кожных изменений). 2. Болезнь Рейтера (формы псориатического артрита, протекаюшей с поражением глаз - конъюнктивитом и уретритом, особенность - развитие их на фоне заболевания).
Подагра - нарушения пуринового обмена. Характерны: повышение содержания мочевой кислоты в крови (гиперурикемия) и отложения уратов в суставах и/или околосуставных тканях. Диагн-кие критерии подагры: 1. Наличие в анамнезе и наблюдение повторных атак острого артрита. 2. Развитие максимума воспаления в течение 1-х суток. 3. Моноартикулярный характер артрита. 5. Гиперемия кожи над воспаленным суставом. 6. Болезненность и припухлость I плюснефарангового сустава. 7. Одностороннее поражение I плюснефарангового сустава. 8. Одностороннее поражение 2-х плюсневых суставов. Дифф диагноз подагрического артрита: 1. Псевдоподагра - пирофосфатная артропатия (хондрокальциноз). Протекает с приступами острого артрита, в синовиальной жидкости обнаруживают микрокристаллы пирофосфата кальция. 2. Псевдоподагра - гидроксиапатитная артропатия (часто развивается у женщин). Характерны множественные очаги кальцификации в периартикулярных тканях, особенно в сухожилиях. 3. Ревматоидный полиартрит (при наличии вторичной подагры).
20. Скв. Показатели активности воспалительного процесса. Принципы интенсивной терапии.
- аутоиммунное ревм-ое заб-е с многочисленными клин-ми проявлениями и непредсказуемым течением, поражающее любые органы или системы, которое довольно часто развивается в течение нескольких месяцев или лет со стойкими или наоборот быстро меняющимися клиническими проявлениями, волнообразным течением, чередованием ремиссий и обострений. Классификационные критерии: 1.Сыпь на скулах: фиксированная эритема, с тенденцией к распространению на носогубную зону. 2.Дискоидная сыпь: эритематозные приподнимающиеся бляшки с прилипающими кожными чешуйками и фолликулярными пробками, на старых очагах возможны атрофические рубцы. 3.Фотосенсибилизация: кожная сыпь, возникающая в результате реакции на солнечный свет. 4.Язвы в ротовой полости: изъязвления полости рта или носоглотки, обычно безболезненные. 5.Артрит: неэрозивный артрит, поражающий 2 или более периферических сустава, проявляющийся болезненностью, отеком и выпотом. 6.Серозит: плеврит (плевральные боли и/или шум трения плевры, и/или плевральный выпот), перикардит (шум трения перикарда при аускультации и/или признаки перикардита при эхокардиографии). 7.Поражение почек: персистирующая протеинурия не менее 0,5 г/сутки и/или цилиндрурия (эритроцитарная, зернистая или смешанная). 8. Поражение ЦНС: судороги, психоз (в отсутствие приема ЛС или метаболических нарушений). 9.Гематологические нарушения: гемолитическая анемия с ретикулоцитозом, лейкопения < 4,0 х10 9 /л (зарегистрированная 2 и более раза), тромбоцитопения < 100 х10 9 /л (при отсутствии приема лекарственных препаратов). 10.Иммунологические нарушения: 1.а-ДНК, 2.анти-Sm, 3.анти-КЛ, 4.положительный тест на волчаночный антикоагулянт, 5.стойкая ложно- положительная реакция Вассермана (не менее 6 месяцев) при лабораторно подтвержденном отсутствии сифилиса. 11.Повышение титров АНФ- антинукл фактор (при отсутствии лекарств, вызывающих волчаночноподобный синдром). Лечение: ремиссия. ГКС: преднизолон и метипреднизолон внутрь, ежедневная дроза 20-25 мг. НПВП используются в течение короткого времени и только у пациентов с низкой степенью вероятности развития побочных эффектов. Аминохинолиновые препараты (хлорохин, гидроксихлорохин) снижают риск тромботических осложнений в дозе 200-400 мг в день. Моноклональные антитела (с высокой иммунолог активность) Белимумаб по 10 мг\кг ежемесячно - назначается больным СКВ с преимущественным поражением кожи, слизистых оболочек, суставов, неактивным волчаночным нефритом. Цитостатики - при прогрессирующем течении, высокой активности, сопровождающимися поражением жизненно-важных органов и систем. циклофосфан 1000 мг в/в ежемесячно в течение 6 месяцев или по 500 мг каждые 2 недели, до 6 инфузий/ мофетила микофенолат 2-3 г в день в течение 6 месяцев. Применение плазмафереза может быть эффективным при цитопении, криоглобулинемии, васкулите и поражении ЦНС, тромботической тромбоцитопенической пурпуре. В случае развитие ХПН показано применение гемодиализа. Нет стрессу, инфекции, инсоляции, диета.
Systemic Lupus Erythematosus Disease activity score (SLEDAI) в этот индекс входит 24 параметра (16-клинических и 8 лабораторных показателей СКВ). Каждому показателю присвоены баллы от 1 до 8 каждому из признаков СКВ, вошедшего в индекс. Более серьезные проявления СКВ, такие как: поражение нервной системы, поражение почек, васкулит - имеют более высокую балльную оценку, чем другие признаки. Общий максимально возможный счет индекса SLEDAI составляет 105 баллов. При проведении оценки активности по индексу SLEDAI необходимо отмечать признаки СКВ, которые присутствовали у пациента в течение 10 предшествующих осмотру дней, независимо от их степени тяжести или улучшения/ухудшения состояния.
21. Ревматоидный артрит. Критерии постановки диагноза и оценки воспалительного процесса. Принципы базисной терапии. Показания к назначению генно-инженерной биологической терапии
- иммуновоспалительное (аутоиммунное) ревм-ое заболевание неизвестной этиологии, хар-еся хроническим эрозивным артритом и системным поражением внутренних органов, приводящее к ранней инвалидности и сокращению продолжительности жизни пациентов. Клин стадия: n. Очень ранняя стадия: длительность болезни 1 года при наличии типичной симптоматики РА q. Поздняя стадия: длительность болезни 2 года и более + выраженная деструкции мелких (III-IV рентгенологическая стадия) и крупных суставов, наличие осложнений. Активность болезни: n. 0 = ремиссия (индекс активности болезни -disease activity score) o. 1 = низкая (2,6< DAS28 5,1) p. 2 = средняя (DAS28 3,2 - 5,1) q. 3 = высокая (DAS28 > 5,1). Внесуставные (системные) проявления: 1. ревматоидные узелки 2. кожный васкулит (язвенно-некротический васкулит, инфаркты ногтевого ложа, дигитальный артериит) 3. васкулиты других органов 4. нейропатия (мононеврит, полинейропатия) 5. плеврит (сухой, выпотной), перикардит (сухой, выпотной) 6. синдром Шегрена 7. поражение глаз (склерит, эписклерит) 8. интерстициальное заболевание легких. Рентгенологическая стадия (по Штейнброкеру, в модификации): I - околосуставной остеопороз II – остеопороз + сужение суставной щели, могут быть единичные эрозии III – признаки предыдущей стадии + множественные эрозии + подвывихи в суставах IV – признаки предыдущей стадии + костный анкилоз. Функц класс: I – полностью сохранены: самообслуживание, непрофессиональная и профессиональная деятельность II – сохранены: самообслуживание, профессиональная деятельность, ограничена: непрофессиональная деятельность III – сохранено: самообслуживание, ограничены: непрофессиональная и профессиональная деятельность IV – ограничены: самообслуживание, непрофессиональная и профессиональная деятельность.
В качестве основного метода оценки активности воспаления при РА рекомендуется применять индекс DAS28. DAS28 = 0,56ÖЧБС+0,28ÖЧПС+0,70lnСОЭ+0,014ООСЗ где ЧБС – число болезненных суставов, ЧПС – число припухших суставов из следующих 28. ООСЗ – общая оценка пациентом состояния здоровья в мм по 100 миллиметровой визуальной аналоговой шкале
Для диагностики РА используют Критерии Американской коллегии ревматологов (1987):
• утренняя скованность - возникающая по утрам скованность в области суставов или околосуставных тканей, сохраняющаяся не менее 1 часа;
• артрит 3 или более суставов - подтвержденное врачом наличие припухлости или выпота, по крайней мере в 3 суставах; возможно поражение до 14 суставов (с 2 сторон): пястнофаланговых, проксимальных межфаланговых, суставов запястья, локтевых, голеностопных;
• артрит суставов кистей - припухлость, по крайней мере одной из следующих групп суставов: суставов запястья, пястнофаланговых и проксимальных межфаланговых;
• симметричный артрит - сходное, однако без абсолютной симметрии, двустороннее поражение суставов (пястнофаланговых, проксимальных межфаланговых, плюснефаланговых);
• ревматоидные узелки - подтвержденное врачом наличие подкожных узелков, локализующихся преимущественно на выступающих участках тела, разгибательных поверхностях или в околосуставных областях;
• РФ - обнаружение (любым методом) повышенных титров РФ в сыворотке крови;
• рентгенологические изменения, типичные для РА: эрозии или околосуставной остеопороз, локализующиеся в суставах кистей и стоп и наиболее выраженные в клинически пораженных суставах.
Основные гр препаратов: НПВС (диклофенак 75-100 мг/сут 2р, ибупрофен 1200-3600мг/сут, ГК и и базисные противовоспалительные препараты (БПВП). «Пошаговую» (step-up) интенсификацию терапии. 1 шаг- монотерапия метотрексатом (10– 15 мг/нед с быстрым увеличением дозы до 25–30 мг/нед) или комбинированная терапия метотрексатом и стандартными БПВП всем пациентам с РА при отсутствии противопоказаний. Селективные БПВП: лефлуномид (20 мг/день) или сульфасалазин (3-4 г/день) при наличии противопоказаний для назначения метотрексата. Низкие (менее 10 мг/сут) дозы ГК используют в качестве так называемой "bridge"-терапии*, т.е. от момента обращения больного к врачу до того момента, когда начнут действовать базисные противовоспалительные препараты, особенно если НПВП не купируют симптомы. +фолиевая кислота на фоне лечения метотрексатом, Кальция и Вит D.
ГИБП: ингибиторы ФНО-a (инфликсимаб, адалимумаб), анти- В клеточный препарат – ритуксимаб (РТМ, 500 мг 2р/сут), и блокатор рецепторов интерлейкина 6 – тоцилизумаб. Применение ГИБП рекомендуется при недостаточной эффективности (умеренная/высокая активность заболевания), монотерапии мметотрексатом или комбинированной терапии МТ и другими БПВП, которые должны применяться в адекватных дозах в течение ≥ 3-х месяцев. Препаратами выбора являются ингибиторы ФНО-a, которые обладают сходной эффективностью и токсичностью Для увеличения эффективности терапии и снижения иммуногенности ряда препаратов, ГИБП целесообразно сочетать с применением метотрексата.
22. Подагра. Клиническая картина. Купирование острого приступа подагры. Профилактика заболевания.+
Подагра – ревматическая патология, вызванная отложением кристаллов солей мочевой кислоты – уратов в суставах, затем в почках. Клиника подагры характеризуется рецидивирующими и прогрессирующими приступами артрита с интенсивными болями и формированием тофусов – подагрических узелков, приводящих к деформации суставов. В дальнейшем поражаются почки, может развиться мочекаменная болезнь и почечная недостаточность.
Симптомы
приступ острого подагрического артрита. внезапное начало, чаще в ночные часы. спровоцирован алкоголем, жирной пищей, травмой, переохлаждением. резчайшими болями в области плюснефалангового сустава 1-го пальца стопы, фебрильным синдромом, опуханием сустава, гиперемией кожи над ним, нарушением функции сустава.
При длительном анамнезе подагры и гиперурикемии высокой степени появляются специфические признаки - тофусы или подагрические узелки, представляющие собой скопление кристаллов уратов в мягких тканей. Излюбленными участками локализации тофусов служат ушные раковины, подкожная клетчатка предплечий, локтей, пальцев рук, стоп, голеней, бедер. Во время приступов подагры тофусы могут вскрываться с выходом наружу беловатого отделяемого.
Диагностика
Общий анализ крови - нейтрофильный сдвиг лейкоцитарной формулы влево, нарастание СОЭ.
биохимический анализ крови - повышенное содержание мочевой кислоты.
На рентгенограммах костей - внутрикостные кистовидные образования различных размеров, обусловленные тофусами. эрозии в субхондральной зоне кости или кистовидные образования с чёткими контурами (симптом "пробойника")
Для взятия суставной жидкости проводят пункцию сустава. Микроскопический анализ синовиальной жидкости - микрокристаллов урата натрия.
биопсии тофусов, - кристаллы мочевой кислоты.
УЗИ почек - уратные конкременты.
Лечение
диета. контролировать вес. ограничение солевой нагрузки и прием достаточного объема жидкости.
Для купирования приступов используются НПВП (индометацин), растительные алкалоиды (колхицин), местные мази и гели. Для активизации выведения мочевой кислоты - назначение урикозурических препаратов - азапропазон. средства, ингибирующие продукцию мочевой кислоты - аллопуринол.
23. Антифосфолипидный синдром. Этиология. Клинические проявления. Методы диагностики. Принципы лечения.
Антифосфолипидный синдром - аутоиммунная патология, в основе которой лежит образование антител к фосфолипидам, являющимся главными липидными компонентами клеточных мембран.
Причины
на фоне вирусных и бактериальных инфекций (гепатита С, ВИЧ).
при злокачественных новообразованиях, приеме лекарственных средств (психотропных препаратов, гормональных контрацептивов), отмене антикоагулянтов. генетической предрасположенности
Симптомы
тромботическую васкулопатию.
рецидивирующие венозные тромбозы. Венозные тромбозы в 2 раза чаще артериальных.
мигрень, судорожный синдром, нейросенсорную тугоухость, деменцию, психические нарушения.
инфаркта миокарда, артериальной гипертензии. поражение клапанов сердца – стеноза или недостаточности.
протеинурию, острую почечную недостаточность.
гепатомегалия, желудочно-кишечные кровотечения, портальная гипертензия, инфаркт селезенки.
ладонной и подошвенной эритемой, трофическими язвами, гангреной пальцев; асептическими некрозами костей.
тромбоцитопения, гемолитическая анемия.
Патология беременности
Диагностика
выявление в плазме крови титров Ат к кардиолипину класса IgG/IgM и волчаночного антикоагулянта.
мониторинге показателей свертывающей системы крови, УЗИ плода и допплерографии маточно-плацентарного кровотока. УЗДГ сосудов. ЭхоКГ.
Лечение
предотвращение тромбоэмболических осложнений. физическую активность, отказ от долгого нахождения в неподвижном состоянии.
назначение непрямых антикоагулянтов (варфарина), прямых антикоагулянтов (гепарина), антиагрегантов (ацетилсалициловой кислоты). глюкокортикоиды, плазмаферез.
24. Анкилозирующий спондилоартрит. Клинические проявления. Оценка активности воспалительного процесса. Принципы лечения.+
Анкилозирующий спондилоартрит- это хроническое воспалительное заболевание позвоночника и суставов с прогрессирующим ограничением движений.
Симптомы
Начинается постепенно. слабость, сонливость, раздражительность, слабые боли в суставах и мышцах.
боль и ощущение скованности в поясничном отделе позвоночника. Симптомы возникают ночью, усиливаются к утру, уменьшаются после горячего душа и физических упражнений.
боли распространяются вверх по позвоночнику. Физиологические изгибы позвоночника сглаживаются.
суставы позвонков срастаются, межпозвонковые диски окостеневают.
сакроилеит (воспаление суставов крестца).
поражения сердечных тканей (миокардит). поражаются ткани глаз, развивается ирит, иридоциклит или увеит.
Диагностика
рентгенологическое исследование, МРТ и КТ позвоночника. общий анализ крови - повышение СОЭ. выявления антигена HLA-В27.
Лечение
глюкокортикоиды и нестероидные противовоспалительные препараты, лечебные блокады. иммунодепрессанты. образ жизни и специальные физические упражнения.
25. Геморрагический васкулит. Этиология, клинические проявления, критерии постановки диагноза. Принципы лечения.+
Геморрагический васкулит – васкулит, характеризующийся отложением в стенках мелких сосудов (артериолах, капиллярах, венулах) IgA-содержащих иммунных комплексов с характерными симметричными геморрагическими высыпаниями, артритом, абдоминальным синдромом и гломерулонефритом.
Причины
Инфекционные заболевания.
Лекарственная терапия.
Аллергическая отягощенность.
переохлаждение, избыточная инсоляция, укусы насекомых, травмы. на фоне сахарного диабета, злокачественных опухолей
Симптомы
начало острое, внезапное, с повышением температуры, слабостью, недомоганием
кожный синдром – мелкопятнистая симметричная склонная к слиянию геморрагическая сыпь
расположена на разгибательной поверхности верхних и нижних конечностей, на ягодицах, реже – на туловище
геморрагических пузырей, язв
суставной синдром – симметричное поражение крупных суставов, преимущественно нижних конечностей (коленный, голеностопный) с отеком, болью, ограничение функции, но без костных изменений
артрита с миалгией и отеком нижних конечностей
абдоминальный синдром – болей в животе по типу кишечной колики, в мезогастрии, , тошнотой, рвотой
желудочно-кишечное кровотечение с дегтеобразным стулом
почечный синдром – гломерулонефрит, ХПН
легочной синдром - кашель со скудным количеством мокроты, кровохарканье, одышка
геморрагический плеврит
поражение сердца - геморрагический перикардит
поражение ЦНС - головные боли, головокружения, плаксивость, раздражительность, менингеальные симптомы, эпилептиформные припадки.
Диагностика
В общем анализе крови - лейкоцитоз и небольшое повышение СОЭ), увеличение количества тромбоцитов и эозинофилов.
Биохимический анализ крови - увеличение иммуноглобулина А и СРБ.
результаты коагулограммы. Отсутствие данных за нарушение свертывания.
В анализе мочи - гематурия, протеинурия, цилиндрурия.
анализ кала на скрытую кровь.
УЗИ, УЗДГ сосудов.
Биопсию с гистологией. - иммуноглобулина А и ЦИК.
Лечение
гипоаллергенную диету
дезагрегантов (пентоксифиллина) и активаторов фибринолиза (никотиновой кислоты). гепарин.
НПВС, ГКС
плазмаферез, иммунодепрессанты
Нефрология
1. Клинические и лабораторные критерии нефротического синдрома. (2)+
Клинические проявления НС:
- жалобы на общую слабость, быструю утомляемость, недомогание, головные боли, отсутствие аппетита, отеки, жажду, сухость во рту, малое количество выделяемой за сутки мочи, неприятные ощущения или тяжесть в поясничной области
- больные малоподвижны, адинамичны, кожа бледная, при выраженном НС сухая, волосы теряют блеск, выпадают
- отеки значительно выражены в области лица, стоп, голеней; появляются на стопах в конце дня или на лице по утрам, затем распространяются на все тело, локализуясь в зависимости от положения тела; отеки наиболее выражены в областях с самым высоким внутрисосудистым гидростатическим давлением (лодыжки и стопы) и самым низким тканевым гидростатическим давлением (ткани гениталий, периорбитальная зона); общий отек может сопровождаться полостными отеками (асцит, гидроперикард, гидроторакс)
Диагностика НС:
1. ОАМ: массивная протеинурия (более 3,0-3.5 г/сут), могут встречаться эритроцитурия, лейкоцитурия, цилиндрурия (гиалиновые, зернистые, восковидные), двоякопреломляющие липиды; олигурия с высокой плотностью мочи (до 1030-1040), с развитием ХПН снижается.
2. ОAK: гипохромная анемия, увеличение СОЭ до 50-60 мм/ч.
3. БАК: гипопротеинемия, гипоальбуминемия (альбумин иногда до 30-35 г/л), повышение 2- и -глобулинов; гиперлипидемия (уровень ХС иногда до 26 ммоль/л), сыворотка имеет хилезный вид (молочно-белого цвета); увеличение уровня креатинина, мочевины; гипокальциемия, гипокалиемия
4. Коагулограмма: признаки гиперкоагуляции
5. Проба Реберга-Тареева: СКФ снижена, канальцевая реабсорбция повышена.
2. Хроническая болезнь почек. Этиология. Классификация. Вопросы диагностики и тактики ведения пациентов в практике врача терапевта+
ХБП - это персистирующее в течение трех месяцев или более поражение органа вследствие действия различных этиологических факторов, анатомической основой которого является процесс замещения нормальных анатомических структур фиброзом, приводящий к его дисфункции.
Критерии ХБП:
1.Повреждение почек 3 месяцев, определяемое как структурные или функциональные нарушения почек с наличием или без снижения СКФ, которое проявляется одним из признаков:
изменения мочи или визуальных тестов, морфологические нарушения.
или
2.СКФ <60 мл/мин/1,73 м² в течение ≥3 месяцев с наличием или без признаков повреждения почек.
Основные факторы риска:
Предрасполагающие: пожилой возраст, семейный анамнез
Инициирующие: СД, АГ, иммунные заболевания, системные инфекции, инфекции мочевых путей, МКБ, обструкция нижних мочевыводящих путей, нефротоксичные препараты
Прогрессирования: АГ, гипергликемия, дислипидемия, курение,выраженная протеинурия
Модифицируемые: диабет, АГ, аутоим заб, хрон восп/систем инф, инфекции и конкременты мочевых путей, , обструкция нижних моч путей, лекарств токсич, дислипидемия, табакокурение, беремен, гипергомоцистеинемия.
Немодиф: пожилые, мужской пол, исходное низкое число нефронов, расовые и этнич особ, семейный анамнез.
-
Стадия
Характеристика
СКФ
мл/мин/1,73 м²
Рекомендуемые мероприятия
1
Повреждение почек
с нормальной или
СКФ
≥ 90
Лечение основного заболевания,
замедление темпов СКФ, сниже-
ние риска сердечно–сосудистых
заболеваний.
2
Повреждение почек
с легким СКФ
60 – 89
+ оценка скорости прогрессиро-
вания.
3
Умеренное СКФ (а, б)
30 – 59
+ выявление и лечение осложне-
ний.
4
Выраженное СКФ
15 – 29
+ подготовка к заместительной
терапии.
5
Почечная
недостаточность
<15
Почечная заместительная терапия
Симптомы: слабость, потеря аппетита; диспесические расстройства; головные боли, утомляемость; наличие отеков; дизурия, никтурия. Пациенты с 1-3 стадией ХБП могут не иметь жалоб, либо предъявлять жалобы по поводу заболевания, приведшего к ХБП.
Физикально: В стадии ХБП I-III нет видимых признаков. При IV-V стадии ХПБ могут быть следующие признаки: кожа сухая, бледная, с жёлтым или «землинистым» оттенком (задержка урохромов). геморрагические высыпания (петехии, экхимозы), расчёсы при зуде.
В терминальной стадии ХПН возникает «припудренность» кожи (за счёт выделений через поры мочевой кислоты).
Неврологические симптомы: уремическая энцефалопатия (в терминальную стадию возможны «порхающий» тремор, судороги, хорея, ступор и кома (кома развивается постепенно или внезапно)). уремическая полиневропатия; эндокринные расстройства (уремический псевдодиабет и вторичный гиперпаратиреоз, часто отмечают аменорею у женщин, импотенцию и олигоспермию у мужчин. У подростков часто возникают нарушения процессов роста и полового созревания); водно-электролитные нарушения. полиурия с никтурией в начальных стадиях ХБП; олигурия, отёки в V стадии ХБП; гипокалиемия в начальную и консервативную стадии (передозировка диуретиков, диарея): мышечная слабость, одышка, гипервентиляция; потеря натрия в начальную и консервативную стадии: жажда, слабость, снижение тургора кожи, ортостатическая артериальная гипотензия, повышение гематокрита и концентрации общего белка в сыворотке крови; задержка натрия в терминальную стадию: гипергидратация, артериальная гипертензия, застойная сердечная недостаточность; гиперкалиемия в терминальную стадию (при повышенном содержании калия в пище, гиперкатаболизме, олигурии, метаболическом ацидозе, а также приёме спиронолактона, ингибиторов АПФ, β-адреноблокаторов; гипоальдостеронизме, скорости клубочковой фильтрации менее 15–20 мл/мин): мышечные параличи, острая дыхательная недостаточность, брадикардия, АВ-блокада.
К лабораторным маркерам относятся протеинурия, гематурия, лейкоцитурия, цилиндрурия.
Протеинурия является ранним и чувствительным маркером почечного повреждения при многих нефропатиях. При этом основным белком мочи, как правило, является альбумин с малым молекулярным весом.
Альбуминурия. В норме у взрослых экскреция альбумина с мочой составляет <30 мг/сут. Микроальбуминурия (30–300 мг/сут) является ранним маркером повреждения почек. В связи с вариативностью альбуминурии необходимо получить не менее двух положительных тестов из трех.
Соотношение концентрации белка (альбумина) к концентрации креатинина в одной и той же порции мочи устраняет влияние изменения концентрации мочи, которые в равной мере воздействуют на концентрацию в моче белка и креатинина.
При выявлении микрогематурии требуется исключить инфекцию мочевых путей, а у пациентов после 40 лет – рак почки. Если микрогематурия сопровождается протеинурией и снижением СКФ, то высока вероятность гломерулярного или сосудистого поражения почек.
Повреждение почек может проявляться также клинико–лабораторными синдромами:
нефротический синдром – протеинурия >3,5 г/сут, гипоальбуминемия, гиперлипидемия, отеки;
нефритический синдром – гематурия, эритроцитарные цилиндры, протеинурия >1,5 г/сут, отеки, АГ;
тубулоинтерстициальный синдром – снижение плотности мочи, электролитные нарушения, протеинурия <1,5 г/сут.
Визуальные маркеры повреждения почек определяются при инструментальном исследовании:
ультразвуковое исследование – изменение размеров почек, повышение эхогенности, объемные образования, камни, нефрокальциноз, кисты
компьютерная томография – обструкция, опухоли, кисты, камни пузыря и мочеточников, стеноз a. renalis
изотопная сцинтиграфия – асимметрия функции, размеров почек
Оценка функции почек В общетерапевтической практике функция почек обычно оценивается с помощью следующих методов:
Cкорость клубочковой фильтрации. o Расчетные формулы. o Клиренс креатинина.
Креатинин плазмы крови.
Цистатин С.
Формула Кокрофта-Голта СКФ мл/мин= (140 - Возраст) х Вес х Коэффициент (0,85 ж; 1 м)// 0,814 х Креатинин сыворотки (мкмоль/л)
Лечение: Для пациентов с ХБП 1-3 стадиями - замедление прогрессирования ХБП путем лечения основного заболевания, приведшего к ХБП, предупреждение и лечение осложнений ХПН. Для пациентов с ХБП 4-5 стадиями - подготовка к заместительной почечной терапии, проведение адекватной диализной терапии: от начала вводного диализа до достижения целевых показателей, лечение осложнений ХПН и диализной терапии.
Тактика: Контроль гипертензии с достижением АД <130/80 мм рт. ст. Применение ингибиторов ангиотензинпревращающего фермента (ИАПФ) или блокаторов рецепторов ангиотензина II (БРА). Контроль гликемии у пациентов с диабетом, добиваясь HbA1c <7%. Отказ от курения.
ИАПФ, которые снижают внутриклубочковую гипертензию и гиперфильтрацию, расширяя выносящие артериолы клубочков. В случае непереносимости БРА. При дислипидемии с повышенным уровнем холестерина липопротеинов низкой плотности показано назначение статинов. Для устранения задержки жидкости применяют тиазидовые диуретики однократно при 1–3 стадиях ХБП, петлевые диуретики 1–2 раза с сутки при 4–5 стадиях. При выраженных отеках возможна комбинация тиазидовых и петлевых диуретиков. Для лечения примнемии применяют препараты железа из расчета 200 мг элементарного железа в сутки в течение 6 месяцев. Развитие ПН характеризуется гиперкалиемией вследствие снижения почечной экскреции калия. Поэтому рекомендуется исключение продуктов, богатых калием (бананы, курага, цитрусовые, изюм, картофель). В тех случаях, когда гиперкалиемия угрожает полной остановкой сердца (>6,5 ммоль/л) вводят внутривенно в течение 5 минут 10 мл 10% раствор глюконата кальция или 10 ед инсулина в 60 мл 40% глюкозы или бикарбонат натрия 8,4% 40 мл. Для лечения гипокальциемии и профилактики гиперпаратиреоза назначают карбонат кальция 0,5–1 г внутрь 3 раза в сутки с едой, а при неэффективности – активные метаболиты витамина D (кальцитриол). Внастоящее время существуют три метода заместительной терапии больных, имеющих терминальную стадию ПН: гемодиализ, перитонеальный диализ и трансплантация почки.
Стадии |
План действий |
1 - 2 |
Коррекция сердечно-сосудистых факторов риска (АГ, дислипидемия, курение, ожирение, гипергликемия, низкая физическая активность) |
3 |
СКФ каждые 3 месяца ИАПФ и/или БРА Избегать нефротоксичных препаратов Коррекция дозы медикаментов |
4 |
Консультация нефролога Подготовка к диализу или трансплантации |
5 |
Диализ или трансплантация |
Наличие факторов риска развития ХБП - Регулярный скрининг ХБП, мероприятия по снижению риска ее развития (первичная профилактика)
С1 Диагностика и этиотропное лечение основного заболевания почек Коррекция общих патогенетических факторов риска ХБП с целью замедления темпов ее прогрессирования Диагностика состояния сердечно-сосудистой системы и коррекция терапии Контроль факторов риска развития и прогрессирования сердечнососудистых осложнений
С2 Мероприятия по стадии 1 + Оценка скорости прогрессирования и коррекция терапии
С3а - 3б Мероприятия по стадии 2 + Выявление, профилактика и лечение системных осложнений дисфункции почек (анемия, дизэлектролитемия, ацидоз, гиперпаратиреоз, гипергомоцистеинемия, БЭН и др.)
С4 Мероприятия по стадии 3 + Подготовка к заместительной почечной терапии
С5 Заместительная почечная терапия + Выявление, профилактика и лечение системных осложнений почечной недостаточности (анемии, нарушений водноэлектролитного, кальций-фосфатного баланса, ацидоза, гипергомоцистеинемии, БЭН)
3. Вопросы кардио-ренального континуума в практике врача-терапевта. Дифференциальная диагностики при снижении функции почек. Тактика. Принципы лечения.
КРС – это патологические взаимообусловленные состояния с вовлечением сердца и почек, развивающиеся вследствие острой или хронической дисфункции одного из органов с последующей острой или хронической дисфункцией другого.
КРС 1-го типа (острый кардиоренальный) – это внезапное, острое ухудшение сердечной деятельности, которое приводит к острому повреждению почек (ОПП). КРС 1-го типа встречается при остром коронарном синдроме в 9-19% случаев. Острая декомпенсация ХСН осложняется ОПП в 24-45% случаев. Клинические и лабораторные проявления ОПП как правило развиваются в первые 4 суток (50% случаев) или в течение 7 суток (70-90% случаев).
КРС 2-го типа (хронический кардиоренальный) характеризуется наличием у пациента ХСН, которая с течением времени приводит к формированию и прогрессированию хронической болезни почек. Частота ХБП среди пациентов с ХСН может составлять 45-63, 6% и является плохим прогностическим фактором сердечно-сосудистой смерти.
КРС 3-го типа или острый ренокардиальный синдром включает в себя первичное и острое нарушение функции почек в результате острого гломерулонефрита, пиелонефрита или острого канальцевого некроза. В свою очередь ОПП вызывает сердечную недостаточность, аритмию и ишемию миокарда. ОПП наиболее часто встречается у пациентов, находящихся в отделениях интенсивной терапии (35%).
КРС 4-го типа характеризуется ХБП, которая приводит к ХСН. Частота распространённости ХБП, во всём мире в течение последнего времени увеличивается и достигает 10-15%. В настоящее время основной причиной ХБП является сахарный диабет, артериальная гипертензия, атеросклероз и ожирение, то есть заболевания, которые наиболее часто встречаются в развитых странах. Риск смерти у пациентов с ХБП от сердечно-сосудистых заболеваний увеличивается в 10-20 раз по сравнению с пациентами без ХБП.
КРС 5-го типа (вторичные кардиоренальные) – это сочетание кардиальной и почечной патологии в результате острого повреждения, при котором нарушение функции одного органа влияет на функцию другого органа. Наиболее часто КРС 5-го типа развивается у септических пациентов. Сепсис является наиболее частым состоянием, которое вызывает нарушение функции миокарда и почек.
Диагностика
При хронических синдромах, трудно определить хронологический порядок вовлечения органов в порочный круг кардиоренальных взаимодействий. Даже в одном клиническом наблюдении в разные временные периоды заболевания возможна взаимная трансформация синдромов (например, КРС 1-го и 2-го типов). Сложен дифференциальный диагноз острого кардиоренального и ренокардиального синдромов при ОПП, ассоциированном с кардиохирургическими вмешательствами. Неоднозначно место АГ в системе кардиоренальных отношений. Развивающаяся дисфункция сердца и почек в зависимости от ситуации может быть отнесена к КРС 5-го (при эссенциальной АГ), 4-го (олигонефрония) или 2-го (клапанные пороки сердца) типа.
Наиболее ранним маркером, обнаруживаемым в крови и моче пациентов с ОПП, служит ассоциированный с нейтрофильной желатиназой липокалин, появление которого опережает повышение уровня креатинина на 48–72 ч.
Значимость определения цистатина С превосходит таковую креатинина в диагностике почечной дисфункции; этот показатель коррелирует с длительностью и тяжестью ОПП, потребностью в заместительной почечной терапии и госпитальной летальностью при операциях на сердце. Повышение уровня цистатина С в сыворотке крови является маркером снижения СКФ, а в моче указывает на канальцевую дисфункцию.
Молекула почечного повреждения – белок, обнаруживаемый в моче после ишемического или токсического повреждения проксимальных канальцев, служит высокоспецифичным маркером ишемического ОПП. Молекула KIM-1 наряду с высокочувствительным NGAL представляет собой важный биомаркер ранних стадий ОПП.
Повышение уровня провоспалительного цитокина интерлейкина-18 в моче также специфично для острой ишемии почечной ткани и не характерно для нефротоксического повреждения, ХБП и инфекции мочевых путей.
Экскреция лизосомального фермента N-ацетил-β-d-глюкозаминидазы с мочой является чувствительным и ранним качественным и количественным маркером канальцевого повреждения. Одновременное исследование 3 биомаркеров (матриксной металлопротеиназы-9, NAG и KIM-1) в моче у больных после кардиохирургических операций повышает чувствительность метода.
При диагностике КРС 1-го и 3-го типов обнаружение острого повреждения миокарда обычно не вызывает затруднений. НУП (BNP, NT-proBNP) являются признанными маркерами ОСН и ОД ХСН, а также независимыми предвестниками сердечно-сосудистых событий и смертности от любой причины как в общей популяции, так и среди пациентов с почечной недостаточностью. Отмечается отрицательная корреляция NT-proBNP с уровнем СКФ, хотя в присутствии ОСН эта связь становится менее сильной.
Тропонины используются в качестве чувствительных маркеров некроза миокарда. Однако повышение уровня тропонинов наблюдается и у пациентов с ХБП без клинической симптоматики ОКС и обусловлено, по-видимому, как снижением их клиренса, так и возможным повреждением миокарда в условиях уремии. Повышенный уровень тропонинов ассоциируется с увеличением смертности при ХБП и имеет прогностическое значение при КРС 4-го типа.
Маркером нарушения метаболизма кардиомиоцитов, окислительного стресса и воспаления, особенно при ОКС, является миелопероксидаза. Определенное значение как в ранней диагностике КРС, так и в патогенезе этого состояния играют провоспалительные цитокины (фактор некроза опухоли-α, ИЛ1, ИЛ6), способствуя повреждению и апоптозу кардиомиоцитов, повреждению миокарда при ишемическом ОПП.
Маркерами почечного повреждения при КРС 2-го типа выступают появление и нарастание МАУ и протеинурии, уровня С-реактивного белка, снижение СКФ.
Неблагоприятные сердечно-сосудистые исходы у пациентов с ХБП (КРС 4-го типа) ассоциируются с повышением уровня в плазме крови тропонинов, асимметричного диметиларгинина (ADMA), ингибитора активатора плазминогена 1-го типа (PAI1), гомоцистеина, НУП, СРБ, сывороточного амилоидного белка А, альбумина, модифицированного ишемией.
Принципы лечения
Оптимальная терапия одинакова для сердечно - сосудистой и почечной защиты и включает в себя соответствующие изменения образа жизни, такие как физическая активность и отказ от курения, достижение адекватно контролируемого АД, уровня липидов в крови, HbA1с и массы тела.
Фармакотерапия состоит из применения ингибиторов АПФ или блокаторов ангиотензиновых рецепторов в максимально переносимой дозе, как правило, в сочетании с другими антигипертензивными препаратами, в частности, блокаторами кальциевых каналов и диуретиками при повышенном АД, и антидиабетической терапией у больных сахарным диабетом.
Использование статинов является обязательным, так же, как и использование аспирина при ХПЗ. Новые формы терапии добавляются по мере прогрессирования нарушений функции почек, такие как фосфат-связующие вещества, добавки витамина D (в том числе аналогов рецепторов витамина D) и эритропоэтин.
4. Хроническая болезнь почек. Вопросы диагностики. Тактика врача терапевта.+
5. Дифференциальная диагностика и врачебная тактика при нефротическом синдроме.+
Нефротический синдром – – клинический синдром, характеризующийся тяжелой протеинурией >3,5г/1,73м2 /сут, гипоальбуминемией, гиперлипидемией и отеками
Дифференциации требуют заболевания, которые протекают с выраженным отечным синдром: НС, цирроз печени, застойная хроническая сердечная недостаточность (ХСН)
Нефротический синдром с появления отеков на лице, на ногах (дни, недели). Может принимать волнообразное течение с эпизодами спонтанного схождения отеков, отеки мягкие, от минимальных до анасарки, легко перемещающиеся в зависимости от положения тела.
Гиперазотемия -Транзиторная на фоне активности НС, нарастает в зависимости от срока давности болезни б/х Гипопротеинемия, гипоальбуминемия, гиперхолестеринемия
оак Ускоренное СОЭ, при аутоиммунных заболеваниях может быть анемия, тромбоцитопения, лейкопения, протеинурия 3, 5 г/сут.
Цирроз печени- с постепенного появления асцита, Наличие вирусного гепатита – В, С, злоупотребление алкоголем, протеинурия- не характерна, гиперазотемия- при развитии гепато-ренального синдрома, чаще при преренальной ОПП, бх- Гипопротеинемия, гипоальбуминемия, Гиперферментемия (АЛТ, АСТ, ГГТП), гипербилирубинемия, тромбоцитопения
Застойная ХСН- Постепенное нарастание отеков на нижних конечностях (месяцы, годы), Одышка, утомляемость, отеки –плотные, на нижних конечностях с трофическими изменения кожи, гиперхолестеринемия, повышение гематокрита, снижение СОЭ, Снижение ФВ <60%, диастолическая дисфункция, признаки ГЛЖ
Тактика лечения/ведения(ликвидация экстраренальных симптомов+достижение частичной ремисси ;): Немедикаментозное лечение: Режим: • свободный, дозированная физическая активность по 30минут 5 раз в неделю. • ограничение употребления натрия хлорид (поваренной соли) < 1-2г/сут Медикаментозное лечение: Фуросемид 1-3мг/кг/сут внутривенно однократно болюсно или Торасемид 5-10-20мг внутрь. Для пациентов с рефрактерными отеками используется комбинация петлевых и тиазидоподобных (Индапамид 2,5-5мг) диуретиков и/или калийсберегающих диуретиков (Спиронолактон 25-100мг/сут), в тяжелых случаях (риск развития нефротического криза) - комбинация диуретиков и альбумина (10%-100мл)
При отсутствии симптомов острого почечного повреждения назначаются с антигипертензивной целью ингибиторы АПФ (Периндоприл 5-20мг/сут) или БРА (Вальсартан 80-320мг/сут). При сохраняющейся гипертонии или наличии ОПП назначают блокаторы Са-каналов (Амлодипин 5-30мг/сут, Дилтиазем 90-320мг/сут, Нифедипин 10-30мг сублингвально При наличии тахикардии и/или симптомов ХСН дополнительно назначают бета-блокаторы – карведилол 12,5-50мг/сут в 2 приема внутрь. Патогенетическая терапия НС правомочна только после верификации морфологического диагноза.
6. Острое повреждение почек. Этиология. Принципы диагностики и врачебная тактика.+
Острое почечное повреждение (ОПП) – синдром стадийного нарастающего острого поражения почек от минимальных изменений почечной функции до ее полной утраты.
Под ОПП с позиции современных рекомендаций понимается наличие любого из следующих признаков:
- увеличение креатинина сыворотки крови ≥0,3 мг/дл (≥26,5 мкмоль/л) в течение 48 час или
- увеличение креатинина сыворотки крови более, чем в 1,5 раза от известного или предполагаемого в течение последних 7 дней исходного значения или
- диурез менее 0,5 мл/кг/час в течение 6 час.
ОПП диагностируется при наличии хотя бы одного из этих критериев.
Этиология и патогенез.
В зависимости от этио-патогенетического механизма выделяют 3 основных варианта ОПП:
1) преренальное ОПП – обусловлено следующими причинами:
- снижение объема циркулирующей крови (кровотечения, рвота, диарея, ожоги, приеме диуретиков);
- перераспределение объемов жидкостей организма (циррозы, нефротический синдром, острые заболевания органов брюшной полости и их осложнения);
- снижение сердечного выброса (острая митральная недостаоточность, миокардит, острый инфаркт миокарда, аритмии, хроническая сердечная недостаточность, тромбоэмболия легочной артерии, тампонада сердца, тяжелые интоксикации);
- периферическая вазодилатация (сепсис, гипоксемия, анафилактический шок);
- спазм сосудов почек при сепсисе и гиперкальциемии;
- дилатация эфферентных артериол, обусловленная действием ингибиторов ангиотензин-превращающего фермента;
2) ренальное ОПП, основными причинами которого являются:
- острый канальцевый некроз (может быть результатом некорригируемого преренального ОПП, токсического воздействия лекарственных препаратов, синдрома длительного сдавления и др.);
- окклюзия сосудов почек (возникает при двустороннем тромбозе или эмболии почечных артерий, двустороннем тромбозе почечных вен, тромбозе малых сосудов почек (атеросклероз сосудов почек, тромботическая тромбоцитопеническая пурпура, антифосфолипидный синдром, ДВС-синдром, системные васкулиты);
- острый тубулоинтерстициальный нефрит (причины - лекарственные средства, инфекционные заболевания (лептоспироз, иерсинеоз, псевдотуберкулез, сальмонеллез, геморрагическая лихорадка с почечным синдромом, туберкулез и др.), гемобластозы (миеломная болезнь, лимфопролиферативные заболевания), а также различные нарушения иммунного характера (системная красная волчанка, острое отторжение трансплантированной почки);
- острый гломерулонефрит;
3) постренальное ОПП; основные причины:
- врожденные аномалии развития мочевыводящих путей;
- нарушение пассажа мочи по мочеточникам (например, при МКБ);
- новообразования (простаты, матки, толстого кишечника и др.);
- гинекологические нарушения, затрудняющие пассаж мочи, связанные с беременностью, эндометриозом;
Клиника. Клиника ОПП неспецифична и определяется заболеванием, которое явилось его причиной.
К симптомам, связанным с ОПП, можно отнести следующие:
- тошнота, рвота, объясняющиеся прогрессированием азотемии;
- гипергидратация: пастозность, отеки подкожной жировой клетчатки;
- гиперволемия: явления левожелудочковой недостаточности вплоть до отека легких;
- множественные подкожные кровоизлияния различной локализации.
Лабораторная диагностика:
1) биохимический анализ крови: повышение концентрация креатинина, мочевины, калия, снижение натрия, кальция, фосфора, хлоридов, ацидоз, диспротеинемия, гипопротеинемия;
2) общий анализ мочи (при наличии диуреза): может быть протеинурия, лейкоцитурия, гематурия (в зависимости от причины ОПП);
3) общий анализ крови: анемия, тромбоцитопения или тромбоцитоз, лейкоцитоз или лейкопения, ускорение СОЭ.
Инструментальная диагностика:
4) УЗИ почек с допплер-исследованием проходимости почечных артерий;
5) УЗИ мочевого пузыря, предстательной железы, органов малого таза (диагностика причины ОПП);
6) в сложных диагностических случаях – КТ почек, забрюшинного пространства и органов малого таза.
Решающее значение для диагностики собственно ОПП имеет оценка уровня креатинина сыворотки крови и диуреза в динамике.
Лечение определяется причиной ОПП.
При преренальном ОПП - инфузионная терапия под контролем ОЦК (введение кристаллоидов). При наличии сосудистого шока – введение вазопрессоров в комбинации с кристаллоидами.
Лечение ренального ОПП - лечение заболевания, послужившего причиной ОПП, а также коррекция и предупреждение осложнений ОПП (гиперкалиемии, гипонатриемии, ацидоза и гиперволемии, при которой может развиваться отек легких).
Коррекция метаболического ацидоза – натрия гидрокарбонат в/в под контролем КЩС крови.
Коррекция гиперкалиемии - кальция хлорид (3-5 мл 10% в течение 2 мин) или кальция глюконат (10 мл 10% в течение 2 мин). Более продолжительный антигиперкалиемический эффект достигается инфузией раствора глюкозы с инсулином, которую следует начинать после введения глюконата кальция (40% раствор глюкозы 300 мл + 8–12 ЕД инсулина на каждые 100 мл раствора).
+Лечение постренального ОПП – максимально быстрое устранение нарушения оттока мочи.
7. Хроническая болезнь почек. Тактика врача терапевта.
Хроническая болезнь почек – это персистирующее в течение трех месяцев или более поражение органа вследствие действия различных этиологических факторов, анатомической основой которого является процесс замещения нормальных анатомических структур фиброзом, приводящий к его дисфункции.
Жалобы: слабость, потеря аппетита; диспесические расстройства; головные боли, утомляемость; наличие отеков; дизурия (покалывание при мочеиспускании), никтурия.
Диагностика ОАК - анемия, ускорение СОЭ, умеренное ↑ количества лейкоцитов, склонность к кровотечению (↓ количества тромбоцитов).
БАК - ↑ продуктов азотистого обмена (мочевина, креатинин, остаточного азота в крови), нарушение электролитного обмена (↑ уровня калия, фосфора и ↓ кальция), уменьшается общий белок в крови, гипокоагуляция (↓ свертываемости крови), ↑ в крови холестерина, общих липидов.
Анализ мочи – протеинурия, гематурия, цилиндрурия.
Проба Реберга - для оценки выделительной функции почек - скорость клубочковой фильтрации (СКФ).
Инструментальные исследования:
УЗИ почек - уменьшение размеров почек, уплотнение и истончение паренхимы;
артериография (при подозрении на стеноз почечной артерии).
каваграфия (при подозрении на восходящий тромбоз нижней полой вены).
биопсия почек
сцинтиграфия
Общие принципы лечения:
Лечение сопутствующих заболеваний.
Профилактика сердечно-сосудистых осложнений путем ведения здорового образа жизни: отказ от курения и систематическая физическая нагрузка.
Контроль приема нефротоксических препаратов.
Противодействие инфекциям путем проведения прививок
Контроль артериального давления.
Использование ингибиторов ангиотензинпревращающего фермента (иАПФ) или блокаторов рецептора ангиотензина II (БРА).
Ограничение употребления белка с пищей.
Контроль гипергликемии у пациентов с СД.
Прекращение курения.
Контроль дислипидемии
плазмоферез. гемодиализ. трансплантации почки.
8.Дифференциальная диагностика и врачебная тактика при нефротическом синдроме.+
Нефротический синдром – клинико-лабораторный симптомокомплекс, проявляющийся выраженной протеинурией (более 3,5 г/сутки), гипоальбумиемией и отеками
Частыми факультативными компонентами нефротического синдрома (но не обязательными) являются:
- гиперхолестеринемия, дислипопротеинемия;
- активация факторов коагуляции (гиперфибриногенемия);
- нарушение фосфорно-кальциевого обмена (гипокальциемия,гипокальциурия, остеопороз);
- иммунодепрессия.
Артериальную гипертензию, гематурию не относят к проявлениям нефротического синдрома.
Классификация.
По происхождению:
1) приобретенный: первичный и вторичный.
2) наследственный;
3) врожденный.
Первичный нефротический синдром является следствием первичных заболеваний почек (хронический гломерулонефрит в 80% случаев),
вторичный – многих заболеваний, при которых почки вовлекаются в патологический процесс вторично. Вторичный нефротический синдром может возникать при следующих заболеваниях:
I. Поражение почек при системных заболеваниях:
1) амилоидозе;
2) сахарном диабете (при диабетической нефропатии);
3) системной красной волчанке, ревматоидным артрите;
4) геморрагическом васкулите;
5) подостром инфекционном эндокардите;
6)парапротеинемиях (множественная миелома, болезнь легких цепей, смешанная криоглобулинемия);
II. Инфекционные заболевания:
1) бактериальные (стрептококковая инфекция, сифилис, туберкулез, сепсис);
2) вирусные (гепатиты В и С, ВИЧ);
3) паразитарные инвазии (малярия, токсоплазмоз, шистоматоз).
III. Поражение почек лекарственными средствами:
1) препараты золота, висмута, ртути;
2) пеницилламин;
3) препараты лития;
4) НПВС;
5) антибиотики и противотуберкулезные препараты;
6) противоподагрические препараты;
7) вакцины и сыворотки.
IV. Опухоли:
1) лимфогранулематоз и неходжкинские лимфомы;
2) солидные опухоли.
V. Другие причины:
1) тромбоз почечных вен;
2) морбидное ожирение;
3) беременность;
4) хроническая сердечная недостаточность;
5) хроническая трансплантационная нефропатия.
По чувствительности к стероидной терапии:
1) стероидочувствительный;
2) стероидорезистентный.
По течению:
1) острый;
2) рецидивирующий;
3) персистирующий;
4) прогрессирующий.
Острым считается нефротический синдром (НС), формирующийся впервые. Рецидивирующий (эпизодический) НС характеризуется чередованием ремиссий и обострений заболевания с возвращением в период обострения признаков НС. Персистирующий вариант встречается примерно у половины больных с НС и характеризуется стабильным упорным течением, несмотря на проводимую терапию. Прогрессирующий (быстропрогрессирующий) нефротический синдром характеризуется быстрым (в течение 1-3 лет) развитием хронической почечной недостаточности.
План обязательного обследования всех больных с впервые развившимся нефротическим синдромом:.
3)общий анализ крови. В большинстве случаев за счет гиповолемии наблюдается повышение гематокрита, а соответственно и относительное количество всех форменных элементов крови и гемоглобина. Если в анализе наблюдается панцитопения необходимо подумать в первую очередь об аутоиммунных заболеваниях (СКВ). Лейкоцитоз может свидетельствовать об инфекционных или нагноительных процессах.
4) общий анализ мочи. Наблюдается протеинурия более 3 г/сутки, мочевой осадок большей частью представлен эритроцитами. Если мочевой осадок скуден, а высокая протеинурия имеет упорное стабильное течение можно заподозрить амилоидоз (необходимо изучить анамнез, УЗИ (гепатоспленомегалия), сделать биопсию)
5) суточная потеря белка.
6) биохимический анализ крови (креатинин, мочевина (оценить функцию почек), общий белок и белковые фракции, холестерин и В-липопротеиды, АСТ, АЛТ, калий, натрий, кальций). При гломерулонефрите общий белок снижен, в белковых фракциях снижены альбумин и гамма-глобулины, повышены альфа2- и бета- глобулины. Повышение гамма-глобулинов наблюдается при коллагенозах, амилоидозе, миеломной болезни. Если общий белок нормальный или повышен можно подумать о миеломной болезни (трепанобиопсия).
7) сахар крови.
8) коагулограмма (тенденция к гиперкоагуляции). Кроме того её нужно исследовать перед назначением гепарина.
9) иммуноглобулины крови.
11) ЭхоКГ
12) ФГДС – исключение рака желудка, перед назначением гепарина и преднизолона необходимо убедиться, что у больного нет язвы или эрозии желудка.
13) УЗИ органов брюшной полости, почек, органов малого таза – исключение объемных образований.
14) ФГ легких – исключение туберкулеза легких, абсцесса, рака.
Гематология
1. Дифференциальный диагноз анемического синдрома. Врачебная тактика. (2)+
Анемия - это патологическое состояние, характеризующееся снижением содержания гемоглобина и количества эритроцитов в единице объема крови.
По этиопатогенетическому признаку выделяют 3 основные группы анемий:
1. Анемии вследствие кровопотери (постгеморрагические).
2. Анемии вследствие нарушения кровообразования (железодефицитные, В12 (фолиево)-дефицитные и др.
3. Анемии вследствие повышенного кроверазрушения (гемолитические).
гипохромная (железодефицитная);
нормохромная (гемолитическая, постгеморрагическая);
гиперхромная (витамин В12-дефицитная, фолиеводефицитная)
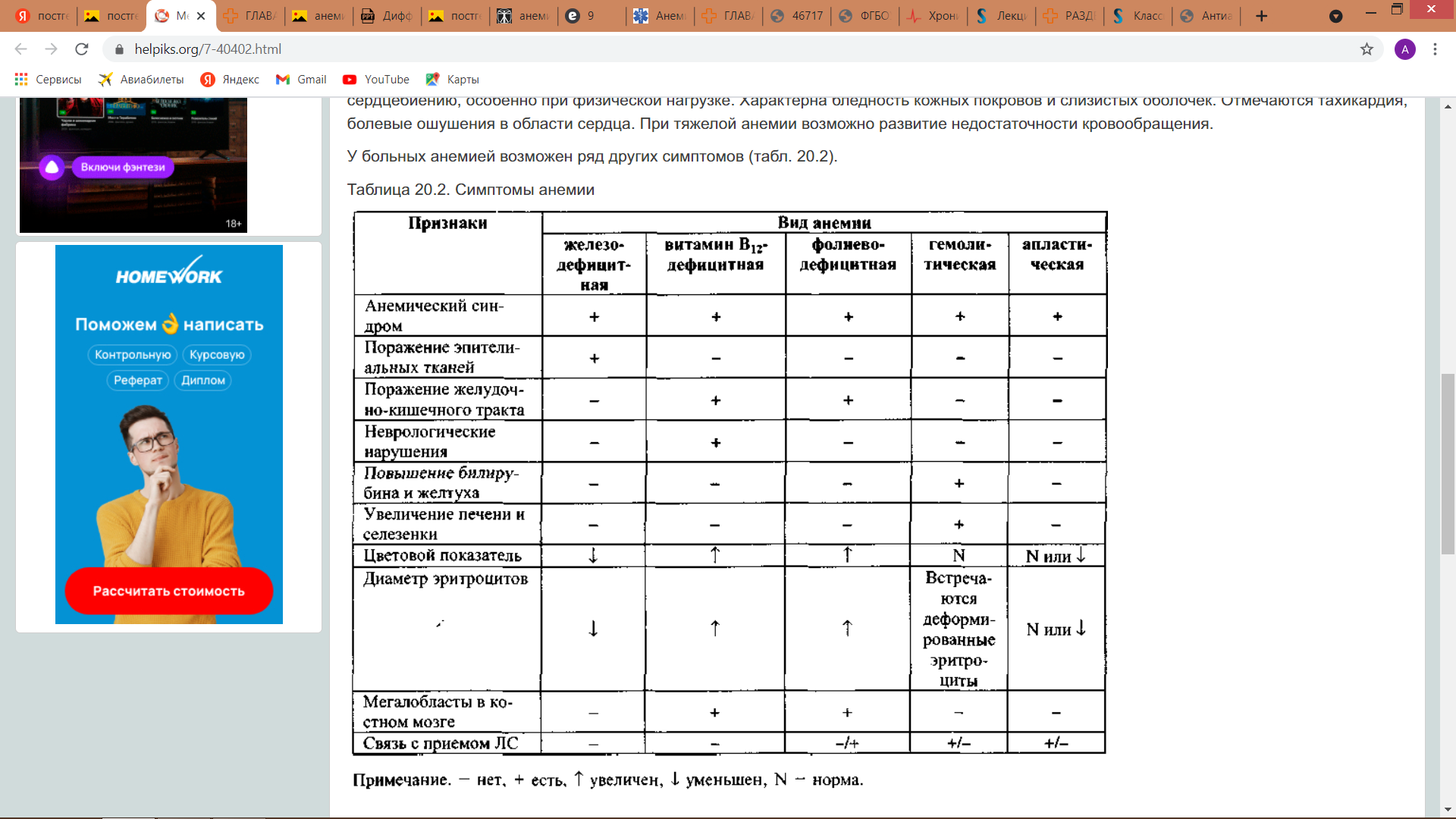

Общие симптомы анемий:
Слабость, повышенная утомляемость, снижение работоспособности, раздражительность, сонливость
Головокружение, головные боли, шум в ушах, мелькание "мушек" перед глазами,
Сердцебиение при небольшой физической нагрузке или в покое
Одышка при небольшой физической нагрузке или в покое
Клинический анализ крови
Принципы лечения:
- устранение этиологических факторов (лечение основного заболевания)
- диета
- витамины
Дифференциальный диагноз анемического синдрома. Врачебная тактика.
По патогенетическому признаку анемии делят следующим образом:
I. Анемии вследствие кровопотери (острые постгеморрагические анемии).
II. Хронические анемии.
1. Анемии вследствие нарушения кровообразования:
а) железодефицитные
б) В12-(фолиево-)дефицитные (мегалобластные анемии).
2. Анемии вследствие повышенного кроверазрушения (гемолитические):
а) наследственные гемолитические
б) приобретенные гемолитические
3. Анемии при хронических заболеваниях (АХЗ).
4. Апластические анемии.
Дифференциальный диагноз гипохромных анемий:
Гипохромные анемии делятся на 2 основные группы:
а) протекающие с недостаточностью железа (железодефицитные или сидеропенические)
б) протекающие с нормальным или повышенным содержанием сывороточного железа (железонасыщенные или сидероахрестические)
Клинический критерий ЖДА: наличие или отсутствие на фоне общеанемического синдрома клинико-лабораторных признаков дефицита железа ("сидеропенического синдрома”), подтверждающие критерии: снижение содержания железа в сыворотке крови, повышение общей железосвязывающей способности сыворотки, снижение коэффициента насыщения трансферрина железом, снижение содержания ферритина сыворотки. В случае диагностических затруднений для дифференциации ЖДА и железоахрестических анемий проводят пробу с десфералом: после в/м введения 500 мг десферала у больных с ЖДА выделяется с мочой за сутки менее 0,6 мг железа, а у больных с железонасыщенной анемией - 5 - 10 мг и более.
Дифференциальный диагноз гиперхромных анемий:
Гиперхромные анемии делятся на 2 основные группы: а) мегалобластические и б) макроцитарные.
Дифференицально-диагностический критерий: наличие в костном мозге мегалобластов (тогда идет дифференциация между В12- и фолиеводефицитными анемиями) или их отсутствие (тогда идет дифференциация между анемиями при при хронических заболеваниях печени, поджелудочной железы, почек; воздействия препаратов мышьяка, золота, лучевой терапии, хронических инфекциях, некоторых формах апластических анемий)
Дифференциальный диагноз В12- и фолиеводефицитной анемий:
Признак |
Дефицит витамина В12 |
Дефицит фолиевой кислоты |
Возраст |
Пожилой |
Любой |
Гистаминорезистентная ахилия |
Часто |
Редко (может иметь место понижение желудочной секреции) |
Полнота, одутловатость лица |
Характерно |
Нехарактерно |
Глоссит |
Характерно |
Крайне редко |
Фуникулярный миелоз |
Часто |
Не наблюдается |
Назначение витамина В12 |
Повышает уровень ретикулоцитов в периферической крови |
Не влияет на уровень ретикулоцитов в периферической крови |
Назначение фолиевой кислоты |
Повышает уровень ретикулоцитов в периферической крови |
Повышает уровень ретикулоцитов в периферической крови |
Содержание фолиевой кислоты в сыворотке и эритроцитах |
В сыворотке часто повышено, в эритроцитах незначительно снижено или в норме |
Понижено |
Наличие метилмалоновой кислоты в моче |
Характерно |
Отсутствует |
Дифференциальный диагноз нормохромных анемий: нормохромные анемии могут быть следствием острой кровопотери, ускоренного гемолиза эритроцитов, поражения костного мозга (апластические анемии) и др. Для дифференциального диагноза используются клинические критерии (общеанемический синдром, острота которого определяется степенью кровопотери; при аплазии + признаки панцитопении) и лабораторные критерии (изменение шокового индекса Альговера: ЧСС/САД, уровень гемоглобина в крови, ретикулоцитоз и др.)
На основании клинического анализа крови, выполненного на современных гематологических анализаторах, можно провести лишь первичную дифференциальную диагностику АС в отношении железодефицитного состояния: нормоцитарная нормохромная анемия с нормальным или высоким RET-HE (гемоглобин в ретикулоцитах) с большой долей вероятности свидетельствует об АХЗ. Микро-, нормоцитарная гипохромная анемия может быть как при истинной ЖДА, так и в случае истощения запасов железа при АХЗ. В плане диагностики и лечения важно дифференцировать ЖДА от перераспределительного дефицита железа (ДЖ) при АХЗ
При ЖДА организм теряет больше железа, чем получает из пищи, или же поступление железа не удовлетворяет потребность организма в нем. Снижается содержание железа в сыворотке и депо, нарушается образование гемоглобина (HGB), развивается микроцитарная гипохромная анемия [10, 11]. У всех больных ЖДА необходимо активно выявлять источники скрытой кровопотери. Женщины страдают значительно чаще мужчин.
8. Множественная миелома. Критерии постановки диагноза. Врачебная тактика. (2)+
Миеломная болезнь - это опухоль, характеризующаяся злокачественным ростом плазматических клеток, секретирующих моноклональный патологический иммуноглобулин, с поражением костей и частым развитием нефропатии.
В течение ряда лет больные могут отмечать лишь увеличение СОЭ. В дальнейшем - слабость, недомогание, похудание, боли в костях
Диффузный остеопороз приводит к болям в костях, переломам.
Рентгенологически - участки разрежения костной ткани.
повышенной восприимчивостью к инфекциям, особенно дыхательных путей.
почечной недостаточности. гиперкальциемию и нефрокальциноз.
Поражение почек характеризуется протеинурией и наличием в моче цилиндров; гематурия не выражена.
Амилоидоз характеризуется отложением амилоида в мышцах (включая язык и сердце), дерме (инфильтраты), суставах (артралгии). анемия.
гиперпротеинемией - повышается вязкость крови - нарушает микроциркуляцию, в ЦНС (головные боли).
анемии и лейкопении, увеличение СОЭ, гиперпро-теинемию, гиперкальциемию.
В костном мозгу обнаруживают повышение содержания плазматических клеток. Рентгенологическое исследование костей, КТ - очаги деструкции.
биопсия костного мозга с миелограммой, трепанобиопсию
Лечение
лучевую терапию, цитостатики (мельфалан, циклофосфан). трансплантации костного мозга
