
диссертации / 63
.pdfкий кишечник превращается в источник патогенных микроорганизмов и их токсинов. Удаление источников эндотоксикоза и дезинтоксикационная тера-
пия являются одними из основных задач послеоперационного периода [10, 33]. Новиков Ю.В. и соавт. (2005) указывают на необходимость интубацион-
ной интестинальной декомпрессии в лечении постишемических расстройств
[24]. Декомпрессия кишечника с активной аспирацией его содержимого, эн-
теральная оксигенация и интралюминальное введение глюкозы, по мнению ряда авторов, не только снижают внутрипросветное давление, улучшают ге-
моперфузию кишечной стенки и удаляют источники эндотоксикации, но и защищают слизистую кишечной стенки путем активации анаэробного глико-
лиза [10, 24, 25, 199].
Противоречивы взгляды о целесообразности применения экстракорпо-
ральной детоксикации в лечении эндотоксикоза при острой окклюзии ВБА.
Так, по мнению Давыдова Ю.А. (1997), гемосорбция оказывает лишь общий детоксикационный эффект, не оказывая при этом необходимого защитного эффекта по отношению к тонкой кишке [10]. Наоборот, Новиков Ю.В. и со-
авт. (2005) утверждают, что помимо общего эффекта, гемосорбция улучшает состояние микроциркуляторного русла кишечника [24]. Противоречивы и единичны мнения, касающиеся характера послеоперационного питания па-
циентов с восстановленной проходимостью кишечной трубки и синдромом короткой кишечной петли [106, 129, 242, 243]. Так, одни авторы указывают на необходимость полного парентерального питания в течение не только раннего послеоперационного периода, но и длительное время после выписки из стационара [12, 117, 181, 201, 248]. К сожалению, по данным Wang M.Y et al. (2007), смертность от катетерного сепсиса у этой категории больных дос-
тигает 25% [248]. Существует и другое мнение, предполагающее необходи-
мость в раннем зондовом энтеральном питании. Введение специальных сме-
сей, по мнению авторов, способствует защите кишечника и снижает явления острой кишечной недостаточности у пациентов, оперированных по поводу острой окклюзии ВБА [11]. Однако, по мнению Vantini I. et al. (2004), незави-
51
симость от энтеральной поддержки может быть достигнута у 40% пациентов с кишечной недостаточностью после обширной резекции кишечника [243]. В
будущем, на смену длительному парентеральному или специальному энте-
ральному питанию у пациентов с синдромом кишечной петли и кишечной недостаточностью, должна прийти трансплантация тонкого кишечника [90, 96, 165, 166, 229, 242].
Таким образом, в проблеме диагностики и лечения острой окклюзии ВБА на сегодняшний день остается много вопросов. Так, отсутствует одно-
значный эффективный алгоритм диагностики острой окклюзии ВБА, разнят-
ся подходы к хирургической тактике и послеоперационной терапии. Однако,
появление новых методов оценки органного и тканевого кровотока, совер-
шенствование эндоскопических и эндоваскулярных технологий, прогресси-
рование методов экстракорпоральной детоксикации, фармакотерапии и трансплантации, позволяют более активно бороться за жизнь пациентов с острой окклюзий ВБА чем 10 – 30 лет назад.
52

Глава 2.
Характеристика больных. Материалы и методы исследования.
Работа выполнена на базе хирургических отделений Городской клинической больницы №12 г. Москвы за период 2007-2013 гг.
2.1. Общая характеристика больных.
Проанализированы результаты хирургического лечения 163 пациентов с острой тромботической и тромбоэмболической окклюзией непарных висцеральных артерий брюшного отдела аорты.
Возраст больных варьировал от 38 до 90 лет. Средний возраст пациентов составил 72,1±11,6 года (медиана 75 лет). Мужчин было – 55 (33,7%),
женщин – 108 (66,3%). Возрастной состав распределился следующим образом: в возрастной группе менее 40 лет было 2 (1,2%) пациентов; в группе от 41 до 50 лет – 6 (3,7%) больных; от 51 до 60 лет – 23 (14,1%) пациента; от 61 до 70 лет – 29 (17,8%) больных; от 71 года до 80 лет – 68 (41,7%) пациентов; от 81 до 90 лет – 33 (20,2%) больных и, наконец, 2 (1,2%) оперированным пациентам было более 90 лет (рис. 1).
Рисунок 1. Возрастной и половой состав пациентов.
53
Как видно из рисунка 1, большинство (n=132 или 80,9%) оперирован-
ных больных входило в состав пожилой и старческой возрастных групп: 29
больных (17,8%) были в возрасте от 61 до 70 лет, 68 (41,7%) пациентов в воз-
расте от 71 до 80 лет и 35 (21,5%) больных старше 81 года.
Все больные имели сопутствующие заболевания (табл. 1).
Таблица 1. Спектр сопутствующих заболеваний. |
|
|
|
|
|
Сопутствующие заболевания |
|
|
Нарушение ритма сердца |
66 |
(40,5%) |
ИБС: атеросклеротический кардиосклероз |
82 |
(50,3%) |
ИБС: постинфарктный кардиосклероз |
37 |
(22,7%) |
ИБС: стенокардия напряжения |
27 |
(16,6%) |
Острый инфаркт миокарда |
6 (3,7%) |
|
Гипертоническая болезнь |
111 (68,1%) |
|
Состояние после перенесенного острого наруше- |
|
|
ния мозгового кровообращения |
35 |
(21,2%) |
Острое нарушение мозгового кровообращения |
12 |
(7,4%) |
ХОБЛ, ХНЗЛ |
56 |
(34,4%) |
Сахарный диабет |
24 |
(14,7%) |
Пневмония |
6 (3,7%) |
|
Эрозивно-язвенное поражение в/о ЖКТ |
9 (5,5%) |
|
Хронический пиелонефрит |
13 |
(8,0%) |
Мочекаменная болезнь |
10 |
(6,1%) |
Желчнокаменная болезнь |
16 |
(9,8%) |
Ожирение |
6 (3,7%) |
|
Среди всех патологий доминировали заболевания сердечно-сосудистой системы. Наиболее часто встречалась ишемическая болезнь сердца (ИБС) с
ее различными проявлениями: атеросклеротическим поражением коронар-
ных артерий страдало 82 (50,3%) пациента, почти половина больных (n=66
или 40,5%) с ОНМзК имели те или иные формы нарушения сердечного рит-
ма. Артериальная гипертензия встречалась у 111 пациентов (68,1%). Стено-
кардия напряжения различных функциональных классов диагностирована в
16,6% (27 больных) случаях. Острый инфаркт миокарда (22,7%) и острое на-
рушение мозгового кровообращения (21,2%) в анамнезе имели примерно ка-
54
ждый пятый больной с ОНМзК. Хроническая артериальная недостаточность головного мозга на фоне атеросклеротического поражения магистральных артерий головы и шеи имелась у 46 (28,2%) пациентов. В острой стадии ин-
фаркта миокарда оперированы 6 (3,7%) и острейшей фазе нарушения мозго-
вого кровообращения – 12 (7,4%) больных.
Второе место по распространенности занимали хронические заболева-
ния легких – 56 пациентов или 34,4% – это различные хронические обструк-
тивные и неспецифические заболевания легочной системы. В 6 (3,7%) случа-
ях оперированные больные страдали пневмонией.
Следующими по частоте встречаемости были заболевания эндокринной системы: сахарный диабет II типа (14,7% или 24 больных), ожирение различ-
ных степеней (3,7% или 6 пациентов) и заболевания щитовидной железы
(3,7% или 6 больных).
Хроническая почечная патология (хронический пиелонефрит, мочека-
менная болезнь) имела место у 23 (14,1%) пациентов, эрозивно-язвенное по-
ражение верхних отделов желудочно-кишечного тракта до операции выявле-
но в 9 (5,5%) случаях. Хронический калькулезный холецистит диагностиро-
ван у 16 (9,8%) больных с ОНМзК.
Остальные сопутствующие заболевания (онкологическая патология,
заболевания крови, печени, суставов и другие) встречались с частотой менее
4 процентов.
Число диагностированных сопутствующих заболеваний варьировало от
1 до 6 нозологий на одного больного с ОНМзК, при этом наиболее часто встречалось 2-4 заболевания на пациента (рис. 2).
55
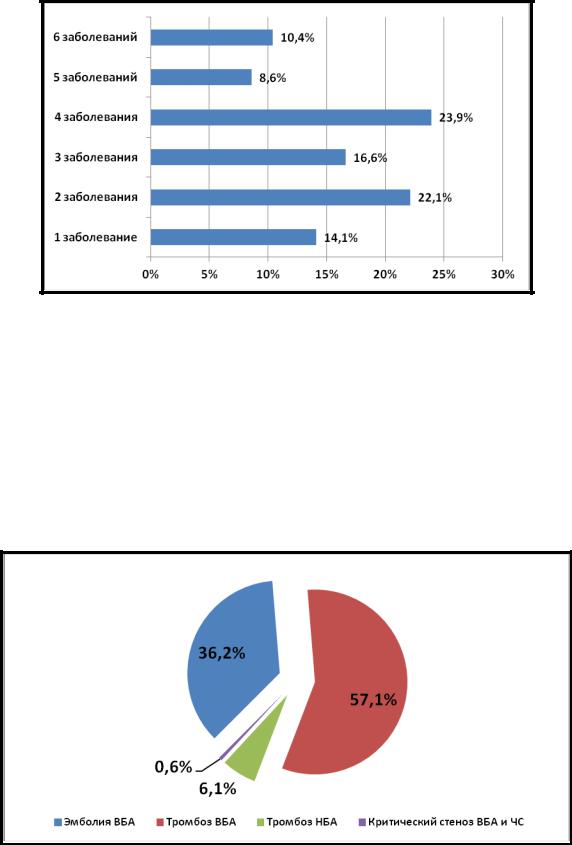
Рисунок 2. Частота встречаемости сопутствующих заболеваний
В зависимости от характера поражения ВБА все пациенты распредели-
лись следующим образом: тромбоэмболия имела место у 59 (36,2%), тромбоз ВБА – у 93 (57,1%) больных, в 10 (6,1%) случаях причиной некроза левой половины ободочной кишки был тромбоз НБА, а у одного пациента (0,6%)
причиной ОНМзК явились критические стеноз устья ВБА и ЧС (рис. 3).
Рисунок 3. Характер острой окклюзии брыжеечных артерий
56

Острая тромбоэмболическая или тромботическая окклюзия устья и проксимальных сегментов ВБА встретилась у 129 (79,1%) пациентов, а тром-
ботическая окклюзия дистальных отделов ВБА или ее интестинальных вет-
вей – в 34 (20,9%) случаях.
Большинство пациентов (155 больных или 95,1%) оперированы в ста-
дии некроза кишечника или в стадии гангрены кишечника и перитонита, в
остальных 8 (4,9%) случаях оперативное вмешательство удалось провести в стадии ишемии кишечника (рис. 4).
Рисунок 4.
Частота оперируемых пациентов с ОНМзК, в
зависимости от стадии заболевания
Объем и характер оперативных вмешательств среди 163 больных ука-
зан на рисунке 5.
Рисунок 5.
Спектр оперативных вмешательств
57
Как видно из рисунка 5, наиболее часто у пациентов с ОНМзК выпол-
нялись комбинированные вмешательства – обструктивная резекция некроти-
зированного кишечника с восстановлением магистрального кровотока в бас-
сейне ВБА и последующими программированными релапаротомиями или без таковых, данный вид операции выполнен у 59 (36,2%) больных. Изолирован-
ные резекции пораженного нероктизированного кишечника с формировани-
ем первичного межкишечного анастомоза осуществлены в 44 (27,0%) случа-
ях; изолированное сосудистое вмешательство в бассейне ВБА без резекции кишечника произведено у 8 (4,9%) пациентов. Наконец, в связи с тотальным некротическим поражением тонкой и/или толстой кишки, операция у 52 (31,9%) больных носила эксплоративный характер, ограничившись ревизией органов брюшной полости.
Помимо острой окклюзии брыжеечных артерий, у 22 (13,5%) пациен-
тов была диагностирована одновременная тромбоэмболия артерий других бассейнов: острая окклюзия магистральных артерий нижних конечностей имела место в 9 случаях, тромбоэмболия артерий верхних конечностей раз-
вилась у 3 пациентов, у остальных 10 больных при дообследовании (ангио-
графия) на предоперационном этапе или на секции выявлены тромбоэмболы в других ветвях брюшного отдела аорты – чревный ствол, почечные артерии,
селезеночная и общая печеночная артерии.
58
2.2. Методы исследования.
Всем пациентам с ОНМзК проводилось комплексное лабораторно-
инструментальное обследование.
2.2.1. Ультразвуковое исследование.
Ультразвуковые исследования органов брюшной полости выполняли на аппарате Voluson E8 Expert (GE, USA), абдоминальным датчиком с часто-
той 3,5 – 5 МГц. Ультразвуковую диагностику провели 131 (80,4%) пациен-
там, исключение составили 32 пациента, оперированных в экстренном по-
рядке с клинической картиной перитонита или пациенты, у которых также на основании клинической картины диагноз ОНМзК не вызывал сомнений.
2.2.2. Ангиографическое исследование абдоминального отдела аор-
ты и непарных висцеральных артерий брюшной аорты.
Ангиографические исследования осуществлены у 27 (16,6%) пациен-
тов, процедуру выполняли на аппарате Siemens Axiom Artis dFC (Германия).
Путем пункции по Сельдингеру правой общей бедренной артерии выполня-
лась аортография брюшного отдела, а также селективная ангиография чрев-
ного ствола, ВБА и НБА в нативном режиме и режиме субтракции с после-
дующим анализом полученных ангиограмм. Для выполнения исследований использовали неионное низкоосмолярное йодсодержащее контрастное веще-
ство Оптирей-350 (Великобритания).
2.2.3. Система для реолитической тромбэктомии AngioJet
(JET9000 MU-ULTRA).
Система для реолитической тромбэктомии AngioJet, Medrad (США) со-
стоит из консоли управления насосами сверхвысокого и низкого давления, а
также одноразовых стерильных катетеров различных диаметров (4-6 Fr), вы-
бор которых зависил от диаметра целевого сосуда. Катетер состоит из двух-
просветной трубки. Внутренний просвет, выполненный из гибкого металла, и
59
предназначен для подачи из консоли системы под большим давлением струи физиологического раствора к кончику катетера. Там раствор попадает в мик-
роскопические сопла, из которых высокоскоростные струи раствора направ-
ляются обратно, в проксимальном направлении, но уже в наружном просвете катетера. В дистальной части внешнего просвета имеются боковые отвер-
стия. Сверхвысокая скорость раствора, около этих отверстий позволяет, за счет эффекта Бернулли, создать зону разряжения. Тромботические массы подтягиваются к кончику катетера, всасываются в его просвет, и мгновенно разрушаясь, выводятся из сосуда через наружный просвет катетера. Различ-
ные типы катетеров предназначены для удаления тромботических масс из со-
судов, от 2 мм в диаметре, до магистральных артерий и вен. Для реолитиче-
ской тромбэктомии из ВБА мы использовали катетер AngioJet XVG, диамет-
ром 5 Fr и длиной 140 см. Реолитическую тромбэктомию применили у 2
(1,2%) пациентов основной группы.
2.2.4. Лазерная допплеровская флоуметрия.
Исследование микроциркуляторного русла кишечника выполняли на аппарате “Анализатор лазерный микроциркуляции крови компьютеризиро-
ванный ЛАКК-02 (исполнение 4)”, научно-производственного предприятия
“Лазма” (г. Москва, Российская Федерация). Микроциркуляцию жизнеспо-
собной тонкой и толстой кишки изучали интраоперационно во время плано-
вых полостных оперативных вмешательств (40 пациентов), микрогемодина-
мику нежизнеспособного кишечника изучали у 45 больных с некрозом тон-
кой или толстой кишки (пациенты контрольной группы и больные со стран-
гуляционной тонкокишечной непроходимостью). Видеолапароскопия в соче-
тании с ЛДФ выполнена у 32 (19,6%) больных.
2.2.5. Лапароскопическое исследование.
Видеолапароскопия применена как метод инструментальной диагно-
стики у 66 (40,5%) пациентов, исследование выполнялось на видеокомплексе
60
