
- •Физиология и биофизика возбудимых тканей.
- •Регуляция физиологических функций.
- •Физиология эндокринной системы.
- •Физиология центральной нервной системы.
- •Физиология сердечно-сосудистой системы.
- •Физиология дыхания.
- •Физиология пищеварительной системы.
- •Физиология обмена веществ и терморегуляция.
- •Физиология выделения.
- •Физиология крови.
- •Физиология сенсорных систем.
- •Физиология высшей нервной деятельности.
Физиология сердечно-сосудистой системы.
Введение.
Чем представлена сердечно-сосудистая система? Исходя из названия, сердцем и кровеносными и лимфатическими сосудами, поэтому этот раздел мы разнесём на две части: физиология сердца и физиология сосудов. Однако, помимо этого, необходимо уметь представлять, схематично изображать сердечно-сосудистую систему. Казалось бы, вопрос очень простой, но, как не странно, проблемный. Дело в том, что сердечно-сосудистая система довольно сложна и разнообразна в морфологическом плане (вены имеют клапаны, часто встречаются двойные капиллярные сети, анастамозы, существует лимфатичекская система, если всё это попытаться изобразить, то схема получится перегруженная), поэтому точно не ясно, насколько подробной должна быть схема – у каждого преподавателя свои требования. Я предложу схему простую и схему средней сложности.
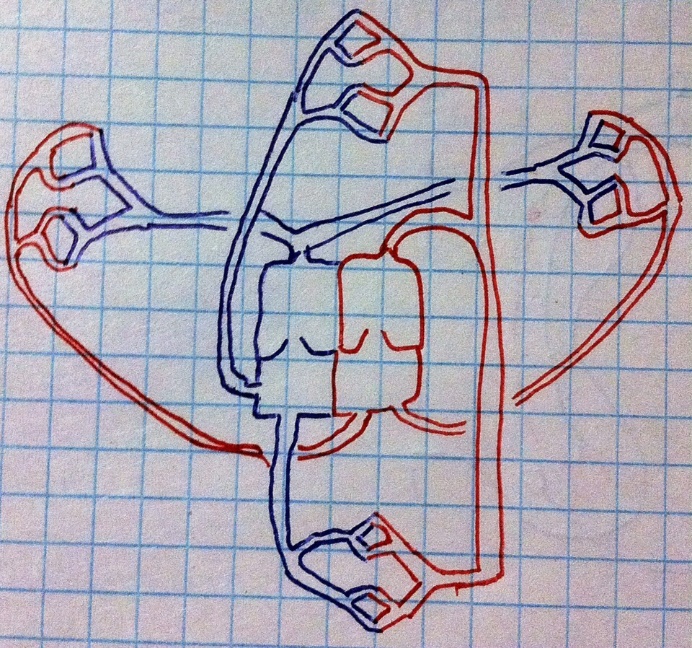
Это простая схема, здесь мы изображаем сердце с четырьмя клапанами (две предсердно-желудочковых и два полулунных), аорту с расходящимися и ветвящимися артериями, деветвящиеся вены, собирающиеся в две полые вены, лёгочный ствол ветвящийся, лёгочные артерии деветвящиеся; сердце для удобства перевёрнуто. Самое главное, знать о существовании двух кругах кровообращения – большом и малом. Большой круг кровоснабжает все ткани, несёт к ним из левого желудочка кровь, богатую кислородом (артериальную), уносит в правое предсердье кровь с углекислым газом (венозную); большой круг идёт от левого предсердия в левый желудочек, аорту, артерии, капилляры, вены и в конце полые вены. Малый круг несёт венозную кровь из правого желудочка в лёгкие, там венозная кровь становится артериальной и направляется в левое предсердье; малый круг идёт от правого предсердья в правый желудочек, лёгочный ствол, лёгочные артерии, капилляры, вены.
А вот это вторая схема.
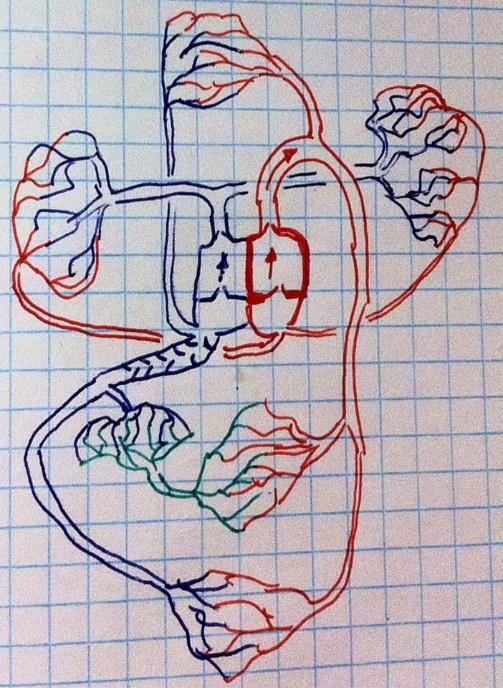
Здесь мы уточняем, что левые камеры сердца имеют более толстую стенку, некоторые вены имеют клапаны, существуют двойные капиллярные сети (кровь по венам от жкт поступает в воротную вену печени, которая сама разветвляется на артерии и капилляры, потом деветвение, образование печёночных вен, впадающих в нижнюю полую).
А каково значение кровообращения в жизнедеятельности организма? Во-первых, кровеносная система выполняет интегративную функцию, т.е. она связывает все точки организма, ибо кровоснабжаются все органы (хрящи и роговица не в счёт), поэтому по сердечно-сосудистой системе можно попасть из любой одной точки организма в любую другую, на этой функции основаны все остальные. Во-вторых, за счёт кровоснабжения из одних тканей в другие транспортируются газы, питательные вещества, токсины, конечные продукты метаболизма, биологически активные вещества (транспортно-трофическая функция). В-третьих, за счёт перераспределения крови возможна регуляция теплоотдачи. В общем за счёт кровообращения все клетки организма обмениваются друг с другом энергией, веществом и информацией – универсальный интегратор.
Физиология сердца.
Теперь перейдём к сердцу. Сердце – это полый мышечный орган. Как устроено сердце? Мы не на анатомии и не на гистологии, поэтому обсудим только те элементы, которые важны с точки зрения физиологии. По макроскопическому строению: в сердце есть 4 камеры (2 предсердья, 2 желудочка), есть 4 клапана (предсердно-желудочковые двустворчатый и трёхстворчатый и два полулунных между желудочками и сосудами), эти клапаны помогают при необходимости изолировать входы-выходы из камер, со стороны лёгочных и полых вен нет специальных клапанов, но в самих лёгочных венах и нижней полой есть свои клапаны, а в верхней полой давление выше, чем в правом предсердье, поэтому она и без клапанов обойдётся. В микроскопическом плане: есть три слоя (самый тонкий эндокард, толще эпикард, значительно больше остальных миокард), эпикард и эндокард представляют собой соединительную ткань, покрытую однослойным эпителием, а миокард представляет собой сочетание кардиомиоцитов и соединительной ткани – в итоге, получается, что сердце примерно на 70% состоит из соединительной ткани, на 30% из кардиомиоцитов. Кардиомиоциты в физиологии классифицируют на 4 группы: сократительные (типичные), элементы проводящей системы (атипичные, пейсмейкеры), секреторные, переходные. Секреторные кардиомиоциты расположены в предсердиях, при избыточном растяжении которых, эти клетки выделяют в кровь натрий-уретический гормон, который уменьшает реабсорбцию натрия в почках, тем самым переводя его из крови в мочу, а натрий за собой из крови уносит часть воды, уменьшая объём циркулирующей крови, снижая тем самым артериальное давление и, соответственно, растяжение предсердий – теперь секреторные клетки довольны и ничего не секретируют. Кардиомиоциты проводящей системы сердца генерируют ПД и распространяют его по всему сердцу в правильном порядке и последовательности. Сократительные кардиомиоциты составляют 99% всех кардиомиоцитов и отвечают собственно за сокращение сердечной мышцы. У сократительных/типичных кардиомиоцитов есть ряд особенностей. Они относятся к поперечно-полосатым мышцам, как и скелетные, но в отличии от них, представлены одноядерными клетками, а не многоядерным симпластом, кардиомиоциты типичные соединяются друг с другом вставочными дисками (особый тип межмембранного взаимодействия) и анастамозами. За счёт анастомозов цитоплазмы многих клеток сообщаются, поэтому говорят, что все типичные кардиомиоциты объединены в функциональный синцитий. Почему функциональный? А потому, что, во-первых, через анастомозы может проходить возбуждение от одной клетке другой (немного похоже по смыслу на электрический синапс, только по-другому устроен), во-вторых, через анастомозы перекидываются миофибриллы из одной клетки в другую – это позволяет сердечной мышце сокращаться объёмно, как бы сжимаясь и уменьшая объём полости сердца. Какие функции выполняет сердце? Насосную (основная, в прямом смысле качает по сосудам кровь) и эндокринную (натрий-уретический гормон предсердий).
Насосная функция для сердца является основной и заслуживает нашего внимательнейшего изучения. Сердце – это насос, но не пропеллером, а с камерами и клапанами, которые работают поочерёдно, т.е. сердце – это фазовый насос, значит, он работает по определённому циклу. Именно сердечный цикл нам и предстоит изучить. Сначала мы разберём его основы, а затем углубимся в детальную работу желудочков. При ЧСС = 75 уд/с длительность сердечного цикла составляет 0,8 с, за это время отдельно взятая камера сердца успевает сократиться (период сокращения – систола) и расслабиться (диастола). Предсердия одновременно находятся в систоле 0,1 с, а в диастоле 0,7 с. Желудочки одновременно находятся в систоле 0,33 с, а в диастоле 0,47 с. Но у предсердий и желудочков циклы несовмещённые, т.е. систола желудочков начинается тогда, когда кончается систола предсердий – циклы смещены друг относительно друга на 0,1 с.
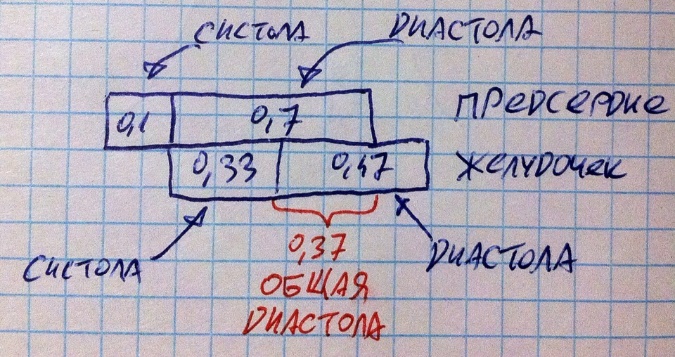
Получается, что общая систола сердца длится только 0,33 с, ибо из 0,47 с диастолы желудочков надо вычесть 0,1 с систолы предсердий. Диастола на самом деле очень важна по двум причинам. Во-первых, во время диастолы происходит наполнение кровью камер сердца, во-вторых, во время систолы сердце пережимает все свои сосуды, останавливая кровоснабжение, а в диастолу оно расслабляется и кровоснабжается. Т.е. при высоком ЧСС короче становится только диастола, в результате чего сердце не успевает нормально наполниться кровью, поэтому в каждый цикл оно выбрасывает меньше крови в сосуды, чем при нормальном ЧСС (низкая эффективность), плюс работа сердца повысилась, а кровоснабжение ухудшилось, ведь оно возможно только в диастолу – ни к чему хорошему такое противоречие не приводит. Поэтому неадекватно повышенный ЧСС не есть хорошо. Пару слов о показателях работы сердца. В диастолу желудочки наполняются кровью до предела, т.е. до максимального объёма (конечный диастолический объём КДО, примерно 140 мл), а в систолу желудочек изгоняет из себя порцию крови (систолический объём СО, примерно 60-70 мл), но всю кровь он изгнать из себя не может, поэтому в нём часть остаётся (конечный систолический объём КСО, 70-80 мл). Это статические показатели, а есть динамические – минутный объём кровотока (количество крови, которое сердце пропускает через себя за минуту), равен произведению систолического объёма на ЧСС (т.е. объём крови, выбрасываемый за раз, умножен на количество этих раз за минуту). Исходя из определения, мы понимаем, что на минутный объём кровотока МОК можно повлиять, увеличив систолический объём (увеличив силу сокращения) или увеличив ЧСС. У тренированных людей сердечная мышца толще и сильнее, поэтому она повышает СО, повышая МОК и не изменяя ЧСС. У нетренированного человека сердечная мышца не настолько сильна, чтобы заметно увеличивать СО, поэтому она увеличивает ЧСС, что менее эффективно (чуть выше мы говорили, почему).
Вот мы разобрались в общем плане насосной функции сердца, а теперь разберёмся детальной в сердечном цикле на примере левого желудочка (у правого цикл похожий, только некоторые цифры ниже, ибо он отвечает за малый круг кровообращения, а цикл предсердий для нас мало примечателен). В систоле левого желудочка есть два периода: период напряжения и изгнания; в периоде напряжения есть две фазы: фаза асинхронного напряжения и изометрического напряжения; в периоде изгнания есть две фазы: быстрая и медленная. В диастоле левого желудочка выделяют следующие периоды: протодиастолический, изометрическое расслабление, наполнение желудочка (имеет быструю и медленную фазу), пресистолический период. Для всех периодов/фаз необходимо знать их длительность, изменение объёма камеры, изменение давления в камере, состояние клапанов, наличие/отсутствие.
Фаза асинхронного сокращения в период напряжения в систолу. Желудочек полностью наполнен кровью, т.е. максимальный объём (КДО), желудочек начинает сокращаться, но так как в миокарде возбуждение и сокращение распространяются волной, то миокард сокращается не мгновенно, а быстро постепенно (асинхронно, типа часть миокарда уже возбуждена и сократилась, а часть ещё нет, но скоро будет), поэтому сокращение и названо асинхронным. В результате этого сокращения давление несколько поднимается, но остаётся в районе нуля, из-за сокращения часть крови выходит из желудочка в предсердье (объём крови поэтому немного уменьшается) и захлопывает за собой створчатый клапан, формируя первый тон сердца, однако тон возникает в конце фазы, поэтому слышаться будет во время следующей фазы. Полулунный клапан закрыт всё это время, ибо в желудочке давление около нуля, а в аорте около 80 мм рт ст (кровь давит на клапан, сохраняя его в закрытом положении). Длится фаза 0,05 с.
Фаза изометрического сокращения в период напряжения в систолу. Как мы уже сказали, в конце предыдущей фазы захлопнулся створчатый клапан и появился первый тон сердца, поэтому в фазу изометрического сокращения слышен первый тон сердца. Оба клапана закрыты (полулунный уже давно закрыт, а створчатый закрылся в конце асинхронного сокращения), поэтому объём крови в камере постоянный (ей некуда входить и выходить), но желудочек так-то сокращается, однако жидкость несжимаема, поэтому объём не меняется, т.е. длина сердечной мышцы неизменна, а напряжение растёт – изометрическое сокращение. Отсюда и название фазы. Мышца давит на жидкость, создавая в ней напряжение – объём не меняется, а вот давление растёт! И растёт оно до 80 мм рт ст, в аорте такое же давление, поэтому давление на полулунный клапан с двух сторон уровнялось, но давление в желудочке вместе с сокращением продолжает расти, поэтому клапан открывается (на этом фаза заканчивается, открытие клапана – начало следующей фазы). Длительность 0,03 с.
Быстрая фаза периода изгнания в систолу. Створчатый клапан закрыт, полулунный открылся, давление в желудочке продолжает сокращаться, поэтому давление дорастает с 80 до 120 мм рт ст, кровь выходит в аорту, поэтому объём крови в желудочке уменьшается. Длительность 0,12 с.
Медленная фаза периода изгнания в систолу. Положение клапанов то же, часть крови уже вышла, поэтому давление начинает потихоньку падать, но кровь продолжает выходить (всё медленнее и медленнее), объём уменьшается до КСО (минимальный), это продолжается до тех пор, пока давление в аорте не станет больше давления в желудочке – на этом систола заканчивается, а кровь начнёт двигаться в обратном направлении. Длительность фазы 0,13 с.
Протодиастолический период в диастолу. Давление в желудочке падает в следствие его расслабления, давление крови в аорте превышает давление в желудочке – кровь идёт обратно в желудочек, немного увеличивая в нём объём крови, но этот ток крови почти сразу захлопывает полулунный клапан, формируя 2-й тон сердца, но он формируется в конце периода, поэтому слышен будет в следующий период. В данном периоде створчатый клапан закрыт, полулунный открыт, а закрывается лишь в конце. Длительность 0,04 с.
Период изометрического расслабления в диастолу. Начинается захлопыванием полулунного клапана, поэтому слышен второй тон сердца. Оба клапана закрыты, поэтому объём камеры постоянен, длины сердечной мышцы постоянна, но она расслабляется, поэтому период назван изометрическим расслаблением. Так как идёт расслабление, давление снижается до 3-4 мм рт ст. длительность 0,08 с.
Быстрая фаза периода наполнения желудочка в диастолу. В результате расслабления желудочка давление в нём падает ниже давления в предсердье, поэтому створчатый клапан отрывается, в желудочек быстро поступает кровь и бьётся о стенки, создавая третий тон сердца (слабый), объём желудочка растёт в следствие наполнения, но давление падает. Длительность фазы 0,08 с.
Медленная фаза периода наполнения желудочка в диастолу. Клапаны в том же положении, в результате выравнивания давлений между двумя камерами кровь поступает медленнее, уже не бьётся о стенки и не создаёт тон, давление близко к нулю, объём немного увеличивается. Длительность 0,17 с.
Пресистолический период в диастолу. Сокращается предсердие, быстро наполняя желудочек кровью, та бьётся о стенки, создавая четвёртый тон сердца. Объём крови увеличивается до максимального (КДО), давление около нуля, но немного растёт из-за толчка предсердья, клапаны в том же положении. Длительность 0,1 с.

Данные приведены для ЧСС = 75 уд/мин. Для справки оценить насосную функцию сердца нам позволяет УЗИ сердца (эхокардиография, предоставляет двух- или трёхмерную картину сердца), тоны сердца (1 и 2) можно выслушивать стетоскопом. 3 и 4 тоны сердца можно зарегистрировать с помощью определить с помощью фонокардиографии (позволяет определить все четыре тона, если прибор нормальной чувствительности). Хотя тоны 1 и 2 несколько сложнее, так как имеют несколько компонентов. Первый тон имеет 4 компонента: клапанный (75% вклад в создание тона), мышечный, сосудистый и предсердный. Второй тон имеет 2 компонента: клапанный (большая доля тона) и сосудистый. Каждый компонент тона подразумевает ту структуру, чьи колебания создают звук, являющийся составляющей частью тона.
Мы изучили физиологию сердца на уровне целого органа (особенности насосной функции), а теперь изучим на уровне клеток и ткани. У клеток и ткани есть 4 основных физиологических свойства: возбудимость, проводимость, автоматия, сократимость. Разберём каждое из этих свойств.
Начнём с возбудимости. Обсудим потенциал действия (возбуждение), возбудимость и заодно сокращение для типичных (сократительных) кардиомиоцитов.
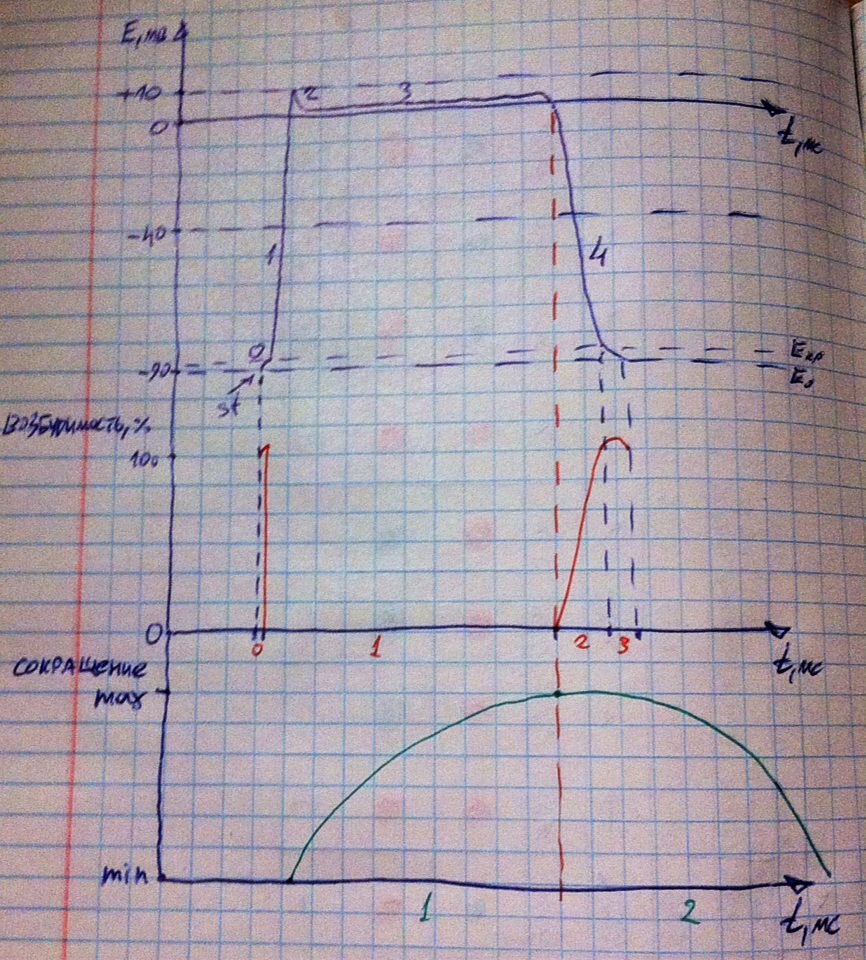
Начнём с ПД. Е-нулевое здесь равно -90 мВ, медленную деполяризацию часто не изображают, так как она крайне мала и во многих источниках не даётся конкретное значение Е-критического, тем не менее, мы обязаны хотя бы символически указать медленную деполяризацию, так как ПД не может стартовать из Е-нулевого, т.е. МПП (медленная деполяризация - 0 фаза на первом графике возбуждения/ПД), она обусловлена открытием ряда натриевых каналов. Далее следует 1-я фаза ПД – быстрая деполяризация, обусловленная открытием всех возможных каналов для натрия, что и обусловливает такое резкое изменение потенциала, но вместе с тем открываются воротные каналы для калия (здесь они особенные, более продолжительного действия) и специальные каналы, которые пропускают одновременно натрий и кальций (открываются при переходе потенциала в -40 мВ во время быстрой деполяризации), роль двух типов этих каналов не видна в быструю деполяризацию. Вторая фаза – начальная быстрая реполяризация, все просто натриевые каналы закрылись, а вот открывшиеся недавно калиевые каналы уже разогнались, ток калия через них обуславливает изменение потенциала в отрицательную сторону (клетка теряет плюсы). Третья фаза – плато ПД, обусловлена тем, что чуть позже калиевых каналов успевают разогнаться натрий-кальциевые каналы (впускают в клетку плюсы, т.е. ионы натрия и кальция, в отличии от калиевых каналов, которые выпускают плюсы в виде ионов калия), два типа этих каналов уравновешивают действие друг друга, потенциал остаётся неизменным (немного выше нуля), если все остальные фазы ПД длятся около милисекунды или меньше, то плато ПД длится до 270 мс! Четвёртая фаза – конечная быстрая реполяризация, натрий-кальциевые каналы выключаются раньше калиевых, поэтому последние берут верх и изменяют потенциал в отрицательную сторону. Следовую деполяризацию, как и медленную деполяризацию, часто не указывают, но вы имеете право это сделать – всё-таки есть Е-нулевое и Е-критическое, значит, есть медленная и следовая деполяризация. Следовой гиперполяризации нет, ибо калиевые каналы не такие «агрессивные», чтобы её создать.
Что происходит с возбудимостью? Понятное дело, что в фазу медленной деполяризации наблюдается первичная экзальтация (очень кратковременная), а вот в быструю деполяризацию (все натриевые каналы открыты – открывать больше нечего), начальную быструю реполяризацию и плато ПД (в эти две фазы мембранный потенциал выше нуля, поэтому все натриевые каналы инактивированы и не могут поддерживать возбуждение) наблюдается абсолютная рефрактерность, причём очень длительная из-за плато ПД. Потом в конечную быструю реполяризацию относительная рефрактерность (гораздо короче абсолютной) и в следовую деполяризацию экзальтация (суперкороткая), дальше ПД заканчивается, идёт покой клеток и нормальная возбудимость.
Как со всем этим соотносится сокращение? Типичные кардиомиоциты, в отличии от скелетной мышечной ткани, получают кальций не только из СПР, но и извне клетки через натрий-кальциевые каналы, поэтому ПД и сокращение начинаются почти одновременно без всяких латентных стадий, как у скелетной мышечной ткани, а дальше сокращение длится, пока в клетку входит кальций и пока она пребывает в абсолютной рефрактерности, ПД проходит стадии быстрой деполяризации, начальной быстрой реполяризации и плато ПД. Что это всё даёт? Это тройное сочетание не просто так! Из-за таких особенностей ПД мы имеем очень длинную абсолютную рефрактерность, во время которой протекает сокращение, из-за этого во время сокращения сердечной мышцы её нельзя возбудить, что исключает возможность тетанических сокращений, которые негативно сказываются на насосной функции сердца (оно должно сокращаться не слишком быстро, чтобы успевать заполнить свои камеры кровью и нормально её потом протолкнуть). Вот этот момент вы должны знать и понимать очень хорошо – это очень хитрое приспособление! Когда натрий-кальциевые каналы закрываются, абсолютная рефрактерность прекращается, мышца расслабляется в связи с прекращением поступления кальция через натрий-кальциевые каналы. Фаза расслабления на большем своём протяжении соответствует нормальной возбудимости. А что это значит? Это цель для одной из сердечных патологий – экстрасистолии. Что это такое? Это когда кардиомиоциты в фазу расслабления внезапно снова возбуждаются, сокращаются и потом расслабляются. Что служит причиной непланового сокращения? Либо есть факторы, повышающие возбудимость миокарда (подпороговые раздражители при этом могут вызвать неплановое сокращение), либо происходит рециркуляция возбуждения, когда в один участок миокарда приходит возбуждение по нормальному пути и по пути, который пошёл в обход и зашёл с тыла, он более длинный, на один участок миокарда возбуждение приходит с двух сторон. От первого сигнала миокард возбудился, сократился, начинает расслабляться, а потом внезапно стимул по проводящей системе в момент расслабления и нормальной возбудимости миокарда, которая зашла с тыла – внеплановое сокращение. А в чём проблема? На миокард регулярно с определённой периодичностью приходит стимул от проводящей системы сердца (по нормальным путям с правильными скоростями проведения), возбуждающий миокард. Когда происходит экстрасистола, из расслабления внезапно включается внеплановое сокращение, а сокращение происходит в фазу абсолютной рефрактерности, в это время на миокард приходит сигнал от проводящей системы сердца, но он полностью игнорируется – это же фаза абсолютной рефрактерности. Внеплановое сокращение переходит спустя время в расслабление, мышца расслабилась и больше не сокращается – стимулов-то больше нет, стимул от проводящий системы пропустили, поэтому ждём следующий стимул от проводящей системы, а пока ждём, сокращения нет – компенсаторная пауза (сердце не работает, ну или его участок). Надо ли говорить, что такие простои нарушают насосную функцию сердца? Очевидно (сердце просто на время перестаёт качать). Чем больше экстрасистол, тем тяжелее сопутствующие патологии и вся клиника.
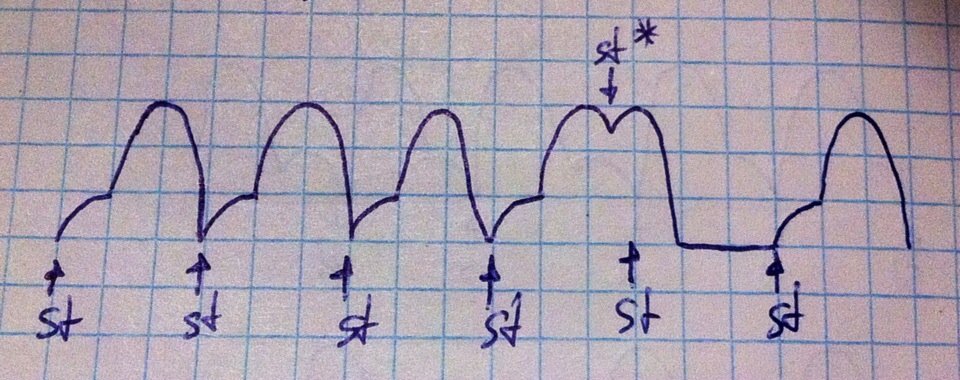
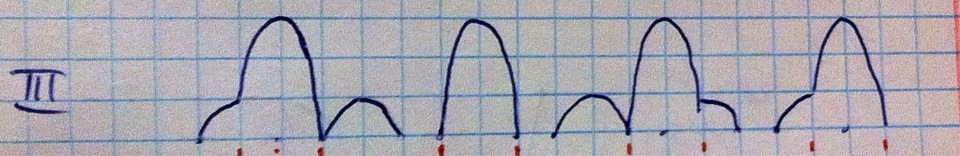
Это кардиограмма (отражает фактическое сокращение предсердий маленькой волной и большой волной желудочки, ну или желудочек в случае лягушки), снизу стимулы от проводящей системы сердца, сверху возвратный импульс и собственно экстрасистола, компенсаторная пауза, между стимулами от проводящей системой равные интервалы (3 клетки) – показатель определённого ритма возбуждений, один из импульсов игнорируется, попадая в фазу внепланового сокращения, сопряжённую с абсолютной рефрактерностью.
Вопросы автоматии и проводимости сердца нам придётся разбирать совместно, ибо они имеют большую логическую связь. Автоматия – способность клетки самостоятельно генерировать ПД без внешних воздействий. Таким свойством обладают клетки проводящей системы сердца (атипичные кардиомиоцитыони же пейсмейкеры, они же вводители ритма). Секрет автоматии кроется в её возбуждении. График ПД атипичного кардиомиоцита см. ниже.
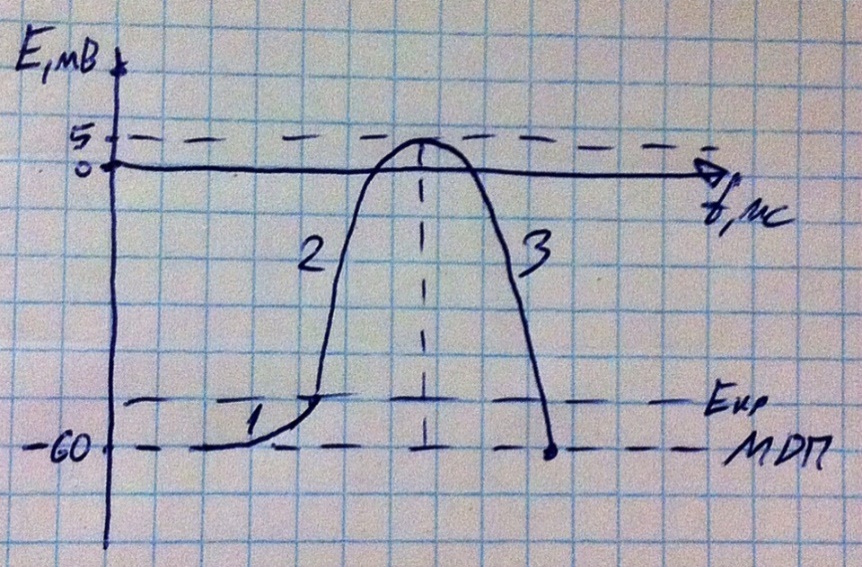
Обратите внимание: здесь не Е-критическое, а максимальный диастолический потенциал (-60 мВ), а вот Е-критическое присутствует. Первая фаза это не просто медленная деполяризация, продуцируемая обычными натриевыми каналами, а это медленная диастолическая деполяризация, продуцируемая медленными натриевыми каналами! Они довольно долго пропускают через себя натрий, поэтому позволяют сделать медленную диастолическую деполяризацию реально очень медленной (сотни милисекунд между прочим, это нужно для правильного ритма сердца). Далее при достижении Е-критического начинается быстрая деполяризация, но не за счёт входа в клетку натрия, а за счёт входа кальция, это менее быстрые и обильные каналы, чем обычные натриевые, поэтому график не крутой, примерно в это время включаются и калиевые каналы, чей эффект заметен в быструю реполяризацию (сто раз это обсуждали). А вот теперь секрет самой автоматии! Медленные натриевые каналы активируются быстрой реполяризацией! Т.е. ПД атипичных кардиомиоцитов своим окончанием включает начало нового ПД. Между ПД нет паузы – сразу после быстрой реполяризации наступает медленная диастолическая деполяризация, поэтому клетка никогда не находится в покое, поэтому к ней не применимо понятие МПП, вместо него есть лишь понятие максимальный диастолический потенциал – просто максимальное (по модулю) достигаемое значение мембранного потенциала, которое однако существует лишь мгновения. Клетки проводящей системы генерируют ПД, проводят его по миокарду, возбуждая его и заставляя его сокращаться.
Структура проводящей системы.
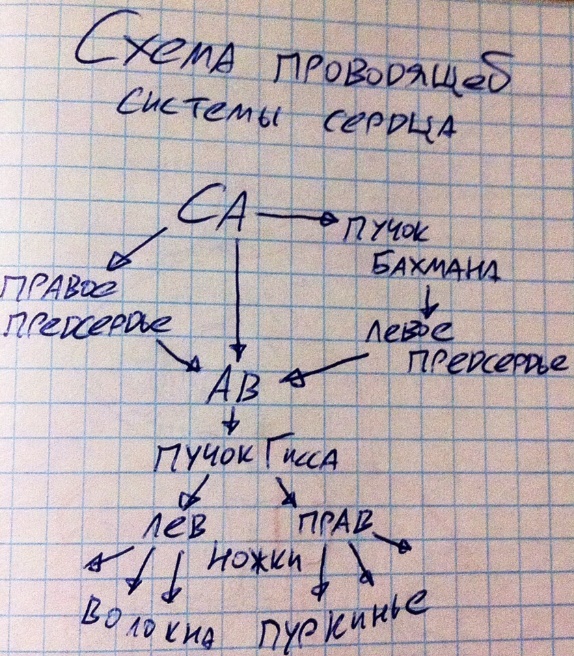
Импульсы генерируются в сино-атриальном узле (СА), по разным путям достигают атрио-вентрикулярного (АВ) узла, в нём происходит задержка (смысл чуть позже расскажу), затем сигнал идёт на пучок Гисса, его ножки, а с них по волокнам Пуркинье, которые заканчиваются на типичных кардиомиоцитах, которые кстати тоже друг на друга перекидывают возбуждение, но по Пуркинье возбуждение идёт быстрее, поэтому их и используют. Из перечисленных элементов автоматией обладают клетки СА, АВ, пучка Гисса и волокон Пуркинье. Но уровень автоматии у них разный! Уровень автоматии – средняя частота выработки импульсов (им/мин). У СА это 80 им/мин, у АВ это 40-50 им/мин, у пучка Гисса это 30 им/мин, у волокон Пуркинье это 20 им/мин. Обратите внимание: по ходу проводящей системы от начала до конца происходит снижение уровня автоматии клеток – это называется убывающим градиентом автоматии сердца. Но на деле из 4-х приведённых вводителей ритма только СА является ведущим, а остальные 3 латентные, т.е. они не генерируют импульсы, а выполняют проводниковую функцию.
Автоматию сердца легко доказать на примере лягушки: необходимо изъять из неё сердце, отсоединив его от сосудов и нервов, но сохранив венозный синус (в нём у лягушки находится СА), сердце поместить в стакан с физ раствором для лягушек (0,65% хлорида натрия) – наблюдайте сокращения.
Теперь конкретнее о проводящей функции. Разные элементы проводящей системы имеют разную скорость проведения импульса: для СА это 0,05 м/, для центральной части АВ это 0,2-0,3 м/с, а в краевой зоне АВ это 0,02-0,03 м/с (позволяет осуществлять задержку сигнала), у пучка Гисса 1-1,5 м/с, у волокон Пуркинье 3-5 м/с, а у самих типичных кардиомиоцитов 0,8-1 м/с. Желудочки имеют больший размер, поэтому нуждаются в такой широкой проводящей системе с высокой скоростью передачи. Так для чего же нужна атрио-вентрикулярная задержка? Если бы этой задержки не было, все бы камеры сокращались почти одновременно, что нецелесообразно для сердца, а вот эта самая задержка (0,1 с) позволяет сначала сократиться предсердиям, а потом уже сокращаться желудочкам, ведь задача предсердий завершить наполнение кровью желудочков, поэтому желудочкам логичнее сокращаться после предсердий.
Настало время поговорить о нарушениях проводимости. Нарушение проводимости между СА и АВ бывает частичным и полным, они приводят к АВ-блокадам сердца. Если что, СА возбуждает предсердия и пускает сигнал на АВ, а АВ является входными воротами для импульсов от СА в желудочки. При неполном нарушении проводимости между узлами возникают блокады 1-й и 2-й степени, а при полном нарушении проводимости блокада 3-й степени.
Начнём с неполных блокад.
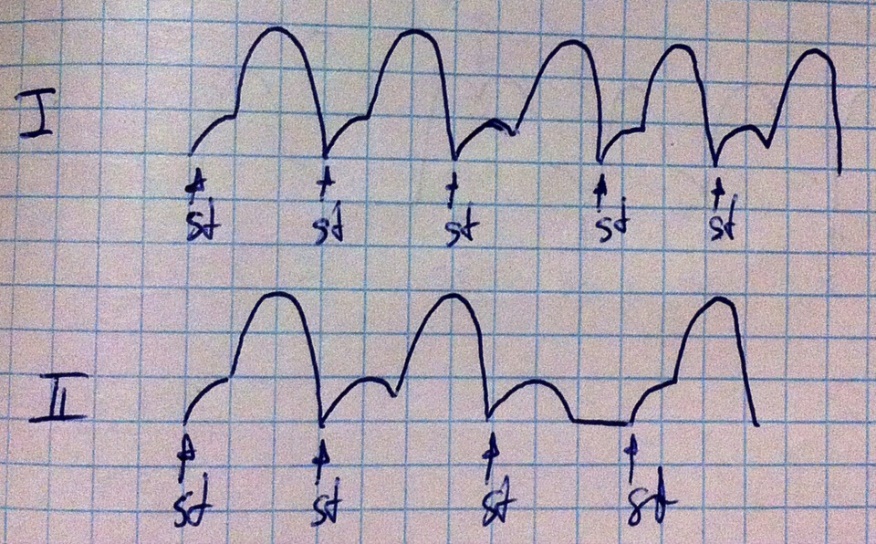
При блокаде первой степени частично нарушены проводящие пути, в следствие чего задержка атрио-вентрикулярная вырастает до 0,21 с, это сопровождается незначительными нарушениями гемодинамики, на кардиограмме (просто кардиограмме, а не электрокардиограмме, не путайте, здесь мы наблюдаем за реальными сокращениями) видим, что систола желудочка отдаляется от систолы предсердий.
При блокаде второй степени нарушения путей куда серьёзнее и время задержки превышает 0,21 с, в следствие чего (слишком большая задержка) систола желудочка просто отсутствует. Частота отсутствующих систол желудочка(ов) (если лягушка, то желудочек, если человек, то желудочки – уточняйте, ибо на физиологии нам приходится говорить и о человеке, и о некоторых животных для практических работ) бывает различной. Периодическое отсутствие систол желудочков приводит к серьёзным нарушением насосной функции сердца и гемодинамики, соотвественно (о том, что такое гемодинамика, позже поговорим ещё).
Полная блокада.
Связь между СА и АВ полностью отсутствует, поэтому на проводящую систему прекращают поступать импульсы вообще, в следствие этого АВ, который был латентным вводителем ритма, становится ведущим для желудочков, а СА остаётся ведущим для предсердий. Но у СА и АВ разный уровень автоматии, поэтому желудочки и предсердья сокращаются с разной частотой, т.е. несогласованно, поэтому систолы предсердий и желудочков могут идти перед друг другом, после, полностью накладываться – как угодно, естественно, это очень серьёзно нарушает насосную функцию сердца и гемодинамику.
При тяжёлых случаях блокады второй степени и при блокадах третьей степени очень серьёзно нарушается насосная функция сердца, а с ней и всё кровообращение, что может приводить к полиорганной недостаточности (ухудшение работы всех органов вследствие ухудшенного кровоснабжения), поэтому таким пациентам ставят электрокардиостимуляторы, согласующие работу предсердий и желудочков, причём современные электрокардиостимуляторы чувствительны кислотности среды, температуре, гормонам и не только, т.е. они могут адекватно реагировать на изменяющиеся условия среды.
Мы обсудили всё необходимое про возбудимость, проводимость, автоматию сердца, коснулись сократимости, вот её сейчас чуть подробнее разберём, а именно, отличия сократимости скелетных и сердечной мышц. Во-первых, для сокращения скелетной мускулатуры необходим кальций из СПР (не сразу выходит), а для сердечной мышцы используется кальций извне клетки (входит по натрий-кальциевым каналам очень быстро) и из СПР (это уже дополнение). Во-вторых, для скелетной мускулатуры характерно наличие латентной стадии (запускается не сразу после возникновения ПД), а у сердечной мышцы такой стадии нет (сопряжение напряжения с ПД за счёт натрий-кальциевых каналов). В-третьих, скелетные мышцы можно возбуждать и в фазу сокращения, и в фазу расслабления, поэтому для них характерны тетанические сокращения, а сердечная мышца в фазу сокращения невозбудима, ибо та совпадает с фазой абсолютной рефрактерности, поэтому в норме не бывает в сердце тетанических сокращений (ибо они нарушают насосную функцию).
Дополнительно можете сказать, что для кардиомиоцитов характерна очень низкая лабильность: если мышечное волокно способно сокращаться с частотой 200 Гц, то сердце ну 1 Гц с кепкой (помните, что частота расчитывается, исходя из лабильности), но низкая лабильность опять-таки нужна для эффективности насосной функции.
Регуляция сердечной деятельности.
Мы обсудили все основные аспекты физиологии самого сердца, а теперь поговорим о регуляции сердечной деятельности. Это вопрос довольно интересный и важный, потому что регуляция сердца обширна и разнообразно, оно постоянно изменяет свою работу в ответ на действие многих различных факторов, ибо деятельность сердца так или иначе связана с многими функциями нашего организма (по ходу изучения этого и последующих разделов вы это заметите). Как вы уже хорошо знаете, существует 3 основных метода регуляции физиологических функций: миогенный (он же физико-химический), гуморальный, нервный. Для сердца характерны и значимы все три, обсудим каждый из них.
Миогенная, она же физико-химическая, она же гемодинамическая регуляция имеет несколько механизмов, которые классифицируются на гетерометрические (возникают в ответ на изменение длины кардиомиоцита, т.е. его растяжение) и гомеометрические (возникают независимо от изменений длины кардиомиоцита). К гетерометрическим относится закон «преднагрузки», к гомеометрическим относят принцип «лестницы» и закон «постнагрузки». Разберёмся в каждом из них.
Закон преднагрузки. Он вам уже известен, мы обсуждали его в качестве примера миогенной регуляции в разделе регуляции физиологических функций. Если предсердье растягивается излишне из-за большого объёма крови в нём, то растягиваются и сами кардиомиоциты, Z-линия и M-линия отдаляются друг от друга (вспомните строение миофибрил), поэтому количество потенциально возможных мостиков между актином и миозином возрастает, от этого сила сокращения возрастает, предсердье прогоняет эту лишнюю кровь, чтобы она не переполняла его. Чем больше крови в предсердье, тем сильнее оно сокращается. Всё просто. Этот механизм имеет ограничение: слишком сильное растяжение приведёт к частичному размыканию миофибрилл, т.е. актин и миозин относительно друг друга разойдутся (потеряют контакт друг между другом) и обратно правильно встать не смогут, после этого кардиомиоцит нормально сокращаться не сможет (если актин и миозин не котактируют друг с другом, то и работать они не могут). Или, если вам будет так понятнее, приведу отдалённый пример: у вас есть шкаф, вы выдвигаете из него выдвижной ящик на 20 см, потом задвигаете обратно, потом выдвигаете на 40 см и обратно – всё просто, без проблем, но если вы выдвигаете ящик до конца и вытаскиваете его, то обратно так просто вы его уже не засунете (придётся как-то его поставить нормально на рельсы, но в кардиомиоцитах некому вставлять актин и миозин на место), вот, когда вы достали выдвижной ящик из шкафа полностью, это и было критическое перерастяжение кардиомиоцитов и миофибрилл, соответственно.
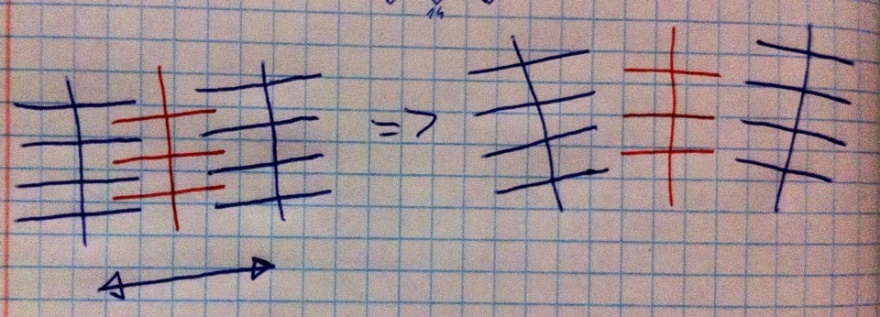
Принцип лестницы. Суть явления состоит в том, что ЧСС и сила сердечных сокращений прямо пропорциональны. Почему? Вспомните работу типичных кардиомиоцитов и тройной график для них, во время сокращения в кардиомиоцит поступает извне кальций через натрий-кальциевые каналы, кальций вносит значительный вклад в формирование ПД и одновременно активирует сокращение. В клетках работает кальциевая АТФаза, которая выкачивает кальций из клетки, а натрий-кальциевые каналы его в клетку впускают. При высокой частоте сердечных сокращений каналы открываются слишком часто и кальций начинает поступать в клетку быстрее, чем выводиться, поэтому он накапливается в клетке, а чем больше кальция в клетке, тем сильнее сокращение. Но причём тут лестница? Если вы составите график-диаграмму зависимости ЧСС от силы сокращения, то заметите, что он будет похож на лестницу.
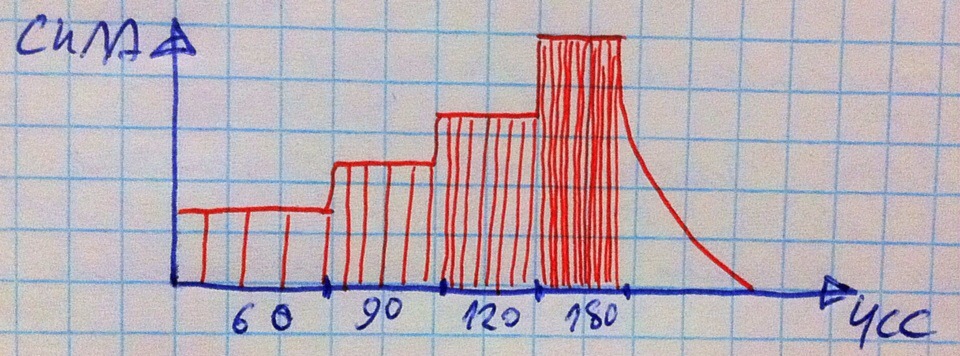
Вертикальные линии под графиком нужны для наглядной демонстрации ЧСС, и вправду получается лестница (чем чаще сердце сокращается, тем сильнее оно сокращается – спасибо накапливающемуся кальцию). Но что это за спадающая линия после? Этот механизм имеет ограничение, называемое «каменным» сердцем. Если высокая ЧСС поддерживается слишком долга и кальция становится слишком много, то миофибриллы сокращаются на максимум, т.е. все возможные актин-миозиновые мостики уже образованы, больше некуда – сердце максимально сжалось и более сокращаться не может, ибо некуда. Максимально сжатое небьющееся сердце подобно камню, отсюда и термин. Сердце перестаёт биться, но спустя некоторое время происходит его естественное расслабление и восстановление нормальной (если это так можно назвать, во всяком случае будет биться) деятельности.
Закон постнагрузки. Это медленный компенсаторный механизм. В чём он заключается? По ряду причин проход крови по сосудам может осложняться (часто причина в атеросклерозе аорты и все виды истинной артериальной гипертензии), причём не временно, а длительно (месяцы, годы), в связи с этим сердцу для того, чтобы проталкивать кровь в прежнем объёме, приходится прилагать больше усилий, ведь проталкивание крови утяжелилось, по этой причине кардиомиоциты гипертрофируются, дабы увеличить силу сокращений. Проблема на некоторое время проходит (более сильное сердце нивелирует проблему затруднённого прохождения крови по сосудам). Однако если причина затруднения прохождения крови по сосудам, например, атеросклероз аорты, не удалена, то она возрастает со временем, а сердце продолжает в ответ гипертрофироваться (кардиомиоциты набухают из-за появления новых миофибрил). Чем это опасно? Вообще каждый кардиомиоцит контактирует с одним капилляром (очень высокий уровень кровоснабжения), но при гипертрофии кардиомиоцит становится слишком большим и потребляет энергии больше обычного, кровоснабжения он требует тоже больше, но больше крови поступать не может, ибо сосудистое обеспечение миокарда развиваться больше, чем есть в норме, не может, это его предел – наступает ишемия, так как потребности кардиомиоцитов выше возможностей кровоснабжения. Плюс такое толстое сердце не может нормально сокращаться (по той же причине, по которой очень толстым людям тяжело нагибаться). Патологическая гипертрофия сердца в ответ на повышенную сопротивляемость сосудов (сложно проталкивать кровь по сосудам), приводит к нарушению насосной функции сердца и его ишемии (недостаточности кровоснабжения миокарда). Закон постнагрузки реализуется в способностях кардиомиоцитов к гипертрофии, однако гипертрофия не всегда патологическая – есть и физиологическая. У профессиональных спортсменов сердце тоже гипертрофировано, поэтому сила его сокращений выше, чем у обычного человека, и оно может повышать минутный объём кровотока при физических нагрузках не за счёт ЧСС, а за счёт увеличения систолического объёма (количество выбрасываемой крови желудочком) за счёт увеличенной силы сокращения. Но в чём разница между спортсменом и больным человеком? У здорового человека нагрузка на сердце в покое нормальная, а сердце в результате тренировок стало гипертрофированным и более сильным, поэтому для обеспечения необходимого МОК сердце сокращается сильно, но редко. А вот у больного нагрузка на сердце в покое повышенная (затруднённая проходимость в сосудах), поэтому гипертрофированное сердце бьётся сильно и часто. У здорового спортсмена гипертрофированное сердце бьётся с нормальной частотой (нагрузка-то на нём обычная), а гипертрофированное сердце больного бьётся с высокой частотой, поэтому оно нуждается в большем притоке энергии и питательных веществ, но при этом у него ухудшено кровоснабжение из-за повышенного ЧСС, т.е. оно очень голодает. Вот в этом разница, пожалуйста, почувствуйте. Примеры болезней и разница между патологической и физиологической гипертрофией это для особо сообразительных, а так достаточно знать суть механизмов и уметь их объяснить.
Теперь перейдём к нервным механизмам регуляции. По нервному механизму выделяют интракардиальную и экстракардиальную регуляцию.
Интракардиальная регуляция осуществляется метасимпатической нервной системой, т.е. её рефлекторные дуги замыкаются на уровне нервного сплетения сердца, не выходя за пределы сердца и не связываясь с ЦНС. Пример интракардиального рефлекса: чувствительный нейрон регистрирует растяжение в правом предсердье, посылает импульс на ассоциативный нейрон, тот на эфферентный, а эфферентный заставляет сильнее сокращаться левый желудочек, чтобы кровь быстрее покидала сердце и перерастяжение ушло. Только не спутайте это с миогенной регуляцией: при миогенной регуляции правое предсердье перерастягивается, в результате чего само же и начинает сильнее сокращаться, а вот при приведённом мною рефлекс перерастяжение происходит в правом предсердье, а усиливается сокращение у левого желудочка – на деле же, конечно, всё одновременно работает.
Экстракардиальная регуляция предполагает участие ЦНС, но рефлексы, реализуемые при такой регуляции, классифицируют на кардио-кардиальные, вазо-кардиальные, висцеро-кардиальные и условные в зависимости от того, где расположены рецепторы для данных рефлексов. Пару слов о рецепторах. Для кардио-кардиальных рефлексов рецепторы расположены в сердце, они регистрируют растяжение стенки сердца (А-рецепторы) и давление (В-рецепторы), примечательно, что для интракардиальных и экстракардиальных (конкретно кардио-кардиальных) рефлекторных дуг первые нейроны общие (а дальше для интракардиального сигнал идёт по нервному сплетению сердца, а для экстракардиального уходит в продолговатый мозг по другим нейронам). Для вазо-кардиальных рефлексов рецепторы установлены в сосудах (устья полых вен и лёгочные артерии – барорецепторы; дуга аорты и кародитные узлы сонных артерий – хемо- и барорецепторы). Для висцеро-кардиальных рефлексов рецепторы установлены во внутренних органах. Условные рефлексы подразумевают сложную работу коры больших полушарий и гипоталамуса, поэтому тут о рецепторах говорить не имеет смысла. Немного обсудили рецепторы, а теперь обсудим всю систему экстракардиальной нервной регуляции в целом.
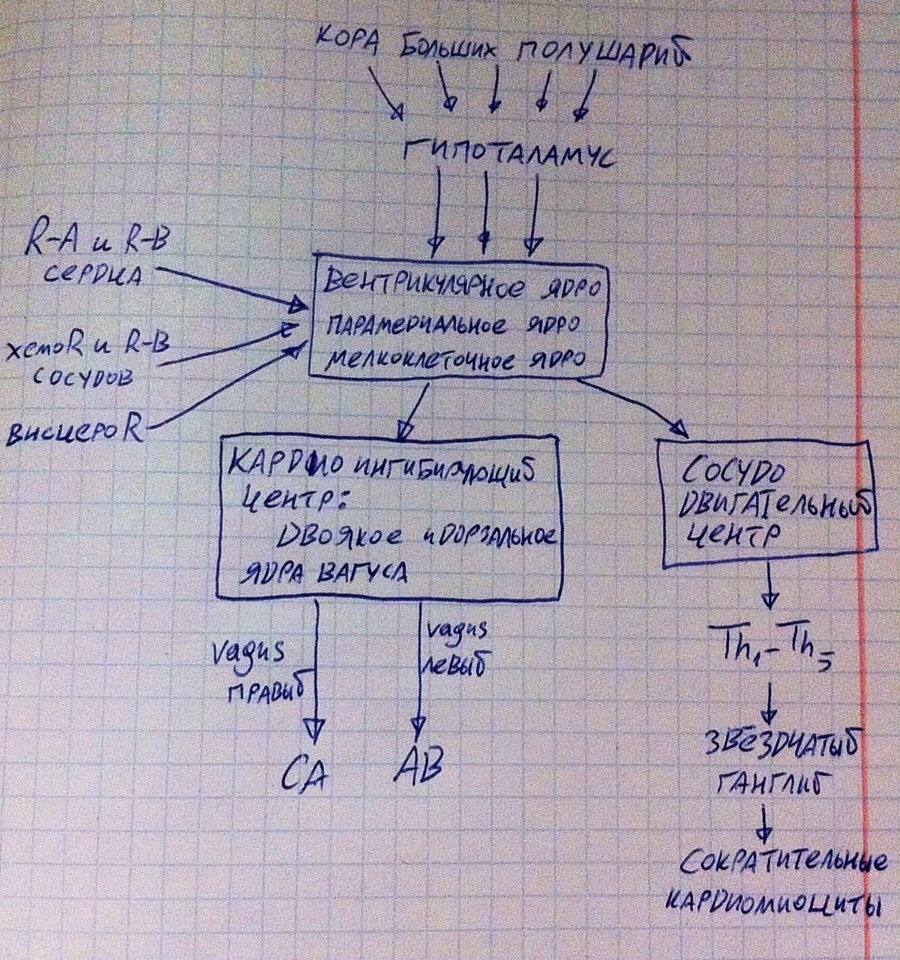
По всем экстракардиальным рефлексам информация с рецепторов сердца, сосудов и органов поступает в продолговатый мозг в вентрикулярное, парамедиальное и мелкоклеточное ядра, там она обрабатывается и направляется либо в кардиоингибирующий центр (парасимпатика), либо в вазомоторный центр (симпатический элемент). Кардиоингибирующий центр посылает сигнал по блуждающему нерву на синусы сердца, причём правый блуждающий нерв на СА, а левый на АВ. Перерезание правого вагуса приведёт к остановке сердца (будьте осторожны на операциях, так сказать). Сигналы из сосудодвигательного центра проходят несколько более сложный путь: они поступают в 1-5-е грудные сегменты спинного мозга, оттуда в звёздчатый ганглий, из него прямо на сократительные кардиомиоциты. Помимо всей этой типичной схемы, кора больших полушарий через гипоталамус вносит свои коррективы в регуляцию сердечной деятельности.
Теперь обсудим, какое же влияние оказывает симпатическая и парасимпатическая иннервация на работу сердца. Вообще эффекты, оказываемые нервами на сердце мы разделяем на 4 типа: инотропный (сила сокращений), хронотропный (время, точнее частота сокращений), батмотропный (возбудимость), дромотропный (проводимость).
Влияние парасимпатики (от кардиоингибирующего центра). Блуждающий нерв (вагус) образует нервно-мышечные синапсы с атипичными кардиомиоцитами в СА и в АВ. В этом синапсе выделяется ацетилхолин, который воспринимается М-холин-рецепторами, которые увеличивают проницаемость мембраны для калия и уменьшают проницаемость для кальция. Эти рецепторы расположены на ионотропных нервных каналах, т.е. быстро реагирующих, поэтому действие вагуса проявляется сразу, но длится оно недолго, ибо в синапсе работает ацетилхолингидролаза (разрушает ацетилхолин, чтобы тот слишком долго не влиял на клетку). Действие вагуса приводит к отрицательным ино-, хроно-, батмо- и дромотропным эффектам. Почему? Выходящий из клетки калий (ведь проницаемость мембраны для него повышена) делает мембранный потенциал более отрицательным (гиперполяризация по сути), поэтому мембрана хуже возбуждается, а при плохой возбуждаемости страдает и проводимость (проводимость – распространение возбуждения, а то, в свою очередь, страдает из-за сниженной возбудимости), сила сокращения страдает из-за уменьшенного поступления кальция в клетку (проницаемость мембраны для него ухудшилась), а частота сокращений падает, ибо СА реже генерирует ПД, так как его медленная диастолическая деполяризация стала ещё медленнее из-за действия калия. Итог: вагус выделяет на СА и АВ ацетилхолин, тот активирует М-холин-рецепторы, повышая проницаемость мембраны для калия и понижая для кальция, оказывая отрицательные ино-, хроно-, батмо- и инотропные эффекты, но действие ацетилхолина не долгое, так как есть фермент, его разрушающий. Но в примечание скажу, что при чрезмерной активности вагуса сердце может его игнорировать и выходить из-под его контроля, что вообще-то не очень хорошо.
Влияние симпатики (от вазомоторного центра). Нейроны в нервно-мышечных синапсах выделяют уже на типичные, т.е. сократительные, кардиомиоциты норадреналин, который оказывает положительные ино- и хронотропный эффекты. Как он это делает? Норадреналин действует на бета-1-адрено-рецепторы типичных кардиомиоцитов, увеличивая проницаемость мембраны для кальция и натрия, облегчая формирование ПД (теперь кардиомиоциты легче возбуждаются и могут чаще сокращаться – вот вам положительный хронотропный эффект), а ещё кальций больше поступает в клетку, поэтому и сокращение будет сильнее, ведь кальция станет больше (положительный инотропный эффект). Однако, в отличии от парасимпатики, симпатика действует с запозданием, ибо каналы для натрия и кальция метаботропные (рецептор не на самом канале, а удалён и сообщается с ним через систему вторичных посредников, поэтому задержка реакции).
В целом мы разобрались в механизме нервной регуляции, но теперь мы немного конкретизируем, разобрав конкретные примеры экстракардиальных рефлексов.
Рефлекс Бейнбриджа. Если поднимается давление в полых венах, это регистрирует барорецептор в устьях полых вен, а правое предсердье растягивается, это регистрирует А-рецептор, то они посылают сигнал в продолговатый мозг и снижают тонус вагуса (уменьшают его тормозящее действие), сердце растормаживается – наблюдаем положительные ино- и хронотропные эффекты. Обычно такое происходит при недостаточности кровообращения, поэтому кровь излишне накапливается в полых венах и правом предсердьи, раздражая в них рецепторы и вызывая этот рефлекс. Это пример кардио-кардиального рефлекса (рецепторы в сердце).
Рефлекс Парина. Увеличение давления в малом кругу кровообращения регистрируется барорецепторами в лёгочных артериях, сигнал отправляется в продолговатый мозг, тонус вагуса повышается, оказываются отрицательные ино-, хроно-, батмо- и дронотропные эффекты. Такая мера предохраняет сосуды от повреждения. Это пример вазо-кардиального рефлекса (рецепторы в сосудах) для малого круга кровообращения.
Сино-каротидный рефлекс. Увеличение давления в большом кругу кровообращения регистрируется барорецепторами в каротидных узлах сонных артерий, сигнал отправляется в продолговатый мозг, тонус вагуса повышается, оказываются отрицательные ино-, хроно-, батмо- и дронотропные эффекты. Такая мера предохраняет сосуды от повреждения. Это пример вазо-кардиального рефлекса (рецепторы в сосудах) для большого круга кровообращения.
Рефлекс Гольца. Резкие удары в брюшину активируют висцеральные рецепторы, сигнал отправляется в продолговатый мозг, тонус вагуса повышается, оказываются отрицательные ино-, хроно-, батмо- и дронотропные эффекты. Это пример висцеро-кардиального рефлекса.
Рефлекс Данини-Ашера. При надавливании на глазные яблоки активируются висцеро-рецепторы, сигнал отправляется в продолговатый мозг, тонус вагуса повышается, оказываются отрицательные ино-, хроно-, батмо- и дронотропные эффекты. Это пример висцеро-кардиального рефлекса.
Теперь об условных рефлексах, т.е. приобретённых, они являются результатом действия коры на центры регуляции сердца через гипоталамус. Простым примером может быть испуг или стресс, в результате которых повышается ЧСС. А вообще сам гипоталамус является высшим центром вегетативной нервной системы, т.е. регулирует и связывает всё, что в нас непроизвольно, а это подавляющее большинство физиологических процессов, но при этом он ещё и согласует эти процессы с произвольными нашими действиями. В общем гипоталамус так очень серьёзно действует на регуляцию сердца, внося туда множество корректив в связи с другими физиологическими процессами. И последнее, что нужно сказать по нервной регуляции, тонус парасимпатики преобладает над симпатикой, т.е. сердце тормозится постоянно. Уровень автоматии СА равен 80 им/мин, а ЧСС у нас 60-70 уд/мин – вот вам и торможение со стороны парасимпатики. Однако у людей в разном возрасте, с разным обменом веществ и многими другими факторами их нормальная ЧСС будет отличаться, поэтому не у всех людей тонус парасимпатики преобладает.
Остался третий тип регуляции – гуморальный. Гуморальных регуляторов у сердца довольно много, подавляющая часть из них активирует сердечную деятельность: адреналин, инсулин, кортикостероиды, серотонин оказывают положительный инотропный эффект, тиреоидные гормоны оказывают положительный хронотропный эффект, аденозин и кальций оказывают сразу хроно- и инотропный положительные эффекты. Среди гуморальных факторов, ингибирующих деятельность сердца можно выделить калий, который оказывает отрицательные ино-, хроно-, батмо- и дромотропный эффекты.
Электрокардиография.
Тему сердца мы завершим одним из главных методов исследования сердца электрокардиографией. Вообще ЭКГ делается во всех больничных отделениях и на всех медицинских осмотрах вне зависимости от того, кардиологическое это отделение или нет, просто ЭКГ показывает практически все заболевания сердца, поэтому использование ЭКГ для пациентов, у которых, как вам кажется, нет проблем с сердцем, необходимо, чтобы сразу исключить вариант патологий сердца (а то привезли вам пациента с проблемами кишечника, а на самом деле причина в сердце, такое бывает часто с разными болезнями, поэтому при диагностике любого заболевания применяют ЭКГ, чтобы сразу исключить сердечную патологию, ну или к удивлению своему выявить её). Электрокардиограмма – графическое описание электрической активности сердца, зарегистрированной на поверхности тела с помощью электродов в различных точках тела, что позволяет оценить пространственное распределение этой активности.
О какой электрической активности идёт речь? Сердце – это полый мышечный орган, чтобы он сокращался, необходимо, чтобы он возбудился, а возбуждение распространяется по сердцу не моментально. Что это значит? У вас возникает возбуждение в одной точке сердца, при этом кардиомиоциты вступают в медленную, потом быструю деполяризацию, заряд с -90 мА доходит до +10 мА, а потом опускается почти до нуля и замирает на какое-то время (плато потенциала действия), а другие участки сердца возбудиться ещё не успели, у них в покое -90 мА. Что получается? В одном участке сердца потенциал один (выше нуля), а в другом -90, т.е. у нас образуется разность потенциалов, которая тождественна понятию электрического тока! Хотя именно в физиологии вы учили немного другой термин – ток действия (ток, возникающий между возбуждённым и невозбуждённым участком мембраны). Как не говори, а ток есть, причём ток распространяется не по одной клетке, а по целому сердцу, т.е. ток там довольно заметный, вот этот самый ток мы регистрируем с помощью электродов электрокардиографа. Как раз вот эти токи (разности потенциалов) обусловливают появление зубцов на ЭКГ. Электрокардиограф имеет электроды (накладываются на части тела, части тела служат проводником токов, которые мы регистрируем), сигнал с электродов идёт по проводам в усилитель (регистрируемые токи по амплитуде очень малы, поэтому они усиливаются в 600-700 раз), затем усиленный сигнал отправляется в гальванометр (измеряет полученные сигналы), тот отправляет сигнал на регистратор (записывает ЭКГ на бумагу или отображает на мониторе), но ещё есть блок питания, ибо прибор работает только при подключению к источнику электрического тока.
Я говорил о том, что электрическую активность сердца регистрируют через нательные электроды, а куда именно накладываются электроды? В зависимости от наложения электродов выделяют 12 отведений.
Стандартные двухполюсные отведения, их 3. Электроды накладываются на предплечья рук и на голень левой ноги. Прибор регистрирует разность потенциалов (электрические токи) между двумя электродами. Если вы считываете информацию с электродов между руками (плюс на левой руке, минус на правой), то это первое стандартное отведение. Если вы считываете информацию между правой рукой и левой ногой (плюс на ноге, минус на правой руке), то это второе стандартное отведение. Если вы считываете информацию между левой рукой и левой ногой (плюс на ноге, минус на левой руке), то это третье стандартное отведение. Если на схеме объединить эти электроды линиями, то получится равнобедренный треугольник Эйнтховина, о смысле которого мы поговорим несколько позже.
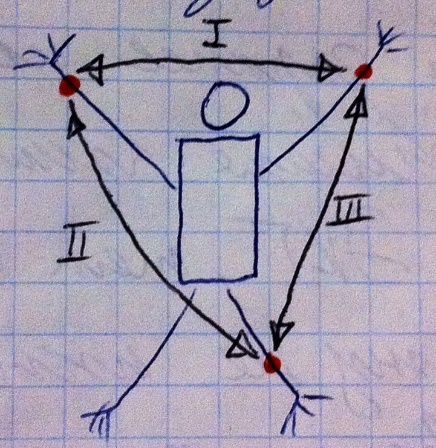
Существуют однополюсные усиленные отведения от конечностей, их тоже 3. Электроды накладываются на те же точки, что и стандартные, но здесь один электрод активный плюс, а два других электрода являются пассивными объединёнными (не будем сильно вдаваться в подробности). Если активный электрод наложен на правую руку, отведение называется aVR (right – правый), если активный электрод на левой руке, отведение называется aVL (left - левый), если активный электрод на левой ноге, отведение называется aVF (food - нога). Регистрируется колебание потенциала на одном электроде.

Ещё существуют грудные отведения, их 6. Здесь к конечностям присоединяются электроды, которые собираются в один провод (общий электрод), который подключён к минусу на приборе, а к плюсу подключён один из грудных электродов. Куда ставят грудные электроды? Первый электрод в 4-е межреберье спарва от грудины, второй электрод слева от грудины, третий на 5-м ребре по парастернальной линии, остальные электроды размещаются по 5-му межреберью, 4-й электрод по среднеключичной линии, 5-й по передней подмышечной, 6-й по средней подмышечной линии. Специально схематично изобразил грудную клетку с пронумерованными рёбрами и анатомическими линиями, где отмечены электроды красными точками (нумерация справа налево).
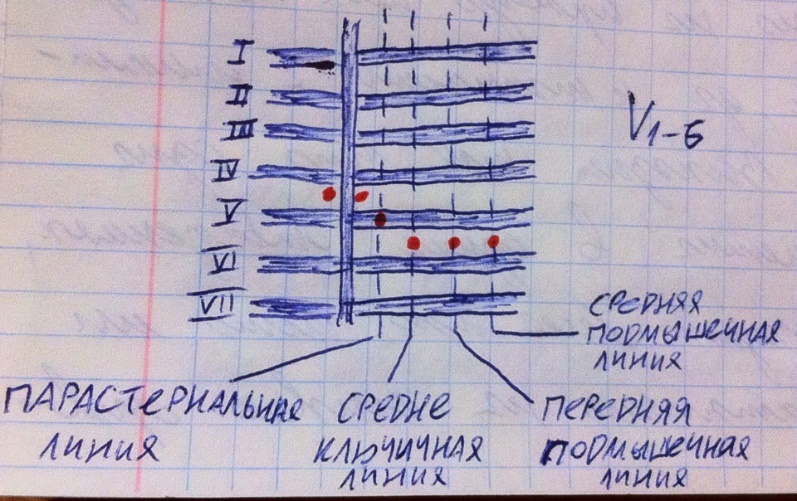
Для чего нужно так много отведений? Дело в том, что, во-первых, такое количество отведений даёт большую точность исследования, во-вторых, разные патологии отражаются в разных отведениях, поэтому для полноценного анализа электрической активности сердца нам необходимо изучить её по ЭКГ во всех отведениях. Кстати существуют и другие отведения, но эти 12 используются везде и всегда.
Небольшое примечание по снятию ЭКГ. Кожу в месте наложения электродов протирают спиртом или чем-то другим, чтобы убрать грязь и сальный секрет с кожи, ибо тот мешает проведению электрических импульсов, регистрируемых через электроды, сами же электроды тоже должны прилежать к телу достаточно плотно. Пациент должен лежать и быть расслабленным, если части тела будут свисать или он сам будет напряжён, то будут напрягаться его скелетные мышцы, которые так-то тоже имеют токи действия, которые перебьют сигналы от сердца и внесут заметные помехи на ЭКГ. Ещё прибор надо заземлять и отколибровать. Если же все скелетные мышцы в покое, электроды наложены правильно, прибор имеет заземление и отколиброван, то ЭКГ будет записана точно и без помех.
Теперь давайте разберём саму ЭКГ, её элементы, и сделаем мы это на основе ЭКГ, зарегистрированной во втором стандартном отведении.
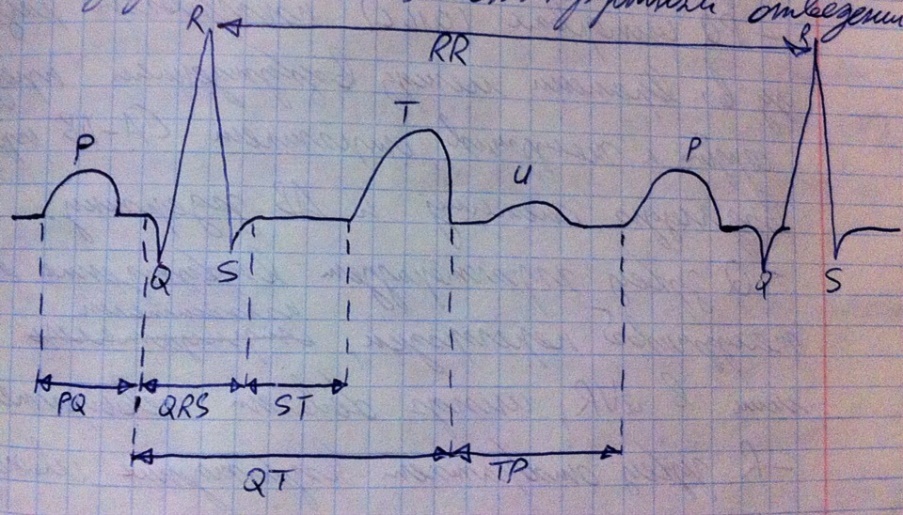
По сути ЭКГ мы представляем, как график, горизонтально отмечается время в секундах, а вертикально отмечается вольтаж в миливольтах (мы же измеряем разность потенциалов, т.е. электрические токи или токи действия). Если в сердце или его отдельных камерах все клетки имеют один потенциал, то разницы потенциалов нет, электрического тока нет, поэтому на ЭКГ мы видим изолинию (горизонтальная прямая на уровне 0 мВ). Если же происходит ситуация, что часть миокарда имеет один потенциал, а вторая часть другой (одна возбуждена, а вторая нет, ну или они обе возбуждены, но находятся в разных стадиях возбуждения), то возникает разница потенциалов, т.е. электрический ток, который приводит к формированию зубцов на ЭКГ. Изначально (на графике) сердце полностью расслаблено, у всех клеток один потенциал (МПП), поэтому на ЭКГ изолиния. Дальше начинается возбуждение предсердий, которое на ЭКГ отображено зубцом P, причём восходящая его часть характеризует возбуждение правого предсердья, а нисходящая характеризует возбуждение левого предсердья. Данный зубец в норме (почти во всех отведениях) положителен. Пока идёт вона возбуждения по предсердьям, одна часть клеток возбуждена (заряд подскакивает до +10 мВ в ходе медленной и быстрой деполяризации, а затем спускается (начальная быстрая реполяризация) почти до 0 мВ и долго остаётся на этом уровне во время плато потенциала действия), а другая нет – отсюда разница потенциалов и появление зубца на ЭКГ, потом все клетки охвачены возбуждением и сохраняют одинаковый заряд – нет разницы потенциалов, на ЭКГ отмечаем изолинию. Тем временем возбуждение ползёт по проводящей системе из СА узла в АВ узел и на желудочки (передача сигнала с предсердий на желудочки только посредством проводящей системы, а миокард этих камер не сообщается, проводящая система невелика по числу клеток, поэтому прохождение по ней импульса не отражается на ЭКГ), затем возбуждение всё-таки доходит до желудочков и те начинают возбуждаться, что на ЭКГ отмечается комплексом зубцов QRS и именно в это время происходит реполяризация (быстрая конечная) предсердий, однако её мы на ЭКГ не видим, так как возбуждение желудочков гораздо ярче и затмевает реполяризацию предсердий. Существует интервал PQ (от начала P до начала Q), который показывает, сколько времени прошло между возбуждением предсердий и желудочков, характеризует состояние проводящей системы и показывает атриовентрикулярную задержку. Зубец Q отрицателен, отображает возбуждение межжелудочковой перегородки. Зубец R положителен и имеет самую большую амплитуду, характеризует возбуждение левого желудочка. Зубец S отрицателен, характеризует возбуждение правого желудочка. Интервал QRS отображает внутрижелудочковую проводимость. Затем весь миокард желудочков возбуждён, потенциал везде одинаковый (немного выше 0 мВ) в фазу плато действия, разницы потенциалов нет – на ЭКГ изолиния, которая будет длиться до зубца T, характеризующего реполяризацию желудочков (быструю конечную), существует интервал ST между концом зубца S и началом зубца T. Возбуждение миокарда желудочков оканчивается быстрой конечной реполяризацией, которая также волной прокатывается по миокарду, создавая разность потенциалов, формируя положительный зубец T, который имеет пологую восходящую и крутую нисходящую часть. Далее следует изолиния, соответствующая полной диастоле сердца, весь миокард в покое, разницы потенциалов нет, хотя может появляться положительный зубец U, чья природа не ясна, да и появляется он очень редко. Теперь по поводу интервалов дополнительно. Интервал QT показывает полную электрическую систолу желудочков (от начала возбуждения до самого конца), а TP характеризует полную диастолу сердца (зубец U не в счёт). Интервал RR по сути показывает длительность сердечного цикла.
Нормативные значения (их вам придётся выучить наизусть увы). P, R, T зубцы положительные, Q, S зубцы отрицательные. Синусный ритм (имеется ввиду ведущий СА). Амплитуды зубцов (мВ): P = 0,05; R = 0,6-1,5; T = 0,3-0,6. Длительность интервалов (с): PQ = 0,12-0,21; QS = 0,06-0,09; QT = 0,32-0,40; RR = 0,75-1,00. ЧСС = 60-80 уд/мин. Систолический показатель (QT : RR * 100%) = 38-40%. Это для второго стандартного отведения.
А теперь давайте просто посмотрим, как выглядит ЭКГ в разных отведениях. Детально всё запоминать нет нужды, обсудим лишь основные особенности. Амплитуда R в стандартных отведениях выше всего во 2-м, средняя в 1-м и наименьшая в 3-м. по усиленным однополюсным конечностным отведениям: в aVR вся ЭКГ перевёрнута, в aVL всё с мелкой амплитудой, в aVF всё более-менее видно. В грудных отведениях принципиально, что в 1-3-м S>R (это правые грудные отведения, они прямо над правым предсердьем, поэтому его зубец проявляется ярче), в 4-м S=R (электрод где-то между влиянием правого и левого желудочка), в 5-6-м S<R (левые грудные отведения, здесь зубец левого желудочка более явный). И напоминаю, что различные патологии часто отражаются изменением некоторых зубцов, но эти изменения видны лишь в конкретных отведениях, поэтому нам важно знать, как всё должно быть в норме во всех 12-ти, чтобы потом заметить и понять патологию.
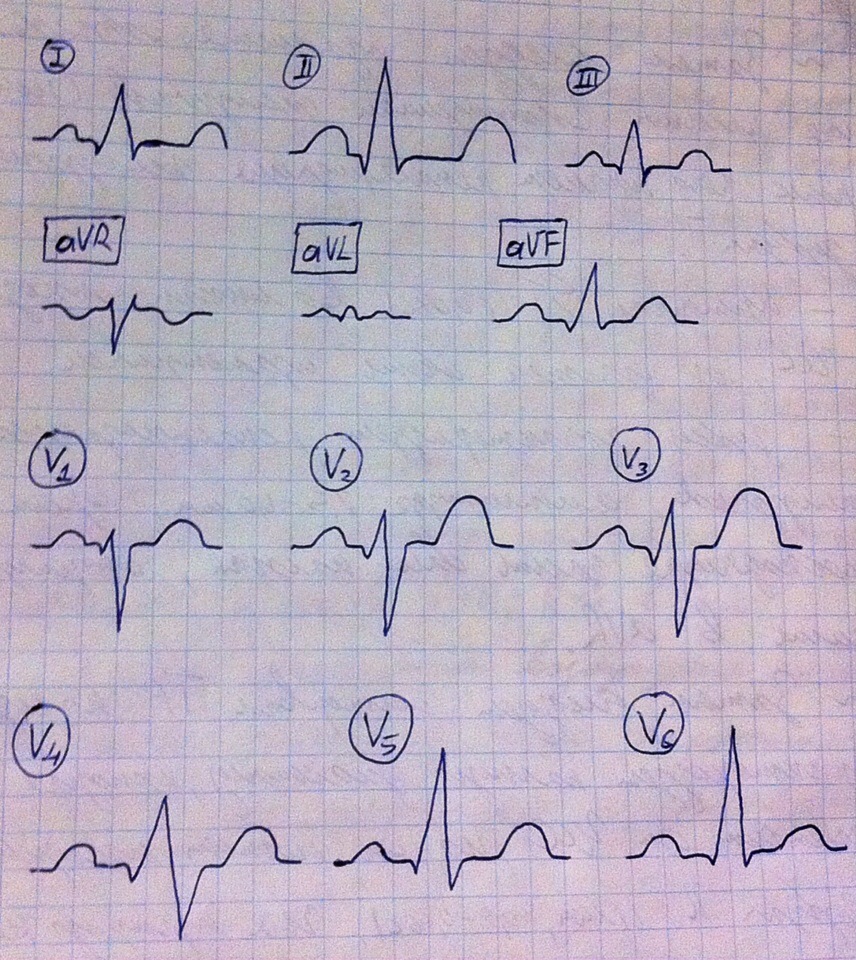
Теперь поговорим о расшифровке ЭКГ, т.е. об алгоритме.
Оценка ритма. Ритм должен быть в норме правильным синусным, он характеризуется тем, что зубец P всегда стоит перед комплексом QRS (это значит, что всегда сначала сокращаются предсердья, потом желудочки), постоянные интервалы PQ (нормальное состояние проводящей системы) и RR (своевременные сокращения без задержек, выпадов и преждевременных сокращений), постоянная форма зубца P (иногда нисходящая фаза пропадает, т.е. отсутствует сокращение левого предсердия, что нельзя назвать нормальным ритмом). Всё, что я написал в скобках, учить не обязательно – это просто примеры для большего понимания.
Подсчёт частоты сердечных сокращений. Если ритм правильный синусовый, то надо 60 секунд разделить на время одного сердечного цикла (равен длительности интервала RR). Мы так делаем, потому что сердечный цикл говорит, сколько он занимает секунд, а потом мы делим 60 секунд на это число, чтобы посчитать число циклов в минуту. Но если ритм неправильный и/или не синусный, то что делать? Тогда вы берёте 6 RR, находите среднее значение (сложить их и разделить на 6), и так же высчитываете ЧСС, как при правильном синусном, но в скобочках указываете значение минимального и максимального RR.
Определение вольтажа. Зубец R во втором стандартном отведении должен иметь амплитуду от 0,5 до 1,5 мВ, если меньше, то вольтаж считается сниженным.
Определение расположения электрической оси сердца ЭОС. Что это вообще такое? Дело в том, что возбуждение распространяется не хаотично, а от предсердий к желудочкам, т.е. имеет конкретное направление, т.е. ЭОС – это результирующий вектор возбуждения (учитывает направление и размер возбуждения), в норме он совпадает с анатомической осью сердца. Если положение сердца меняется или в нём происходит гипертрофия, то эта ось смещается, поэтому-то нам и важно уметь её определять. Сейчас на рисунке вы увидите ЭОС (показан стралочкой), которая заключена в треугольнике Эйнтховена (стандартные отведения), а к вектору опущены линии, перпендикулярные сторонам треугольника. Схема не простая но попытайтесь понять.

Как видите, пространство между перпендикулярами самое большое во 2-м отведении, в 1-м поменьше, а в 3-м наименьшее, отсюда и амплитуда зубцов R соответствующая. Вспомните, мы же говорили, что в стандартных отведениях R2>R1>R3. А почему так происходит? Дело в том, что вектор показывает ход возбуждения, которое обусловливает разность потенциалов (разность потенциалах максимальна на его концах) и все зубцы на ЭКГ. Если какое-то отведение будет параллельно ЭОС, то амплитуда в нём будет максимальная (так как разность потенциалов на концах вектора максимальна, а если отведение ему параллельно, то на концах этого отведения будет точно такая же разница потенциалов), если это отведение станет перпендикулярным ЭОС, то амплитуды вообще не будет (максимальную разницу потенциалов и амплитуду зубцов, соответственно, мы видим при параллельном расположении, а чем сильнее мы отклоняемся от параллельности в сторону перпендикулярности, тем меньше будет разница потенциалов и амплитуда зубцов). В общем это немного непростой вопрос для понимания – тут бы неплохо знать физику. Но даже если вы не знаете физику, то это не беда – смотрите на рисунок. Если ось смещается вправо (вращение по часовой стрелке), то она становится более параллельной к третьему отведению, поэтому вот этот «чёрный коридорчик» на рисунке расширится, а другие, наоборот, станут более узкими, поэтому при повороте ЭОС вправо (по часовой стрелке) амплитуда зубца R становится максимальной в 3-м отведении, а если ЭОС смещается влево (против часовой), то вектор становится более параллелен первому отведению, там R зубец и вырастает. Проще говоря! В норме ЭОС почти параллельна 2-му отведению, поэтому зубец R там максимален, при смещении ЭОС вправо (по часовой) ЭОС становится почти параллельной 3-му отведению, поэтому там зубец R становится максимальным, а если ЭОС смещается влево (против часовой), то ЭОС становится почти параллельным 1-му отведению, поэтому зубец R максимален в нём. Итак, как определить положение ЭОС? Просто сравните амплитуду зубца R в трёх стандартных отведениях: максимальный R во 2-м отведении – нормальное положение ЭОС, максимальный R в 3-м отведении – ЭОС смещена вправо, максимальный R в 1-м отведении – ЭОС смещена влево. Смещение ЭОС обусловлено смещением сердца или гипертрофией миокарда.
Оценка зубцов и интервалов. Вы проверяете форму и длительность зубцов, длительность интервалов и особенно важно, чтобы интервал ST был на изолинии.
Что нам может показать ЭКГ? На ЭКГ мы можем увидеть и гипертрофию миокарда, и инфаркты миокарда, и блокады, и экстрасистолы и многое другое, большинство патологий сердца. Но подробнее всё это вы изучите на других кафедрах, у нас же здесь нормальная физиология, поэтому мы просто скажем, что ЭКГ позволяет оценить в миокарде возбудимость, проводимость и автоматию. Проводимость оценим по длительности интервалов PQ (проводимость между предсердиями и желудочками) и QRS (внутрижелудочковая проводимость), а уровень автоматии оцениваем на основе ЧСС и ритма (если вдруг у вас ведущим станет АВ, то ритм будет неправильный несинусный).
Физиология сосудов.
Мы полностью обсудили тему сердца (ну конечно, это не вся физиология сердца вообще, а лишь те основы, которые вам нужно усвоить на данный момент обучения), а теперь можем приступить к не менее важной части сердечно-сосудистой системы – самим сосудам. Подробно обсудим кровеносные сосуды и гемодинамику, но ещё уделим немного внимания лимфатической системе.
Как и во всех темах частной физиологии здесь мы начнём с морфо-функциональной характеристики кровеносных сосудов. В анатомию и гистологию сильно углубляться не будем, затронем лишь моменты, важные с точки зрения физиологии. Все кровеносные сосуды делят на амортизационные (они же буферные), резистивные, обменные, ёмкостные.
К амортизационным сосудам относится лёгочный ствол, аорта и начальные отделы ветвей, отходящих от неё, т.е. сосуды, принимающие основной «удар» от сердца. Эти сосуды в средней оболочке имеют множество окончатых мембран из эластина, который позволяет сосудам быть эластичными. Эластичность – способность предмета изменять форму под действием силы, а после её прекращения полностью восстанавливать форму. В других темах мы уже ни раз говорили об этих сосудах, но напомню всё ещё раз. Эти сосуды за счёт эластичности облегчают работу сердца, снижая систолическое давление, и позволяют обеспечивать постоянное движение крови. Что было бы, если амортизационные сосуды были бы жёсткими, как стальная труба? Сердце выбрасывало бы кровь в сосуд и полностью проталкивало бы всю кровь по сосуду, давление достигало бы 150 мм рт ст (цифра не точная, ибо как-то не решался никто проверить), кровь бы двигалась по артериям, но только пока сердце сокращается, т.е. в систолу, а в диастолу сердце расслаблено и нет ничего, чтобы двигало кровь, поэтому кровь стоит на месте. В итоге, высокое давление, нагрузка на сердце и непостоянное движение крови в сосудах. А что происходит, если амортизационные сосуды эластичны? Сердце сокращается, выбрасывает в сосуд кровь, но проталкивает по нему лишь часть крови, следовательно, нагрузка на сердце ниже и давление составит 120 мм рт ст. а что с остальной частью крови? Она остаётся в сосуде и растягивает его (недаром он эластичный). Далее сердце перестаёт сокращаться (диастола), давление немного упало и теперь сосуд начинает сжиматься, восстанавливать свою форму (недаром он эластичный), тем самым проталкивая кровь по сосудам, пока сердце находится в состоянии диастолы. Итак, выходит, что эластичные сосуды снижают систолическое давление, нагрузку на сердечную мышцу, а также обеспечивают непрерывное движение крови по сосудам (т.е. она движется в систолу за счёт сердца, а в диастолу за счёт сосуда). В дополнение скажу (необязательно к запоминанию), что кровь, бегущая по сосуду, обладает кинетической энергией, когда же кровь растягивает стенку сосуда, то часть кинетической энергии превращается в потенциальную (энергия, которая раньше двигала кровь по сосуду, теперь растягивает стенку сосуда), но сосуд эластичный, поэтому в дальнейшем произойдёт обратный переход – потенциальная энергия в кинетическую (энергия, которая растягивала стенки, теперь толкает кровь по сосуду), причём здесь не происходит потери энергии в других её формах, т.е. всё то, что мы вложили в сосуд, то мы и вернём обратно в полном объёме. Что это означает на практике? А это значит, что данные сосуды практически не влияют на артериальное давление. Кровь по сосудам проталкивается под определённым давлением, а давление – это сила, с которой кровь давит на стенки сосуда (если по-простому), а мы сказали, что амортизационные сосуды эластичны, т.е. вся энергия, сообщаемая кровью посредством её давления на сосуды, возвращается от сосудов к крови. Вот и выходит, что давление как бы и не изменяется, на самом деле оно меняется, но это связано с работой сердца (в систолу же давление в системе явно больше, чем в диастолу). А вот в резистивных сосудах стенка совсем не эластичная, поэтому кровь, оказывая на неё давление, теряет часть своей энергии, ибо сосудистая стенка не эластична и приложенную к ней энергию не возращает, поэтому артериальное давление заметно уменьшается по ходу таких сосудов. О какой энергии в крови речь? Давление – это сила, с которой кровь давит на стенку сосуда. Мы говорили, что всякая жидкость – это молекулы, которые движутся. Всё, что движется, обладает кинетической энергией. Молекулы жидкости движутся хаотично, поэтому сталкиваются друг с другом и со стенками сосуда. Сталкиваясь с неподвижной стенкой сосуда, молекулы сообщают часть энергии стенке сосуда, а свою кинетическую энергию теряют (закон сохранения и превращения энергии), т.е. начинают двигаться медленнее. В амортизационных сосудах стенка всю полученную от молекул крови энергию возвращает им обратно, кинетическая энергия молекул крови не изменяется в целом, давление тоже не изменяется. В резистивных сосудах стенка не эластична, а потому не может возвращать энергию, молекулы ударяются о стенку, теряют часть кинетической энергии, сообщая её стенке сосуда (кинетическая энергия превращается в тепловую, т.е. форма стенки остаётся постоянной); чем дальше кровь движется по резистивным сосудам, тем больше кинетической энергии теряют её молекулы и тем ниже становится артериальное давление. Как связано артериальное давление и кинетическая энергия? Чем ниже кинетическая энергия, тем медленнее движутся молекулы жидкости, а значит, они врезаются в стенку сосуда уже с меньшей скоростью, т.е. жидкость уже с меньшей силой давит на стенку сосуда, т.е. давление ниже.
Резистивные сосуды. К ним относятся артерии среднего и малого калибра, артериолы, сфинктеры (сосудистые). Как я уже успел упомянуть, их средняя стенка очень богата гладко-мышечными клетками, поэтому сосуды, во-первых, не являются эластичными, следовательно, гасят артериальное давление, во-вторых, они способны существенно изменять свой просвет, регулируя кровоснабжение тех или иных органов и тканей. Т.е. суть этих сосудов в гашении артериального давления и регуляции кровоснабжения. Как понижается артериальное давление, мы сказали абзацем выше. Как происходит регулирование кровоснабжения? Данные сосуды оказывают сопротивление крови, движущейся по ним, поэтому их и называют резистивными (сопротивляющимися). В чём это выражается? Допустим, через одну трубку вы пытаетесь качать 5 литров воды в минуту, для этого вы прикладываете усилие в 10 условных единиц, но если вы захотите качать 5 литров в минуту по трубке, чей диаметр в 2 раза меньше, то вам придётся приложить усилие в, скажем, 25 условных единиц – через более узкие места сложнее проходить, думаю, все это знают. Вот так же и эти сосуды, сужаясь, оказывают сопротивление току крови. Из физики вы, наверное, помните, что электрический ток идёт по пути наименьшего сопротивления, это же касается и тока жидкости, тока крови. Вот у вас есть магистральный сосуд, от него отходит 3 одинаковых сосуда, по которым проходит равное количество крови, но вот один из сосудов сузился, тогда поэтому сосуду проходит лишь 50% объёма крови от его нормы, другие 50% распределяются между другими двумя сосудами. Вот так работают резистивные сосуды. Эти сосуды очень важны для нас, так как они регулируют общее артериальное давление и кровоснабжение тканей. Почему важно регулировать кровоснабжение тканей? У многих тканей метаболизм в разных состояниях имеет разный уровень, поэтому и потребность ткани в кровоснабжение разная, например, покоящейся мышце крови надо совсем немного, а вот, когда она работает, надо приносить к ней глюкозу и кислород, попутно уносить из неё углекислый газ и молочную кислоту (на самом деле нуждается в глюкозе мышца только спустя какое-то время после начала работы, да и кислорода самого она использует немного, углекислого газа выделяет немного, но это всё тонкости биохимии).
Обменные сосуды. К ним относят кровеносные капилляры. Они характеризуются крайне тонкой стенкой, что позволяет производить обмен веществами между кровью и тканями. При этом для транспорта веществ через сосудистую стенку могут использоваться все 4 известных вида транспорта веществ.
Ёмкостные сосуды. К ним относятся все вены. Они служат для возврата крови к сердцу, в них сосредотачивается 80% объёма всей крови. Вены, в которых крови приходится двигаться против гравитации, имеют клапаны, которые позволяют двигаться крови только в одном направлении. Кровь в артериях движется за счёт довольно сильного артериального давления, в венах давление очень низкое, так что же движет в них кровь? Во-первых, разница давлений всё-таки есть между разными отделами сердечно-сосудистых систем, это подтягивает кровь из вен в сердце, во-вторых, присасывающее действие грудной клетки – когда она расширяется, расширяются и сосуды, работая, как насосы, в-третьих, некоторые вены лежат между двумя артериями, которые расширяются при прохождении через них пульсовой волны, при этом они сдавливают вену, проталкивая в ней кровь, за счёт клапанов кровь движется не в разные стороны, а только вперёд, в-четвёртых, многие вены находятся вблизи мышц или в самих мышцах, которые сокращаются и оказывают тот же эффект на вены, что и пульсирующие артерии, только сильнее, в-пятых, кровь по венам может двигаться под действием гравитации, например, в верхней полой вене. Всё это помогает продвигать кровь по венам, но ещё важно заметить, что у ряда вен имеется чётко выраженный мышечный слой, который может влиять на просвет сосуда, поэтому из четырёх типов сосудов только ёмкостные и резистивные сосуды являются физиологически активными, так как они меняют свой просвет, влияя на показатели гемодинамики, т.е. они влияют на физиологические функции и участвуют в их регуляции.
Теперь собственно поговорим о гемодинамике, о которой мы не раз уже упоминали. Динамика – это движение и изменение в широком смысле слова, гемо – кровь. Нас интересует не столько само понятие гемодинамики, сколько её показатели. Какие показатели? Линейная скорость, объёмная скорость, сопротивление, давление. Разберём каждый из этих показателей.
Сопротивление. Характеризует то, как сложно проталкивать кровь через сосуд. Чем выше сопротивление, тем выше давление необходимо, чтобы кровь прошла по нему, следовательно, эти сосуды снижают давление. О том, как происходит снижение давления в сосудах вследствие сопротивления, мы говорили выше. Сопротивление сосуда току крови/жидкости по нему определяется по формуле Пуазеля: R = (l * h) : (3,14 * r^4), где R – сопротивление, l – длина сосуда, h – вязкость крови/жидкости, r – радиус сосуда (в формуле он взят в четвёртой степени). Длина сосудов у нас не меняется (они становятся немного длиннее в течение жизни, но это процесс настолько медленный, что мы его не учитываем), вязкость крови может меняться, но обычно для этого требуются дни и недели, т.е. не самый лабильный показатель, а вот радиус сосудов меняется постоянно и очень быстро, т.е. сопротивление сосудов на деле зависит от просвета сосудов, причём заметьте, тут обратная зависимость – чем больше просвет сосуда, тем ниже сопротивление, причём в формуле радиус взят в 4-й степени, т.е. просвет сосуда может измениться несильно, но сопротивление изменится очень ощутимо. Формулу Пуазеля запоминать необязательно – запомните, что сопротивление коренным образом определяется просветом сосудов.
Объёмная скорость. Объёмная скорость отражает, какой объём крови проходит через поперечное сечение сосуда в единицу времени, единицы измерения – литры в минуту (л/мин). Иными словами, вы берёте сосуд, ставите в нём блок-пост (называйте, как хотите) и считайте, какой объём крови пройдёт через пост за минуту. Это физиологически важный показатель, он характеризует уровень кровоснабжения тканей и органов (чем больше крови приливает к тканям в объёмном плане, тем больше они получат кислорода и питательных веществ и отдадут больше продуктов выделения). Объёмную скорость можно рассчитать по следующей формуле: Q = P / R, где Q – объёмная скорость кровотока, P – давление, R – сопротивление. Объёмная скорость прямо пропорциональна давлению, так как то является её движущей силой, но обратно пропорционально сопротивлению, так как то по сути мешает объёму крови проходить по сосуду. Как изменяется объёмная скорость крови в сосудах разных типов?
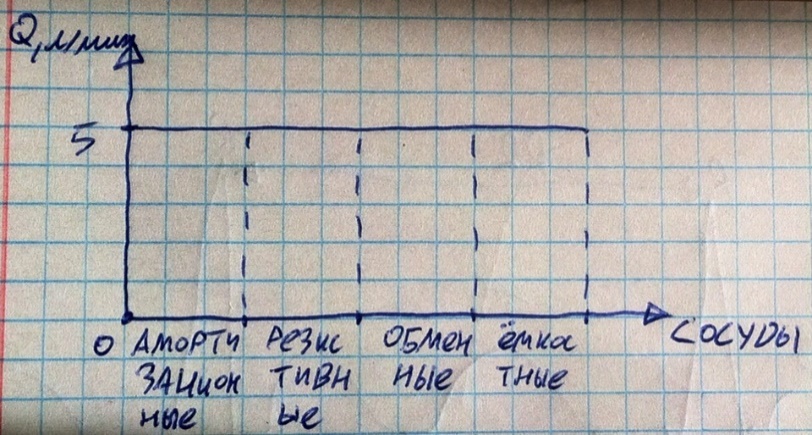
Примечательно, что скорость не изменяется, но имейте ввиду, что это график для сосудистых отделов! Т.е. в графе «резистивные сосуды» имеется ввиду результат по всем резистивным сосудам вместе взятым (сумма), в отдельных же сосудах скорость отличается. Почему суммированная объёмная скорость в разных сосудистых отделах (коих 4) не изменяется? Ну смотрите, прошло у нас, допустим, 3 литра крови по амортизационным сосудам, дальше этому объёму предстоит пройти по резистивным сосудам. Почему по следующему отделу пройдёт именно 3, а не больше или не меньше? А потому, что у нас замкнутая кровеносная система, убыть и прибыть крови не может, как было 3 литра, так и останется – кровь никуда не девается и ни откуда не берётся (не трогаем гемолиз и гемопоэз, это немного другое). И почему этот объём будет проходить через разные отделы сосудов за одно и то же время? Да потому, что если в одном отделе скорость была бы выше, чем в другом, то в первом кровь бы скапливалась. Всё логично. Вот именно поэтому объёмная скорость во всех отделах (отдел – сумма всех сосудов одного физиологического типа) сосудов постоянна. Измеряется объёмная скорость крови в отдельных сосудах (иными словами их кровенаполнение) реографией или флуометрией.
Линейная скорость. Она отражает расстояние, которое пройдёт отдельная точка в крови за единицу времени вдоль сосуда. Т.е. берёте эритроцит, например, и смотрите, какое расстояние в сосуде он преодолеет за секунду. Единицы измерения – сантиметры в секунду (см/с). Линейная скорость определяется по следующей формуле: V = Q / S, где V – линейная скорость, Q – объёмная скорость, S – площадь поперечного сечения сосуда (радиус в квадрате, умноженный на 3,14). Линейная скорость прямо пропорциональна объёмной, ибо обе эти скорости подразумевают прохождение какого-то количества крови вдоль сосуда, т.е. обе характеризуют поток, чем он обильнее, тем выше скорость и та, и другая. Линейная скорость обратно пропорциональна просвету сосуда (радиусу/диаметру), чем уже сосуд, тем выше линейная скорость. Почему? Представьте, что вы поливаете огород из шланга, объёмная скорость там постоянная, струя бьёт недалеко (линейная скорость невысокая), а потом вы сдавливаете конец шланга, при этом струя начинает бить гораздо дальше. Вы уменьшили просвет и увеличили линейную скорость, ибо, чтобы проталкивать тот же объём, но при меньшем просвете, линейную скорость необходимо увеличить, чтоб жидкость успевала проходить через узкий проход. Как изменяется линейная скорость крови в разных отделах сосудов? Как я говорил ранее, линейная скорость зависит от объёмной и от просвета сосудов. Объёмная скорость относительно постоянна (вспомните её график) во всех отделах сосудов, а вот просвет сосудов суммарный в разных отделах разный. Просвет аорты не такой уж и большой, но затем она ветвится, просвет суммарный становится больше, а чем больше просвет, тем ниже линейная скорость. Поэтому по ходу отдела амортизационных сосудов скорость падает с 50 до 35 см/с, далее в отделе резистивных сосудов ветвления ещё больше, суммарный просвет растёт, линейная скорость падает с 35 аж до 0,05 см/с! В капиллярах падает с 0,05 до 0,01 см/с. Почему в капиллярах так медленно? Потому что капилляров у нас не счесть, как много, суммарный просвет у них очень большой. Затем отдел ёмкостных сосудах, т.е. венах, скорость поднимается с 0,01 до 25 см/с, потому что вены не ветвятся, а сливаются в более редкие и крупные, суммарный просвет падает, но почему скорость поднимается лишь до 25, если в самом начале было 50 см/с? Дело в том, что если смотреть на большой круг кровообращения, то выходит из сердца одна аорта, а приходят две полые вены, вен почти всегда в 2 раза больше, чем соответствующих артерий, поэтому суммарный просвет вен больше, а линейная скорость в них ниже.
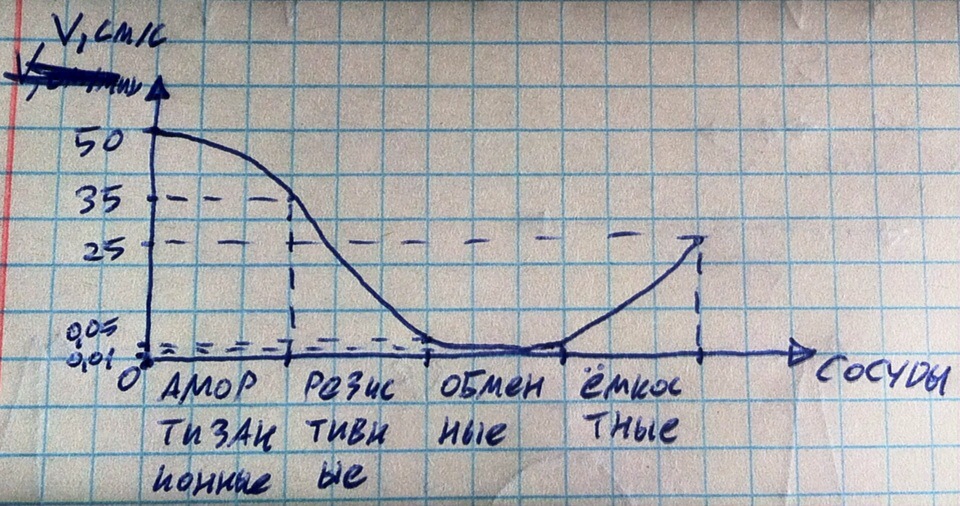
Измеряют линейную скорость кровотока в отдельных сосудах с помощью ультразвуковой доплерографии. А ещё вам надо знать особый термин – время кругооборота кровотока, которое отражает, за сколько один эритроцит полностью пройдёт по двум кругам кровообращения, в нормальных условиях это время составляет 23 секунды.
Артериальное давление. Этот вопрос мы обсуждали далеко не раз, однако повторим. Давление – сила, с которой жидкость давит на стенку сосуда или сила, с которой молекулы жидкости бьются о стенку сосуда. Единицы измерения – милиметры ртутного столба (мм рт ст). Кровяное давление – соответственно, сила, с которое кровь давит на стенку сосуда. Давление можно вычислить по формуле: P = Q * R, где P – кровяное давление, Q – объёмная скорость крови, R – сопротивление сосудов кровотоку. Кровяное давление прямо пропорционально обоим параметрам, почему? Допустим, у вас есть сектор в сосуде, через него за минуту прошло 100 мл крови, а значит, Х молекул в крови ударилось о стенку сектора сосуда 10Х раз, сообща 100Х условных единиц энергии. А если объёмная скорость кровотока вырастет в 2 раза? Тогда за то же время через сектор сосуда пройдёт 200 мл крови, 2Х молекул, которые ударятся о стенку сосуда 20Х раз и сообщат 200Х условных единиц энергии стенке. Т.е. чем выше объёмная скорость, тем больше молекул пройдёт через сосуд и ударится об его стенку, т.е. окажет большее давление. Поэтому чем выше объёмная скорость крови, тем выше кровяное давление. Как влияет сопротивление? Мы говорили, что ключевой фактор сопротивления – это просвет сосуда. Представьте, что объёмная скорость в сосуде не меняется, но просвет его уменьшился, при этом уменьшился объём сосуда, но число молекул крови осталось прежним, они стали ближе друг к другу (объём и свободное пространство уменьшилось), поэтому молекулы чаще врезаются друг в друга и в стенки, а значит, и давление стало выше. А как давление меняется в разных отделах сосудов?
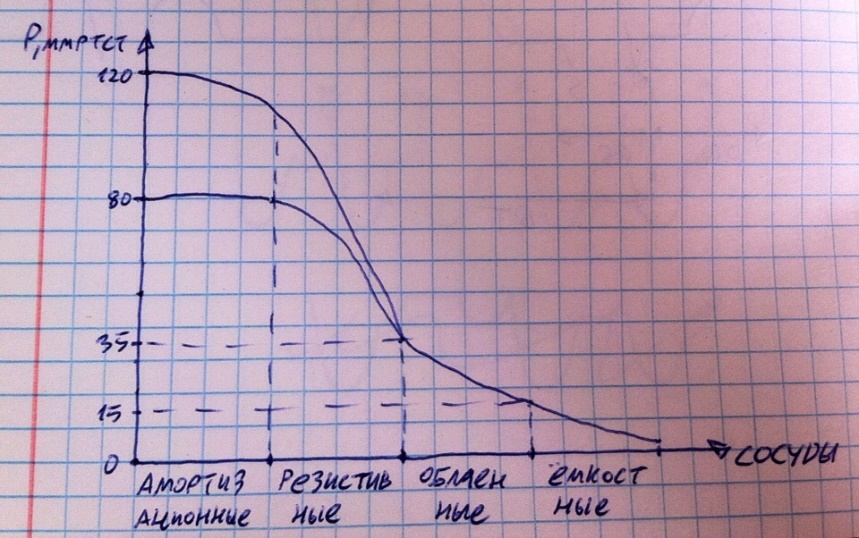
Давление по ходу сосудов уменьшается, причину этого я описывал выше (молекулы жидкости при ударе о стенки сосудов постепенно теряют кинетическую энергию и реже бьются о стенку, оказывая меньшее давление), но это не касается амортизационных сосудов. Но почему у нас раздвоенный график на уровнях амортизационных и резистивных сосудов? Дело в том, что у нас есть давление в артериях (а эти два отдела полностью представляют артерии) постоянно скачет между систолическим и диастолическим, что связано с особой работой сердца, поэтому давление в этих отделах непостоянно, но постепенно уровень давления и размер его колебаний уменьшается по мере приближения к капиллярам. Две самые принципиальные цифры, которые надо запомнить на графике – это 35 и 15 мм рт ст. Давление в венах самое низкое, близится к нулю. Давление постоянно уменьшается для того, чтобы в сосудистой системе существовала разница давлений, которая является движущей силой крови по сосудам, если бы в одном из отделов давление повышалось, то кровь бы двигалась не в том направлении, но этого не происходит, ибо давление постоянно падает вследствие постоянного сопротивления (амортизационные сосуды не в счёт).
С клинической и физиологической точки зрения более интересным является не всё кровяное давление, а артериальное, так как оно больше, переменчиво и в большей мере отражает работу сердечно-сосудистой системы. Артериальное давление – это кровяное давление в артериях, амортизационных и резистивных сосудах. Как измеряется артериальное давление? Способов довольно много. Существуют прямые и непрямые методы измерения артериального давления, к прямым относится метод посредством катетеризации, к непрямым относятся пальпаторный метод Рива-Роччи, аускультативный метод Короткова и метод артериальной осциллографии. Разберёмся в каждом методе. Но перед этим надо заметить, что есть 4 вида давления, которые мы исследуем: систолическое, диастолическое, пульсовое и среднее. Систолическое давление максимально и отражает вклад сердца в формирование давления (обусловлено систолой желудочка левого). Диастолическое давление показывает вклад сосудов в формирование давления (происходит в диастолу, обусловлено работой аорты по проталкиванию крови и тонусом резистивных сосудов, чем выше тонус, тем выше давление). Пульсовое давление – разница между систолическим и диастолическим, оно пропорционально систолическому объёму, т.е. количеству крови, которое левый желудочек выбрасывает в аорту, снижение пульсового давления и, соответственно, систолического объёма говорит о неэффективной работе сердца, нарушении его насосной функции по разным причинам. Среднее давление это не среднее арифметическое систолического и диастолического, а результирующая всего давления. Как это понимать? По аналогии со средней скоростью. Например, автомобиль ехал один час со скоростью 80 км/ч, а потом три часа со скоростью 60 км\ч. Средняя скорость будет рассчитываться как (80 + 60 * 3) / 4 = 65 км/ч, а не (80 + 60) / 2 = 70 км/ч. Видите разницу? В сердечном цикле диастола длится дольше систолы, поэтому среднее давление будет ближе к диастолическому, чем к систолическому, как в примере про машину. Среднее давление наиболее значимо с клинической и физиологической точки зрения, так как все рецепторы в нашем теле реагируют только на уровень среднего давления, плюс систолическое и диастолическое давление очень часто изменяются, а среднее относительно постоянно, а потому лучше отражает внутреннюю картину происходящего.
Прямой метод измерения артериального давления путём катетеризации артерий. Суть состоит в том, что датчик давления помещается непосредственно в артерию, остаётся там на довольно продолжительный срок и позволяет постоянно и с высокой точностью отслеживать уровень артериального давления. Катетеризируют часто артерии в подмышечной впадине. Данный метод позволяет измерить систолическое и диастолическое давление, а пульсовое можно посчитать. Собственно, прямым этот метод назван потому, что является инвазивным, а датчик непосредственно воспринимает давление в сосуде. Однако данный метод по понятным причинам ограничен в применении, он в основном используется для лежачих больных, которые чаще всего находятся в тяжёлом состоянии, в связи с чем нуждаются в постоянном мониторинге основных жизненных показателей, в том числе и артериального давления.
Непрямые методы называются так, потому что они не контактируют с давлением внутри самих сосудов, а регистрируют его опосредованно. Пальпаторный метод Рива-Роччи. На плечо (выше локтевого сгиба) надевается манжета, в которую накачивается воздух через помпу-насос и шланг, с манжетой связан сфигмоманометр. Как проводится исследование? Исследователь пальпирует пульс на лучевой артерии исследуемого, в манжету накачивают воздух до тех пор, пока пульс не перестанет пальпироваться, после этого продолжить накачивать воздух в манжету для небольшого запаса, после этого вентиль на насосе медленно откручивается, давление в манжете постепенно падает, как только исследователь снова начинает ощущать пульс у исследуемого, он регистрирует давление на сфигмоманометре, которое показывает систолическое давление. На чём основан метод? Мы нагнетаем давление в манжету, та сжимает плечо, а с ним и все сосуды в плече. Если давление манжеты превышает давление систолическое в сосудах, то сосуды полностью пережимаются, по ним не распространяется пульсовая волна, поэтому она не пальпируется на лучевой артерии, но как только давление в манжете становится меньше, чем систолическое давление в сосуде, то он перестаёт пережиматься и по нему проходит пульсовая волна на лучевую артерию, поэтому пульс на лучевой артерии для нас служит детектором систолического давления, которое мы увидим на сфигмоманометре. Данный метод прост в применении, но мало информативен, ибо позволяет оценить лишь систолическое давление, плюс у некоторых людей в связи с индивидуальными особенностями или состоянием здоровья пульс на лучевой артерии практически не пальпируется.
Непрямой аускультативный метод измерения артериального давления по Короткову является модификацией метода Рива-Роччи. Также используется сфингоманометр, манжета, шланги, насос с вентилем, но, вместо пальпации пульса на лучевой артерии, мы выслушиваем пульс (хотя правильнее сказать не пульс, а тоны) в области локтевого сгиба (на внутренней стороне, там очень близко лежат артерии) с помощью фонендоскопа. Мы также накачиваем манжету по прекращения слышимости пульса с запасом. Затем слегка откручиваем вентиль, давление в манжете падает, как только в фонендоскопе слышится первый «тон», отмечаем на сфигмоманометре систолическое давление, продолжаем снижать давление в манжете и слушать, скоро тоны прекратятся, последний тон будет показателем диастолического давления на сфигмоманометре. Если у вас достаточно хороший слух, то самый громкий из всех тонов указывает на среднее давление на сфигмоманометре (вам может показаться, что первый тон самый громкий, но это не так). На чём основан механизм метода? Когда мы не пережимаем ничем сосуд, кровь в нём идёт ламинарными потоками, т.е. кровь движется параллельно стенке и давит на неё, но не слишком. Когда давление в манжете выше систолического, сосуд пережат. Но, когда давление в манжете опускается ниже систолического, сосуд становится частично пережатым, поэтому кровь через него проходит, но только вихревыми потоками (кровь завихряется из-за того, что быстро проходит через узкое пространство) и бьётся сильно о стенки сосуда, создавая тоны, которые мы и слышим. Когда давление в манжете опускается ниже диастолического, сосуд вообще перестаёт быть пережатым, в нём идут только ламинарные токи и мы ничего не слышим. Этот метод относительно прост, доступен, безболезненный (как и все непрямые) и позволяет узнать все 4 вида давления (пульсовое можно посчитать, а среднее зафиксировать по самому громкому тону, хотя это уже не так просто).
Непрямой метод артериальной осциллографии осуществляется наложением электродов на предплечье и позволяет регистрировать все виды артериального давления. В чём плюсы и недостатки метода? Недостаток в том, что требуется особое оборудование и умение с ним обращаться. Преимущество в том, что возможен постоянный мониторинг артериального давления без инвазирования сосудов, а по Короткову возможны лишь единичные измерения (никакого постоянного мониторинга), при прямом методе возможен мониторинг артериального давления, но он требует инвазирования сосудов.
Какие факторы влияют на артериальное давление? Их 5: деятельность сердца, эластичность сосудов, тонус сосудов, объём циркулирующей крови, вязкость крови. Именно сердце под большим давлением выталкивает кровь в сосуды, поэтому основной вклад в формирование давление делает сердце. Про эластичность амортизационных сосудов мы уже говорили, они снижают систолическое давление и поддерживают диастолическое. Тонус резистивных сосудов: сосуды сужаются, их объём уменьшается, но количество молекул крови остаётся неизменным, а вот свободного пространства для молекул становится меньше, они чаще бьются о стенку сосуда, оказывая повышенное давление. Объём циркулирующей крови: допустим, объём сосудов не изменялся, а вот крови самой, её молекул стало больше, поэтому и свободного пространства для этих молекул стало меньше, теперь они чаще ударяются о стенки сосуда, оказывая большее давление. Вязкость крови, чем более вязкая жидкость, тем больше сил надо приложить, чтобы она могла продвигаться по сосуду, а движущая сила крови – давление, значит, чем выше вязкость, тем выше организм сделает давление (вязкость крови в основном определяется количеством в ней форменных элементов и белков).
Мы не раз говорили о таком понятии, как пульс. Что же он из себя представляет? Пульс – это ритмичные колебания стенки артерий в следствие работы сердца. Т.е. в буквальном смысле сердце выбрасывает в аорту объём крови, её стенки начинают колебать, эти колебания распространяются по всем артериям с довольно высокой скоростью. Пульс мы можем пропальпировать (классика – лучевая артерия) и оценить его по ряду характеристик, имеющих кстати клиническое значение: факт наличия, частота, симметричность, напряжённость. Что означают эти характеристики? Факт наличия, думаю, здесь пояснения излишни – отсутствие пульса может означать прекращение или очень слабую работу сердца, хотя имейте ввиду, что у некоторых людей в принципе плохо пальпируется пульс на лучевой артерии, поэтому лучше всего проверять по сонной. Симметричность, необходимо пальпировать пульс на обеих руках, если удары не совпадают на двух руках, скорее всего, имеются склеротические поражения сосудов (допустим, в руке в артерии склеротическая бляшка, которая повышает жёсткость сосуда, поэтому тот быстрее проводит пульсовую волну). Частота пульс отражает частоту сердечных сокращений. Напряжённость пульса отражает, как сильно надо надавить на область артерии, чтобы пульс перестал пальпироваться, чем больше вы для этого прикладываете сил, тем выше у человека артериальное давление (хитрый метод определить давление у человека без всякого оборудования, правда метод без точных цифр). Поскольку пульс – это колебание, которое волной распространяется по сосудам, можно измерять скорость этой волны, её скорость тем выше, чем выше жёсткость сосудов, которая повышается в случае атеросклероза. Нормальная скорость пульсовой волны в амортизационных сосудах 5,5-8,0 м/с, а в резистивных 6,0-9,5 м/с. Специальным инструментальным методом исследования пульса является сфигмография. Пример сфигмограммы ниже.
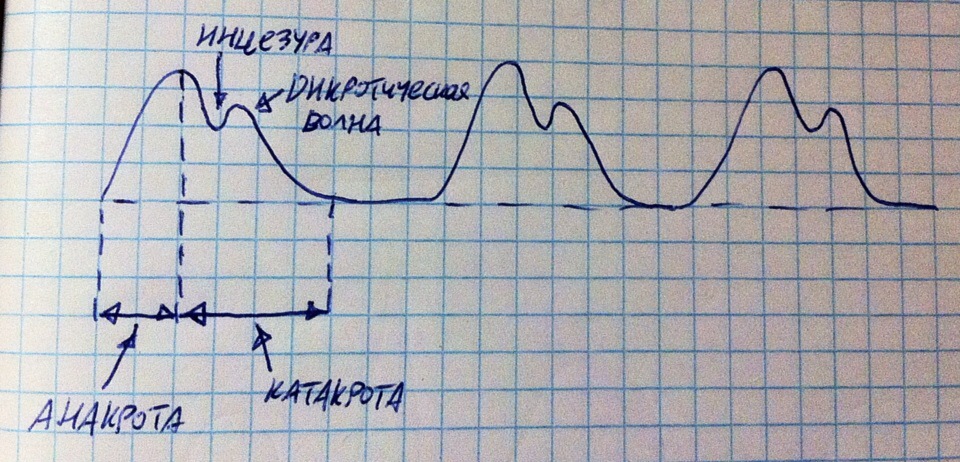
График показывает, как происходит колебание стенки артерии (пульс), и во многом отражает работу сердца. Поднимающаяся часть графика – анакрота – происходит в результате расширения артерий из-за систолы левого желудочка (выбрасывает резко много крови, заставляя стенки артерий колебаться), затем идёт диастола, сердце перестаёт выбрасывать кровь, поэтому колебания сходят на нет – катакрота, однако если вы вспомните сердечный цикл, там была стадия протодиастолы, когда кровь возвращалась в сердце, тем самым захлопывая полулунный клапан и ударяясь об него, от чего возникало новое колебание (от этого удара крови о клапан и от его схлопывания), на графике оно отражается в форме дикротического зубца. Между основным зубцом и дикротическим имеется углубление – инцезура. Забавно, что плятизмограмма (показывает кровенаполнение сосуда) и сфигмограмма (показывает колебание артериальной стенки – пульс) имеют одинаковый график, но характеризуют разные процессы. Почему же графики похожи? Дело в том, что все стадии этих графиков обусловлены одними и теми же особенностями деятельности сердца (наличие систолы и диастолы с протодиастолическим периодом).
Теперь обсудим микроциркуляторное русло и лимфатическую систему. Давайте посмотрим, что происходит в кровеносных капиллярах. Дело в том, что существует гидростатическое давление, которое мы как раз проходили, оно есть как у самой крови (толкает жидкость из сосуда в тканевую жидкость, в начале капиллярного русла, т.е. в артериальном конце оно составляет 35 мм рт ст, а в венозном конце всего 15 мм рт ст), так и у тканевой жидкости (толкает жидкость из тканевой жидкости в сосуд, составляет всего 3 мм рт ст). Но ещё есть онкотическое давление (сила, с которой белки притягивают к себе жидкость, точнее воду; белки тканевой жидкости тянут на себя жидкость давлением в 5 мм рт ст, а белки крови – альбумины в основном – тянут на себя кровь давлением в 25 мм рт ст). И каков результат всех этих давлений?
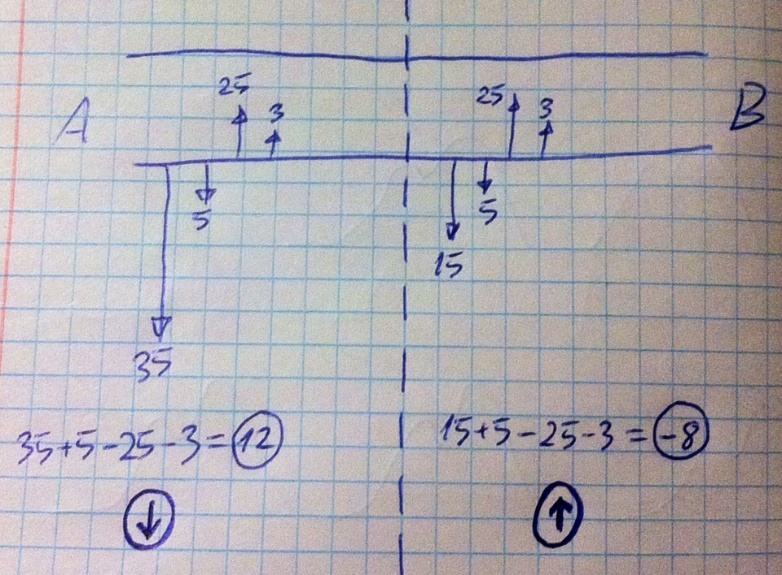
В артериальном конце гидростатическое давление крови (35 мм рт ст) и онкотическое давление белков тканевой жидкости (5 мм рт ст) толкают жидкость из сосуда в тканевую жидкость, гидростатическое давление тканевой жидкости (3 мм рт ст) и онкотическое давление белков крови (25 мм рт ст) толкают жидкость из тканевой жидкости в сосуд – в результате суммации всех давлением получаем 12 мм рт ст, которые толкают жидкость из сосуда в тканевую жидкость. Что происходит в венозном конце? Тут разница в том, что гидростатическое давление ниже – всего 15 мм рт ст. Гидростатическое давление крови (15 мм рт ст) и онкотическое давление тканевой жидкости (5 мм рт ст) толкают кровь из сосуда в тканевую жидкость, гидростатическое давление тканевой жидкости (3 мм рт ст) и онкотическое давление белков крови (25 мм рт ст) толкают жидкость из тканевой жидкости в сосуд – в результате суммации всех давлением получаем -8 мм рт ст, которые толкают жидкость из тканевой жидкости в сосуд. Однако есть одно «но» выталкивающая сила в артериальном конце выше, чем затягивающая сила в венозном конце (12 против 8), поэтому в тканях скапливается жидкость. Вот, чтобы не происходило отёка тканей и уменьшения объёма циркулирующей крови, существую лимфатические капилляры и лимфатическая система, которая, как дренаж, собирает все излишки жидкости (и «мусор» всякий заодно) и отправляет обратно в кровеносную систему. Чисто морфологически лимфатическая система незамкнутая, начинается слепыми капиллярами, заканчивается впадением протоков в магистральные вены, включает капилляры, узлы, сосуды, стволы и протоки. Функции лимфатической системы: дренажная (отток лишней жидкости из тканей и возврат в кровеносную систему) и защитная (лимфатические узлы – периферические органы иммунопоэза). Факторы продвижения лимфы по системе такие же, как и у вен: разница давлений, присасывающее действие грудной клетки, сокращения мышц, пульсации примыкающих артерий, имеются клапаны. Лимфатические капилляры есть везде, где есть кровеносные капилляры, кроме ЦНС, там лимфу замещает ликвор, а вот в таких тканях, как хрящевая и роговица, вообще никаких сосудов нет, в них питательные вещества распространяются диффузно.
Регуляция тонуса сосудов.
Теперь обсудим такую интересную тему, как тонус сосудов и его регуляцию.
Вы уже проходили тему мышечного тонуса, говоря о тонусе скелетной мускулатуры, но тонус у скелетной мускулатуры и у сосудов – совершенно разные понятия. У сосудистого тонуса есть три разновидности, для каждой из которых нужно своё собственное определение, поэтому в общем определении нет особого смысла, но если оно вам позарестно надо, то сосудистый тонус – способность сосуда длительное время поддерживать определённый просвет без признаков утомления. Разберёмся подробнее в видах сосудистого тонуса.
Гистохимический тонус поддерживается адвентициальной оболочкой сосуда (внешняя), которая способна растягиваться под давлением и сжиматься (в какой-то мере эластична). Базальный тонус обусловлен исключительно самими гладко-мышечными клетками средней оболочки сосуда. ГМК обладают автоматией, т.е. они сами для себя генерируют ПД. Автоматия позволяет им самостоятельно запускать своё сокращение, т.е. причиной базального тонуса является сокращение ГМК под действием своих собственных импульсов. Нервный тонус – многие кровеносные сосуды иннервируются симпатическим отделом вегетативной нервной системы, по этим нервам постоянно поступают импульсы, заставляющие ГМК сокращаться больше, в результате просвет сосуда становится очень маленьким. Обычно все сосуды (капилляры не в счёт) имеют адвентициальную, мышечную оболочку и иннервируются симпатикой, а потому сосудам присущи все три вида сосудистого тонуса, поэтому в общем мы можем сказать, что сосудистый тонус – это способность сосудов длительно поддерживать определённый просвет через сокращение ГМК без признаков утомления, под действием ЦНС. Однако есть некоторые сосуды, которые иннервируются парасимпатическим отделом вегетативной нервной системы, но их крайне мало.
Тонус сосудов довольно важен, его поддерживают амортизационные (ну в какой-то степени), резистивные (это их главная фишка) и ёмкостные (часть из них) сосуды, из них активно изменяют уровень тонуса резистивные сосуды, регулируя кровоснабжение органов и тканей, а также внося вклад в поддержание определённого уровня артериального давления. Тонус сосудов сказывается на всех параметрах гемодинамики: сопротивление сосудов определяется радиусом сосуда, который является следствием тонуса сосуда; объёмная скорость крови зависит от сопротивления сосудов, которое зависит от радиуса сосуда, а тот зависит от тонуса сосудов; линейная скорость зависит от просвета сосудов, а тот зависит от тонуса сосудов; артериальное давление тем выше, чем выше тонус сосудов. В связи с такой важностью сосудистый тонус нуждается в регуляции, которую мы изучим. Тут, как и почти со всеми физиологическими функциями, есть три метода регуляции: миогенный, гуморальный и нервный.
Миогенный. ГМК сокращаются при поступлении кальция в клетку извне (из тканевой жидкости), ГМК имеет специальные кальциевые каналы, которые имеют специальные рецепторы, чаще механорецепторы. Как они работают? По каким-то причинам в артерии стало приливать очень много крови, которая стала растягивать сосуд (опасность разрыва), это растяжение улавливают механорецепторы ГМК и открывают каналы для кальция, тот поступает в клетку, усиливая сокращение, тонус сосуда увеличивается, он предохраняет себя от перерастяжения и разрыва. Пример. Человек лежит, артерии ног расслаблены, затем он резко встаёт, вся кровь стекает в ноги, оттекает от головы. Мы бы должны были потерять сознание, но сосуды ног быстро наращивают тонус (именно миогенно), поэтому в ноги уходит не вся кровь, часть остаётся в голове и туловище.
Нервная (рефлекторная) регуляция.
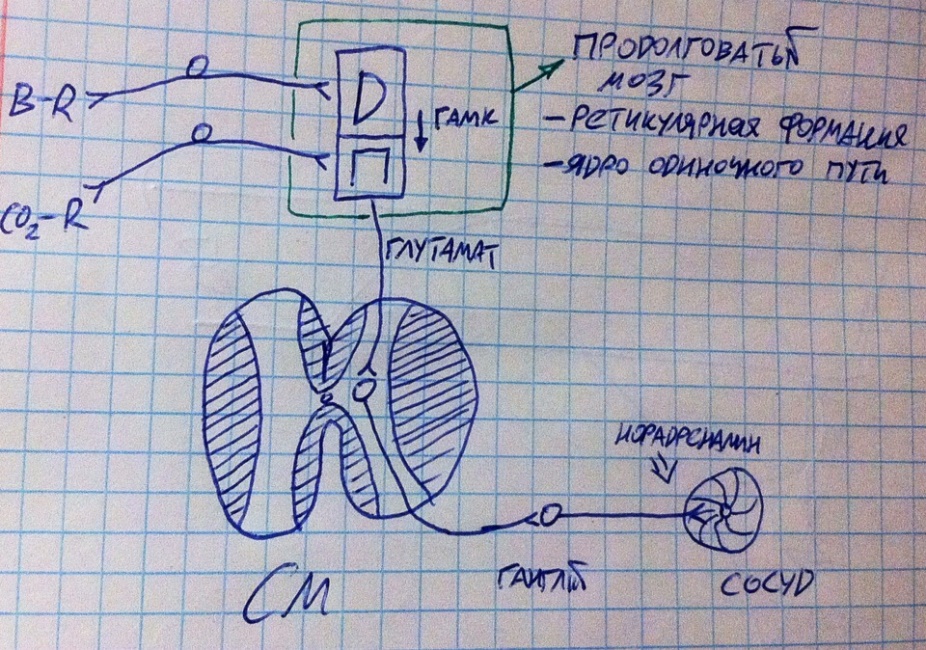
Ни для кого не секрет, что нервная регуляция осуществляется посредством рефлекторных актов, поэтому нам необходимо разобрать полноценные рефлекторные дуги. Начнём с рецепторов, они подразделяются на хеморецепторы (воспринимают концентрацию углекислого газа и кислорода) и барорецепторы (воспринимают артериальное давление). В дуге аорты и синокаротидных узлах имеются оба типа рецепторов, в лёгочном стволе только барорецепторы (хеморецепторы туда ставить не имеет смысла, ибо там течёт венозная кровь, ведь это малый круг кровообращения). Вазомотрный центр находится в продолговатом центре в составе ретикулярной формации и ядра одиночного пути, имеет прессорный и депрессорный отделы. Прессорный отдел посылает аксоны в спинной мозг на преганглионарные нейроны, возбуждая их глутаматом (аминокислота-нейромедиатор), аксон преганглионарных нейронов выходит из спинного мозга через передний рог, оттуда он идёт до ганглия, где передаёт сигнал на постганглионарный нейрон, тот посылает свой аксон в регулируемый сосуд, выделяет на его ГМК норадреналин (возбуждающий нейромедиатор), который увеличивает проницаемость мембраны для кальция, открывая соответствующие каналы и усиливая сокращение/тонус, сужая просвет сосуда. Почти все сосуды иннервируются только симпатикой. Выходит, рефлкексы способствуют только повышению тонуса сосудов? Нет, ведь в вазомоторном центре существует депрессорный отдел, который при необходимости тормозит прессорный отдел с помощью ГАМК (гамма-амино-маслянная кислота, тормозной нейромедиатор), снижая тонус симпатики, в результате чего нервный тонус сосуда ослабляется, а просвет увеличивается. Для большего понимания разберём примеры прессорного и депрессорного рефлексов. Предположим, у нас в крови слишком много углекислого газа, это фиксируют рецепторы, увеличивая вентиляцию лёгких (активное удаление углекислого газа из крови и обогащение её кислородом), но для активизированных лёгких и крови нужно больше (она должна успевать переносить газы, которые лёгкие нам любезно представляют или забирают), поэтому необходимо поднять артериальное давление за счёт деятельности сердца и тонуса сосудов, нас пока интересуют только сосуды. В чём заключается именно наш прессорный рефлекс? Хеморецетор в синокаротидном узле фиксирует повышенную концентрацию углекислого газа, создаёт нервный импульс, через чувствительный нейрон отправляет сигнал в прессорный отдел вазомоторного центра, тот повышает тонус симпатики по оговоренному нами пути, в нервно-мышечных синапсах выделяется больше норадреналина, кальция в ГМК входит больше, сокращения больше, тонус выше, просвет уже, давление артериальное выше. Пример депрессорного рефлекса: у нас излишне высокое давление, это фиксируют барорецепторы в дуге аорты и посылают сигнал в депрессорный отдел вазомоторного центра через чувствительный нейрон, депрессорный отдел тормозит прессорный, снижая тонус симпатики, поэтому на ГМК в синапсах выделяется меньше норадреналина, меньше кальция поступает в ГМК, сокращение становится меньше, тонус меньше, просвет больше, давление меньше. Помимо этих классических структур система нервной регуляции связывается и с другими нервными центрами, а также с гипоталамусом, так как в регуляции многих физиологических функций имеет значение уровень кровоснабжения, который определяется тонусом сосудов.
Гуморальная регуляция. Гуморальные факторы регуляции в зависимости от оказываемого эффекта делят на вазоконстрикторы (усиливают тонус, уменьшают просвет сосуда) и вазодилататоры (ослабляют тонус, увеличивают просвет). К вазоконстрикторам относятся ангиотензин-2 и серотонин, к вазодилататорам относятся углекислый газ (локально), монооксид азота, брадикинин, эндотелин-1, гистамин. Ряд приведённых факторов способен оказывать влияние на заметное количество сосудов и даже на всю систему сосудов в целом, но большинство факторов действуют строго локально. Почему так? Дело в том, что нервная система регулирует в основном общее артериальное давление и общий уровень кровообращения, если бы нервная система регулировала кровоснабжение отдельно каждой ткани и органа, то это было бы большой информационной нагрузкой для неё, вместо этого, для решения локальных вопросов у нас есть гуморальный способ регуляции, который успешно решает локальные вопросы и является более простым в использовании. Например, какая-то ткань начинает очень активно работать, её метаболизм значительно ускоряется (значит, ей нужно усиленное кровоснабжение, которого пока нет), т.е. ускоряется и катаболизм, в результате которого усиливается выделение углекислого газа (конечный продукт метаболизма), а углекислый газ является гуморальным фактором регуляции, который вызывает вазодилатацию, т.е. тонус сосуда снижается, просвет увеличивается, кровенаполнение сосуда и уровень кровоснабжение ткани увеличивается – её потребность удовлетворена. Кстати имейте ввиду, что углекислый газ является гуморальным фактором только локально, т.е. он так работает, если его концентрация повышается в отдельных сосудах, если же его концентрация будет повышена во всех сосудах, то это будет свидетельствовать о неэффективности дыхания, поэтому концентрация углекислого газа в крови будет зафиксирована хеморецепторами, что приведёт к включению ряда рефлексов (повышение интенсивности работы сердца, тонуса сосудов, вентиляции лёгких), т.е. повышение общей концентрации углекислого газа в кровотоке активирует нервную регуляцию, а не гуморальную – почувствуйте разницу. Ещё один пример того, как ткани сами локально регулируют своё кровоснабжение: допустим небольшая зона мозга активировалась, а потому требует усиленного кровоснабжения, поэтому нейроны выделяют монооксид азота, который проникает в ГМК сосудов, вызывает их дилатацию – тонус снижается, просвет увеличивается, кровоснабжение улучшается в соответствие потребностям активировавшейся ткани. Отдельного нашего внимания заслуживают два таких гормона, как адреналин и ренин. Адреналин для одних сосудов является вазодилататором, а для других вазоконстриктором, что зависит от того, какой именно адренорецептор находится в сосудах: взаимодействие адреналина с альфа-1-адренорецепторами приводит к вазоконстрикции, взаимодействие адреналина с бета-2-рецепторами приводит к вазодилатации. Зачем двоякое действие? Вспомните, что адреналин готовит тело к экстримальным нагрузкам, соответственно, ему необходимо перераспределить кровоснабжение в пользу мышц и сердца (в их сосудах вазодилатация), а вот органы ЖКТ и кожа отдают часть своей порции кровоснабжения (на время стрессовой ситуации их функция угнетается, в сосудах вазоконстрикция). Что же касается ренина? Вообще ренин – это фермент, он расщепляет ангиотензиноген (путём ограниченного протеолиза) в крови, тот превращается в ангиотензиноген-1, попадает в лёгкие, где локальными ферментами превращается в ангиотензин-2, который вызывает вазоконстрикцию и повышение артериального давления. Ренин выделяется почками в том случае, если давление в их сосудистой системе слишком низкое. Зачем они это делают? Физиологию выделительной системы и в частности почек нам ещё только предстоит рассмотреть, но заранее скажу, что первым шагом в работе почек является клубочковая фильтрация, движущей силой которой является давление крови (точнее разница давлений, но сейчас это не суть), если давление снижено, уровень клубочковой фильтрации почек снижается, как и вся их выделительная функция, что довольно опасно для организма, поэтому почки по своему усмотрению могут поднимать артериальное давление, причём очень заметно повышают.
Для справки. Повышение тонуса сосудов приводит к повышению сопротивления (давление на кровь усложняет её прохождение по сосуду), давления (сосуд давит на кровь, отсюда давление) и линейной скорости (чем меньше просвет, тем она выше – по аналогии с пережатым шлангом), а объёмная скорость падает (результатом повышенного тонуса является повышенное сопротивление, которое мешает движению крови). При снижении тонуса обратные эффекты.
Исследование тонуса сосудов. Что является показателем тонуса сосудов? Тонус сосудов – длительное поддержание определённого просвета сосудов в следствие сокращения ГМК при участии ЦНС. Т.е. прямым показателем тонуса сосуда является его просвет, опосредованным показателем является линейная скорость крови в сосуде. Если вы вспомните тему гемодинамики, то линейная скорость определяется объёмной скоростью и просветом сосуда, чем меньше просвет (следствие высокого тонуса), тем выше линейная скорость. С помощью ультразвукового исследования мы можем увидеть просвет сосуда и узнать линейную скорость крови в нём, что охарактеризует тонус этого сосуда. Скорость крови в сосуде позволяет узнать ультразвуковая доплерография, скорость сравниваем с нормой, а оценить просвет мы можем с помощью режима ультразвукового дуплексного сканирования, в этом режиме на экране движущиеся объекты (кровь) окрашиваются в один цвет, а неподвижные объекты (стенка сосуда и окружающие ткани) окрашиваются в другой цвет, поэтому мы можем просто измерить ширину просвета сосуда (просвет сосуда занят кровью, которая на экране имеет отличный от других тканей цвет) и сравнить с нормой. Суженный просвет и повышенная линейная скорость свидетельствует о повышенном сосудистом тонусе. Помимо самого тонуса сосудов, исследуют и гуморальную регуляцию сосудов. Каким образом? Также с помощью УЗИ оценивают просвет сосуда, затем вводят в сосуд вазоконстриктор или вазодилататор и наблюдают за реакцией сосуда, реакция может быть полноценной, слабой, отсутствовать, а иногда и быть обратной. Обычно к патологии сосудов приводит дисфункция эндотелия, он же отвечает за восприятия большинства гуморальных факторов регуляции тонуса сосудов, если реакция сосудов на введение гуморальных факторов далека от нормы, это свидетельствует о нарушении функции эндотелия, т.е. мы одновременно исследуем и регуляцию тонуса, и состояние эндотелия сосудов.
Избранные вопросы.
Функциональная система регуляции артериального давления.

Как и все функциональные системы, эта имеет объект (артериальное давление), метаболизм, рецептор объекта, центральную регуляцию (ЦНС и эндокринную систему), вегетативную (сердце, резистивные сосуды, почки, печень, селезёнка, красный костный мозг) и поведенческую регуляцию. Конструкция у всех функциональных систем примерно одна и та же, меняется лишь объект регуляции и механизмы вегетативной регуляции, их мы и изучим. Напомню, что артериальное давление определяется 5-ю факторами: деятельность сердца, эластичность сосудов, тонус амортизационных сосудов, объём циркулирующей крови, вязкость крови. Органы, приведённые в вегетативной регуляции, как раз влияют на артериальное давление через 4 из 5 факторов, определяющих артериальное давление (из всех факторов не регулируется только эластичность сосудов, ибо эта мера относительно постоянная). Чем интенсивнее работает, тем выше артериальное давление, ведь именно сердце его создаёт. Тонус сосудов также вносит вклад в формирование давления (механизм мы не раз обсуждали выше). Объём циркулирующей крови регулируется почками, которые отвечают за выведение «лишней» жидкости из организма с мочой, но почки могут не выводить всю эту жидкость с мочой и оставить её в крови, увеличив тем самым объём циркулирующей крови (обеспечивается путём усиления реабсорбции воды в почечных канальцах нефронов). Как регулируется вязкость крови? Она определяется количеством белков и форменных элементов крови, которое регулируется системой крови. Система крови – совокупность органов, обеспечивающих продукцию и разрушению основных компонентов крови (форменные элементы и белки как раз имеются ввиду), и сама кровь. К системе крови относится большое количество органов; форменные элементы крови генерируются в основном в красном костном мозге (есть и другие органы гемопоэза, но они кардинально не изменяют количественный состав, они отвечают за качественный состав крови, т.е. не влияют на вязкость крови), разрушаются они в селезёнке (в основном в ней), печени, красном костном мозге, лимфатических узлах, причём это справедливо для эритроцитов, но они занимают львиную долю форменных элементов крови, поэтому мы и обращаем внимание именно на них; белки крови синтезируются и разрушаются в основном печенью. Как вы видите, из всей системы крови наиболее значимыми органами, регулирующими уровень белков и форменных элементов крови, являются печень, селезёнка и красный костный мозг, поэтому я их и написал на схеме. Какова роль метаболизма и поведенческой регуляции? С метаболизмом всё относительно просто. Если какая-то ткань активировалась, она выделяет углекислый газ, заставляя сосуд расширяться, давление в нём немного падает (локальная регуляция). Если много тканей (много скелетных мышц, например) активировались, то во всей крови поднимается концентрация углекислого газа, что вызывает рефлексы, усиливающие вентиляцию лёгких и повышающие общее артериальное давление (центральная регуляция). Вот так метаболизм может влиять на артериальное давление. Если у человека сердце работает очень слабо (по разным причинам), то давление заметно снижается, а давление – движущая сила крови в сосудах, т.е. при пониженном давлении кровь циркулирует медленнее, кровоснабжение всех тканей снижается, т.е. они ужимаются в притоке питательных веществ и кислорода, а потому им приходится снизить уровень своего метаболизма. Так артериальное давление влияет на метаболизм. Во всех функциональных системах влияние между объектом и метаболизмом всегда взаимное. Как работает поведенческая регуляция? Это могут быть влияния коры через гипоталамус, а может быть влияние через деятельность скелетной мускулатуры и дыхательных мышц, в частности. Чуть подробнее. Как кора работает через гипоталамус? При сильном волнении или в ожидании больших физических нагрузок кора посылает сигналы в гипоталамус, тот посылает сигнал в продолговатый мозг, чтобы тот увеличил интенсивность работы сердца (помимо прямого действия нервной системы, дополнительно производится выброс адреналина надпочечниками по команде от ЦНС), следствием повышенной интенсивности работы сердца является повышение артериального давления. Если вы закроете глаза и попытаетесь убедительно представить, что ваше тело испытывает очень высокую физическую нагрузку, то ваша ЧСС может подняться даже на 30 уд/мин, однако такая способность поведенческой регуляции у разных людей в разной степени – не факт, что у всех из вас это получится (у кого-то больше, у кого-то меньше, у спортсменов это вообще мало заметно, ибо у них сердце повышает интенсивность в основном за счёт силы, а не частоты сокращений). Как мы можем влиять на АД посредством скелетной мускулатуры? Да много способов есть: вы можете начать бежать (так вы измените метаболизм мышц и функциональной системе придётся откликнуться и повысить АД в соответствии с повышенным метаболизмом), а можете перестать бежать – и всё в таком духе. Как повлиять на АД посредством дыхательных мышц? Мы имеем произвольный контроль над этими мышцами, поэтому можем управлять лёгочной вентиляцией, как захотим. Если у нас повышенное давление в следствие чрезмерно интенсивной работы сердца после пробежки, мы можем глубже дышать, тогда сердце постепенно «успокоится», а АД снизится. На чём это основано? Пока вы бежите, ваш метаболизм повышен, вам необходимо получать очень много кислорода и выделять много углекислого газа, для этого повышается эффективность лёгочной вентиляции (газообмен между организмом и воздухом) и артериальное давление (ускоряет кровь, чтобы та успевала приносить и уносить газы для этого газообмена). Если вы бежали слишком быстро или много, при этом вы далеко не спортсмен, то дыхание у вас становится «поверхностным», т.е. дышите вы часто, но в каждом акте дыхание обмен газов собственно невелик, т.е. эффективность такого дыхания низкая, чтобы это как-то компенсировать, организм дополнительно повышает АД через повышение ЧСС, которая уже слишком высока и причиняет вам значительный дискомфорт. Вот вы останавливаетесь, начинаете дышать менее редко, зато глубоко – эффективность такой вентиляции выше, чем при поверхностном дыхании, концентрации газов в крови нормализуются, потребность в слишком высокой ЧСС отпадает, давление снижается до адекватного уровня, достаточного для такой вентиляции. Вот и всё про функциональную систему регуляции артериального давления, её схема кажется большой, но на самом деле из неё вам необходимо запомнить только органы для вегетативной регуляции, а остальные элементы у всех функциональных систем одинаковые, ну кроме самого объекта, конечно. А как запомнить эти органы? Вы должны запомнить 5 факторов, определяющих АД, а исходя из этих факторов (ну кроме фактора эластичности сосудов) вспомните органы, которые их определяют (сердце – сердце; тонус сосудов – резистивные сосуды; объём циркулирующей крови – почки; вязкость крови – печень, селезёнка, красный костный мозг).
В дополнение к теме мы должны обсудить особенности кровоснабжения некоторых органов и на этом закончим тему сердечно-сосудистой системы.
Особенности лёгочного кровообращения. По лёгочным артериям движется венозная кровь, а по лёгочным венам движется артериальная кровь, это связано с особенностями малого круга кровообращения (его задача доставить кровь к лёгким и обратно, чтобы она там оксигенировалась и лишилась углекислого газа). Между кровью в капиллярах малого круга кровообращения и воздухом внутри альвеол лёгких существует тонкая прослойка – аэрогематический барьер, который состоит из эндотелиоцитов и их базальной мембраны, периваскулярного пространства, базальная мембрана альвеолоцита, уплощенная часть самого альвеолоцита. Однако венозная кровь обеднена питательными веществами, а ткани лёгких вообще-то нуждаются в притоке питательных веществ, поэтому лёгкие дополнительно получают артериальное кровоснабжение от большого круга кровообращения, а вот венозный отток происходит только по малому кругу кровообращения (ну а зачем дополнительный венозный отток от большого круга кровообращения, нужды в нём особо нет).
Особенности коронарного кровообращения, т.е. кровоснабжения сердца. Сердце кровоснабжается коронарными артериями, которые выходят из луковицы аорты, снабжают перикард и миокард (эндокард снабжается кровью в самих камерах сердца), отток происходит по венам, которые открываются в правое предсердье. Самым интересным моментом в кровоснабжении сердца является кровоснабжение миокарда – в нём очень обширная сосудистая сеть, настолько, что каждый кардиомиоцит контактирует с капилляром, т.е. очень хорошо снабжён миокард. Ещё особенность состоит в том, что миокард постоянно сокращается, так вот в моменты систол камер сердца миокард в их составе сокращается и пережимает сосуды, а в диастолу расслабляется и раскрывает сосуды, т.е. кровоснабжение миокарда реально происходит только во время диастолы.
Особенности мозгового кровообращения. А вот это действительно интересный с клинической точки зрения вопрос. Поговорим конкретно о снабжении головного мозга. Оно осуществляется через две внутренние сонные и две позвоночные артерии, которые заходят с разных сторон в полость черепа. Позвоночные сливаются в базилярную, которая даёт ряд ветвей, в том числе задние мозговые, внутренние сонные тоже дают ряд ветвей, в том числе передние и средние мозговые. Ветви внутренних сонных и базилярной артерии образуют сеть анастомозов, называемую Велизиевым кругом. За счёт такого круга анастомозов по идее из 4-х магистральных сосудов мы можем блокировать 3, но мозг всё равно будет кровоснабжаться. Делать этого я вам не рекомендую, ибо кровообращение серьёзно нарушится, потому что такая система не компенсирует всё полноценно, т.е. подстраховки в форме Велизиевого круга вам должно хватить, чтобы добраться до больницы, обследоваться и начать лечение, если вы будите долго ходить с блокированным магистральным сосудом, то это повлечёт повреждения сосудов и самого мозга. Но открою вам страшный секрет: полноценный Велизиев круг имеется лишь у 20% людей, у остальных же 80% какие-либо анастомозы либо слишком узкие, либо и вовсе отсутствуют, т.е. страховка менее эффективная. Есть ещё один очень важный момент в кровоснабжении головного мозга – гематоэнцефалический барьер. Состав барьера: эндотелий и базальная мембрана капилляра, периваскулярное пространство, слой из плотно соединённых отростков астроцитов. Астроциты из своих отростков формируют трубку, внутри которой пролегает сосуд, именно астроциты решают, какие вещества из крови проникнут в нервную ткань, а какие нет, астроциты поглощают их, а потом отдают нейронам. Особенность гематоэнцефалического барьера в его крайне избирательной проницаемости, которая может изменяться при разных физиологических состояниях, данный барьер мешает попаданию многих лекарственных препаратов в мозг (вот это реально проблема), но при этом он также мешает многим токсинам попасть в нервную ткань.
Особенности почечного кровообращения. Почки состоят в основном из нефронов, которые состоят из капсулы Боумена-Шумлянского и почечного канальца. Об особенностях кровоснабжения теперь. Во-первых, к капсуле подходит приносящая артериола большого диаметра, разветвляется на капилляры, те собираются в выносящую артериолу, которая имеет меньший диаметр, из-за меньшего диаметра выносящей артериолы возникает повышенное сопротивление кровотоку, поэтому давление в капиллярной сети повышается, следовательно, жидкость из капилляров усиленно выходит в капсулу, за счёт чего происходит клубочковая фильтрация (плазма крови почти без белков проникает из кровеносного сосуда в полость нефрона – образуется первичная моча). Во-вторых, выносящая артериола затем снова разветвляется на капилляры вдоль канала нефрона, т.е. в почках имеется двойная капиллярная сеть. В-третьих, между приносящей и выносящей артериолами, капсулой и дистальным извитым канальцем сформирован юкста-гломерулярный аппарат, регулирующий давление в почечном кровообращении для поддержания нормальной клубочковой фильтрации (её движущей силой является давление). Ещё у почек существует такая особенность, как поворотно-противоточная система. Не знаю, насколько справедливо её относить к особенностям почечного кровообращения, но это спрашивают совместно некоторые преподаватели, поэтому расскажу. Вообще система сложная и до конца не исследованная, но разберём одну из главных её особенностей. Первичная моча спускается вниз по петле Генгле, в которой есть аквапорины (каналы, качающие воду из петли), вода из канала уходит в тканевую жидкость, поэтому первичная моча становится очень концентрированной, в ней много натрия, затем, поднимаясь по петле Генгле, натрий уходит из канала нефрона через ионные каналы, забирая с собой часть воды (он же осмотически активен) в тканевую жидкость (эта тканевая жидкость общая для нисходящей и восходящей частей петли Генгле, тканевая жидкость, получая натрий из восходящей части, становится более осмотичной и легче притягивает к себе воду через аквапорины из нисходящей части петли Генгле. Т.е. получается, что за счёт сообщения между собой (близкого прилегания) восходящей и нисходящей частей петли Генле и существования в ней аквапоринов и ионных каналов для натрия происходит существенное выкачивание воды из мочи и её концентрирования, получается, что моча имеет гораздо более высокую концентрацию ионов, чем кровь и осмотическое давление её выше, ибо многие из этих ионов осмотически активны.
Существует ещё такой вопрос, каким механизмом регулируется деятельность сердца в первое время после трансплантации? Помним, что существует 3 механизма регуляции: миогенный (в случае сердца его ещё называют гемодинамическим), гуморальный и нервный (рефлекторный). После пересадки нервам требуется время, чтоб прорасти, рецепторы по некоторым данным повреждены и им потребуется время, чтобы восстановиться, поэтому в первое время сердце работает на гемодинамической регуляции.
Последний вопрос – связь здорового образа жизни и профилактики заболеваний сердечно-сосудистой системы. Под здоровым образом жизни я имею ввиду нормальную двигательную активность, рациональное питание и отсутствие особо вредных привычек. Начнём с двигательной активности. Смотрите. В нашем теле протекает метаболизм, который заключается в синтезе и разрушении молекул (очень грубо говоря), причём метаболизм довольно активный в норме. Почему важно поддерживать метаболизм на нормальном уровне? А вот такая ситуация: в ходе нормальной жизнедеятельности все клеточные структуры повреждаются, после чего функционируют неправильно, большинство из них не репарируется, но благодаря высокому метаболизму эти дефектные структуры быстро разрушаются, а вместо них, синтезируются новые целые. Получается так, что все повреждённые части клетки быстро заменяются на новые нормальные. А если вы ведёте малоподвижный образ жизни, ваш общий уровень метаболизма снижается, тогда и обновление всех клеточных структур замедляется, и повреждения устраняются отнюдь не сразу, более того, они накапливаются, а повреждённые структуры клеток функционируют неправильно, что приводит к многочисленным заболеваниям. Также имеет смысл то, что независимо от того, нормальная у вас подвижность или нет, ваш аппетит сильно не меняется, поэтому потребляете вы нормальное количество калорий, а сжигаете мало, поэтому вы набираете лишний вес, что может со временем привести к ожирению (имейте ввиду, что лишние калории откладываются не только в форме нейтральных жиров, но и в форме холестерола, избыток которого в крови приводит к развитию атеросклероза), оно приведёт к сахарному диабету 2-го типа, а тот в свою очередь способствует развитию атеросклероза и патологиям печени, что ещё больше увеличит вероятность развития атеросклероза. В нашей крови существуют липопротеины высокой плотности, которые с помощью фермента ЛХАТ (лицетинацилхолестеролтрансфераза) изымают холестерол из клеток, затем уносят его в печень, которая выводит его из организма в виде желчных кислот, т.е. эти липопротеины и фермент способствуют снижению количества холестерола в организме, снижая риск развития атеросклероза. ЛХАТ тем активнее, чем выше ваша физическая активность. Ну вот и получается, что низкая физическая активность, малоподвижный образ жизни так или иначе приводит к развитию атеросклероза. Что касается рационального питания? Неправильное питание может приводить к самым разнообразным заболеваниям, но рассмотрим только те моменты в питании, которые приводят к поражениям сердечно-сосудистой системы. Высокая калорийность (за счёт жиров и углеводов) приводит как к синтезу нейтральных жиров (опасно ожирением, которое вызывает сахарный диабет 2-го типа, жировое перерождение печени с возможным последующим некрозом и атеросклероз), так и к излишнему синтезу холестерола (прямой риск развития атеросклероза). Также повышение содержание холестерола в организме может быть следствием его избыточного поступления с пищей. Атеросклероз также может запускаться окислительным стрессом, который может развиваться вследствие недостатка таких антиоксидантов, как витамины А, С, Е (ни для кого не секрет, что многие люди страдают гиповитаминозом по многим витаминам). Многие люди недополучают с пищей полиненасыщенные жирные кислоты, к которым относятся и омега-3-жирные кислоты, которые способствуют растворению и выведению холестерола из организма, хроническая недостаточность полиненасыщенных жирных кислот повышает риск развития атеросклероза. В настоящее время в пище очень много пищевых добавок, которые относятся к пищевым ксенобиотикам, частое поступление которых сказывается на функциях печени, а печень занимает центральное место в метаболизме белков и аминокислот, углеводов и липидов, следствием поражения печени могут стать разнообразные заболевания, в том числе и атеросклероз. При условии генетической предрасположенности у вас может развиться сахарный диабет второго типа при злоупотреблении быстрыми углеводами (многие этим грешат). Злоупотребление алкоголем приводит к ацетилированию всех ферментов печени и выведению их из строя (просто при обезвреживании этиловый спирт быстро превращается в ацетальдегид, а тот превращается в уксусную кислоту, но медленно, поэтому при обильном поступлении в организм этилового спирта, ацетальдегид накапливается и инактивирует фермент печени, выводя её из строя), итогом обезвреживания этилового спирта является ацетил-КоА, из которого синтезируются жирные кислоты, а потом нейтральные жиры, которые могут способствовать развитию жирового перерождения печени, а то приведёт к атеросклерозу. Как видите, все патогенетические факторы приводят нас к атеросклерозу. Чем он опасен? Если он поражает амортизационные сосуды (аорта – излюбленное место), то он снижает их эластичность (атеросклеротические бляшки крайне жёсткие), что приводит к развитию патологической гипертрофии и артериальной гипертензии, затем к инфаркту миокарда. Также атеросклеротические бляшки в резистивных сосудах не позволяют активно менять просвет, регулируя кровоснабжение тканей в соответствие их потребностям, вместо этого просвет постоянно узкий, а ткани страдают от гипоксии в связи с недостаточным кровоснабжением, что приводит к нарушению функций этой ткани. Более того, в области атеросклеротической бляшки вполне может сформироваться тромб в следствие нерабочего эндотелия (эндотелий сосудов тормозит излишнее тромбообразование, но в области бляшки он не работает), который может полностью перекрыть сосуд – острое нарушение кровообращения, что очень опасно для тканей. Особенно для мозга. Такое нарушение кровообращения в мозге называется ишемическим инсультом, а если забитый сосуд ещё и лопнет, то это будет геморрагический инсульт. В общем атеросклероз обусловливает большинство болезней сердечно-сосудистой системы, а факторов, способствующих его развитию, очень много, он может быть обусловлен генетически, но в подавляющем большинстве случаев он обусловлен вашим образом жизни, что мы только что и обсудили. Мы ничего не сказали про курение и приём наркотиков. Табачный дым содержит более 3000 ядовитых веществ и способен вызывать огромное множество заболеваний, точнее не вызывать, а способствовать их развитию, атеросклероз в их числе. При осуществлении внутривенного введения наркотического препарата непрофессионалами очень часто происходит занесение в кровь инфекции, которая может разрушать створки клапанов сердца (довольно частые случаи). Гораздо подробнее вы рассмотрите механизмы всех приведённых явлений, в том числе и атеросклероза, в курсе биохимии.
