
- •Физиология и биофизика возбудимых тканей.
- •Регуляция физиологических функций.
- •Физиология эндокринной системы.
- •Физиология центральной нервной системы.
- •Физиология сердечно-сосудистой системы.
- •Физиология дыхания.
- •Физиология пищеварительной системы.
- •Физиология обмена веществ и терморегуляция.
- •Физиология выделения.
- •Физиология крови.
- •Физиология сенсорных систем.
- •Физиология высшей нервной деятельности.
Физиология крови.
Общие аспекты физиологии крови.
Разбирая любую тему в физиологии, мы практически всегда говорим о внешней и внутренней средах. Нужно понимать разницу между ними. Всё, что находится вне организма, а также полости тела, сообщающиеся со внешней средой (полости ЖКТ, дыхательные пути и тд) относятся ко внешней среде, а цитоплазма клеток, межклеточное вещество, лимфа, кровь, ликвор, замкнутые полости (плевральная, брюшинная и тд) относятся ко внутренней среде. Внутренняя среда отграничена (относительно) от внешней и в ней поддерживается гомеостаз, этим внутренняя среда отличается от внешней. Основными компонентами внутренней среды являются кровь, лимфа и тканевая жидкость – они по сути объединяют весь организм и в определённом смысле постоянно переходят друг в друга, другими словами, сообщаются. В связи с таким статусом по составу и свойствам данных жидкостей можно судить о многих процессах, происходящих в организме. А самой главной и «информативной» биологической жидкостью и компонентом внутренней среды является кровь. Причина такой показательности крови заключается в том, что на большинство патологических процессов организм реагирует системно, а кровь в нём выполняет интегративную (объединяющую функцию), т.е. она в эти реакции обязательно включается, а вторая причина заключается в том, что даже если системной реакции нет, то патологический очаг всё равно контактирует с кровью, а потому может на неё влиять. Например, у человека есть острое местное воспаление, но, несмотря на то, что оно местное, общая реакция организма присутствует, которая со стороны крови характеризуется увеличением количества лейкоцитов как в целом, так и конкретных (нейтрофилов обычно), также изменяется количество и соотношение белков плазмы крови. По этой причине при диагностике самых различных заболеваний практически всегда назначают тот или иной вид анализа крови.
Перед тем, как начать разговор о самой крови, нужно сказать, что такое система крови. Система крови – это совокупность органов, участвующих в продукции и разрушении основных составляющих крови, а также собственно кровь (она не орган, а ткань). Органы, продуцирующие основные элементы крови: красный костный мозг (создаёт все форменные элементы в той или иной степени дифференцировки), печень (создаёт большинство белков плазмы крови), тимус (антигеннезависимая дифференцировка лимфоцитов), лимфатические узлы (антигензависимая дифференцировка лимфоцитов). Органы гемолиза (утилизаторы эритроцитов): красный костный мозг, селезёнка, лимфатические узлы, печень. Кстати печень ещё и белки крови при необходимости может утилизировать.
Функции крови. Функций у крови довольно много, однако по сути есть две основные (интегративная и защитная), а остальные функции являются их следствием.
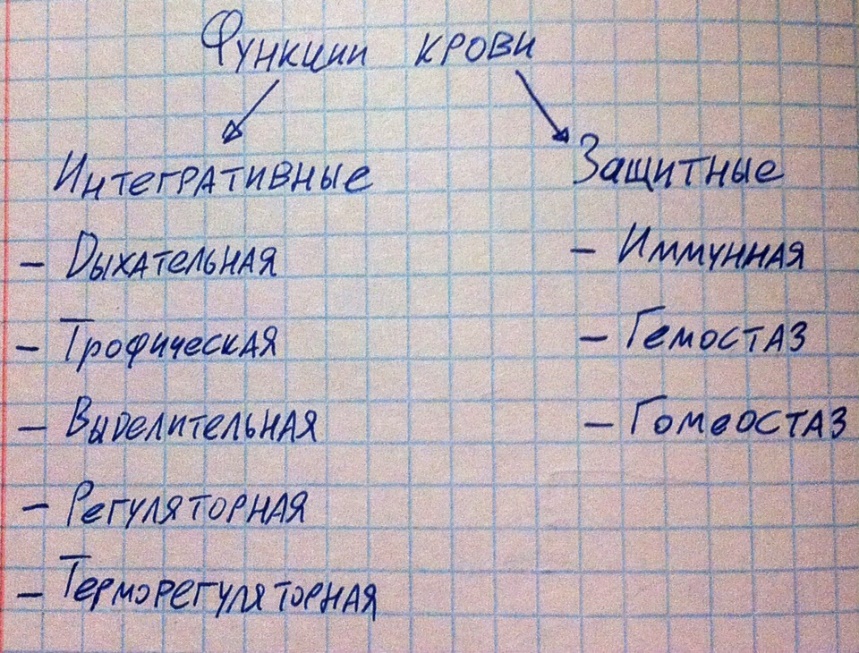
Суть интегративной функции заключается в том, что подавляющее большинство наших тканей кровоснабжаются, следовательно, с помощью крови молекула может попасть из одной любой точки организма в любую другую точку организма. Т.е. интегративная функция = транспортная, а в зависимости от того, что транспортируется, функции называют конкретнее: транспорт газов - дыхательная функция; транспорт питательных веществ – трофическая функция; транспорт конечных продуктов обмена – выделительная функция; транспорт гормонов – регуляторная функция; транспорт тепла – терморегуляторная. Насчёт последней функции надо немного пояснить. Кровь выступает теплоносителем в нашем организме, например, в условиях гипотермии в организме повышен катаболизм, чтобы ткани согрелись, но большинство тканей разогреваются слабо, а вот печень очень сильно, кровь, проходит через печень, забирает часть тепла, приходит в холодные ткани и отдаёт его им.
Что касается защитных функций? Иммунитет – система защиты организма от чужеродного генетического материала или собственного трансформировавшегося. В крови содержатся и клеточные (лейкоциты) и гуморальные (комплимент, антитела) эффекторы иммунитета. Гемостатическая функция подразумевает, что при необходимости кровь может сворачиваться с целью остановки кровотечения (хотя гемостаз может и по другим причинам включаться). Гомеостатическая функция заключается в том, что в крови есть резервы для поддержания гомеостаза, например, буферные системы крови препятствуют сильному изменению pH.
Состав циркулирующей крови. Кровь имеет две основные составляющие: плазму (жидкость) и форменные элементы (твёрдая часть). На долю плазмы приходится 55-60% от крови, доля воды от всей плазмы 90%, доля белков – 7%, доля прочей органики – 2%, доля минеральных веществ – 1%. Доля же форменных элементов от крови составляет 40-45%, среди них на долю эритроцитов приходится 96%, на долю лейкоцитов – 3%, на долю тромбоцитов – 1%.
Константы крови. Константа – это «постоянная», в случае с кровью константой мы называем диапазон нормальных значений того или иного фактора крови. Эти константы разделяют на жёсткие и пластичные. Жёсткие константы обычно имеют узкий диапазон, а отклонение от них на небольшие значения уже может приводить к последствиям для организма. К жёстким константам относятся: pH, порциальное напряжение кислорода и углекислого газа, осмотическое и онкотическое давление крови, ионный и белковый состав крови. Пластичные константы имеют часто более широкий диапазон, к последствиям для организма приводят только сильные отклонения от таких констант. К пластическим константам относятся: объём и вязкость циркулирующей крови, гематокрит и скорость оседания эритроцитов (СОЭ), количество форменных элементов и гемоглобина.
Некоторые константы мы должны разобрать подробно.
Гематокрит. Гематокрит – это доля форменных элементов от крови. В норме у женщин составляет 41-45%, у мужчин 44-48%. Гематокрит во многом определяет вязкость крови, а также может указывать на скрытые кровотечения и является показателем уровня кровопотери (чем ниже гематокрит, тем хуже). Дело в том, что при кровотечениях организм компенсирует потерянный объём крови за счёт жидкости, но не за счёт форменных элементов (этот процесс включается гораздо позже и медленнее протекает), поэтому в крови доля форменных элементов будет уменьшаться.
Гематокрит по большей части определяется содержанием в крови эритроцитов, которое регулируется системой крови.
Физиологические изменения гематокрита происходят при адаптации к высокогорью – увеличивается кислородная ёмкость крови за счёт увеличения числа эритроцитов. Патологическое снижение гематокрита может быть связано с кровопотерей или некоторыми видами анемии. Патологическое увеличение гематокрита может быть связано с сильным обезвоживанием (теряется жидкость крови, а доля форменных элементов, соответственно, становится выше при неизменном их количестве).
Осмотическое давление крови. По сути это сила, с которой кровь притягивает в себя воду, обусловленная высоким содержанием в крови осмотически активных веществ (в основном неорганических ионов типа натрия, кальция, хлорида). В норме составляет примерно 7,3 атмосферы.
Осмотическое давление крови определяется концентрацией в ней осмотически активных ионов. В основном это давление регулируют почки, ибо они являются дирижёрами водно-солевого обмена.
Патологическое изменение осмотического давления крови связано с изменением концентрации в ней осмотически активных ионов, что происходит при потере или задержке ионов в организме, а также при потере или задержки воды в организме (если количество ионов неизменно, а вода теряется, то концентрация и осмотическое давление растёт). Это может происходить при патологиях почек, длительных рвоте или поносах, обильном потоотделении.
Онкотическое давление крови. Это сила, с которой белки плазмы крови притягивают воду в кровь, т.е. онкотическое давление подобно осмотическому, но вызывают его не осмотически активные ионы, а белки (в основном альбумины). В норме составляет 25 мм рт ст. Это давление важно для поддержания правильной микроциркуляции.
Онкотическое давление крови определяется содержанием в ней альбуминов, которые синтезируются печенью, так что основным регулятором онкотического давления крови является печень.
Количество альбуминов и, соответственно, онкотическое давление крови могут понижаться по довольно большому ряду причин: длительный дефицит незаменимых аминокислот в организме (в таком случае они изымаются из альбуминов), общее длительное голодание (альбумины разбираются до аминокислот, которые отправляются в глюконеогенез), острое воспаление различных органов и тканей (печень повышает продукцию альфа-глобулинов, но снижает продукцию альбуминов), различные патологии печени (сниженная функция печени выражается и в сниженной продукции альбуминов), кровотечения и плазморрагии (альбумины покидают сосудистое русло), некоторые патологии почек (при деструкции клубочков альбумины из крови проходят в нефрон, но механизмов для их реабсорбции нет, поэтому они покидают организм с мочой).
Отдельного внимания заслуживает такой вопрос, как pH крови.
Нормальные значения pH составляют 7,39-7,40, если ниже, то это ацидоз (закисление), если выше, то это алкалоз (защелачивание). При pH 7,35-7,38 наблюдается компенсированный ацидоз, при 7,34 и ниже – некомпенсированный. При pH 7,41-7,45 наблюдается компенсированный алкалоз, при 7,46 и ниже – некомпенсированный. Разница между компенсированным и некомпенсированным заключается в том, что при компенсированном отклонение pH под контролем и неопасно, а при некомпенсированном механизмы контроля pH истощены, а его значение чревато рядом патологических изменений в организме.
Ацидоз и алкалоз (некомпенсированные) крайне опасны для организма, так как вызывают нарушение кровообращения и вызывают гипоксии различных типов, механизмы которых вы подробно изучите в курсе патологической физиологии. Причины бывают разного характера: респираторные, метаболические, выделительные, экзогенные – всё это опять-таки на курсе патологической физиологии.
Поскольку ацидоз и алкалоз являются довольно опасными состояниями, а pH является жёсткой константой крови, в организме должны существовать соответственные защитные механизмы. Одними из главных таких механизмов служат буферные системы. Буферная система – это амфотерное вещество или комплекс двух гомологичных солей (в основе такой соли обычно лежит сильное основание и слабая кислота). Причиной ацидоза является увеличение концентрации протонов, а причиной алкалоза является увеличение концентрации гидроксид-иона. Основным же принципом работы любой буферной системы является связывание свободных протонов или гидроксид-ионов, что устраняет причину ацидоза/алкалоза.
Всего существует 4 типа буферов: карбонатный, фосфатный, белковый, гемоглобиновый.
Схема работы буферов изображена на рисунке ниже. Механизм работы карбонатного и фосфатного понятен из рисунка. Белковые же буферы работают за счёт амино- или карбоксильных групп в зависимости от заряда белка. Гемоглобиновые буферы работают несколько иначе, нежели белковые, ибо их буферная активность сопряжена с присоединение газов (гемоглобин присоединяет протон в комплексе с углекислым газом в связи с изменением конформации гемоглобина).

Во всех примерах я привёл случаи именно с ацидозом, так как наш организм гораздо чаще сталкивается именно с ним, поэтому и буферные системы в основном нацелены на борьбу с ацидозом.
Функциональная система поддержания постоянного pH.
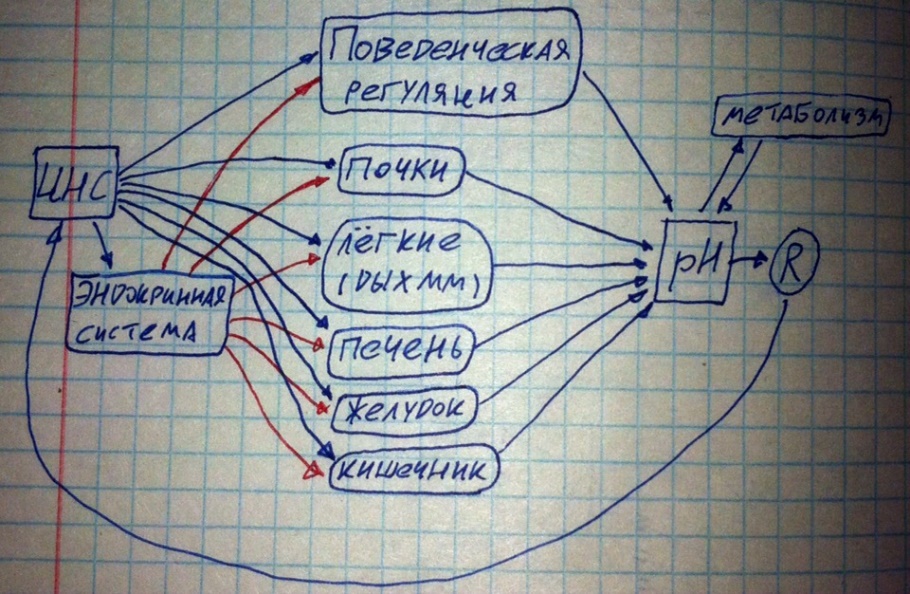
Кислотность среды воспринимается хеморецепторами, расположенными в рефлектогенных областях магистральных сосудов и в головном мозге. Главный центр по данным вопросам расположен в гипоталамусе, но ещё участвует и дыхательный центр.
Конечно, мы говорили о том, что существуют буферные системы, которые связывают протоны и гидроксид-ионы, препятствуя развитию ацидоза/алкалоза, но в том-то и дело, что они связали причинный ион, но из организма не вывели, для последнего и существуют органы, которые мы указали на рисунке функциональной системы. Разберёмся в особенностях их работы.
Лёгкие, а если быть точным, то дыхательные мышцы. Уровень лёгочной вентиляции определяет содержание углекислого газа в крови (чем интенсивнее вентиляция, тем сильнее «выветривается» углекислый газ), который, в свою очередь, закисляет кровь, так как может превращаться в угольную кислоту, способную диссоциировать и давать протоны. Лёгочная вентиляция способна очень быстро изменять свою интенсивность и существенно влиять на pH крови, поэтому это один из главных регуляторов (начальная мера по борьбе с ацидозом/алкалозом). Кстати этот механизм работает даже если причина ацидоза/алкалоза не в углекислом газе.
Почки. Являются одним из главных механизмов регуляции, особенно в долгосрочной перспективе. Почки в основном настроены на борьбу с ацидозом. Существует 4 механизма по выведению протонов из организма (запоминать их, пожалуй, необязательно).
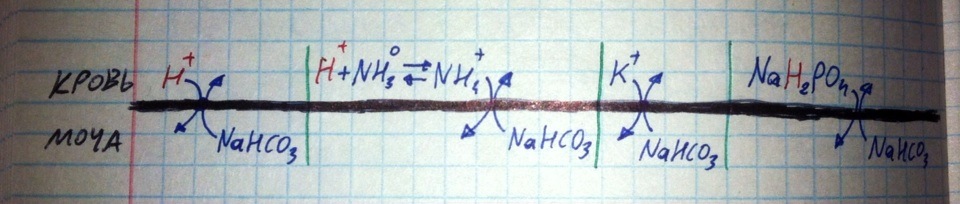
Как видите, организм выводит протоны (фактор ацидоза), но всасывает натрий и гидрокарбонат, которые образуют соль со слабощелочной реакцией, плюс происходит восполнение ёмкости карбонатного буфера – всё это противостоит ацидозу. В случае алкалоза все эти механизмы просто угнетаются.
Органы желудочно-кишечного тракта. Они в меньшей степени участвуют в регуляции pH крови. В основном это делает печень. При ацидозе она запускает глюконеогенез, в котором расходуются различные кислоты (пируват, лактат, щавелеуксусная кислота и тд), чем больше кислот израсходует, тем меньше те будут давать протонов и тем слабее ацидоз. В случае алкалоза печень активирует различные пути катаболизма, в основном гликолиз, ПДК, ЦТК, в которых образуются кислые продукты, что нейтрализует алкалоз. Желудок же секретирует в свой просвет кислое содержимое, а кровь при этом защелачивает. Кишечник (да и поджелудочная) секретируют слабо щелочное содержимое, а кровь закисляют.
Что можно сказать о поведенческой регуляции? Человек может употребить в пищу кислые или щелочные продукты питания для нейтрализации ацидоза/алкалоза.
В плане взаимоотношений метаболизма и pH всё просто. Чем активнее метаболизм, тем кислее среда (продукты катаболизма кислые). Сильное изменение pH нарушает метаболизм, так как все ферменты имеют свой pH-оптимум, выход за пределы которого чреват снижением активности ферментов.
Функциональная система обеспечения постоянства осмотического давления крови.
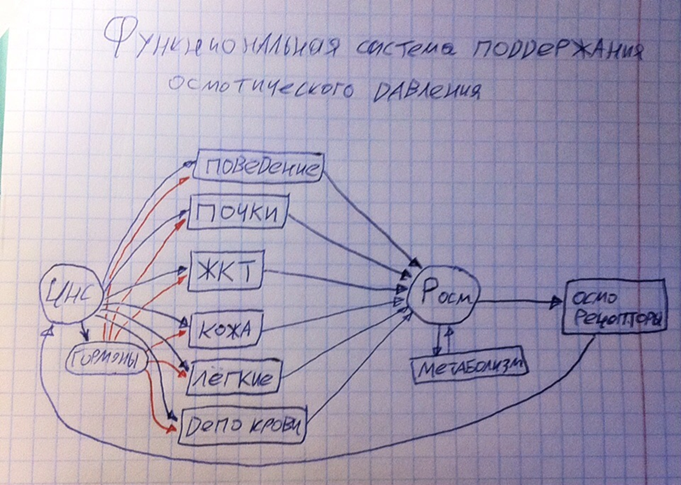
Основные рецепторы и нервные центры расположены в гипоталамусе. Осмотическое давление крови регулируется через концентрацию осмотически актвиных ионов. По большей части эта задача ложится на почки, которые могут изменять реабсорбцию данных ионов и воды. Органы ЖКТ, кожа (потовые железы) и лёгкие могут выделять секреты, содержащие воду и данные ионы, что может приводить к изменению концентрации их в крови.
Депо крови здесь даётся в том плане, что в случае чего оно сгладит перепад осмотического давления. Каким образом? Ну грубо говоря, в нормальной крови 0,9% хлорида натрия, так уж вышло, что в циркулирующей крови (4 л, допустим) концентрация упала до 0,7%, т.е. осмотическое давление упадёт, тогда из депо крови целый литр крови с концентрацией хлорида натрия 0,9% выйдет и тоже будет циркулировать по сосудам, тогда концентрация хлорида натрия в циркулирующей крови уже будет 0,74%, что уже немного получше. Т.е. грубо говоря, депо крови – это «запаска» не только по жидкости и форменным элементам, но и по осмотически активным ионам.
Белки плазмы крови. Как мы говорили ранее, белков в крови довольно много (7% от всей плазмы крови), и выполняют они довольно много функций (большинство функций крови).
Представителей белков много, поэтому они нуждаются в классификации, в основе которой лежит их подвижность в электрофорезе, выделяют 3 основных класса белков: альбумины, глобулины, фибриноген.
Альбуминовые белки разделяют на преальбумины и альбумины. Преальбумины связывают и транспортируют тироксин и ретинол (витамин А). Альбумины же вообще переносят почти все гидрофобные молекулы (у него много специальных кластеров для таких дел).
Глобулины разделены на альфа, бета и гамма. Среди альфа есть альфа-1-группа и альфа-2-группа. Кто есть среди альфа-1-группы? Альфа-1-глобулин является иммуномодулятором. Антитрипсин ингибирует протеазы крови. Альфа-1-фетопротеин переносит жирные кислоты от матери к плоду через плаценту. Кто есть среди альфа-2-группы? Церрулоплазмин связывает и транспортирует медь. Гаптоглобин связывает гемоглобин и не даёт ему выйти с мочой. Альфа-2-макроглобулин ингибирует протеазы крови. Кто есть среди бета-глобулинов? Трансферрин связывает и транспортирует железо. Гемопексин связывает и уничтожает гем. С-реактивный белок выступает иммуномодулятором и является медиатором воспаления. А гамма-глобулины - это антитела, их функции и разновидности вы узнаете на кафедре микробиологии. Также нужно знать, что альфа-глобулины – это белки ответа острой фазы (их количество существенно возрастает при остром воспалении). Я привёл только некоторые примеры белков, так-то их, конечно, больше.
С фибриногеном должно быть всё понятно – это первый плазматический фактор свёртываемости крови, из него образуется фибрин, который полимеризуется и позволяет формировать липкую сеть для кровяного сгустка, который призван запечатать дыры в сосудах и предотвратить кровепотерю.
Мы привели функции отдельных белков, а если же перечислить функции вообще всех белков плазмы крови в целом, то получим следующие: транспортная (альбумины переносят липофильные вещества), регуляторная (альбумины переносят некоторые гормоны), иммунная (альфа-глобулины участвуют в остром воспалении, а гамма-глобулины являются гуморальными эффекторами специфического иммунитета), регуляция жидкого состояния крови (белки свёртывающей, противосвёртывающей и фибринолитической систем), гомеостатическая функция (примеров много, но вот альбумины поддерживают онкотическое давление).
Скорость оседания эритроцитов. Измеряется специальным размеченным прибором, с работой которого вы подробно ознакомитесь в руководстве к лабораторным работам. В норме у мужчин составляет 1-10 мм/ч, у женщин 2-15 мм/ч. СОЭ определяется соотношением белков плазмы крови. При остром воспалении в крови альбуминов становится меньше (печени не до них), а альфа-глобулинов становится больше (печень сосредоточена на их синтезе), при таком соотношении белки снижают (по модулю) отрицательный заряд эритроцитов, в результате чего тем проще слипаться и оседать (отрицательный заряд на мембране эритроцитов отталкивает их друг от друга и не даёт слипаться). Таким образом, повышение СОЭ свидетельствует о наличии острого воспаления.
Форменные элементы крови. Выше мы обсудили все моменты, касающиеся плазмы крови, теперь перейдём к «твёрдой» части крови – форменным элементам.
Эритроциты. Нормальное содержание 3,7-5,0 * 10^12 шт/л. Главные функции: транспорт газов (углекислого и в особенности кислорода) и буферная (гемоглобиновый буфер, довольно мощный). Второстепенные функции: транспорт некоторых питательных и биологически активных веществ, перенос группа-специфических белков (группы крови, например).
Лейкоциты. Нормальное содержание 4-9 * 10^9 шт/л. Представлены нейтрофилами, эозинофилами, базофилами, лимфоцитами, моноцитами. Процентное соотношение лейкоцитов называется лейкоцитарной формулой. Выглядит она следующим образом.
Лейкоциты |
Доля от общего |
Нейтрофилы |
47-72% |
Эозинофилы |
0,5-5% |
Базофилы |
0-1% |
Лимфоциты |
18-40% |
Моноциты |
2-9% |
Однако имейте ввиду, что в разных источниках данные могут несколько отличаться. Данную формулу необходимо знать наизусть. В клинической практике она имеет большое значение, например, повышение содержания нейтрофилов может указывать на острое воспаление, а повышение эозинофилов – на развитие аллергической реакции 1-го типа.
Нейтрофилы. Основная функция – фагоцитоз, причём нейтрофилов относят к так называемым «микрофагам», так как они способны поглощать только мелкие объекты вроде бактерий и «обломков» клеток. Киллерная функция: бактерию недостаточно поглотить, её нужно ещё и убить, для чего есть специальные факторы (лактоферин, катионные белки, лизоцим, липопероксидаза). Данные клетки являются основными при остром воспалении.
Эозинофилы. Основных задач две: противопаразитарное действие и антагонизм базофилов. Противопаразитарное действие осуществляется следующим образом: на поверхности паразита имеются антигены, к ним могут присоединяться антитела или комплимент, а у эозинофилов есть рецепторы к антителам и комплименту – так эозинофилы распознают цель, далее они продуцируют вещества, повреждающие клетки паразитов. Антагонизм базофилам проявляется следующим образом: базофилы выделяют гистамин, а эозинофилы выделяют гистаминазу (разрушают гистамин), базофилы выделяют гепарин, а эозинофилы выделяют арилсульфатазу (разрушает гепарин). Антагонизм базофилам можно назвать антиаллергической функцией.
Базофилы. Участвуют в воспалительных и аллергических реакциях, с помощью гистамина расширяют сосуды, с помощью гепарина повышают их проницаемость. Базофилы, вышедшие из сосуда (остаются в периваскулярном пространстве) называются тучными клетками.
Лимфоциты. Т-киллеры оказывают цитотоксическое действие различными путями (секреция повреждающих веществ). Т-хелперы участвуют в антигензависимой дифференцировке лимфоцитов. В-лимфоциты (точнее плазмоциты) занимаются продукцией антител.
Моноциты. Способны трансформироваться в макрофаги, эпителиоидные и гигантские клетки (суть это не сильно меняет, это больше представляет интерес для морфологической диагностики). Они способны к фагоцитозу довольно крупных объектов, в отличии от нейтрофилов. Моноциты также обладают киллерным действием. Однако важно отметить, что макрофаги вообще являются «дирижёрами» воспалительных реакций, ибо выделяют множество биологически активных веществ, регулирующих все процессы, протекающие при воспалении.
Преобладание лимфоцитов и макрофагов в очаге свидетельствует о хроническом воспалении.
По лейкоцитам необходимо запомнить их количество, формулу и основные функции, а описанные механизмы приведены просто для наглядности и понимания.
Тромбоциты. Нормальное содержание в крови 180-320 * 10^9 шт/л. Конечно, первостепенная функция – обеспечение гемостаза (свёртываемость крови), тромоциты сами по себе составляют основу кровяных сгустков, да ещё и продуцируют свои факторы свёртываемости крови. Помимо этого, они имеют группа-специфические белки и обеспечивают трофику внутренней стенки сосудов.
Гемоглобин. Этот белок не относится к белкам плазмы крови, так как находится внутри эритроцита (пожалуйста, не путайте). Гемоглобин является основным белком эритроцитов, так как составляет 90% от всех белков эритроцитов.
Структура гемоглобина. Это сложный олигомерный глобулярный белок. Имеет 4 субъединицы (потому олигомерный), субъединицы в форме глобул (потому глобулярный), в каждой субъединице имеется железосодержащая простетическая группировка – гем (потому сложный). За счёт олигомерности белок обладает свойством кооперации (способность субъединиц повышать сродство к лиганду после присоединения этого лиганда к одной из субъединиц), что обуславливает форму кривой диссоциации оксигемоглобина в зависимости от порциального напряжения кислорода (см. тему физиологии дыхания). Более подробно структура гемоглобина рассматривается в курсе биохимии.
Физиологические виды гемоглобина. Существует полиморфизм гемоглобина (общее строение, функции и свойства меняются не сильно). У взрослых 98% гемоглобина – гемоглобин А (2 альфа-цепи, 2 бета-цепи), 2% гемоглобина А2 (2 альфа-цепи, 2 дельта-цепи). У эмбриона в первое время эмбриональный гемоглобин (2 кси-цепи, 2 эпсилонт-цепи), а чуть позже у него появляется на долгое время фетальный гемоглобин (2 альфа-цепи, 2 гамма-цепи).
Патологические виды гемоглобина. Гликозилированный гемоглобин HbA1c (образуется при длительной гипергликемии при сахарном диабете, плохо функционирует), гемоглобин разновидности А3 (к нему присоединён глутатион), мет-гемоглобин (железо имеет заряд +3, вместо +2 – это серьёзно нарушает его функцию).
Соединения гемоглобина с газами. Комплекс кислорода и гемоглобина называется оксигемоглобином (одна молекула гемоглобина присоединяет до 4-х молекул кислорода). Комплекс гемоглобина и углекислого газа называется карбогемоглобином. Карбогемоглобин и оксигемоглобин являются непрочными соединениями, при изменении порциального давления/напряжения газов и pH они могут легко диссоциировать, что физиологически значимо, а вот соединение гемоглобина с угарным газом – карбоксигемоглобин – крайне прочное и едва ли диссоциирует, что нарушает функцию гемоглобина, не позволяя ему переносить нормальные для организма кислород и углекислый газ. Карбогемоглобин и карбоксигемоглобин не путайте, пожалуйста.
Содержание гемоглобина в крови. Норма для мужчин 130-160 г/л, для женщин 120-150 г/л. Данный параметр крайне важен, так как именно количество гемоглобина определяет кислородную ёмкость крови, снижение уровня гемоглобина может приводить к гипоксии, которая негативно влияет на все органы и системы. Два основных состояния, при которых снижается содержание гемоглобина: кровопотеря (мы просто теряем эритроциты, а с ними и гемоглобин) и анемии (разновидностей и причин у этой группы болезней множество, количество эритроцитов при них может быть нормальным или сниженным). Существует множество методов определения концентрации гемоглобина в крови, но все они так или иначе построены на измерении длины световой волны (грубо говоря, чем краснее кровь, тем больше в ней гемоглобина), так как гемоглобин – это пигмент (молекула, имеющая цвет).
Гемолиз. Если переводить данный термин дословно, то он означает разрушение крови (гемо = кровь; лиз = разрушать). Однако на самом деле гемолиз – это процесс разрушения эритроцитов. видов гемолиза довольно много, его классификаций тоже.
Классификация по значению. По значению гемолиз может быть физиологическим и патологическим. Физиологический гемолиз протекает в красном костном мозге, лимфатических узлах, печени и селезёнке, ему подвергаются старые деструктивные эритроциты. Этот процесс необходим, чтобы отработанные эритроциты сменялись новыми, нормально функционирующими. Напоминаю, что у эритроцитов нет ядра, а потому нет генетического материала, который поддерживал бы обновление клетки, поэтому клетка со временем копит поломки и приходит в негодность – отсюда необходимость в утилизации. Патологическим же гемолизом можно считать разрушение относительно нормальных и молодых эритроцитов вне органов нормального гемолиза.
Классификация по месту. Гемолиз может быть внутрисосудистым и внесосудистым (при кровоизлияниях в ткани).
Классификация по этиологическому фактору. Эта классификация для патологического гемолиза. Этиологические факторы можно разделить на 3 типа: физические, химические, биологические.
К физическим факторам относятся ионизирующие излучения, сильное повышение температуры, изменение осмотического давления. Про осмотическое давление нужно знать конкретно механизмы. Если осмотическое давление раствора равно таковому в эритроците, то с эритроцитом ничего не происходит. Если раствор гипоосмотический, то в эритроцит за счёт осмоса поступает вода, он надувается и лопается – осмотический гемолиз. Если же раствор гиперосмотический, то осмосом вода выходит из эритроцита в раствор, эритроцит сморщивается (возможна необратимая деструкция).
Раствор |
Реакция эритроцита |
Механизм |
Норм осмоляльность |
Нет реакции |
Нет причин для каких-либо процессов |
Гиперосмоляльный |
Сморщивание эритроцита |
Вода осмотически выходит из эритроцита в раствор |
Гипоосмоляльный |
Гемолиз |
Вода осмотически входит из раствора в эритроцит и тот лопается |
Однако очень важно ввести такое понятие, как осмотическая резистентность эритроцитов. Это способность эритроцитов сохранять форму при изменении осмоляльности раствора. Что это значит на практике? Раствор хлорида натрия 0,9% для наших эритроцитов условно нормальной осмоляльности, а вот 0,8% уже гипоосмоляльный, но эритроцит при 0,8% надуваться и лопаться не станет, он начнёт «сдаваться» только где-то на 0,5%, например, т.е. у эритроцитов есть «запас прочности» на случай колебаний осмотического давления крови.
К химическим факторам относят различные токсические соединения. Например, мышьяк и нафталин.
К биологическим факторам относятся яды, производимые живыми организмами, а также возможна прямая деструкция (малярийный плазмодий механически разрушает эритроциты).
Физиология системы поддержания жидкого состояния крови.
Гемостаз. Гемостаз – процесс свёртывания крови. По сути кровь переходит в более плотное состояние, делается это с целью остановки кровотечения. Процесс, конечно, очень важный, ведь существенные кровопотери восполняются достаточно медленно, а нарушенная гемодинамика при этом осложняет работу всех органов.
Выделяют 2 основных типа гемостаза: сосудисто-тромбоцитарный и плазмо-коагуляционный.
Сосудисто-тромбоцитарный. Такой вид гемостаза протекает в довольно мелких сосудах. Последовательность процессов для наглядности приведена на рисунке ниже.
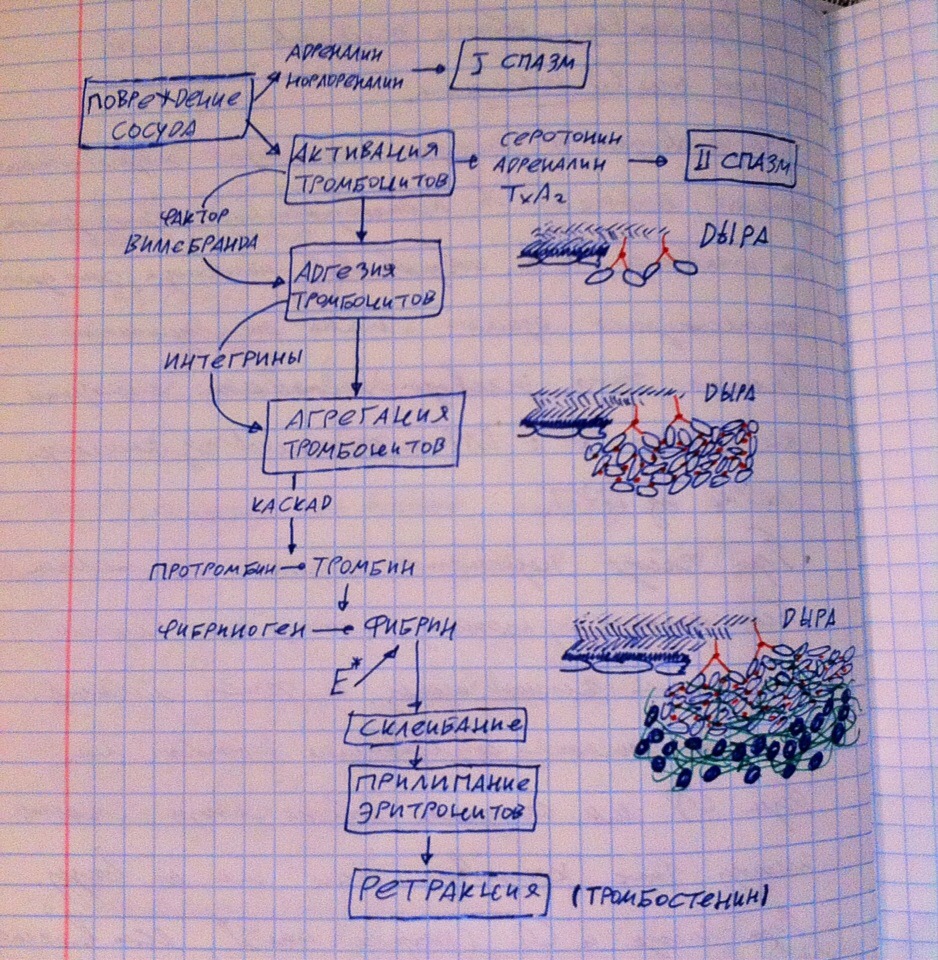
В данном виде гемостаза выделяют следующие стадии: первичный спазм сосуда, образование тромбоцитарной пробки, ретракция тромбоцитарной пробки.
Если максимально упростить, то суть будет следующая. Фаза первичного спазма. Повреждённый сосуд спазмируется, что хорошо, потому что через суженный сосуд в принципе меньше крови проходит, следовательно, и кровопотеря ниже. Фаза образования тромбоцитарной пробки. Повреждённый эндотелий сосуда перестаёт подавлять тромбоциты, те в месте повреждения сосуда начинают активироваться и выделять биологически активные вещества, позволяющие им прилипать к краям «дыры» в сосуде и друг к другу – так тромбоциты залепляют всю «дыру», образуя «белый тромб», который не пропускает через себя форменные элементы, но пропускает плазму, т.е. утечка жидкости всё ещё есть. По этой причине активируются факторы свёртывания крови, образуется фибрин, который «склеивает» белый тромб (выступает в роли герметика), после чего тот становится непроницаемым для плазмы, к фибрину могут прилипать эритроциты – образуется «красный тромб». Фаза ретракции. Тромбоциты имеют белок тромбостенин, который позволяет им по сути сжиматься, чтобы тромбоцитарная пробка стала плотнее и меньше перекрывала просвет сосуда (так надёжнее и удобнее). Вот такое описание – это минимум, который вам следует запомнить, для удобства смотрите на рисунок (подключайте зрительную память) – на рисунке изображено, как тромбоциты на месте повреждения слипаются, образуя белый тромб, потом склеиваются фибрином, потом приходят эритроциты, потом ретракция.
Теперь подробное описание механизма. Фаза первичного спазма сосуда. При повреждении эндотелия из него высвобождается много адреналина и норадреналина, которые обладают вазоконстрикторным действием, отсюда спазм, который снижает кровопотерю. Фаза образования тромбоцитарной пробки. В норме эндотелий выделяет противоагрегационные вещества, подавляющие активность тромбоцитов (чтоб они не клеились), но повреждённый эндотелий делать этого не может, поэтому на месте «дыры» тромбоциты начинают активироваться и выделять ряд биологически активных веществ: серотонин, адреналин и тромбоксан А2 вызывают вторичный спазм сосуда (продливают спазм, чтобы хватило времени на образование тромба), а фактор Виллибранта запускает адгезию тромбоцитов. Адгезия – прилипание тромбоцитов к краям повреждённого сосуда (к базальной мембране, если быть точным). Фактор Виллибранта одним концом прилипает к сосуду, а двумя другими к тромбоцитам – так и осуществляется адгезия. Затем тромбоциты высвобождают интегрины (помогают слипанию тромбоцитов) и вырабатывают множество АДФ для снижения поверхностного заряда (чем ниже заряд на поверхности тромбоцитов, тем им легче слипаться, ведь они больше не отталкиваются одноимённым зарядом) – эти факторы способствуют агрегации тромбоцитов (агрегация – слипание тромбоцитов друг с другом). Как я и сказал, образуется белый тромб (белая тромбоцитарная пробка), которая непроницаема для форменных тел, но проницаема для плазмы. При любом повреждении сосуда всегда запускаются факторы свёртывания крови, которые приводят к образованию фибрина, который герметизирует белый тромб, чтобы тот был непроницаем для плазмы, а вдобавок прилипают эритроциты (красный тромб). Фаза ретракции. С помощью тромбостенина тромбоциты сжимают тромбоцитарную пробку, чтобы она надёжно запечатала «дыру» и сильно не перекрывала просвет сосуда.
Плазмо-коагуляционный. Такой вид гемостаза протекает уже в более крупных сосудах. На рисунке ниже представлена последовательность взаимодействия плазменных факторов свёртывания крови.
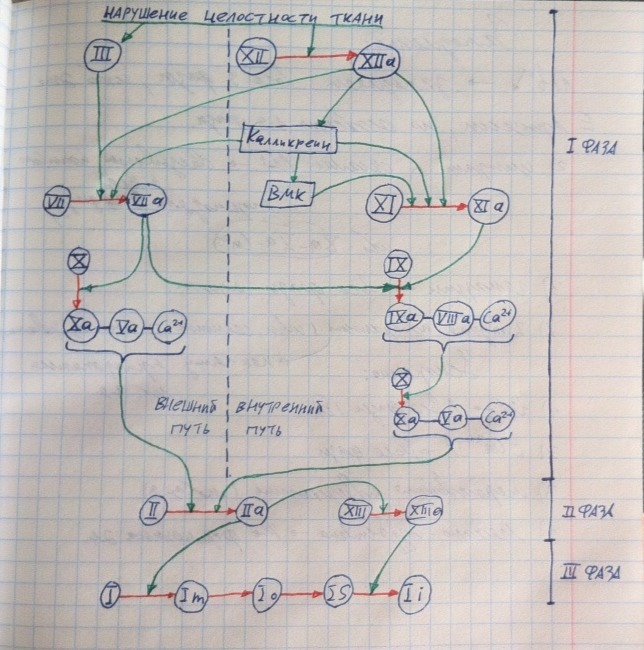
В данном виде гемостаза выделяют 3 фазы: образование протромбиназы, образование тромбина, образование фибрина. Также надо знать, что в зависимости от пускового фактора выделяют внешний и внутренний механизм.
Плазматические факторы свёртывания крови обозначаются римскими цифрами, большинство из них является проферментами, которые активируют друг друга путём ограниченного протеолиза. Если фактор, будучи ферментом, активирован, то к римской цифре приписывают букву «а».
По сути сам следует запомнить эту схему и уметь объяснить, что происходит. Этим сейчас и займёмся.
Внешний механизм. Он запускается тромбопластином (сразу активный), который поступает в кровь только при повреждении сосуда (в норме же его в крови нет), т.е. при действии какого-то внешнего фактора, вот поэтому данный путь называется внешним (тромбопластин поступает извне). Тромбопластин – это 3-й фактор. Он активирует 7-й, а 7-й активирует 10-й. Из активных 10, 5 и 4 (кальций) собирается комплексный фермент – протромбиназа. Так происходит фаза образования протромбиназы. Затем протромбиназа превращает протромбин в тромбин (активация 2-го фактора), попутно активированный 2-й фактор активирует 13-й. Так происходит фаза образования тромбина. Затем тромбин (он же 2-й активированный фактор) превращает фибриноген в фибрин (активация 1-го фактора). Фибрин полимеризуется, образуя крупные нити/фибриллы (это обозначено буковками), но это всё нестабилизированный фибрин, 13-й фактор (мы активировали его на 2-й фазе) ковалентно сшивает фибрин, делая его стабильным. Так происходит фаза образования фибрина.
Внутренний механизм. Он активируется фактором Хагемана (12-й), который циркулирует в крови и активируется при повреждениях сосуда, изменении химико-физического состояния крови, температуры и тд. Поскольку 12-й фактор изначально находится в крови, механизм запускаемого им гемостаза называют внутренним. 12-й фактор активирует 11-й и ряд иных веществ, 11-й активирует 9-й (7-й тоже может активировать 9-й – это своеобразный шунт между внешним и внутренним механизмами). 9, 8 и 4 факторы образуют комплексный фермент, который активирует 10-й фактор, после чего из 10, 5 и 4 происходит сборка протромбиназы. Так происходит фаза образования протромбиназы по внутреннему механимзу, следующие две фазы у внутреннего и внешнего механизмов аналогичны.
При плазмо-коагуляционном гемостазе образуется множество нитей тромбина, в которые попадают форменные элементы крови – образуется довольно крупный сгусток крови, способный (при определённых условиях) закупорить «дыру» в крупном сосуде. Почему я говорю про определённые условия? Когда вам берут кровь из вены, кровь сама по себе не остановится, но если вы её зажмёте, то спустя пару минут плазмо-коагуляционный гемостаз сделает своё дело.
Помимо плазменных факторов свёртывания крови, существуют и тромбоцитарные (продуцируются тромбоцитами), которые играют немалую вспомогательную роль. Информация о которых дана во второй таблице ниже.
Таблица по плазменным факторам свёртывания крови. (да-да, 6-го фактора нет, его исключили из классификации)
|
Название |
Функции |
1 |
Фибриноген |
Превращается в нерастворимый фибрин, полимеризуется в сеть, служащую основой кровяного сгустка |
2 |
Протромбин |
Превращается в тромбин, активирует фибриноген |
3 |
Тромбопластин |
Активация 7-го фактора, запуск внешнего механизма гемостаза |
4 |
Кальций |
Входит в состав протромбиназы (10+5+4), которая активирует протромбин, входит в состав комплекса, активирующего 10-й фактор (9+8+4) |
5 |
Проакцерилин |
Входит в состав протромбиназы |
7 |
Проконвертин |
Превращается в конвертин, активирует 9 и 10 факторы |
8 |
Антигемофилический фактор А |
Входит в комплекс, активирующий 10 фактор (9+8+4) по внутреннему механизму |
9 |
Антигемофилический фактор В |
Входит в комплекс, активирующий 10 фактор (9+8+4) по внутреннему механизму |
10 |
Стюарт-Прауер |
Входит в состав протромбиназы |
11 |
Предшественник плазматического тромбопластина |
Активирует 9 фактор по внутреннему механизму |
12 |
Хагеман |
Активирует 7 и 11 факторы, запускает гемостаз |
13 |
Фибрин стабилизирующий фермент |
Ковалентно сшивает фибриновые белки (так гораздо прочнее) |
Таблица по тромбоцитарным факторам свёртывания крови.
|
Название |
Функции |
1 |
Акцелератор глобулин |
Аналог проакцелирина (5-й плазм) |
2 |
Акцелератор тромбина |
Ускоряет полимеризацию фибрина |
3 |
Тромбоцитарный тромбопластин |
Аналогичен тромбопластину (3-й плазм) |
4 |
Антигепариновый фактор |
Блокирует гепарин, который препятствует свёртыванию |
5 |
Свёртывающий фактор |
Аналог фибриногена |
6 |
Антиплазмин |
Тормозин фибринолиз |
7 |
Антитромбопластин |
Тормозит протромбиназу |
8 |
Ретрактозим |
Запускает ретракцию тромба |
9 |
Серотонин |
Спазм сосуда |
10 |
Котромбопластин |
Активатор тромбопластина |
11 |
Фибрин стабилизирующий фермент |
Аналог Хагемана (12-го плазм) |
12 |
АДФ |
Способствует агрегации тромбоцитов |
Теперь мы полностью обсудили оба вида гемостаза, однако нужно хорошо усвоить, чем они отличаются, помимо того, что сосудисто-тромбоцитарный работает в мелких, а плазмо-коагуляционный в крупных сосудах. Вы, наверное, обратили внимание на то, что в обоих случаях работают и тромбоциты, и факторы свёртывания крови. Так в чём же разница? При сосудисто-коагуляционном гемостазе формируется тромбоцитарная пробка, в основе которой лежат тромбоциты, факторы свёртывания крови включаются для образования небольшого количества фибрина, который нужен как герметик для тромбоцитарной пробки. При плазмо-коагуляционном гемостазе образуется кровяной сгусток, в основе которого лежит фибрин, т.е. здесь основная роль у факторов свёртывания крови, а форменные элементы склеиваются фибрином.
Фибринолитическая система. Фибринолиз – процесс ферментативного (гидролитического) разрушения нестабилизированного фибрина и фибриногена. Основная задача данной системы состоит в адекватном ограничении гемостаза, чтобы свёртывание крови не выходило за пределы очага повреждения сосуда и не затрудняло кровоток, помимо этого, фибринолиз помогает «рассасывать» тромбы в сосудах (это патологическое образование).
Фибринолиз имеет внешний и внутренний механизм. Внешний механизм активируется тканевым активатором плазмина (ТАП) или урокиназой (данные вещества в норме в крови не циркулируют, а попадают в неё, если происходит повреждение сосуда, поэтому механизм назван внешним). Внутренний механизм активируется веществами, находящимися в крови, отсюда и название «внутренний». Внутренний механизм бывает Хагеман зависимым и Хагеман независимым. При Хагеман зависимом активатором фибринолиза служат 12-й фактор плазматический (фактор Хагемана), калликреин или ВМК.
Вне зависимости от того, какой механизм активации задействован, конечным результатом является активация плазмина – фермента, гидролизующего нестабилизированный фибрин и фибриноген.
Тот факт, что фибринолиз может запускаться продуктами гемостаза (Хагеман зависимый), доказывает, что основной задачей фибринолиза является адекватное ограничение гемостаза.
Противосвёртывающая система (антикоагулянтная система). Данная система блокирует гемостаз на всех трёх его стадиях. По факту антикоагулянты отвечают за то, чтобы в сосудах не происходил необоснованный гемостаз.
По механизму действия антикоагулянты разделяются на: антитромбопластины (блок 1-й фазы гемостаза), антитромбаны (блок 2-й фазы), ингибиторы сборки фибрина (блок 3-й фазы).
По происхождению антикоагулянты разделяют на первичные (циркулируют в крови постоянно) и вторичные (образуются только в ходе гемостаза). Первичные антикоагулянты не дают развиться необоснованному гемостазу, а вторичные, образуясь в ходе гемостаза, блокируют его распространение.
Взаимодействие свёртывающей (гемостаз), противосвёртывающей (антикоагулянтной) и фибринолитической системы как основа поддержания жидкого состояния крови. Основная роль гемостаза, конечно, прекращение кровотечений путём затвердевания крови в месте утечки, однако он также поддерживает жидкое состояние крови, так как активирует фибринолитическую систему (Хагеман зависимый механизм) и продуцирует вторичные антикоагулянты. Фибринолитическая система в норме ограничивает распространение гемостаза, не давая крови затвердевать, а при патологии (тромбозе) участвует в рассасывании тромбов. Противосвёртывающая система через вторичные антикоагулянты сдерживает распространение гемостаза, сохраняя кровь жидкой, а через первичные антикоагулянты не даёт необоснованно сворачиваться (затвердевать) крови, сохраняя её жидкой. Когда все три системы работают правильно, кровь остаётся жидкой и сворачивается только в месте кровотечения.
Существуют два патологических процесса, связанных с нарушением баланса свёртывающей и противосвёртывающей систем, которые я приведу вам для наглядности. Это тромбоз и ДВС-синдром. (учить не надо – просто для наглядности)
Тромбоз – типовой патологический процесс прижизненного внутрисосудистого пристеночного свёртывания крови. Существует три основных условия тромбообразования (триада Вирхова): повреждение стенки сосуда (необязательно кровотечение – просто поломка эндотелия), нарушение баланса свёртывающей и противосвёртывающей систем крови, замедление кровотока и/или изменение тока (турбулентные токи). Так вот при операциях или во время родов происходит кровотечение, на что печень реагирует, увеличивая синтез плазменных факторов свёртывания крови, таким образом, свёртывающая система начинает преобладать над противосвёртывающей, поэтому в венах нижних конечностей могут образовываться крупные тромбы, поэтому людям запрещают первое время ходить после родов и тяжёлых операций, так как есть вероятность отрыва тромба и развития тромбоэмболии. Как видите из-за того, что антикоагулянтов было недостаточно, развился патологический гемостаз, что доказывает важность баланса свёртывающей и противосвёртывающей систем для поддержания жидкого состояния крови.
Смысл синдрома диссеминированного внутрисосудистого свёртывания крови (ДВС-синдрома) заключается в том, что во всех сосудах (преимущественно в микроциркуляторном русле) происходит множественное тромбообразование, в результате чего почти полностью расходуются факторы свёртывания крови и тромбоциты, а затем запускается Хагеман зависимый фибринолиз, который уничтожает весь оставшийся в крови фибрин и фибриноген, после чего кровь больше вообще не может сворачиваться, что приводит к множественным кровотечениям и серьёзному нарушению микроциркуляции и кровоснабжения органов. Данный синдром имеет высокую летальность и множество причин, но одна из причин – недостаток антикоагулянтов, что провоцирует гемостаз тут и там.
Факторы, влияющие на скорость свёртывания крови.
Замедляющие факторы. Во-первых, низкие температуры. Низкие температуры снижают скорость ферментативных реакций (требуемая энергия активации выше), а гемостаз по сути построен на множестве ферментативных реакций, отсюда замедление. Во-вторых, снижение концентрации кальция в крови. Этого можно добиться цитратом или оксалатом натрия, которые связывают кальций крови. Причина замедления гемокоагуляции заключается в том, что кальций является её обязательным участником (4-й фактор плазматический). В-третьих, антикоагулянты, в частности гепарин. Он блокирует гемокоагуляцию на всех фазах. В-четвёртых, гладкие швы и силикон. На подобных поверхностях кровяной сгусток или пробка тромбоцитарная просто не могут закрепиться.
Ускоряющие факторы. Во-первых, повышение температуры. Повышает скорость ферментативных реакций в гемостазе. Во-вторых, повышение концентрации кальция в крови. Это 4-й фактор плазматический, необходимый для гемокоагуляции. В-третьих, шероховатые поверхности. На них кровяному сгустку и тромбоцитарной пробке проще зацепиться. В-четвёртых, механическое воздействие. Оно может привести к разрушению форменных элементов крови и выходу из них дополнительного количества факторов свёртывания крови.
Группы крови как проявление иммунной специфичности организма.
На поверхности человеческих клеток имеется множество специфических молекул, которые можно считать антигенами. В норме наш организм не воспринимает наши антигены, как чужеродные. На поверхности форменных элементов крови тоже имеются различные антигены, группы которых разделены на группы крови. Систем разделения групп крови очень много, наиболее клинически значимы системы АВ0 и резус-фактора.
Специфичность в данном случае будет заключаться в том, что у разных людей может быть разная группа крови (признак отличия одного человека от другого = специфичность). Иммунная же составляющая будет заключаться в том, что у людей есть свои антигены (своей группы крови) и могут быть антитела к чужим антигенам (чужим группам крови), отсюда иммунная составляющая. Так просто можно объяснить иммунную специфичность.
АВ0-система. У человека есть ген, кодирующий фермент. Данный фермент создаёт на поверхности эритроцита антиген. У этого гена есть аллели, которые кодируют нерабочий фермент, фермент, делающий аглютиноген-А, и фермент, кодирующий аглютиноген-В. Следовательно, существует 4 группы крови по данной системе. Но также в крови будут постоянно циркулировать аглютинины (антитела к чужим антигенам). Аглютинины бывают альфа и бета. На таблице ниже описано, какие аглютиногены (антигены Аг) и аглютинины (антитела Ат) присутствуют в крови при конкретных группах крови.
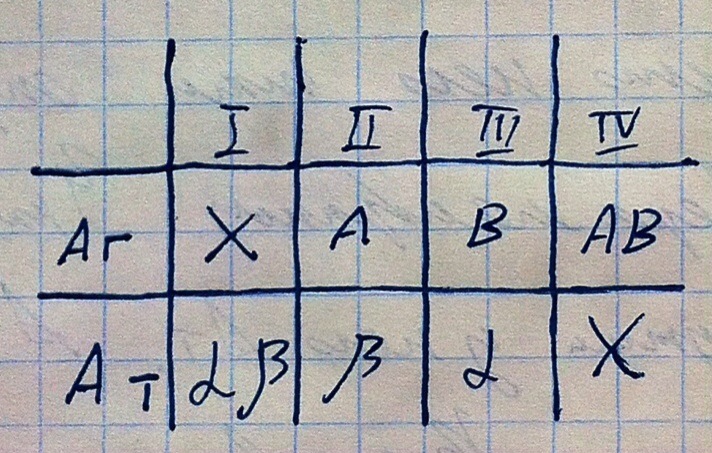
Как определяются группы крови? Исследуемую кровь смешивают с сыворотками. Первая сыворотка имеет аглютинины альфа и бета, вторая альфа, третья бета. Если аглютинины встретятся с одноимёнными аглютиногенами, произойдёт аглютинация (слипание эритроцитов, в крови же видна прозрачная плазма и красные хлопья).
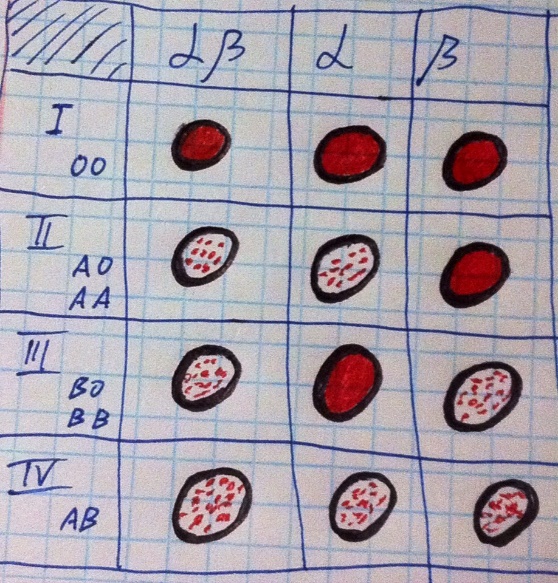
Резус-фактор система. Построена по немного похожему типу. Имеются 3 гена, но из них наиболее важен один, отвечающий за фермент, который создаёт резус-антиген на поверхности эритроцита. Здесь всего две группы: положительные и отрицательные. Отличие заключается в том, что у человека с резус-отрицательной кровью антитела к резус-антигену вырабатываются при контакте, а изначально в крови не циркулируют. Второе отличие состоит в том, что в случае встречи антитела и антигена будет не агглютинация, а гемолиз. И это вносит свои коррективы, которые мы обсудим.
Человеку с резус-отрицательной кровью можно один раз перелить резус-положительную кровь, ибо у реципиента нет антител, но спустя некоторое время антитела выработаются, и если этому человеку снова перелить резус-положительную кровь, то начнётся гемолиз из-за контакта антител и антигенов.
Беременность. Как известно, эритроциты матери и плода не встречаются из-за гемато-плацентарного барьера, поэтому женщина с резус-отрицательной кровью может вынашивать ребёнка с резус-положительной кровью, но во время родов плацента деформируется и кровь смешивается, а организм матери начинает выработку антител к резус-антигену. Во время последующей беременности резус-положительным ребёнком антитела матери попадут в кровь ребёнка и запустят у него гемолиз, что серьёзно отражается на здоровье плода, возможен даже выкидыш. Во избежание подобного беременным вводят специальные сыворотки против антител к резус-антигену.
Анализ крови на резус-фактор также проводят смешиванием крови с сывороткой, содержащей антитела к резус-фактору.
Избранные вопросы.
Основы переливания крови. При переливании крови соблюдают 3 главных правила. Во-первых, переливаются строго одинаковые группы крови. Во-вторых, помимо определения групп крови, дополнительно смешивают кровь донора и реципиента (а то мало ли, может, по исследуемым группам они совместимы, а по всем остальным нет). В-третьих, реципиенту вливают сначала малую порцию донорской крови, затем смотрят на реакцию, потом вливают остальное. Такие меры предосторожности связаны с возможными тяжёлыми последствиями при вливании несочетаемой крови.
Определение групп крови = биологическая совместимость; смешивание крови донора и реципиента = индивидуальная совместимость.
В последнее время переливают плазму, растворы или элементы крови, а цельную кровь редко.
Принципы изготовления плазмозамещающих растворов. Плазмозамещающий раствор в первую очередь предназначен для повышения объёма циркулирующей крови в случае кровопотери, однако абы что в сосуды не нальёшь, поэтому к плазмозамещающим растворам предъявляется ряд требований, суть которых заключается в безопасности данного раствора и выполнении этим раствором ряда функций/свойств плазмы крови. Соответствие плазмозамещающего раствора свойствам и функциям плазмы крови: раствор должен иметь такое же осмотическое давление, как плазма (в идеале идентичный состав по основным минеральным веществам); раствор должен иметь pH, как у плазмы; необходима идентичная вязкость раствора и наличие фосфатного и карбонатного буферов; в идеале в растворе должен быть альбумин для формирования онкотического давления. Требования по безопасности: раствор должен быть стерильным, нетоксичным, не должен содержать аллергены.
Депо крови и их физиологическое значение. Депо крови называют органы и анатомические структуры, в которых может скапливаться (в норме, а не в патологии) кровь, которая там застаивается и не циркулирует по сосудам. К таким депо относят печень, селезёнку и кожу, хотя справедливо сюда ещё отнести вены большого наполнения. Все перечисленные депо при необходимости свои «запасы» крови отправлять в общий кровоток, чтобы она не покоилась, а циркулировала по сосудам. Активация депо происходит при кровопотерях или при необходимости поднять артериальное давление, т.е. для выполнения компенсаторных реакций, в этом и заключается физиологический смысл депо крови.
