
- •Вопросы к экзамену по органической и физколлоидной химии
- •Предмет и значение органической и физколлоидной химии для биологических наук,
- •Теория химического строения органических соединений а.М. Бутлерова. Значение
- •Значение теории а. М. Бутлерова для развития химии и химического прогнозирования
- •Ф ункциональные группы
- •Химическая связь:
- •Электронные эффекты: индуктивный, мезомерный. Сопряженные системы.
- •Классификация органических реакций
- •Изомерия в органической химии: структурная, пространственная, межклассовая, оптическая. Асимметрический атом углерода. Энантиомеры. Диастериомеры. Рацематы. Проекционные формулы Фишера.
- •А лканы. Номенклатура, изомерия, способы получения, физические и химические свойства, нахождение в природе. Их использование в сельском хозяйстве, промышленности и быту.
- •Нахождение в природе:
- •Использование:
- •Химические свойства алкадиенов
- •Арены. Ароматичность. Эффект сопряжения (на примере бензола). Получение, химические свойства и применение бензола и его гомологов.
- •Методы получения коллоидных систем: диспергирование, физическая и химическая конденсация, замена растворителя, пептизация.
- •Виды устойчивости коллоидных систем:
- •Студни: получение, строение и свойства. Синерезис. Тиксотропия. Мембранное равновесие Доннана.
Химические свойства алкадиенов
Алкадиены - ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны. Наличие сопряженных двойных связей увеличивает реакционную способность молекулы и обуславливает необычный механизм некоторых реакций.
Гидрирование
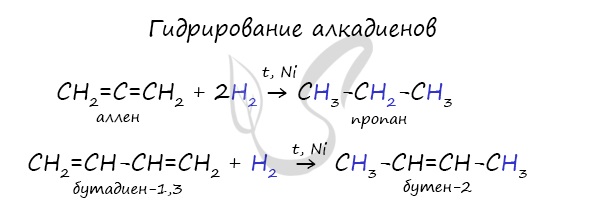
Галогенирование
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение брома по кратным связям к органическому веществу.
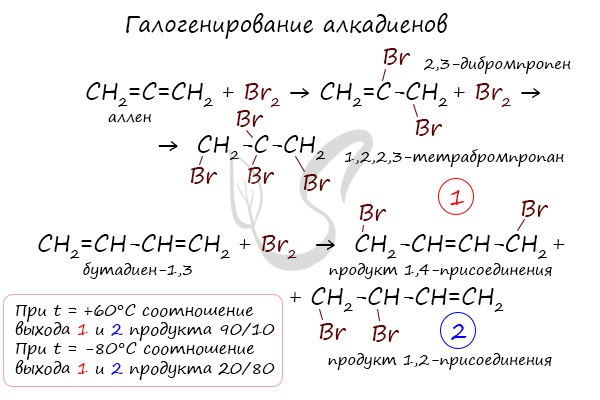
Гидрогалогенирование
Алкадиены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.

Окисление
При горении алкадиены, как и все органические соединения, сгорают с образованием углекислого газа и воды - полное окисление.
2CH2=CH-CH=CH2 + 11O2 → 8CO2 + 6H2O
Полимеризация
Полимеризация - цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.

Натуральным каучуком называется высокомолекулярный эластичный продукт, получаемый из каучуконосных растений, например из бразильской гевеи. Синтетический каучук. Каучук и изделия из вулканизованного каучука (резины) играют огромную роль в технике и быту. Нет ни одной отрасли промышленности, где бы не применялись резиновые изделия. Однако практически значимым каучуконосом оказалась лишь бразильская гевея, и после первой мировой войны, чтобы не зависеть от импортного сырья, во многих странах, в том числе и в нашей стране, начались работы по созданию синтетического каучука. Получаемые полимеризацией изопрена и других диеновых углеводородов синтетические каучуки по свойствам хотя и близки, но не вполне тождественны природному каучуку.
Впервые производство синтетического каучука в промышленном масштабе было организовано у нас, причем в основу лег способ, разработанный С. В. Лебедевым (реакция Лебедева)
В 1922—1925 гг. были проведены первые исследования полимеризации диенов в водных эмульсиях в присутствии перекисных соединений как инициаторов радикальной полимеризации.
Метод эмульсионной полимеризации диенов и некоторых других непредельных соединений интересен тем, что в качестве первичного продукта образуется стойкая водная суспензия, содержащая каучук в виде мельчайших частичек, т. е. синтетический латекс, удобный для многих областей технического применения каучука.
Арены. Ароматичность. Эффект сопряжения (на примере бензола). Получение, химические свойства и применение бензола и его гомологов.
Ароматические углеводороды (арены) - это соединения, содержащие одно или несколько бензольных колец.
Бензольное кольцо – циклическая группа атомов углерода с особым характером σ и π-связей.
Ароматичность (ароматическая система) — особое свойство химических соединений, которые имеют:
- сопряженное (связанное) кольцо;
- особую полуторную (ароматическую) связь;
- проявляют аномально высокую стабильность.
Сопряженной называется система, в которой имеет место чередование простых и кратных связей, либо соседство атома, имеющего вакантную р-орбиталь или неподеленную пару p-электронов. Бензол является замкнутой сопряженной системой. Формула Кекуле показывает, что бензол – это ненасыщенный углеводород, в молекуле которого есть три π-связи. Если же мы рассмотрим электронное строение бензола, то увидим, что это π.π-сопряжённая система (атомы углерода sp2-гибридизованы, все σ-связи лежат в одной плоскости, а p-орбитали расположены перпендикулярно этой плоскости и перекрываются не попарно, а образуя общее электронное облако, в котором делокализовано 6 электронов).
Сопряжение – это выравнивание связей и зарядов в реальной молекуле (или частице) по сравнению с идеальной, но несуществующей структурой. Можно дать и другое определение этому явлению: это процесс дополнительного взаимодействия p-электронных орбиталей, приводящий к делокализации электронной плотности. Сопряжение – это энергетически выгодный для молекулы процесс. при образовании связи (т.е. при взаимодействии атомных орбиталей) выделяется энергия, значит, внутренняя энергия системы понижается, и она становится более стабильной. Так как при сопряжении происходит дополнительное перекрывание орбиталей, то выделяется и дополнительная энергия, и система становится ещё более стабильной. Энергия, выделяющаяся в результате сопряжения, называется энергией сопряжения. Количественно – это разность энергий соединения с сопряжёнными двойными связями и соединения с изолированными двойными связями (где сопряжение невозможно). Чем больше атомов участвует в сопряжении, тем выше энергия сопряжения, тем стабильнее молекула. Поэтому в природе распространены соединения, молекулы которых содержат длинные сопряжённые цепи. Замкнутые сопряжённые системы более стабильны, чем открытые, т.к. энергия сопряжения замкнутых сопряжённых систем выше (в случае бензола – это 151 кДж/моль).



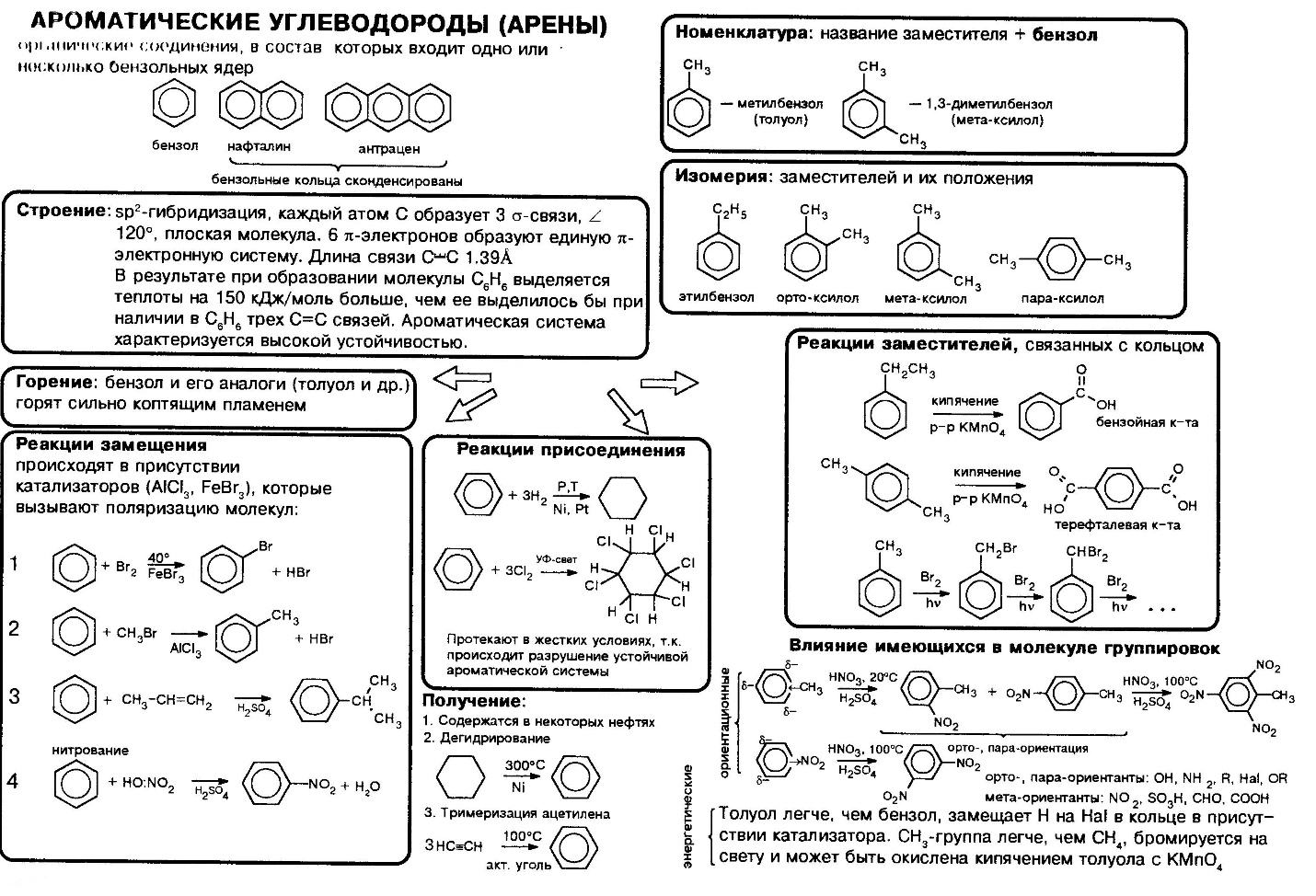
Бензол C6H6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C6H5NO2(растворитель, из него получают анилин), хлорбензола C6H5Cl, фенола C6H5OH, стирола и т.д.
Толуол C6H5–CH3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Хлорпроизводные бензола используют для защиты растений. Они являются химическими средствами борьбы с микроорганизмами, растениями и животными.
Стирол C6H5 – CH = CH2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.
Циклоалканы. Напряженность циклов. Конформации. Номенклатура, изомерия, способы получения, химические свойства, распространение в природе.
Изопреноиды: терпены, терпеноиды, каротиноиды. Распространение в растительном мире, биологическое значение.
Галогенпроизводные углеводородов. Классификация, номенклатура, получение, химические свойства и применение.
Одноатомные спирты. Номенклатура, получение, физические и химические свойства. Метиловый, этиловый спирты; их применение.
Двух- и трехатомные спирты. Номенклатура, получение, физические и химические свойства. Этиленгликоль, глицерин. Распространение в природе, применение.
Фенолы. Номенклатура, получение, химические свойства.
Липиды. Классификация и их биологическая роль. Жиры. Получение, физические и химические свойства, биологическая роль.
Амины. Номенклатура, получение, химические свойства и значение.
Аминоспирты. Этаноламин, холин, ацетилхолин, их строение, свойства, нахождение в природе и биологическое значение.
Карбоновые кислоты. Номенклатура, получение, свойства и значение. Муравьиная, уксусная, бензойная и салициловая кислоты.
Амиды кислот. Номенклатура, получение. Амиды угольной кислоты. Мочевина. Биурет, Применение мочевины и ее производных.
Дикарбоновые кислоты. Номенклатура, получение, свойства и значение. Отношение к нагреванию.
Оксикислоты. Классификация, номенклатура, получение, химические свойства. Дегидратация оксикислот. Гликолевая, молочная, яблочная, β-оксимасляная, винная, лимонная кислоты.
Оксокислоты. Номенклатура, получение, химические свойства и биологическая значение. Глиоксалевая, пировиноградная, ацетоуксусная.
Альдегиды. Номенклатура, получение, химические свойства и значение.
Кетоны. Номенклатура, получение, химические свойства и значение.
Углеводы. Распространение в природе. Понятие о фотосинтезе. Биологическая роль. Классификация.
Моносахариды: рибоза, дезоксирибоза, ксилоза, глюкоза, манноза, галактоза, фруктоза. Распространение в природе. Строение и свойства.
Дисахариды; трегалоза, сахароза, мальтоза, лактоза и целлобиоза. Строение, свойства, биологическое значение.
Полисахариды. Крахмал, клетчатка, гликоген. Распространение в природе, строение, свойства и значение. Гидролиз полисахаридов.
Классификация, изомерия, номенклатура, получение, физические и химические свойства аминокислот. Заменимые и незаменимые аминокислоты.
Белки. Классификация белков (протеины, протеиды). Структура, строение, свойства и биологическая роль.
Гетероциклических системы. Классификация, ароматичность и биологическая роль.
Нуклеиновые кислоты (ДНК и РНК). Строение и биологическая роль.
Нуклеиновые кислоты делятся на два больших класса: 1) дезоксирибонуклеиновые кислоты (ДНК), которые при полном гидролизе дают аденин, гуанин, цитозин, тимин, дезоксирибозу и фосфорную кислоту; 2) рибонуклеиновые кислоты (РНК) .гидролизующиеся до аденина, гуанина, цитозина, урацил а, рибозы и фосфорной 553кислоты. Следовательно, ДНК отличается от РНК тем, что в состав ее молекул входит другая пентоза (дезоксирибоза вместо рибозы) и другое пиримидиновое основание (тимин вместо урацила).
Основы химической термодинамики. Функции состояния; внутренняя энергия, энтальпия, энтропия, свободная энергия Гиббса.
Первое начало термодинамики. Энергетика химических процессов. Термохимия. Закон Гесса.
Энтропия. Ее статистический смысл. Второе и третье начало термодинамики.
Свободная энергия Гиббса. Критерии направленности химических процессов.
Скорость химических реакций. Ее зависимость от концентрации. Кинетические уравнения. Порядок реакции и методы его определения.
Влияние температуры на скорость химической реакции. Температурный коэффициент реакции. Уравнение Аррениуса. Энергия активации.
Влияние катализатора на скорость химической реакции. Гомогенный и гетерогенный катализ. Особенности ферментативного катализа.
Давление насыщенных паров, температура кипения и замерзания разбавленных растворов неэлектролитов и электролитов. Законы Рауля.
Осмос. Осмотическое давление растворов. Уравнение Вант-Гоффа. Биологическая роль осмотического давления.
Буферные растворы. Их состав, свойства и биологическая роль. Понятие о буферной емкости.
Физическая и химическая адсорбция. Моно- и полимолекулярная адсорбция, Изотермы адсорбции. Уравнения Фрейндлиха и Ленгмюра.
Адсорбция потенциалопределяющих ионов. Правило Пескова–Фаянса. Ионообменная адсорбция. Процессы адсорбции в организме животных.
Поверхностно-активные вещества /ПАВ/. Строение молекул ПАВ. Правило Дюкло-Траубе. Применение ПАВ.
Дисперсные системы. Классификация дисперсных систем. Коллоидные растворы и их значение в биологии.
Молекулярно-кинетические свойства коллоидных систем. Броуновское движение, диффузия, вязкость, осмотическое давление.
Оптические свойства дисперсных систем. Поглощение и рассеивание света. Эффект Тиндаля. Уравнение Рэлея. Нефелометрия.
Строение коллоидной частицы. Электрокинетические явления: электрофорез, электроосмос. Практическая значимость этих явлений.
Структурной единицей коллоидного раствора является мицелла – сложное структурное образование, состоящее из агрегата, потенциалопределяющих ионов и противоионов.

Внутреннюю часть мицеллы составляет агрегат основного вещества, который состоит из большого числа молекул или атомов кристаллического или аморфного строения. Агрегат электронейтрален, но обладает большой адсорбционной способностью и способен адсорбировать на своей поверхности ионы из раствора – потенциалопределяющие ионы (ПОИ). При выборе потенциалопределяющих ионов пользуются эмпирическим правилом Пескова – Фаянса – Панета: «На твердой поверхности агрегата в первую очередь адсорбируются ионы, которые:
- входят в состав агрегата;
- способны достраивать кристаллическую решетку агрегата;
- образуют малорастворимое соединение с ионами агрегата; изоморфны с ионами агрегата».
В
случае иодида серебра это ионы
 или
или
 .
Какие конкретно ионы будет сорбировать
зависит от избытком реактива.
.
Какие конкретно ионы будет сорбировать
зависит от избытком реактива.
В нашем примере в избытке раствора нитрата серебра потенциалопределяющими ионами являются положительные ионы серебра.
