
лекции / все лекции по охт
.pdf
РИСУНОК

Во 2-м случае, когда на скорость реакции температура влияет сильнее, чем концентрация, для получения максимальной скорости на всем протяжении процесса выгодно взять систему из 2-х реакторов РИС-Н и РИВ (рис.).

РЕАКТОРЫ ДЛЯ ОБРАТИМОЙ ЭКЗОТЕРМИЧЕСКОЙ
РЕАКЦИИ
Эффективное проведение обратимых
экзотермических реакций требует, как известно
(см. лекцию «гомогенные процессы»),
приближения режима процесса
к ЛОТ «см. зависимости r(T) и х(Т)».
Такое приближение к ЛОТ
можно осуществить, например,
если секционировать реакционную
зону, т.е. разделить ее на участки,
(слои катализатора, если реактор –
каталитический) и отводить тепло
от нагретой реакционной смеси за
счет реакции после каждого
участка (см. рис. реактора ниже).

Пример реактора для проведения обратимой экзотермической реакции и режим процесса в нем

ПРИМЕРЫ РЕАКТОРОВ ДЛЯ ПРОВЕДЕНИЯ ОБРАТИМЫХ ЭКЗОТЕРМИЧЕСКИХ РЕАКЦИЙ
а) полочный аппарат с вводом холодного газа и теплообменниками;
По аналогии с предыдущим слайдом изобразите изменение параметров процесса
в реакторе.
б) трубчатый реактор.
Рис. Изменение параметров
в трубчатом реакторе
АВТОТЕРМИЧЕСКИЕ РЕАКТОРЫ
Рассмотренные примеры реакторов для проведения обратимых экзотермических реакций относятся к группе автотермических реакторы, в которых поддержание необходимой температуры осуществляется за счет теплоты химического процесса (за счет внутренних источников) без использования внешних источников энергии. Такие химические реакторы, широко используются в крупнотоннажных производствах, например, серной и азотной
кислот, аммиака...

Б) Сложные реакции
Селективность процесса зависит не только от концентрации и порядков реакции (целевой и побочной), но и от соотношения констант скоростей реакций.
|
/ |
|
|
W |
|
|
k c |
n1 |
|
|
|
|
|
|
1 |
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
S |
|
R |
|
A R |
|
|
1 |
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|
W |
|
n1 |
k c |
n2 |
|
k |
2 |
|
|
|
|
1 |
2 |
|
|||||||||
|
|
|
k c |
|
|
|
n2 n1 |
|
|
|
) |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
1 |
|
|
c |
|
|
|
|
( E |
-E |
|
||||
|
|
|
|
А |
1 |
A |
|
|
2 |
A |
|
|
|
|
|
k |
|
|
|
|
n2 n1 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
k1 |
A |
1 |
|
20 e |
RT |
c |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
k10 |
|
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Повышение температуры благоприятно и для интенсивности, и для селективности процесса, если Е1 > Е2 (Е1 - энергия активации целевой реакции). В противном случае (Е1 < Е2) для роста селективности благоприятно снижение температуры процесса, но при этом падает его интенсивность.

НЕОДНОЗНАЧНОСТЬ И МНОЖЕСТВЕННОСТЬ СТАЦИОНАРНЫХ РЕЖИМОВ В АДИАБАТИЧЕСКОМ РЕАКТОРЕ
Если в адиабатическом реакторе проводят экзотермическую реакцию, то система уравнений материального и теплового балансов может иметь как одно, так и несколько решений.
Покажем на примере РИС-Н при протекании в нем реакции 1-го порядка. Математически процесс в РИС-Н описывается уравнениями:
x |
|
r |
А |
|
|
τ |
|
|
|
с |
|
|
|
0 |
откуда было получено уравнение адиабаты:
|
|
Т T |
|
|
|
|
0 |
|
|
τ |
|
Т Т |
0 |
Т |
АД |
|
|
||
P
сp
x |
А |
Т |
|
|
r ;
|
|
к τ |
; |
АД |
|
||
1 |
к τ |
|
|
|
|
Левая часть уравнения пропорциональна теплоотводу qТ из реакционной зоны проходящим реакционным потоком и представляет собой
прямолинейную зависимость от Т , правая часть – теплоподводу qр за счет протекания экзореакции и представляет собой S-образную зависимость от Т.
По существу уравнение адиабаты –это уравнение теплового баланса. Решим
его графически и найдем температуру Т в реакторе.
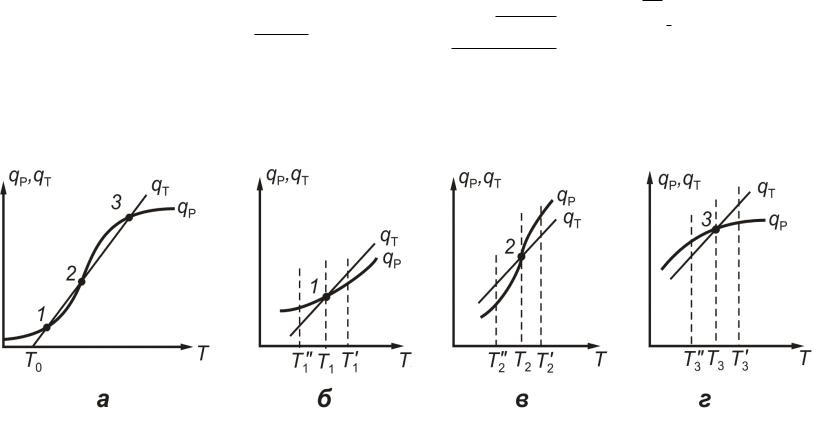
ГРАФИЧЕСКОЕ РЕШЕНИЕ УРАВНЕНИЯ ТЕПЛОВОГО БАЛАНСА (УРАВНЕНИЯ АДИАБАТЫ)
Т Т |
|
Т |
|
x |
Т |
|
|
к τ |
; k k |
E |
0 |
АД |
АД |
|
e RT |
||||||
|
|
А |
|
1 |
к τ |
0 |
|
|||
|
|
|
|
|
|
|
|
|
qT
qp
АНАЛИЗ РЕШЕНИЯ
Решение уравнение адиабаты имеет 1 или 3 корня (рис.) Все режимы 1, 2 или 3 – стационарные. Нелинейная зависимость
между тепловыделением qp(Т) в реакторе от температуры обусловливает возможность появления неоднозначных стационарных режимов (несколько точек пересечения с линейной зависимостью qТ(Т).
В низкотемпературном режиме 1 скорость и степень превращение в реакторе – небольшие. При почти полном
превращении в режиме 3 температура в реакторе будет большая, равная адиабатическому разогреву. Привлекательным может оказаться среднетемпературный режим 2.
Для проверки условий его реализации рассмотрим свойства всех стационарных режимов.
