
- •Модуль по химии №4
- •1. Какие явления относятся к поверхностным?
- •2. Поверхностное натяжение жидкостей (определение и формула для расчета). Механизм возникновения поверхностного натяжения. Факторы, влияющие на величину поверхностного натяжения.
- •3. Дайте определение понятию “адсорбция”. Основные термины (адсорбент, адсорбтив, адсорбат, десорбция).
- •4. Деление адсорбции в зависимости от природы действующих сил на химическую и физическую. Примеры.
- •5. Адсорбция на границе жидкость – газ: уравнение адсорбции гиббса, его анализ. Изотерма адсорбции, предельная адсорбция г.
- •7. Ориентация молекул пав в поверхностном слое (принцип независимости поверхностного действия Ленгмюра). Правило дюкло-траубе.
- •8. Адсорбция на границе двух несмешивающихся жидкостей (адсорбция жидкость – жидкость).
- •9. Теория мономолекулярной адсорбции Ленгмюра. Уравнение Ленгмюра, его анализ.
- •10. Адсорбция на границе твёрдое тело – газ: удельная адсорбция; факторы, влияющие на адсорбцию газов на поверхности твердых адсорбентов.
- •11. Молекулярная адсорбция (адсорбция твердое тело – раствор неэлектролита или слабого электролита), её особенности. Факторы, влияющие на молекулярную адсорбцию.
- •12. Ионная адсорбция (адсорбция твердое тело – раствор сильного электролита), её особенности. Виды ионной адсорбции (эквивалентная, избирательная, ионнообменная).
- •14. Классификация дисперсных систем по размерам частиц диспергированного вещества: взвеси, коллоидные системы, истинные растворы.
- •15. Условия получения коллоидных растворов.
- •16. Методы получения коллоидных систем: диспергационные и конденсационные методы.
- •17. Пептизация как физико-химическое дробление осадков до частиц коллоидного размера. Адсорбционная пептизация. Диссолюционная пептизация. Биологическое значение пептизации.
- •18. Методы очистки коллоидных систем: фильтрация, ультрафильтрация. Диализ, электродиализ, компенсационный диализ (принцип работы аппарата «искусственная почка»).
- •20. Электрокинетические явления: электрофорез и электроосмос.
- •21. Оптические свойства коллоидных систем (опалесценция, эффект фарадея – тиндаля, окраска).
- •23. Агрегативная устойчивость коллоидных систем.
- •24. Явление коагуляции коллоидных систем. Скрытая и явная коагуляции. Факторы, вызывающие коагуляцию.
- •25. Коагуляция электролитами: правило шульце – гарди, порог коагуляции. Коагуляция смесями электролитов (аддитивное действие, антогонизм, синергизм).
- •26. Коллоидная защита, ее механизм. Биологическое значение.
- •27. Высокомолекулярные соединения (вмс). Классификация вмс: по природе происхождения (природные, синтетические, искусственные); по строению (линейные, разветвленные, сетчатые).
- •28. Растворы высокомолекулярных соединений (вмс) как истинные растворы, их особенности. Оптические и молекулярно – кинетические свойства растворов вмс.
- •29. Растворение вмс. Явление набухания вмс. Степень набухания как количественная характеристика процесса набухания. Факторы, влияющие на степень набухания.
- •30. Вязкость растворов вмс, её особенность. Причины высокой вязкости вмс. Характеристическая вязкость (уравнение марка – куна – хаувинка). Факторы, влияющие на вязкость.
- •31. Белки как представители полиэлектролитов. Изоэлектрическое состояние белка, изоэлектрическая точка белка (иэт). Заряд белковой молекулы в кислой и щелочной средах.
- •32. Нарушение устойчивости растворов вмс: застудневание (факторы, влияющие на студнеобразование). Свойства студней. Синерезис, понятие об интермицелярной жидкости.
- •33. Нарушение устойчивости растворов вмс: высаливание.
- •34. Нарушение устойчивости растворов вмс: коацервация.
30. Вязкость растворов вмс, её особенность. Причины высокой вязкости вмс. Характеристическая вязкость (уравнение марка – куна – хаувинка). Факторы, влияющие на вязкость.
Вязкость жидкостей можно для простоты определить как сопротивление жидкости передвижению одного еѐ слоя относителоьно другого при сдвиге, растяжении и других видах деформации.
Вязкость характеризуют интенсивностью работы, затрачиваемой на осуществление течения газа или жидкости с определѐнной скоростью. При ламинарном сдвиговом течении жидкости между двумя плоскопараллельными пластинками, верхняя из которых движется с постоянной скоростью v под действием силы F , а нижняя неподвижна, слои жидкости перемещаются с разными скоростями: от максимальной у верхней пластинки до нуля у нижней. Если между η и γ имеется линейная зависимость, жидкость называется ньютоновской, а отношение η : γ называется динамической вязкостью (или просто вязкостью) ε. Жидкости для которых эта зависимость является нелинейной называются неньютоновскими.
Истинные растворы НМС являются ньютоновскими жидкостями, для них вязкость описывается уравнением Ньютона:
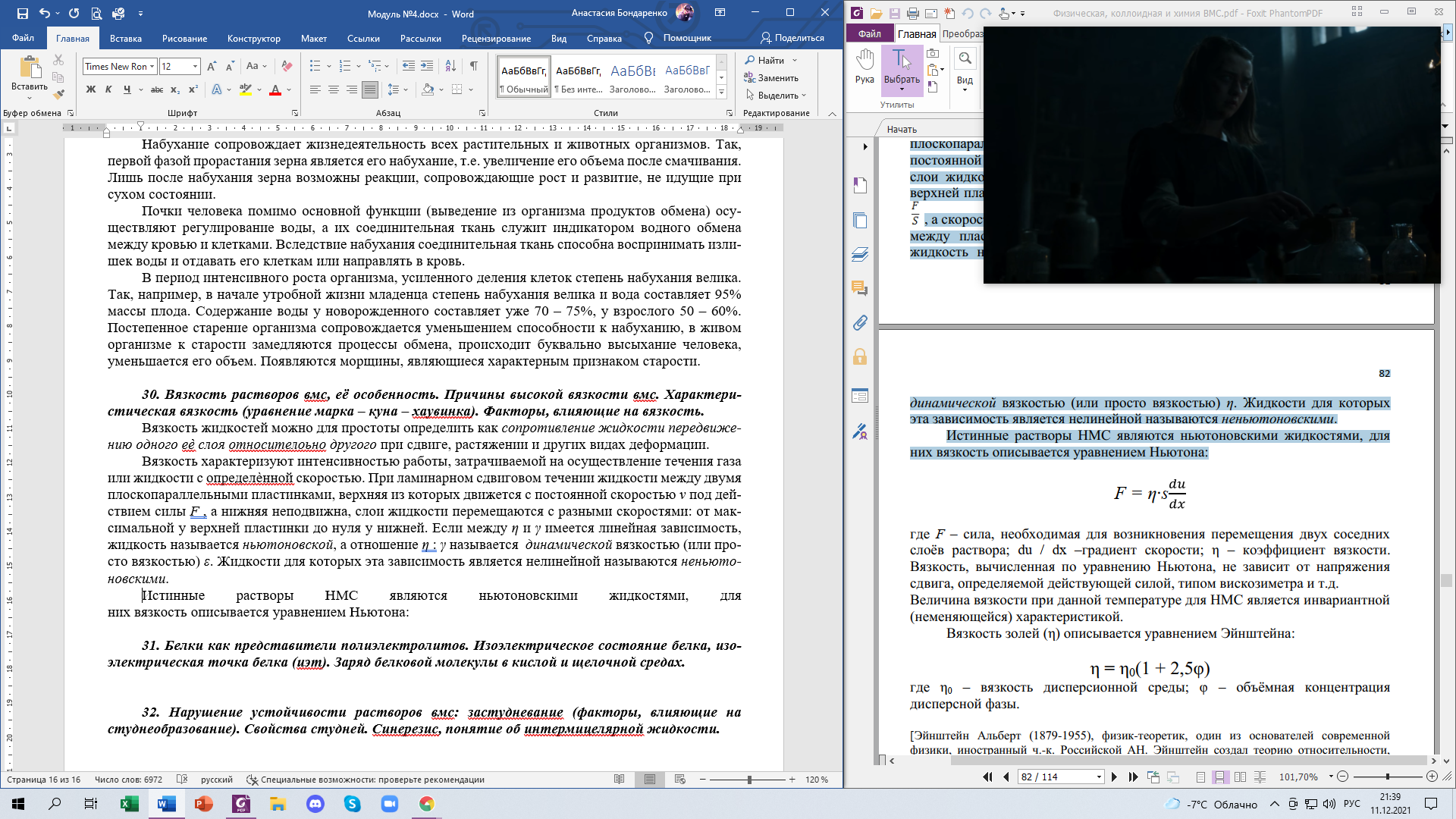
где F – сила, необходимая для возникновения перемещения двух соседних слоѐв раствора; du / dx –градиент скорости; ε – коэффициент вязкости. Вязкость, вычисленная по уравнению Ньютона, не зависит от напряжения сдвига, определяемой действующей силой, типом вискозиметра и т.д. Величина вязкости при данной температуре для НМС является инвариантной (неменяющейся) характеристикой.
Вязкость золей (ε) описывается уравнением Эйнштейна:
![]()
где ε0 – вязкость дисперсионной среды; φ – объѐмная концентрация дисперсной фазы.
Величину [ε] называют характеристической вязкостью или предельным числом вязкости.
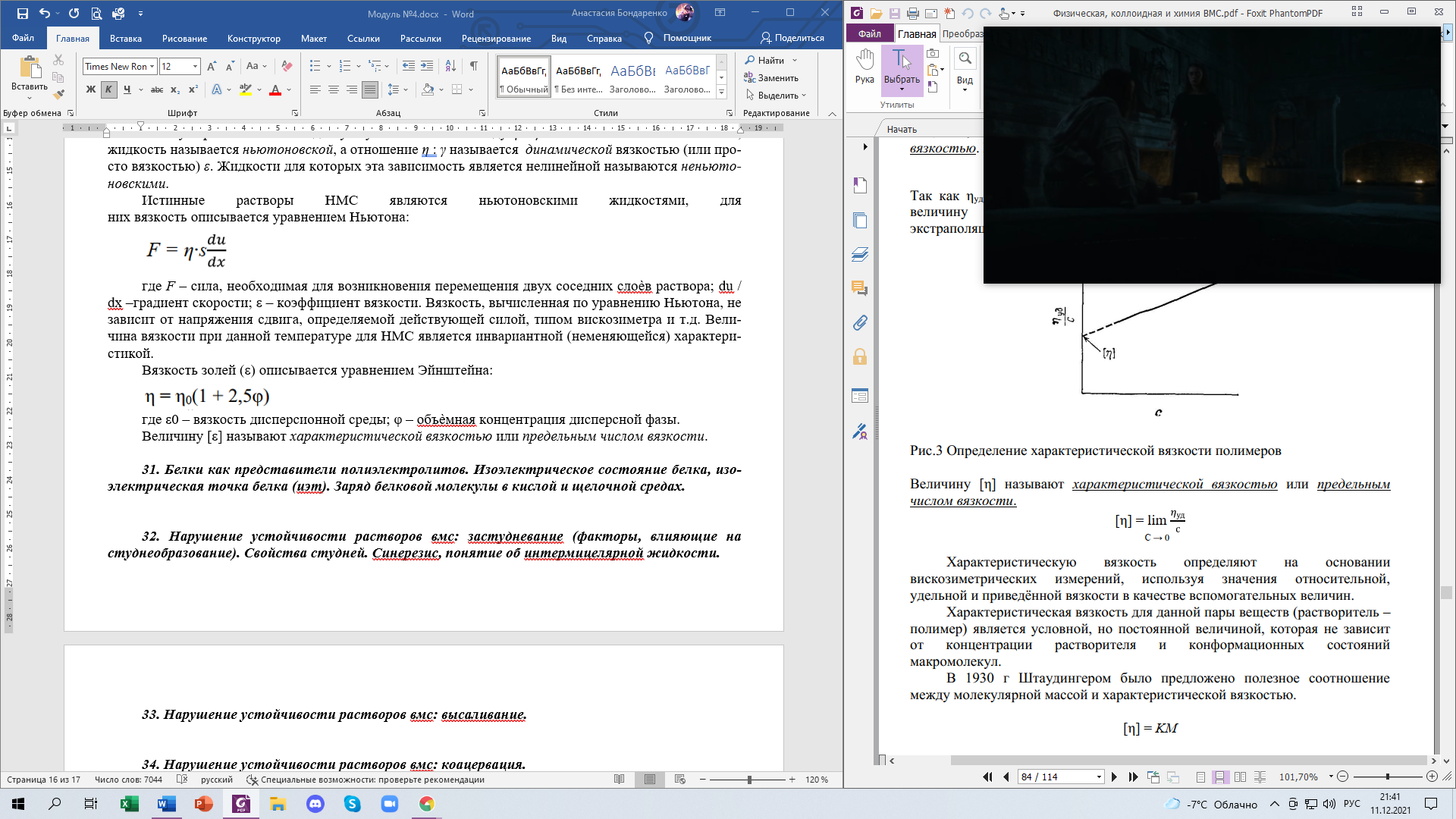
Характеристическую вязкость определяют на основании вискозиметрических измерений, используя значения относительной, удельной и приведѐнной вязкости в качестве вспомогательных величин.
Характеристическая вязкость для данной пары веществ (растворитель – полимер) является условной, но постоянной величиной, которая не зависит от концентрации растворителя и конформационных состояний макромолекул.
В 1930 г Штаудингером было предложено полезное соотношение между молекулярной массой и характеристической вязкостью.
[n] = KM
Это соотношение имело ряд недостатков. Поэтому позже оно было модифицировано. В настоящее время оно известно, как уравнение МаркаКуна-Хаувинка и имеет следующий вид:
[n] = KMα
где К – постоянная величина, экспериментально определяемая для данных макромолекул и растворителя. Показатель степени α зависит от формы макромолекул. Для белков компактной структуры – глобулярных белков – он составляет около 0,5. Для молекул, находящихся в конформации беспорядочного клубка, показатель степени возрастает до 2. Молекулярная масса, определяемая по уравнению Марка-Куна-Хаувинка, называется средневязкостной молекулярной массой Мε.
Величина характеристической вязкости позволяет определить как относительную молекулярную массу полимера, так и размеры и форму его макромолекул. Например, если растворы белков характеризуются величинами [ε, лежащими между 3,0 и 4,0 см3/г, то столь малое значение данных величин указывает на глобулярную, весьма компактную структуру этих белков, форма которых незначительно отличается от сферы. Большие значения [ε указывают либо на высокую степень асимметричности белков, либо на большой объѐм, занимаемый данными белками в растворе.
