- •Строение водорода
- •Физические свойства водорода
- •Химические свойства водорода
- •1. Взаимодействие с галогенами
- •2. Взаимодействие с кислородом
- •3. Взаимодействие с серой
- •4. Взаимодействие с азотом
- •5. Взаимодействие со сложными веществами (оксидами металлов и неметаллов)
- •6. Взаимодействие с активными металлами
- •Получение водорода
- •Применение водорода
- •Общая характеристика элементов VII-a группы
- •Особые свойства фтора, как наиболее электроотрицательного элемента
- •Ахождение в природе
- •Способы получения
- •Химические свойства галогенов
- •Способы получения галогеноводородов и их свойства
- •Способы получения галогеноводородов и их свойства
- •Кислородсодержащие соединения галогенов
- •Оксикислоты хлора
- •Реакции разложения hClO
- •Гипохлорит калия
- •Получение белильной извести
Способы получения галогеноводородов и их свойства
HF H2 + F2 – не получается из-за высокой Q
1)СaF2 + H2SO4 → CaSO4↓ + 2HF↑
t летуча
2)KHF2 → KF + HF
hν
HCl 1) H2 + Cl2 → 2HCl
2) NaClк + H2SO4 конц. → NaHSO4 + HCl↑
3) BCl3 + H2O → H3BO3 + HCl↑
Способы получения галогеноводородов и их свойства
F H2 + F2 – не получается из-за высокой Q
1)СaF2 + H2SO4 → CaSO4↓ + 2HF↑
t летуча
2)KHF2 → KF + HF
hν
HCl 1) H2 + Cl2 → 2HCl
2) NaClк + H2SO4 конц. → NaHSO4 + HCl↑
3) BCl3 + H2O → H3BO3 + HCl↑





Кислородсодержащие соединения галогенов
Галогены непосредственно с кислородом не взаимодействуют. Это обусловлено небольшой энергией связи Г-О и невозможностью использовать высокие температуры для осуществления реакций окисления, т.к. для них ∆S0 <0, оксиды получают косвенным путём.
При 25ºС сравнительно стабильны следующие кислородные соединения:
+1 +4 +6 +7
Cl2O ClO2 Cl2O6 Cl2O7
в соединениях с О2 хлор проявляет степени окисления (с. о.):
с. о. +1 +3 +4 +5 +6 +7
оксид Cl2O ClO2
Cl2O4 Cl2O6 Cl2O7
кислота HClO HClO2 HClO2 HClO3 HClO3 HClO4
HClO3 HClO4
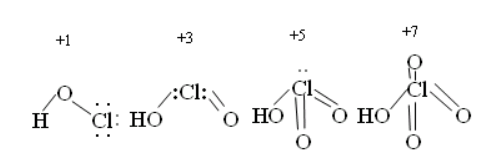
Если сопоставить свойства кислот со структурой молекул, то можно отметить следующее: с ростом степени окисления хлора уменьшается число несвязывающих электронных пар и происходит постепенное достраивание кислородного окружения хлора до тетраэдрического.
Увеличение силы кислот HClO – HСlO4 обусловлено тем, что с ростом числа кислородных атомов электронные облака всё больше стянуты к центральному атому и связь Н – О становится всё более полярной.
Окислительные свойства уменьшаются, у оксо-анионов
ClO-, ClO2-, ClO3-, ClO4- - увеличивается прочность связи кислорода с хлором.
Оксикислоты хлора

Возрастание силы кислот связано с увеличением количества кислорода, который оттягивает на себя электронную плотность и прочность связи Н – О ослабевает.
Возрастание устойчивости связано с увеличением степени окисления хлора и большим количеством электронов, принимающих участие в образовании связи. Во всех соединениях Cl – в sp3 гибридизации.
Самая высокая окислительная способность у хлорноватистой кислоты, за счет атомарного кислорода.
HСlO = HCl + O