
3748
.pdf
|
12 |
|
2.1. Sn |
2.10.Pt |
2.19.Ca |
2.2. Mg |
2.11. Fe |
2.20.Hg |
2.3.Cu |
2.12. Co |
2.21.F |
2.4.Ag |
2.13. Ni |
2.22.Al |
2.5.K |
2.14. Br |
2.23.P |
2.6.S |
2.15.Cl |
2.24.N |
2.7.Cr |
2.16.J |
2.25. Mn |
2.8.Pb |
2.17.Zn |
|
2.9.Sb |
2.18.Cd |
|
Тема 3. Химическая связь
При изучении этой темы следует уяснить современные представления о природе химической связи. Так, механизм образования химической связи удобнее рассмотреть с позиций методы валентных связей. На основе современных представлений о строении атома объяснить свойства химической связи: энергию, длину, насыщаемость, направленность, полярность. Разберитесь в особенностях ионной, металлической и водородной связи.
3.1.По какому механизму образования ковалентной связи построены молекулы J2 и NH3?
3.2.По какому механизму образования ковалентной связи построены молекулы F2, H2O? В какой из молекул связь является полярной? Почему?
3.3.На основании сравнения величин относительной электроотрицательности для р-элементов, проследите как изменяется полярность связи в молекулах
NH3 и РН3.
3.4.Приведите схему образования молекулы N2 (с учетом перекрывания электронных облаков соединяющихся атомов). Сколько сигма- и пи-связей в молекуле азота?
3.5.Молекулы H2О и СО2 содержат по две полярные связи каждая. Почему молекула Н2О полярная, СО2 – неполярная?
3.6.По какому механизму образования ковалентной связи построен ион аммония NH4+?
13
3.7.Используя значения относительной электроотрицательности, укажите и объясните направление общей электронной пары для соединений HF и CF.
3.8.Дипольные моменты H2O и H2S равны 1,84 Д и 0,93 Д соответственно. В какой молекуле связь более полярна?
3.9.Сколько сигма- и писвязей в молекулах O2, N2, Br2?
3.10.Исходя из метода валентных связей, сделайте вывод о возможных валентностях серы в стационарном и возбужденном состоянии.
3.11.Дипольный момент СО2 равен нулю, а H2O – 1,84 Д. Как построены эти молекулы?
3.12.По какому механизму образования ковалентной связи построен ион оксония H3O+?
3.13.Приведите примеры молекул, между атомами которых возникает водородная связь. Как влияет водородная связь на свойства веществ?
3.14.Какие атомные орбитали участвуют в образовании химической связи сероводорода H2S? Полярная ли эта молекула?
3.15.Какой тип связи в галогенидах щелочных металлов? Почему?
3.16.Почему молекула Cl2 неполярна, а JCl полярна?
3.17.Объясните в каких молекулах CO, CO2, HBr, Br2 связь полярная, в каких неполярная?
3.18. По какому механизму образования ковалентной связи построены молекулы N2, HCl, H2O?
3.19. В каких молекулах возникает ионная связь? Приведите примеры.
3.20.Чем отличается металлическая связь от ковалентной?
3.21.Приведите схему образования молекулы O2 (с учетом перекрывания электронных облаков соединяющихся атомов)? Какие связи в молекуле кислорода?
3.22.По какому механизму образования ковалентной связи построены молекулы Br2 и PH3?
3.23.Молекулы H2O и CO2 содержат по две полярные связи каждая. Почему молекула H2O полярна, а CO2 – неполярна?
3.24.Дипольный момент CO2 равен нулю, а H2S – 0,93 Д. Как построены эти молекулы?
3.25.В каких случаях возникает водородная связь? Приведите примеры.
14
Тема 4. Концентрация растворов
Состав раствора количественно выражают чаще всего через массовую долю, молярную и эквивалентную (нормальную) концентрацию, а также титр.
Массовая доля – это отношение массы компонента В к массе раствора. Обычно ее выражают в процентах.
(B) |
m(B) |
100 (%) . |
(4.1) |
|
m |
||||
|
|
|
Например, 5 % раствор хлорида натрия означает, что в 100г раствора содержится 5 г NaCl.
Молярная концентрация – это отношение количества растворенного вещества В к объему раствора:
с(В) |
|
n(B) |
(моль/дм3 ) . |
(4.2) |
||||
|
V |
|||||||
|
|
|
|
|
|
|
|
|
Количество вещества можно найти по формуле |
|
|||||||
|
n(B) |
|
|
m(B) |
, |
|
(4.3) |
|
|
|
|
|
|||||
|
|
|
|
|
M(B) |
|
||
тогда, |
c(B) |
|
|
m(B) |
. |
(4.4) |
||
|
|
|
||||||
|
|
|
|
M(B) V |
|
|||
Одномолярный раствор – это раствор, содержащий 1 моль вещества в 1 дм3 раствора. Для обозначения молярной концентрации используют символ М, например, 1М – одномолярный (с = 1 моль/дм3); 0,1 М – децимолярный (с = 0,1 моль/дм3); 0,01 М – сантимолярный (с = 0,01 моль/дм3); 0,001 М – миллимолярный (с = 0,001 моль/дм3).
Молярная концентрация эквивалента (нормальная концентрация) –
это отношение количества вещества эквивалента к объему раствора:
|
с(1/ z) |
n(1/ zB) |
(моль/дм3 ) , |
(4.5) |
|||
|
|
V |
|||||
|
|
|
|
|
|
||
|
с(1/ zB) |
|
|
m |
|
||
или |
|
|
. |
(4.6) |
|||
|
M(1/ zB) V |
||||||
Эквивалентом называют реальную или условную частицу вещества, которая может замещать, присоединять, высвобождать или быть какимлибо другим способом равноценна по химическому действию одному иону

15
водорода в кислотно-основных или ионно-обменных реакциях или одному электрону в окислительно-восстановительных реакциях.
Формула эквивалента для вещества В имеет вид 1/z В, где 1/z называют фактором эквивалентности (его еще обозначают fэкв), а z – эквивалентным числом. Например, для H2SO4 фактор эквивалентности равен ½, эквивалентное число равно 2, при условии, что оба иона водорода будут участвовать в химической реакции.
Молярная и нормальная концентрация связаны между собой формулой с(1/z В) = z c (B).
Титр – это отношение массы растворенного вещества (в г) к объему его раствора (в см3).
T(B) |
m(B) |
(г/см3 ). |
(4.7) |
|
|
||||
V |
||||
|
|
|
Зная титр раствора, можно вычислить молярную и нормальную концентрацию:
с(В) |
n(B) 1000 |
|
|
m(B) 1000 |
T(B) 1000 |
, |
(4.9) |
|||||
V |
|
|
|
|
M(B)V |
|
M(B) |
|
||||
|
|
|
|
|
|
|||||||
или |
c(1/zB) |
T(B) 1000 |
. |
|
|
|
(4.9а) |
|||||
|
|
|
|
|
|
|||||||
|
|
|
|
M(1/ zB) |
|
|
|
|
||||
Плотность раствора (ρ) – это отношение массы раствора к его |
||||||||||||
объему: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
(г/см3 ) . |
|
|
|
(4.10) |
|||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
V |
|
|
|
|
||||
Соотношение между массовой долей (в%), плотностью и молярной (или нормальной) концентрацией следующее:
с(В) |
10 |
, |
|
(4.11) |
|
|
|
||||
|
|
M(B) |
|
||
c(1/zB) |
|
10 |
. |
(4.11а) |
|
|
|||||
|
|
M(1/ zB) |
|
||
Пример 1. Определите массовую долю (в%) азотной кислоты в 4,3 М растворе HNO3, плотность которого составляет 1,14 г/см3.
Решение. Из формулы 4.11 находим выражение массовой доли ω
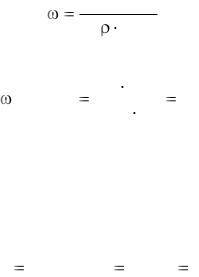
16
с(В)М(В) . 10
Молярная масса азотной кислоты равна 63,0 г/моль,
(HNO |
3 ) |
4,3 |
63,0 |
23,8%. |
|
|
|
||||
1,14 10 |
|||||
|
|
|
|||
Пример 2. Определите массу хлорида бария, необходимую для приготовления 2 дм3 децинормального раствора.
Решение. Фактор эквивалентности BaCl2 равен ½, эквивалентная масса равна половине молярной массы:
M(1/ 2BaCl |
2 ) |
M(BaCl |
2 ) |
|
208,2 |
104,1г/моль . |
2 |
|
2 |
||||
|
|
|
|
|||
Из формулы 4.6 находим выражение массы:
m(BaCl2) = c(1/2BaCl2) M(1/zBaCl2)V = 0,1 ∙ 104,1 ∙ 2 = 20,8 г.
4.1.Раствор с массовой долей КОН 15% имеет плотность ρ = 1,14 г/см3. Рассчитаете его молярную концентрацию.
4.2.Определите массу NaCl, которая требуется для приготовления 2 дм3 0,1 М раствора.
4.3.Определите массу BaCl2, которая требуется для приготовления 500 см3: а) 0,2 н. раствора; б) 0,1 М раствора.
4.4.Какова молярная концентрация 0,15 н. раствора H3PO4?
4.5.Какова молярная концентрация раствора с массовой долей H3PO4
14,6% (плотность ρ = 1,08 г/см3)?
4.6.Какова эквивалентная (нормальная) концентрация серной кислоты с массовой долей 8% (плотность ρ = 1,055 г/см3)?
4.7.В 200 см3 раствора находится 0,166 г иодида калия. Рассчитайте молярную концентрацию и титр этого раствора.
4.8.В 200 см3 раствора содержится 1 г NaOH. Вычислите молярную концентрацию и титр этого раствора.
4.9.1,825 г хлороводорода содержится в 500 см3 раствора. Определите молярную концентрацию и титр этого раствора.
4.10.Титр раствора NaCl составляет 0,0058 г/см3. Какова его молярная концентрация?
17
4.11.Сколько граммов HCl содержится в 1 дм3 0,1 М раствора соляной кислоты?
4.12.Титр раствора H2SO4 составляет 0,0049 г/см3. Какова его нормальная (эквивалентная) концентрация?
4.13.Определите массу нитрата натрия, которая требуется для приготовления 2 дм3 децимолярного раствора.
4.14.Определите массовую долю (в%) карбоната калия в его 2 М растворе
(ρ = 1,21 г/см3).
4.15.Рассчитайте титр 0,05 н. раствора H2SO4.
4.16.Титр раствора Ba(OH)2 равен 0,00855 г/см3. Какова нормальная (эквивалентная) концентрация этого раствора?
4.17.Сколько граммов H2SO4 содержится в 2 дм3 0,2 н. раствора серной кислоты?
4.18.Определите массовую долю (в%) КОН в его 2 М растворе (ρ = 1,095 г/см3).
4.19.Сколько граммов AgNO3 необходимо взять для приготовления 2 дм3 0,05 М раствора?
4.20.Титр Ba(OH)2 равен 0,0086 г/см3. Какова его нормальная (эквивалентная) концентрация?
4.21.Определите нормальную (эквивалентную) концентрацию фосфорной кислоты с ρ = 1,060 г/см3.
4.22.Титр раствора AgNO3 равен 0,00169 г/см3. Определить его молярную концентрацию.
4.23.Какую массу сульфита натрия необходимо взять для приготовления 2 дм3 0,1 н. раствора Na2SO3, участвующего в полуреакции
Na2SO3 - 2ē + H2O = Na2SO4 + 2H+?
4.24.Определите массу NaOH, необходимую для приготовления 200 см3 раствора с массовой долей NaOH 30% (плотность раствора ρ = 1,33 г/см3).
4.25.В 40 г воды растворили 3,5 г медного купороса CuSO4 ∙ 5H2O. Рассчитать массовую долю (в%) сульфата меди в полученном растворе.
Тема 5. Определение кислотности растворов электролитов
По степени диссоциации электролиты делят на сильные и слабые. Сильные электролиты практически полностью диссоциируют в растворах.
18
К ним относятся: 1) неорганические кислоты – соляная HCl, иодоводородная HJ, бромоводородная HBr, азотная HNO3, серная H2SO4, хлорная HClO4, марганцовая HMnO4; 2) гидроксиды щелочных и щелочно-
земельных металлов – KOH, NaOH, LiOH, Ba(OH)2, Ca(OH)2; 3) все соли, в
том числе считающиеся практически нерастворимыми в воде, так как они в действительности растворяются, но в очень малой степени. Растворы таких солей сильно разбавлены, в них нет недиссоциированных молекул, а есть только ионы, число которых незначительно.
Слабые электролиты – вещества, которые частично диссоциируют на ионы. К ним относятся: 1) неорганические кислоты – угольная H2CO3, кремневая H2SiO3, сернистая H2SO3, азотистая HNO2, фосфорная H3PO4, хлорноватистая HClO, циановодородная (синильная) HCN, борная H3BO3, сероводородная H2S и др.; 2) малорастворимые в воде гидроксиды металлов, гидроксид аммония и вода; 3) органические кислоты: муравьиная HCOOH, уксусная CH3COOH, щавелевая H2C2O4 и др. ; 4) комплексные ионы, например, [Ag(NH3)2]+.
По кислотно-основным свойствам растворы подразделяются на кислые, нейтральные и щелочные. Это качественная характеристика среды. Для количественной характеристики используют молярную концентрацию ионов водорода. Более удобно кислотность (основность) водных растворов выражать через десятичный логарифм молярной концентрации ионов Н+, взятый с обратным знаком. Эта величина
называется водородным показателем и обозначается символом рН: |
|
рН = - lg c(H+). |
(5.1) |
По аналогии с рН введен гидроксильный показатель рОН, |
|
рОН = - lg c(OH-). |
(5.2) |
Ионное произведение воды Kω – постоянную величину для чистой воды и водных растворов – также можно представить в логарифмической
форме |
|
Кw = с(Н+) с (ОН-) = 1 ∙ 10-14, |
(5.3) |
рКw = рН + рОН = 14. |
(5.4) |
Если раствор нейтральный , то рН = рОН = 7. В кислом растворе рН < 7, в щелочном растворе рН > 7.
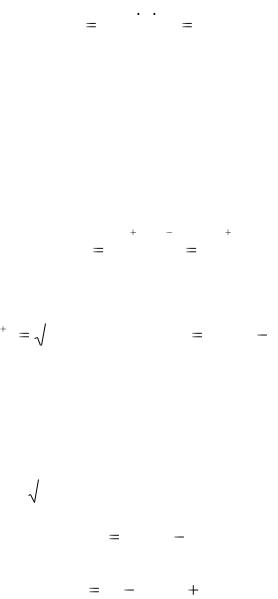
19
Определение рН среды – важная аналитическая задача. При расчете рН сильных кислот и оснований учитывают их практически полную диссоциацию в воде.
Пример 1. Считая диссоциацию хлороводородной кислоты в воде полной, вычислите рН 0,01 М раствора HCl.
Решение. Концентрация ионов водорода в растворе равна концентрации хлороводородной кислоты
с(Н+) = 0,01 моль/дм3, рН = - lg c(H+), рН = - lg 1 ∙10-2 = 2.
Пример 2. Рассчитать рН 0,56% раствора гидроксида калия (ρ = 1 г/см3). Решение. Определяем молярную концентрацию 0,56% раствора
КОН по формуле 4.11.
с(КОН) |
0,56 1 10 |
0,1 моль / дм3 |
, |
|
|
||||
56 |
||||
|
|
|
рОН = - lg c(OH-) = - lg 0,1 = 1,
рН = 14 – рОН = 14 -1 = 13.
Слабые кислоты и основания диссициациируют в растворе мало.
HA + H2O = H3O+ + A-.
Можно считать, что с(НА) = [HA], и [H+] = [A-], тогда выражение константы кислотности Ка принимает следующий вид:
|
|
|
[H ][A ] |
|
|
|
[H ]2 |
|
|
|
|||||||||||||
|
|
Ka |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
||
|
|
[HA] |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
c(HA) |
|
|
|
||||||||||||
отсюда |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
pK a |
1 |
lg c(HA) . |
|
|||||
[H ] Ka c(HA) |
|
и |
pH |
|
|
(5.5) |
|||||||||||||||||
2 |
2 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Аналогично, допуская, что в растворе слабого основания |
|||||||||||||||||||||||
единственным источником OH- – ионов может быть равновесие |
|
||||||||||||||||||||||
|
|
В + Н2О = ВН+ + ОН-, |
|
|
|
||||||||||||||||||
получаем |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
[OH-] = Kв с(В), (где Кв – константа основности) |
|
||||||||||||||||||||||
|
|
рОН |
1 |
pK |
|
1 |
lg c(B), |
|
|
|
|||||||||||||
|
|
2 |
в |
2 |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
или рН 14 |
|
|
1 |
pK в |
|
|
|
1 |
lg c(B). |
|
|
(5.6) |
|||||||||||
2 |
2 |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
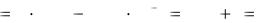
20
Значения рКa и pKв приведены в Приложении 1.
Пример 3. Рассчитайте рН 0,01 М раствора уксусной кислоты. Решение. Показатель константы кислотности рКа уксусной кислоты
согласно справочным данным равен 4,76. Решение проводим по формуле 5.5.
рН |
1 |
4,76 |
1 |
lg1 10 2 |
2,38 1 3,38. |
|
2 |
2 |
|||||
|
|
|
|
5.1.Рассчитать рН 0,01 М раствора HNO3.
5.2.Рассчитать рН 0,02 М раствора NaOH.
5.3.Рассчитать рН 0,36% раствора HCl (ρ = 1 г/см3).
5.4.Рассчитать рН 0,6% раствора уксусной кислоты (ρ = 1 г/см3).
5.5.Рассчитать рН 0,17% раствора аммиака (ρ = 1 г/см3).
5.6.Рассчитать рН 0,5% раствора аммиака (ρ = 0,996 г/см3).
5.7.Рассчитать рН 0,6% раствора гидроксида натрия (ρ = 1,005 г/см3).
5.8.Рассчитать рН водного раствора, 200 см3 которого содержат 4,0 г гидроксида натрия.
5.9.Рассчитать рН водного раствора, 100 см3 которого содержат 0,56г гидроксида калия.
5.10.Рассчитать рН 0,02 М раствора HClO4.
5.11.Рассчитать рН раствора ,1 дм3 которого содержит 5,6 г гидроксида калия.
5.12.Рассчитать рН 0,05 М раствора HNO3.
5.13.Рассчитать рН 0,01 М раствора NH4OH.
5.14.Рассчитать рН 1% раствора хлорной кислоты HClO4 (ρ = 1,005 г/см3).
5.15.Рассчитать рН 0,3% раствора уксусной кислоты (ρ = 1 г/см3).
5.16.Рассчитать рН раствора молочной кислоты HC3H5O3 с концентрацией 0,01 моль/дм3.
5.17.Рассчитать рН раствора бензойной кислоты C6H5COOH с концентрацией 0,1 моль/дм3.
5.18.Рассчитать рН раствора муравьиной кислоты HCOOH, с концентраций 0,02 моль/дм3.
5.19.Рассчитать рН 0,02 М раствора LiOH.
5.20.Рассчитать рН 0,05 М раствора NaOH.
21
5.21.Рассчитать рН 0,03 М раствора КОН.
5.22.Рассчитать рН водного раствора, 100 см3 которого содержат 2г гидроксида натрия.
5.23.Рассчитать рН раствора, 2 дм3 которого содержат 0,2 моль HCl.
5.24.Рассчитать рН 0,15% раствора уксусной кислоты (ρ = 1 г/см3).
5.25.Рассчитать рН 0,34% раствора аммиака (ρ = 1 г/см3).
Тема 6. Гидролиз солей
Для предложенных водных растворов солей Вашего варианта определите возможность протекания реакции гидролиза. Необходимо вспомнить, что реакция между ионами соли и водой протекает только в том случае, если образуются слабые (в том числе малорастворимые) электролиты (см. Приложение 4). Это приводит к смещению равновесия в диссоциации воды и, следовательно, к изменению рН среды. Таким образом, чтобы выполнить это задание, надо знать сильные и слабые кислоты и основания, а также шкалу рН в водных растворах. Соли, образованные сильной кислотой и сильным основанием не приводят к смещению равновесия и изменению рН среды.
В случае протекания реакции гидролиза запишите соответствующие уравнения реакции, определите тип гидролиза (по катиону или аниону) и определите реакцию среды (рН >7; рН = 7; рН<7).
6.1.Bi(NO3)3, KCl, K2SO4, BaCl2, Na2SO3.
6.2.KJ, Na2HPO4, SnCl2, NaCl, NaNO3.
6.3.MgCl2, FeCl2, Na2S, Na2SO4, NaCl.
6.4.K2CO3, NaBr, AlCl3, KCl, Ba(CH3COO)2.
6.5.KJ, Fe(NO3)3, Ca(NO3)2, NH4NO3, NH4NO2.
6.6.LiCl, Ca(CH3COO)2, Na2SO4, BaCl2, (NH4)2SO4.
6.7.Na2SO4, (NH4)2SO4, Al2(SO4)3, Na2SO3, NaNO3.
6.8.NH4NO2, CaCl2, KCl, NaNO3, KCN.
6.9.Na2SO3, K2SO4, K2S, NaNO3, FeCl3.
6.10.Ba(NO3)2, FeCl3, NaBr, K2SO4, (NH4)2S.
6.11.Na2SO4, Na2CO3, (NH4)2CO3, KJ, SnCl2.
6.12.K2SO3, BiCl3, NH4Cl, KJ, NaNO3.
