
5598
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Хабаровская государственная академия экономики и права»
Кафедра естественнонаучных дисциплин
ПИЩЕВАЯ ХИМИЯ
Методические указания по выполнению лабораторных работ для студентов 2 го курса направления 19.03.04
«Технология продукции и организация общественного питания» очной и заочной форм обучения
Хабаровск 2014
ББК В 3
Х 12
Пищевая химия : Методические указания по выполнению лабораторных работ для студентов 2 го курса направления 19.03.04 «Технология продукции и организация общественного питания» очной и заочной форм обучения / сост. И. А. Жарская. – Хабаровск : РИЦ ХГАЭП, 2014. – 52 с.
Рецензент доцент кафедры химии Дальневосточного государственного медицинского университета канд.хим.наук Н. Н. Минаева
Утверждено издательско-библиотечным советом академии в качестве методических указаний для студентов
© Хабаровская государственная академия экономики и права, 2014
2
СОДЕРЖАНИЕ Введение……………………………………………………………………………….4 Тема 1. Белковые вещества……………………………………….………………….5
Лабораторная работа 1.1. Определение свежести мяса и рыбы методом люминисцентного анализа……………………………………………………………5 Тема 2. Углеводы………………………………………………………………….…..7
Лабораторная работа 2.1. Определение содержания сахаров в продуктах питания………………………………………………………………………………...7
Лабораторная работа 2.2. Определение качества мёда…………………………....10
Тема 3. Липиды (жиры и масла)……………………………………………………18
Лабораторная работа 3.1. Определение качества жиров и масел………………...18 Лабораторная работа 3.2. Анализ жиров методом люминисцентного анализа....23 Тема 4. Минеральные вещества и вода………………………………………….…25 Лабораторная работа 4.1. Определение содержания ионов кальция /(в соках, винах) титриметрическим методом………………………………………………...25 Лабораторная работа 4.2. Определение содержания ионов железа (III) в белых винах методом фотометрии………………………………………………...……….27 Тема 5. Витамины……………………………………………………………………29
Лабораторная работа 5.1. Определение β-каротина в овощах и фруктах методом фотометрии………………………………………………………………………..…29 Тема 6. Пищевые кислоты…………………………………………………………..32
Лабораторная работа 6.1. Методы определения кислот в пищевых продуктах…40 Лабораторная работа 6.2. Определение хлоридов и сульфатов в минеральной воде методом ионообменной хроматографии……………………………………..42 Тема 7. Биологически активные добавки……………………………..……………44 Лабораторная работа 7.1. Определение содержания этанола в белых и красных винах методом рефрактометрии……………………………………………………44 Лабораторная работа 7.2. Определение кофеина в чае экстракционноспектрометрическим методом…………………………………………...………….47 Библиографический список…………………………………………………………50
Приложение……………………………………………………………………...…..51
3
ВВЕДЕНИЕ
Пищевая химия – это наука о химическом составе пищевых систем (сырьё, полуфабрикаты, готовые пищевые продукты), его изменениях в ходе технологического потока под влиянием различных факторов (физических, химических, биохимических и т.д.), а также о методах анализа веществ, входящих в пищевые системы.
Современные специалисты в области пищевых производств должны в совершенстве владеть методами анализа, исследования и контроля сырья, полуфабрикатов и готовой продукции для обеспечения оптимального ведения технологического процесса, отсутствия брака, высокого качества готовой продукции.
Методические указания по курсу «Пищевая химия» знакомят студентов с основными приёмами и методами анализа, используемыми в технологии продуктов питания. В результате выполнения лабораторных работ студенты должны приобрести теоретические представления и практические навыки экспериментальной работы по оценке качества пищевых продуктов.
Каждая работа выполняется студентами после изучения соответствующего теоретического материала, ознакомления с планом и описанием методики работы. Факт выполнения задания фиксируется в лабораторном журнале.
Оформленная лабораторная работа включает следующие разделы:
1.Название работы.
2.Цель лабораторной работы.
3.Метод анализа, используемого в работе.
4.Названия этапов работы.
5.Полученные результаты, расчеты и графики.
6.Вывод.
Защита выполненных лабораторных работ осуществляется каждым студентом индивидуально.
4
ТЕМА 1. БЕЛКОВЫЕ ВЕЩЕСТВА
ЛАБОРАТОРНАЯ РАБОТА 1.1.
ОПРЕДЕЛЕНИЕ СВЕЖЕСТИ МЯСА И РЫБЫ МЕТОДОМ ЛЮМИНИСЦЕНТНОГО АНАЛИЗА
Мясо относится к категории скоропортящихся продуктов. Оно подлежит постоянному ветеринарному и санитарному контролю. Существующие методы исследования мяса (ГОСТ 7269-79) весьма трудоёмки. Органолептические показатели – субъективны. Люминесцентный метод – наиболее простой и быстрый. Метод основан на определении цвета люминесценции, который при различных состояниях продукта претерпевает изменения. Этот метод особенно показателен для определения фальсификации фарша одного вида другим, а также замене части мяса субпродуктами или другими добавками. Метод позволяет выявить мясо, заражённое цистериками.
Цель работы – определить качество рыбы и мяса на основе люминесценции.
Реактивы, материалы и оборудование
Мясорубка или гомогенизатор; колбы; фильтры бумажные; воронки; цилиндры; нож или скальпель; пинцет; чашки Петри; люминоскоп.
Ход работы:
1. Анализ мяса. Анализу подвергаются как срезы, так и экстраты мяса.
- Острым ножом делают срез мяса и в чашке Петри помещают в люминоскоп. Цвет люминесценции сравнивают с данными в нижеприведённой таблице.
Показатели люминесценции говядины и мясного экстракта в зависимости от степени свежести
Степень свежести |
Цвет люминесценции |
|
мяса говядины |
|
|
|
|
|
|
Мышечная ткань |
Экстракт |
|
|
|
Свежее мясо |
От тёмно-коричневого до |
Прозрачный |
|
красно-коричневого |
|
|
|
|
Несвежее мясо |
Тусклый, тёмно-коричневый, |
Мутный, светло- |
|
неравномерный с серыми и |
жёлтый с зеленоватым |
|
зелёными пятнами. |
оттенком |
|
|
|
|
5 |
|
-Для приготовления экстракта мяса 10 г мяса измельчают, помещают в колбу и заливают 50 см3 дистиллированной воды. Настаивают 10 мин, периодически взбалтывая, фильтруют через двойной бумажный фильтр, помещают в люминоскоп.
-Исследование фарша котлет. Мясное изделие разрезают по центру на 2 части и рассматривают невооружённым глазом. По цвету и рисунку разреза определят наличие посторонних примесей. Затем рассматривают в камере люминоскопа.
-Исследование мяса, поражённого цистериками. Мясо нарезают тонкими пластинками длиной 5, шириной 2 – 3, толщиной 0,5 см и помещают в ультрафиолетовые лучи. Изолированные цистерики люминесцируют розовым цветом, а цистерики, включённые в мышечную часть, приобретают оранжевый оттенок, придающий всей картине тёмно-красный фон.
2. Анализ рыбы
-Острым ножом делают срез рыбы и в чашке Петри помещают в люминоскоп. Отделяют жабры и помещают в люминоскоп.
-Приготовление спиртового экстракта рыбы. 10 г рыбы измельчают, помещают в колбу и заливают 50 см3 спирта. Настаивают 10 мин, периодически взбалтывая, фильтруют через двойной бумажный фильтр, помещают в люминоскоп.
Цвет люминесценции сравнивают с нижеприведёнными данными.
Усвежей рыбы жабры не люминесцируют; поверхность тела люминесцирует слабым серым цветом с заметным фиолетовым оттенком, причём непигментированные участки имеют светло-фиолетовый, а пигментированные – тёмно-фиолетовый цвет. Мышцы на разрезе светятся тусклым серо-фиолетовым цветом, зеленовато-синим, иногда серо-жёлтым цветом. Кровь в сосудах имеет темно-коричневое свечение.
Лежалая, но допустимая в пищу рыба люминесцирует интенсивным белым цветом с голубоватым оттенком.
Урыбы, имеющей признаки начальной порчи, на свежем разрезе мышц появляются яркие пятна канареечного цвета, иногда сплошное жёлтое свечение.
Спиртовая вытяжка из мышц рыбы люминесцирует бледно-голубым цветом с желтоватым оттенком; по мере увеличения степени порчи рыбы цвет люминесценции становится ярко-жёлтым.
6
ТЕМА 2. УГЛЕВОДЫ
ЛАБОРАТОРНАЯ РАБОТА 2.1.
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ САХАРОВ В ПРОДУКТАХ ПИТАНИЯ
В современных пищевых производствах для придания продуктам сладкого вкуса в основном используют сахарозу и сахарозаменители природного происхождения (глюкозно-фруктовые сиропы, фруктозу, сорбит, ксилит), а также синтетические подсластители – аспартам, цикламаты, сахарин.
Чаще всего используется сахароза (тростниковый, свекольный сахар). Сахароза – невосстанавливающийся сахар, но она способна к кислотному или ферментативному гидролизу с образованием инвертного сахара.
Общий сахар – это суммарное содержание сахарозы и редуцирующих сахаров, выраженное в процентах сахарозы. Метод основан на окислении общего сахара дихроматом калия в сильнокислой среде:
C12H22O11+8Cr2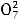
 +64H+→12CO2+16Cr+3+43H2O;
+64H+→12CO2+16Cr+3+43H2O;
C6H12O6+4Cr2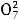
 +32H+→6CO2+8Cr3++22H2O.
+32H+→6CO2+8Cr3++22H2O.
Соединения хрома Cr3+ окрашены в сине-зеленый цвет, их количество пропорционально содержанию общего сахара в анализируемом продукте.
Определение содержания Cr3+ проводят фотоколориметрически.
Цель работы – определить содержание общего сахара в исследуемом продукте фотометрическим методом.
Реактивы, материалы и оборудование
Дихромат калия; раствор сахарозы 0,004мг/см3; серная кислота концентрированная; сульфат цинка, 0,5 М раствор; гидроксид натрия, 1М раствор; колбы мерные 100, 200 см3; пипетки 10 см3; мерные цилиндры 25 см3; бюретка; водяная баня; плитка электрическая; весы; фотоэлектроколориметр с набором кювет.
Ход работы
1.Приготовление реактивов
1.1.Основной реактив: 49 г дихромата калия растворяют при нагревании в 300 см3 воды, отдельно в 300 см3 воды медленно при перемешивании вводят 300 см3 концентрированной серной кислоты и охлаждают. В мерную колбу вместимостью 1000 см3 сначала помещают раствор дихромата калия, затем серную кислоту, объём доводят водой до метки, осторожно перемешивают.
7
1.2. Стандартный раствор сахарозы 1,000 0 г сахарозы взвешивают с точностью до 0,000 2 г и растворяют в мерной колбе вместимостью250 см3. Объём раствора доводят до метки дистиллированной водой.
2.Построение градуировочного графика.
В6 мерных колб вместимостью 100 см3 вносят 25мл раствора дихромата калия. Затем во все колбы последовательно вносят 0; 2; 4; 6; 8; 20 см3
стандартного раствора сахарозы. Затем во все колбы из бюретки приливают дистиллированную воду до объема 50 см3 (т.е. добавляют в каждую колбу соответственно 25, 23, 21, 19, 17 и 5 см3 воды ), таким образом получают серию растворов, содержащих соответственно 0; 8; 16; 24; 32 и 80 мг сахарозы в 100 см3.
Содержимое каждой колбы нагревают на кипящей водяной бане в течение 10 мин, охлаждают под струёй водопроводной воды. После чего объём растворов доводят до метки дистиллированной водой и перемешивают.
Измеряют оптическую плотность полученных растворов на фотоэлектроколориметре при длине волны λ=670 нм и толщине кюветы 5 см. В качестве раствора сравнения используют раствор с нулевой концентрацией сахарозы. Оптическую плотность каждого раствора определяют не менее 3 раз и из полученных данных берут среднее значение. По этим данным строят график зависимости величин оптической плотности от содержания сахарозы в 100 см3 раствора, мг/100 см3.
3.Подготовка образца к испытанию Анализируемый образец измельчают в ступке. Затем готовят водную вытяжку объекта исследования. Примерные навески:
Хлеб, мука, галеты – 2 г Несладкое печенье – 4 г
Натуральные соки (кроме виноградных) – 4 г Хлеб ржаной, сдобные хлебобулочные изделия, печенье – 2 г Мука – 5 г Корпуса конфет, леденцы – 1 г
Навеску, взятую с точностью до 0,01 г, растворяют в стакане до 60 С. При этом могут возникнуть следующие варианты:
С. При этом могут возникнуть следующие варианты:
а) Если растворяется в воде без остатка (леденцы, сироп, соки), то полученный в стаканчике раствор охлаждают и переносят в мерную колбу 100 или 200 см3. Объём раствора доводят до метки дистиллированной водой и хорошо перемешивают.
8
б) Если в изделии находится вещества, нерастворимые в воде, мешающие определению – белки, жиры, пектины, крахмал и т.п., то навеску переносят в мерную колбу вместимостью 100 см3 или 200 см3, смывая частицы дистиллированной водой. Колбу с жидкостью помещают в термостат, нагретый до 60 С. При этой температуре выдерживают колбу в течение 15 мин, периодически помешивая. За это время практически все сахара переходят в раствор. Охладив раствор, осаждают мешающие компоненты, прибавляя к нему 5 см3 0,5М раствора ZnSO4 и 2,5 см3 1М раствора КОН или NaOH. Затем доводят раствор до метки дистиллированной водой и фильтруют.
С. При этой температуре выдерживают колбу в течение 15 мин, периодически помешивая. За это время практически все сахара переходят в раствор. Охладив раствор, осаждают мешающие компоненты, прибавляя к нему 5 см3 0,5М раствора ZnSO4 и 2,5 см3 1М раствора КОН или NaOH. Затем доводят раствор до метки дистиллированной водой и фильтруют.
4.Определение общего сахара В мерную колбу 100 см3 отбирают 10 см3 прозрачного фильтрата, добавляют
мерным цилиндром 25 см3 дихромата калия и 15 см3 воды. Колбу нагревают на кипящей водяной бане в течение 10 мин. Охлаждают, добавляют до метки дистиллированную воду, перемешивают и определяют оптическую плотность так же как при построении калибровочного графика.
5.Расчёт содержания общего сахара По градуировочному графику находят содержание сахарозы раствора, что
соответствует содержанию сахарозы во взятой пробе, выраженной в мг/100 см3. Содержание общего сахара в ω% в анализируемом продукте вычисляют по формуле


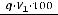 ,
,
где q – содержание общего сахара, найденное по калибровочному графику; V1 – объем мерной колбы;
V2 – объем фильтрата, взятый для реакции с дихроматом калия; m – масса навески исследуемого вещества.
Вопросы и задания для самоподготовки
1.Напишите формулу сахарозы. Какие моносахариды образуются при кислотном гидролизе сахарозы?
2.Что такое инвертированный сахар? Как он образуется? Объясните, почему пищевой сахар не даёт реакцию серебряного зеркала, а инвертированный даёт.
3.Напишите формулы мальтозы и сахарозы. Наблюдается ли явление мутаротации в свежеприготовленных растворах этих дисахаридов?
4.Какие углеводы относятся к усваиваемым и не усваиваемым? Какие функции в организме человека они выполняют? Приведите по одному примеру из каждой группы углеводов.
9
5.Какая реакция лежит в основе фотометрического определения сахаров? Почему, используя реакцию, можно определить суммарное содержание сахаров, а не индивидуальную сахарозу?
6.Что такое карамелизация сахаров?
ЛАБОРАТОРНАЯ РАБОТА 2.2. ОПРЕДЕЛЕНИЕ КАЧЕСТВА МЁДА
Мёд – природный сладкий продукт, вырабатываемый пчелами. В отличие от сахара и других сладких продуктов в мёде хорошо выраженный сладкий вкус со сложным ароматом. Мёд имеет высокую энергетическую ценность – 1280 кДж на 100 г и, самое важное, имеет биологическую ценность обусловленную содержанием витаминов, аминокислот, ферментов, минеральных веществ,
антибиотики придающие бактерицидные свойства мёду.
Мёд содержит сахара, которые легко усваивают организмом, кроме того, мёд содержит алкалоиды лечебных растений, поэтому он обладает жаропонижающим, противовоспалительными свойствами. Натуральный мёд представляет собой сладкую, вязкую ароматическую жидкость или закристаллизованную массу различной консистенции и различных тональных цветов от бесцветной жёлто-коричневой до тёмно-бурых тонов.
Натуральный мёд по биологическому происхождению подразделяется на
-цветочный;
-падевый;
-смешанная смесь цветочного и падевого мёда.
Цветочный мёд квалифицируется:
-на монофлерный – собранный с одного вида растений (липовый,
акациевый, гречишный, подсолничнековый, вересковый);
-полифлерный – собранный с различных видов растений.
Падевый мёд образуется при сборе пчёлами пади и медвяной росы. Падь – жидкость выделяемая насекомыми – тля, черви. Медвяная роса – сладкий сок,
выделяемый листьями или хвоей, при резкой смене температуры и давления. С
листьев хвойных пород – хвойный мёд имеет зеленоватый оттенок. Такой мёд
10
