
Полезные материалы за все 6 курсов / Учебники, методички, pdf / Биохимия в рисунках
.pdfЗадания для самопроверки и самокоррекции
Задача 1. Подтверждением диагноза бери-бери, поставленного врачом, послужил результат анализа мочи, показавший :
А. Повышенное показание оксалата В. Повышенное количество лактата
С. Повышенное количество ацетоацетата D. Повышенное количество пирувата
Е. Повышенное количество глутамата
Задача 2. У больного туберкулезом после курса лечения изониазидом, антагонистом пиридоксина, лабораторно подтверждена аминоацидурия. Нарушение каких метаболических реакций является побочным эффектом препарата?
А. Трансаминирование аминокислот В. Окислительное дезаминирование аминокислот
С. Трансметилирование аминокислот D. β-окисление высших жирных кислот Е. Обезвреживание биогенных аминов
Задача 3. При превращении проколлагена в коллаген происходит
гидроксилирование аминокислот лизина и пролина. Какой витамин участвует в
этом процессе?
А. А В. В6 С. Вс
D. С
Е. РР
Задача 4. После длительного приема сульфаниламидов у больной развилась анемия. Выберите причину её развития.
А. Нарушение синтеза кобаламина В. Нарушение синтеза фолиевой кислоты С. Гиповитаминоз К
D.Гиповитаминоз А Е.Гиповитаминоз В1
Правильность решения проверьте, сопоставив их с эталонами ответов.
1-D, 3-D, 5-B.
30
РАЗДЕЛ 3. ВВЕДЕНИЕ В ОБМЕН ВЕЩЕСТВ БИОЭНЕРГЕТИКА
Биоэнергетика, или биохимическая термодинамика , занимается изучением энергетических превращений, сопровождающих биохимические реакции.
Ее основополагающие принципы позволяют объяснить, почему протекают одни реакции и невозможны другие. Небиологические системы могут совершать работу за счет тепловой энергии, биологические - за счет энергии химических процессов.
В чем важность этой темы для медицины и фармацевтики?
Вся необходимая энергия должна поступать в организм в виде топлива - питательных продуктов. Вопрос о том, как организм извлекает эту энергию - основа для понимания процессов нормального питания. Истощение энергетических ресурсов ведет к голодной смерти, запасание избыточной энергии в форме питательных веществ
– к ожирению. Коррекция нарушений обменных процессов с помощью фармацевтических средств также должна учитывать энергетические потребности организма.
Все химические реакции живой клетки подчиняются законам термодинамики.
1 закон : внутренняя энергия системы вместе с ее окружением остается постоянной, она лишь переходит из одной формы в другую. Самопроизвольно химические процессы могут протекать могут протекать только в одном направлении - к достижению равновесия, т.е. к максимальной энтропии. Энтропия - мера хаоса, неупорядоченности.
2 закон : энтропия при самопроизвольных процессах возрастает. Самопроизвольно разупорядоченная система никогда не превратиться в упорядоченную, для обращения надо затратить дополнительную энергию.
Практически проще предсказать направление химических реакций с помощью свободной энергии системы, которую можно измерить.
G = Н - T S
Энергетическое состояние любой системы можно выразить, используя это
выражение.
G- это та часть энергии системы, которую можно использовать для совершения работы;
ТS - связанная энергия, которая не может быть использована на работу;
Н - энтальпия - внутренняя энергия системы (может быть измерена экспериментально)
если G < 0, то реакция экзергоническая, т.е. протекает самопроизвольно, с освобождением энергии (эти реакции поставляют клетке энергию);
если |
G > 0, то реакция эндергоническая, т.е. идет |
|
с потреблением энергии; |
|
|
если |
G = 0 - это состояние равновесия. |
31 |
Жизненно важные процессы - реакции синтеза, мышечное сокращение, проведение нервного импульса, активный транспорт - получают энергию путем химического
сопряжения с окислительными реакциями, т.е. происходит сопряжение экзергонических реакций с эндергоническими.
Экзергоническими реакциям обычно являются катаболические реакции - распад
или окисление “топливных” молекул (энергосодержащих нутриентов), которые поступают в составе пищевых продуктов.

 Эндергоническими являются реакции анаболизма - реакции синтеза сложных биоорганических соединений – клеточных макромолекул.
Эндергоническими являются реакции анаболизма - реакции синтеза сложных биоорганических соединений – клеточных макромолекул.
•Совокупность всех биохимических превращений химических веществ в живом организме представляет собой метаболизм.
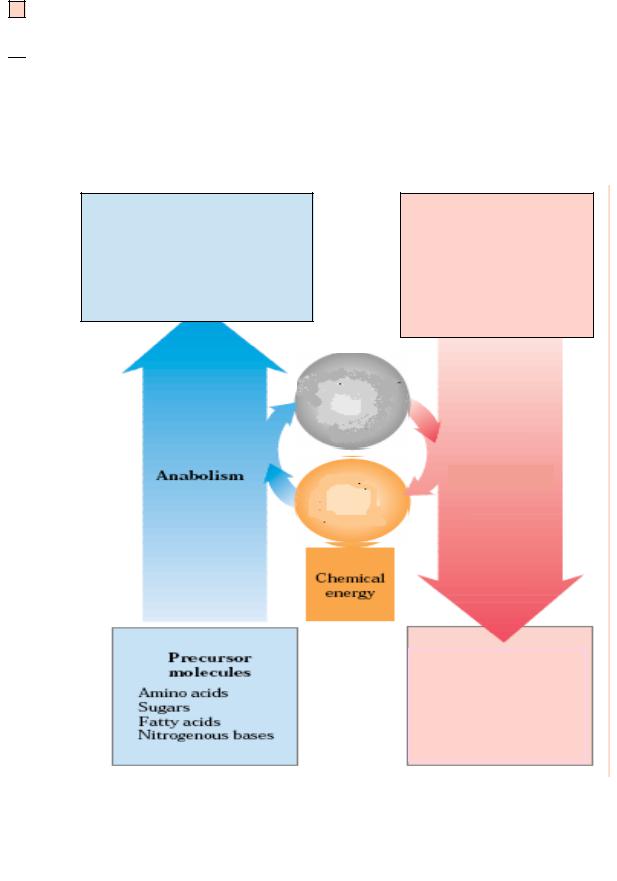
I. Сопряжение эндергонических процессов с экзергоническими
Клеточные макромолекулы:
белки
полисахариды
липиды нуклеиновые кислоты
|
|
|
АДФ+Ф |
|
|
|
НАД+ |
|
|
|
НАДФ+ |
|
|
|
ФАД |
|
|
|
АТФ |
|
анаболизм |
|
|
|
|
|
НАДН+ |
|
|
|
|
|
|
|
НАДФН+ |
|
|
|
ФАДН2 |
|
|
|
химическая |
|
|
|
энергия |
|
|
|
|
|
Молекулы- |
|
|
предшественники: |
|
||
аминокислоты |
|
||
|
моносахара |
|
|
жирные кислоты |
|
||
азотистые основания |
|
||
Энергосодержащие нутриенты:
углеводы
липиды
белки
катаболизм
Энергетически бедные конечные продукты
СО2 Н2О
NН3
Катаболические пути освобождают свободную энергию в виде
АТФ, НАДН, НАДФН и ФАДН2.
Эта энергия может быть использована в анаболических путях для
превращения малых молекул в клеточные макромолекулы.
32
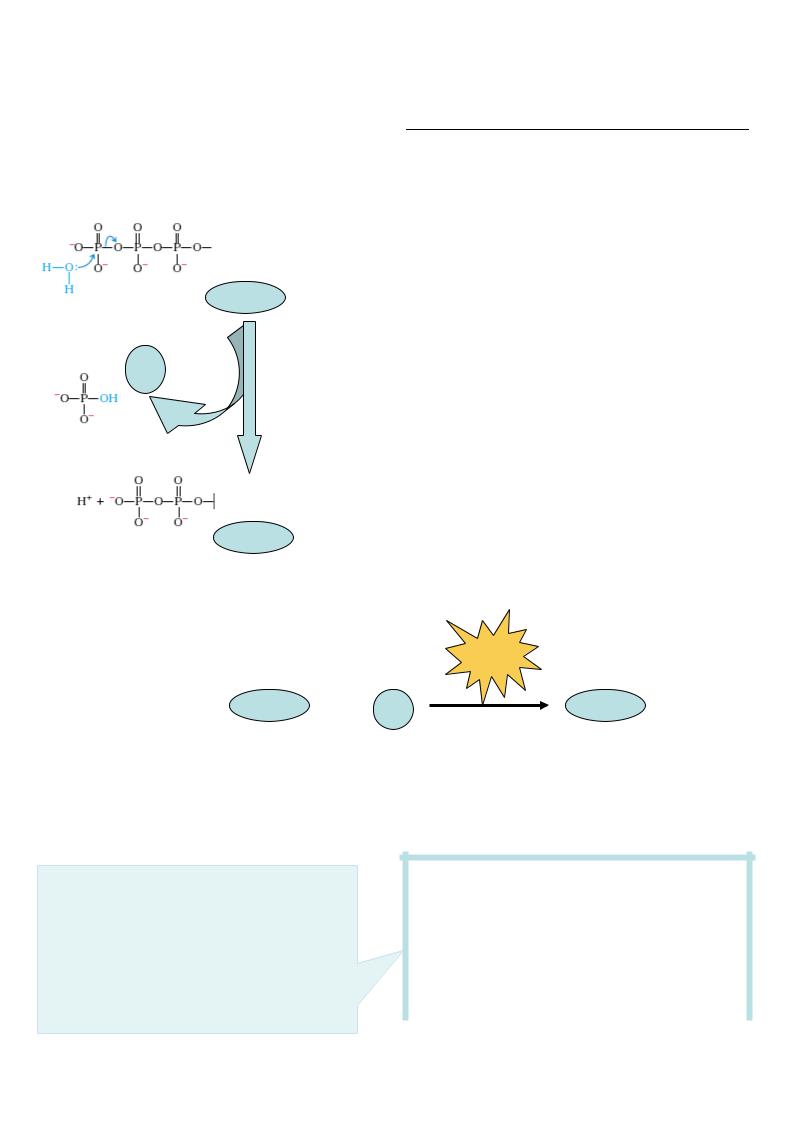
Для сопряжения этих процессов обычно необходим посредник, т.е. в процессе экзергонической реакции синтезируются соединения с высоким энергетическим
потенциалом ~Е, которые в дальнейшем используются в эндергонических реакциях. Так передается химическая энергия от экзергонического к эндергоническому
процессу. Вещества с высоким энергетическим потенциалом - макроэргические (~Е) - это биомолекулы, которые имеют высокую стандартную свободную энергию переноса
концевой фосфатной группы.
~ |
рибоза |
|
аденин |
|
|
|
|
|
Главным макроэргом в живых |
||||||
|
|
|
|
|
|||
|
АТФ |
|
|
|
организмах является |
||
|
|
|
|
аденозинтрифосфат (АТФ), который |
|||
|
|
|
|
|
обеспечивает передачу свободной |
||
|
|
|
|
|
энергии от экзергоническим процессам к |
||
Ф |
|
|
|
|
эндергоническим |
||
гидролиз |
(~) означает, что перенос группы, |
||||||
|
|
|
|
|
соединенной такой связью, |
||
|
|
|
|
|
сопровождается выделением большого |
||
|
|
|
|
|
количества свободной энергии. |
||
|
|
|
|
|
Свободная энергия гидролиза концевой |
||
|
|
|
|
|
фосфатной группы АТФ |
||
|
рибоза |
|
аденин |
|
|
|
= - 30,5 кДж/моль. |
|
|
|
|
|
|||
|
|
|
|
|
|
G0 |
|
|
АДФ |
|
|
|
|||
|
|
|
|
|
|
|
|
Синтез АТФ из АДФ и фосфата (т.е. фосфорилирование АДФ) происходит в организме двумя путями, которые отличаются источником энергии для образования макроэргической связи :
энергия
АДФ + Ф |
АТФ |
1.Окислительное фосфорилирование (основной путь синтеза) – осуществляется за счет энергии окисления различных веществ (метаболитов или субстратов окисления).
2. Субстратное фосфорилирование - осуществляется за счет энергии разрыва макроэргических связей субстрата.
Кроме АТФ, существуют и другие |
макроэрги: |
|
G0 |
|
|
макроэрги - метаболиты углеводного, |
|
|
|
|
|
фосфоенолпируват |
- 61,9 |
кДж/моль |
|||
липидного и аминокислотного |
|||||
карбамоилфосфат |
- 51, 4 кДж/моль |
||||
обменов, а также фосфагены |
|||||
1,3-дифосфоглицерат - 49,3 |
кДж/моль |
||||
(креатинфосфат), которые выступают |
|||||
в качестве резервуаров |
креатинфосфат |
- 43,1 кДж/моль |
|||
макроэргических связей: |
|
|
|
|
|
|
|
|
|
||
|
|
33 |
|||

Итак, накопление энергии в специфических фосфатных связях АТФ лежит в основе механизма переноса энергии в живой клетке. Но живая клетка - неравновесная система, поэтому возможно и накопление химической энергии в макроэргических связях за счет извлечения ее из питательных веществ.
Важно понимать, что извлечь энергию можно не непосредственно из питательных веществ, поступающих с пищей, а из продуктов их распада, которые образуются в
процессе обмена веществ.
Обмен веществ в организме человека складывается из следующих последовательных стадий
1.Поступление питательных веществ - белков, жиров, углеводов, витаминов, минеральных веществ, воды - в составе продуктов питания.
 2. Переваривание питательных веществ в ЖКТ до простых веществ, способных всасываться слизистой кишечника.
2. Переваривание питательных веществ в ЖКТ до простых веществ, способных всасываться слизистой кишечника.
 3. Биотранспорт продуктов переваривания кровью и лимфой, проникновение их через мембраны сосудов и клеток до определенных органов и тканей.
3. Биотранспорт продуктов переваривания кровью и лимфой, проникновение их через мембраны сосудов и клеток до определенных органов и тканей.
 4. Внутриклеточный метаболизм (в узком смысле слова) - промежуточный обмен.
4. Внутриклеточный метаболизм (в узком смысле слова) - промежуточный обмен.
 5. Выделение (секреция ) из организма концевых продуктов обмена веществ: углекислого газа, воды, мочевины и др.
5. Выделение (секреция ) из организма концевых продуктов обмена веществ: углекислого газа, воды, мочевины и др.
34
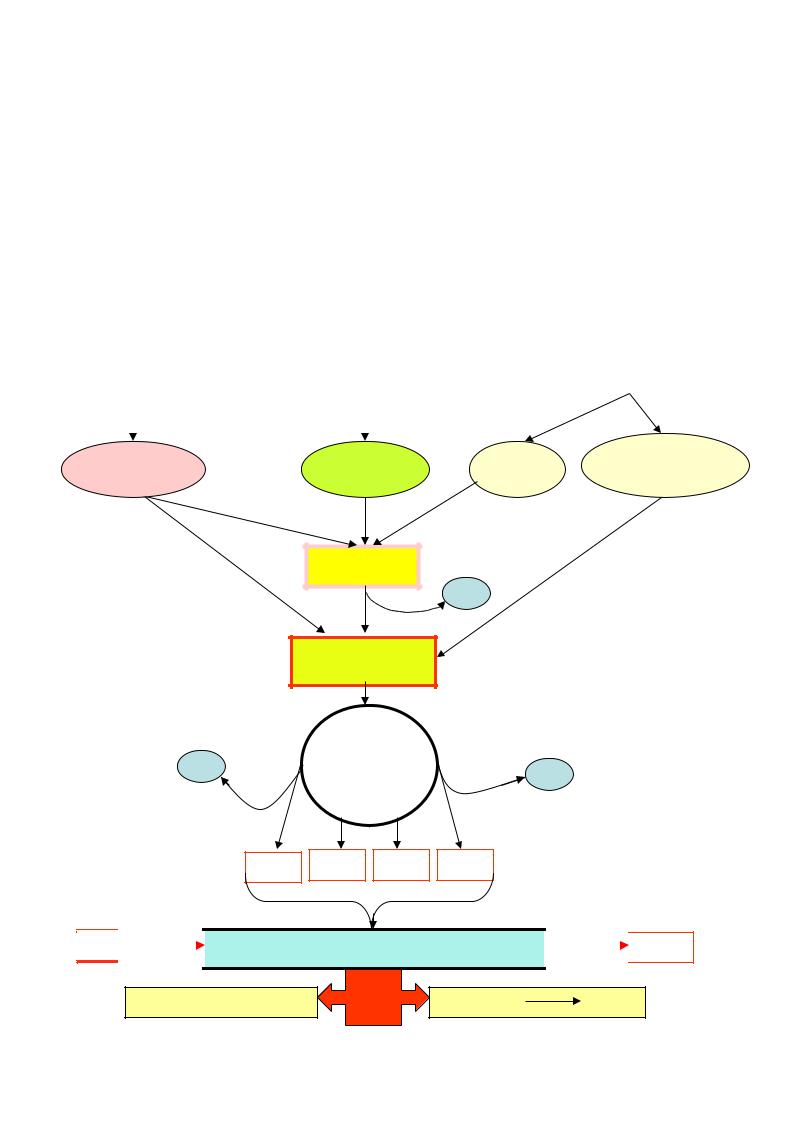
3 стадия (общая для всех обменов) - окисление ацетил~КоА до конечных метаболитов углекислого газа и воды. Эта стадия протекает в митохондриях - энергетических станциях клеток и состоит из двух процессов:
цикла трикарбоновых кислот (ЦТК), в результате которого образуется |
СО2, а атомы |
водорода используются для восстановления коферментов НАД и ФАД. |
Водород - это |
универсальное энергетическое топливо, которое используется в дыхательной цепи для образования энергии и воды.
системы электронного транспорта в мембранах митохондрий, в котором атомы водорода переносятся на кислород с образованием воды. Эта система сопряжена с окислительным фосфорилированием, в результате которого энергия биологического окисления используется для синтеза АТФ.
БЕЛКИ |
|
УГЛЕВОДЫ |
|
ЛИПИДЫ |
||
|
|
|
|
|
|
|
аминокислоты |
моносахариды |
глицерин |
жирные кислоты |
пируват
СО2
ацетил-КоА
СО2 |
ЦТК |
СО2 |
|
|
|
2Н+ |
2Н+ 2Н+ 2Н+ |
|
О2 
 Дыхательная цепь митохондрий
Дыхательная цепь митохондрий 
 Н2О
Н2О
тепло |
энергия |
АДФ + Ф |
АТФ |
|
35
III. Пути потребления кислорода в реакциях биологического окисления
Все многообразие реакций окисления, идущих с потреблением кислорода, можно свести к 4 основным типам.
1. Оксидазный путь (80-90% потребления кислорода)
Продукты - окисленный субстрат, вода и энергия. Реализуется в митохондриях в дыхательной цепи.
2. Оксигеназный путь (8-12% потребления кислорода): |
|
|
|
с помощью монооксигеназ: один атом кислорода включается в окисляемый |
|
|
субстрат, другой - в молекулу воды; |
|
с помощью диоксигеназ: оба атома кислорода входят в окисляемый субстрат |
||
|
Цель этого свободного (т.е. несопряженного) окисления - превращение природных |
|
|
или неприродных субстратов (ксенобиотиков) в микросомах печени, коры |
|
|
надпочечников, поэтому называется микросомальным окислением. |
|
|
Таким путем холестерин окисляется в стероидные гормоны и желчные кислоты, |
|
|
тирозин - в меланины. Этим же путем обезвреживаются в печени |
токсичные |
|
метаболиты и ксенобиотики - лекарственные препараты или яды. |
|
|
Микросомальные цепи представляют собой короткие цепи переноса протонов и |
|
|
электронов, источником которого служит НАДФН. а активатором кислорода - |
|
|
цитохром Р-450: |
|
3. Пероксидазный путь - с образованием перекиси водорода с помощью |
||
|
пероксидобразующих ферментов - флавопротеинов |
|
|
Таким путем окисляются аминокислоты, биогенные амины и др. |
|
|
Образование токсичного пероксида является “издержкой”, однако, в |
|
|
фагоцитирующих клетках (например, лейкоцитах) пероксид служит для |
|
|
обезвреживания патогенных бактерий. |
|
4. Свободнорадикальное окисление происходит под действием |
активных форм |
|
|
кислорода (АФК), которые образуются при одноэлектронном восстановлении |
|
• |
кислорода: |
|
супероксид-анион |
|
|
• |
перекись водорода Н2О2 |
|
• |
гидроксильный радикал |
|
• |
синглетный кислород |
|
АФК - очень реакционноспособные молекулы, которые спонтанно ускоряют цепные
реакции перекисного окисления липидов (ПОЛ) и окислительно модифицируют другие биомолекулы - белки, нуклеиновые кислоты и др.
Эти процессы потребления кислорода активно протекают в мембранах, где
имеются ненасыщенные жирные кислоты в составе фосфолипидов. Цель этого процесса - обновление мембран и регуляция их проницаемости.
Супероксиданион активирует образование в тканях NО-радикала, который способствует вазодилатации, а также, превращается в пероксинитрит ОNООН,
который индуцирует апоптоз - запрограммированную смерть клеток.
Антиоксиданты, например, витамин Е - токоферол - способны улавливать свободные радикалы, снижая тем самым токсичность кислорода.
36
IV. Биологическое окисление
•Биологическое окисление, сопровождающееся потреблением кислорода и образованием энергии
и воды, называется тканевым дыханием . Это многостадийный процесс переноса водородов
(протонов и электронов) от субстратов окисления через ряд промежуточных переносчиков к
кислороду с образованием воды и выделением энергии.
•Субстраты окисления SH2 образуются в ходе катаболизма белков, жиров и углеводов. Это
вещества, которые подвергаются дегидрированию, т.е. отщеплению атомов
водорода.
• Водород |
Н2 - универсальное энергетическое |
|
|
|
используется в тканевом |
топливо, которое |
||
дыхании для образования энергии и воды. |
||
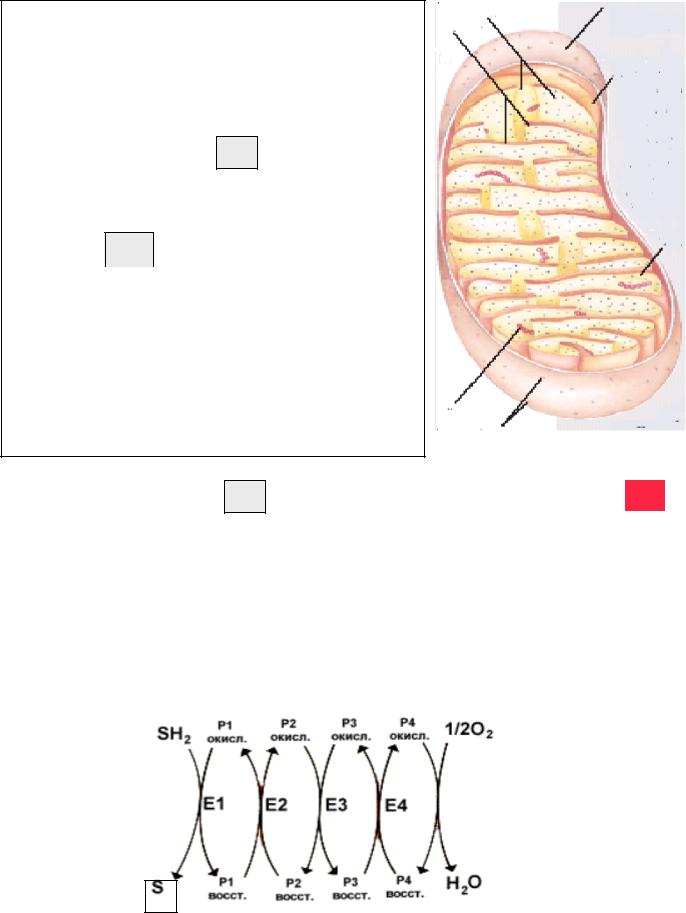
•Тканевое дыхание представлено
полиферментной цепью переноса электронов и протонов (ЦПЭ), которая называется
дыхательной митохондриальной цепью или
дыхательным ансамблем. Она имеет структурную организацию, т.к. ее компоненты встроены во
внутреннюю мембрану митохондрий (от 5 до 20 тыс. ансаблей в одной митохондрии).
АТФ-синтаза |
внешняя |
|
мембрана |
||
кристы |
внутренняя
мембрана
рибосомы протонные каналы
Промежуточные переносчики (Р) при транспорте электронов от исходного донора электронов (субстрата) SH2 к терминальному акцептору – кислороду О2
Полный процесс представляет собой цепь последовательных окислительно-
восстановительных реакций, в ходе которых происходит взаимодействие между переносчиками. Каждый промежуточный переносчик (P) вначале выступает в роли акцептора электронов и протонов и из окисленного состояния переходит в восстановленную форму. Затем он передает электрон следующему переносчику и снова возвращается в окисленное состояние. На последней стадии переносчик передает электроны кислороду, который затем, присоединяя протоны, восстанавливается до воды.
SH2 |
|
1/2О2 |
|
|
|
|
|
Н2О |
37 |
S |
|
||
|
|
|
|
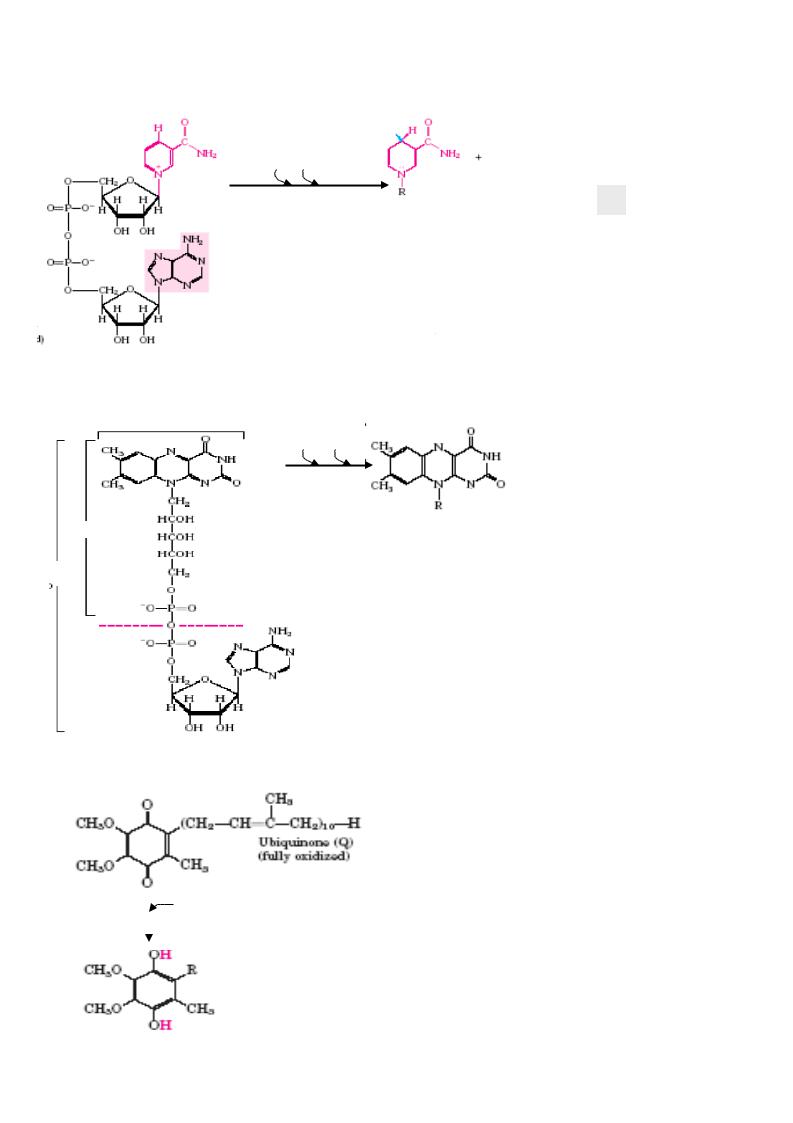
1. НАД-зависимые дегидрогеназы
Н
2Н+2е- ..
+ Н+
НАДН (восстановленная форма)
НАД+ (окисленная форма)
Сложные ферменты, которые катализирует реакции окисления непосредственно субстратов S (первичные
дегидрогеназы).
- (активная форма витамина РР) - кофермент этих ферментов, акцептируя два протона и два электрона ( 2Н
S превращается в восстановленную форму
НАДН.
2. Флавиновые дегидрогеназы или флавопротеины (ФП)
ФМН
ФАД
ФАД, (ФМН)
(окисленные)
2Н+2е- |
Н |
Сложные ферменты, |
|
|
|
простетическими группами |
|
|
|
которых является |
ФМН |
Нили ФАД (активные формы
ФАДН2 (ФМНН2) витамина В2).
(восстановленные)
Дегидрогеназы, содержащие ФАД, катализируют окисление некоторых субстратов, например, янтарной кислоты (сукцината), т.е. это первичные дегидрогеназы (сукцинатдегидрогеназа).
Дегидрогеназа, содержащая ФМН, акцептирует
протоны и электроны от восстановленных |
НАДН- |
коферментов НАДН, т.е. это |
|
дегидрогеназа. |
|
3. Убихинон - КоQ
|
|
|
КоQ |
|
|
|
|
(окисленный |
) |
|
|
2Н+2е- |
||
|
|
|||
|
|
|
||
|
|
|
||
|
ОН |
|||
38 |
|
|
КоQН2 |
|
|
|
восстановленный) |
||
ОН( |
||||
Небольшая молекула, растворимая в
липидной части мемебраны |
( |
благодаря |
неполярной боковой цепи |
), поэтому она |
|
легко перемещается в толще мембраны.
Название «убихинон» возникло из-за его повсеместной распространенности в
природе.
Кофермент Q является своеобразным коллектором протонов и электронов 2Н+2е-
от восстановленных коферментов ФМНН2 и
ФАДН2 переходя при этом в восстановленную форму КоQН2.
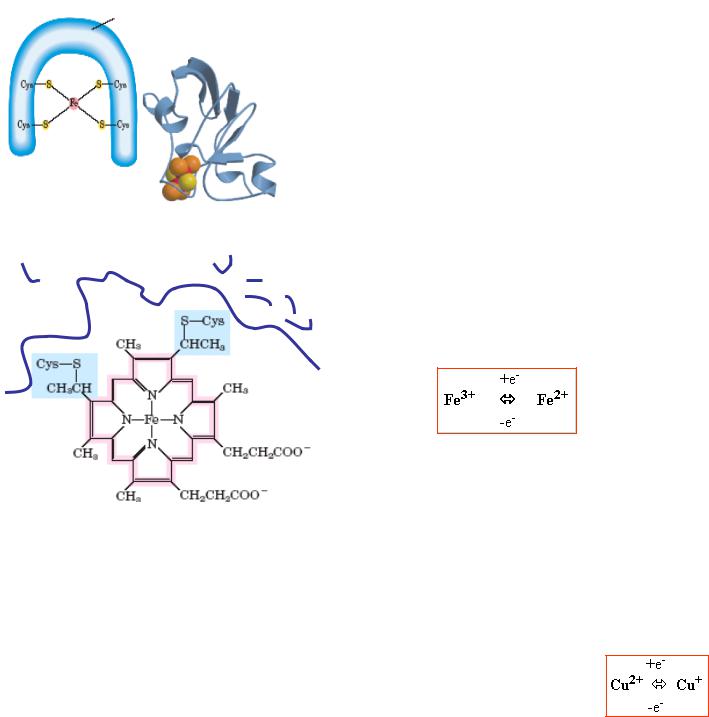
белок
белок
гем С
4. Железо-серные белки
Это сложные белки, содержащие негеминовое железо и серу, которые могут обратимо окисляться и восстанавливаться, т.е. переносить электроны. Расположены в липидном слое мембраны Эти окислительно-восстановительные системы
стабильны только в составе молекул белков. Они могут содержать от 2 до 6 ионов железа, образующих комплексы различного состава с неорганическим сульфидом и SH-группами остатков цистеина белка.
5. Цитохромы |
|
|
|
|
Это сложные белки |
– |
гемопротеины, |
|
|||
|
содержащие гем (подобные гему гемоглобина) - |
||
|
прочно связанную простетическую группу. Гем |
||
|
содержит геминовое |
железо, способное менять |
|
валентность, т.е. переносить только электроны.
Цитохромы отличаются друг от друга как белковым компонентом, так и заместителями в геме, следовательно, физико-химическими свойствами, т.е. окислительно-
восстановительными потенциалами.
В дыхательной цепи цитохромы служат переносчиками электронов и располагаются соответственно величине окислительно-восстановительного потенциала следующим образом: цит.b, цит.с1, цит.с, цит.а, а3.
Цитохром аа3 - цитохромоксидаза - терминальный фермент, который переносит электроны непосредственно на кислород (аэробный фермент), состоит из 6 субъединиц, кроме геминового железа содержит ионы меди, переносящий электроны. В переносе электронов участвуют сначала ионы железа цитохромов а и а3, а затем ион меди цитохрома а3.
V. Молекулярная организация цепи переноса электронов
Все участники цепи переноса электронов структурно объединены в четыре окислительно-восстановительные системы – мультиферментные комплексы (I - IV),
встроенные в липидный матрикс внутренних мембран митохондрий. |
2Н+2е- |
|
||
Процесс окисления начинается с переноса протонов и электронов |
с |
|||
окисляемого субстрата |
SH2 |
на НАД+ или ФАД (это зависит от природы субстрата). |
39 |
|
