
- •Поверхностные явления и адсорбция
- •Физический смысл поверхностного натяжения
- •Принцип минимума свободной энергии: в системах, обладающих избытком свободной энергии, могут самопроизвольно протекать
- •Адсорбция – процесс самопроизвольного изменения концентрации какого-либо вещества у поверхности раздела двух фаз
- •Адсорбция определяется природой поглощаемого вещества и поглотителя, ее величина зависит от температуры, давления
- •Теория мономолекулярной адсорбции Лэнгмюра
- •Типичная изотерма мономолекулярной адсорбции на твердой поверхности
- •Для адсорбции из растворов: Для адсорбции газов:
- •Уравнение Фрейндлиха
- •Изотерма адсорбции Фрейндлиха
- •Для экспериментального определения величины адсорбции на поверхности твердого тела используется уравнение:
- •Адсорбция на границе границе жидкость (раствор) – газ
- •Для разбавленных растворов активность равна концентрации, и уравнение
- •Зависимость поверхностного натяжения от концентрации вещества
- •Правило Дюкло-Траубе — поверхностная активность ПАВ одного и того же гомологического ряда в
- •Дисперсные системы
- •по агрегатному состоянию
- •По степени взаимодействия частиц дисперсной фазы (ДФ)
- •Методы получения лиофобных коллоидных систем
- •Условия для образования коллоидных растворов химическим методом
- •Химическая конденсация
- •Пептизация –заключающийся в
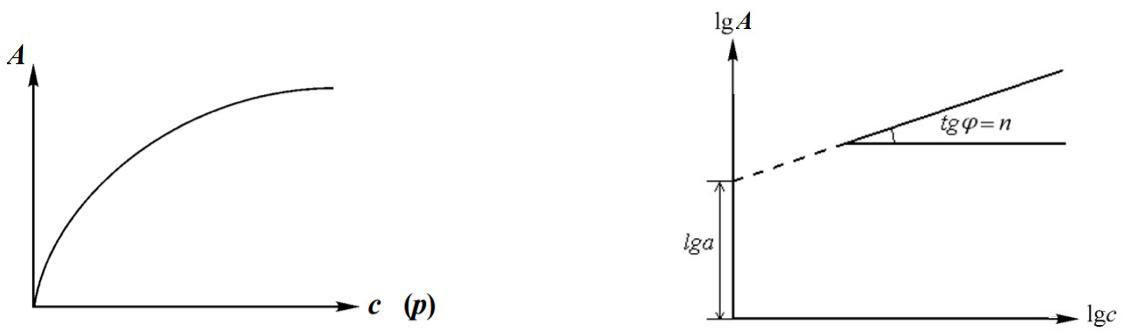
Изотерма адсорбции Фрейндлиха |
Линеаризованное уравнение |
|
Фрейндлиха |
А a Cn |
lg А lg a n lg C |

Для экспериментального определения величины адсорбции на поверхности твердого тела используется уравнение:
A C0 Cравн V m
с0 — исходная концентрация вещества; сравн — равновесная концентрация,
установившаяся после определенного по времени контакта адсорбента с раствором (газовой смесью); V — объем раствора (газовой смеси); m — масса адсорбента. Размерность [ɑ] = [моль/г].

Адсорбция на границе границе жидкость (раствор) – газ
(гиббсовская адсорбция)
Особенность границы раздела жидкой и газообразной фаз
на границе раздела фаз нет активных центров, поверхность жид-кости гладкая;
силы взаимодействия со стороны жидкой и газообразной фаз не одинаковы, поэтому силовым полем со стороны газообразной фазы можно пренебречь;
молекулы адсорбата свободно перемещаются по поверхности ад-сорбента
(жидкости).
Фундаментальное уравнение Гиббса
a d Гi RTi dai
Г – избыточное количество адсорбата в поверхностном слое по сравнению с объемной фазой (моль/м2), ai – активность i-го
компонента в состоянии равновесия, Т – температура (К),
R – универсальная газовая постоянная, dσ – бесконечно малое изменение поверхностного натяжения при бесконечно малом изменении равновесной активности (dai).

Для разбавленных растворов активность равна концентрации, и уравнение
принимает вид: C d Гi RTi dCi
В упрощенном виде, когда речь идет о конечном интервале концентраций, данное уравнение можно записать следующим образом:
Гi Cср 2 1
RT C2 С1
Вещества, для которых Г>0, снижают поверхностное натяжение и называются поверхностно-активными веществами (ПАВ).
Вещества, для которых Г<0, повышают поверхностное натяжение и называются поверхностно-инактивными веществами (ПИВ).
Вещества, не влияющие на поверхностное натяжение (Г=0), называют поверхностно- неактивными (ПНАВ).
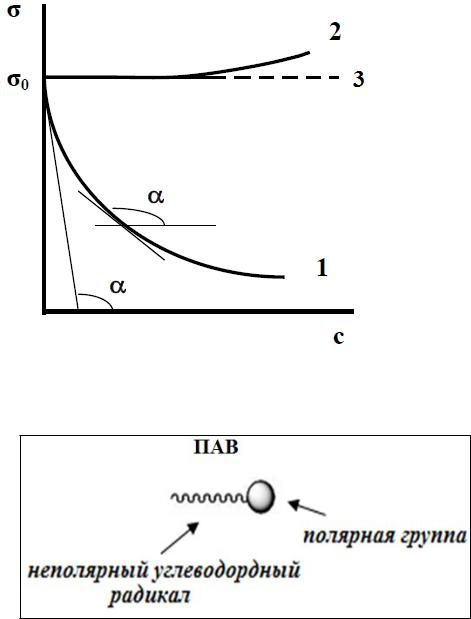
Зависимость поверхностного натяжения от концентрации вещества
1 |
– поверхностно-активное вещество (ПАВ) |
Г 0 |
2 |
– поверхностно-инактивное вещество (ПИВ) |
Г 0 |
3 |
– поверхностно-неактивное вещество (ПНАВ) |
|
Поверхностная активность (только для ПАВ)
d |
-tgα=g |
|
g lim |
|
|
|
dC C 0 |
|
Характеризует способность ПАВ накапливаться в поверхностном слое, снижая поверхностное натяжение. Размерность [g] = [Дж·м·моль–1] = [Н·м2·моль–1].
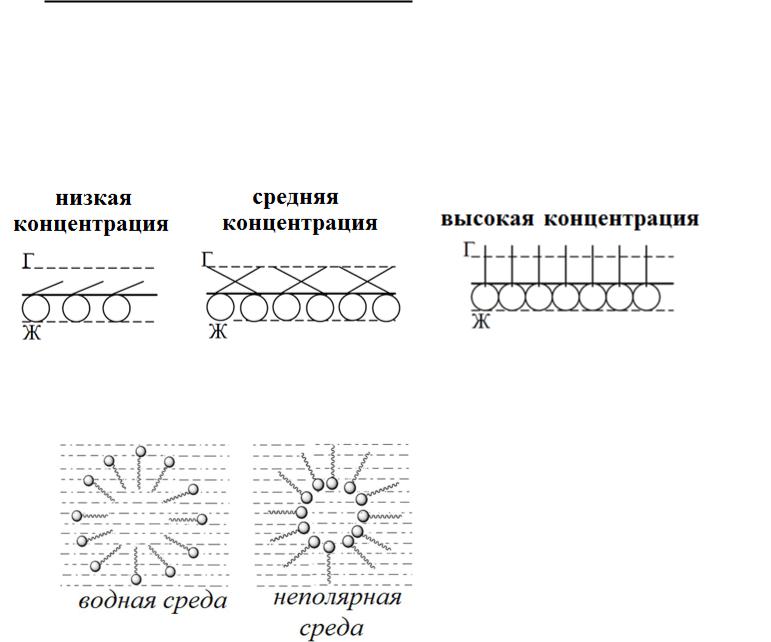
Правило Дюкло-Траубе — поверхностная активность ПАВ одного и того же гомологического ряда в водном растворе возрастает в среднем в 3,2 раза при увеличении цепи на одну группу -СН2-.
Строение поверхностного слоя при адсорбции ПАВ на границе вода – воздух
Когда все места на поверхности заполнены образуется насыщенный адсорбционный слой, который представляет собой молекулярную пленку адсорбированного вещества.
Дисперсные системы
•Дисперсной называется двух- или многофазная, т.е. гетерогенная система, в которой, по крайней мере, одна из фаз представлена очень маленькими частицами, размеры которых тем не менее заметно превосходят молекулярные.
•Частицы раздробленного вещества при этом называются дисперсной фазой (ДФ), а гомогенная фаза, в которой они распределены (растворитель), представляет собой
дисперсионную среду (ДС).
Классификация дисперсных систем
по степени дисперсности
грубодисперсные – частицы с радиусом больше 10-7 м, не обладают осмотическим давлением, не фильтруются через бумажные фильтры и являются неустойчивыми
коллоидно-дисперсные – частицы с радиусом от 10-9 до 10-7 м, частицы находятся в непрерывном хаотическом движении, вследствие чего обладают кинетической устойчивостью, осмотическим давлением, и способностью к диффузии.
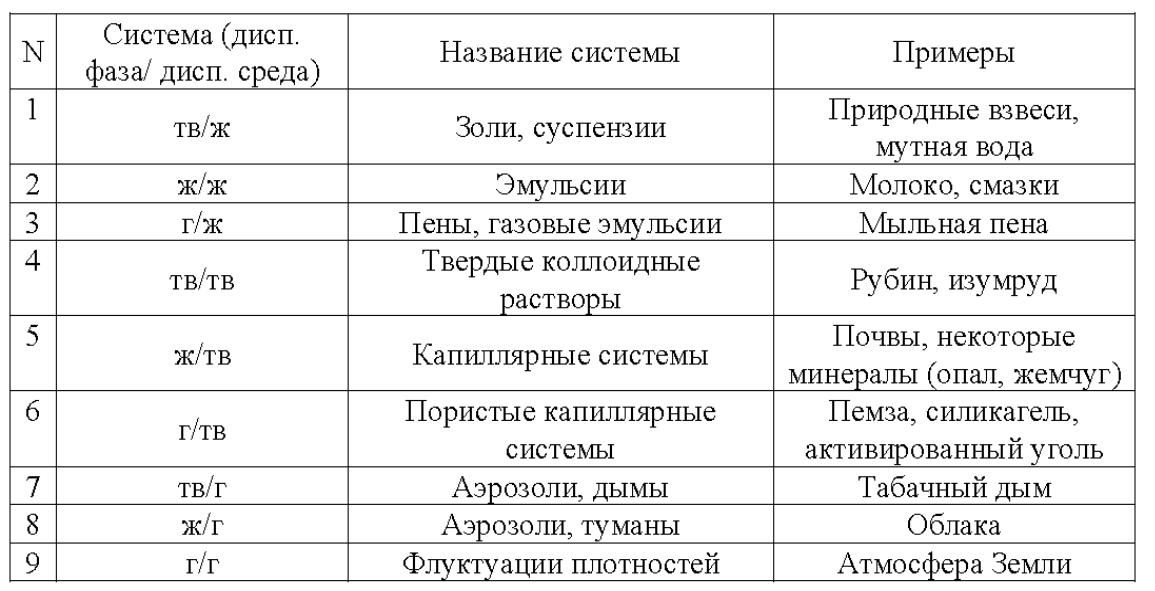
по агрегатному состоянию
По степени взаимодействия частиц дисперсной фазы (ДФ)
свободнодисперсные – частицы ДФ не связаны между собой и могут свободно перемещаться (аэрозоли, разбавленные суспензии и эмульсии, лиозоли).
связнодисперсные – одна из фаз структурна закреплена и не может перемещаться свободно (капиллярно-пористые тела, твердые растворы, гели и студни, пены).
По степени взаимодействия частиц дисперсной фазы (ДФ)
лиофильные - термодинамически устойчивые системы, образующиеся при самопроизвольном диспергировании одной из фаз (растворы мыл и др. ПАВ)
лиофобные - термодинамически неустойчивые, что связано с большим запасом свободной поверхностной энергии на развитой межфазной поверхности раздела, получение их требует затраты внешней энергии
Методы получения лиофобных коллоидных систем
•Методы диспергирования основаны на раздроблении твердых тел до частиц коллоидного размера и образовании таким образом коллоидных растворов: механическое дробление, дробление ультразвуком, электрический метод.
•Методы конденсации - объединение молекул и ионов в истинных растворах в более крупные коллоидные частицы
физические методы метод замены растворителя метод конденсации паров
химические методы основаны на проведении химических реакций, сопровождающихся образованием нерастворимых или малорастворимых веществ
реакции восстановления (Ag2O+H2 → 2Ag↓ +H2O) реакции окисления (2H2S + SO2 → 3S↓ + 2Н2О)
реакции обмена (СuСl2+ Na2S → CuS↓ + 2NaCl) реакции гидролиза (FеСl3 +ЗН2O → Fe(OH)3↓ +3HCI)
• Метод пептизации
