
- •Введение
- •Лабораторная работа 1. Отбор проб пищевых продуктов, сельскохозяйственного сырья, кормов и почвы
- •Лабораторная работа 2. Подготовка проб для определения стронция-90 и цезия-137 радиохимическими методами
- •Лабораторная работа 3. Приготовление титрованных растворов носителей для радиохимического анализа
- •Задание 1. Приготовление титрованного раствора стабильного стронция и определение титра по сульфату стронция
- •Задание 2. Приготовление титрованного раствора иттрия и определение титра по оксалату иттрия
- •Задание 3. Приготовление титрованного раствора стабильного цезия и определение его титра
- •1. Определение титра раствора по сурьмяно-йодиду цезия
- •2. Определение титра раствора по висмут-иодиду цезия
- •Лабораторная работа 4. Определение содержания стронция-90 в почВе
- •Задание 1. Выделение и концентрирование стронция-90
- •Задание 2. Выделение иттрия-90 и определение активности стронция-90 (по иттрию-90)
- •Лабораторная работа 5. Радиометрический анализ выделенных препаратов
- •Энергии бета-спектра
- •Лабораторная работа 6. Определение химического выхода носителей Задание 1. Определение химического выхода носителя иттрия
- •Стронция
- •Лабораторная работа 7. Идентификация и проверка радиохимической чистоты
- •Лабораторная работа 8. Расчет содержания стронция-90 в пробе
- •Лабораторная работа 9. Определения содержания стронция-90 в пищевых продуктах, сельскохозяйственном сырье и кормах оксалатным методом
- •Задание 1. Определение концентрации цезия-137 в пищевых продуктах, сельскохозяйственном сырье и кормах
- •Задание 2. Определение концентрации цезия-137 в почвах
- •Контрольные вопросы
- •Инструкция по технике безопасности при работе в радиохимической лаборатории
Лабораторная работа 6. Определение химического выхода носителей Задание 1. Определение химического выхода носителя иттрия
Краткие теоретические сведения. Химический выход иттрия в долях единицы определяется отношением массы осадка (мг) оксалата иттрия на подложке после высушивания (лабораторная работа 4, задание 2, п.10) к массе внесенного хлорида или нитрата иттрия в составе титрованного раствора в пересчете на оксалат иттрия (лабораторная работа №4, задание 1, п.12) по формуле:
![]() ,
,
где m2 – масса подложки с осадком, мг;
m1 – масса подложки без осадка, мг;
М – масса введенного в пробу носителя, мг.
Пример расчета. В подкисленный НС1 и приготовленный для накопления итттрия-90 фильтрат, было внесено 50 мг иттрия в пересчете на оксалат виде титрованного раствора (2 см3 с содержанием иттрия 25 мг в 1 см3 в расчете на оксалат иттрия). Масса осадка оксалата иттрия без подложки после высушивания и взвешивания оказалась равной 22 мг. Отсюда химический выход (Х.В.) иттрия в долях единицы составляет:
![]() .
.
Химический выход радиоактивного изотопа иттрия (иттрий-90) соответствует химическому выходу стабильного иттрия, вводимого в составе титрованного раствора (0,44).
Выполнение работы:
1. Рассчитать химический выход носителя иттрия, используя данные о титре раствора иттрия (лабораторная работа 3, задание 2, п.10), объеме использованного носителя (лабораторная работа 4, задание 1, п.12) и результаты, полученные в лабораторной работе №4, п.22.
Задание 2. Определение химического выхода носителя
Стронция
Краткие теоретические сведения. Химический выход стронция в долях единицы определяется по формуле:
![]() ,
,
где, Мкон. – масса стабильного стронция, содержащегося в растворе после выделения и концентрирования, мг (лабораторная работа 4, задание 2, п.2);
Мнач. – масса стронция в исходной вытяжке, мг. Она равна сумме массы природного стронция в почве и массы внесенного носителя (Мнач. = Мприр. + Мносит.).
Для расчета этих масс необходимо определить концентрацию стабильного стронция в соответствующих растворах. Ее определяют на пламенном фотометре (ПАЖ-1 или ПАЖ-2) с помощью литиевого светофильтра, пропускающего свет с длиной волны 670,8 нм (можно также определять атомно-абсорбционным методом на приборе AAS-IN). В основу фотометрического анализа положено изменение интенсивности окрашивания пламени в зависимости от концентрации химического элемента, распыляемого с помощью эжектора непосредственно в пламя газовой горелки прибора. Наиболее простым инструментом для этих целей служит пламенный фотометр.
В возбужденном состоянии (за счет температуры пламени) атомы каждого элемента излучают характерный, присущий только этому элементу свет, укладывающийся в диапазон длин волн видимого спектра. Если на пути светового потока поставить светофильтр, тем самым, выделив пучок света с определенной длиной волны, то на чувствительном элементе прибора возникает импульс тока, величина которого будет пропорциональная интенсивности данного светового луча. Ток фотоэлемента, преобразованный и усиленный в приборе, вызовет отклонение стрелки на шкале микроамперметра.
Стронций определяют по атомно-резонансной полосе поглощения с длиной волны 460,7 нм или по молекулярной полосе 670 нм. На пламенных фотометрах, стронций, как правило, определяют с помощью литиевого светофильтра, пропускающего свет с длиной волны 670,8 нм.
Прибор для определения концентрации стронция в растворах с помощью фотоэффекта, как правило, имеют очень высокую чувствительность и избирательность, поэтому определение химического выхода стабильного стронция в данном радиохимическом анализе рекомендуется выполнять методом фотометрии пламени.
Для того чтобы узнать концентрацию искомого элемента в растворе, нужно предварительно проградуировать шкалу прибора путем измерения заранее приготовленной серии растворов с известной концентрацией этого элемента. Для этого составляют серию растворов сравнения из ceми (или пяти) концентраций исследуемого элемента и фотометрируют на приборе. По данным измерений строится градуировочный график. После этого, при тех же установочных параметрах, определяют число делений шкалы прибора, на которое отклонится стрелка прибора пpи фотометрировании раствора с неизвестной концентрацией этого же элемента. Затем по градуировочному графику определяют искомую концентрацию. Внешний вид и органы управления пламенного фотометра ПАЖ-1 приведены на рисунке 1.
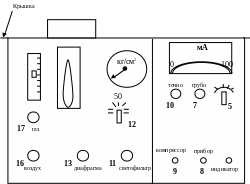
Рис.1. Анализатор жидкостной пламенно-фотометрический ПАЖ-1
Порядок работы:
1. Подготовить прибор к работе в следующей последовательности:
- проверить положение тумблеров 8 и 9 (прибор и компрессор), они должны быть выключены;
- подсоединить прибор к сети и включить тумблеры 8 и 9;
- ручку 16 (воздух) повернуть до упора направо (оптимальное давление 0,4 кг/см2);
- проверить, засасывается ли через капилляр дистиллированная вода из стаканчика;
- снять верхнюю крышку прибора. Установить светофильтр номер 4 напротив горелки;
- ручку 17 (газ) поставить на максимальный расход, поджечь газ (спичками). Уменьшить расход до 45 единиц (по шкале с поплавком);
- закрыть крышку прибора. Прогнать чистую воду примерно 30 мин.
Выполнение работы:
1. Фильтрат, полученный в лабораторной работе 4 (задание 2, п.14), подкисляют соляной кислотой до рН 3-4, переносят в мерную колбу емкостью 100 см3 и доводят дистиллированной водой до метки, тщательно перемешивают (первое разведение 1:100), отбирают пипеткой 1 см3, переносят в другую мерную колбу на 50 см3 и разбавляют водой до метки (второе разведение 1:50) т.е. число разведений в данной методике равно 5000 (100×50). Для определения количества носителя стронция в фильтрате (лабораторная работа №4, задание 2, п. 14) необходимо знать число разведений носителя стронция и концентрацию (мг/ см3) носителя в растворе после разведений. Определение числа разведений носителя стронция покажем на примере.
Пример расчета. Условно примем, что в мерной колбе на 50 см3 после внесения туда фильтрата, подкисления соляной кислотой и доведения дистиллированной водой до метки содержится 160 мг металлического стронция или его концентрация будет составлять 3,2 мг/ см3 (160 мг:50 см3=3,2 мг/ см3). При внесении 1 см3 этого раствора в колбу на 50 мл и доведении дистиллированной водой до метки концентрация носителя стронция снизится до 0,064 мг/ см3 (3,2 мг : 50 см3 = 0,064 мг/ см3). Таким образом, в примере число разведений носителя стронция составляет 2500 раз (160:0,064=2500 или 50×50= 2500).
2. Приготовить растворы для градуировки прибора. Для этого в диапазоне концентраций растворов, от максимально ожидаемой с учетом разбавлений до минимально обнаруживаемой прибором (0,005 мг/ см3), составляется серия растворов сравнения.
При определении химического выхода стронция на пламенном фотометре необходимо, прежде всего, знать, какое количество стабильного стронция было внесено в приготовленные к экстрагированию пробы в начальной стадии анализа в виде титрованных растворов.
Пример расчета. В приготовленную навеску почвы (100 г) внесли 5 см3 титрованного раствора стронция с титром 50 мг/см3 (всего 250 мг). Естественная концентрация стабильного стронция в почве в среднем составляет 10-3 %, что соответствует примерно 1,3 мг в пересчете на первоначальную влажность в 100 г навески почвы взятой для анализа. Фактическое среднее содержание стабильного стронция в растворах после экстрагирования контрольных образцов почвы (стаканы №3 и 4), установленное по результатам фотометрирования, составило 2,06 мг. (Оно определяется умножением значений концентрации стронция, установленной при фотометрировании растворов после экстрагирования кислотами в стаканах номер 3 и 4, на их объемы в мл, суммированием и определением среднего значения). Суммарное содержание стабильного стронция в пробе почвы в начальной стадии анализа, таким образом, будет составлять 252,06 мг (250+2,06). Следовательно, при 100%-ном химическом выходе максимально ожидаемая концентрация стронция в объеме раствора, взятого для фотометрирования с учетом разбавления, будет составлять:
СSr макс = 252,06 мг : 2500 = 0,101 = 0,1 мг/ см3,
где 2500 – число разбавлений.
Для приготовления 500 см3 исходного рабочего раствора указанной концентрации используемого для приготовления серии растворов сравнения (семь или пять) необходимо в колбу вместимостью 500 см3 внести 2,0 см3 титрованного раствора стронция (25 мг/ см3) и довести объем раствора дистиллированной водой до метки [(2,0 см3×25 мг/ см3):500 см3 = 0,1 мг/ см3]. Используя этот рабочий раствор, готовят серию растворов сравнения для градуировки прибора. Для этого в семь мерных колб (допускается и пять) вместимостью 100 см3 бюреткой вносят количества исходного раствора в соответствии с таблицей 2:
Таблица 2. Объемы исходного рабочего раствора для приготовления растворов сравнения
Показатели |
№ колб |
||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Объем исходного рабочего раствора хлористого стронция, см3 |
100
|
80
|
60
|
40
|
20
|
10
|
5
|
Концентрация стронция в растворе, мг/см3 |
0,1 |
0,08 |
0,06 |
0,04 |
0,02 |
0,01 |
0,004 0,0040 0,005 |
Объемы растворов в колбах доводят до метки раствором 2 н. HCl и тщательно перемешивают.
3. Подготовить анализатор жидкостной пламенно-фотометрический к работе в следующей последовательности:
- проверить положение тумблеров 8 и 9 (прибор и компрессор), они должны быть выключены;
- подсоединить прибор к сети и включить тумблеры 8 и 9;
- ручку 16 (воздух) повернуть до упора направо (оптимальное давление 0,4 кг/см2);
- проверить, засасывается ли через капилляр дистиллированная вода из стаканчика;
- снять верхнюю крышку прибора. Установить светофильтр номер 4 напротив горелки;
- ручку 17 (газ) поставить на максимальный расход, поджечь газ (спичками). Уменьшить расход до 45 единиц (по шкале с поплавком);
- закрыть крышку прибора. Прогнать чистую воду примерно 30 мин;
- ручкой 13 установить диафрагму в среднее положение – 2. Ручка 12 ирисовой диафрагмы должна быть установлена на 50.
4. Провести измерения, для этого:
- ручкой 5 установить диапазон 10;
- погрузить капилляр в стакан с чистой дистиллированной водой и ручками 7 (грубо) и 10 (точно) установить «нуль» на шкале;
- погрузить капилляр в стакан с максимальной концентрацией раствора (если стрелка зашкаливает, ручкой 5 изменить диапазон чувствительности). После выбора диапазона чувствительности шкалу можно расширить до «100», повернув ручку 12 ирисовой шкалы;
- проверить «нуль» по чистой воде и «100» по раствору с максимальной концентрацией;
- фотометрировать серию стандартных растворов, погружая сначала капилляр в чистую воду, а затем в соответствующий раствор;
- таким же образом фотометрировать исследуемые растворы. Записывать показания прибора в зависимости от номера пробы в рабочую тетрадь (число делений на шкале микроамперметра)
5. Выключить прибор.
Перед выключением прибора прогнать в течение 30 мин чистую дистиллированную воду. Затем:
- выключить газ ручкой 17 и перекрыть магистральный кран;
- ручки 8 и 9 поставить в положение «выкл.»;
- выключить прибор из розетки.
6. По полученным результатам построить градуировочный график в координатах: деления шкалы прибора от 0 до 100 – концентрация стронция от 0 до 0,1 мг/см3. Из градуировочного графика определяют цену деления (ЦД) шкалы прибора:
![]() ,
мг/см3/дел,
,
мг/см3/дел,
где Сi–концентрация стронция в каждом растворе из серии, мг/см3;
ai – показания прибора при фотометрировании каждого из растворов серии, деления;
n – число растворов в градуировочной серии.
Пример расчета. При фотометрировании серии растворов сравнения с концентрациями, указанными в таблице 2 стрелка микроамперметра прибора отклонялась при измерении раствора №1 на 100 делений, №2-78, №3-60, №4-37,5, №5-20, №6-11, №7-5,5 делений. Тогда цена деления прибора будет равна 0,00101(1,01×10-3) мг/см3/дел. [(0,1+0,08+0,06+0,04+0,02+0,01+0,005):(100+78+60+37,5+20+11+5,5) = 0,00101].
Концентрация стронция в каждом из исследуемых растворов определяется умножением цены деления на число делений, на которое отклонилась стрелка при фотометрировании данного раствора. При измерении раствора с неизвестной концентрацией (лабораторная работа №4, задание 2, п.14) стрелка прибора отклонилась на 84 деления. Тогда концентрация стронция в растворе, взятом на фотометрирование, равна 0,085 мг/см3 (0,00101 мг//дел×84 дел=0,085 мг/ см3). Учитывая разведение в данном примере (2500) можно найти общее количество стронция в анализируемой пробе, обнаруженное с помощью пламенного фотометра: 0,085×2500 = 212,5 мг.
Химический выход (Х.В.) стронция в долях единицы определяется по отношению найденного количества стронция к внесенному в начале анализа:
![]()
Определить концентрацию стронция можно также с помощью градуировочного графика. При измерении семи растворов сравнения с концентрациями в порядке убывания соответственно 0,1, 0,08, 0,06, 0,04, 0,02, 0,01 и 0,005 мг/см3 стрелка микроамперметра отклонялась соответственно на 100, 78, 60, 37,5 20, 11, 5,5 делений. По данным измерений строится градуировочный график в координатах: ось ординат (вертикальная) – деления шкалы прибора от 0 до 100, ось абсцисс (горизонтальная) – концентрация стронция от 0 до 0,1 мг/ см3. Через полученные точки проводят прямую, экстраполяция которой на ось абсцисс дает искомую концентрацию. Градуировочный график по результатам фотометрирования растворов сравнения приведен на рис. 2 (прилож.3). Отклонение стрелки микроамперметра фотометра на 84 деления при фотометрировании раствора неизвестной концентрации стронция соответствует его концентрации установленной с помощью калибровочного графика равной 0,085 мг/см3 раствора. На оси ординат находят значение, соответствующее отклонению стрелки микроамперметра на шкале прибора при фотометрировании раствора (84 деления). С этой точки проводят горизонтальную прямую до пересечения с наклонной графика. Из точки пересечения на ось абсцисс опускается вертикальная прямая. Место пересечения вертикальной прямой и оси абсцисс дает искомое значение концентрации стронция в испытуемом растворе численно равное 0,085 мг/см3 (рис. 2, приложение 3). Цена деления составляет 0,001 мг/см3 (0,01 мг/см3 : 10 дел. = 0,001 мг/ см3/дел).
Если вносится титрованный раствор стронция в пробы исследуемых образцов не 5 см3, а другое количество миллилитров и титр раствора носителя стронция равен не 50 мг/см3, а другой, то в этом случае делается перерасчет.
Пример расчета. При измерении концентрации стронция в растворах стаканов №3 и 4 (260 и 265 см3) стрелка амперметра на приборе отклонялась соответственно на 7,5 и 8 делений. Цена деления прибора предварительно установленная при фотометрировании серии растворов сравнения в нашем примере составляла 0,00101 мг/см3/дел. Тогда количество стабильного стронция в стаканах №3 и 4 соответственно составляло 1,97 и 2,14 мг (7,5×0,00101×260=1,97 и 8×0,00101×265=2,14). Содержание стабильного стронция в растворе в среднем составляло 2,06 мг [(1,97+2,14):2=2,06 мг]. Аналогичные результаты дает определение концентрации стронция в растворах стаканов №3 и №4 установленное с помощью калибровочного графика (рис.3, прилож.1).
