
Билет№26 Кровотечения во время беременности
Кровотечения в акушерской практике, связанные с беременностью
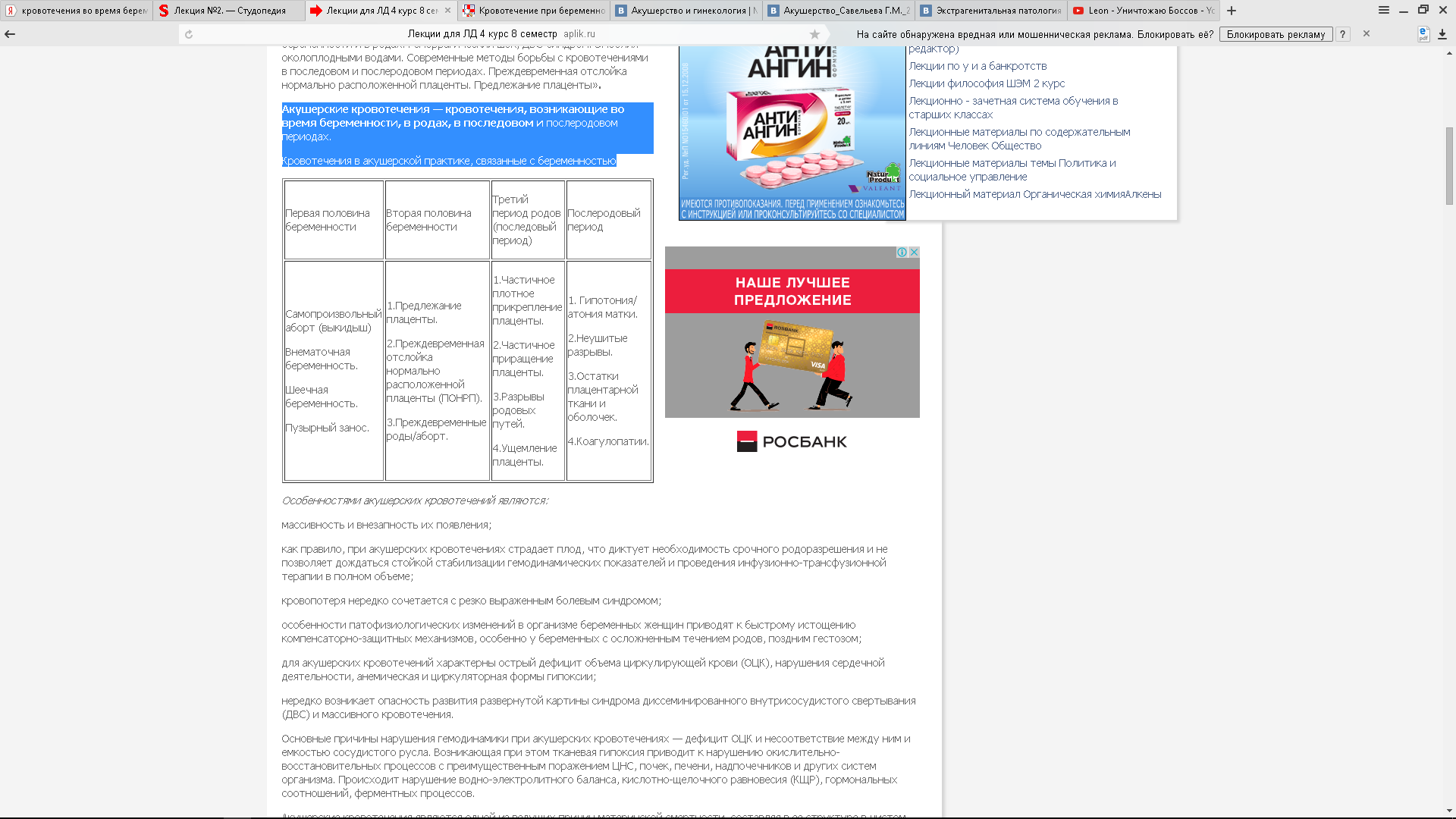
Особенностями акушерских кровотечений являются:
массивность и внезапность их появления;
как правило, при акушерских кровотечениях страдает плод, что диктует необходимость срочного родоразрешения и не позволяет дождаться стойкой стабилизации гемодинамических показателей и проведения инфузионно-трансфузионной терапии в полном объеме;
кровопотеря нередко сочетается с резко выраженным болевым синдромом;
особенности патофизиологических изменений в организме беременных женщин приводят к быстрому истощению компенсаторно-защитных механизмов, особенно у беременных с осложненным течением родов, поздним гестозом;
для акушерских кровотечений характерны острый дефицит объема циркулирующей крови (ОЦК), нарушения сердечной деятельности, анемическая и циркуляторная формы гипоксии;
нередко возникает опасность развития развернутой картины синдрома диссеминированного внутрисосудистого свертывания (ДВС) и массивного кровотечения.
Основные причины нарушения гемодинамики при акушерских кровотечениях — дефицит ОЦК и несоответствие между ним и емкостью сосудистого русла. Возникающая при этом тканевая гипоксия приводит к нарушению окислительно-восстановительных процессов с преимущественным поражением ЦНС, почек, печени, надпочечников и других систем организма. Происходит нарушение водно-электролитного баланса, кислотно-щелочного равновесия (КЩР), гормональных соотношений, ферментных процессов.
Акушерские кровотечения являются одной из ведущих причин материнской смертности, составляя в ее структуре в чистом виде — 20–25%, как конкурирующая причина — 42%, а как фоновая — до 78% случаев. Показатель акушерских кровотечений колеблется от 3 до 8% по отношению к общему числу родов, при этом 2–4% акушерских кровотечений связаны с гипотонией матки в последовом и раннем послеродовом периоде, около 1% случаев возникают при преждевременной отслойке нормально расположенной плаценты и предлежании плаценты.
Возможными причинами кровотечения в акушерской практике являются: прерывание беременности всех сроков, предлежание плаценты, преждевременная отслойка нормально расположенной плаценты, разрыв матки, разрыв мягких родовых путей в родах, гипо- и атонические кровотечения в раннем послеродовом периоде (см таблицу).
Наследственные или приобретенные дефекты системы гемостаза могут явиться причиной кровотечения как во время беременности, так и в родах или в послеродовом периоде.
Кровотечения могут быть и по таким причинам, как псевдоэрозия, полипы и рак шейки матки, травма половых органов, варикозные узлы во влагалище и др., но они встречаются редко.
Группа риска беременных по кровотечению
Важным мероприятием в профилактике кровотечений является формирование групп риска по возникновению этой патологии во время беременности, родов и в послеродовом периоде. В эти группы включаются беременные женщины:
с заболеваниями почек, печени, эндокринных желез, кроветворения, сердечно-сосудистой системы и нарушением жирового обмена.
в анамнезе которых имели место бесплодие любой этиологии, гипофункция яичников, признаки общего и генитального инфантилизма, нарушение менструальной функции, аборты, осложненные роды, воспалительные заболевания женских половых органов.
у которых во время данной беременности отмечались хронические и острые инфекции, паразитарные и аллергические заболевания, миома матки, узкий таз, многоводие, многоплодие, крупный плод, неправильное положение плода, поздний гестоз, анемия, перенашивание беременности.
Должно проводится своевременное обследование, консультация смежных специалистов и лечение беременных перечисленных групп риска.
Самопроизвольный аборт (дополнительный материал)
Среди причин маточных кровотечений, связанных с беременностью, одно из первых мест занимает самопроизвольный аборт — прерывание беременности в первые 22 нед. Его причинами могут быть различные патологические состояния организма женщины.
Среди анатомических факторов следует выделить инфантилизм, нарушение развития матки, истмико-цервикальную недостаточность, травматические повреждения матки при искусственном аборте или родах, опухоли.
К функциональным факторам относятся инфекционные заболевания, перенесенные в детстве, искусственные аборты, воспалительные заболевания половых органов, нарушение функционального состояния желез внутренней секреции, патологические роды в анамнезе, экстрагенитальная патология.
Помимо этого, причинами самопроизвольного аборта могут стать нарушения системы мать–плацента–плод и хромосомные нарушения.
Особенностями неотложного состояния при самопроизвольном аборте являются:
боли в нижних отделах живота;
кровянистые выделения, которые могут принимать характер кровотечения;
повышение тонуса матки;
наличие структурных изменений в шейке матки, в результате чего происходит раскрытие маточного зева и изгнание плодного яйца (целиком или частично).
Основные направления терапии зависят от стадии самопроизвольного аборта: угрожающий аборт, начавшийся, аборт в ходу, неполный или полный самопроизвольный аборт.
Беременные с любой клинической формой прерывания беременности должны лечиться в стационаре.
В случае угрожающего и начавшегося (при незначительном кровотечении) аборта — постельный режим; средства, способствующие снижению сократительной активности матки (метацин, партусистен, гинипрал, фенотерол, магния сульфат — кормагнезин, магния сульфат), и гормональная терапия по показаниям (дюфастон или утрожестан, дексаметазон или метипред). Лечение проводится под динамическим контролем УЗИ.
При аборте в ходу и неполном аборте — выскабливание матки; при массивном кровотечении — гемотрансфузия.
Лечебно-тактические мероприятия при самопроизвольном аборте на догоспитальном этапе:
Оценка общего состояния беременной, степени анемизации, геморрагического шока по индексу Альговера (шоковый индекс) и кровопотери.
Выяснение срока беременности и акушерской ситуации.
Экстренная доставка беременной с самопроизвольным абортом в гинекологическое отделение (доставка больных в стационар производится в горизонтальном положении).
Неотложная помощь беременным с выкидышем и значительной кровопотерей на догоспитальном этапе сводится к лечению геморрагического шока. Для лечения гиповолемического шока необходимо ввести: полиоксидин 400 мл, или волекам 400 мл, или полиглюкин 400 мл; затем 400 мл реополиглюкина и 400 мл желатиноля. Скорость внутривенного введения растворов — вначале 20 мл/мин, затем — дробно по 100–150 мл под контролем состояния легких и величины АД. Одновременно проводят и другие мероприятия по борьбе с геморрагическим шоком. Инфузионная терапия осуществляется до момента поступления в стационар. При наличии полного аборта вводят сокращающие матку средства: 1 мл окситоцина внутривенно струйно с 10 мл изотонического раствора хлористого натрия или 1 мл метилэргометрина (метилэргобревин) внутривенно струйно.
Внематочная (эктопическая) беременность (дополнительный материал) — беременность, при которой оплодотворенная яйцеклетка развивается вне полости матки.
По локализации — внематочная беременность может быть в маточной трубе, яичнике, шейке матки, в рудиментарном роге при однорогой матке, в брюшной полости. По клиническому течению — прогрессирующая и нарушенная в случае разрыва плодовместилища наружного (разрыв трубы, яичника) или внутреннего (трубный аборт).
Факторами риска развития эктопической беременности являются: перенесенные ранее аднексит, эндомиометрит, аборты; нарушение гормональной функции яичников; генитальный инфантилизм; эндометриоз; перенесенные операции на внутренних половых органах.
Ведущий симптом — мажущие кровянистые выделения тёмного цвета из половых путей на фоне задержки менструации, боли внизу живота или признаки острого живота.
Дифференциальная диагностика: эктопическая беременность; полипы, новообразования, воспалительные процессы в шейке матки (причину выявляют при гинекологическом исследовании — осмотр при помощи зеркал); трофобластическая болезнь — диагноз уточняют при УЗИ (в полости матки разрастания, напоминающие гроздья винограда); дисменорея.
Лечебно-тактические мероприятия при нарушенной внематочной беременности:
оценка общего состояния больной и степени кровопотери;
уточнение гинекологического и акушерского анамнеза;
срочная госпитализация в гинекологическое отделение; транспортировку осуществляют в горизонтальном положении с опущенным головным концом. При транспортировке следует добиваться поддержания артериального давления на уровне 80–100 мм рт. ст. При массивной кровопотере госпитализация осуществляется реанимационно-хирургической бригадой.
Неотложная терапия на догоспитальном этапе включает инфузионную терапию: внутривенное введение 400 мл полиоксидина или 400 мл декстрана (декстрана, полиглюкина, реополидекса), внутривенно введение 500 мл 5% раствора глюкозы и 3 мл 5% раствора аскорбиновой кислоты. Терапия глюкокортикоидами и ингаляция кислорода по показаниям.
ПРЕДЛЕЖАНИЕ ПЛАЦЕНТЫ. ПРЕЖДЕВРЕМЕННАЯ ОТСЛОЙКА НОРМАЛЬНО РАСПОЛОЖЕННОЙ ПЛАЦЕНТЫ
Частота предлежания плаценты по отношению к общему числу родов колеблется от 0,2 % до 0,9 % и не имеет тенденции к снижению, что объясняется возрастанием числа абортов и внутриматочных вмешательств. Особую опасность возникновения массивных акушерских кровотечений представляет острая преждевременная отслойка нормально расположенной плаценты. Хотя ее частота не превышает 0,4–1,4 % по отношению ко всем беременным, однако в 30 % случаев она является причиной кровотечений, приводящих к летальному исходу.
Предлежание плаценты
Предлежание плаценты – неправильное прикрепление ее в матке, когда она расположена в области нижнего маточного сегмента, над внутренним зевом, частично или полностью перекрывая его, и находится ниже предлежащей части плода, т. е. на пути его рождения.
Классификация:
1) центральное предлежание: внутренний зев полностью перекрыт плацентой;
2) боковое предлежание: предлежат 1-2 дольки плаценты в пределах зева. Рядом с дольками при влагалищном исследовании определяются шероховатые плодные оболочки;
3) краевое: нижний край плаценты находится у краев внутреннего зева, не заходя на него. В пределах зева только плодовые оболочки;
4) низкое прикрепление: плацента имплантируется в нижнем сегменте, но ее край не доходит до внутреннего зева на 60–70 мм.
Различают также полное (центральное) и неполное предлежание (боковое, краевое).
Этиология и патогенез предлежания плаценты
Основная причина предлежания — дистрофические изменения слизистой матки. К факторам предрасполагающим можно отнести:
1) воспалительные процессы матки, послеродовые септические заболевания;
2) большое число родов, абортов;
3) деформацию полости матки, аномалии развития;
4) миому матки;
5) дисфункцию яичников и коры надпочечников;
6) инфантилизм;
7) курение;
8) низкую протеолитическую активность плодного яйца.
Патогенез (теории):
1) первичная имплантация в области перешейка;
2) миграция плаценты из тела матки;
3) возникновение из placenta capsularis.
Симптоматология и клиническое течение предлежания
плаценты
Ведущим симптомом предлежания плаценты является кровотечение. В основе его лежит отслойка плаценты от стенок матки вследствие расположения её в нижнем сегменте матки в ходе беременности, а затем быстрого развертывания (растяжения) его во время родов; ворсинки предлежащей плаценты в силу ее недостаточной растяжимости теряют связь со стенками матки, вскрываются интервиллезные (межворсинчатые) пространства. В зависимости от вида предлежания плаценты кровотечение может возникнуть на протяжении беременности или вовремя родов. Так, при центральном (полном) предлежании кровотечение нередко начинается рано, во II триместре; при боковом и краевом (неполном) в III триместре или в родах.
Частота кровотечений возрастает в последние 2 недели беременности, когда в организме женщины происходит сложная и многообразная перестройка, направленная на обслуживание родового акта. Сила кровотечения при полном предлежании плаценты обычно значительнее, чем при частичном.
Первое кровотечение чаще начинается спонтанно, без всякой травмы, может быть умеренным или обильным, не сопровождается болью. Тяжесть состояния женщины в большинстве случаев определяется объемом наружной кровопотери. Иногда первое кровотечение столь интенсивно, что может сопровождаться смертельным исходом, а неоднократные повторные кровотечения, хотя и весьма опасны (приводят к анемизации беременной) по исходу могут быть более благоприятными.
Гипоксия плода также один из основных симптомов предлежания плаценты. Степень гипоксии зависит от многих факторов, ведущим из которых является площадь отслойки плаценты и ее темп.
При предлежании плаценты беременность и роды часто осложняются косым и поперечным положением плода, тазовым предлежанием, недонашиванием, слабостью родовой деятельности, нарушением течения послеродового периода в связи с врастанием плаценты, гипо- и атоническими кровотечениями в ранний послеродовый период, эмболией околоплодными водами и тромбоэмболией, восходящей инфекцией.
В отличие от правильно расположенной плаценты, предлежащая плацента находится в области внутреннего зева, куда восходящим путем неминуемо распространяется инфекция, для которой сгустки крови являются весьма благоприятной средой. К тому же защитные силы организма значительно ослаблены предшествующими кровотечениями. Восхождению инфекции способствуют диагностические и терапевтические мероприятия, проводимые влагалищно. Поэтому септические осложнения при предлежании плаценты возникают в несколько раз чаще по сравнению с беременными, у которых плацента расположена нормально.
Диагностика предлежаний плаценты
анамнез;
объективное исследование (осмотр, акушерские приемы, аускультация и т. д.);
влагалищное исследование только для уточнения диагноза, при подготовленной операционной
* при закрытом зеве через своды определяется массивная, мягкая губчатая ткань;
* при раскрытии зева на 3 см и более прощупывается губчатая ткань вместе с оболочками;
осмотр шейки матки в зеркалах для диф. диагностики;
УЗИ (наиболее объективный и безопасный метод).
При выявлении предлежания в сроке свыше 24 недель:
госпитализация;
повторное УЗИ;
полное клиническое обследование;
пролонгирование беременности до 36–37 недель в отделении патологии беременности.
При кровянистых выделениях, удовлетворительном состоянии женщины:
строгий постельный режим;
спазмолитики;
токолитики;
инфузионно-трансфузионная терапия;
профилактика гипоксии, СДР плода;
гемостатическая терапия;
vit. Е, С, В1, В6.
Выбор метода родоразрешения зависит от:
объема кровопотери;
времени возникновения кровотечения;
состояния беременной и плода;
состояния родовых путей;
срока беременности;
формы предлежания и положения плода.
Роды через естественные родовые пути возможны при:
1) частичном предлежании;
2) незначительной кровопотере;
3) хорошей родовой деятельности;
4) хорошо прижатой головке;
5) при соответствии размеров.
Показано:
1) вскрытие плодного пузыря при раскрытии шейки матки > или равном 4 см. (ранняя амниотония), если кровотечение продолжается — кесарево сечение;
2) усиление сократительной функции матки внутривенным введением утеротоников;
3) спазмолитики;
4) профилактика гипотонического кровотечения;
5) ручное отделение и выделение последа.
Течение беременности и родов при предлежании плаценты
Лечение беременных с предлежанием плаценты при сроке беременности свыше 24 недель осуществляется только в акушерских стационарах. Несмотря на прекращение кровянистых выделений из половых путей беременные с предлежанием плаценты ни при каких условиях не подлежат выписке до родов. При выборе способа лечения следует руководствоваться прежде всего силой кровотечения, степенью малокровия больной, общим ее состоянием, видом предлежания плаценты, сроком беременности и состоянием плода.
Если кровотечение незначительное и начинается при недоношенной беременности, а состояние больной удовлетворительное то назначается: строгий постельный режим, препараты миолитического и спазмолитического действия, улучшающие координированный характер сократительной деятельности матки и более плавное постепенное растяжение нижнего ее сегмента; лечение анемии; препараты, улучшающие маточно-плацентарный кровоток и обменные процессы.
Для улучшения обменных процессов обязательно использование комплекса витаминов, эссенциале, липостабила. Целесообразно назначение теоникола, курантила, свечей с платифиллином. По показаниям применяется седативная терапия (настой травы пустырника, корень валерианы, седуксен), так же антигистаминные препараты (димедрол, пипольфен, супрастин).
Беременным с предлежанием плаценты слабительные противопоказаны. При необходимости назначают очистительную клизму.
Показаниями к кесареву сечению во время беременности являются:
повторяющиеся кровопотери, объем которых превышает 200 мл.;
сочетание небольших кровопотерь с анемией;
одномоментная кровопотеря 250 мл. и более и продолжающееся кровотечение.
В этих случаях операция производится по жизненным показаниям со стороны матери независимо от срока беременности и состояния плода.
Плановое кесарево сечение производят при полном предлежании плаценты на 38-й неделе беременности, не ожидая возможного кровотечения.
Показанием к плановому кесареву сечению может также служить частичное предлежание плаценты в сочетании с другой акушерской или соматической патологией.
Во время родов показанием к абдоминальному родоразрешению является полное предлежание плаценты.
При частичном предлежании плаценты кесарево сечение в родах показано при:
1) обильном кровотечении, при малых степенях раскрытиях маточного зева;
2) наличии сопутствующей акушерской патологии.
Для предотвращения прогрессирования отслойки частично предлежащей плаценты в порядке подготовки к операции необходимо произвести амниотомию.
Шеечная беременность
Шеечная беременность является редкой, но очень тяжелой патологией. Характеризуется она тем, что плодное яйцо имплантируется и развивается в шеечном канале. Шейка матки в силу анатомических и функциональных особенностей не может служить плодовместилищем. Прерывание шеечной беременности ведет к сильному кровотечению из сосудов шейки, поврежденных ворсинами хориона.
Причинами шеечной беременности могут быть неполноценность слизистой оболочки матки вследствие неоднократных выскабливаний, воспалительных изменений или снижение способности плодного яйца к нидации(имплантации).
При развитии беременности в канале шейки последняя приобретает бочкообразную форму, наружный зев располагается эксцентрично, стенки истончены и растянуты. Тело матки более плотное, чем шейка и меньше ее по размерам.
До 5–6ой недели какие либо особые признаки шеечной беременности отсутствуют и, как правило, диагноз уточняется при появлении кровотечения. При обследовании больной необходимо обратить внимание на форму шейки, расположение наружного зева, характер кровянистых выделений (яркие, пульсирующие струйкой). Ввести палец в канал, как правило, невозможно.
Попытки лечить таких больных консервативно неэффективны. Инструментальное удаление плодного яйца при шеечной беременности сопровождается усилением кровотечения.
Лечение: операция экстирпации матки, проводимая по экстренным показаниям. Тампонаду шейки матки можно производить только на время подготовки к операции.
Преждевременная отслойка нормально расположенной
плаценты
Преждевременная отслойка нормально расположенной плаценты – преждевременное отделение ее (до рождения ребенка) от стенки матки.
Этиология.
Предрасполагающие факторы:
1) поздний токсикоз;
2) гипертоническая болезнь;
3) пиелонефрит;
4) субмукозная миома матки;
5) многоводие;
6) многоплодие;
7) аутоиммунные состояния, аллергия;
8) болезни крови;
9) сахарный диабет;
10) перенашивание;
11) гиповитаминозы (vit. Е).
Механические факторы являются разрешающим моментом:
1) психические и физические травмы;
2) короткая пуповина;
3) быстрое излитие околоплодных вод при многоводии;
4) запоздалый или преждевременный разрыв плодного пузыря;
5) быстрое рождение I плода при монохориальной двойне.
Преждевременной отслойке предшествуют хронические нарушения маточно-плацентарного кровообращения:
спазм артериол и капилляров;
васкулопатия, повышение проницаемости;
повышение вязкости крови со стазом эритроцитов.
Патогенез:
отслойка начинается с геморрагий в decidua basalis;
разрушение базальной пластинки децидуальной ткани;
образование ретроплацентарной гематомы;
сдавление, деструкция прилегающей плаценты;
нарушение сократительной функции матки, диффузное пропитывание кровью миометрия, брюшины, параметрия (матка Кювелера).
Классификация:
1) частичная отслойка
* прогрессирующая
* не прогрессирующая
2) полная
Клиника, диагностика преждевременной отслойки нормально
расположенной плаценты
1) кровянистые выделения темного цвета (во время схватки не усиливаются), может и не быть выделений;
2) острая боль в животе (особенно при ретроплацентарной гематоме);
3) клиника внутреннего кровотечения;
4) гипертонус матки: она напряжена, резко болезненна, увеличена, иногда ассиметрична;
5) пальпация плода затруднена;
6) гипоксия плода, сердцебиение выслушивается с трудом;
7) при большой кровопотере (> 1000 мл.) признаки геморрагического шока и ДВС-синдрома.
Диагностика: УЗИ; клиническая картина; анамнез; КТГ.
Дифференциальная диагностика с предлежанием плаценты
при предлежании плаценты:
нет болевого синдрома;
кровотечение наружное, алая кровь;
обычная форма и консистенция матки, матка безболезненная;
плод хорошо пальпируется;
сердцебиение мало страдает;
данные УЗИ;
состояние больной соответствует объему наружного кровотечения;
схватки усиливают кровотечение;
нет признаков раздражения брюшины.
Лечение преждевременной отслойки нормально расположенной
плаценты
Выбор метода родоразрешения и врачебная тактика зависит от:
выраженности кровотечения;
состояния матери и плода;
срока беременности;
состояния родовых путей;
состояния гемостаза.
При легкой степени отслойки во время беременности:
тщательный контроль;
полное клиническое обследование;
спазмолитики;
препараты железа;
лечение гипоксии плода;
коррекция нарушений гемостаза.
При выраженной клинической картине во время беременности – срочное родоразрешение путем операции кесарево сечение.
Предлежание плаценты (дополнительные материалы) — патология плаценты, при которой плацента частично или полностью перекрывает область внутреннего зева, т. е. оказывается на пути прохождения ребенка.
Предрасполагающие факторы: рубец на матке; осложненный акушерско-гинекологический анамнез; миома матки.
Ведущий и единственный симптом: повторяющиеся маточные кровотечения во второй половине беременности. Кровотечению, как правило, предшествуют неоднократные кровянистые выделения из половых путей, усиливающиеся по мере увеличения срока беременности. Обильное кровотечение начинается внезапно, наличие болей не характерно. Кровотечение за короткий промежуток времени угрожает стать массивным — 1000–2000 мл. У беременной (роженицы) быстро нарастают симптомы геморрагического шока, так как устойчивость организма беременной к кровопотере резко снижена из-за предшествующих кровопотерь и нередко развивающейся постгеморрагической гипохромной анемии (гемоглобин меньше 100 г/л).
Дифференциальная диагностика: шеечная беременность; преждевременная отслойка нормально расположенной плаценты; разрыв матки; заболевания крови; разрыв варикозно расширенных вен влагалища.
Лечебно-тактические мероприятия на догоспитальном этапе:
Определение степени тяжести общего состояния больной (частота пульса, дыхания, АД, шоковый индекс Альговера (отношение пульса к значению систолического АД, в норме 0,5), окраска кожных покровов).
Выяснение акушерской ситуации (срок беременности, наличие или отсутствие регулярной родовой деятельности).
Выявление изменения формы матки, определение ее тонуса, болезненности, характера предлежащей части с помощью осторожного наружного обследования. Влагалищное исследование возможно только при развернутой операционной в связи с опасностью развития профузного маточного кровотечения.
Оценка состояния плода (шевеление, сердцебиение).
Оценка степени и характера кровотечения из родовых путей. В родах при доношенной беременности кровопотеря 350–400 мл считается предельно допустимой (пограничной), так как она может быть компенсирована за счет адаптационных возможностей организма женщины; кровопотеря более 0,5% от веса беременной или роженицы считается патологической и требует проведения лечебных мероприятий.
При незначительных кровянистых выделениях на догоспитальном этапе лечения не требуется. При обильных кровянистых выделениях необходимо немедленно начинать инфузионную терапию, направленную на восполнение ОЦК и стабилизацию состояния женщины. Высокая молекулярная масса, длительная циркуляция в крови декстранов делают их предпочтительными при массивной кровопотере: полиглюкин 400 мл внутривенно, желатиноль 400 мл внутривенно; возможно применение производных этих препаратов. Более эффективно применение растворов крахмала (инфукол ГЭК, рефортан ГЭК, стабизол ГЭК, HAES). Препарат последнего поколения рефортан ГЭК — гидроксиэтилкрахмал для внутривенных вливаний в количестве 500 мл 6% раствора длительно циркулирует в сосудистом русле, имеет исключительно внутрисосудистое распределение, улучшает реологические свойства крови и микроциркуляцию, наименее опасен в смысле коагулопатий.
Для уменьшения сократительной активности матки показано внутримышечное введение спазмолитиков (дротаверин, но-шпа, спазоверин, спаковин): 10 мл 25% раствора магния сульфата, 2 мл 2% раствора папаверина.
С целью профилактики внутриутробной гипоксии плода рекомендуется 20 мл 40% глюкозы и 2–3 мл 5% раствора аскорбиновой кислоты внутривенно, ингаляция воздушно-кислородной смеси 40–60%.
Гемостатическая терапия — дицинон или амбен 2–4 мл внутривенно.
Транспортировка больной должна осуществляться в горизонтальном положении, при доношенном сроке беременности — с приподнятой головной частью туловища для уменьшения дыхательной недостаточности.
Беременная (роженица) с предлежанием плаценты должна быть доставлена в акушерский стационар, располагающий реанимационным и оперативным отделениями. Персонал акушерского стационара в обязательном порядке заблаговременно извещают о поступлении тяжелой больной. По прибытии в стационар больная должна быть передана непосредственно дежурному врачу.
Преждевременная отслойка нормально расположенной плаценты (ПОНРП) — патология беременности, при которой происходит полная или частичная отслойка плаценты от стенок матки во время беременности или в первом или втором периоде родов (т. е. до рождения ребенка).
Предрасполагающие факторы: поздний гестоз, артериальная гипертензия, заболевания почек, осложненный акушерско-гинекологический анамнез, миома матки, быстрое опорожнение матки при многоводии, многоплодии, крупном плоде; травмы живота.
Клинические проявления: сильные боли в нижних отделах живота в поздние сроки беременности или в родах; чувство напряжения матки; кровотечение — наружное (из родовых путей), внутреннее (в область ретроплацентарной гематомы до 500–1500 мл), комбинированное; слабость, головокружение, недомогание; бледность кожных покровов, тахикардия, артериальная гипотензия; значительное снижение или исчезновение движений плода.
Кровотечение при ПОНРП связано с двойным нарушением гемостаза за счет уменьшения сократительной способности матки, так как мышцы стенки пропитаны кровью, и за счет развития ДВС-синдрома.
Объем общей кровопотери при ПОНРП способен колебаться в пределах от 600 до 2500 мл, малый объем внешней кровопотери может не соответствовать тяжести состояния больной. При ПОНРП может развиться синдром полиорганной недостаточности таких жизненно важных органов, как печень, почки, легкие, сердце, мозг, который выражается в эндогенной интоксикации организма, резкой гипоксии и развитии дисциркуляторных нарушений в легких, почках, плаценте, матке.
У плода быстро нарастают симптомы внутриутробной гипоксии. При отслойке плаценты на треть и более плод всегда погибает.
ПОНРП дифференцируют с предлежанием плаценты, разрывом матки и другими состояниями, сопровождающимися болью в животе (острый аппендицит). При предлежании плаценты отсутствуют болезненность и напряжение матки, доступны для пальпации части плода, обычно не нарушена его жизнедеятельность. При разрыве матки в анамнезе есть указания на осложненные аборты, роды, перенесенные операции на матке.
Тактика врача СМП при ПОНРП:
Определение степени тяжести общего состояния больной (частота пульса, дыхания, АД, шоковый индекс Альговера, окраска кожных покровов). Следует отметить, что АД на фоне гестозов второй половины беременности может быть снижено до нормальных цифр, что маскирует истинный характер кровопотери.
Выяснение акушерской ситуации (срок беременности, наличие или отсутствие регулярной родовой деятельности, характер появления болей в матке, их локализация). Необходимо выявить изменения формы матки, определить ее тонус, болезненность, наличие симптомов раздражения брюшины, степень и характер кровотечения из родовых путей.
Оценка состояния плода (шевеление, сердцебиение).
Проведение на догоспитальном этапе беременной (роженице) с ПОНРП инфузионной терапии, направленной на поддержание функции жизненно важных органов и ЦНС (аналогичной терапии при предлежании плаценты).
Пациентку с ПОНРП необходимо немедленно госпитализировать в ближайший акушерский стационар.
Кровотечения, обусловленные коагулопатией (ДВС)
Причины: массивная кровопотеря при гипо- и атонии матки, преждевременная отслойка нормально расположенной плаценты, эмболия околоплодными водами, длительное (более 2 нед) пребывание мертвого плода в матке, гестоз, разрыв матки, кесарево сечение.
Ведущие симптомы: нарастание объема кровопотери и тяжести геморрагического шока, неэффективность мероприятий, направленных на лечение гипо- и атонии матки, появление кровоподтеков в местах инъекций; кровь, вытекающая из родовых путей или в рану при операции кесарева сечения, образует рыхлые сгустки (в тяжелых случаях не свертывается); матка плотная, хорошо контурируется.
Неотложная терапия направлена на предотвращение или выведение из геморрагического шока. Лечебно-тактические мероприятия на догоспитальном этапе направлены на экстренную доставку беременных (рожениц) в акушерский стационар, оборудованный лабораторией для исследования показателей свертывающей системы крови и располагающий возможностями для динамического исследования коагулограммы, а также реанимационным отделением и квалифицированными кадрами для осуществления лечения оперативными методами.
Транспортировку больных осуществляют в горизонтальном положении под непрерывным наблюдением за АД, частотой пульса, дыхания. В помощь может быть вызвана реанимационно-хирургическая бригада. Обязательны ИВЛ и кислородно-воздушная ингаляция. Акушерский стационар должен быть заранее оповещен о прибытии тяжелобольной беременной или роженицы.
Основные направления терапии:
Лечение необходимо начинать с восстановления системной гемодинамики путем введения растворов с высокой молекулярной массой — оксиэтилированного крахмала (6% и 10% HAES-steril) из расчета 10–20 мг/кг/ч, волекама от 500 до 1000 мл, растворов декстрана не более 400 мл.
Категорический отказ от введения гепарина с целью прерывания внутрисосудистого свертывания ввиду отсутствия четкой диагностики 1-й фазы ДВС-синдрома и перехода ее во 2-ю фазу ДВС.
Использование ингибиторов протеаз (апротекс, контрикал, гордокс) в дозе не менее 10 мг/кг/ч с целью подавления избыточного фибринолиза и предотвращения прогрессирования внутрисосудистого свертывания крови, антиагрегантного действия.
Стимуляция сосудисто-тромбоцитарного звена гемостаза (дицинон или этамзилат) 4 мл, 0,5 г активного вещества, внутривенно.
Использование транексамовой кислоты (трансамча, цикло-Ф) — антиплазминового препарата в дозе 500–750 мг на физиологическом растворе.
Учитывая развитие гипогликемии при массивной кровопотере, целесообразно включение в инфузионно-трансфузионную терапию растворов концентрированных углеводов (глюкоза 10–20%, 400 мл). Введение данных растворов способствует не только восстановлению энергетических ресурсов, но и потенцирует гемодинамический эффект.
При нестабильной гемодинамике и продолжающемся кровотечении показана глюкокортикоидная терапия — преднизолон не менее 10 мг/кг/ч или гидрокортизон не менее 100 мг/кг/сут.
ДВС-синдром в акушерстве (дополнительный материал)
Диссеминированное внутрисосудистое свертывание крови — это неспецифическая патология гемостаза.
В основе этого процесса лежит рассеянное свертывание крови в циркуляции с образованием множественных микросгустков и агрегатов клеток крови, блокирующих микроциркуляцию и вызывающих дистрофические изменения в органах с последующим развитием гипокоагуляции и тромбоцитопении потребления.
Это приводит к появлению тромбогеморрагий, гипоксии, ацидоза, интоксикации организма продуктами белкового распада и другими метаболитами и возникновению вторичных кровотечений.
ДВС-синдром всегда вторичен. Часто он осложняет течение инфекционно-воспалительных процессов, особенно генерализованных, и септических состояний. ДВС-синдром является неизменным компонентом всех шоковых состояний, обильных кровотечений.
К развитию ДВС-синдрома может приводить острый внутрисосудистый гемолиз при переливании несовместимой крови, при многих видах гемолитических анемий, массивных гемотрансфузиях и реинфузиях крови, введении гемопрепаратов, содержащих активированные факторы свертывания.
Причиной ДВС-синдрома может быть лечение препаратами, вызывающими агрегацию тромбоцитов, повышающими свертываемость крови и снижающими ее противосвертывающий и фибринолитический потенциал, особенно при их комбинированном применении (альфа-адреномиметики, синтетические прогестины, аминокапроновая кислота и другие ингибиторы фибринолиза).
Из акушерской патологии опасны в плане развития ДВС-синдрома преждевременная отслойка плаценты, предлежание плаценты, ее ручное отделение, эмболия околоплодными водами, внутриутробная гибель плода, привычное невынашивание, эклампсия, гестоз, кесарево сечение, интенсивный массаж матки, обильные кровотечения.
ДВС-синдром может развиваться при различных экстрагенитальных заболеваниях: врожденных синих пороках сердца, коарктации аорты, тромбоэмболии легочной артерии, диффузных миокардитах, гипертонической болезни, аутоиммунных заболеваниях, аллергических реакциях лекарственного и иного генеза, деструктивных процессах в почках, печени, поджелудочной железе, сахарном диабете и другой патологии.
Большинство этиологических факторов вызывает повреждение тканей и поступление в кровь большого количества тканевого тромбопластина (фактор III), под его влиянием происходит превращение неактивного фактора VII в активный VIIа.
Далее этот комплекс активирует фактор Х по внешнему пути, т. е. под влиянием тканевого тромбопластина происходит активация внешнего (тканевого) пути свертывания крови.
Аналогами тканевого тромбопластина являются внутриклеточные и тканевые протеазы, коагулазы из бактерий и змеиных ядов. Также под влиянием этиологических факторов происходит повреждение эндотелия и обнажение коллагена в субэпителиальной зоне.
Это приводит к адсорбции XII, XI, IX факторов свертывания, высокомолекулярного кининогена и прекалликреина и их активации.
Таким образом происходит включение внутреннего пути активации свертывания крови.
Важную роль в формировании ДВС-синдрома играют тромбоциты и эритроциты. Обязательным компонентом является агрегация тромбоцитов и вовлечение их в процесс тромбообразования.
В периферической крови и сосудах малого калибра в большом количестве выявляются активированные формы и агрегаты этих клеток, в плазме повышается содержание продуктов дегрануляции тромбоцитов, укорачивается продолжительность их жизни и циркуляции и уменьшается количество (тромбоцитопения потребления).
Эритроциты при ДВС-синдроме подвергаются макро- и микротравматизации, вследствие чего их жизнь и циркуляция укорачиваются и возникает симптомокомплекс внутрисосудистого гемолиза.
Он сопровождается развитием анемии, повышением в плазме свободного гемоглобина, непрямого билирубина и ретикулоцитозом.
Патогенез
Важнейшей патогенетической особенностью ДВС-синдрома является активация не только системы свертывания, но и фибринолитической, калликреин-кининовой, комплемента. Вследствие этого в крови появляется много продуктов белкового распада.
Многие из них высокотоксичны, вызывают дезорганизацию сосудистой стенки, усугубляют микроциркуляторные нарушения, вторично усиливают свертывание крови и агрегацию тромбоцитов или, наоборот, тормозят.
В процессе развития ДВС в плазме снижается количество антикоагулянтов и компонентов фибринолитической системы.
В крови накапливаются промежуточные продукты свертывания — растворимые комплексы фибрина. Они блокируют конечный этап свертывания. Это приводит к тому, что сначала развивается нормо- а затем и гипокоагуляционное состояние.
Кроме того, вследствие гипоксии, нарушается сосудисто-тромбоцитарный гемостаз, эндотоксины и продукты протеолиза влияют на сосудистую стенку, снижается количество тромбоцитов и факторов свертывания.
Все это приводит к развитию геморрагического синдрома.
В патогенезе ДВС-синдрома имеют значение также нарушения микроциркуляции. Этот процесс связан с блокадой сосудов сгустками фибрина и агрегатами клеток, сладж-синдромом. Результатом является развитие полиорганной недостаточности.
Классификация
По течению выделяют молниеносные, острые, подострые и хронические формы ДВС-синдрома.
В основе этой классификации лежит признак скорости развития геморрагических проявлений ДВС. Острота и выраженность ДВС-синдрома определяются скоростью поступления в кровь и количеством активаторов гемостаза.
Молниеносные формы развиваются в течение нескольких десятков минут и встречаются, например, при эмболии околоплодными водами. При остром течении ДВС-синдром развивается в течение нескольких часов (до суток).
Это характерно для сепсиса, в том числе после аборта, объемных операций, краш-синдрома, синдрома массивных гемотрансфузий, отслойки плаценты, тяжелого гестоза.
ДВС-синдром подострого течения развивается в течение нескольких дней (до 3-х недель) и наблюдается при аутоиммунных состояниях, а также при многих акушерских патологиях.
Хроническое течение ДВС встречается чаще всего. Он может длительное время протекать бессимптомно, однако при прогрессировании заболевания-индуктора появляется геморрагический синдром и разворачивается клиника.
Такая ситуация встречается при длительно текущем гестозе, привычном невынашивании беременности, хроническом гломерулонефрите, гипертонической болезни, сахарном диабете и других заболеваниях.
Встречаются также рецидивирующие формы ДВС-синдрома. Им свойственно периодическое стихание и нарастание геморрагических проявлений.
В связи с изменением коагуляционных параметров выделяют 4 стадии ДВС-синдрома.
I стадия — гиперкоагуляция и агрегация тромбоцитов.
II стадия — переходная, с нарастающей коагулопатией и тромбоцитопенией, разнонаправленными сдвигами в общих коагуляционных тестах.
III стадия — глубокая гипокоагуляция вплоть до полной несвертываемости крови.
IV стадия — исход (восстановление или развитие осложнений).
Клиническая картина ДВС-синдрома является отражением тромботических и ишемических повреждений органов и тканей и геморрагического синдрома.
Тромботические явления. Могут наблюдаться тромбозы в измененных сосудах, в брыжеечной артерии с последующим некрозом кишечника, тромбоэндокардиты.
Геморрагический синдром. Может быть локальным и распространенным. Возможно появление кровоподтеков в местах инъекций, в подкожной и забрюшинной клетчатке, носовых, желудочно-кишечных, легочных и почечных кровотечений, кровоизлияний в различные органы.
Микроциркуляторные нарушения. Они связаны с микротромбированием в токе крови и оседанием этих сгустков в мелких сосудах. В результате нарушается оксигенация тканей, снижаются функции внутренних органов.
Часто развивается острая почечная недостаточность, которая проявляется снижением диуреза вплоть до анурии, появлением в моче белка, цилиндров, нарастанием уровней креатинина и мочевины.
Нарушения гемодинамики. Микротромбирование приводит к полной блокаде микроциркуляции, в результате чего происходит сброс крови по артериоло-венулярным шунтам. В начальной фазе преобладает спазм артериол с централизацией кровообращения. Затем развивается парез микрососудов с явлениями стаза.
Анемический синдром. В его основе лежит внутрисосудистый механический гемолиз в сочетании с кровоточивостью. Внутрисосудистый гемолиз обычно не носит стремительного характера, связанная с ним анемизация с высоким ретикулоцитозом проявляется через несколько суток. При тяжелых кровотечениях возникает острая постгеморрагическая анемия.
Нарушение репарации тканей. Отмечаются плохое заживление ран, нагноительные процессы, развиваются келоидные рубцы. Это связано с нарушением активации тромбоцитов, миграции макрофагов, микроциркуляции.
Диагностика. Принципы лечения
В диагностике имеют значение клиническая картина, оценка причинно-следственной связи между заболеванием-индуктором и развитием геморрагического синдрома. Важное значение имеют лабораторные методы диагностики. Используют определение количества тромбоцитов, их агрегационной функции, определение ретракции кровяного сгустка, времени свертывания крови, протромбинового индекса, тромбинового времени, показателей фибринолитической системы, маркеров ДВС.
Лечение. Хронический ДВС-синдром, развивающийся у здоровых людей, не нуждается в лечении, поскольку он является адаптацией организма к изменившимся условиям существования. Остальные формы лечат в зависимости от стадии.
В первую очередь необходимо устранить акушерскую патологию, вызвавшую ДВС-синдром, затем нормализовать центральную и периферическую гемодинамику, далее восстанавливают гемокоагуляционные свойства и нормализуют фибринолиз.
Для усиления антикоагулянтной активности вводят гепарин. Свежезамороженная плазма является источником антитромбина III, плазминогена, факторов свертывания и естественных антиагрегантов. Воздействовать на тромбоцитарное звено гемостаза можно с помощью дезагрегантов.
К ним относятся ингибиторы простагландинсинтетазы (аспирин, индометацин), активаторы аденилатциклазы и ингибиторы фосфодиэстеразы (курантил, трентал, препараты, содержащие никотиновую кислоту, спазмолитики), мембраностабилизирующие антиагреганты (реополиглюкин и другие низкомолекулярные декстраны).
Для удаления избыточного количества активаторов свертывания крови эффективен плазмоферез и введение ингибиторов протеаз. Усилить лизис тромбов можно с помощью фибринолитических средств.
Геморрагический шок — клиническая категория для обозначения критических состояний, связанных с острой кровопотерей, в результате которой развивается кризис макро- и микроциркуляции, синдром полиорганной и полисистемной недостаточности. К развитию геморрагического шока приводят геморрагии, превышающие 1000 мл, т. е. кровопотеря более 20% ОЦК (компенсированная стадия); кровотечение считается массивным, если превышает 30–35% ОЦК — 1500 мл (декомпенсированная обратимая стадия); кровопотеря свыше 50% ОЦК — декомпенсированная необратимая стадия, подобное кровотечение угрожает жизни.
Особенности геморрагического шока при акушерской патологии:
Часто сопровождается развитием синдрома ДВС.
При предлежании плаценты характеризуется резкой гиповолемией, артериальной гипотензией, гипохромной постгеморрагической анемией.
Нередко развивается на фоне предшествующей тяжелой формы гестоза беременных.
При преждевременной отслойке нормально расположенной плаценты характеризуется гиповолемией на фоне хронического сосудистого спазма, хронической формы синдрома ДВС.
При геморрагическом шоке, развившемся вследствие гипотонического кровотечения в раннем послеродовом периоде, характерен кратковременный период неустойчивой компенсации, после которого быстро наступают необратимые изменения, характеризующиеся стойкими нарушениями гемодинамики, дыхательной недостаточностью и синдромом ДВС с профузным кровотечением, обусловленным потреблением факторов свертывания крови и резкой активацией фибринолиза.
При разрыве матки характерны симптомы гиповолемии и недостаточности внешнего дыхания.
Лечение геморрагического шока акушерской этиологии начинается на догоспитальном этапе. Основные мероприятия по его лечению сводятся к следующему: проведение акушерских пособий и операций местного гемостаза; оказание анестезиологического пособия, устранение дыхательной недостаточности; проведение инфузионно-трансфузионной терапии, направленной на восстановление состава, свойств и ОЦК; устранение расстройств кислотно-основного состояния (КОС).
Транспортировку больной проводят в горизонтальном положении с опущенной головной частью, в пути проводят введение инфузионных растворов. Для уменьшения дыхательной недостаточности проводят ингаляцию кислорода через аппарат КИ-3М или АН-8М; пациентке может быть дан наркоз закисью азота с кислородом в соотношении 1:2, при необходимости — интубация и искусственная вентиляция легких.
Инфузионно-трансфузионная терапия проводится по индивидуальной программе для каждой больной с учетом особенностей геморрагического шока, характерного для акушерской патологии; сопутствующих заболеваний (сердца, почек и т. д.); наличия признаков гестоза.
Лечение геморрагического шока предполагает введение противошоковых растворов: полиоксидин 400 мл, или волекам 400 мл, или полиглюкин 400 мл; скорость введения 20 мл/мин, а при улучшении состояния — дробное введение по 100–150 мл под контролем состояния легких. Необходимо помнить, что введение избыточного количества кровезаменителей на основе декстрана может привести к усилению нарушений в свертывающей системе крови — гемодилюционной коагулопатии, в результате чего кровотечение из половых путей и матки усиливается; pеополиглюкин 400 мл + желатиноль 400 мл; 5% раствор глюкозы 500 мл и 6 ЕД инсулина или 10% раствор глюкозы и 7 ЕД инсулина; 5 мл 5% раствора унитиола; 100 мг ККБ; 4–6 мл дицинона или этамзилата натрия.
Для улучшения почечного кровотока — 10 мл 2,4% раствора эуфиллина или 5 мл трентала.
Для борьбы с ацидозом — 5% раствор бикарбоната натрия 100 мл.
Для снятия периферической вазоконстрикции — 2 мл 2% раствора но-шпы.
В острой фазе геморрагического шока — глюкокортикоиды.
Для выведения жидкости — лазикс 40-80мг, маннитол 2 г/кг массы. Большие дозы диуретиков у беременных используют редко ввиду их влияния на ОЦК, перфузию плаценты и на внутриутробный плод.
В инфузионной терапии можно применить солевые растворы электролитов: трисоль, дисоль, хлосоль, трисамин — 250 мл или лактосол 500 мл.
При стойкой утрате сосудистого тонуса на фоне восполнения кровопотери внутривенно медленно вводят допамин 1 мл в 150 мл изотонического раствора натрия хлорида, или 0,3 — 0,5 мл мезатона, или 0,3 — 0,5 мл 2% раствора норадреналина.
В острой фазе геморрагического шока можно использовать глюкокортикоиды: преднизолон 30–60 мг, дексазон — 408 мг, гидрокортизон 125–250 мг внутримышечно или внутривенно.
Периферическую вазоконстрикцию снимают введением 2 мл 2% раствора но-шпы.
Объем инфузионно-трансфузионной терапии зависит от объема кровопотери, показателей гематокрита, длительности шока. При кровопотере в объеме 1 л объем переливаемых жидкостей должен быть больше потерянного объема крови в 1,5 раза; при кровопотере 1,5 литра — в 2 раза; при кровопотере 2 л — в 2,5 раза. 75% от потерянного объема должны быть восстановлены в первые 1–2 ч от начала кровотечения.
Перед началом инфузии необходимо провести катетеризацию мочевого пузыря и оценить цвет мочи, наличие добавочных примесей (крови), количество мочи до, во время и после инфузионно-трансфузионной терапии.
Геморрагический шок в акушерстве (дополнительный материал)
Геморрагический шок возникает в ответ на патологическую кровопотерю. Развивается синдром малого выброса, гипоперфузия тканей, полиорганная и полисистемная недостаточность. Геморрагический шок в акушерстве остается одной из причин материнской смертности (2—3 место среди причин материнской смертности).
Этиология. Причинами геморрагического шока в акушерстве являются потеря более 1000 мл крови, или >15% ОЦК, или >1,5% от массы тела. Угрожающими жизни кровотечениями считаются:
1) потеря 100% ОЦК в течение 24 часов или 50% ОЦК за 3 часа;
2) кровопотеря со скоростью 150 мл/мин или 1,5 мл/кг/мин (>20 мин;
3) одномоментная кровопотеря >1500—2000 мл (25—35% ОЦК).
При экстрагенитальной патологии, гестозах, слабости родовой деятельности, при неадекватном обезболивании родов симптомы шока могут появиться и при меньшей кровопотере (800-1000 мл).
Причиной геморрагического шока является кровотечение, которое может быть обусловлено:
• преждевременной отслойкой нормально расположенной и предлежащей плаценты;
• разрывом матки;
• частичным плотным прикреплением или приращением, плаценты;
• гипотонией и атонией матки;
• врожденными дефектами гемостаза;
Способствуют кровотечению состояния, когда нарушается гемостаз в организме матери вследствие попадания в ее кровоток тромбопластических субстанций от плода и элементов плодного яйца: эмболия околоплодными водами, мертвый плод в матке.
Патогенез. В акушерстве на развитие геморрагического шока оказывает влияние травматических фактов ввиду наличия боли во время родов при неадекватном обезболивании, различных операциях и манипуляциях: акушерских щипцах, ручном обследовании матки, ушивании разрывов родовых путей, при преждевременной отслойке нормально расположенной плаценты, разрывах матки и т.д.
Кровопотеря >15% ОЦК приводит к ряду компенсаторных реакций, включающих в себя стимуляцию симпатической нервной системы вследствие рефлексов с барорецепторов синокаротидной зоны и крупных внутригрудных артерий, активацию гипоталамо-гипофизарно-надпочечниковой системы с высвобождением катехоламинов, ангиотензина, вазопрессина, антидиуретического гормона. Это способствует спазму артериол, повышению тонуса венозных сосудов (увеличению венозного возврата и преднагрузки), увеличению частоты и силы сердечных сокращений, уменьшению экскреции натрия и воды в почках. Вследствие того, что гидростатическое давление в капиллярах снижается в большей степени, чем в интерстиции, начиная с первого часа и до 40 часов после кровопотери, происходит медленное перемещение межклеточной жидкости в сосудистое русло (транскапиллярное восполнение). Снижение кровотока в органах и тканях приводит к изменениям кислотно-основного состояния (КОС) артериальной крови — повышению концентрации лактата и увеличению дефицита оснований (ВЕ). С целью поддержания нормального рН при воздействии ацидемии на хеморецептор дыхательного центра в стволе головного мозга увеличивается минутная вентиляция, ведущая к снижению РаСО2.
При кровопотере >30% ОЦК происходит декомпенсация, проявляющаяся артериальной гипотензией — снижением систолического артериального давления (АДсист) менее 90 мм рт. ст. Продолжающийся выброс стрессорных гормонов вызывает гликогенолиз, липолиз с умеренными гипергликемией и гипокалиемией. Гипервентиляция больше не обеспечивает нормальный рН артериальной крови, вследствие этого развивается ацидоз. Дальнейшее снижение тканевого кровотока ведет к усилению анаэробного метаболизма с увеличением выделения молочной кислоты. Прогрессирующий метаболический лактоацидоз снижает рН в тканях и блокирует вазоконстрикцию. Артериолы расширяются и кровь заполняет микроциркуляторное русло. Ухудшается сердечный выброс, может развиваться повреждение эндотелиальных клеток с последующим синдромом диссеминированного внутрисосудистого свертывания крови (ДВС).
При кровопотере >40% ОЦК и снижении АДсист <50 мм рт. ст. за счет ишемии центральной нервной системы происходит дополнительная стимуляция симпатической нервной системы с формированием на некоторое время так называемого второго плато АД. Без энергичной интенсивной терапии шок переходит в необратимую стадию, характеризующуюся распространенным повреждением клеток, полиорганной недостаточностью (ПОН), ухудшением сократимости миокарда вплоть до остановки сердечной деятельности.
После восстановления сердечного выброса и тканевого кровотока наблюдаются более выраженные повреждения органов, чем в период гипотензии. Вследствие активизации нейтрофилов, выделения ими перекисных радикалов кислорода, высвобождения медиаторов воспаления из ишемизированных тканей, а это в свою очередь приводит к повреждению клеточных мембран, увеличению проницаемости легочного эндотелия с возможным развитием острого респираторного дистресс синдрома (ОРДС), внутридольковому повреждению печени с увеличением уровня трансаминаз в плазме. Возможен спазм прегломерулярных артериол почек, приводящий к острому некрозу канальцев и острой почечной недостаточности (ОПН). Вследствие нарушения функции печени и снижения синтеза глюкозы, кетонов и торможения периферического липолиза снижается поступление энергетических субстратов к сердцу и мозгу.
Акушерские кровотечения подразделяют на 4 класса в зависимости от величины кровопотери.
У пациенток с кровотечением 1 класса редко встречается дефицит ОЦК, признаков шока нет.
При кровотечении 2 класса часто присутствуют жалобы на необъяснимое беспокойство, чувство холода, ощущение нехватки воздуха или плохое самочувствие. Отмечаются признаки легкого или компенсированного геморрагического шока: умеренные тахикардия, тахипноэ. Могут быть ортостатические изменения АД, нарушения периферического кровообращения в виде положительного теста заполнения капилляров, пульсовое АД < 30 мм рт. ст. Тест заполнения капилляров выполняется путем прижатия ногтевого ложа, возвышения большого пальца в течение 3 секунд до появления белого окрашивания. После окончания давления розовая окраска должна восстановиться менее чем за 2 секунды.
Кровотечение 3 класса характеризуется проявлениями умеренного геморрагического шока: выраженными гипотензией, тахикардией и тахипноэ. Нарушения периферического кровообращения более выражены. Кожные покровы могут быть холодными и влажными.
При кровотечении 4 класса пациентки находятся в тяжелом или декомпенсированном геморрагическом шоке: возможны отсутствие пульсации на периферических артериях, не определяющееся АД, олигурия (диурез <0,5 мл/кг/час) или анурия. В отсутствие адекватной объемозамещающей инфузионной терапии можно ожидать развития циркуляторного коллапса и остановки сердечной деятельности.
Эмболия околоплодными водами
Синдром эмболии околоплодными водами подразумевает попадание амниотической жидкости в кровоток матери, в легочную артерию и ее ветви.
Амниотическая жидкость проникает в кровоток матери либо трансплацентарно через дефекты плаценты и межворсинчатое пространство, либо трансцервикально через поврежденные сосуды шейки матки. Для попадания амниотической жидкости в кровоток матери внутриматочное давление должно превышать давление в межворсинчатом пространстве. При разрыве шейки матки, богатой венозной системой, околоплодные воды могут попадать в кровоток и при нормальном внутриматочном давлении.
Попаданию околоплодных вод в кровяное русло матери способствуют:
• преждевременное вскрытие плодного пузыря, особенно высокий боковой надрыв плодных оболочек;
• чрезмерно сильная родовая деятельность, приводящая к стремительным родам;
• преждевременная отслойка нормально расположенной плаценты;
• кесарево сечение;
• разрывы матки;
• переношенная беременность;
• длительная активация родовой деятельности окситоцином;
• многоводие.
Попадание околоплодных вод в межворсинчатый кровоток, а затем в легкие вызывает раздражение интерорецепторов сосудов элементами амниотической жидкости (казеозная смазка, чешуйки эпителия, меконий).
Рефлекторное раздражение сосудистых интерорецепторов легких, образование тромбоцитарно-фибриновых микросгустков блокируют легочные капилляры, повышает легочное сосудистое сопротивление, вызывая гипертензию в малом круге кровообращения с развитием легочного сердца, острой легочно-сердечной недостаточности, гипотонии.
Околоплодные воды обладают тромбопластиновой активностью, поэтому при попадании их в кровь в мелких сосудах, особенно в легких, происходит отложение фибриновых и тромбоцитарных микросгустков. В результате развивается ДВС-синдром, сопровождающийся блокадой ретикулоэндотелиальной системы, и это способствует выраженной коагулопатии. Кровь при эмболии околоплодными водами теряет способность к свертыванию, что особенно резко проявляется после рождения плода. Возникает тяжелое маточное кровотечение. Одновременно появляются геморрагические диатезы, кровоточивость десен, гематомы в местах инъекций.
Первым проявлением эмболии околоплодными водами является шок. Если не наступает быстрая смерть, то через 30—60 мин (иногда и через 9 ч) развивается массивное кровотечение.
Клиническая картина развивается остро в конце первого и во втором периодах родов. Резко и внезапно ухудшается общее состояние, падает артериальное давление, появляются одышка, кашель, боль за грудиной, цианоз лица. Сознание нередко спутанное, отмечается моторное возбуждение. При тяжелом течении могут наблюдаться тонические и клонические судороги, симптомы кардиогенного шока, признаки острой сердечно-легочной недостаточности. Возможна молниеносная смерть.
Диагноз на первых этапах устанавливается на основании клинической картины. Если пациентка выживает, проводят рентгенографическое исследование грудной клетки, электрокардиографию.
На рентгенограммах отмечаются признаки отека легких; на ЭКГ — признаки левосторонней сердечной недостаточности.
Патологоанатомическим подтверждением эмболии околоплодными водами становится присутствие амниотомическои жидкости в артериолах и капиллярах легких. Могут выявляться чешуйки эпидермиса, частички казеозной смазки, меконий, слизистые субстанции кишечника плода. При центрифугировании содержимого правых отделов сердца возможно его разделение на три слоя, верхний из которых состоит из околоплодных вод.
Лечение эмболии околоплодными водами заключается в восстановлении функции дыхания, сердечно-сосудистой системы, нормализации коагуляционных свойств крови. Для восстановления дыхания производят интубацию трахеи, проводят искусственную вентиляцию легких. Для нормализации функции сердечно-сосудистой системы применяют инфузионно-трансфузионную терапию. Лечение коагуляционных осложнений осуществляется по принципам терапии острой формы ДВС-синдрома.
После проведения неотложных мероприятий осуществляют быстрое и осторожное родоразрешение путем кесарева сечения. Если эмболия возникает в конце второго периода родов, то накладывают акушерские щипцы.
С целью остановки маточного кровотечения в раннем послеродовом периоде сначала перевязывают подвздошные артерии с двух сторон, при отсутствии эффекта показана экстирпация матки
Профилактика кровотечения во время беременности
Важным мероприятием в профилактике кровотечений является формирование групп риска по возникновению этой патологии во время беременности, родов и послеродовом периоде, своевременное обследование, консультации смежных специалистов и лечение беременных, входящих в группы риска.
Дородовая госпитализация должна быть за 2-3 недели до срока родов для обследования и подготовки к родам и прогнозирования метода родоразрешения.
