
Учебники 80137
.pdf
|
|
|
|
Таблица 5 |
|
Названия ароматических карбоновых кислот |
|||
Формула кислоты |
Название кислоты |
|||
|
|
|||
|
|
|
международное |
тривиальное |
|
COOH |
|
|
|
|
|
|
бензолкарбоновая |
бензойная |
|
COOH |
|
|
|
|
|
|
4-метилбензолкарбоновая n-толуиловая |
|
|
CH3 |
|
|
|
COOH |
|
1,2-бензолдикарбоновая |
|
|
|
COOH |
|
фталевая |
|
|
|
|
|
|
|
COOH |
|
1,4-бензолдикарбоновая |
|
|
|
|
терефталевая |
|
|
COOH |
|
|
|
COOH |
|
1,3-бензолдикарбоновая |
|
|
|
|
|
изофталевая |
|
|
COOH |
|
|
|
|
COOH |
|
1-нафтолкарбоновая |
|
|
|
|
a-нафтойная |
|
CH |
CH |
COOH |
|
|
|
|
|
3-фенил-2-пропеновая |
коричная |
|
|
|
21 |
|

Название трех-, четырех- и других многоосновных кислот образуется из названия дикарбоновых кислот, в которых третья (или более) карбоксильная группа рассматривается как заместитель и обозначается приставкой КАРБОКСИ-. Например,
CH3
1 |
2 |
3 |
4 |
|
5 |
|
6 |
||||
HOOC |
|
CH2 |
|
CH |
|
CH |
|
CH2 |
|
COOH |
|
|
|
|
|
|
|||||||
|
|
|
|
||||||||
COOH
3-карбокси-4-метилгександиовая кислота
Сложные эфиры
Название сложных эфиров R – C – OR¢ карбоновых кислот образуют из
½½
О
названий спиртового радикала (R¢–) и названия кислотного остатка. Примеры образования названий сложных эфиров:
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|||||
|
|
|
O |
H3C |
|
C |
H3C |
|
CH2 |
C |
|||||||||
|
|
|
|
|
|||||||||||||||
H |
|
C |
|
O |
|
CH3 |
|
|
O |
|
CH3 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O CH2 CH3 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
метилметаноат (М), |
метилэтаноат (М), |
|
этилпропаноат (М), |
||||||||||||||||
метилформиат (Т) |
метилацетат (Т) |
|
|
этилпропионат (Т) |
|||||||||||||||
Сложные эфиры называют также, указывая полное название кислоты. Например:
O H3C C 
O CH2 CH2 CH3
пропиловый эфир уксусной кислоты или пропилацетат
Пероксиды
Соединения, имеющие группировку –О–О–, называются пероксидами. По международной номенклатуре соединения R–O–OH называют, помещая название радикала перед словом «гидропероксид» или используя приставку ГИДРОПЕРОКСИ перед названием углеводорода. Довольно часто в традиционной русской терминологии гидропероксиды называют, записывая слово «гидроперекись» перед названием радикала. Так, соединение (а) будет называться гидроперекись этила; соединение (б) - гидроперекись о-ксилила:
22

а) |
б) |
|||||||
|
|
O |
|
|
|
|
OH |
|
|
|
|
||||||
CH3–CH2–O-OH |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
CH3 |
|
этилгидропероксид |
|
|
|
|
|
|
|
|
гидропероксиэтан о-толилгидропероксид 1-гидроперокси-2,3-диметилбензол
Соединения, имеющие группировку R – O – O – R¢, называют по международной номенклатуре, помещая названия радикалов R и R¢ в алфавитном порядке перед словом «пероксид». Например,
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3–O–O–C5H11 |
СH3–CH2–O–O–CH2–CH3 |
|
C |
|
|
O |
|
O |
|
|
C |
|||||||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
метилпентилпероксид |
диэтилпероксид |
|
дибензоилпероксид |
|||||||||||||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Кислоты, содержащие группу |
|
C |
|
O |
|
OH , |
называются перокси- |
|||||||||||||||
|
|
|
||||||||||||||||||||
кислотами (надкислотами, гидропероксидами кислот). При образовании названия приставку ПЕРОКСИ– помещают перед тривиальным названием кислоты, а по международной номенклатуре перед названием с окончанием
– ОВАЯ КИСЛОТА. Например,
|
|
|
|
|
O |
O |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
H |
||||
CH3 |
CH2 |
CH2 |
|
C |
|
O |
|
OH |
|
|
|
|
|
|
|
|||
|
|
|
|
|
C |
|
|
|
||||||||||
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пероксибутановая кислота (М), |
бензолпероксикарбоновая кислота (М), |
пероксимасляная кислота (Т) |
пероксибензойная кислота (Т) |
Укоренившиеся названия некоторых пероксикислот:
23

|
|
|
O |
|
|
|
O |
|
|
|
|
O |
|||||||||
H |
|
C |
|
O |
|
OH |
H3C |
|
C |
|
O |
|
OH |
|
|
|
C |
|
O |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пермуравьиная |
|
перуксусная |
пербензойная |
|||||||||||||||||
|
|
|
|
или |
|
|
|
или |
|
|
|
или |
|||||||||
надмуравьиная кислота |
надуксусная кислота |
надбензойная кислота |
|||||||||||||||||||
Гидрокси- и оксокислоты
Гидроксикислоты можно рассматривать как кислоты, в радикале которых один или несколько атомов водорода замещены на гидроксильную группу. В радикале оксокислот имеется карбонильная группа. Названия гидроксикислот по международной номенклатуре образуют, исходя из названия основной кислоты и указывая положение и количество гидроксильных групп. Нумерацию атомов углерода начинают с карбоксильной группы. Названия оксокислот образуют подобным же образом, опуская номер карбоксильного углерода, т.к. он всегда имеет номер 1.
CH3 |
|
C |
|
COOH |
HOOC |
|
|
CH |
|
|
CH |
|
COOH |
CH3 |
|
|
CH |
|
|
CH2 |
|
C |
|
COOH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
CH3 |
|
|
|
O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
2-оксопропановая |
2,3 – дигидроксибутан- |
4-метил-2-оксопентановая |
||||||||||||||||||||||||||
|
кислота |
диовая кислота |
|
|
|
|
|
кислота |
||||||||||||||||||||
Для некоторых соединений со смешанными функциями часто используется тривиальная номенклатура:
HO – CH2 – COOH |
CH3 – CH – COOH |
HOOC–CH2–CH–COOH |
|
| |
| |
|
OH |
OH |
гидроксиэтановая (М), |
2-гидрокси- |
2-гидроксибутандиовая (М), |
гликолевая кислота (Т) |
пропановая (М), |
яблочная кислота (Т) |
|
молочная кислота (Т) |
|
HOOC – CH – CH – COOH |
СH3 – C – COOH |
|
| |
| |
|| |
OH |
OH |
O |
2,3-дигидроксибутандиовая (М), |
2-оксопропановая (М), |
|
винная кислота (Т) |
пировиноградная кислота (Т) |
|
24
Амины
Амины по рационально-функциональной и международной номенклатуре рассматривают как производные аммиака, в котором один или несколько атомов водорода замещены на углеводородные радикалы. В зависимости от количества радикалов различают амины первичные, у которых атом азота связан с одним радикалом, вторичные – с двумя радикалами, третичные – с тремя радикалами. Такая номенклатура очень удобна для обозначения так называемых моноаминов, являющихся производными только одной молекулы аммиака. Названия аминов производят, указывая количество и названия радикалов и добавляя окончание –АМИН. Например,
H |
CH3 |
CH3 |
CH3 |
/ |
/ |
/ |
/ |
N – H |
N – H |
N – CH3 |
N – CH3 |
\ |
\ |
\ |
\ |
H |
H |
H |
CH3 |
аммиак |
метиламин |
диметиламин |
триметиламин |
|
(первичный) |
(вторичный) |
(третичный) |
По международной номенклатуре название аминов складывается из соответствующего наименования углеводорода с прибавлением приставки АМИНО- и цифры, указывающей местоположение аминогруппы - NH2. Например,
1 |
2 |
3 |
4 |
СН3 – СН – СН – СН3
½½
NН2 СН3 2-амино-3-метилбутан
Диамины и полиамины рассматривают как углеводороды, в которых
два или несколько атомов водорода замещены остатками аммиака или аминогруппой –NH2. В зависимости от количества аминогрупп различают моно, ди-, триамины. Их названия производят, присоединяя окончание -ДИАМИН, -ТРИАМИН и т.д. к названию основного углеводорода, либо к названиям двух-, трех-, и поливалентных радикалов. Например: –СН2–СН2– диметилен,
–СН2–СН2–СН2– триметилен, –СН2–СН2–СН2–СН2 – тетраметилен и т.д.
СН2 – СН2 |
СН2 – СН2 – СН2 |
||
½ |
½ |
½ |
½ |
NH2 |
NH2 |
NH2 |
NH2 |
1,2-диаминоэтан (М) или |
1,3-диаминопропан (М) или |
||
диметилендиамин (Р) |
триметилендиамин (Т) |
||
25

Ароматические амины можно рассматривать как производные бензола, в которых один или несколько атомов водорода замещены на аминогруппу.
NH2 |
NH2 |
|
|
|
|
|
|
NH2 |
аминобензол (М), |
1,3-диаминобензол (М), |
|||||
анилин (Т) |
м-диаминобензол (Р) |
|||||
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
N |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Третичному амину |
|
|
|
|
можно дать три равнозначных на- |
|
|
|
|||||
звания: диметилфениламин; N.N–диметиламинобензол; N,N- диметиланилин. Аминопроизводные толуола называют толуидинами, аминопроизвод-
ные ксилола – ксилидинами. Например, |
|
||||||
H3C |
|
|
|
|
|
|
п-толуидин (Т), |
|
|
|
|
|
|
||
|
|
|
|
|
NH2 |
4-метиламинобензол (М) |
|
|
|
|
|
||||
H3C |
|
|
|
|
|
|
1-амино- 2,4-диметилбензол (М), |
|
|
|
|
|
|
||
|
|
|
|
|
NH2 |
2,4-диметиланилин (Р), |
|
|
|
|
|
||||
|
|
|
|
|
|
|
2,4-ксилидин (Т) |
|
|
|
|
CH3 |
|
||
Четырехзамещенные основания – производные катиона аммония (NH4+) рассматривают как производные либо солей, либо гидроксида аммония, в котором все четыре атома водорода замещены на радикалы. Например:
[NH4]+Cl- |
[N(CH3)4]+Cl |
[NH4]+OH |
[N(CH3)4]+OH- |
хлорид |
хлорид |
гидроксид |
гидроксид |
аммония, |
тетраметиламмония, |
аммония, |
тетраметиламмония. |
ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА (ПАВ)
Все поверхостно-активные вещества делятся на две большие группы: ионогенные и неионогенные. В свою очередь ионогенные ПАВ в зависимости от характера образующихся при диссоциации в водных растворах длинноцепочечных ионов делятся на катионные и анионные. Кроме того, имеются еще и амфолитные (амфотерные) ПАВ, которые содержат в молекуле две функциональные группы, образующие при диссоциации в зависимости от рН раствора противоположно заряженные поверхостно-активные ионы: катионы или анионы.
26

Основой для получения ПАВ служат парафины, олефины, высшие жирные спирты, кислоты, фенолы и их производные, их названия и лежат в основе всего названия соединения. ПАВ имеют дифильное строение, т.е. они содержат одновременно гидрофобную и гидрофильную группы. В качестве гидрофобной группы (отталкивающейся от воды) обычно выступает углеводородный радикал, содержащий 10 – 18 углеводородных атомов. К гидро-
фильным группам (имеющим сродство к воде) относятся - OH, -NH2, -COOH, -SO3H, -COOMe, -SO3Me и др. Для ПАВ характерны тривиальные названия.
Анионные ПАВ
Из применяемых на практике ПАВ анионные по объемам производства значительно превосходят все остальные. Наиболее важные из них:
Мыла (соли высших жирных кислот) – RCOO-Me+. Например, мыла натриевые, кальциевые синтетических жирных кислот (смесь кислот с nc в составе R от 5 до 25) нашли применение в средствах антикоррозионной защиты металлов, для приготовления консистентных смазок, добавок к дорожным битумам.
Асидол (смесь свободных нефтяных кислот) - RCOOH. Асидол-мылонафт (смесь свободных нефтяных кислот и их натриевых
солей). Эти соединения применяются как антисептики для пропитки шпал, деэмульгаторы и пластификаторы.
Алкилсульфаты (соли алкилсерных кислот) - ROSO3Na. Это сложные эфиры высших спиртов и серной кислоты, нейтрализованные щелочью.
Триэтаноламинсульфаты (ТЭАС) - CnH2n+1O–SO3NH(C2H4OH)3,
где n = 10 – 18; |
|
Прогресс (натриевые |
соли вторичных алкилсульфатов на основе |
α-олефинов) - |
|
CnH2n+1–CH–OSO3Na, |
где n = 6 – 16. |
CH3
Это название, как и многие другие, легче понять, исходя из способа получения соединения:
R–CH=CH2 + H2SO4→R–CH–SO3H NaOH |
R–CH–OSO3Na + H2O. |
α–олефин |
|
CH3 |
CH3 |
ПАВ этого типа используются как смачиватели при изготовлении бетона, вспениватели при производстве пенобетона, обезжириватели металлических поверхностей, диспергаторы при производстве латексов.
Неонол (алкилполиоксиэтиленсульфаты натрия). Схема его получения:
27

R |
|
OH + mCH2 |
|
|
CH2 |
|
|
R |
|
O |
|
(CH2 |
|
CH2 |
|
O)m |
|
H |
|
|
|
|
|
|||||||||||
|
O |
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
+ SO3 |
RO |
|
(CH |
|
CH2 |
|
O)mSO3H + NaOHR |
|
|
O |
|
|
|
(CH2 |
|
CH2 |
|
O) |
SO Na, |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
3 |
|
где R=СnH2n+1, n=10 – 13, m = 3.
Данное ПАВ используется как пенообразователь, диспергатор, смачиватель.
Сульфонаты (соли алкил- и алкилароматических сульфокислот) – RSO3Na. При производстве этих ПАВ используются самые различные
углеводороды или их производные, которые сначала сульфируются, а затем нейтрализуются щелочами.
Сульфонол (натрий алкилбензолсульфонаты) – CnH2n+1C6H4SO3Na, где n = 12-18, или
R
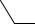 SO3Na.
SO3Na.
Некаль (смесь натрий моно-, ди- и трибутилнафталинсульфонатов) - (C4H9)nC10H6SO3Na, где n = 1 – 3
R |
SO3Na |
|
. |
Катионные ПАВ
Это в основном амины и их соли, а также соли азотсодержащих гетероциклов.
Триалкиламин – (CnH2n+1)3N, где n = 7 – 9. Используется как ингибитор коррозии в кислых средах, флотореагент, экстрагент цветных металлов,
фобизатор и пленкообразователь.
Пеназолин 17-20 (смесь имидазолинов и аминоамидов с алкильным радикалом):
|
|
|
|
амид |
амино |
|
алкил |
||||||||||
|
NH + R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
CO |
|
|
|
|
|
NH |
|
|
|
|
CnH2n+1 |
|
, n = 17 - 20 . |
|
|
|
|
NH |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||||||
|
C |
|
|
|
|
|
|
|
|
|
|
||||||
R
имидазолин
28
Пеназолины - прекрасные эмульгаторы и пенообразователи в кислых средах, эмульгаторы асфальта, ингибиторы коррозии, гидрофобизаторы цемента, бетона.
Неионогенные ПАВ
Это сложные эфиры высших жирных кислот, многоатомных спиртов или продукты взаимодействия оксида этилена со спиртами, кислотами, аминами, фенолами и другими соединениями, имеющими подвижный атом водорода.
Стеарат сахарозы (смесь сложных эфиров сахарозы и стеариновой кислоты) – C12H14O3(OH)6(OOCC17H35)2. Используется как добавка к мою-
щим веществам, антивспенивающая и антикоррозионная добавка, присадка к смазочным маслам.
Синтанол ДС-10 (моноалкиловые эфиры полиэтиленгликоля на осно-
ве первичных жирных спиртов) – CnH2n+1O(C2H4O)mH, где n = 10 – 18, m = 8 – 10.
ОП-7 и ОП-10 (моноалкилфеноловые эфиры полиэтиленгликоля) –– CnH2n+1C6H4O(C2H4O)mH, где n = 8-10, m = 7-10. Это замечательный эмуль-
гатор, смачиватель, компонент моющих обезжиривающих композиций, стабилизатор глинистых дисперсий.
Синтамид-10 (полиэтиленгликолевые эфиры моноэтаноламидов син-
тетических жирных кислот)- |
CnH2n+1CONH–CH2–CH2–O(C2H4O)mH, |
где n = 10 – 16, m = 10. Используется |
как смачиватель, эмульгатор, стабили- |
затор пены, компонент моющих композиций.
Высокомолекулярные ПАВ
Наибольшее распространение получили ПАВ на основе целлюлозы. КМЦ – карбоксиметилцеллюлоза (натриевая соль продукта этерифи-
кации целлюлозы монохлоруксусной кислотой)
[-C6H7O2(OH)3-m(OCH2COONa)m-]n, где n = 500, m = 1-3.
Применяется для увеличения сроков схватывания бетонной смеси, вместе с другими компонентами повышает прочность, водонепроницаемость и морозостойкость изделий из бетона, в сочетании с латексами и ПВА используется для улучшения свойств минераловатных плит.
О - Этилцеллюлоза ЛК (неионогенное ПАВ – простой эфир целлюлозы и этилового спирта) – [-C6H7O2(OH)3-m(OC2H5)m-]n, где m = 2-3. Это адгезионная добавка к пластмассам, лакам, краскам, эмалям, пленкам.
ГКЖ – 94 - (моноэтилсилоксан) [-(C2H5)SiH-O-]n, где n = 9-14. Это прекрасный гидрофобизатор, пеногаситель.
29

Подводя итог, можно отметить, что химическое название ПАВ нередко дает возможность понять не только строение, но и метод производства, а последнее, в свою очередь, определить класс и принцип действия вещества.
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ (ВМС)
Все высокомолекулярные соединения по строению основной цепи делятся на два больших класса:
1. Высокомолекулярные соединения, основная цепь которых построена из одинаковых атомов, например, из атомов углерода (карбоцепные полимеры):
... C C C C C C C C C C ...
или
...










 ...
...
Атомы углерода основной цепи могут быть связаны с водородом или с какими-либо другими атомами или группами.
Из природных органических полимеров к карбоцепным относятся натуральный каучук, а из неорганических – все модификации элементарного углерода (аморфный углерод, графит, алмаз). К синтетическим карбоцепным полимерам относятся все высокомолекулярные предельные, непредельные и ароматические углеводороды.
Название карбоцепных полимеров складывается обычно из названия исходного мономера, входящего в качестве элементарного звена в состав макромолекулы полимера, и приставки ПОЛИ-. Например, полимер, полученный из этилена CH2=CH2, называется полиэтиленом; полимер, получен-
ный из винилхлорида CH2=CHCl – поливинилхлоридом; полимер бутадиена CH2=CH–CH=CH2 – полибутадиеном и т.д. Причем название исходного мо-
номера может быть дано по любой номенклатуре.
Если полимер получен в результате совместной полимеризации нескольких разных мономеров, то в названии сополимера отражается название каждого из них. Например:
1,3-бутадиен |
стирол |
полибутадиенстирол
30
