
- •Сборник задач и методические указания
- •140400.62 “Электроэнергетика и электротехника”
- •Контрольная работа №1
- •2.1. Механика
- •2.1.1. Основные законы и формулы
- •2.1.2. Примеры решения задач по механике
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Контрольная работа №2
- •3.1. Молекулярная физика и термодинамика
- •3.1.1. Основные законы и формулы
- •3.1.2. Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •3.2. Электростатика
- •Основные законы и формулы
- •3.2.2. Примеры решения задач
- •Решение
- •Решение
- •Решение
- •3.3. Постоянный электрический ток
- •3.3.1. Основные законы и формулы
- •3.3.2. Примеры решения задач
- •Решение
- •Решение
- •Решение
- •4. Задачи для контрольных заданий
- •86. Азот находится при нормальных условиях. Найти:
- •5. Варианты контрольных работ
- •5.1. Контрольная работа №1 Механика
- •5.2. Контрольная работа №2 Молекулярная физика. Электростатика. Постоянный ток
- •Приложение
- •Основные физические постоянные Плотности ρ газов
- •Диэлектрическая проницаемость ε
- •Удельное сопротивление ρ и температурный коэффициент α проводимости
- •Библиографический список
- •140400.62 “Электроэнергетика и электротехника”
- •Составители:
- •394026 Воронеж, Московский просп.,14
- •140400.62 “Электроэнергетика и электротехника”
Решение
Для решения задачи удобно воспользоваться распределе- нием молекул по относительным скоростям u:
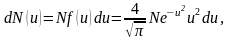
где
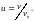
Так
как часть молекул обладает скоростями
превышающими vв,
а часть
меньшими, чем νв,
то

Наиболее вероятная скорость при Т = 900 К
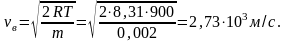
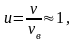
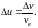
Отсюда
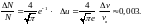
Пример
6. Найти
среднюю продолжительность
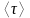 свобод-
ного пробега молекул кислорода при
температуре Т=250
К
и давлении P
=100 Па.
свобод-
ного пробега молекул кислорода при
температуре Т=250
К
и давлении P
=100 Па.
Решение
Средняя продолжительность свободного пробега молекул – величина, обратная среднему числу столкновений, происходящих за 1 секунду:
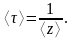
Так
как
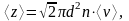 то
то
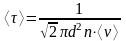 .
.
Здесь
n
– концентрация молекул кислорода,
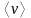 - средняя арифметическая скорость
молекул кислорода.
- средняя арифметическая скорость
молекул кислорода.
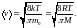
Из
уравнения состояния идеального газа
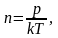
тогда
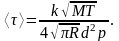
Эффективный
диаметр молекул кислорода (величина
справочная) d
= 0,36 нм
=
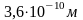 .
После подстановки числовых значений
получим
.
После подстановки числовых значений
получим
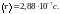
Пример 7. Определить отношение удельных теплоём- костей для смеси газов, содержащей гелий массой m1=8 г и водород массой m2 = 2 г.
Решение
Для
нагревания смеси газов массой
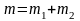 на T
при постоянном объёме ей необходимо
сообщить количество теплоты
на T
при постоянном объёме ей необходимо
сообщить количество теплоты
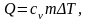 где
где
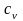 -
удельная теплоёмкость смеси.
-
удельная теплоёмкость смеси.
Часть
этого количества теплоты,
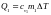 пойдёт на нагревание гелия, другая часть
пойдёт на нагревание гелия, другая часть
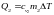 - на нагревание водорода.
Тогда
- на нагревание водорода.
Тогда
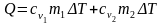 ,
,
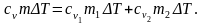
Отсюда
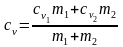 .
.
Аналогично находим ср смеси:
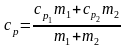 .
.
Здесь
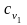 ,
,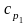 и
и
 ,
,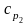 -
удельные теплоёмкости гелия и водорода
соответственно:
-
удельные теплоёмкости гелия и водорода
соответственно:
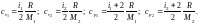
Так как гелий – газ одноатомный, то i1=3, водород – газ двухатомный, следовательно, i2=5.
Отношение удельных теплоёмкостей:
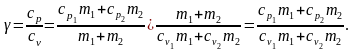
Подставляя выражение для удельных теплоёмкостей, получим:
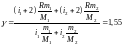 .
.
Пример 8. В цилиндре под поршнем находится водород массой m = 0,02 кг при температуре Т1 = 300К. Водород сначала расширялся адиабатно, увеличив свой объём в n1=5 раз, а затем был сжат изотермически, причём объём газа уменьшился в n2 =5 раз. Найти температуру в конце адиабатического расширения и работу, совершаемую газом при этих процессах. Изобразить процесс графически.
Решение
Температуры и объёмы газа, совершающего адиабатный процесс, связаны между собой соотношением
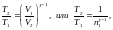
где
γ
– отношение теплоёмкостей газа при
постоянном давлении и постоянном объёме;
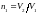 .
.
Отсюда получаем следующее выражение для конечной температуры
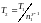 .
.
Работа газа при адиабатном расширении может быть определена по формуле
 ,
,
где СV – молярная теплоёмкость газа при постоянном объёме.
Работа А2 газа при изотермическом процессе может быть выражена в виде
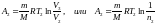 ,
,
г де
n2=V2/V3.
де
n2=V2/V3.
Произведём вычисления, учитывая что для водорода как двухатомного газа γ=1,4, i=5 и M=2·10-3кг/моль, получим
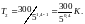
Так как 50,4=1,91 (находится логарифмированием), то
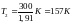 .
.
Тогда
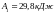 ;
;
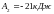 .
.
Знак минус показывает, что при сжатии работа газа совершается над внешними силами. График процесса представлен на рисунке.
Пример 9. Вычислить КПД цикла, состоящего из изобарного, адиабатного и изотермического процессов, если в результате изобарного процесса газ нагревается от Т1=300 К до Т2=600 К.
