
- •150104, 150702, 200503, Направления 223200
- •Содержание
- •9. Лабораторная работа №7. Определение константы скорости инверсии сахара………………………………………………....31
- •Поверхностные явления лабораторная работа № 1 адсорбция уксусной кислоты углем
- •Цель работы – изучение зависимости величины адсорбции уксусной кислоты от ее концентрации, построение изотермы адсорбции и определение постоянных a0 и b в уравнении Ленгмюра. Порядок выполнения работы
- •Лабораторная работа № 2 определение поверхностного натяжения жидкостей
- •Электролиты
- •Электропроводность электролитов
- •Кондуктометрическое титрование
- •Электродвижущие силы
- •Кинетика химических реакций
- •Определение константы скорости реакции омыления уксусно-этилового эфира
- •Определение константы скорости инверсии сахара
- •394026 Воронеж, Московский просп., 14
- •Методические указания
Лабораторная работа № 2 определение поверхностного натяжения жидкостей
Существование молекулярного поверхностного слоя приводит к тому, что увеличение поверхности требует затраты работы. Величина этой работы, отнесенная к единице поверхности, получила название коэффициента поверхностного натяжения.
Одним из способов определения поверхностного натяжения жидкостей является измерение давления образования пузырьков воздуха внутри жидкости. Если трубку с капиллярным кончиком опустить в жидкость и создать разность между давлениями воздуха внутри трубки и вне ее, то по мере увеличения этой разности у кончика капилляра будет образовываться пузырек воздуха. Сила поверхностного натяжения будет препятствовать образованию этого пузырька. Чтобы пузырек смог преодолеть эту силу и оторваться от кончика трубки, давление должно достигнуть некоторой вполне определенной величины.
Если трубку погрузить в жидкость с другим коэффициентом поверхностного натяжения, то необходимое для отрыва пузырька давление будет иметь другую величину. Отношение максимального давления P1 в первом случае к максимальному давлению P2 во втором случае равно отноше-
нию коэффициентов поверхностного натяжения первой 1 и второй 2 жидкостей:
![]() . (1)
. (1)
Если
известен коэффициент поверхностного
натяжения одной из жидкостей, то можно
вычислить его для другой жидкости. Для
многих жидкостей коэффициенты
поверхностного натяжения известны.
Например, коэффициент поверхностного
натяжения чистой воды при 20 C
равен 7,28мкДж/см2 (![]() н/м).
н/м).
Вода является сильно полярным веществом. Если добавлять к ней менее полярные вещества, то наблюдается адсорбция их на границе воды с воздухом. Концентрируясь на поверхности воды, эти вещества понижают ее поверхностное натяжение. Такие вещества называют поверхностно-активными. Различные поверхностно-активные вещества в различной степени понижают поверхностное натяжение. Чем активнее вещество, тем при определенной концентрации оно больше понижает поверхностное натяжение.
Адсорбция поверхностно активного вещества на данной поверхности раздела находится в линейной зависимости от его поверхностной активности, как это видно из формулы Гиббса:
![]() ,
(2)
,
(2)
где Г – адсорбция; с
– концентрация поверхностно-активного
вещества, моль/л; R –
универсальная газовая постоянная; T
– абсолютная температура;
![]() – поверхностная активность.
– поверхностная активность.
Цель работы – ознакомление с одним из методов определения поверхностного натяжения жидкостей. Исследование влияния концентрации поверхностно-активных веществ на величину поверхностного натяжения.
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
Д
Рис. 1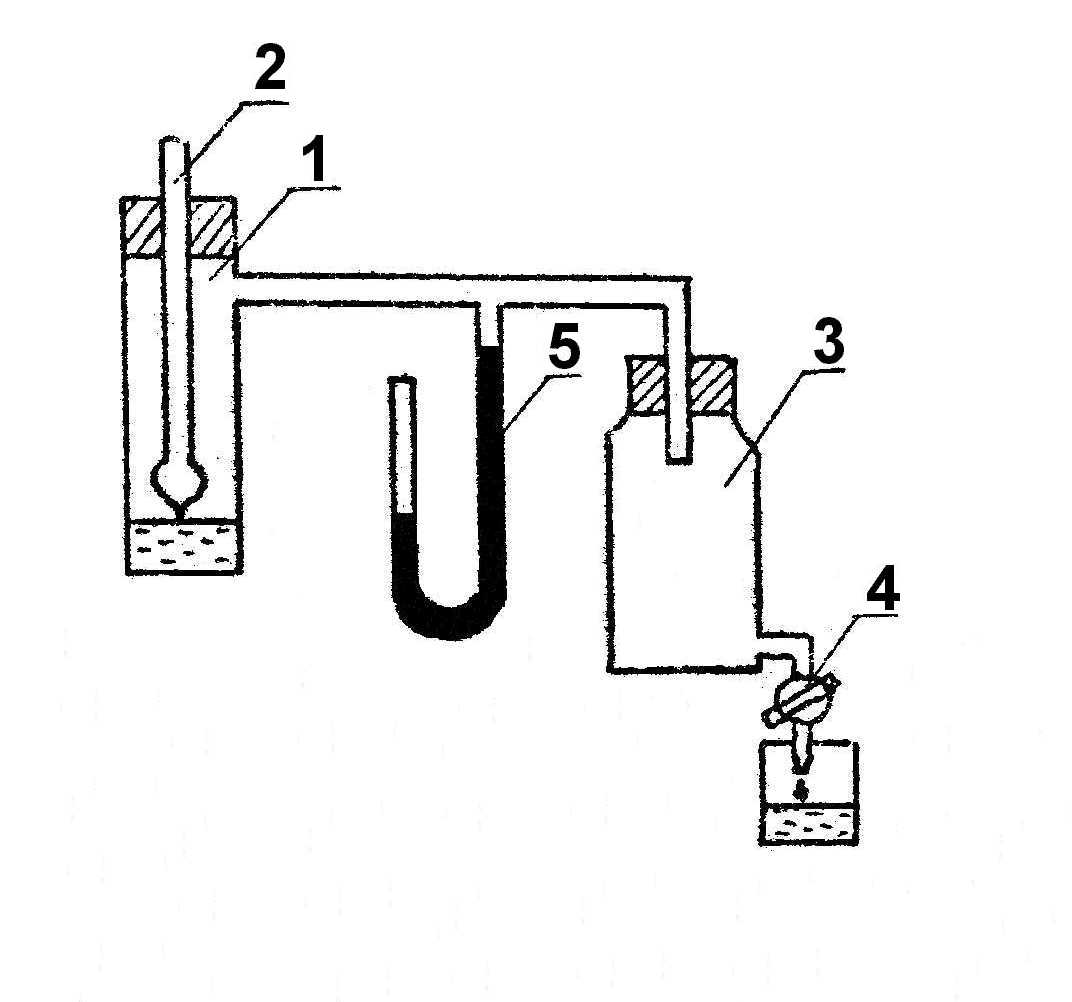
![]() .
.
Далее для опыта готовят водные растворы поверхностно-активного вещества (спирта, карбоновой кислоты, ацетона, и др.) следующих концентраций: 1; 0,5; 0,25; 0,125; 0,0625 М путем последовательного разбавления исходного 1 М раствора
помощью двух мерных
колб на 50 мл и мерной пипетки на 25 мл.
Налить в первую мерную колбу 25 мл
исходного 1 М раствора поверхностно-активного
вещества и до метки добавить воды.
Полученный 0,5 М раствор взболтать и
отобрать пипеткой 25 мл его в другую
мерную колбу для последующего разбавления,
а с оставшейся половиной раствора
проводить исследование и т.д. Пробирку
тщательно ополоснуть испытуемым
раствором, затем налить такое количество
его, чтобы кончик капилляра только
слегка касался жидкости, и измерить
давление, как указывалось выше, для всех
пяти концентраций, снимая по 8 – 10
значений для каждого раствора. Определив
среднее значение максимальной разности
давления в момент отрыва пузырька
воздуха для всех растворов (P2),
также зная величины P и
для воды, по соотношению (1) находят
коэффициенты поверхностного н
Рис.2.
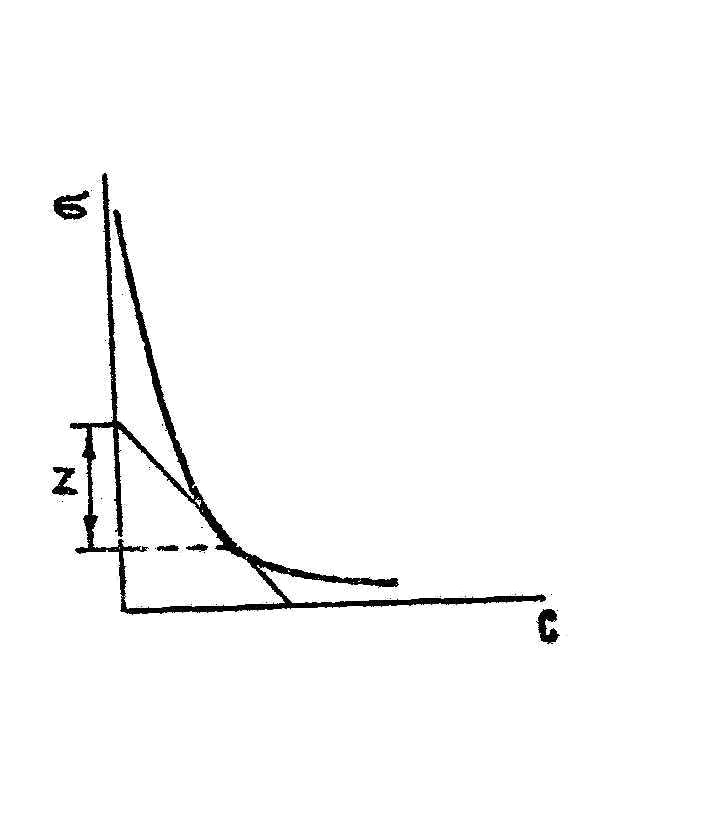 атяжения
этих растворов. Пользуясь таблицей,
составленной из вычисленных коэффициентов
поверхностного натяжения и соответствующих
им концентраций растворов, строят график
= f(c).
Этот график дает возможность определить
величину
для раствора любой к
атяжения
этих растворов. Пользуясь таблицей,
составленной из вычисленных коэффициентов
поверхностного натяжения и соответствующих
им концентраций растворов, строят график
= f(c).
Этот график дает возможность определить
величину
для раствора любой к![]() ,
так как согласно построению
,
так как согласно построению
![]() .
Подставив значение Z =
.
Подставив значение Z =
![]() в уравнение Гиббса (2), получим формулу
для расчета адсорбции поверхностно-активного
вещества на границе раздела раствора
с воздухом: Г = Z/RT.
Сделав такие вычисления для всех
исследованных концентраций, строят
кривую зависимости адсорбции от
концентрации Г = f(с)
и делают вывод о характере адсорбции
поверхностно-активного вещества.
в уравнение Гиббса (2), получим формулу
для расчета адсорбции поверхностно-активного
вещества на границе раздела раствора
с воздухом: Г = Z/RT.
Сделав такие вычисления для всех
исследованных концентраций, строят
кривую зависимости адсорбции от
концентрации Г = f(с)
и делают вывод о характере адсорбции
поверхностно-активного вещества.
КОНТРОЛЬНЫЕ ВОПРОСЫ
по теме “Поверхностные явления. Адсорбция”
Что понимают под адсорбцией?
Какова природа адсорбционных сил?
Что называется физической, химической адсорбцией?
Как зависит величина адсорбции от давления или концентрации адсорбируемого вещества? Уравнение Ленгмюра. Уравнение Фрейндлиха.
Что понимают под предельной адсорбцией?
Какие величины и как определялись в работе “Адсорбция уксусной кислоты углем”?
Что такое капиллярная конденсация?
Что такое поверхностное натяжение? В каких единицах выражается коэффициент поверхностного натяжения?
Адсорбционная формула Гиббса. Какие вещества называются поверхностно-активными и инактивными?
Как зависит коэффициент поверхностного натяжения от концентрации поверхностно-активного вещества?
Какова зависимость адсорбции от температуры, от поверхностной активности ?
