
- •О.Б. Кукина, о.Р. Сергуткина, д.В. Федосов химические и физико-химические методы исследования.
- •Оглавление
- •Введение
- •Порядок выполнения лабораторных работ и правила работы в химической лаборатории
- •Химическая идентификация и количественный анализ
- •Классификация методов исследования строительных материалов
- •Работа 2. Исследование физико-химической активности поверхности кремнеземсодержащих материалов фотоколориметрическим методом
- •2.4. Рабочее задание
- •Работа 3. Разработка методики определения рН водной вытяжки из камня строительных материалов
- •Вопросы для подготовки к занятию
- •3.4. Рабочее задание
- •Приложение 1
- •Приложение 2
- •Приложение 3
- •Библиографический список рекомендуемой литературы
- •Заключение
- •Химические и физико-химические методы исследования
- •270106 «Производство строительных материалов, изделий и конструкций»
- •394006 Воронеж, ул. 20-летия Октября, 84
Работа 2. Исследование физико-химической активности поверхности кремнеземсодержащих материалов фотоколориметрическим методом
2.1. Цель работы
Усвоить сущность оптических спектроскопических методов исследования состава и свойств строительных материалов.
Овладеть техникой фотоколориметрического анализа и оценкой физико-химической активности поверхности кремнеземсодержащих строительных материалов.
Провести компьютерную обработку результатов эксперимента.
2.2. Подготовка к работе
УСВОИТЬ ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Спектроскопия базируется на квантовой теории, согласно которой атому или молекуле в стационарном состоянии соответствует некоторая последовательность энергетических уровней. Переход частицы из одного состояния в другое сопровождается испусканием или поглощением кванта электромагнитного излучения, которое регистрируется соответствующими приборами в виде спектра.
В оптических спектроскопических методах исследования изучаются спектры электромагнитного излучения длиной волны 10-8…10-3 м, которое испускается, поглощается или рассеивается веществом. Абсорбционный анализ - это анализ по поглощению света в видимой, ультрафиолетовой и инфракрасной областях спектра. На поглощении света в видимой части cпектра истинными растворами основаны фотоколориметрия и спектрофотометрия; взвесями - турбидиметрия, на рассеянии света взвесями - нефелометрия.
Сущность атомно-абсорбционной спектроскопии основана на том, что при взаимодействии со световой энергией в атомах поглощающего вещества происходит переход валентных электронов на более высокие энергетические уровни. Электронные переходы, вызванные поглощением строго определенных квантов световой энергии, характеризуются наличием строго определенных полос поглощения в спектрах. Фотометрические методы анализа, к которым относятся фотоколориметрия и спектрофотометрия, применяются для изучения состава и свойств строительных материалов. Прибор для проведения исследования содержит пять основных узлов:
1) источник излучения;
2) монохроматор, где выделяется длина волны, при которой происходит наиболее интенсивное поглощение;
3) исследуемый образец;
4) приёмник излучения;
5) устройство, регистрирующее спектр.
В фотоколориметрии проводится сравнение интенсивности окраски исследуемого и стандартного (с точно известной концентрацией) растворов. Основные узлы фотоэлектроколориметра представлены на рис. 4.

Рис. 4 Схема основных узлов фотоэлектроколориметра
Основной закон фотометрии устанавливает зависимость уменьшения интенсивности монохроматического светового потока It , прошедшего через слой окрашенного раствора концентрацией с и толщиной l, от интенсивности падающего света I0 .
It = I0 · 10 -ε l C , (4)
где ε - молярный коэффициент поглощения раствора концентрации 1моль/дм3, зависящий от длины волны падающего света, природы растворенного вещества, температуры.
Преобразуем уравнение (4), взяв отношение I0 : It и прологарифмировав обе части уравнения
(I0 : It) = 10 ε l C ; lg ( I0 : It ) = lg ( 10 ε lC )
Отношение (I0 : It) = D называется оптической плотностью. В результате преобразования выражения (3) получим
D = ε l C, (5)
откуда следует, что оптическая плотность прямо пропорциональна концентрации окрашенного вещества и толщине поглощающего слоя.
Зависимость (5) использована для разработки методов фотометрических исследований. В методе сравнения измеряют оптическую плотность исследуемого раствора и стандартного с известной концентрацией. Затем вычисляют концентрацию исследуемого раствора.
![]() (6)
(6)
Пример 4. Для определения железа в воде фотоколориметрическим методом в мерную колбу емкостью 50,0 см3 ввели 10,0 см3 стандартного раствора железа (ТFe3+ = 0,01000 мг/см3), во вторую колбу такой же емкости – 25,0 см3 исследуемой воды. После добавления соответствующих реактивов и доведения объёма раствора до 50,0 см3 были определены оптические плотности растворов на КФК-2: D1=0,26; D2 = 0,42. Вычислите содержание железа в воде в мг/дм3.
Решение. Рассчитаем концентрацию стандартного раствора железа в колбе для фотоколориметрирования
![]()
В данном исследовании использован метод сравнения и концентрация исследуемого раствора вычисляется по формуле (5)
![]()
![]()
В колбе для фотоколориметрирования анализируемая вода была разбавлена в два раза, поэтому содержание железа - 6,462 мг/дм3.
Упражнение 4. Для определения содержания в воде железа в двух мерных колбах емкостью 50,0 см3были приготовлены стандартный и исследуемые растворы. Для приготовления стандартного раствора взяли 8,0 см3 раствора соли железа (ТFe3+=0,01000 г/см3), а для приготовления исследуемого – 25,0 см3 воды. После добавления соответствующих реактивов до 50 см3 оптической плотности растворов определили на фотоколориметре: DСТ = 0,65; DИССЛ = 0,62. Вычислите концентрацию железа в исследуемой воде в мг/дм3.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Метод построения калибровочного графика более длителен, но в нем меньше случайных ошибок. В соответствии с основным законом фотометрии (5) график в координатах; концентрация - оптическая плотность должен быть линеен и прямая должна проходить через начало координат. Калибровочный график строят по нескольким растворам с точно известной концентрацией.
Пример 5. С целью изучения активности кремнеземсодержащих строительных материалов по отношению к щелочной среде получили данные для построения калибровочной кривой (рис. 5).
Концентрация стандартного раствора SiO2, мг / дм3 |
Оптическая плотность, D |
0,05 |
0,10 |
0,30 |
0,17 |
0,50 |
0,30 |
0,70 |
0,39 |
0,90 |
0,53 |

Р ис.5.
Калибровочный график зависимости
оптической плотности
ис.5.
Калибровочный график зависимости
оптической плотности
от концентрации стандартного раствора SiO2
Навески кварцевого песка различной степени дисперсности и массой 1,0000 г залили 100 cм3 раствора соды, в котором происходят следующие реакции:
Nа2СО3 + 2 Н2О ↔ 2 NаОН + Н2СО3,
SiO2 + 2 NаОН ↔ Nа2SiO3 + Н2О,
в результате чего песок частично переходит в раствор.
В течение 1,5 ч суспензии периодически встряхивали, затем пипеткой взяли по 10 cм3 отфильтрованной жидкой фазы, приготовили растворы для фотоколориметрирования и определили оптическую плотность
Проба S, м2/г D
1 0,05 0,20
2 0,20 0,24
3 0,40 0,28.
Определите массу SiO2 (мг) перешедшую в раствор с I г песка и с I м2 поверхности.
Решение. По калибровочной кривой (рис. 4) найдем концентрацию SiO2:
проба I ─ 0,33 мг/дм3, проба 2 ─ 0,40 мг/дм3, проба 3 ─ 0,48 мг/дм3.
Эти результаты соответствуют массе SiO2, перешедшей в раствор с одной десятой части анализируемой пробы, т.к. для фотоколориметрирования из 100 см3 отфильтрованной жидкой фазы брали только 10 см3. Поэтому с I г песка в раствор переходит соответственно: 3,3; 4,0; 4,8 мг/г. Эти результаты соответствуют активности единицы массы песка.
Площадь поверхности первой пробы 0.05 м2/г. С этой поверхности в раствор переходит 0,33 мг песка, а с 1м2 навески в раствор перейдёт 6,60 мг песка:
0,05 м2 ─ 0,33 мг;
1,00 м2 ─ 6,60 мг.
Для второй и третьей проб с удельной поверхностью 0,20 и 0,40 м2 / г в раствор перейдёт соответственно 2,00 и 1,20 мг/г песка, что соответствует активности единицы площади песка.
Полученные данные представим графически (рис. 6).

Рис. 6. Зависимость активности кварцевого песка от степени дисперсности
Как следует из полученных данных, с увеличением степени дисперсности удельная активность массы песка увеличивается, а удельная активность поверхности песка уменьшается.
Упражнение 5. С целью определения растворимости силикатной составляющей перлита получили данные для построения калибровочной кривой (рис. 7).
Концентрация стандартного раствора в пересчете на SiO2, мг/дм3 |
Оптическая плотность, D |
0,2 |
0,03 |
0,4 |
0,07 |
0,6 |
0,10 |
0,8 |
0,14 |
1,0 |
0,17 |
1,2 |
0,21 |
Навески перлита массой 1,000 г взболтали с 100 см3 воды и оставили на хранение при температуре 250С. Через 1; 7 и 14 сут отбирали по 10 см3 и определяли оптическую плотность, данные по которой представлены в табл. 6. По калибровочному графику найдите концентрацию в мг/дм3, пересчитайте на растворимость SiO2 в мг/г и мг/м2 и сделайте вывод, как изменяются эти величины в зависимости от степени дисперсности перлита и длительности взаимодействия с водой. Значения растворимости (мг/г и мг/м2) в зависимости от степени дисперсности через 1, 7, 14 суток представьте так же в виде рис. 7.

Р ис. 7. Калибровочный график зависимости оптической плотности
от концентрации стандартного раствора в пересчёте на SiO2
Таблица 6
Влияние степени дисперсности перлита и времени его контакта с водой
на растворимость силикатной составляющей
Степень дисперсности, S, м2/г |
Оптическая плотность через сутки |
Растворимость перлита через сутки |
|||||||
1 |
7 |
14 |
|||||||
1 |
7 |
14 |
мг/г |
мг/м2 |
мг/г |
мг/м2 |
мг/г |
мг/м2 |
|
0,1 |
0,03 |
0,05 |
0,06 |
|
|
|
|
|
|
0,3 |
0,08 |
0,15 |
0,17 |
|
|
|
|
|
|
0,5 |
0,15 |
0,21 |
0,23 |
|
|
|
|
|
|
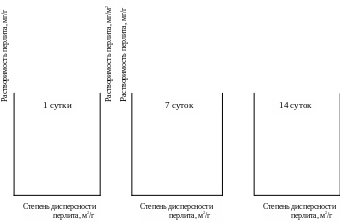
Рис. 8. Зависимость силикатной составляющей перлита от степени дисперсности
и времени контакта с водой
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Вопросы для подготовки к занятию
Классификация и назначение главных спектроскопических методов исследования, применяемых для исследования состава, структуры и свойств строительных материалов.
Атомно-абсорбционная спектроскопия, происхождение спектров поглощения.
Основной закон фотометрии, оптическая плотность.
Методы, аппаратура и условия проведения фотоколориметрических исследований (ошибки фотометрии).
Литература: [3 ─ гл. 3; 4 ─ 7.1, 7.2, 7.4]
2.3. Оборудование, химическая посуда, реактивы
Весы технохимические, аналитические, фотоколориметр КФК – 2..
Мерные колбы, плоскодонные колбы, бюретка, цилиндры, воронки, пипетки.
Растворы силиката натрия и молибдата аммония, карбоната натрия, аскорбиновая и лимонная кислота.
Персональный компьютер, принтер.
