
- •ЛЕКЦИЯ 4(дистанционно)
- •1. Строение, классификация и номенклатура комплексных соединений(КС).
- •Биолиганды:
- •n- координационное число -
- •Дентантность – число связей, образуемых лигандом и комплексообразователем
- •Вернер Альфред (12.XII.1866–15.XI.1919)
- •Изомерия КС:
- •Классификация и номенклатура комплексных соединений
- •• III тип: наиболее распространена классификация по
- •Комплекс называется следующим образом:
- •2. Химическая связь и свойства комплексных соединений (КС)
- •Метод валентных связей
- •Теория кристаллического поля
- •Типы электроных переходов при поглощении света
- •1,10- Фенантролин
- •Изомерия КС:
- •Теория Льюиса
- •Свойства КС
- •Свойства КС
- •КС в аналитической химии
- •Дентантность – число связей, образуемых лигандом и комплексообразователем
- •Аффинная хроматография
- •3. Комплексные соединения в диагностике
- •Аффинная хроматография

1,10- Фенантролин

Изомерия КС:
Гидратная (ионизационная, координационная)
[Cr(H2O)6]Cl3 – трихлорид гексааквахрома (III) – фиолетового цвета,
λ = 400 – 450 нм
[CrCl(H2O)5]Cl2∙H2O – моногидрат дихлорид пентааквахлорохрома (III)
– сине-зеленого цвета,
[CrCl2(H2O)4]Cl∙2H2O – дигидрат хлорид тетрааквадихлорохрома (III)
– зеленого цвета.
λ = 510 – 580 нм

Теория Льюиса
Кислота Льюиса – вещество, способное принять электронную пару от основания.
Основание Льюиса – вещество, обладающее электроной парой.
Устойчивые комплексы образуются:
между жёстким КО и жёстким L
или
между мягким КО и мягким L
«МЯГКИЕ» - легко поляризуемые КО и L( большим радиусом и числом электронов)

Свойства КС
1)КС в водных системах- ист.р-ры, ГДС,КДС. Истинные растворы – диссоциируют:
[Ag(NH3)2]Cl = [Ag(NH3)2]+ + Cl–
[Ag(NH3)2]+ Ag+ + 2NН3
закон действующих масс:
Kн [Ag ][NH3]2 6 10 8 [[Ag(NH3)2] ]
Константа диссоциации — это константа нестойкости: чем меньше константа ионизации, тем устойчивее комплекс.
Kуст [[Ag(NH3 )2 ] ] [Ag ][NH3 ]2



Свойства КС
2) Реакции обмена в водных растворах протекают в направлении более прочного связывания ионов
образуется более прочная связь лигандов новым КОобразуется более прочная связь КО с новым лигандом
3) Окислительно- восстановительные реакции
изменяется степень окисления КО;
изменяется потенциал окислителя;
изменяется потенциал восстановителя
4)Кислотно-основные свойства:за счет ионов внешней сферы;за счет диссоциации лигандов
5)КС влияют на состояние гомо- гетерогенных системрастворяют осадки;образуют осадки

КС в аналитической химии
Определение кальция в растворе
[МеJnd] + (Н2ТрБ)2- |
|
[MeTрБ]2- + Jnd2- + 2 Н+ |
|
5 мл аммиачного буфера
Кристаллы индикатора (хромоген черный)
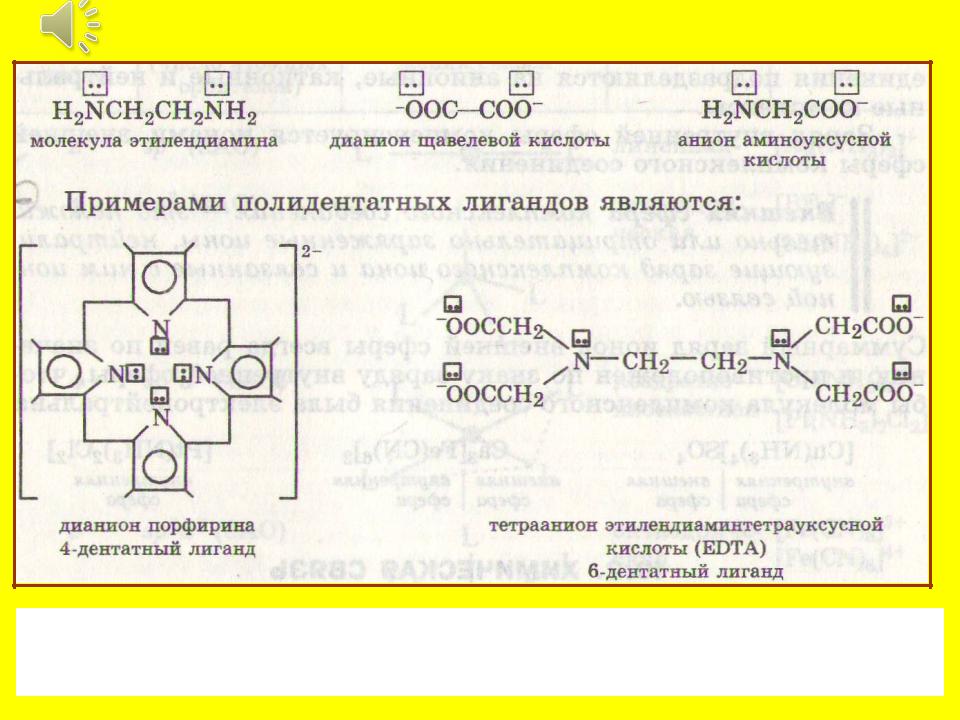
Дентантность – число связей, образуемых лигандом и комплексообразователем

