
- •Вопрос 121 Ферменты в медицине и фармацевтической промышленности. Преимущества иммобилизованных ферментов, способы иммобилизации. Иммобилизация целых клеток
- •2. Применение ферментов в качестве лс (энзимотерапия):
- •3. Использование ферментов в лабораторной диагностике:
- •Вопрос 122 Биохимические основы фармакокинетики лекарственных средств. Всасывание, метаболизм, распределение и выделение лекарственных препаратов. Пролекарства
- •2. Повышение активности лекарств
- •3. Изменение фарм. Действия:
Вопрос 121 Ферменты в медицине и фармацевтической промышленности. Преимущества иммобилизованных ферментов, способы иммобилизации. Иммобилизация целых клеток
В медицине ферменты используются:
В энзимодиагностике
В энзимотерапии
В лабораторной диагностике
1. Энзимодиагностика заключается в постановке диагноза заболевания на основе
определения активности ферментов в биолог. жидкостях человека.
Принципы энзимодиагностики основаны на следующих позициях:
При повреждении клеток в крови или др. биолог.жидкостях (например, в моче) увеличивается концентрация внутриклеточных ферментов повреждённых клеток;
Количество высвобождаемого фермента достаточно для его обнаружения;
Активность ферментов в биологических жидкостях, обнаруживаемых при повреждении клеток, стабильна в течение достаточно длительного времени и отличается от нормальных значений;
Ряд ферментов имеет преимущественную или абсолютную локализацию в определённых органах (органоспецифичность);
Существуют различия во внутриклеточной локализации ряда ферментов.
Примеры:
Появление в плазме крови ферментов, имеющих только цитозольную
локализацию, свидетельствует о воспалительном процессе. Обнаружение митохондриальных или ядерных ферментов может говорить о некрозе.
Лактатдегидрогеназа (ЛДГ) состоит из 4х субъединиц 2х типов: М (мышца –
muscle) и H (сердце – heart), их комбинации лежат в основе формирования 5 изоформ ЛДГ
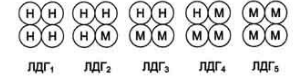
ЛДГ1 и ЛДГ2 активны в сердце и почках, ЛДГ4 и ЛДГ5 – в скелет. мышцах и печени
Изоформы ЛДГ отличаются электрофоретической подвижностью, что позволяет
устанавливать тканевую принадлежность при заболевании, сопровождающемся повышением уровня ЛДГ (при инфаркте миокарда будет повышен уровень ЛДГ1 и ЛДГ2, а при гепатите – ЛДГ5)
Креатинкиназа (КК) – димер, состоящий из субъединиц 2х типов: М (мышца –
muscle) и В (мозг – brain)

При инфаркте миокарда наблюдают изменения в крови активности ферментов,
которые зависят от времени, прошедшего от начала развития инфаркта и от зоны поражения
Почти сразу после закупорки сосуда поднимается уровень КК, который быстро
удаляется из крови (максимум активности – 24ч после инфаркта)
АСТ (аспартатаминотрансфераза) повышается через 4-6ч после начала инфаркта,
максимум активности наблюдается в течении 2-3х дней
Уровень ЛДГ также увеличивается через несколько часов после наступления
инфаркта, максимум активности наблюдают на 3-4 день. Также уровень ЛДГ коррелирует с размерами повреждения сердечной мышцы.
2. Применение ферментов в качестве лс (энзимотерапия):
В качестве заместительной терапии: при заболеваниях ЖКТ, связанных с
недостаточностью секреции пищеварительных соков
Пепсин используют при ахилии, гипо- и анацидных гастритах.
Недостаточность панкреатических ферментов может быть компенсирована
приёмом внутрь препаратов, содержащих основные ферменты поджелудочной железы (фестал, мезим-форте и др.)
В качестве дополнительных терапевтических средств:
Протеолитические ферменты (трипсин, химотрипсин) применяют при местном
воздействии для обработки гнойных ран с целью расщепления белков погибших клеток, для удаления сгустков крови или вязких секретов при воспалительных заболеваниях дыхательных путей.
При тромбозах и тромбоэмболиях используют препараты фибринолизина,
стрептолиазы, стрептодеказы, урокиназы.
Фермент гиалуронидазу (лидазу), катализирующий расщепление гиалуроновой
кислоты, используют для рассасывания рубцов после ожогов и операций (гиалуроновая кислота образует сшивки в соединительной ткани).
Аспарагиназа, катализирующая реакцию катаболизма аспарагина, нашла
применение для лечения лейкозов (лейкозные клетки не могут синтезировать аспарагин и получают его из плазмы крови; если имеющийся в плазме аспарагин разрушать введением аспарагиназы, то в лейкозных клетках наступит дефицит аспарагина и в результате – нарушение метаболизма клетки и остановка прогрессирования заболевания)
