
- •I. Химия белка
- •Функции белков:
- •5. Классификация и характеристика простых белков (альбумины, глобулины, гистоны, протамины, протеиноиды).
- •1. Альбумины
- •2. Глобулины
- •3.Гистоны
- •4.Протамины
- •5.Протеноиды
- •6. Классификация и характеристика сложных белков (липопротсины, хром-мопротеины, нуклеопротеины, гликопротеины, фосфопротеины).
- •II. Ферменты. Витамины.
- •7. Химическая природа ферментов, Активный и аллостерический центры фермента, их роль.
- •8. Виды специфичности ферментов. Основные пути активации и ингибирования ферментативной активности.
- •9. Мультиферментные комплексы и изоферменты. Клиническое значение определения активности изоферментов. Энзимодиагностика. Ферментативные лекарственные препараты.
- •1. Зависимость скорости реакции от температуры
- •2. Зависимость скорости реакции от рН
- •3. Зависимость скорости реакции от концентрации субстрата
- •4. Зависимость от концентрации фермента
- •11. Классификация ферментов. Общая характеристика класса оксидоредуктаз. Основные подклассы. Коферменты оксидоредуктазных реакций.
- •Характеристика фермента
- •12. Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций.
- •13. Классификация ферментов. Общая характеристика гидролаз. Основные подклассы гидролаз.
- •14. Классификация ферментов. Общая характеристика класса лиаз. Коферменты лиазных реакций.
- •15. Классификация ферментов. Общая характеристика изомераз и лигаз. Коферменты изомеразных или глазных реакций.
- •16. Классификация витаминов. Причины развития витаминной недостаточности в организме человека. Авитаминозы, гиповитаминозы, гипервитаминозы, Антивитамины.
- •17. Витамин в1, его химическая структура, признаки витаминной недостаточности. Нарушение углеводного обмена при - витаминной недостаточности.
- •18. Витамины pp и в2, их структура, участие в обмене веществ, признаки витаминной недостаточности.
- •19. Витамины с и р, их структура, признаки витаминной недостаточности и влияние на обмен веществ.
- •20. Витамин биотин, их структура, признаки витаминной недостаточности и участие в обмене веществ.
- •21. Витамин b12, и фолиевая кислота, участие в обмене веществ и признаки витаминной недостаточности.
- •22. Витамины а, е, к. Признаки витаминной недостаточности, участие в обмене веществ.
- •23. Витамин d, химическая природа витамина, гормонально-активные формы, участие витамина в обмене веществ. Рахит. Основные пути метаболизма. БиоэнергетическиЙ обмен.
- •24. Понятие об обмене веществ. Катаболизм и анаболизм, их характеристика и взаимосвязь. Виды метаболических путей. Центральные метаболиты.
- •26. Дыхательная цепь. Ферментные комплексы дыхательной цепи, их локализация. Редокс - потенциалы ферментных систем. Ингибиторы переноса электронов.
- •27. Окислительное фосфорилирование. Значение и механизм процесса. Расообщение дыхания и фосфорилирования. Свободное окисление. Субстратное фосфорилирование.
- •28. Свободнорадикальное окисление. Понятие о перекисном окислении липидов.
- •29. Антиоксидантная система организма. Неферментативные антиоксиданты. Антиоксидантные ферменты.
- •IV. Обмен углеводов.
- •30. Классификация и химическая структура углеводов, их роль в обеспечении жизнедеятельности организма. Переваривание и всасывание углеводов в пищеварительном тракте. Мальабсорбция.
- •32. Структура гликогена и его синтез в клетках печени и мышц. Функциональные отличия гликогена этих тканей. Распад гликогена. Гликогенозы.
- •33. Гликолиз. Биологическое значение, химизм процесса. Необратимые этапы и ключевые ферменты гликолиза. Биоэнергетика и регуляция этого процесса. Эффект Пастера.
- •II этап - окислительное декарбоксилирование пвк
- •III этап - Цикл Кребса
- •35. Апотомический путь обмена глюкозы (пентозный цикл). Окислительная и неокислительная ветви процесса. Биологическое значение пентозного цикла.
- •36. Глюконеогенез. Основные субстраты и ключевые ферменты процесса. Цикл Кори.
- •38. Патология углеводного обмена. Сахарный диабет. Нарушения углеводного и липидного обменов при этом заболевании.
- •V. Обмен липидов
- •39. Классификация и химическая структура липидов. Роль липидов в обеспечении жизнедеятельности организма.
- •40. Биологические мембраны, их структурные компоненты. Функции биологических мембран.
- •41. Холестерин, его биосинтез и биологическая роль. Гиперхолестеринемия. Атеросклероз. Роль липопротеинов в обмене холестерина.
- •1)Наследственная.
- •42. Классификация и химическая структура фосфолипидов. Биологическая роль, переваривание, биосинтез и распад фосфолипидов. Липотропные вещества.
- •43. Переваривание и всасывание липидов, роль желчи в этом процессе. Желчные кислоты. Ресинтез липидов в клетке эпителия кишечника. Транспортные формы липидов. Биологическая роль жировых депо.
- •44. Липолиз триглицеридов в тканях. Окисление глицерина. Биоэнергетика процесса.
- •45. Окисление жирных кислот. Внутриклеточная локализация и биоэнергетика процесса. Особенности обмена жирных кислот с нечетным количеством углеродных атомов и ненасыщенных жирных кислот.
- •46. Синтез жирных кислот. Внутриклеточная локализация, ферменты и коферменты процесса. Биосинтез триглицеридов.
- •47. Образование и распад кетоновых тел. Кетогенез в норме и при патологии.
- •48. Гормональная регуляция липидного обмена. Патология липидного обмена: гиперлипидемии, липоидозы, жировое перерождение печени, ожирение, атеросклероз.
- •3. Конденсация йодтирозинов
- •1. Аминокислоты и их производные:
- •2. Пептиды
1. Аминокислоты и их производные:
(таурин, ДОФАмин, ГАМК, глицин, ацетилхолин, гомоцистеин, адреналин, серотонин, гистамин)
2. Пептиды
•функционируют только в высших отделах нервной системы
•Выполняют одновременно функцию нейромедиаторов и гормонов
•Передают информацию от клетки к клетке по системе циркуляции
Пептиды
•Нейрогипофизарные гормоны (вазопрессин, либерины, статины)
•Опиатоподобные пептиды – эндорфины (вызывают обезболивание, действуя на те же рецепторы, что и опиаты (морфин)
•Пептиды сна
•Пептиды памяти (скотофобин, белок S-100)
Образуются пептиды в результате реакций ограниченного протеолиза, а разрушаются под действием протеиназ.
Энкефалины – эндогенные антистрессовые биорегуляторы обладают отчётливым противошоковым эффектом.
Белки миелиновой оболочки
Основной белок Протеолипидная белковая фракция Кислый протеолипид
Липиды
Находятся в клеточных и субклеточных мембранах нейронов и в миелиновых оболочках. На фосфоглицериды приходится 60% от всех липидов в сером веществе и 40% в белом веществе. В белом веществе холистерина, сфингомиелинов, цереброзидов больше, чем в сером веществе.
Функции липидов нервной ткани
1.Структурная – липиды входят в состав клеточных мембран нейронов
2.Липиды обеспечивают надёжную электрическую изоляцию
3.Защитная – ганглиозиды являются антиоксидантами и защищают ткань мозга при повреждении от перекисного окисления липидов
4.Регуляторная – фосфотидилинозиты являются предшественниками биологически активных веществ
Энергетический обмен головного мозга
Головной мозг хорошо снабжается кровью и имеет интенсивный энергетический обмен. При спокойном состоянии организма мозг утилизирует около 20% поглощенного кислорода и 60% глюкозы, которая полностью окисляется до СО2 и Н2О в цитратном цикле и путем гликолиза.
В клетках головного мозга практически единственным источником энергии, который должен поступать постоянно, является глюкоза. Только при продолжительном голодании клетки начинают использовать дополнительный источник энергии — кетоновые тела.
Зависимость головного мозга от глюкозы означает, что резкое падение уровня глюкозы в крови, например, в случае передозировки инсулина у диабетиков, может стать опасным для жизни.
Нейромедиаторы и нейрогормоны
Нейромедиаторы — короткоживущие вещества локального действия; они выделяются в синаптическую щель и передают сигнал соседним клеткам.
Нейрогормоны — долгоживущие вещества дальнего действия, поступающие в кровь. Однако граница между двумя группами достаточно условная, поскольку большинство медиаторов одновременно действует как гормоны.
Химическое строение
Наиболее известным и часто встречающимся нейромедиатором является ацетилхолин, сложный эфир холина и уксусной кислоты. К нейромедиаторам относятся некоторые аминокислоты, а также биогенные амины, образующиеся при декарбоксилировании аминокислот.
Норадреналин действует на адренэргические рецепторы. Повышение цАМФ приводит фосфорилированию белков постсинаптической мембраны
Дофамин, серотонин, ГАМК.
Депрессия связана с недостатком катехоламинов. Нарушение обмена серотонина может быть причиной возникновения психических заболеваний. Острый стресс приводит к снижению серотонина в синаптической щели. При болезни Паркинсона в полосатом теле мозга снижено содержание дофамина.
ГАМК – медиатор торможения. При недостатке ГАМК у детей после рождения возникают судороги.
Глицин – медиатор торможения, подобный ГАМК. Функционирует в синапсах спинного мозга.
93. Биохимия мышечной ткани. Важнейшие белки мышц. Креатин, креатин-фосфат, креатинин, их синтез и биологическая роль.
Белки саркоплазмы миоглобин, белки–ферменты
Белки миофибрилл
Сократительные белки: миозин, актин, актомиозин
Регуляторные белки: тропомиозин, тропонин
Белки стромы эластин, коллаген
Миоглобин
Дыхательный белок мышц.
Гемопротеин
содержит 153 аминокислотных остатка.
Основная функция – перенос кислорода в мышцах.
Состоит из 1 полипептидной цепи, уложенной в пространстве в виде глобулы.
Миозин
Составляет 50 – 55% от массы миофибрилл.
Фибриллярный белок.
Период полураспада – 20 дней.
Состоит из 2 тяжелых цепей (мол. масса 200 000 Да) и 4 легких цепей (мол. масса 20 000 – 25 000 Да)
Активные центры головки миозина обладают АТФ-азной активностью:
АТФ + Н2О → → АДФ + Рн + Е
Актин
Составляет 20% от массы миофибрилл.
Небольшой глобулярный белок.
Состоит из 1 полипептидной цепи (374 аминокислотных остатка).
Молекула глобулярного актина способна к спонтанной агрегации, образуя фибриллярный актин
Тропомиозин
фибриллярный белок. состоит из 2 α-спиралей.
на 1 молекулу тропомиозина приходится 7 молекул актина.
молекула тропомиозина закрывает активные центры связывания актина
Тропонин
Глобулярный белок.
В состав входят 3 субъединицы:
Тн-Т – тропомиозинсвязывающая субъединица – отвечает за связь с тропомиозином
Тн-С – кальцийсвязывающая субъединица – обладает сродством к ионам Са2+
Тн-I – ингибиторная субъединица – ингибирует АТФ-азную активность, препятствуя взаимодействию актина и миозина
Особенности энергетического обмена в мышечной ткани
Источники энергии
1.Реакции субстратного фосфорилирования (креатинкиназная реакция)
2.Аденилаткиназная (миокиназная) реакция
3.Гликолиз и гликогенолиз
4.Окислительное фосфорилирование
Креатинкиназная реакция
Преимущества:
Самый быстрый способ синтеза АТФ (каждая молекула креатинфосфата образует 1 молекулу АТФ)
Максимально эффективен
Не требует кислорода.
Включается мгновенно.
Не дает побочных продуктов.
Креатин мышц резервирует энергию в макроэргических связях и передает эту энергию для участия в акте мышечного сокращения
Недостаток: малый резерв субстрата (на 20 секунд работы)
Биосинтез и распад креатина Креатин и креатининфосфат
– важные азотистые вещества мышцы.
Находится креатин в мышцах, ткани мозга, миокарде в свободном состоянии и в форме фосфокреатина.
При переходе от покоя к работе мышцы сначала используют АТФ, образующийся из креатинфосфата – это наиболее быстрый путь генерации АТФ.
Синтез креатина
Первая стадия синтеза креатина протекает в почках под действием глицин-амидинотрансферазы.
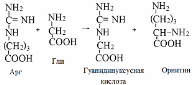
Вторая стадия – метилирование - протекает в печени.

В мышцах имеется высокоэнергетическое вещество – креатинфосфат.
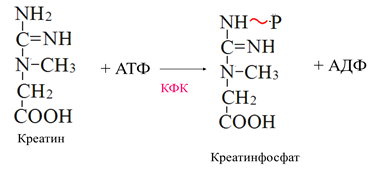
Креатинин образуется в результате неферментативного дефосфорилирования креатинфосфата.
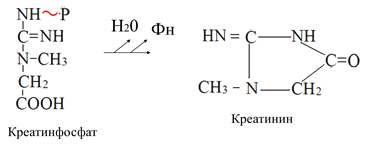
Содержание в плазме крови
В плазме крови в небольших количествах содержатся креатин и креатинин. Содержание креатинина в плазме крови - 44-100 ммоль/л у мужчин, у женщин - чуть меньше. С мочой креатин выделяется только у детей, у взрослых – креатинин. При болезнях почек с нарушением фильтрации выделение креатинина уменьшается, а его количество в крови увеличивается. В норме суточное выделение креатинина с мочой пропорционально мышечной массе.
Диагностическое значение уровень креатинина в сыворотке – чувствительный показатель состояния функции почек, снижение выделение креатинина с мочой наблюдается при гипертиреозе и прогрессирующей мышечной дистрофии в связи со снижением скорости синтеза креатина.
Повышение выделения креатина наблюдается при переохлаждении организма. заболеваниях скелетной мускулатуры (при нарушении трофики и структуры мышц), при этом креатинурия сопровождается снижением содержания креатинина в моче, что связано с нарушением механизма превращения креатина в креатинин.
Аденилаткиназная реакция
•Реакция идет только в мышечной ткани!
2 АДФ → АТФ + АМФ
Гликолиз и гликогенолиз
Преимущества:
•Не требует присутствия кислорода
•Большой резерв субстратов
•Используется гликоген мышц и глюкоза крови
Недостатки:
•Небольшая энергоэффективность
•Накапливаются недоокисленные продукты (лактат)
•Гликолиз начинается лишь через 10 – 15 секунд после начала мышечной работы
Окислительное фосфорилирование
Преимущества:
•Наиболее энергетически выгоден (например, при окислении 1 молекулы глюкозы получается 38 АТФ)
•Имеет самый большой резерв субстратов (глюкоза, гликоген, глицерин, кетоновые тела)
•Продукты распада (СО2 и вода) безвредны
Недостатки:
• Требует большого количества кислорода
