
- •I. Химия белка
- •Функции белков:
- •5. Классификация и характеристика простых белков (альбумины, глобулины, гистоны, протамины, протеиноиды).
- •1. Альбумины
- •2. Глобулины
- •3.Гистоны
- •4.Протамины
- •5.Протеноиды
- •6. Классификация и характеристика сложных белков (липопротсины, хром-мопротеины, нуклеопротеины, гликопротеины, фосфопротеины).
- •II. Ферменты. Витамины.
- •7. Химическая природа ферментов, Активный и аллостерический центры фермента, их роль.
- •8. Виды специфичности ферментов. Основные пути активации и ингибирования ферментативной активности.
- •9. Мультиферментные комплексы и изоферменты. Клиническое значение определения активности изоферментов. Энзимодиагностика. Ферментативные лекарственные препараты.
- •1. Зависимость скорости реакции от температуры
- •2. Зависимость скорости реакции от рН
- •3. Зависимость скорости реакции от концентрации субстрата
- •4. Зависимость от концентрации фермента
- •11. Классификация ферментов. Общая характеристика класса оксидоредуктаз. Основные подклассы. Коферменты оксидоредуктазных реакций.
- •Характеристика фермента
- •12. Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций.
- •13. Классификация ферментов. Общая характеристика гидролаз. Основные подклассы гидролаз.
- •14. Классификация ферментов. Общая характеристика класса лиаз. Коферменты лиазных реакций.
- •15. Классификация ферментов. Общая характеристика изомераз и лигаз. Коферменты изомеразных или глазных реакций.
- •16. Классификация витаминов. Причины развития витаминной недостаточности в организме человека. Авитаминозы, гиповитаминозы, гипервитаминозы, Антивитамины.
- •17. Витамин в1, его химическая структура, признаки витаминной недостаточности. Нарушение углеводного обмена при - витаминной недостаточности.
- •18. Витамины pp и в2, их структура, участие в обмене веществ, признаки витаминной недостаточности.
- •19. Витамины с и р, их структура, признаки витаминной недостаточности и влияние на обмен веществ.
- •20. Витамин биотин, их структура, признаки витаминной недостаточности и участие в обмене веществ.
- •21. Витамин b12, и фолиевая кислота, участие в обмене веществ и признаки витаминной недостаточности.
- •22. Витамины а, е, к. Признаки витаминной недостаточности, участие в обмене веществ.
- •23. Витамин d, химическая природа витамина, гормонально-активные формы, участие витамина в обмене веществ. Рахит. Основные пути метаболизма. БиоэнергетическиЙ обмен.
- •24. Понятие об обмене веществ. Катаболизм и анаболизм, их характеристика и взаимосвязь. Виды метаболических путей. Центральные метаболиты.
- •26. Дыхательная цепь. Ферментные комплексы дыхательной цепи, их локализация. Редокс - потенциалы ферментных систем. Ингибиторы переноса электронов.
- •27. Окислительное фосфорилирование. Значение и механизм процесса. Расообщение дыхания и фосфорилирования. Свободное окисление. Субстратное фосфорилирование.
- •28. Свободнорадикальное окисление. Понятие о перекисном окислении липидов.
- •29. Антиоксидантная система организма. Неферментативные антиоксиданты. Антиоксидантные ферменты.
- •IV. Обмен углеводов.
- •30. Классификация и химическая структура углеводов, их роль в обеспечении жизнедеятельности организма. Переваривание и всасывание углеводов в пищеварительном тракте. Мальабсорбция.
- •32. Структура гликогена и его синтез в клетках печени и мышц. Функциональные отличия гликогена этих тканей. Распад гликогена. Гликогенозы.
- •33. Гликолиз. Биологическое значение, химизм процесса. Необратимые этапы и ключевые ферменты гликолиза. Биоэнергетика и регуляция этого процесса. Эффект Пастера.
- •II этап - окислительное декарбоксилирование пвк
- •III этап - Цикл Кребса
- •35. Апотомический путь обмена глюкозы (пентозный цикл). Окислительная и неокислительная ветви процесса. Биологическое значение пентозного цикла.
- •36. Глюконеогенез. Основные субстраты и ключевые ферменты процесса. Цикл Кори.
- •38. Патология углеводного обмена. Сахарный диабет. Нарушения углеводного и липидного обменов при этом заболевании.
- •V. Обмен липидов
- •39. Классификация и химическая структура липидов. Роль липидов в обеспечении жизнедеятельности организма.
- •40. Биологические мембраны, их структурные компоненты. Функции биологических мембран.
- •41. Холестерин, его биосинтез и биологическая роль. Гиперхолестеринемия. Атеросклероз. Роль липопротеинов в обмене холестерина.
- •1)Наследственная.
- •42. Классификация и химическая структура фосфолипидов. Биологическая роль, переваривание, биосинтез и распад фосфолипидов. Липотропные вещества.
- •43. Переваривание и всасывание липидов, роль желчи в этом процессе. Желчные кислоты. Ресинтез липидов в клетке эпителия кишечника. Транспортные формы липидов. Биологическая роль жировых депо.
- •44. Липолиз триглицеридов в тканях. Окисление глицерина. Биоэнергетика процесса.
- •45. Окисление жирных кислот. Внутриклеточная локализация и биоэнергетика процесса. Особенности обмена жирных кислот с нечетным количеством углеродных атомов и ненасыщенных жирных кислот.
- •46. Синтез жирных кислот. Внутриклеточная локализация, ферменты и коферменты процесса. Биосинтез триглицеридов.
- •47. Образование и распад кетоновых тел. Кетогенез в норме и при патологии.
- •48. Гормональная регуляция липидного обмена. Патология липидного обмена: гиперлипидемии, липоидозы, жировое перерождение печени, ожирение, атеросклероз.
- •3. Конденсация йодтирозинов
- •1. Аминокислоты и их производные:
- •2. Пептиды
33. Гликолиз. Биологическое значение, химизм процесса. Необратимые этапы и ключевые ферменты гликолиза. Биоэнергетика и регуляция этого процесса. Эффект Пастера.
— это анаэробный распад глюкозы до лактата.
С6Н12О6 + 2АДФ +2Фн = 2 лактата + 2АТФ + 2Н20.
-включает 11 реакций и 2 этапа.
Значение гликолиза
Благодаря гликолизу организм осуществляет ряд функций в условиях недостаточности кислорода.
Когда на Земле не было кислорода, то гликолиз был основным источником энергии.
Особенности гликолиза
-Ферменты гликолиза локализуются в цитоплазме.
-Наиболее интенсивен гликолиз в: эритроцитах, работающей мышце, эмбриональной ткани, опухоли.
-3 необратимые реакции (киназные).
Первый этап гликолиза
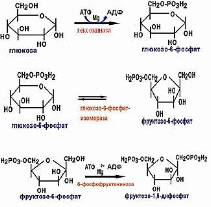

Второй этап гликолиза

В активном центре фермента глицеральдегидфосфатдегидрогеназы содержатся SН-группы цистеина.
На первом этапе происходит отщепление водорода с альдегидной группы субстрата, а второй водород от SН-группы активного центра.
Водород переходит на НАД, в результате получаем НАДН+Н+, образуется фермент-субстратный комплекс, который взаимодействует с фосфорной кислотой.
Свободная энергия, освобождённая при окислении альдегидной группы, сохраняется в высокоэнергетической фосфатной группе.

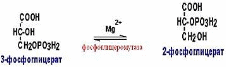
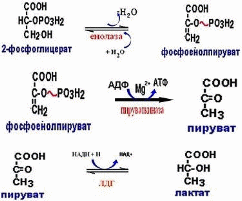
НАДН+Н+, образующийся при окислении глицеральдегид-3фосфата,вновь окисляется в НАД, восстанавливая при этом ПВК до лактата.
Эта реакция происходит в анаэробных условиях
Баланс гликолиза
АТФ образуется за счёт двух реакций субстратного фосфорилирования (ПК, фосфоглицераткиназной).
Из глюкозы образуется 4АТФ.
2АТФ тратится в гликолизе на фосфорилирование (ГК, ФФК реакции).
Гексокиназная реакция -1АТФ
Фосфофруктокиназная реакция -1АТФ
Фосфоглицераткиназная реакция 2АТФ
Пируваткиназная реакция 2АТФ
Итого: 4 – 2 = 2АТФ
Регуляция гликолиза
-Гексокиназа – аллостерический фермент, ингибируется глюкозо-6-фосфатом. Инсулин стимулирует синтез глюкокиназы, которая не ингибируется глюкозо-6-фосфатом.
-Фосфофруктокиназа - аллостерический фермент. Положительный модулятор – АМФ, АДФ, Фн, цАМФ, ионы двухвалентных металлов.
-Отрицательный модулятор – АТФ и цитрат.
Когда величина значительна, то происходит угнетение ФФК.
Эффект Пастера -торможение гликолиза кислородом.
Причина этого: кислород окисляет НАДН+Н и он не восстанавливает ПВК в лактат.
- Пируваткиназа – аллостерический фермент.
Положительный модулятор – АДФ.
Отрицательный модулятор – АТФ, ацетил-КоА, жирные кислоты.
Гликолиз обратим. Биологическое значение обратимости гликолиза:
-освобождение тканей от лактата,
-возможность осуществления глюконеогенеза
34. Аэробный (дихроматический) распад глюкозы. Роль пируватдегидрогеназного комплекса в процессе окислительного декарбоксилирования пирувата. Биоэнергетика аэробного распада глюкозы.
Аэробный распад глюкозы Основной путь катаболизма глюкозы. Дихотомический распад молекулы глюкозы на 2 триозы. Происходит в нервной ткани, почках, печени, сердце. Поставляет энергию в клетку. Требуется кислород.
В процессе аэробного распада глюкозы выделяют три этапа:
Гликолитическая фаза (распад глюкозы до пирувата в цитозоле клеток).
Окислительное декарбоксилирование ПВК (в митохондриях).
Цикл трикарбоновых кислот (в митохондриях).
I этап аэробного распада – гликолиз без последней реакции. Все реакции протекают в цитоплазме.
Две реакции идут с затратой энергии (гексокиназная, фосфофруктокиназная).
Субстратное фосфорилирование обеспечивает на одну молекулу глюкозы 4 молекулы АТФ.
2 НАДН+Н+ (на 1 молекулу глюкозы) образуются в глицеральдегидфосфатдегидрогеназной реакции, проникают в митохондрии, где дают 3*2=6 АТФ.
Большинство реакций обратимы, три реакции необратимые (гексокиназная, фосфофруктокиназная, пируваткиназная).
Баланс: приход 6+4= 10АТФ. расход 2АТФ. 10-2 = 8АТФ.
