
1. Внутриутробный период развития человека. Повреждающие факторы, их последствия. Алкоголизм и потомство. Алкогольная эмбриофетопатия. Внутриутр период — от момента зачатия до рождения — продолж 270 дней, но на практике расчет обычно ведут на 280 дней (10 лунных месяцев), начиная счет с первого дня последнего менстр. цикла женщины. Срочными родами =происходящие на 38 — 41-й неделе бер-ти, преждеврем — ранее 38-й нед , запоздалыми — при сроке 42 недели и более. I. Внутриутробный этап: а) собственно зародышевый период; б) период имплантации; в) фаза эмбрионального развития (по 75-й день); г) фетальный период (с 76-го дня до рождения): — ранний фетальный подпериод (с 76-го дня до конца 28-й недели); — поздний фетальный подпериод (после 28-й недели до рождения). П. Интранаталъный этап. Периоды внутриутробного развития: А. Терминальный, или собственно зародышевый-с мо- мента оплодотв яйцеклетки до имплантации образов-ся бластоцита в слизистую оболочку матки. 1 неделя. Б. имплантация. -40 часов, 2 дня. Повреждения зиготы тератогенными факторами в первые две недели после оплодотв вызывают гибель зародыша, внематочную беременность, пороки развития с нарушением оси зародыша (симметрич, асимметрич и не полностью разделившиеся близнецы, циклопия, сирингомиелия, аплазия почек т.д.), Пороки развития, возникшие на этом сроке гестации, в том числе и вследствие хромосомных аббераций и мутаций генов, называют бластопатиями. В. Эмбрионал период. Длится по 75-й день внутриутробного развития. Питание зародыша происходит из зародышевого мешка (амниотрофный тип питания). Закладка и органогенез п очти всех внутренних органов будущего ребенка. Однако сроки макс их развития неодинаковы. В зависимости от этого образуются а ааномалии плода. Поражения зародыша под возд тератогенных экзо- и эндоген факторов от момента прикрепления его к стенке матки до сформ-я плаценты -эмбриопатиями. Они проявл-я пороками раз- вит отдел органов и систем, тератомами (эмбриоцитомами). прерыв берем-и. Г. Фетальный период продолжается с 76-го дня внутриутробного развития до рождения. Выделяют ранний фетальный подпериод (с 76-го дня внут- риутробного развития до конца 28-й недели) и п о з д н и й детальный подпе- риод (после 28-й недели и до рождения). Болезни, возникающие с 76-го дня внутриутробной жизни до рождения, называются ф е т о п а т и я м и. Поражения плода могут вызвать преждевре- менное прекращение беременности с рождением маловесного, функционально незрелого ребенка, асфиксию при рождении, метаболические и другие нару- шения адаптации к внеутробной жизни. Проявлениями фетопатии явл задержка внутриутробного развития, врожден пороки развития, гипоплазии и дисплазии отдел органов и тканей, врожденные болезни, избыточное разрастание соединит и др тканей при инфекциях. Поздний детальный период обеспеч процессы депонирования многих компонентов питания, кот не могут быть в достаточном кол-ве введены ребенку с материнским молоком соли Ca, Fe, Сu, В12). Поздний фетальный подпериод переходит в интранатальный этап-от времени появл регуляр родовых схваток до момента перевязки (пережатия) пуповины ( от 2 — 4 до 15 — 18 ч). В это время возможны возник-е травм ЦНС и ПНС , наруш пуповинного кровообр или дыхания, инфицирование плода флорой, в том числе патогенной, из родовых путей. Повреждающие действия: 1.Эмбриотоксический эф- смерть плода. 2.Тератогенный- пороки развития. 3. Дефекты развития плода- нарушение и повреждение органов плода. 4.Нарушение роста плода. 5.Нарушение адаптационной способности. 6.Мутагенный эффект. Известно несколько сотен тератогенных факторов, однако практическое значение у человека имеют всего лишь несколько: · Эндокринные заболевания матери (сахарный диабет); · Физические воздействия (температурные или ионизирующие); · Химические вещества, к которым относятся некоторые медикаменты и алкоголь; · Биологические факторы (инфекции — токсоплазмоз, краснуха и др.) Алкоголь. Уже при умеренном и непродолжительность потреблении этилового спирта число сперматозоидов уменьшается в семенной жидкости примерно на 30 процентов, при длительном — на 65-70 процентов. При этом резко падает активная подвижность сперматозоидов. Этиловый спирт отрицательно влияет на оплодотворяющую активность сперматозоидов. Однако следует заметить, что действие это обратимо. Вызываемое этиловым спиртом угнетение функции мужских половых желез вплоть до бесплодия следует рассматривать в виде двухстадийного процесса. Первая стадия — обратимые явления уменьшения синтеза тестостерона и уменьшения образования сперматозоидов со сниженными функциями. Они являются следствием действия спирта и продуктов его окисления на половые железы, гипофиз и гипоталамус. Вторая стадия — завершающий этап длительного потребления алкогольных напитков. Характеризуется он нарушениями ткани печени и половых желез, что приводит к необратимому повреждению системы клеток яичек, производящих сперматозоиды. У женщин, страдающих алкоголизмом, часто встречаются расстройства менструального цикла, наступает преждевременный климакс, иногда на 10-15 лет раньше, чем у непьющих. Яичники могут подвергаться жировому перерождению и продуцировать незрелые яйцеклетки. Женщины, злоупотребляющие алкогольными напитками, реже беременеют, и у них труднее сохранить беременность. Известно, что длительное злоупотребление алкоголем нарушает функции многих органов и систем и, прежде всего, головного мозга. Страдают мышление, память, интеллект. Алкоголизм часто сопровождается табакокурением. При алкоголизме имеется целый ряд сопутствующей патологии. Выявлена прямая связь между потреблением алкоголя и распространенностью артериальной гипертензии: у лиц, злоупотребляющих алкоголем, это заболевание встречается в 3 раза чаще, чем у трезвенников. Даже небольшое количество алкоголя при длительном использовании является тератогенным (от 1,0 до 3,0 г чистого спирта в день), оказывая прямое повреждающее действие на генетический аппарат клетки и влияя на структуры и функционирование хромосом. Употребление алкоголя до, во время зачатия или во время беременности в 30-50% случаев нарушает нормальное развитие плода, что может приводить к возникновению комплекса врожденных дефектов и рождению психически и физически неполноценного ребенка. Этот синдром имеет несколько названий: «алкогольный синдром плода», «алкогольная эмбриопатия», «фетальный или плодный алкоголизм», «алкогольная эмбриофетопатия» и описан многими исследователями [3, 15]. Для него характерно: церебральная недостаточность и задержка психического развития с олигофренией в дальнейшем (93-95%); задержка внутриутробного развития (80-90% детей); черепно-лицевые аномалии (84-88%); мышечная гипотония (40-62%); гиперреактивность и агрессивность (54-60%); врожденные пороки развития, в основном – патология сердечных перегородок (30-50%). Частота развития полного алкогольного синдрома плода, по данным литературы, составляет 2-5%, но отдельные его проявления встречаются значительно чаще (у каждого 2-3 ребенка, рожденного от родителей, злоупотребляющих алкоголем). В дальнейшем у таких детей наблюдаются нарушения внимания, импульсивность, расстройства настроения, поведения со склонностью к нарушению общественного порядка и симптомы оппозиционно-вызывающего поведения. Даже при отсутствии при рождении признаков алкогольной эмбриофетопатии у детей из семей алкоголиков часто наблюдается низкий коэффициент интеллектуальности, а также агрессивность, расстройство речи, неврозы, энурез, эпилепсия, олигофрения, аномалии зрения и слуха. Алкогольный синдром плода (алкогольная эмбриофетопатия, фетальный алкогольный синдром, ФАС) развивается у детей, чьи матери употребляли спиртные напитки во время беременности. Среди его проявлений – дефицит веса и роста, нарушения поведения и интеллекта, умственная отсталость, заячья губа и другие специфические особенности строения лица и черепа. Главная причина развития фетального алкогольного синдрома – токсическое действие алкоголя и продуктов его распада на организм ребенка. Этому способствуют легкая проходимость алкоголя через плаценту, отсутствие алкогольдегидрогеназы в печени эмбриона, подавление синтеза клеточной и бесклеточной РНК, развитие алкогольной гипогликемии, нарушение трансплацентарного транспорта эссенциальных аминокислот, цинка и других полезных веществ. 2. Ранний и поздний фетальный периоды и их характеристика. Фетальный период. Продолжительность от 9-ой недели до рождения. В этот период характерно гемотрофное питание плода. В фетальном периоде целесообразно выделять 2 подпериода: ранний и поздний. -Ранний фетальный подпериод. Продолжительность от 9 недель до 28 недель (~2 мес- 7 мес). В этот период происходит интенсивный рост и тканевая дифференцировка органов плода. Обычно воздействие неблагоприятных факторов уже не приводит к формированию пороков строения, но может проявляться задержкой роста и дифференцировки (гипоплазии) органов или нарушением дифференцировки тканей (дисплазии). В связи с тем, что иммунитет только начинает формироваться, то ответ на инфекцию выражается соединительнотканными пролиферативными реакциями, приводящими к циррозам и фиброзам. Совокупность изменений плода, возникающих в этом периоде, называется общим термином — “ранние фетопатии”. -Поздний фетальный период. Продолжительность от 28 недель до родов, то есть до отхождения околоплодных вод. Поражения плода в этом периоде не влияют на процессы формирования органов и дифференцировки тканей, но могут вызвать преждевременное прекращение беременности с рождением маловесного и функционально незрелого ребёнка. При повреждающем действии инфекции возникает уже настоящий инфекционный процесс с морфологическими и клиническими признаками заболевания, характерным для данного возбудителя. В этот период происходит депонирование тех питательных веществ, которые ребёнок не сможет получать в достаточном количестве с материнским молоком. Депонируются соли кальция, железа, меди и витамин В12. Кроме того, в последние 10-12 недель беременности достигается высокая степень зрелости и защиты функций жизненно важных органов плода от возможных нарушений оксигенации и травматизма в родах, а накопленные при трансплацентарной передаче иммуноглобулины матери обеспечивают высокий уровень пассивного иммунитета. В последние недели беременности также осуществляется созревание “сурфактанта”, обеспечивающего нормальную функцию лёгких и эпителиальных выстилок дыхательного и пищеварительного трактов.
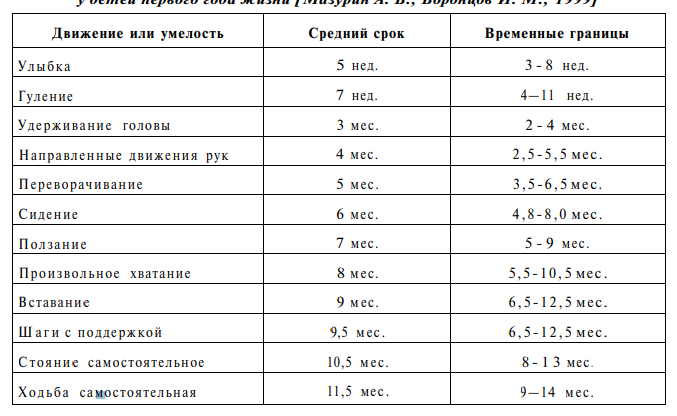
Вредные факторы, влияющие на плод во время фетального периода, провоцируют развитие фетопатий, для которых морфологические пороки не характерны. Пороки развития в этот период могут возникнуть лишь в органах, не окончивших своего формирования (ткань головного мозга, зубы, гениталии, лёгкие). Для этого периода характерно формирование так называемых «вторичных» пороков развития — то есть искажения развития нормально сформированных органов вследствие воспалительных процессов (например, токсоплазмоз, вирусные инфекции) или нарушений созревания, приводящих к формированию дисплазий или гипоплазий органов и тканей. 3. Периоды новорожденности, грудного возраста и их характеристика. Период новорожденности — это период адаптации ребенка к условиям внеутробной жизни, длительность которого составляет 28 дней с момента рождения. Выделяют ранний неонатальный период (от перевязки пуповины до окончания 6х суток). И поздний (с 7го по 28 день жизни). Период с 23 недели внутриутробного развития до 7 дня жизни-перинатальный. III. Внеутробный этап: а) период новорожденности (от рождения до 28 дней жизни); б) грудной возраст (с 1-го по' 12-й месяц); в) период раннего детства (1- 3 года); г) 1-й период детства (от 3 до 7 лет) - дошкольный возраст; д) 2-й период детства (девочки 7-11 лет, мальчики 7-1 2 лет) – младший школьный возраст; е) старший школьный возраст (девочки с 12 лет, мальчики с 13 лет). Период грудного возраста — с 29-го дня жизни ребенка после рождения до конца первого года жизни. Этот период характеризуется интенсивным нарастанием массы тела ребенка и роста, интенсивным физическим, нервно-психическим, интеллектуальным развитием. Само название говорит о близком контакте ребенка с матерью в этом периоде. В период грудного возраста закладывается фундамент здоровья человека. У грудного ребенка имеется врожденная потребность в активном познании окружающего его мира. Период новорожденности хар-ся рядом значительных морфологических, функциональных и биохимических преобразований: • Начало легочного дыхания и функц-я малого круга кровооб- р с перекрытием путей внутриутробной гемодинамики (артер протока, овального отверстия, венозного протока, пупочных артерий и вены) и возрастанием кровотока в сосудах легких и головного мозга. • Начало энтерального питания. Активность пластических процессов и быстрая прибавка массы, тела обесп-ся большим функционал на- пряжением ЖКТ и хар-м питания. На смену ге- матотрофному питанию (через плаценту) и амниотрофному питанию приходит лактотрофный тип питания (грудное молоко). • Организм ребенка приспосабливается к новым, внеутробным условиям су- ществования. Функции организма находятся в состоянии неустойчивого равновесия. Новорожд ребенку свойственна высокая уязви- мость:для поврежд факторов, адаптационные процессы легко нарушаются. • Пограничные сост-я: физиол. желтуха, транзитор потеря первонач массы тела, половой криз и т. д. • Незаконченность морф строения многих органов и систем, ЦНС ПНС. что проявляется в особенностях всех регуляторных процессов и интегративной деятельности функциональных систем. Процессы торможения преобладают над процессами возбуждения. Начало выработки первых условно-рефлекторных связей с окружающей средой. В трехнедельном возрасте многие дети начинают отвечать на общение улыбкой и мимикой радости. • Своеобразие специфического и неспецифического иммунитета, которое трактуется как транзиторный иммунодефицит. Гуморальный иммунитет обеспечивается главным образом материнскими IgG, получаемыми трансплацентарно в последнем триместре беременности. Отсутствие секреторного IgA компенсируется тем, что в женском молоке содержится его большое количество. Уровень I gM низкий. Функциональная активность лимфоцитов низкая. Несовершенство завершающей фазы фагоцитоза. Низкая резистентность по отношению к условно-патогенной, гноеродной, грамотрицательной флоре, некоторым вирусам (герпес, цитомегаловирус, Коксаки В). Характерная патология • Состояния, непосредственно связанные с актом родов: кардиореспираторная депрессия, асфиксия, синдром дыхательных расстройств, кровоизлияния в различные органы, родовые травмы, гемолитическая болезнь и др. • Инфекции врожденные и приобретенные: внутриутробные инфекции, заболевания пупка и пупочной ранки, поражения кожи, кишечника, дыхательных путей, сепсис. Склонность к генерализации инфекции, эволюции в шоковое состояние. • Недоношенность. • Уродства, дефекты развития. Грудной возраст продолжается с 29-го дня после рождения до конца 1-го года жизни. Для грудного возраста характерно: • Тесный контакт ребенка с матерью. Мать кормит своим молоком ребенка. • Высокий темп роста, морфологического и функционального совершенствования всех органов и систем. В течение первого года жизни длина тела новорожденного увеличивается на 50%, масса тела утраивается. • Высокий темп роста обеспечивается интенсивным обменом веществ и преобладанием анаболических процессов, чем объясняется высокая потребность в основных питательных веществах и калориях. Относительная энергетическая потребность детей этого возраста в 3 раза превышает потребность взрослого человека. Для удовлетворения высокой потребности в энергии ребенок нуждается в большем количестве пищи на килограмм массы. • Совершенствуются морфологическая структура и функции нервной системы ребенка. По мере дифференцирования ЦНС быстрым темпом происходит нервно-психическое развитие ребенка. Рано, с первых недель жизни, формируются условные рефлексы (1-я сигнальная система). Быстрыми темпами происходит развитие двигательных умений, формируются сложные локомоторные акты (функция кисти, самостоятельная ходьба). К концу года — развитие речи (2-я сигнальная система). К году происходит увеличение массы мозга в 2–2.5 раза. Отмечается интенсивная дифференцировка нервных клеток мозга в первые 5–6 мес жизни ребенка. Большое значение в развитии имеет ориентировочный рефлекс, отражающий врожденную потребность ребенка в движении и деятельности органов чувств. Нервные связи между ребенком и окружающими людьми устанавливаются посредством мимики, жеста, голосовых интонаций. Развитие тонких движений пальцев рук способствует развитию мозга и речи. Имеет большое значение возникновение связи между словами и ответными двигательными реакциями ребенка, затем связывание малышом зрительного и слухового восприятия объектов со словами, названиями предметов при их показе, связи с отдельными действиями («дай», «покажи») — это оптимальный ход развития, необходимый как основа для последующих периодов детства. Потребность контакта со взрослыми определяет психическое развитие ребенка. • После 3—4 месяцев жизни ребенок теряет трансплацентарно приобретенный иммунитет, а формирование собственных систем иммунитета происходит сравнительно медленно. Однако отсутствие тесного контакта с другими детьми объясняет относительно редкую заболеваемость вирусными детскими инфекциями (корь, скарлатина, ветряная оспа, краснуха и др.). По сравнению с периодом новорожденности происходит некоторое снижение количества Т- и В-лимфоцитов, снижение материнского IgG, начиная с 2–3 мес. В 4–6 мес наблюдается первый критический период иммунитета, который характеризуется ослаблением пассивного гуморального иммунитета, полученного от матери, и отмечается самый низкий уровень специфических антител — физиологическая гипоиммуноглобулинемия. Синтез собственного IgG начинается ребенком с 2–3 мес жизни, постоянный уровень его устанавливается после 8 мес–1 года. Уровень IgM к концу года жизни достигает 50% уровня взрослого. Нарастание секреторного IgA происходит медленно. Содержание IgE у здорового ребенка на протяжении года незначительное, при проявлениях атопического дерматита значительно возрастает. Для грудного периода характерен синтез IgM, не оставляющих иммунологической памяти. В связи с указанным наблюдается высокая чувствительность к респираторно-синцитиальным вирусам, вирусам парагриппа и аденовирусам; атипично протекает корь, коклюш, не оставляя иммунитета. Неспецифические факторы резистентности. У детей грудного возраста наблюдается высокое содержание лизоцима и пропердина, быстро нарастает уровень комплемента сыворотки крови и с первого месяца жизни содержание его не отличается от уровня взрослого. С 2–6 мес формируется завершающая фаза фагоцитоза к патогенным микроорганизмам, за исключением пневмококка, стафилококка, клебсиеллы, гемофильной палочки. Характерная патология • Несбалансированное питание может быть причиной задержки физического, нервно-психического и интеллектуального развития. В условиях интенсивного роста неадекватное потребностям растущего организма питание может приводить к развитию дефицитных состояний (рахит, анемия, дистрофия). • Аномалии конституции (экссудативно-катаральный и лимфатико-гипопластический диатезы). • Сохраняется склонность к генерализации воспалительного процесса, к общей ответной реакции на любое воздействие — при инфекционных заболеваниях могут развиваться судороги, менингеальные явления, токсикоз, обезвоживание. Организм чувствителен к гноеродным микробам и особенно к возбудителям кишечных инфекций (в том числе к вирусам и условно-патогенной флоре). Высокая чувствительность к PC-вирусу, вирусам парагриппа, аденовирусам. • Нередко развиваются желудочно-кишечные дисфункции, что объясняется особенностями органов пищеварения и необходимостью их интенсивного функционирования (высокая потребность в пластических веществах и энергии). • Анатомо-физиологические особенности органов дыхания: узость дыхательных путей, незрелость ацинусов и другие способствуют возникновению бронхиолитов и пневмоний, течение которых отличается особой тяжестью. • Атипично протекают детские инфекции (корь, коклюш), не оставляя иммунитета. • Высока частота синдрома внезапной смерти. 4.Преддошкольный, дошкольный, младший школьный и старший школьный периоды детского возраста, их характеристика. Период раннего детства (с 1 года до 3 лет). Детям этой возрастной группы присущи следующие черты: • Стремительно совершенствуются двигательные навыки, происходит развитие интеллектуальной сферы, развитие речи. • Сохраняется высокий темп роста и развития, хотя он ниже, чем на первом году жизни. • Характерна большая степень зрелости функциональных систем. • Стремительно расширяются контакты с другими детьми на фоне собственного формирующегося и пока несовершенного иммунитета. Повышена чувствительность к неблагоприятным влияниям внешней среды. • Постепенно меняется характер питания: расширяется ассортимент продуктов, «кусочковое» питание, совершенствуются навыки самостоятельной еды. Важное значение имеет выработка гигиенических навыков. Характерная патология • Широко распространена инфекционная патология: детские инфекции (ветряная оспа, скарлатина, корь, коклюш), ОРВ И и др. • Высокий травматизм, в том числе аспирация инородных тел, случайные отравления. • Склонность к гиперплазии лимфоидной ткани, проявления лимфатикогипопластического и нейроартритического диатеза. • Дебют большей части аллергических заболеваний. 1-й период детства (дошкольный возраст) (от 3 до 7 лет). Функциональные особенности • Несколько ослабевает интенсивность обмена энергии, что проявляется в постепенном снижении основного обмена и напряженности процессов роста. • Интенсивное развитие интеллекта, физической силы, ловкости, усложняется игровая деятельность, улучшается память. Ребенок легко запоминает стихи, пересказывает рассказы, усваивает иностранный язык, развиваются тонкие двигательные навыки. • Совершенствуется речь. В 5 лет словарный запас составляет 2500 слов, ребенок начинает логически мыслить, делать обобщения. • Появляются половые различия в поведении и играх мальчиков и девочек. Возрастает потребность в общении с другими детьми. Подражание как хорошему, так и плохому. • В 5—6 лет начинается смена молочных зубов на постоянные. • Иммунная защита уже достигает известной зрелости. Снижается склонность к генерализации процесса и токсическим реакциям, отчего клиническая картина многих заболеваний приобретает характер болезней взрослых. • Ребенок готовится к поступлению в школу. Характерная патология • Острые инфекционные заболевания, однако они протекают легче, чем у более младших детей, и дают меньше осложнений. • Высока частота атопических, паразитарных, иммунокомплексных заболеваний. Формируются многие хронические заболевания полигенной природы. • Болезни органов дыхания, в том числе аллергической природы. • Высокий травматизм в этом возрасте — основная причина смертности. 2-й период детства (младший школьный возраст) (девочки 7— 11 лет, мальчики 7-12 лет). Функциональные особенности • Продолжается совершенствование функций организма ребенка. • Происходит замена молочных зубов на постоянные. • Имеются четкие половые различия между мальчиками и девочками по типу роста, созревания, телосложения. • Быстро развивается интеллект, улучшается память. Развиваются сложнейшие координационные движения мелких мышц, благодаря чему возможно письмо. • Ребенок начинает посещать школу, меньше бывает на свежем воздухе, возрастают нагрузки на нервную систему и психику, больше времени проводит за письменным столом. Характерная патология • Нарушения осанки. • Нарушения зрения. • Кариес зубов. • Сохраняется высокая инфекционная заболеваемость, а также заболеваемость желудочно-кишечными, сердечными и аллергическими заболеваниями. • Увеличивается число детей с ожирением. • Основной причиной смертности остается травматизм. Старший школьный возраст (девочки с 12 лет, мальчики с 13 лет). Для этого периода характерно: • Завершение созревания всех морфелогических и функциональных структур. • Выраженная перестройка эндокринной системы, интенсивное половое созревание, становление репродуктивной системы и сексуального поведения индивидуума. Подростковая гиперсексуальность. • Социальные особенности, обусловленные изменениями характера и условий обучения, условий быта, выбором профессии. • Скачок роста, сочетающийся с энергичной нейроэндокринной перестройкой и интенсификацией деятельности всех функциональных систем. • Гетерохрония развития органов и систем. • Формирование психохарактерологических особенностей, стереотипов поведения и вредных привычек, влияющих на здоровье не только в подростковом периоде, но и в последующей жизни. Отклонения в состоянии здоровья, свойственные этому возрастному периоду. • Нарушения физического и полового развития. Проблема репродуктивного здоровья. • Нестабильность гормональной, нейрогенной и вегетативной регуляции деятельности внутренних органов, приводящая к их функциональным расстройствам, в том числе к нейроциркуляторной дисфункции, диффузному нетоксическому зобу, гипо- и гипертоническим состояниям. • Заболевания желудочно-кишечного тракта (гастриты, дуодениты, язвенная болезнь). • Ввиду эндокринной перестройки и усиления воздействия экзогенных факторов на иммунную систему отмечается подъем хронических воспалительных, аутоиммунных, лимфопролиферативных и некоторых вирусных заболеваний. Тяжесть атопических заболеваний у многих подростков ослабевает. • Нарушения питания (тучность). • В настоящее время увеличивается распространение токсикомании, наркоманий, заболеваний, передающихся половым путем. 5.Анатомо-физиологические особенности головного и спинного мозга у детей. Закладка нервной системы происходит на 1-й неделе внутриутробного развития. Наибольшая интенсивность деления нервных клеток головного мозга приходится на период от 10 до 18-й недели внутриутробного развития, что можно считать критическим периодом формирования ЦНС. Если число нервных клеток взрослого человека принять за 100 %, к моменту рождения ребенка сформировано только 25 % клеток, к 6 месяцам – 66 %, а к году – 90–95 %. К рождению ребенка головной мозг относительно массы тела большой и составляет: у новорожденного – 1/8-1/9 на 1 кг массы тела, у ребенка 1 года – 1/11-1/12, у ребенка 5 лет – 1/13-1/14, у взрослого – 1/40. Только к концу первого полугодия мозг ребенка макроскопически приближается к мозгу взрослого человека. Нарастает и его масса. У новорожденного он составляет 360–370г, к 6 мес – около 600 г, к концу года – около 900 г. У новорожденных малодифференцированая структура больших полушарий. Проводящие пути (кроме пирамидных) достаточно развиты, но пирамидные пути миелинизируются лишь в 5—6 мес. Дифференцировка нервных клеток достигается к 3 годам, а к 8 годам кора головного мозга по строению похожа на кору головного мозга взрослого человека. Кровоснабжение мозга у детей лучше, чем у взрослых. Это объясняется богатством капиллярной сети, которая продолжает развиваться и после рождения. Обильное кровоснабжение мозга обеспечивает потребность быстрорастущей нервной ткани в кислороде. А ее потребность в кислороде в 20 с лишним раз выше, чем мышц. У новорожденного сформированы полушария головного мозга, основные борозды и крупные извилины, которые имеют малую высоту и глубину. Мелкие извилины формируются лишь к 5—6 годам. С увеличением полушарий, утолщением коры меняются форма, глубина, высота борозд и извилин. Височная доля после рождения развита лучше, чем другие доли мозга, однако ее борозды и извилины неглубоки, фрагментированы и окончательно оформляются только к 7 годам. Затылогная доля на ранних этапах относительно мала, но содержит все борозды и извилины. К 5—7 годам значительные изменения происходят и в лобной доле (в нижнетеменной и нижней лобной борозде) за счет возникновения многих мелких дополнительных борозд. У новорожденных недостаточно дифференцированы серое и белое вещество, их соотношение в течение первых лет жизни несколько изменяется, что связано с перераспределением нервных клеток. Некоторые клетки головного мозга новорожденного сохраняют эмбриональный характер. Вещество мозга очень чувствительно к повышению внутричерепного давления. Возрастание давления ликвора вызывает быстрое нарастание дегенеративных изменений нервных клеток, а более длительное существование гипертензии обусловливает их атрофию и гибель. Это находит подтверждение у детей, которые страдают внутриутробно развившейся гидроцефалией. Твердая мозговая оболочка у новорожденных относительно тонкая, сращена с костями основания черепа на большой площади. Венозные пазухи тонкостенны и относительно уже, чем у взрослых. Мягкая и паутинная оболочки мозга новорожденных исключительно тонки, субдуральное и субарахноидальное пространства уменьшены. Цистерны, расположенные на основании мозга, напротив, относительно велики. Водопровод мозга (сильвиев водопровод) шире, чем у взрослых. По мере развития нервной системы существенно изменяется и химический состав головного мозга. Уменьшается количество воды, увеличивается содержание белков, нуклеиновых кислот, липопротеидов. Спинной мозг к рождению более развит, чем головной. Шейное и поясничное утолщения спинного мозга у новорожденных не определяются и начинают контурироваться после 3 лет жизни. Темп увеличения массы и размеров спинного мозга более медленный, чем головного мозга. Удвоение массы спинного мозга происходит к 10 месяцам, а утроение – к 3-5 годам. Длина спинного мозга удваивается к 7-10 годам, причем она увеличивается несколько медленнее, чем длина позвоночника, поэтому нижний конец спинного мозга с возрастом перемещается кверху. Это должно учитываться при выборе уровня выполнения спинномозговой пункции, при котором не повреждается вещество мозга. Спинной мозг новорожденного относительно длиннее, чем у взрослого, и доходит до нижнего края III поясничного позвонка. В дальнейшем рост спинного мозга отстает от роста позвоночника, в связи с чем нижний конец его как бы перемещается кверху. Быстрее растет грудной отдел, затем шейный, и медленнее всех поясничный и крестцовый отделы. Располагаясь в спинномозговом канале, спинной мозг оканчивается у 5-летнего ребенка на уровне I—I I поясничных позвонков в виде конуса, от которого далее вниз тянутся нити конского хвоста. К 5—6 годам соотношение спинного мозга и позвоночного канала становится таким же, как и у взрослого. В 18 лет нижний конец спинного мозга находится на уровне верхнего края II поясничного позвонка. Рост спинного мозга продолжается приблизительно до 20 лет. Масса его увеличивается в 8 раз по сравнению с периодом новорожденности. Внутричерепные нервы миелинизируются к 3 мес, периферические — к 3 годам. Вегетативная нервная система функционирует с самого рождения, обеспечивая поддержание сосудистого тонуса, адаптационно-трофические реакции и регуляцию деятельности внутренних органов. Однако регуляторные функции вегетативной нервной системы у детей первых месяцев жизни легко нарушаются при воздействии не адекватных возрасту внешнесредовых факторов. 6.Врожденные рефлексы. Формирование условных рефлексов и второй сигнальной системы. Особое значение в периоде новорожденности имеют, так называемые, основные безусловные рефлексы. Основные безусловные рефлексы новорождённого и грудного ребёнка делятся на две группы: сегментарные двигательные автоматизмы, обеспечивающиеся сегментами мозгового ствола (оральные автоматизмы) и спинного мозга (спинальные автоматизмы). Оральные сегментарные автоматизмы: Сосательный рефлекс: При введении указательного пальца в рот на 3-4 см ребёнок делает ритмичные сосательные движения. Рефлекс отсутствует при парезе лицевых нервов, глубокой умственной отсталости, в тяжелых соматических состояниях. Поисковый рефлекс (рефлекс Куссмауля): При поглаживании в области угла рта происходит опускание губы, отклонение языка и поворот головы в сторону раздражителя. Надавливание на середину верхней губы вызывает открытие рта и разгибание головы. При надавливании на середину нижней губы опускается нижняя челюсть и сгибается голова. Этот рефлекс особенно хорошо выражен до кормления и слабо выражен у ребёнка сразу после кормления. Обращают внимание на симметричность рефлекса с двух сторон. Поисковый рефлекс наблюдается до 3—4 мес., затем угасает. Асимметрия рефлекса — односторонний парезлицевого нерва. Рефлекс отсутствует — двухстороннийпарезлицевого нерва, поражение ЦНС. Хоботковый рефлекс: Быстрый удар пальцем по губам вызывает вытягивание губ вперед. Этот рефлекс сохраняется до 2—3 мес. Ладонно-ротовой рефлекс (рефлекс Бабкина): При надавливании большим пальцем на область ладони новорождённого (обеих ладоней одновременно), ближе к тенару, происходит открывание рта и сгибание головы. Рефлекс ярко выражен у новорождённых в норме. Вялость рефлекса, быстрая истощаемость или отсутствие свидетельствуют о поражении ЦНС. Рефлекс может отсутствовать на стороне поражения при периферическом парезеруки. После 2 мес. он угасает и к 3 мес. Исчезает. Спинальные двигательные автоматизмы: Защитный рефлекс новорождённого: Если новорождённого положить на живот, то происходит рефлекторный поворот головы в сторону. Этот рефлекс выражен с первых часов жизни. У детей с поражением центральной нервной системызащитный рефлекс может отсутствовать, и, если не повернуть пассивно голову ребёнка в сторону, он может задохнуться. Рефлекс опоры и автоматическая походка новорождённых: У новорождённого нет готовности к стоянию, но он способен к опорной реакции. Если держать ребёнка вертикально на весу, то он сгибает ноги во всех суставах. Поставленный на опору ребёнок выпрямляет туловище и стоит на полусогнутых ногах на полной стопе. Положительная опорная реакция нижних конечностей является подготовкой к шаговым движениям. Если новорождённого слегка наклонить вперед, то он делает шаговые движения (автоматическая походка новорождённых). Иногда при ходьбе новорождённые перекрещивают ноги на уровне нижней трети голеней и стоп. Это вызвано более сильным сокращением аддукторов, что является физиологичным для этого возраста и внешне напоминает походку при детском церебральном параличе. Реакция опоры и автоматическая походка физиологичны до 1 — 1,5 месяцев, затем они угнетаются и развивается физиологическая астазия-абазия. Только к концу 1 года жизни появляется способность самостоятельно стоять и ходить, которая рассматривается как условный рефлекс и для своего осуществления требует нормальной функции коры больших полушарий. У новорождённых с внутричерепной травмой, родившихся в асфиксии, в первые недели жизни реакция опоры и автоматическая походка часто угнетены или отсутствуют. При наследственных нервно-мышечных заболеваниях реакция опоры и автоматическая походка отсутствуют из-за резкой мышечной гипотонии. У детей с поражением центральной нервной системы автоматическая походка задерживается надолго. Рефлекс ползания (Бауэра) и спонтанное ползание: Новорождённого укладывают на живот (голова по средней линии). В таком положении он совершает ползающие движения — спонтанное ползанье. Если к подошвам приставить ладонь, то ребёнок рефлекторно отталкивается от неё ногами и ползание усиливается. В положении на боку и на спине эти движения не возникают. Координации движений рук и ног при этом не наблюдается. Ползающие движения у новорождённых становятся выраженными на 3 — 4-й день жизни. Рефлекс физиологичен до 4 месяцев жизни, затем он угасает. Самостоятельное ползание является предшественником будущих локомоторных актов. Рефлекс угнетен или отсутствует у детей, родившихся в асфиксии, а также при внутричерепных кровоизлияниях, травмах спинного мозга. Следует обратить внимание на асимметрию рефлекса. При заболеваниях центральной нервной системы ползающие движения сохраняются до 6 — 12 месяцев, как и другие безусловные рефлексы. Хватательный рефлекс: Появляется у новорождённого при надавливании на его ладони. Иногда новорождённый так сильно обхватывает пальцы, что его можно приподнять вверх (рефлекс Робинзона). Этот рефлекс является филогенетически древним. Новорождённые обезьяны захватом кистей удерживаются на волосяном покрове матери. При парезахрук рефлекс ослаблен или отсутствует, у заторможенных детей — реакция ослаблена, у возбудимых — усилена. Рефлекс физиологичен до 3 — 4 месяцев, в дальнейшем на базе хватательного рефлекса постепенно формируется произвольное захватывание предмета. Наличие рефлекса после 4 — 5 месяцев свидетельствует о поражении нервной системы. Такой же хватательный рефлекс можно вызвать и с нижних конечностей. Надавливание большим пальцем на подушечку стопывызывает подошвенное сгибание пальцев. Если же пальцем нанести штриховое раздражение на подошву стопы, то происходит тыльное сгибание стопы и веерообразное расхождение пальцев (физиологический рефлекс Бабинского). Рефлекс Галанта: При раздражении кожи спины паравертебрально вдоль позвоночника новорождённый изгибает спину, образуется дуга, открытая в сторону раздражителя. Нога на соответствующей стороне часто разгибается в тазобедренном и коленном суставах. Этот рефлекс хорошо вызывается с 5 — 6-го дня жизни. У детей с поражением нервной системы он может быть ослаблен или вовсе отсутствовать в течение 1-го месяца жизни. При поражении спинного мозга рефлекс отсутствует длительно. Рефлекс физиологичен до 3 — 4-го месяца жизни. При поражении нервной системы эту реакцию можно наблюдать во второй половине года и позже. Рефлекс Переса: Если провести пальцами, слегка надавливая, по остистым отросткам позвоночника от копчика к шее, ребёнок кричит, приподнимает голову, разгибает туловище, сгибает верхние и нижние конечности. Этот рефлекс вызывает у новорождённого отрицательную эмоциональную реакцию. Рефлекс физиологичен до 3 — 4-го месяца жизни. Угнетение рефлекса в период новорождённости и задержка его обратного развития наблюдается у детей с поражением центральной нервной системы. Рефлекс Моро: Вызывается различными и не различными приемами: ударом по поверхности, на которой лежит ребёнок, на расстоянии 15 см от его головки, приподниманием разогнутых ног и таза над постелью, внезапным пассивным разгибанием нижних конечностей. Новорождённый отводит руки в стороны и открывает кулачки — 1 фаза рефлекса Моро. Через несколько секунд руки возвращаются в исходное положение — II фаза рефлекса Моро. Рефлекс выражен сразу после рождения, его можно наблюдать при манипуляциях акушера. У детей с внутричерепной травмой рефлекс в первые дни жизни может отсутствовать. При гемипарезах, а также при акушерскомпарезеруки наблюдается асимметрия рефлекса Моро. При резко выраженной гипертонии имеется неполный рефлекс Моро: новорождённый только слегка отводит руки. В каждом случае следует определить порог рефлекса Моро — низкий или высокий. У грудных детей с поражением центральной нервной системы рефлекс Моро задерживается надолго, имеет низкий порог, часто возникает спонтанно при беспокойстве, различных манипуляциях. У здоровых детей рефлекс хорошо выражен до 4 — 5-го месяца, затем начинает угасать; после 5-го месяца можно наблюдать лишь отдельные его компоненты. К концу 2-й и на 3-й недели жизни у ребёнка вырабат условный вестибуляр рефлекс на положение для кормления грудью. К концу 1-го месяца -защитный усл рефлекс (мигательные движения век) на звуковой раздражитель. В конце 2-го-на свет. С 2-месячного возраста--накопление условных рефлексов, обр-ся с участием всех анализаторов, развив дифференцировка сигналов, чётче становятся ориентировочные реакции. В 3 месяца-натуральный зрительный рефлекс на кормление грудью: ребёнок узнаёт мать, начинает гулить и др. В 4-месячном возрасте ребёнок различает основные спектрал цвета и музыкал тона; движения становятся более свободными, он тянет руку к игрушкам, ощупывает предметы. В возрасте 5 месяцев-узнаёт близких ему людей, отказывается брать чужую грудь, по-разному реагирует на неодинаковый тон обращения к нему. У 6-месячного ребёнка эмоциональные, мимические и голосовые реакции становятся более активными; он произносит отдельные слоги (“ма”, „ба", “па”), много двигается, пытается ползать, хорошо ест с ложечки и при её приближении открывает рот. В возрасте 7 месяцев ребёнок самостоятельно тянет в рот бутылочку, хорошо сидит и ползает, играет погремушками. В 8 месяцев отыскивает необходимые предметы взглядом, проявляет интерес к новым предметам, опираясь, становится на ноги. После 9 месяцев ребёнок правильно ориентируется в названиях некоторых предметов, узнаёт имена близких людей, выговаривает отдельные слова. В 6—7 мес при правильном воспитании ребенок начинает устанавливать связь некоторых слов с определенными предметами или действиями. Если взрослый, взяв ребенка на руки, будет неоднократно подносить его к какому-либо предмету, находящемуся на определенном месте, и, показывая на предмет подкреплять словами, например, «часы», «где часы?», то в 6—7 мес на вопрос: «где часы?» ребенок повернет голову в сторону называемого предмета и зафиксирует на нем свой взгляд. Однако слово в данном случае обозначает лишь один конкретный предмет. Например, слово «часы» обозначает лишь те часы, на которые показывала мать. И только к концу 1-го года (в 10—11 мес) в результате установления большого количества разнообразных связей с одним и тем же словом оно становится обобщенным, «сигналом множественных сигналов». На протяжении 2-го и 3-го года жизни при условии правильного воспитания быстро развивается деятельность второй сигнальной системы. Слова, понимаемые (сенсорная речь) и произносимые ребенком (активная речь), приобретают все более обобщенный характер. Обобщения ребенок делает в результате установления разнообразных связей одного и того же слова с разнообразными предметами и действиями, например, тогда, когда слово «киса» произносится и когда ему показывают белую пушистую кошку или маленькую серую или просто изображение кошки. Затем начинает объединять по наиболее характерным признакам: все что ползает (таракан, божья коровка, жук) объединяет словом «жук», всех людей в белых халатах (в магазине, парикмахерских и т. д.) — словом «доктор». Развитие второй сигнальной системы происходит на основе чувственного опыта ребенка, и между первой и второй сигнальной системой должно быть постоянное взаимодействие. Каждое слово, произносимое ребенком раннего возраста, должно опираться на чувственный образ. 7.Психомоторное и физическое развитие ребенка на первом году жизни. Под физическим развитием понимается динамический процесс изменений морфологических и функциональных признаков организма, обусловленных наследственными факторами и конкретными условиями внешней среды. Уровень физического развития и его темпы определяются социально-экономическими условиями, питанием, заболеваемостью и другими факторами. Под термином рост подразумевают количественное изменение размеров тела и его частей. Процессы роста подчиняются определенным законам и закономерностям. Физическое и психомоторное развитие детей в I полугодии. Вес тела доношенного новорожденного обычно составляет 3200–3500 г. Для расчета массы тела в I полугодии жизни можно использовать формулы: 1) масса тела может быть определена как сумма: Масса тела при рождении + 800 г x з, где з – число месяцев в течение I полугодия; 800 г – средняя ежемесячная прибавка массы тела в течение I полугодия; 2) масса тела ребенка 6 месяцев равна 8200 г, за каждый недостающий месяц вычитается по 800 г. Таким образом, за II полугодие ребенок прибавляет в весе 2 кг 850 г и к году должен весить в среднем 10,5 кг. к 4,5 месяцам происходит удвоение веса при рождении, к 1 году вес утраивается и составляет в среднем 10–10,5 кг. В первые годы жизни весовая прибавка составляет в среднем 2 кг, в препубертатном периоде – 5–6 кг. 1мес - 600г. 2 мес - 800г. 3 мес- 800г. 4 мес - 750г. 5 мес - 700г. 6 мес – 650г. 7 мес- 600г. 8 мес- 550г. 9 мес – 500г. 10 мес- 450г. 11 мес – 400г. 12 мес – 450 г. От 1 года до 2 – 2500-2600г. ОТ 2-3 лет – 2200г Маловесные дети дают убыль веса около 9 %; у детей, рожденных до 1000 г, убыль веса доходит до 15 %. Восстановление веса у них происходит медленно – до двух и более недель. Достижение веса нормального доношенного ребенка до 3200–3500 г и длины 50–51 см у недоношенных и маловесных происходит к 1–1,5 месяцам (2000–2500 г масса тела при рождении), к 2–2,5 месяцам (1500–2000 г) и к 3–3,5 месяцам (1000 г). Для II полугодия жизни ориентировочную массу тела можно рассчитать по формулам: 1) масса тела при рождении + плюс прибавка массы тела за II полугодие:(800 х 6) + 400г ч (n – 6), где n – возраст в месяцах; 400 г – средняя ежемесячная прибавка массы тела за II полугодие; 2) масса тела ребенка 6 месяцев равна 8200 г, за каждый последующий месяц прибавляется по 400 г (у детей до 12 месяцев). Рост новорожденного ребенка 50 см (возможны колебания роста от 45 до 55 см). Ежемесячные прибавки роста составляют в первом полугодии по 2–1 см. За первый год жизни ребенок вырастает на 25 см, и рост его к году достигает 75 см. На втором году жизни рост увеличивается на 12 см, за третий год – на 7–8 см, в дальнейшем за год ребенок вырастает на 5 см, и к 4 годам его рост удваивается, а к 12 годам – утраивается по сравнению с ростом при рождении. Рост ребенка с 7 по 9-й месяц увеличивается ежемесячно на 2 см, а с 9 по 12-й месяц – на 1,5–1 см. Таким образом, во II полугодии ребенок вырастает на 10 см. Психомоторное развитие детей в I полугодии. В возрасте 2 месяцев ребенок спокойно бодрствует, подолгу рассматривает висящие над ним игрушки, улыбается, когда с ним разговаривают, начинает держать или хорошо держит головку. В 3 месяца ребенок на обращенную к нему речь отвечает улыбкой, звуками, оживленными движениями рук и ног. Долго лежит на животе, поддерживаемый под мышки, крепко упирается ногами, согнутыми в тазобедренных суставах, хорошо держит голову. ощупывает руки, перебирает руками одеяло, пеленки. В 4 месяца он начинает гулить, по звуку определят местонахождение предмета, издающего звук, подолгу занимается висящими над кроваткой игрушками. В 5 месяцев он подолгу гулит, пускает пузыри, знает близких ему лиц, различает интонацию, с которой к нему обращаются. Движения его рук четкие, Он берет погремушку и долго держит ее в руке. Переворачивается со спины на живот, крепко упирается ножками, стоит при поддержке. В 6 месяцев он начинает произносить отдельные слова («ма», «ба», «да» и др.). Свободно сам берет игрушку и подолгу ею играет.Переворач с живота на спину, начинает передвигаться по манежу, немного подползая. При виде подносимой пищи сам открывает рот, хорошо ест из ложечки. к 7-8 месяцам появляется координация движений, устанавливается ползание. возникает лепет. ребенок подолгу лежит, играя погремушкой, стучит, размахивает ею. Хорошо ползает, легко садится, держась за пальцы взрослого; стоит, держась за барьер. . Выполняет по просьбе движения «ладушки». Игрушками постукивает, рассматривает их.Сам садится, сидит, ложится. В 8-9 месяцев ребенок стоит в кроватке, переступает ногами вдоль спинки кровати. К году делает первые шаги. Некоторые дети начинают ходить с 10-11 месяцев, другие с 1 года 4 месяцев. усиливается эмоциональная деятельность. на заигрывание «догоню, догоню», играет в прятки, выполняет по просьбе взрослых некоторые движения – «дай ручку», «до свидания» и пр. На 10-11 месяце ребенок произносит отдельные слова, к году-10-12 слов. он знает название некоторых предметов и имена людей, повторяет за взрослыми разнообразные звуки и слоги. он выполняет несложные поручения, сосредоточенно играет; накладывает один предмет на другой, снимает и надевает кольцо и др. В 1,5 года ребенок произносит целые предложения, с интересом рассматривает картинки. В два года ребенок может воспринимать несложные сказки и рассказы. К третьему году речь занимает ведущее место в общении. Окружность головы 6-месячного ребенка равна 43 см, в дальнейшем окружность головы за каждый последующий месяц увеличивается на 0,5 см. Окружность груди у детей в 6 месяцев равна 45 см, за каждый последующий месяц (до года) она увеличивается на 0,5 см. Молочные зубы прорезываются в следующие сроки: центральные нижние и верхние резцы – в период от 6до9 месяцев, боковые нижние и верхние резцы – от 9 до 12 месяцев. В конце года жизни у ребенка имеется обычно 8 зубов.
Возраст (в месяцах) |
Основные навыки |
1 - 1,5 |
Лежа на животе поднимает голову. Улыбается. |
2 |
Лежа на животе приподнимается на руках, гулит. |
3 |
Следит взглядом за игрушками |
4 |
Переворачивается с живота на спину. Громко смеется. Оборачивается на голос. Узнает мать. |
5 |
Переворачивается со спины на живот. Хватает погремушку.Отличает чужих от близких. |
6-7 |
Сидит без поддержки. Берет предметы одной рукой. |
8-9 |
Ползает. Встает, держась за опору. Произносит папа , мама неосознанно |
10-11 |
Называет родителей папа и мама. Понимает слово "нет".Знает свое имя, название частей тела. |
12 |
Самостоятельно ходит. Пьет из чашки. |
15 |
Бегает. Правильно называет 4-6 предметов, когда ему указывают на них |
18 |
Рисует каракули. Называет предмет по картинке. Употребляет 7- 20 слов. Пользуется ложкой. |
24 |
Строит предложения из двух слов. Употребляет 50 слов. Находит нужную картинку |
30 |
Идет по лестнице, меняя ноги. Строит дом из кубиков. Зовет себя : Я. |
36 |
Стоит на одной ноге. Ездит на трех колесном велосипеде. Рисует окружность, крест. Знает стихи. Моет руки. |
48 |
Строит из кубиков по модели. Играет в ролевые игры с детьми. Рассказывает истории |
 8.Влияние
внешней среды на физическое и психическое
развитие ребенка. Интеллектуальное,
эмоциональное развитие ребенка. Роль
семьи.
Большое значение в раннем
возрасте имеет способность к обучению
при помощи импритинг а («запечатления»
образца поведения).
В течение первого
года жизни младенцы все лучше знакомятся
со своими родителями и другими значимыми
для них людьми из их социального
окружения. У ребенка
появляется чувство доверия и формируется
привязанность к любимому человеку.
Формирование привязанности многокомпонентно
и синхронно; процесс развития взаимодействия
матери и ребенка происходит благодаря
стимулам, вызывающим взаимную любовь
(установление контакта
«глаза в глаза», прикосновения, голос
матери, подражательное обучение,
ритмичный разговор, тренировка движений
ребенка, запах матери, тепло матери,
бактериальная флора матери, крик ребенка,
запах ребенка и т. д.). Новорожденные,
которые воспитываются в семье, постоянно
слышат голоса родителей и видят их лица.
Близкие люди являются сильными
стимулами раннего формирования
коммуникативных функций новорожденного.
Физическая близость с матерью, являющаяся
в первые месяцы жизни своеобразным
продолжением внутриутробного
существования, формирует
чувство защищенности и оптимального
эмоционального состояния ребенка.
Поведение и характер
ребенка, достигшего школьного возраста,
в значительной степени определяется
вниманием тех людей, которые ухаживали
за ним в раннем детстве. Дети, которые
воспитывались родителями, как правило,
более приспособлены к школьной жизни.
Если же ребенка воспитывали бабушка
или дедушка, такие дети хуже адаптируются
к школе, у этих детей значительно хуже
развиты координированные движения.
Дети, которые воспитываются в детских
учреждениях (яслях, детских садах),
отличаются более ранним
формированием и совершенствованием
двигательных умений, в то же время
у них хуже развиты речевые навыки и
образное мышление. В зависимости от
условий среды, воспитания и различных
заболеваний у ребенка может задерживаться
нормальное развитие высшей нервной
деятельности, поэтому врач-педиатр
должен давать советы родителям по
гармоничному воспитанию детей.
В
первую очередь физическое развитие
зависит от питания, от обеспеченности
организма необходимым для развития
полным комплексом питательных веществ
— нутриентов: белков, жиров, углеводов,
минеральных солей, витаминов и множества
других веществ, соблюдается ли режим
занятий и отдыха, верно ли дозируются
физические и умственные нагрузки. Резкие
отклонения от нормы физического развития
— сигнал для родителей: они здесь
упускают что-то важное, необходимо
предпринять все меры к оздоровлению
ребенка.
Экологические
факторы, атмосферное давление,
температура окружающей среды постоянно
взаимодействуют на организм ребенка.
Под влиянием нагрузки и положительных
эмоций от физических упражнений, занятий
спортом на свежем воздухе, организм
ребенка функционально изменяется.
Ребенок,
приученный с детства к физкультурным
занятиям, занимается ними охотно, с
радостью и удовольствием. Такой
ребенок будет расти не только крепким
физически, но и лучше развит интеллектуально,
ведь эти два развития неразрывно
соединены друг с другом. Отлично, если
ребенок в будущем достигнет высоких
спортивных достижений, но, даже просто
занимаясь физическими упражнениями,
он сможет избежать многих заболеваний,
вырасти активным и здоровым.
Также
одним из важных факторов являются
ультрафиолетовые лучи.
Именно поэтому нарастание массы тела
и роста изменяются в зависимости от
времени года. Определенно, набор массы
тела и роста в какой-то мере зависят от
географического и климатического
местонахождения. Увеличение роста
костей и усиление обмена веществ
происходит за счет совершаемых движений
ребенком. Отсюда значение воспитательной
педагогической работы и особенно в
области физического воспитания и
организации образа жизни ребенка
(достаточное пребывание на свежем
воздухе, нормальный сон, активный
двигательный режим). Физическое развитие
организма в целом служит для измерения
функциональной зрелости всего
организма.
9.Законы нарастания массы
тела ребенка в различные возрастные
периоды.
Вес тела доношенного
новорожденного обычно составляет
3200–3500 г. Индивидуальные различия
доволь-
но велики
от 2600 г до 4500 г и более. Доношенные
новорожденные дети
с
массой тела 2500 г и ниже считаются
родившимися с задержкой внутриутроб-
ного
развития, а с массой 4500 r
и более — крупными.
После рождения
в течение первых дней происходит
незначительная, так
называемая
физиологическая потеря
первоначальной массы тела
в пределах
5
— 8% исходной, т. е. 150 — 300 г. Основной
причиной может быть недоедание
в
первые 3 дня, связанное с медленным
нарастанием лактации, а также с
позд-
ним
прикладыванием к груди и недостаточным
поступлением жидкости в ор-
ганизм,
с выделением мекония, мочи, начавшимися
потерями через кожу и
легкие,
высыханием пуповинного остатка.
Обычно масса тела восстанавливает-
ся
к 7 — 8-му дню жизни, иногда этот
процесс идет более медленно и
заканчи-
вается
к 11 — 12-му дню жизни.
Для расчета
массы тела в I полугодии жизни можно
использовать формулы: 1) масса тела
может быть определена как сумма:
Масса тела при рождении +
800 г x з, где з – число
месяцев в течение I полугодия; 800 г –
средняя ежемесячная прибавка массы
тела в течение I полугодия; 2) масса
тела ребенка 6 месяцев равна 8200 г, за
каждый недостающий месяц вычитается
по 800 г.
Таким образом, за II
полугодие ребенок прибавляет в весе
2 кг 850 г и к году должен весить в
среднем 10,5 кг.
к 4,5 месяцам происходит
удвоение веса при рождении, к 1 году
вес утраивается и составляет в
среднем 10–10,5 кг. В первые годы жизни
весовая прибавка составляет в среднем
2 кг, в препубертатном периоде – 5–6
кг.
1мес - 600г.
2 мес - 800г.
3 мес-
800г.
4 мес - 750г.
5 мес - 700г.
6 мес –
650г.
7 мес- 600г.
8 мес- 550г.
9 мес –
500г.
10 мес- 450г.
11 мес – 400г.
12 мес
– 450 г.
От 1 года до 2 – 2500-2600г.
ОТ
2-3 лет – 2200г
Маловесные дети дают
убыль веса около 9 %; у детей, рожденных
до 1000 г, убыль веса доходит до 15 %.
Восстановление веса у них происходит
медленно – до двух и более недель.
Достижение веса нормального доношенного
ребенка до 3200–3500 г и длины 50–51 см у
недоношенных и маловесных происходит
к 1–1,5 месяцам (2000–2500 г масса тела при
рождении), к 2–2,5 месяцам (1500–2000 г) и к
3–3,5 месяцам (1000 г).
Нормальными
колебаниями массы тела на первом году
жизни можно
считать
величины, отклоняющиеся не более чем
на 9 — 10% от средних пока-
зателей
в большую или меньшую сторону.
Для
II полугодия жизни ориентировочную массу
тела можно рассчитать по
формулам:
1) масса тела при рождении
+ плюс прибавка массы тела за II
полугодие:(800 х 6) + 400г ч (n – 6), где n –
возраст в месяцах; 400 г – средняя
ежемесячная прибавка массы тела за II
полугодие;
2) масса тела ребенка 6
месяцев равна 8200 г, за каждый последующий
месяц прибавляется по 400 г (у детей
до 12 месяцев).
На втором году жизни
прибавка массы тела составляет 2,5 кг,
а в препу-
бертатном
и пубертатном периоде достигает иногда
5 — 6 кг в год. Масса тела
в
возрасте 2—11 лет равна: 10,5 + 2п, где
п — возраст ребенка до 11 лет,
а
10,5 кг — средняя масса годовалого
ребенка.
Не всегда показатели массы
тела и длины тела нарастают параллельно.
В процессе развития
происходит чередование
периодов преимущественного
роста
в длину с ростом в «ширину».
Так называемый период первой
полноты
наступает
в возрасте 3 — 4 лет. Период первого
вытягивания наступает
от 4 до
5,5
лет у мальчиков и после 6 лет у
девочек. Период второй
полноты (преиму-
щественный
рост в «ширину») — 8 — 10 лет. Период
второго вытягивания-
11—12
лет у мальчиков и 9—10 лет у девочек.
10.Законы нарастания роста и пропорции
детского тела в различные возрастные
периоды.
Рост новорожденного
ребенка 50 см (возможны колебания роста
от 45 до 55 см). Ежемесячные прибавки роста
составляют в первом полугодии по 2–1
см.
. Чем
младше
ребенок, тем интенсивнее его рост. В
первые 3 месяца жизни длина
тела
увеличивается на 3 см ежемесячно, или
на 9 см за квартал, во 2-м кварта-
ле
— на 2,5 см ежемесячно, в 3-м квартале —
на 1,5 см и в 4-м кварта-
ле
— на 1 см в месяц. Рост ребенка с 7 по 9-й
месяц увеличивается ежемесячно на 2 см,
а с 9 по 12-й месяц – на 1,5–1 см. Таким
образом, во II полугодии ребенок вырастает
на 10 см.
За первый год
жизни ребенок вырастает на 25 см, и
рост его к году достигает
75 см. На втором году жизни рост
увеличивается на 12 см, за третий год –
на 7–8 см, в дальнейшем за год ребенок
вырастает на 5 см, и к 4 годам
его рост удваивается,
а к 12 годам – утраивается
по сравнению с ростом при рождении.
С 2 до 12 лет долженствующую длину тела
можно вычислить по фор-
муле:
возраст (годы) х 6+ 77 см.
После
этого с 11 — 12 лет у мальчиков и с 9 — 10
лет у девочек начинается новое ускорение
роста с достижением максимума роста
в возрасте от 13,5 до 15,5 лет у мальчиков
(в среднем по 8 — 10 см и более в год) и в
возрасте 10 — 115 лет у девочек, однако
могут быть
индивидуальные разли-
чия,
связанные с типом конституции. Вытягивание
мальчиков 11 — 12 лет идет
исключительно
за счет нижних конечностей. Между
14 и 15 годами ноги пере-
стают
расти и наступает пик скорости роста
для туловища. У девочек эти осо-
бенности
относятся соответственно к 9 и 11—12
годам. Прекращение роста
в
длину происходит у юношей в 18—19 лет, у
девушек — в 16—17 лет.
11.Анатомо-физиологические особенности
кожи, подкожно-жировой клетчатки,
лимфатической системы у детей.
Кожа состоит
из эпидермиса и дермы.
Эпидермис
у новорожденных и детей 1-го года жизни,
как и у детей более старшего возраста
и у взрослых, имеет многослойную
структуру. Однако он значительно
тоньше. Роговой слой
эпидермиса содержит много влаги, очень
тонкий, рыхлый, состоит из 2—3 рядов
ороговевших, слабо связанных между
собой клеток, роговые пластинки легко
отторгаются. Это определяет легкую
ранимость эпидермиса. Процесс
митотического деления клеток совершается
интенсивно не только в базальном, но и
в шиловидном и зернистом слоях, чем
объясняется быстрая смена слоев
эпидермиса у детей.
Дерма
(собственно кожа) у новорожденных и
детей грудного возраста тоньше,
чем в старшем возрасте, и отличается по
структуре. Дерма состоит из двух слоев:
верхнего — сосочкового
и нижнего — сетчатого.
Характеризуется преимущественно
клеточным строением и слабым
развитием эластических, коллагеновых,
аргирофильных, мышечных волокон;
содержит много недифференцированных
соединительнотканных, в том числе
тучных, клеток. Только к
6 годам гистологическое строение
дермы приближается к таковому у взрослых,
хотя коллагеновые волокна еще тонкие,
а эластические волокна развиты
слабо.
Кожные покровы ребенка
раннего возраста не случайно часто
становятся «органом-мишенью» аллергических
реакций. В эпидермисе, дерме и подкожной
клетчатке имеется относительно большее,
чем у детей старшего возраста, количество
клеток, участвующих в распознавании,
представлении и эффекторном ответе
(клетки Лангенгарса, тучные клетки,
лимфоциты, эозинофилы). Кожа
новорожденного и ребенка раннего
возраста богата кровеносными
сосудами, пронизана густой сетью
широких капилляров. Стенки большинства
сосудов представлены одним рядом
эндотелиальных клеток, им свойственна
повышенная проницаемость. Наружное
применение препаратов йода может
привести к угнетению функции щитовидной
железы. По этим же причинам опасность
генерализации инфекций на коже у детей
первых лет жизни гораздо выше, чем в
более старшем возрасте.
Потовые
эккринные железы сформированы уже к
моменту рождения. Однако в течение
первых 3—4 месяцев они слабо проявляют
свою функциональную активность, имеют
недоразвитые выводящие протоки.
Дальнейшее созревание структур потовых
желез, вегетативной нервной системы и
терморегулирующего центра центральной
нервной системы обеспечивает
совершенствование потоотделения.
Адекватность потоотделения
складывается в течение первых 7 лет
жизни. Полное развитие апокринних
потовых желез происходит в первый год
жизни. Начинают они функционировать
к 8-10 годам, но активно—в период полового
созревания.
Сальные железы у
новорожденных гистологически не
отличаются от желез у взрослых. Они
активно функционируют в грудном возрасте
и распространены по всей коже, за
исключением ладоней и подошв. Особенно
их много в области лица,
волосистой части головы, спины, ануса,
гениталий. У новорожденных часто
на коже кончика и крыльев носа, а иногда
и на прилегающих участках кожи щек
имеются желтовато-белые
точки (milia) — избыточное скопление
секрета в поверхностно расположенных
кожных сальных железах. После 1-го
года жизни функция сальных желез
значительно снижается (часть желез
вообще полностью атрофируется) и
усиливается лишь в период
полового созревания. Себорея
(seborrhoea) - патологическое состояние кожи,
обусловленное усиленной функцией
сальных желез. Сухая себорея нередко
сопутствует экссудативному диатезу.
Волосы на голове новорожденного
не имеют сердцевины.
Возрастной особенностью является
замедленный рост волос в
первые 2 года жизни (0,2 мм ежедневно
по сравнению с 0,3—0,5 мм у детей старшего
возраста) и быстрая их смена.
На первом году жизни волосы сменяются
несколько раз. С возрастом толщина
волос на голове увеличивается. Брови
и ресницы у новорожденных развиты
сравнительно мало, но в дальнейшем
растут быстро, и у детей 3-5 лет они
достигают почти такой же длины, как и у
взрослых. В области лобка, в подмышечных
впадинах волосы появляются в период
полового созревания; к этому же времени
начинается их рост на лице у
мальчиков.
Функциональные особенности
кожи новорожденного и ребенка первых
лет жизни.
Защитная функция кожи
от неблагоприятных внешних воздействий
(механических, химических, инфекционных)
имеет ряд особенностей. Легкая ранимость
кожи обусловлена тонкостью рогового
слоя эпидермиса, незрелостью местного
иммунитета, малой плотностью кожи ввиду
слабого развития упругих
эластических и
коллагеновых волокон. рН кожи
новорожденного составляет 6,7 — близко
к нейтральной среде. В то же время у
детей более старшего возраста
водно-липидная мантия с кислой реакцией
(рН 4,5—6,0) препятствует проникновению
в кожу микробов и ослабляет или
нейтрализует повреждающее действие
химических веществ. Систематическая
мацерация кожи мочой и калом способствует
разжижению водно-липидной мантии
эпидермиса. Бактерицидные свойства
кожи снижаются также при ее обезжиривании
(спиртом, эфиром и т. п.) и охлаждении
организма. Согревание,
наоборот, повышает защитную функцию
кожи. Низкий уровень образования
пигмента меланина в меланоцитах
базального слоя эпидермиса делает кожу
грудных детей чувствительной
к повреждающему действию солнечных
лучей. Поэтому следует с особой
осторожностью назначать им ультрафиолетовое
облучение.
Терморегулирующая
функция кожи у новорожденных и детей
первых месяцев жизни несовершенна.
Они предрасположены к
переохлаждению и перегреванию. Это
связано с большей поверхностью тела,
тонкостью и нежностью кожных покровов,
хорошо развитой сосудистой сетью в
сочетании с несовершенством
регуляции кровотока в коже, слабым
функционированием потовых желез,
незрелостью центров терморегулции.
Тонкость
эпидермиса и слабое развитие
соединительнотканных волокон
дермы обусловливают их повышенную
чувствительность. Раздражение кожи
при плохом уходе (мокрые, грязные
пеленки), различных кожных заболеваниях
может явиться причиной беспокойства
ребенка, нарушения сна, отражаясь на
состоянии нервной системы и всего
организма в целом. С ростом ребенка
нервный аппарат кожи становится менее
доступным для внешних раздражителей.
Кожа
является местом образования ферментов,
биологигески активных веществ, витамина
D.
Жировая ткань начинает формироваться
на 4—5-м месяце внутриутробного
развития. Вначале жир откладывается
на голове и шее, затем на туловище
и позднее на верхних и нижних конечностях.
У новорожденного общее колигество
жировой ткани тесно связано со сроками
гестации и у доношенного ребенка
составляет до 14-16% от массы тела:
В
постнатальном периоде происходит
интенсивное накопление
жира внутри клеток
белой жировой ткани. Уже к 5 месяцам
отмечают увеличение его содержания
в организме почти в 3 раза.
У
новорожденных хорошо развита бурая
жировая ткань. Наибольшие скопления
ее находятся в межлопаточной
и аксиллярной областях, в области
щитовидной и зобной желез, перикарда,
вокруг пищевода, почек
и надпочечников,
трахеи, в брыжейке тонкой кишки, в
паху и
по ходу больших сосудов.
У доношенного новорожденного масса
бурой жировой ткани составляет 1—3%
от всей массы тела. Основной функцией
бурой жировой ткани является так
называемый несократительный термогенез,
т. е. теплопродукция, не связанная с
мышечным сокращением. Максимальная
способность к теплопродукции бурой
жировой ткани определяется в первые
дни жизни. С возрастом способность бурой
жировой ткани к теплопродукции снижается,
она постепенно заменяется белой.
Глубоконедоношенные и дистрофированные
дети с малым запасом бурой жировой ткани
очень легко охлаждаются и нуждаются в
согревании.
Особенностью подкожной
клетчатки у новорожденных и грудных
детей является сохранение
в ней участков ткани эмбрионального
характера, обладающей как
жиронакапливающей, так и кровообразующей
функцией. Подкожную жировую клетчатку
детей раннего возраста считают
ретикулогистиоцитарньм органом,
напоминающим по гистогенезу и функциям
костный мозг. По химическому составу
подкожная клетчатка новорожденных и
детей грудного возраста отличается от
клетчатки взрослого: в ней содержится
больше твердых
жирных кислот - пальмитиновой и стеариновой
и меньше — жидкой олеиновой кислоты.
Преобладание содержания твердых жирных
кислот с более высокой точкой плавления
обеспечивает более плотный тургор
тканей детей первого года жизни и
наклонность к образованию локальных
уплотнений и отека кожи и подкожной
жировой клетчатки (склерема,
склередема).
Максимального содержания
подкожного жира ребенок достигает
примерно в 9-месячном
возрасте. В течение 1—3-го года
жизни увеличение жировой ткани происходит
как за счет увеличения количества
жировых клеток (липоцитов),
так и за счет увеличения их
размеров. После 6-летнего возраста
более интенсивно происходит увеличение
размеров жировых клеток.
Больше жира откладывается на
лице, где жировые тела щеки (тела Биша)
содержат много твердых жирных кислот,
на ягодицах, бедрах, животе (здесь
преобладает содержание жидких кислот).
Исчезает подкожная жировая клетчатка
вначале на животе и груди, затем на
конечностях и в последнюю очередь
на лице.
Как и в организме взрослого,
у ребенка жировая ткань играет роль
механигеской защиты и стабилизации
внутренних органов, сосудов и
нервных стволов, участвует в
гомеостазировании температуры
тела.
Лимфоузлы. Закладка на
2-м месяце внутриутробной жизни. С этого
же времени (и до конца жизни)
осуществляется их кроветворная
функция — продукция лимфоцитов.
К 5-му месяцу в отдельных лимфоузлах
можно видеть намечающуюся границу между
будущим корковым и мозговым веществом,
развивается капсула лимфоузлов.
Лимфоузлы состоят из паренхиматозной
(лимфоидной) ткани с крупными синусами
и ограничены очень нежной и тонкой
капсулой. Элементы ретикулярной и
соединительнотканной стромы узла
(трабекулы, перегородки)
и капсулы практически отсутствуют.
Недостаточна дифференцировка
иммунокомпетентных клеток лимфатических
узлов. По этим причинам плохо
осуществляется защитная (барьерная)
функция.
После года барьерная
функция лимфоузлов возрастает, они
задерживают микробы, отвечая на внедрение
инфекции островоспалительной гнойной
(при кокковой флоре) или казеозной (при
туберкулезной инфекции) реакцией. Этим
объясняют высокую частоту лимфаденитов
у детей в возрасте 1—3 лет.
К 7-8 годам
в лимфатических узлах образуются
соединительнотканные перегородки
(трабекулы), более узкими становятся
синусы. Лимфатические синусы - это
щели между капсулой, трабекулами и
паренхимой лимфатического узла, по
которым течет лимфа. Это действенный
барьер, задерживающий микробов, опухолевые
клетки, инородные частицы. Появляется
возможность местного иммунологического
подавления инфекции. В связи с этим
возникает реакция лимфатического узла
на инфекцию в виде увеличения его
размера, болезненности. Для детей
дошкольного и младшего школьного
возраста характерны периферические
лимфадениты, увеличение носоглоточной
миндалины (аденоиды), небных миндалин
и т. д В возрасте 1 — 3 лет лимфатические
узлы имеют довольно хорошо развиты и
реагируют на внедрение возбудителя
местной воспалительной
реакцией.
К 12 — 13 годам строение и
функция лимфатических узлов соответствуют
таковым взрослого человека. Они
задерживают и подавляют проникшую в
них патогенную флору без видимых
изменений или кратковременно увеличиваясь
в размерах и в дальнейшем нормализуясь.
В период полового созревания рост узлов
останавливается, и они частично
подвергаются обратному развитию.
Возрастная инволюция лимфоидной ткани,
ее замещение соединительной, жировой
тканями так же характерна для периферических
органов иммунной системы, как и для
центральных.
12.Анатомо-физиологические
особенности костной и мышечной систем
у детей.
В скелете человека
различают более 200 костей. В зависимости
от выполняемых функций отдельные кости
имеют различное внутреннее строение.
Выделяют четыре основных вида костей:
трубчатые, губчатые, плоские, смешанные.
Все кости состоят из следующих основных
компонентов: клеток, органического
матрикса, минеральных веществ. Костная
ткань детей содержит больше
воды, чем у взрослых.
В
первые годы жизни происходят интенсивные
процессы переформирования костной
ткани, от грубоволокнистого до
пластинчатого строения. Костная
ткань в это время особенно чувствительна
к воздействию неблагоприятных факторов.
У
детей раннего возраста в строении
скелета хрящевая ткань
представлена в большей степени, чем у
взрослого человека. У новорожденного
кости черепа, диафизы трубчатых костей
состоят из костной ткани; эпифизы
бедренной и большеберцовой костей,
таранная, пяточная, кубовидная кости,
тела позвонков и дуги имеют только
точки окостенения. Большинство
эпифизов, все губчатые кости кистей,
часть губчатых костей стоп представлены
хрящевой тканью. Точки окостенения
в них после рождения появляются в
определенной последовательности.
Совокупность имеющихся у ребенка точек
окостенения называется «костным
возрастом» и характеризует уровень
биологического развития.
Интенсивный
рост и переформирование костной ткани
поддерживаются специфическим для
детского возраста обильным
кровоснабжением, что предрасполагает
к более частому развитию гематогенных
остеомиелитов, чем у
взрослых.
Продольный рост
костей происходит за счет развития
ростковой хрящевой
ткани в метаэпифизарных зонах (зоны
роста), которые страдают в первую
очередь при различных патологических
процессах (рахит, остеомиелит, ревматоидный
артрит), длительном приеме гормональных
препаратов.
Поперечный рост
костей обеспечивается надкостницей,
которая у детей имеет выраженную толщину
и функциональную активность. Данные
особенности надкостницы имеют также
большое значение при травматических
повреждениях в качестве защитного
фактора (переломы без
смещения костных фрагментов по типу
«зеленой веточки»).
Череп
ребенка после рождения имеет следующие
особенности. Стреловидный, венечный,
затылочный швы закрываются с
3—4-месячного возраста. Боковые
роднички у доношенных новорожденных
закрыты. Задний (малый) родничок
располагается на уровне затылочных
швов теменных костей. Он открыт до 4-8
недель после рождения у 25%
новорожденных. Передний (большой)
родничок, расположенный в месте
соединения венечного и продольного
швов в виде ромба, может иметь различные
размеры. Расстояние между средними
точками противостоящих краев может
составлять от 3 х 3 см до 1,5 х 2 см. Закрытие
большого родничка происходит к 12-18
месяцам.
Формирование зубов
начинается с конца второго месяца
внутриутробного развития из двух
зачатков: из эпителиальной закладки -
эмаль, из мезенхимальной закладки
— дентин.
Молочные зубы
прорезываются начиная с 5 месяцев.
Ориентировочная формула для определения
количества зубов до двух лет жизни:
п — 4, где п — количество месяцев. Полный
молочный прикус должен быть у
ребенка к двум годам жизни.
Время сохранения молочных зубов и
появления постоянных называют периодом
сменного прикуса (в среднем от 5 до 12
лет).
Позвоночник у детей раннего
возраста имеет выраженную подвижность
и гибкость, что определяется большим
количеством хрящевой
ткани. Между вторым и четвертым
месяцами, когда ребенок начинает активно
поднимать и удерживать голову,
появляется передний
изгиб шейной части
позвоночника. После начала
ходьбы формируются
изгибы поясничного (лордоз) и
грудного отдела позвоночника
(кифоз).
Фиксация позвоночника
несовершенна, что связано
с развитием мышц, и легко приводит к
сколиозам и патологическим
осанкам. Нарушение осанки —
отклонение позвоночника в сагиттальной
и фронтальной плоскости, которая
определяется состоянием мышечного
тонуса и привычностью для ребенка
измененной позы. Патологические
осанки приводят к нарушениям функции
внутренних органов.
Грудная клетка
у детей первого года жизни характеризуется
превалированием поперечного
диаметра, горизонтальным расположением
ребер и малой длиной. В дальнейшем за
счет роста грудной клетки в длину и
увеличения переднего диаметра
опускаются передние концы ребер.
Данный процесс происходит до 12 лет.
Резкое увеличение поперечного
диаметра грудной клетки происходит к
15 годам.
Таз у детей раннего
возраста имеет форму воронки.
Интенсивный рост костей таза происходит
до 6 лет. С 11—12 лет наиболее интенсивное
развитие костей таза отмечают у девочек.
К 15 годам соотношение межакромиального
и межтрохантерного расстояний у девочек
составляет около 1,15, у мальчиков - 1,3 и
более.
Осмотр костной системы
проводится в определенной по
следовательности: в фас, сбоку, со спины,
определяется также нарушение походки.
Мышцы
у новорожденного и ребенка грудного
возраста развиты слабо; они составляют
около 25 % массы его тела, тогда
как у взрослого — не менее 40—43 % У детей
первых месяцев жизни отмечается
повышенный тонус мышц, так
называемая физиологическая
гипертензия, которая связана с
особенностями функционирования
центральной нервной системы. Тонус
сгибателей преобладает над тонусом
разгибателей; этим объясняется тот
факт, что дети грудного возраста, если
их распеленать, обычно лежат с согнутыми
руками и ногами. Постепенно эта гипертензия
исчезает.
Сила и тонус мышц у
ребенка слабые. Двигательная способность
появляется сначала у мышц шеи и
туловища, а потом уже у мышц конечностей.
Мышечная сила постепенно нарастает.
Особенно интенсивно развивается
мускулатура в период полового созревания,
происходит нарастание силы и точности
движений. Мальчики обычно отличаются
лучшим мышечным тонусом, чем девочки.
Формирование и рост мышечных волокон
заканчивается к 20—23 годам.
При
обследовании детей обращают внимание
на силу и тонус мышц. Сила мышц у детей
грудного возраста измеряется лишь
приблизительно путем определения того
усилия, которое необходимо для
противодействия тому или другому
движению ребенка; у детей старшего
возраста сила мышц измеряется, так же
как и у взрослых, с помощью динамометра.
Мышечная сила у детей раннего возраста
определяется попыткой отнять игрушку.
У детей более старшего возраста проводится
ручная динамометрия.
В 1—2 мес ребенок
должен удерживать голову в вертикальном
положении, в 3— З,5 мес — при поддержке
подмышки упираться ногами, в 6 мес —
самостоятельно сидеть и поворачиваться
со спины на живот и обратно, в 7—8 мес
ползать, в 10 мес — стоять без опоры, в
12 мес — делать первые самостоятельные
шаги.
13.Анатомо-физиологические
особенности сердечно-сосудистой системы
у детей. Внутриутробное кровообращение
плода. Частота пульса и кровяное давление
у детей. Скорость кровотока и минутный
объем сердца.
прослушивание
сердечных тонов через брюшную стенку
матери возможно с IV месяца беременности.
Обогащенная кислородом кровь
поступает из плаценты через венозный
(аранциев) проток в нижнюю полую вену
и смешивается там с венозной кровью,
оттекающей от нижних конечностей.
Большая часть этой смешанной крови
благодаря специальной заслонке нижней
полой вены (евстахиева заслонка) в
правом предсердии направляется через
овальное окно в левое предсердие,
левый желудочек, а оттуда в аорту и через
подключичные артерии к мозгу и верхним
конечностям.
Внутриутробное
(фетальное, плацентарное) кровообращение.
Газообмен и обмен
продуктов метаболизма осуществляются
в плаценте , система кровообращения
которой сообщается с системой
кровообращения плода через пупочный
канатик (пуповину), включающий: 1) одну
пупочную вену (ток крови в сторону
плода), 2) две пупочные артерии (ток крови
в сторону плаценты). При этом кровь плода
и матери не смешивается.
ешивается.
Кровь от материнской плаценты через
пупочную вену плода притекает в его
нижнюю полую вену, где, смешиваясь
с его венозной кровью от нижней
половины тела, заполняет правое
предсердие.
Отсюда основной поток
идет через открытое
овальное окно, т.е. отверстие
(дефект) в межпредсердной перегородке в
левое предсердие и левый желудочек и
дальше – в большой круг. Это —
первый физиологический, естественный
шунт. Из левого желудочка часть
крови идет в аорту и сосуды головы и
верхней половины тела. А та часть крови,
которая в правых отделах прошла в правый
желудочек через трехстворчатый клапан,
а затем — в легочную артерию, уходит в
нисходящую аорту
через второй физиологический шунт —
открытый артериальный проток:
нормальное соединение легочной артерии
и аорты.
Существуют экстракардиальные
шунты . 1) венозный (аранциев)
проток (сброс крови из пупочной вены в
нижнюю полую вену), 2) артериальный
(боталлов) проток (сброс
крови из легочного ствола в аорту).
Имеется интракардиальный шунт —
открытое овальное отверстие (сброс
крови из правого предсердия в левое).
Правый
желудочек работает с большей нагрузкой,
поскольку преодолевает большее
сопротивление (сопротивление большого
круга кровообращения и не расправленных
легких). Давление в легочной артерии
приблизительно на 10 мм рт. ст.
выше, чем в аорте. Легогное кровообращение
составляет незначительную часть от
минутного объема правого желудочка, а
сами легкие поглощают
кислород, вместо того
чтобы обогащать им организм плода. В
тканях плода циркулирует смешанная
кровь (артериальная и венозная). При
этом наиболее оксигенированная
кровь поступает в печень и верхние
сегменты тела (включая головной мозг),
наименее оксигенированная кровь — в
нижние сегменты тела (включая внутренние
органы).
После рождения ребенка
наступают резкие изменения гемодинамики
(устанавливается внеутробное
кровообращение).
• Прекращается
кровообращение по сосудам пупочного
канатика вследствие пережатия пуповины
и отделения ребенка от матери.
•
Резко падает сопротивление
в сосудах малого круга кровообращения
(снижается в 5-10 раз). Это происходит
в связи: 1) с расправлением легких при
первом вдохе новорожденного, который
возникает вследствие раздражения
дыхательного центра на фоне активизации
рецепторного аппарата, а также влияния
гипоксии; 2) с повышением концентрации
кислорода в легочных сосудах и расширением
мышечных артерий и артериол (при участии
выделяемого брадикинина).
• Уменьшается
давление в правых отделах сердца
(расширение сосудов малого круга
кровообращения) и возрастает давление
в левых отделах сердца (интенсификация
функции большого круга кровообращения).
•
Правые и левые отделы сердца из параллельно
функционирующих (во внутриутробном
периоде развития) становятся последовательно
включенными.
• Закрывается овальное
отверстие вследствие повышения давления
в левых отделах сердца (в частности,
в левом предсердии) и закрытия клапана
овального отверстия. К 3-6 месяцам жизни
у части детей дефект ликвидируется
(зарастает). Незаращение овального
отверстия обнаруживают почти у 50% детей
в возрасте 5 лет и у 10-25% взрослых.
•
Происходит спазм артериального
протока. Это возникает в первые часы
жизни ребенка из-за повышения концентрации
кислорода в крови; изменения градиента
давления в артериальном протоке; снижения
синтеза простагландина Е2, обладающего
свойствами дилататора. Окончательное
закрытие артериального
протока (вследствие деструкции
эндотелия и пролиферации слоев под
интимой) у 95% детей происходит к 5-6
неделям жизни. У новорожденных в
течение 1—2 суток жизни можно наблюдать
«переходное кровообращение» (одновременное
наличие лево-правого шунта через
артериальный проток и право-левого
шунта через овальное отверстие).
•
Венозный проток, запустевший после
прекращения функции сосудов пуповины,
постепенно облитерируется.
•
Постепенно увеличиваются абсолютные
показатели массы сердца, но относительные
показатели уменьшаются. Масса сердца
новорожденного составляет 0,8% от
массы тела, а у взрослого — 0,4%. Рост
сердца наиболее интенсивен в течение
первых 2 лет жизни, в возрасте 12-14 лет
и 17-20 лет.
• Увеличивается масса
миокарда желудочков — в большей степени
левого. Толщина миокарда правого и
левого желудочков у новорожденного
одинаковая и составляет приблизительно
5 мм. За период детства масса миокарда
правого желудочка увеличивается
приблизительно в 10 раз, а левого — в 17
раз.
• Происходит тканевая
дифференцировка сердца. В первые
годы жизни увеличиваются толщина
мышечных волокон и размеры кардиомиоцитов,
появляются септальные перегородки
и поперечная исчерченность
волокон, увеличивается диаметр и
происходит перемоделирование проводящих
миоцитов, возникает «специализация»
клеток миокарда и осуществляется
становление функции их мембран. В
возрасте 3-10 лет, при относительно
медленном темпе увеличения массы сердца,
происходит его окончательная
дифференцировка, идет процесс
обогащения ткани сердца соединительнотканными
и эластическими компонентами.
•
Неоднократно изменяется
положение сердца в грудной клетке.
У новорожденного сердце расположено
высоко (из-за высокого стояния диафрагмы),
а его продольная ось направлена почти
горизонтально. В периоды интенсивного
роста ребенка наблюдают «вертикализацию»
положения сердца, в периоды замедления
роста - его «горизонтализацию».
•
Увеличиваются размеры кровеносных
сосудов большого круга кровообращения.
В их стенках развиваются мышечные и
эластические волокна. Интенсивно
утолщается интима сосудов.
Меняется соотношение просвета артерий
и вен: у новорожденного оно составляет
1:1, у ребенка в возрасте 16 лет - 1:2.
Развивается сеть коллатеральных сосудов
и капилляров. Формируется клапанный
аппарат вен.
• В сосудах малого
круга кровообращения в первые месяцы
жизни происходит противоположный
процесс - инволюция мышечного слоя и
гиперплазированной внутренней
оболочки и значительное увеличение
просвета сосудов.
• Увеличивается
с возрастом ударный (систолический)
объем крови, главным образом за счет
увеличения мощности миокарда
левого желудочка. Минутный объем
крови увеличивается менее интенсивно
вследствие замедления частоты сердечных
сокращений.
8.Влияние
внешней среды на физическое и психическое
развитие ребенка. Интеллектуальное,
эмоциональное развитие ребенка. Роль
семьи.
Большое значение в раннем
возрасте имеет способность к обучению
при помощи импритинг а («запечатления»
образца поведения).
В течение первого
года жизни младенцы все лучше знакомятся
со своими родителями и другими значимыми
для них людьми из их социального
окружения. У ребенка
появляется чувство доверия и формируется
привязанность к любимому человеку.
Формирование привязанности многокомпонентно
и синхронно; процесс развития взаимодействия
матери и ребенка происходит благодаря
стимулам, вызывающим взаимную любовь
(установление контакта
«глаза в глаза», прикосновения, голос
матери, подражательное обучение,
ритмичный разговор, тренировка движений
ребенка, запах матери, тепло матери,
бактериальная флора матери, крик ребенка,
запах ребенка и т. д.). Новорожденные,
которые воспитываются в семье, постоянно
слышат голоса родителей и видят их лица.
Близкие люди являются сильными
стимулами раннего формирования
коммуникативных функций новорожденного.
Физическая близость с матерью, являющаяся
в первые месяцы жизни своеобразным
продолжением внутриутробного
существования, формирует
чувство защищенности и оптимального
эмоционального состояния ребенка.
Поведение и характер
ребенка, достигшего школьного возраста,
в значительной степени определяется
вниманием тех людей, которые ухаживали
за ним в раннем детстве. Дети, которые
воспитывались родителями, как правило,
более приспособлены к школьной жизни.
Если же ребенка воспитывали бабушка
или дедушка, такие дети хуже адаптируются
к школе, у этих детей значительно хуже
развиты координированные движения.
Дети, которые воспитываются в детских
учреждениях (яслях, детских садах),
отличаются более ранним
формированием и совершенствованием
двигательных умений, в то же время
у них хуже развиты речевые навыки и
образное мышление. В зависимости от
условий среды, воспитания и различных
заболеваний у ребенка может задерживаться
нормальное развитие высшей нервной
деятельности, поэтому врач-педиатр
должен давать советы родителям по
гармоничному воспитанию детей.
В
первую очередь физическое развитие
зависит от питания, от обеспеченности
организма необходимым для развития
полным комплексом питательных веществ
— нутриентов: белков, жиров, углеводов,
минеральных солей, витаминов и множества
других веществ, соблюдается ли режим
занятий и отдыха, верно ли дозируются
физические и умственные нагрузки. Резкие
отклонения от нормы физического развития
— сигнал для родителей: они здесь
упускают что-то важное, необходимо
предпринять все меры к оздоровлению
ребенка.
Экологические
факторы, атмосферное давление,
температура окружающей среды постоянно
взаимодействуют на организм ребенка.
Под влиянием нагрузки и положительных
эмоций от физических упражнений, занятий
спортом на свежем воздухе, организм
ребенка функционально изменяется.
Ребенок,
приученный с детства к физкультурным
занятиям, занимается ними охотно, с
радостью и удовольствием. Такой
ребенок будет расти не только крепким
физически, но и лучше развит интеллектуально,
ведь эти два развития неразрывно
соединены друг с другом. Отлично, если
ребенок в будущем достигнет высоких
спортивных достижений, но, даже просто
занимаясь физическими упражнениями,
он сможет избежать многих заболеваний,
вырасти активным и здоровым.
Также
одним из важных факторов являются
ультрафиолетовые лучи.
Именно поэтому нарастание массы тела
и роста изменяются в зависимости от
времени года. Определенно, набор массы
тела и роста в какой-то мере зависят от
географического и климатического
местонахождения. Увеличение роста
костей и усиление обмена веществ
происходит за счет совершаемых движений
ребенком. Отсюда значение воспитательной
педагогической работы и особенно в
области физического воспитания и
организации образа жизни ребенка
(достаточное пребывание на свежем
воздухе, нормальный сон, активный
двигательный режим). Физическое развитие
организма в целом служит для измерения
функциональной зрелости всего
организма.
9.Законы нарастания массы
тела ребенка в различные возрастные
периоды.
Вес тела доношенного
новорожденного обычно составляет
3200–3500 г. Индивидуальные различия
доволь-
но велики
от 2600 г до 4500 г и более. Доношенные
новорожденные дети
с
массой тела 2500 г и ниже считаются
родившимися с задержкой внутриутроб-
ного
развития, а с массой 4500 r
и более — крупными.
После рождения
в течение первых дней происходит
незначительная, так
называемая
физиологическая потеря
первоначальной массы тела
в пределах
5
— 8% исходной, т. е. 150 — 300 г. Основной
причиной может быть недоедание
в
первые 3 дня, связанное с медленным
нарастанием лактации, а также с
позд-
ним
прикладыванием к груди и недостаточным
поступлением жидкости в ор-
ганизм,
с выделением мекония, мочи, начавшимися
потерями через кожу и
легкие,
высыханием пуповинного остатка.
Обычно масса тела восстанавливает-
ся
к 7 — 8-му дню жизни, иногда этот
процесс идет более медленно и
заканчи-
вается
к 11 — 12-му дню жизни.
Для расчета
массы тела в I полугодии жизни можно
использовать формулы: 1) масса тела
может быть определена как сумма:
Масса тела при рождении +
800 г x з, где з – число
месяцев в течение I полугодия; 800 г –
средняя ежемесячная прибавка массы
тела в течение I полугодия; 2) масса
тела ребенка 6 месяцев равна 8200 г, за
каждый недостающий месяц вычитается
по 800 г.
Таким образом, за II
полугодие ребенок прибавляет в весе
2 кг 850 г и к году должен весить в
среднем 10,5 кг.
к 4,5 месяцам происходит
удвоение веса при рождении, к 1 году
вес утраивается и составляет в
среднем 10–10,5 кг. В первые годы жизни
весовая прибавка составляет в среднем
2 кг, в препубертатном периоде – 5–6
кг.
1мес - 600г.
2 мес - 800г.
3 мес-
800г.
4 мес - 750г.
5 мес - 700г.
6 мес –
650г.
7 мес- 600г.
8 мес- 550г.
9 мес –
500г.
10 мес- 450г.
11 мес – 400г.
12 мес
– 450 г.
От 1 года до 2 – 2500-2600г.
ОТ
2-3 лет – 2200г
Маловесные дети дают
убыль веса около 9 %; у детей, рожденных
до 1000 г, убыль веса доходит до 15 %.
Восстановление веса у них происходит
медленно – до двух и более недель.
Достижение веса нормального доношенного
ребенка до 3200–3500 г и длины 50–51 см у
недоношенных и маловесных происходит
к 1–1,5 месяцам (2000–2500 г масса тела при
рождении), к 2–2,5 месяцам (1500–2000 г) и к
3–3,5 месяцам (1000 г).
Нормальными
колебаниями массы тела на первом году
жизни можно
считать
величины, отклоняющиеся не более чем
на 9 — 10% от средних пока-
зателей
в большую или меньшую сторону.
Для
II полугодия жизни ориентировочную массу
тела можно рассчитать по
формулам:
1) масса тела при рождении
+ плюс прибавка массы тела за II
полугодие:(800 х 6) + 400г ч (n – 6), где n –
возраст в месяцах; 400 г – средняя
ежемесячная прибавка массы тела за II
полугодие;
2) масса тела ребенка 6
месяцев равна 8200 г, за каждый последующий
месяц прибавляется по 400 г (у детей
до 12 месяцев).
На втором году жизни
прибавка массы тела составляет 2,5 кг,
а в препу-
бертатном
и пубертатном периоде достигает иногда
5 — 6 кг в год. Масса тела
в
возрасте 2—11 лет равна: 10,5 + 2п, где
п — возраст ребенка до 11 лет,
а
10,5 кг — средняя масса годовалого
ребенка.
Не всегда показатели массы
тела и длины тела нарастают параллельно.
В процессе развития
происходит чередование
периодов преимущественного
роста
в длину с ростом в «ширину».
Так называемый период первой
полноты
наступает
в возрасте 3 — 4 лет. Период первого
вытягивания наступает
от 4 до
5,5
лет у мальчиков и после 6 лет у
девочек. Период второй
полноты (преиму-
щественный
рост в «ширину») — 8 — 10 лет. Период
второго вытягивания-
11—12
лет у мальчиков и 9—10 лет у девочек.
10.Законы нарастания роста и пропорции
детского тела в различные возрастные
периоды.
Рост новорожденного
ребенка 50 см (возможны колебания роста
от 45 до 55 см). Ежемесячные прибавки роста
составляют в первом полугодии по 2–1
см.
. Чем
младше
ребенок, тем интенсивнее его рост. В
первые 3 месяца жизни длина
тела
увеличивается на 3 см ежемесячно, или
на 9 см за квартал, во 2-м кварта-
ле
— на 2,5 см ежемесячно, в 3-м квартале —
на 1,5 см и в 4-м кварта-
ле
— на 1 см в месяц. Рост ребенка с 7 по 9-й
месяц увеличивается ежемесячно на 2 см,
а с 9 по 12-й месяц – на 1,5–1 см. Таким
образом, во II полугодии ребенок вырастает
на 10 см.
За первый год
жизни ребенок вырастает на 25 см, и
рост его к году достигает
75 см. На втором году жизни рост
увеличивается на 12 см, за третий год –
на 7–8 см, в дальнейшем за год ребенок
вырастает на 5 см, и к 4 годам
его рост удваивается,
а к 12 годам – утраивается
по сравнению с ростом при рождении.
С 2 до 12 лет долженствующую длину тела
можно вычислить по фор-
муле:
возраст (годы) х 6+ 77 см.
После
этого с 11 — 12 лет у мальчиков и с 9 — 10
лет у девочек начинается новое ускорение
роста с достижением максимума роста
в возрасте от 13,5 до 15,5 лет у мальчиков
(в среднем по 8 — 10 см и более в год) и в
возрасте 10 — 115 лет у девочек, однако
могут быть
индивидуальные разли-
чия,
связанные с типом конституции. Вытягивание
мальчиков 11 — 12 лет идет
исключительно
за счет нижних конечностей. Между
14 и 15 годами ноги пере-
стают
расти и наступает пик скорости роста
для туловища. У девочек эти осо-
бенности
относятся соответственно к 9 и 11—12
годам. Прекращение роста
в
длину происходит у юношей в 18—19 лет, у
девушек — в 16—17 лет.
11.Анатомо-физиологические особенности
кожи, подкожно-жировой клетчатки,
лимфатической системы у детей.
Кожа состоит
из эпидермиса и дермы.
Эпидермис
у новорожденных и детей 1-го года жизни,
как и у детей более старшего возраста
и у взрослых, имеет многослойную
структуру. Однако он значительно
тоньше. Роговой слой
эпидермиса содержит много влаги, очень
тонкий, рыхлый, состоит из 2—3 рядов
ороговевших, слабо связанных между
собой клеток, роговые пластинки легко
отторгаются. Это определяет легкую
ранимость эпидермиса. Процесс
митотического деления клеток совершается
интенсивно не только в базальном, но и
в шиловидном и зернистом слоях, чем
объясняется быстрая смена слоев
эпидермиса у детей.
Дерма
(собственно кожа) у новорожденных и
детей грудного возраста тоньше,
чем в старшем возрасте, и отличается по
структуре. Дерма состоит из двух слоев:
верхнего — сосочкового
и нижнего — сетчатого.
Характеризуется преимущественно
клеточным строением и слабым
развитием эластических, коллагеновых,
аргирофильных, мышечных волокон;
содержит много недифференцированных
соединительнотканных, в том числе
тучных, клеток. Только к
6 годам гистологическое строение
дермы приближается к таковому у взрослых,
хотя коллагеновые волокна еще тонкие,
а эластические волокна развиты
слабо.
Кожные покровы ребенка
раннего возраста не случайно часто
становятся «органом-мишенью» аллергических
реакций. В эпидермисе, дерме и подкожной
клетчатке имеется относительно большее,
чем у детей старшего возраста, количество
клеток, участвующих в распознавании,
представлении и эффекторном ответе
(клетки Лангенгарса, тучные клетки,
лимфоциты, эозинофилы). Кожа
новорожденного и ребенка раннего
возраста богата кровеносными
сосудами, пронизана густой сетью
широких капилляров. Стенки большинства
сосудов представлены одним рядом
эндотелиальных клеток, им свойственна
повышенная проницаемость. Наружное
применение препаратов йода может
привести к угнетению функции щитовидной
железы. По этим же причинам опасность
генерализации инфекций на коже у детей
первых лет жизни гораздо выше, чем в
более старшем возрасте.
Потовые
эккринные железы сформированы уже к
моменту рождения. Однако в течение
первых 3—4 месяцев они слабо проявляют
свою функциональную активность, имеют
недоразвитые выводящие протоки.
Дальнейшее созревание структур потовых
желез, вегетативной нервной системы и
терморегулирующего центра центральной
нервной системы обеспечивает
совершенствование потоотделения.
Адекватность потоотделения
складывается в течение первых 7 лет
жизни. Полное развитие апокринних
потовых желез происходит в первый год
жизни. Начинают они функционировать
к 8-10 годам, но активно—в период полового
созревания.
Сальные железы у
новорожденных гистологически не
отличаются от желез у взрослых. Они
активно функционируют в грудном возрасте
и распространены по всей коже, за
исключением ладоней и подошв. Особенно
их много в области лица,
волосистой части головы, спины, ануса,
гениталий. У новорожденных часто
на коже кончика и крыльев носа, а иногда
и на прилегающих участках кожи щек
имеются желтовато-белые
точки (milia) — избыточное скопление
секрета в поверхностно расположенных
кожных сальных железах. После 1-го
года жизни функция сальных желез
значительно снижается (часть желез
вообще полностью атрофируется) и
усиливается лишь в период
полового созревания. Себорея
(seborrhoea) - патологическое состояние кожи,
обусловленное усиленной функцией
сальных желез. Сухая себорея нередко
сопутствует экссудативному диатезу.
Волосы на голове новорожденного
не имеют сердцевины.
Возрастной особенностью является
замедленный рост волос в
первые 2 года жизни (0,2 мм ежедневно
по сравнению с 0,3—0,5 мм у детей старшего
возраста) и быстрая их смена.
На первом году жизни волосы сменяются
несколько раз. С возрастом толщина
волос на голове увеличивается. Брови
и ресницы у новорожденных развиты
сравнительно мало, но в дальнейшем
растут быстро, и у детей 3-5 лет они
достигают почти такой же длины, как и у
взрослых. В области лобка, в подмышечных
впадинах волосы появляются в период
полового созревания; к этому же времени
начинается их рост на лице у
мальчиков.
Функциональные особенности
кожи новорожденного и ребенка первых
лет жизни.
Защитная функция кожи
от неблагоприятных внешних воздействий
(механических, химических, инфекционных)
имеет ряд особенностей. Легкая ранимость
кожи обусловлена тонкостью рогового
слоя эпидермиса, незрелостью местного
иммунитета, малой плотностью кожи ввиду
слабого развития упругих
эластических и
коллагеновых волокон. рН кожи
новорожденного составляет 6,7 — близко
к нейтральной среде. В то же время у
детей более старшего возраста
водно-липидная мантия с кислой реакцией
(рН 4,5—6,0) препятствует проникновению
в кожу микробов и ослабляет или
нейтрализует повреждающее действие
химических веществ. Систематическая
мацерация кожи мочой и калом способствует
разжижению водно-липидной мантии
эпидермиса. Бактерицидные свойства
кожи снижаются также при ее обезжиривании
(спиртом, эфиром и т. п.) и охлаждении
организма. Согревание,
наоборот, повышает защитную функцию
кожи. Низкий уровень образования
пигмента меланина в меланоцитах
базального слоя эпидермиса делает кожу
грудных детей чувствительной
к повреждающему действию солнечных
лучей. Поэтому следует с особой
осторожностью назначать им ультрафиолетовое
облучение.
Терморегулирующая
функция кожи у новорожденных и детей
первых месяцев жизни несовершенна.
Они предрасположены к
переохлаждению и перегреванию. Это
связано с большей поверхностью тела,
тонкостью и нежностью кожных покровов,
хорошо развитой сосудистой сетью в
сочетании с несовершенством
регуляции кровотока в коже, слабым
функционированием потовых желез,
незрелостью центров терморегулции.
Тонкость
эпидермиса и слабое развитие
соединительнотканных волокон
дермы обусловливают их повышенную
чувствительность. Раздражение кожи
при плохом уходе (мокрые, грязные
пеленки), различных кожных заболеваниях
может явиться причиной беспокойства
ребенка, нарушения сна, отражаясь на
состоянии нервной системы и всего
организма в целом. С ростом ребенка
нервный аппарат кожи становится менее
доступным для внешних раздражителей.
Кожа
является местом образования ферментов,
биологигески активных веществ, витамина
D.
Жировая ткань начинает формироваться
на 4—5-м месяце внутриутробного
развития. Вначале жир откладывается
на голове и шее, затем на туловище
и позднее на верхних и нижних конечностях.
У новорожденного общее колигество
жировой ткани тесно связано со сроками
гестации и у доношенного ребенка
составляет до 14-16% от массы тела:
В
постнатальном периоде происходит
интенсивное накопление
жира внутри клеток
белой жировой ткани. Уже к 5 месяцам
отмечают увеличение его содержания
в организме почти в 3 раза.
У
новорожденных хорошо развита бурая
жировая ткань. Наибольшие скопления
ее находятся в межлопаточной
и аксиллярной областях, в области
щитовидной и зобной желез, перикарда,
вокруг пищевода, почек
и надпочечников,
трахеи, в брыжейке тонкой кишки, в
паху и
по ходу больших сосудов.
У доношенного новорожденного масса
бурой жировой ткани составляет 1—3%
от всей массы тела. Основной функцией
бурой жировой ткани является так
называемый несократительный термогенез,
т. е. теплопродукция, не связанная с
мышечным сокращением. Максимальная
способность к теплопродукции бурой
жировой ткани определяется в первые
дни жизни. С возрастом способность бурой
жировой ткани к теплопродукции снижается,
она постепенно заменяется белой.
Глубоконедоношенные и дистрофированные
дети с малым запасом бурой жировой ткани
очень легко охлаждаются и нуждаются в
согревании.
Особенностью подкожной
клетчатки у новорожденных и грудных
детей является сохранение
в ней участков ткани эмбрионального
характера, обладающей как
жиронакапливающей, так и кровообразующей
функцией. Подкожную жировую клетчатку
детей раннего возраста считают
ретикулогистиоцитарньм органом,
напоминающим по гистогенезу и функциям
костный мозг. По химическому составу
подкожная клетчатка новорожденных и
детей грудного возраста отличается от
клетчатки взрослого: в ней содержится
больше твердых
жирных кислот - пальмитиновой и стеариновой
и меньше — жидкой олеиновой кислоты.
Преобладание содержания твердых жирных
кислот с более высокой точкой плавления
обеспечивает более плотный тургор
тканей детей первого года жизни и
наклонность к образованию локальных
уплотнений и отека кожи и подкожной
жировой клетчатки (склерема,
склередема).
Максимального содержания
подкожного жира ребенок достигает
примерно в 9-месячном
возрасте. В течение 1—3-го года
жизни увеличение жировой ткани происходит
как за счет увеличения количества
жировых клеток (липоцитов),
так и за счет увеличения их
размеров. После 6-летнего возраста
более интенсивно происходит увеличение
размеров жировых клеток.
Больше жира откладывается на
лице, где жировые тела щеки (тела Биша)
содержат много твердых жирных кислот,
на ягодицах, бедрах, животе (здесь
преобладает содержание жидких кислот).
Исчезает подкожная жировая клетчатка
вначале на животе и груди, затем на
конечностях и в последнюю очередь
на лице.
Как и в организме взрослого,
у ребенка жировая ткань играет роль
механигеской защиты и стабилизации
внутренних органов, сосудов и
нервных стволов, участвует в
гомеостазировании температуры
тела.
Лимфоузлы. Закладка на
2-м месяце внутриутробной жизни. С этого
же времени (и до конца жизни)
осуществляется их кроветворная
функция — продукция лимфоцитов.
К 5-му месяцу в отдельных лимфоузлах
можно видеть намечающуюся границу между
будущим корковым и мозговым веществом,
развивается капсула лимфоузлов.
Лимфоузлы состоят из паренхиматозной
(лимфоидной) ткани с крупными синусами
и ограничены очень нежной и тонкой
капсулой. Элементы ретикулярной и
соединительнотканной стромы узла
(трабекулы, перегородки)
и капсулы практически отсутствуют.
Недостаточна дифференцировка
иммунокомпетентных клеток лимфатических
узлов. По этим причинам плохо
осуществляется защитная (барьерная)
функция.
После года барьерная
функция лимфоузлов возрастает, они
задерживают микробы, отвечая на внедрение
инфекции островоспалительной гнойной
(при кокковой флоре) или казеозной (при
туберкулезной инфекции) реакцией. Этим
объясняют высокую частоту лимфаденитов
у детей в возрасте 1—3 лет.
К 7-8 годам
в лимфатических узлах образуются
соединительнотканные перегородки
(трабекулы), более узкими становятся
синусы. Лимфатические синусы - это
щели между капсулой, трабекулами и
паренхимой лимфатического узла, по
которым течет лимфа. Это действенный
барьер, задерживающий микробов, опухолевые
клетки, инородные частицы. Появляется
возможность местного иммунологического
подавления инфекции. В связи с этим
возникает реакция лимфатического узла
на инфекцию в виде увеличения его
размера, болезненности. Для детей
дошкольного и младшего школьного
возраста характерны периферические
лимфадениты, увеличение носоглоточной
миндалины (аденоиды), небных миндалин
и т. д В возрасте 1 — 3 лет лимфатические
узлы имеют довольно хорошо развиты и
реагируют на внедрение возбудителя
местной воспалительной
реакцией.
К 12 — 13 годам строение и
функция лимфатических узлов соответствуют
таковым взрослого человека. Они
задерживают и подавляют проникшую в
них патогенную флору без видимых
изменений или кратковременно увеличиваясь
в размерах и в дальнейшем нормализуясь.
В период полового созревания рост узлов
останавливается, и они частично
подвергаются обратному развитию.
Возрастная инволюция лимфоидной ткани,
ее замещение соединительной, жировой
тканями так же характерна для периферических
органов иммунной системы, как и для
центральных.
12.Анатомо-физиологические
особенности костной и мышечной систем
у детей.
В скелете человека
различают более 200 костей. В зависимости
от выполняемых функций отдельные кости
имеют различное внутреннее строение.
Выделяют четыре основных вида костей:
трубчатые, губчатые, плоские, смешанные.
Все кости состоят из следующих основных
компонентов: клеток, органического
матрикса, минеральных веществ. Костная
ткань детей содержит больше
воды, чем у взрослых.
В
первые годы жизни происходят интенсивные
процессы переформирования костной
ткани, от грубоволокнистого до
пластинчатого строения. Костная
ткань в это время особенно чувствительна
к воздействию неблагоприятных факторов.
У
детей раннего возраста в строении
скелета хрящевая ткань
представлена в большей степени, чем у
взрослого человека. У новорожденного
кости черепа, диафизы трубчатых костей
состоят из костной ткани; эпифизы
бедренной и большеберцовой костей,
таранная, пяточная, кубовидная кости,
тела позвонков и дуги имеют только
точки окостенения. Большинство
эпифизов, все губчатые кости кистей,
часть губчатых костей стоп представлены
хрящевой тканью. Точки окостенения
в них после рождения появляются в
определенной последовательности.
Совокупность имеющихся у ребенка точек
окостенения называется «костным
возрастом» и характеризует уровень
биологического развития.
Интенсивный
рост и переформирование костной ткани
поддерживаются специфическим для
детского возраста обильным
кровоснабжением, что предрасполагает
к более частому развитию гематогенных
остеомиелитов, чем у
взрослых.
Продольный рост
костей происходит за счет развития
ростковой хрящевой
ткани в метаэпифизарных зонах (зоны
роста), которые страдают в первую
очередь при различных патологических
процессах (рахит, остеомиелит, ревматоидный
артрит), длительном приеме гормональных
препаратов.
Поперечный рост
костей обеспечивается надкостницей,
которая у детей имеет выраженную толщину
и функциональную активность. Данные
особенности надкостницы имеют также
большое значение при травматических
повреждениях в качестве защитного
фактора (переломы без
смещения костных фрагментов по типу
«зеленой веточки»).
Череп
ребенка после рождения имеет следующие
особенности. Стреловидный, венечный,
затылочный швы закрываются с
3—4-месячного возраста. Боковые
роднички у доношенных новорожденных
закрыты. Задний (малый) родничок
располагается на уровне затылочных
швов теменных костей. Он открыт до 4-8
недель после рождения у 25%
новорожденных. Передний (большой)
родничок, расположенный в месте
соединения венечного и продольного
швов в виде ромба, может иметь различные
размеры. Расстояние между средними
точками противостоящих краев может
составлять от 3 х 3 см до 1,5 х 2 см. Закрытие
большого родничка происходит к 12-18
месяцам.
Формирование зубов
начинается с конца второго месяца
внутриутробного развития из двух
зачатков: из эпителиальной закладки -
эмаль, из мезенхимальной закладки
— дентин.
Молочные зубы
прорезываются начиная с 5 месяцев.
Ориентировочная формула для определения
количества зубов до двух лет жизни:
п — 4, где п — количество месяцев. Полный
молочный прикус должен быть у
ребенка к двум годам жизни.
Время сохранения молочных зубов и
появления постоянных называют периодом
сменного прикуса (в среднем от 5 до 12
лет).
Позвоночник у детей раннего
возраста имеет выраженную подвижность
и гибкость, что определяется большим
количеством хрящевой
ткани. Между вторым и четвертым
месяцами, когда ребенок начинает активно
поднимать и удерживать голову,
появляется передний
изгиб шейной части
позвоночника. После начала
ходьбы формируются
изгибы поясничного (лордоз) и
грудного отдела позвоночника
(кифоз).
Фиксация позвоночника
несовершенна, что связано
с развитием мышц, и легко приводит к
сколиозам и патологическим
осанкам. Нарушение осанки —
отклонение позвоночника в сагиттальной
и фронтальной плоскости, которая
определяется состоянием мышечного
тонуса и привычностью для ребенка
измененной позы. Патологические
осанки приводят к нарушениям функции
внутренних органов.
Грудная клетка
у детей первого года жизни характеризуется
превалированием поперечного
диаметра, горизонтальным расположением
ребер и малой длиной. В дальнейшем за
счет роста грудной клетки в длину и
увеличения переднего диаметра
опускаются передние концы ребер.
Данный процесс происходит до 12 лет.
Резкое увеличение поперечного
диаметра грудной клетки происходит к
15 годам.
Таз у детей раннего
возраста имеет форму воронки.
Интенсивный рост костей таза происходит
до 6 лет. С 11—12 лет наиболее интенсивное
развитие костей таза отмечают у девочек.
К 15 годам соотношение межакромиального
и межтрохантерного расстояний у девочек
составляет около 1,15, у мальчиков - 1,3 и
более.
Осмотр костной системы
проводится в определенной по
следовательности: в фас, сбоку, со спины,
определяется также нарушение походки.
Мышцы
у новорожденного и ребенка грудного
возраста развиты слабо; они составляют
около 25 % массы его тела, тогда
как у взрослого — не менее 40—43 % У детей
первых месяцев жизни отмечается
повышенный тонус мышц, так
называемая физиологическая
гипертензия, которая связана с
особенностями функционирования
центральной нервной системы. Тонус
сгибателей преобладает над тонусом
разгибателей; этим объясняется тот
факт, что дети грудного возраста, если
их распеленать, обычно лежат с согнутыми
руками и ногами. Постепенно эта гипертензия
исчезает.
Сила и тонус мышц у
ребенка слабые. Двигательная способность
появляется сначала у мышц шеи и
туловища, а потом уже у мышц конечностей.
Мышечная сила постепенно нарастает.
Особенно интенсивно развивается
мускулатура в период полового созревания,
происходит нарастание силы и точности
движений. Мальчики обычно отличаются
лучшим мышечным тонусом, чем девочки.
Формирование и рост мышечных волокон
заканчивается к 20—23 годам.
При
обследовании детей обращают внимание
на силу и тонус мышц. Сила мышц у детей
грудного возраста измеряется лишь
приблизительно путем определения того
усилия, которое необходимо для
противодействия тому или другому
движению ребенка; у детей старшего
возраста сила мышц измеряется, так же
как и у взрослых, с помощью динамометра.
Мышечная сила у детей раннего возраста
определяется попыткой отнять игрушку.
У детей более старшего возраста проводится
ручная динамометрия.
В 1—2 мес ребенок
должен удерживать голову в вертикальном
положении, в 3— З,5 мес — при поддержке
подмышки упираться ногами, в 6 мес —
самостоятельно сидеть и поворачиваться
со спины на живот и обратно, в 7—8 мес
ползать, в 10 мес — стоять без опоры, в
12 мес — делать первые самостоятельные
шаги.
13.Анатомо-физиологические
особенности сердечно-сосудистой системы
у детей. Внутриутробное кровообращение
плода. Частота пульса и кровяное давление
у детей. Скорость кровотока и минутный
объем сердца.
прослушивание
сердечных тонов через брюшную стенку
матери возможно с IV месяца беременности.
Обогащенная кислородом кровь
поступает из плаценты через венозный
(аранциев) проток в нижнюю полую вену
и смешивается там с венозной кровью,
оттекающей от нижних конечностей.
Большая часть этой смешанной крови
благодаря специальной заслонке нижней
полой вены (евстахиева заслонка) в
правом предсердии направляется через
овальное окно в левое предсердие,
левый желудочек, а оттуда в аорту и через
подключичные артерии к мозгу и верхним
конечностям.
Внутриутробное
(фетальное, плацентарное) кровообращение.
Газообмен и обмен
продуктов метаболизма осуществляются
в плаценте , система кровообращения
которой сообщается с системой
кровообращения плода через пупочный
канатик (пуповину), включающий: 1) одну
пупочную вену (ток крови в сторону
плода), 2) две пупочные артерии (ток крови
в сторону плаценты). При этом кровь плода
и матери не смешивается.
ешивается.
Кровь от материнской плаценты через
пупочную вену плода притекает в его
нижнюю полую вену, где, смешиваясь
с его венозной кровью от нижней
половины тела, заполняет правое
предсердие.
Отсюда основной поток
идет через открытое
овальное окно, т.е. отверстие
(дефект) в межпредсердной перегородке в
левое предсердие и левый желудочек и
дальше – в большой круг. Это —
первый физиологический, естественный
шунт. Из левого желудочка часть
крови идет в аорту и сосуды головы и
верхней половины тела. А та часть крови,
которая в правых отделах прошла в правый
желудочек через трехстворчатый клапан,
а затем — в легочную артерию, уходит в
нисходящую аорту
через второй физиологический шунт —
открытый артериальный проток:
нормальное соединение легочной артерии
и аорты.
Существуют экстракардиальные
шунты . 1) венозный (аранциев)
проток (сброс крови из пупочной вены в
нижнюю полую вену), 2) артериальный
(боталлов) проток (сброс
крови из легочного ствола в аорту).
Имеется интракардиальный шунт —
открытое овальное отверстие (сброс
крови из правого предсердия в левое).
Правый
желудочек работает с большей нагрузкой,
поскольку преодолевает большее
сопротивление (сопротивление большого
круга кровообращения и не расправленных
легких). Давление в легочной артерии
приблизительно на 10 мм рт. ст.
выше, чем в аорте. Легогное кровообращение
составляет незначительную часть от
минутного объема правого желудочка, а
сами легкие поглощают
кислород, вместо того
чтобы обогащать им организм плода. В
тканях плода циркулирует смешанная
кровь (артериальная и венозная). При
этом наиболее оксигенированная
кровь поступает в печень и верхние
сегменты тела (включая головной мозг),
наименее оксигенированная кровь — в
нижние сегменты тела (включая внутренние
органы).
После рождения ребенка
наступают резкие изменения гемодинамики
(устанавливается внеутробное
кровообращение).
• Прекращается
кровообращение по сосудам пупочного
канатика вследствие пережатия пуповины
и отделения ребенка от матери.
•
Резко падает сопротивление
в сосудах малого круга кровообращения
(снижается в 5-10 раз). Это происходит
в связи: 1) с расправлением легких при
первом вдохе новорожденного, который
возникает вследствие раздражения
дыхательного центра на фоне активизации
рецепторного аппарата, а также влияния
гипоксии; 2) с повышением концентрации
кислорода в легочных сосудах и расширением
мышечных артерий и артериол (при участии
выделяемого брадикинина).
• Уменьшается
давление в правых отделах сердца
(расширение сосудов малого круга
кровообращения) и возрастает давление
в левых отделах сердца (интенсификация
функции большого круга кровообращения).
•
Правые и левые отделы сердца из параллельно
функционирующих (во внутриутробном
периоде развития) становятся последовательно
включенными.
• Закрывается овальное
отверстие вследствие повышения давления
в левых отделах сердца (в частности,
в левом предсердии) и закрытия клапана
овального отверстия. К 3-6 месяцам жизни
у части детей дефект ликвидируется
(зарастает). Незаращение овального
отверстия обнаруживают почти у 50% детей
в возрасте 5 лет и у 10-25% взрослых.
•
Происходит спазм артериального
протока. Это возникает в первые часы
жизни ребенка из-за повышения концентрации
кислорода в крови; изменения градиента
давления в артериальном протоке; снижения
синтеза простагландина Е2, обладающего
свойствами дилататора. Окончательное
закрытие артериального
протока (вследствие деструкции
эндотелия и пролиферации слоев под
интимой) у 95% детей происходит к 5-6
неделям жизни. У новорожденных в
течение 1—2 суток жизни можно наблюдать
«переходное кровообращение» (одновременное
наличие лево-правого шунта через
артериальный проток и право-левого
шунта через овальное отверстие).
•
Венозный проток, запустевший после
прекращения функции сосудов пуповины,
постепенно облитерируется.
•
Постепенно увеличиваются абсолютные
показатели массы сердца, но относительные
показатели уменьшаются. Масса сердца
новорожденного составляет 0,8% от
массы тела, а у взрослого — 0,4%. Рост
сердца наиболее интенсивен в течение
первых 2 лет жизни, в возрасте 12-14 лет
и 17-20 лет.
• Увеличивается масса
миокарда желудочков — в большей степени
левого. Толщина миокарда правого и
левого желудочков у новорожденного
одинаковая и составляет приблизительно
5 мм. За период детства масса миокарда
правого желудочка увеличивается
приблизительно в 10 раз, а левого — в 17
раз.
• Происходит тканевая
дифференцировка сердца. В первые
годы жизни увеличиваются толщина
мышечных волокон и размеры кардиомиоцитов,
появляются септальные перегородки
и поперечная исчерченность
волокон, увеличивается диаметр и
происходит перемоделирование проводящих
миоцитов, возникает «специализация»
клеток миокарда и осуществляется
становление функции их мембран. В
возрасте 3-10 лет, при относительно
медленном темпе увеличения массы сердца,
происходит его окончательная
дифференцировка, идет процесс
обогащения ткани сердца соединительнотканными
и эластическими компонентами.
•
Неоднократно изменяется
положение сердца в грудной клетке.
У новорожденного сердце расположено
высоко (из-за высокого стояния диафрагмы),
а его продольная ось направлена почти
горизонтально. В периоды интенсивного
роста ребенка наблюдают «вертикализацию»
положения сердца, в периоды замедления
роста - его «горизонтализацию».
•
Увеличиваются размеры кровеносных
сосудов большого круга кровообращения.
В их стенках развиваются мышечные и
эластические волокна. Интенсивно
утолщается интима сосудов.
Меняется соотношение просвета артерий
и вен: у новорожденного оно составляет
1:1, у ребенка в возрасте 16 лет - 1:2.
Развивается сеть коллатеральных сосудов
и капилляров. Формируется клапанный
аппарат вен.
• В сосудах малого
круга кровообращения в первые месяцы
жизни происходит противоположный
процесс - инволюция мышечного слоя и
гиперплазированной внутренней
оболочки и значительное увеличение
просвета сосудов.
• Увеличивается
с возрастом ударный (систолический)
объем крови, главным образом за счет
увеличения мощности миокарда
левого желудочка. Минутный объем
крови увеличивается менее интенсивно
вследствие замедления частоты сердечных
сокращений.
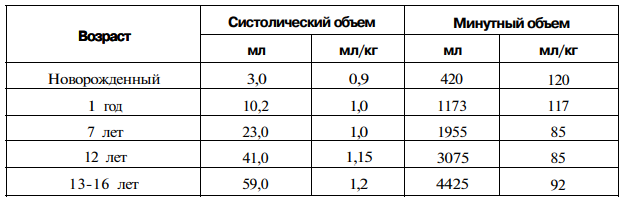 •
Скорость кровотока у
новорожденного в 2 раза выше,
чем у взрослого, а вязкость крови — в
10 раз выше. ОЦК у новорожденного
составляет приблизительно 90 мл/кг, у
взрослого - 50 мл/кг. Систолигеский
показатель (процентное отношение
длительности систолы сердца к длительности
сердечного цикла) у новорожденного на
10-20% выше данного показателя у взрослых.
•
Замедляется с возрастом частота сердечных
сокращений. Этот процесс тесно связан
с увеличением ударного
объема крови и
формированием вагусной иннервации
сердца. Наибольшую частоту
сокращений сердца (около 140 уд./мин) можно
наблюдать у новорожденных (на фоне
интенсивного обмена веществ).
•
Увеличивается с возрастом артериальное
давление (преимущественно систолическое).
Это связано с увеличением ударного
объема крови, повышением тонуса
мышечных сосудов, созреванием
рецепторного аппарата сосудов, увеличением
физических нагрузок. Максимальные
темпы увеличения артериального давления
наблюдают у детей первых 2—3 лет жизни,
а также в препубертатном и пубертатном
периодах развития (на фоне ускоренных
темпов роста).
•
Скорость кровотока у
новорожденного в 2 раза выше,
чем у взрослого, а вязкость крови — в
10 раз выше. ОЦК у новорожденного
составляет приблизительно 90 мл/кг, у
взрослого - 50 мл/кг. Систолигеский
показатель (процентное отношение
длительности систолы сердца к длительности
сердечного цикла) у новорожденного на
10-20% выше данного показателя у взрослых.
•
Замедляется с возрастом частота сердечных
сокращений. Этот процесс тесно связан
с увеличением ударного
объема крови и
формированием вагусной иннервации
сердца. Наибольшую частоту
сокращений сердца (около 140 уд./мин) можно
наблюдать у новорожденных (на фоне
интенсивного обмена веществ).
•
Увеличивается с возрастом артериальное
давление (преимущественно систолическое).
Это связано с увеличением ударного
объема крови, повышением тонуса
мышечных сосудов, созреванием
рецепторного аппарата сосудов, увеличением
физических нагрузок. Максимальные
темпы увеличения артериального давления
наблюдают у детей первых 2—3 лет жизни,
а также в препубертатном и пубертатном
периодах развития (на фоне ускоренных
темпов роста).
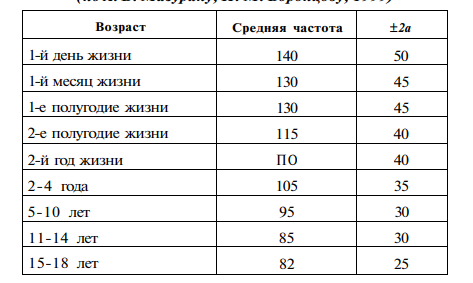
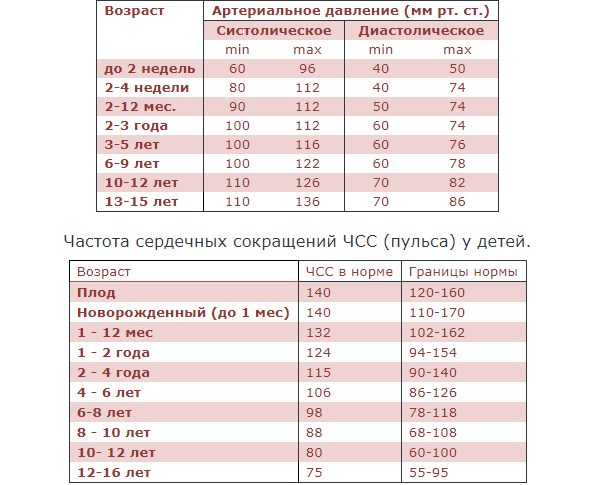
14.Анатомо-физиологические
особенности органов дыхания у детей.
Плод
совершает «дыхательные» движения с
конца I триместра внутриутробного
развития. Легкие плода секретируют
жидкость (у доношенного перед рождением
до 300 мл в сутки), поступающую в околоплодные
воды. Благодаря тому, что «дыхательные»
движения плода совершаются при
закрытой голосовой щели, околоплодная
жидкость в легкие не попадает и по уровню
и соотношению лецитина и сфингомиелина
в околоплодной жидкости можно судить
о зрелости легких (синтеза
сурфактанта).
Сурфактант —
поверхностно-активное вещество,
синтезируемое альвеолоцитами II типа и
клетками Клара, препятствующее спадению
альвеол на выдохе, участвующее в регуляции
микроциркуляции в легких и обладающее
бактерицидной активностью.
К моменту
рождения ребенка морфологическое
строение еще несовершенно. Интенсивный
рост и дифференцировка дыхательных
органов продолжаются в течение первых
месяцев и лет жизни. Формирование
органов дыхания заканчивается в
среднем к 7 годам, и в дальнейшем
увеличиваются только их размеры. Все
дыхательные пути у ребенка имеют
значительно меньшие размеры и более
узкие просветы, чем у взрослого.
Особенностями их морфол. строения
у детей первых лет жизни являются:
1)
тонкая, нежная, легкоранимая сухая
слизистая оболочка с недостаточным
развитием желез, со сниженной продукцией
секреторного иммуноглобулина A (SIgA)
и недостаточностью сурфактанта;
2)
богатая васкуляризация подслизистого
слоя, представленного преимущественно
рыхлой клетчаткой и содержащего мало
эластических и соединительнотканных
элементов;
3) мягкость и
податливость хрящевого каркаса нижних
отделов дыхательных путей,
отсутствие в них и в легких эластической
ткани.
Мягкость ребер и податливость
грудной клетки - Облегчение прохождения
по родовым путям, но склонность к
парадоксальному дыханию.
«Экспираторное»
строение грудной клетки (ребра расположены
почти под прямым углом к позвоночнику)-
Ограниченные возможности увеличения
дыхательного объема.
Высокое стояние
диафрагмы- Диафрагмальный тип дыхания,
уменьшение дыхательного объема при
вздутии кишечника.?
Нос и
носоглоточное пространство. У
детей раннего возраста нос и носоглоточное
пространство малых размеров,
короткие, уплощенные из-за недостаточного
развития лицевого скелета. Раковины
толстые, носовые ходы узкие, нижний
формируется только к 4 годам. Пещеристая
ткань развивается к 8 —9 годам.
Придаточные
полости носа. К рождению
ребенка сформированы лишь
гайморовы пазухи; лобная и решетчатая
представляют собой незамкнутые
выпячивания слизистой оболочки,
оформляющиеся в виде полостей только
после 2 лет, основная пазуха отсутствует.
Полностью все придаточные полости носа
развиваются к 12—15 годам.
Слезно-носовой
канал. Короткий, клапаны его
недоразвиты, выходное отверстие
расположено близко от угла век, что
облегчает распространение инфекции
из носа в конъюнктивальный мешок.
Глотка. У
детей раннего возраста относительно
широкая, небные миндалины
при рождении отчетливо видны, но не
выступают из-за хорошо развитых дужек.
Их крипты и сосуды развиты слабо, что в
какой-то мере объясняет редкие заболевания
ангиной на первом году жизни. К концу
первого года лимфоидная ткань
миндалин, в том числе носоглоточной
(аденоиды), нередко гиперплазируется,
особенно у детей с диатезами. Барьерная
их функция в этом возрасте низкая,
как у лимфатических узлов. Разросшаяся
лимфоидная ткань заселяется вирусами
и микробами, образуются очаги инфекции
— аденоидит и хронический
тонзиллит.
Щитовидные хрящи образуют
у маленьких детей тупой
закругленный угол, который после 3
лет становится у мальчиков более острым.
С 10 лет формируется уже характерная
мужская гортань. Истинные голосовые
связки у детей короче, чем у взрослых,
чем и объясняется высота и тембр детского
голоса.
Трахея. У детей
первых месяцев жизни чаще
воронкообразная, в более старшем
возрасте преобладают цилиндрическая
и коническая формы. Верхний конец
ее расположен у новорожденных значительно
выше, чем у взрослых (на уровне IV шейных
позвонков ), и постепенно опускается,
как и уровень бифуркации трахеи (от III
грудного позвонка у новорожденного до
V —VI в 12—14 лет). Каркас трахеи состоит
из 14—16 хрящевых полуколец, соединенных
сзади фиброзной перепонкой (вместо
эластической замыкающей пластины у
взрослых). В перепонке содержится много
мышечных волокон, сокращение или
расслабление которых меняет просвет
органа. Трахея ребенка очень подвижна,
что наряду с меняющимся
просветом и мягкостью хрящей иногда
приводит к щелевидному спадению ее на
выдохе (коллапс) и является причиной
экспираторной одышки или грубого
храпящего дыхания (врожденный стридор).
Симптомы стридора обычно исчезают к 2
годам, когда хрящи становятся более
плотными.
Бронхиальное дерево. К
моменту рождения бронхиальное
дерево сформировано. Размеры
бронхов интенсивно увеличиваются на
первом году жизни и в пубертатном
периоде. Их основу составляют хрящевые
полукольца в раннем детстве, не
имеющие замыкающей эластической
пластинки и соединенные фиброзной
перепонкой, содержащей мышечные волокна.
Хрящи бронхов очень
эластичные, мягкие, пружинят и легко
смещаются. Правый главный бронх
является обычно почти прямым продолжением
трахеи, поэтому именно в нем чаще
обнаруживаются инородные тела.
Бронхи, как и трахея, выстланы
многорядным цилиндрическим эпителием,
мерцательный аппарат которого
формируется уже после рождения
ребенка.
Из-за увеличения толщины
подслизистого слоя и слизистой оболочки
на 1 мм суммарная площадь просвета
бронхов новорожденного уменьшается на
75 % (у взрослого — на 19%). Активная моторика
бронхов недостаточна из-за слабого
развития мышц и мерцательного эпителия.
Незаконченная миелинизация блуждающего
нерва и недоразвитие дыхательной
мускулатуры способствуют слабости
кашлевого толчка у маленького
ребенка; скапливающаяся в бронхиальном
дереве инфицированная слизь закупоривает
просветы мелких бронхов, способствует
ателектазированию и
инфицированию легочной ткани.
функциональной особенностью
бронхиального дерева маленького ребенка
является недостаточное выполнение
дренажной, очистительной функции.
Легкие. У
ребенка, как и у взрослых, легкие имеют
сегментарное строение.
Сегменты отделены друг от друга узкими
бороздками и прослойками соединительной
ткани (дольчатое легкое). Основной
структурной единицей является ацинус,
но терминальные его бронхиолы заканчиваются
не гроздью альвеол, как у
взрослого, а мешочком
(sacculus). Из «кружевных» краев
последнего постепенно формируются
новые альвеолы, число которых у
новорожденного в 3 раза меньше, чем
у взрослого. Увеличивается
диаметр каждой альвеолы (0,05 мм у
новорожденного, 0,12 мм в 4 —5 лет, 0,17 мм к
15 годам). Параллельно нарастает жизненная
емкость легких. Межуточная ткань в
легком ребенка рыхлая, богата сосудами,
клетчаткой, содержит очень мало
соединительнотканных и эластических
волокон. В связи с этим легкие ребенка
первых лет жизни более полнокровны и
менее воздушны, чем у взрослого.
Недоразвитие эластического каркаса
легких способствует как возникновению
эмфиземы, так и ателектазированию
легочной ткани.
Склонность к ателектазу
усиливается из-за дефицита сурфактанта,
пленки, регулирующей поверхностное
альвеолярное натяжение и вырабатываемой
альвеолярными макрофагами. Именно
этот дефицит является причиной
недостаточного расправления легких у
недоношенных после рождения (физиологический
ателектаз).
Плевральная полость. У
ребенка она легко растяжима в связи
со слабым прикреплением париетальных
листков. Висцеральная плевра, особенно
у новорожденных, относительно толстая,
рыхлая, складчатая, содержит ворсинки,
выросты, наиболее выраженные в синусах,
междолевых бороздах.
Диафрагма. В
связи с особенностями грудной клетки
диафрагма играет у маленького ребенка
большую роль в механизме
дыхания, обеспечивая глубину вдоха.
Слабостью ее сокращений частично
объясняется крайне поверхностное
дыхание новорожденного.
Основными
функц. физиологическими особенностями
органов дыхания являются: поверхностный
характер дыхания; физиологическая
одышка (тахипноэ), нередко неправильный
ритм дыхания; напряженность процессов
газообмена и легкое возникновение
дыхательной недостаточности.
1.Глубина
дыхания, абсолютный и относительный
объемы одного дыхательного акта у
ребенка значительно меньше, чем у
взрослого. При крике объем дыхания
увеличивается в 2 —5 раз.
2.Газообмен
у детей осуществляется более энергично,
чем у взрослых, благодаря богатой
васкуляризации легких, скорости
кровотока, высокой диффузионной
способности. В то же время функция
внешнего дыхания у маленького ребенка
нарушается очень быстро из-за недостаточных
экскурсий легких и расправления
альвеол.
Частота дыхания ребенка
новорожденного — 40 — 60 в 1 мин,
годовалого — 30 —35, 5 — 6 лет —20 —25, 10
лет— 18 — 20, взрослого— 15 — 16 в 1
мин.
15.Анатомо-физиологические
особенности органов пищеварения и
печени у детей.
К моменту
рождения пищеварительный тракт ребенка
является одной из наиболее зрелых систем
организма, но адаптирован
к питанию исключительно грудным
молоком.
Полость рта. У
новорожденного и ребенка первых месяцев
жизни полость рта имеет ряд особенностей,
обеспечивающих акт сосания. К ним
относятся относительно малый объем
полости рта и большой язык, хорошее
развитие мышц рта и щек, валикообразные
дубликатуры слизистой оболочки десен
и поперечные складки на слизистой
оболочке губ, жировые тела щеки (комочки
Биша), отличающиеся значительной
упругостью в связи с преобладанием в
них твердых жирных кислот. Слюнные
железы недостаточно развиты. Однако
недостаточное слюноотделение объясняется
в основном незрелостью регулирующих
его нервных центров. По мере их созревания
количество слюны увеличивается, в связи
с чем в 3—4-месячном возрасте у ребенка
нередко появляется так называемое
физиологическое слюнотечение вследствие
не выработанного еще автоматизма ее
проглатывания.
Пищеварение с ротовой
полости, там амилаза, лизоцим, пептидаза.
Эвакуация через 1-2 часа при естественном,
3-4 при искуственном. Переваривание в
тонкой кишке за счет пакреатических
ферментов. Интенсивный гидролиз и
всасывание. В толстом – реабсорбция
воды, солей и органических в-в.
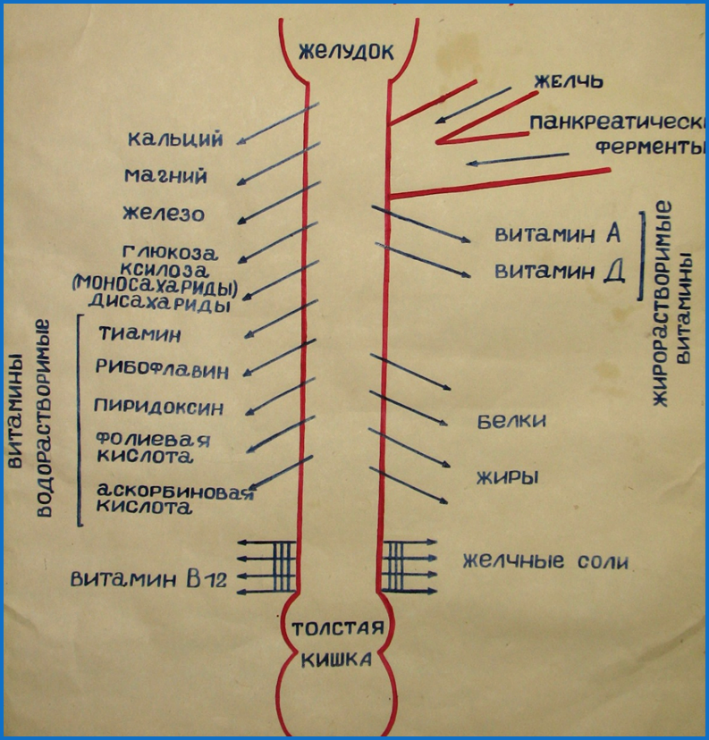 В
первые 3 мес. жизни ребенка:
- слюна
вязкая и вырабатывается в небольшом
количестве, необходимом для
герметизации полости рта при сосании;
— желудок находится в состоянии
физиологического гипертонуса,
имеет небольшой объем, не должен и не
может служить резервуаром и органом
перемешивания пищи. Кардиальный отдел
желудка развит слабо, а пилорический
— хорошо (феномен «открытой
бутылки»), что создает предпосылки
к возникновению срыгивания в случаях
перекорма и заглатывания ребенком
воздуха. Кислотообразование в
желудке находится на низком уровне.
Сразу после рождения происходит
кратковременное «закисление» (в основном
за счет молочной кислоты) желудка
(рН=2,0), выполняющее барьерную роль при
становлении биоценоза пищеварительного
тракта, с последующим установлением рН
на уровне 4—6. В желудке функционируют
лишь две фракции пепсинов:
химозин и гастриксин, а также
желудочная липаза, адаптированные
к низкому уровню интрагастральной
кислотности; Основным действующим
ферментом желудочного сока является
химозин (сычужный фермент, лабфермент),
обеспечивающий первую фазу пищеварения
— створаживание молока. Пепсин (в
присутствии соляной кислоты) и липаза
продолжают гидролиз белков и жиров
створоженного молока.
В грудном возрасте
желудок расположен горизонтально.
По мере роста и развития в период, когда
ребенок начинает ходить, желудок
постепенно принимает вертикальное
положение, и к 7-10 годам он располагается
так же, как у взрослых. Емкость желудка
постепенно увеличивается: при рождении
она составляет 7 мл, в 10 дней –
80 мл, в год – 250 мл, в 3 года –
400–500 мл, в 10 лет – 1500 мл.Рассчитать
объем разового приема пищи для детей
первого года жизни можно по формуле Н.
Ф. Филатова:V =
30 мл + 30 × n,где n – возраст в месяцах.
Созревание секреторного аппарата
желудка происходит раньше и интенсивнее
у детей, находящихся на искусственном
вскармливании, что связано с адаптацией
организма к более трудно перевариваемой
пище.
— поджелудочная железа:
функциональные возможности ограничены.
Липолитическая активность пищеварительных
соков обеспечивает липолиз
жира грудного молока благодаря
участию в пищеварении липазы желудочного
сока и, что особенно важно, липазы
женского молока; Внешнесекреторная
функция заключается в выработке
панкреатического сока. В его состав
входят альбумины, глобулины, микроэлементы
и электролиты, а также большой набор
ферментов, необходимых для переваривания
пищи, в том числе протеолитических
(трипсин, химопсин, эла-стаза и др.),
липолитических (липаза, фосфолипаза А
и В и др.) и амилолитичес-ких (а- и р-амилаза,
мальтаза, лактаза и др.). Внутрисекреторная
функция поджелудочной железы осуществляется
путем синтеза гормонов (инсулин, глюкагон,
липокаин), участвующих в регуляции
углеводного и жирового обмена.
—
печень: У детей печень имеет
относительно большие размеры, масса ее
у новорожденных составляет 4 — 6% от
массы тела (у взрослых — 3%). Паренхима
печени малодифференцирована, дольчатость
строения выявляется только к концу
первого года жизни, она полнокровна,
вследствие чего быстро увеличивается
в размерах при различной патологии,
особенно при инфекционных заболеваниях
и интоксикациях. К 8-летнему возрасту
морфологическое и гистологическое
строение печени такое же, как у
взрослых.
Печень выполняет разнообразные
и очень важные функции: 1) вырабатывает
желчь, которая участвует в кишечном
пищеварении, стимулирует моторную
деятельность кишечника и санирует его
содержимое; 2) депонирует
питательные вещества, в основном
избыток гликогена; 3) осуществляет
барьерную функцию, ограждая организм
от экзогенных и эндогенных патогенных
веществ, токсинов, ядов, и принимает
участие в метаболизме лекарственных
веществ; 4) участвует в
обмене веществ и преобразовании
витаминов A, D, С,
B12, К; 5) в период внутриутробного развития
является кроветворным органом.
Функциональные
возможности печени у маленьких детей
сравнительно низкие. Особенно
несостоятельна ее ферментативная
система у новорожденных. В частности,
метаболизм непрямого
билирубина, высвобождающегося при
гемолизе эритроцитов, осуществляется
не полностью, результатом чего
является физиологическая желтуха.
Желчный пузырь. У
новорожденных желчный пузырь расположен
глубоко в толще печени и
имеет веретенообразную форму, длина
его около 3 см. Типичную грушевидную
форму он приобретает к 6 —7 мес и достигает
края печени к 2 годам. Желчь детей по
своему составу отличается от желчи
взрослых. Она бедна желчными кислотами,
холестерином и солями, но богата
водой, муцином, пигментами, а в
период новорожденности, кроме того, и
мочевиной.
Характерной и благоприятной
особенностью желчи ребенка является
преобладание таурохолевой кислоты
над гликохолевой, так как таурохолевая
кислота усиливает бактерицидный
эффект желчи, а также ускоряет отделение
панкреатического сока. Желчь
эмульгирует жиры, растворяет жирные
кислоты, улучшает перистальтику.
—
тонкая кишка относительно роста
длиннее (на 1/3), чем у взрослых, и имеет
наиболее высокую в
сравнении с другими отделами
пищеварительного тракта степень
морфофункциональной зрелости.
Активность лактазы
максимальна — в 10 раз выше, чем у
взрослых. В связи с большой пищевой
нагрузкой и дистальным типом пищеварения
(у старших детей и взрослых пищеварение
в основном происходит в проксимальных
отделах тонкой кишки) резервные
возможности пищеварительно-транспортного
конвейера ребенка первого года жизни
очень ограничены. Наряду с полостным,
мембранным и симбиотическим (бактериальным)
пищеварением у ребенка первых месяцев
жизни важную роль играет пиноцитоз.
Пиноцитоз является одновременно формой
внутриклеточного (вакуольного) пищеварения
и везикулярного всасывания, характерной
именно для неонатального периода.
Пиноцитоз обеспечивает всасывание
через кишечную стенку в нерасщепленном
виде непосредственно
в кровь белков
грудного молока
(лактоальбумина и лактоглобулина),
а также иммуноглобулинов.
При естественном вскармливании это
оптимизирует белковый обмен и поддерживает
уровень пассивного иммунитета. При
искусственном вскармливании пиноцитоз
неизмененных белков коровьего молока
и пептидов может стать причиной
сенсибилизации к ним;
— толстая
кишка: после рождения происходит
заселение пищеварительного тракта
микрофлорой. В становлении микробного
пейзажа, в преодолении транзиторного
дисбиоценоза исключительно важную роль
выполняет раннее прикладывание
новорожденного к груди. микрофлора
у детей, находящихся на исключительно
грудном вскармливании, представлена
преимущественно бифидобактериями
и бифидобактероидами (титр 10 10—10 2
). На долю сопутствующей (кишечная
палочка, лактобактерии, ацидофильные
палочки и энтерококки) и остаточной
флоры (стафилококк, протей) приходится
не более 1—4%. Нормальный биоценоз и
барьерная функция кишечника поддерживается
только благодаря иммуноглобулинам,
лизоциму и ряду других защитных
факторов материнского молока. В случае
перевода ребенка на искусственное и
смешанное вскармливание увеличивается
представительство кишечной палочки и
энтерококков, количество бифидобактерий
уменьшается. Активная моторика
отражается на частоте опорожнения
кишечника. У грудных детей дефекация
происходит рефлекторно, в первые 2 нед
жизни до 3—6 раз в сутки, затем реже, к
концу первого года жизни она становится
произвольным актом. В первые 2—3 дня
после рождения ребенок выделяет меконий
(первородный кал) зеленовато-черного
цвета. Он состоит из желчи, эпителиальных
клеток, слизи, энзимов, проглоченных
околоплодных вод. Испражнения здоровых
новорожденных, находящихся на естественном
вскармливании, имеют кашицеобразную
консистенцию, золотисто-желтую окраску,
кисловатый запах.
С 4—5 месяцев до
1 года:
— слюноотделение
становится обильным, достигая к 1-му
году 150 мл/сут. Слюна приобретает
способность ослизнення
пищи и пенообразования, возрастает
ее бактерицидность;
— желудок:
сохраняется физиологический гипертонус,
объем постепенно увеличивается,
после введения прикормов
кислотность желудочного сока возрастает;
— печень относительно велика
(край правой доли печени по среднеключичной
линии выступает на 1—2 см ниже реберной
дуги). Выделение желчных кислот невелико,
что при искусственном вскармливании
создает предпосылки к развитию стеатореи;
— кишечник: сохраняется
преимущественно тонкокишечный
тип пищеварения, но пиноцитоз
прекращается, барьерная функция
кишечной стенки возрастает;
—
микрофлора кишки с введением прикорма
меняется — увеличивается представительство
ГР-флоры, кишечной палочки — 300-600 млн/г,
в том числе возможно появление (до 10%)
ее дефектных форм, титр бифидобактерий
снижается до 10 '—10~и , кокки составляют
до 25% всей микрофлоры. Ранний перевод
ребенка на искусственное вскармливание
способствует сенсибилизации, а также
форсирует темпы созревания пищеварительного
тракта ребенка. При этом происходит
пролиферация в слизистой оболочке
антрального отдела желудка G-клеток,
продуцирующих гастрин, и Eel-клеток,
вырабатывающих гистамин. Это один из
факторов, создающих в перспективе
предпосылки к формированию интрагастральной
гиперацидности и хронической
гастродуоденальной патологии.
После
1 года: — желудок приобретает
пластический тонус, объем желудка
и кислотность желудочного сока с
возрастом увеличиваются. Основной
протеазой желудка становится пепсиноген
А;
— поджелудочная железа:
выработка панкреатического секрета
и ферментов возрастает;
— печень:
до 7 лет
правая доля по среднеключичной линии
выступает из-под реберной дуги на
1—1,5 см, в более старшем возрасте ее
пальпируют у края реберной дуги;
—
кишечник: снижается
активность лактазы. Область наиболее
интенсивного усвоения питательных
веществ смещается в проксимальные
отделы тонкой
кишки.
16.Особенности пищеварения
у детей. Бактериальная флора
кишечника.
Пищеварение с ротовой
полости, там амилаза, лизоцим, пептидаза.
Эвакуация через 1-2 часа при естественном,
3-4 при искуственном. Переваривание в
тонкой кишке за счет пакреатических
ферментов. Интенсивный гидролиз и
всасывание. В толстом – реабсорбция
воды, солей и органических в-в.
Первые
3 мес.
— микрофлора у детей,
находящихся на исключительно грудном
вскармливании, представлена преимущественно
бифидобактериями и бифидобактероидами
(титр 10 10—10 2 ). На долю сопутствующей
(кишечная палочка, лактобактерии,
ацидофильные палочки и энтерококки) и
остаточной флоры (стафилококк, протей)
приходится не более 1—4%. Нормальный
биоценоз и барьерная функция кишечника
поддерживается только благодаря
иммуноглобулинам, лизоциму и ряду
других защитных факторов материнского
молока. В случае перевода ребенка на
искусственное и смешанное вскармливание
увеличивается представительство
кишечной палочки и энтерококков,
количество бифидобактерий уменьшается.
4-5
мес до года.
— микрофлора кишки с
введением прикорма меняется — и ГР-
увеличивается представительство
кишечной палочки — 300-600 млн/г, в том
числе возможно появление (до 10%) ее
дефектных форм, титр бифидобактерий
снижается до 10 '—10~и , кокки составляют
до 25% всей микрофлоры. Ранний перевод
ребенка на искусственное вскармливание
способствует сенсибилизации, а также
форсирует темпы созревания пищеварительного
тракта ребенка. При этом происходит
пролиферация в слизистой оболочке
антрального отдела желудка G-клеток,
продуцирующих гастрин, и Eel-клеток,
вырабатывающих гистамин. Это один из
факторов, создающих в перспективе
предпосылки к формированию интрагастральной
гиперацидности и хронической
гастродуоденальной патологии.
Микрофлора. В
период внутриутробного развития кишечник
плода стерилен. Заселение его
микроорганизмами происходит сначала
при прохождении родовых путей матери,
затем через рот при контакте детей с
окружающими предметами. Желудок
и двенадцатиперстная кишка содержат
скудную бактериальную флору. В
тонком и особенно толстом кишечнике
она становится разнообразнее, количество
микробов увеличивается; микробная флора
зависит в основном от вида вскармливания
ребенка. При вскармливании материнским
молоком основной флорой является В.
bifidum, росту которой способствует
(бетта-лактоза женского молока. При
введении в питание прикорма или
переводе ребенка на вскармливание
коровьим молоком в кишечнике преобладает
грамотрицательная кишечная палочка,
представляющая собой условно-патогенный
микроорганизм. В связи с этим у детей,
находящихся на искусственном
вскармливании, чаще наблюдаются
диспепсии. По современным представлениям,
нормальная кишечная флора выполняет
три основные функции: 1) создание
иммунологического барьера; 2) окончательное
переваривание остатков пищи и
пищеварительных ферментов; 3) синтез
витаминов и ферментов. Нормальный
состав микрофлоры кишечника (эубиоз)
легко нарушается под влиянием
инфицирования, неправильного режима
питания, а также нерационального
использования антибактериальных средств
и других препаратов, приводящих к
состоянию кишечного
дисбактериоза.
17.Анатомо-физиологические
особенности органов мочевыделения у
детей.
К моменту рождения
морфологическое и функциональное
созревание почек еще не закончено.
У детей младшего возраста размеры почек
относительно больше, отношение их массы
к массе тела новорожденного составляет
1:100, к массе тела у взрослых — 1:200. Верхний
полюс находится на уровне XI—XII грудных
позвонков, нижний — на уровне IV поясничного
позвонка, т.е. ниже гребешка подвздошной
кости. К 2 годам эти топографические
особенности исчезают. В дальнейшем рост
почек соответствует росту тела. Строение
их в первые годы жизни дольчатое.
Жировая капсула выражена слабо,
поэтому у детей младшего возраста почки
более подвижны.
Недостаточно развиты и почечные
канальцы, юкстагломерулярный аппарат
у детей младшего возраста не сформирован.
Морфологическое созревание коркового
вещества заканчивается к 3—5 годам, а
почки в целом — к школьному возрасту.
Почки
выполняют две основные функции:
1) регулируют
состав внеклеточной жидкости и
кислотно-основного состояния
организма;
2) обеспечивают
выведение из организма токсических
веществ или продуктов метаболизма,
подлежащих удалению.
При замене
материнского молока коровьим белковая
нагрузка резко возрастает, увеличивается
количество продуктов, подлежащих
удалению, почки работают с большим
напряжением, рН крови легко сдвигается
в кислую сторону.
Низкая величина клубочковой
фильтрации приводит к так называемому
физиологическому ацидозу, от которого
зависят такие клинические симптомы,
как расстройство глубины и ритма дыхания,
цианоз. К этому метаболическому
ацидозу присоединяется канальцевый
ацидоз, возникающий из-за сниженной
активности ферментов, участвующих в
выведении водородных ионов. Способность
почек к выведению избытка Н+ развивается
лишь во втором полугодии жизни.
Мочеточники.
У детей раннего возраста мочеточники
относительно шире, чем у взрослых,
более извилисты, гипотоничны: их
мышечные и эластические волокна
развиты слабо. Все это предрасполагает
к застою мочи и присоединению
микровоспалительного процесса в
вышележащих отделах.
Мочевой
пузырь. У грудных детей расположен
выше, чем у взрослых, имеет овальную
форму и более развитую слизистую
оболочку. По мере роста ребенка
происходит утолщение мышечного слоя
и эластических волокон. Емкость пузыря
у новорожденного — до 50 мл, у
годовалого ребенка — до 200 мл.
В первые 3—4 дня жизни мочи
выделяется очень мало или ее вовсе
нет в связи с экстраренальными потерями
и малым поступлением воды. Моча может
содержать небольшое количество белка
и эритроцитов, что нельзя рассматривать
как признак воспаления. Число мочеиспусканий
у новорожденных — 20—25, у грудных детей
— не менее 15 в сутки. По сравнению со
взрослыми дети выделяют мочи относительно
больше в связи с интенсивным обменом
веществ и своеобразиями рациона питания.
Большое влияние на диурез оказывает
температура воздуха. При высокой
температуре количество мочи уменьшается,
при низкой, наоборот, увеличивается.
Имеет значение и питьевой режим. У детей
после года происходит быстрое нарастание
выделения фосфатов, калия, хлоридов. В
то же время количество мочевой кислоты
остается на одном и том же уровне. Очень
высокое содержание мочевой кислоты и
ее солей у новорожденного наблюдается
на 3—4-й день жизни.
Формирование
условного рефлекса и навыков
опрятности можно начинать с 5—6
мес. К концу первого года жизни в
периоды бодрствования ребенок должен
проситься на горшок. Однако во время
сна, увлекательных игр, волнения
непроизвольное мочеиспускание может
наблюдаться у детей до
трехлетнего возраста.
Вследствие
адаптации, количество выделяемой мочи
значительно уменьшается. Так как мочевая
кислота не выводится полностью из
организма и задерживается в почках, её
концентрация возрастает. В связи с этим,
моча ребенка становится не прозрачной
и приобретает характерный окрас. Первые
симптомы возникают, как правило, к концу
первой недели жизни младенца и зачастую
исчезают в течение 2-3 дней.
18.
Особенности кроветворения и характеристика
периферической крови у детей в различные
возрастные периоды.
Кровь
новорожденного. Общее количество крови
у детей не является постоянной
величиной и зависит от массы тела,
времени перевязки пуповины, доношенности
ребенка. В среднем у новорожденного
объем крови составляет около 14,7% его
массы тела, т. е. 140—150 мл на 1 кг (500мл)
массы тела, а у взрослого — соответственно
5,0—5,6%, или 50—70 мл/кг.
В периферической
крови здорового новорожденного
повышено содержание гемоглобина
(170—240 г/л) и эритроцитов (5—7-1012/л),
а цветовой показатель колеблется от
0,9 до 1,3. С первых же часов после рождения
начинается распад
эритроцитов, что клинически
обусловливает появление
физиологической желтухи.
К
рождению фетальный гемоглобин
составляет 60-85%, а взрослый 15-40%. После
рождения количество HbF в циркулирующей
крови снижается примерно на 3% в неделю,
достигая к 6 месяцам 2—3%.
Эритроциты
полихроматофильны, имеют различную
величину (анизоцитоз), преобладают
макроциты. Диаметр
эритроцитов в первые дни жизни составляет
7,9—8,2 мкм (при норме 7,2—7,5 мкм). Ретикулоцитоз
в первые дни достигает 22—42 % (у
взрослых и детей старше 1 мес 6—8 %),
встречаются ядерные формы
эритроцитов — нормобласты. Минимальная
резистентность (осмотическая стойкость)
эритроцитов несколько ниже, т. е. гемолиз
наступает при больших концентрациях
NaCl — 0,48—0,52%, а максимальная — выше
0,24—0,3%. У взрослых и детей школьного и
дошкольного возраста минимальная
резистентность равна 0,44—0,48%, а максимальная
— 0,28—0,36%.
Эритропоэз при рождении
протекает в 5 раз интенсивнее, чем у
детей старше года и взрослых, но после
рождения выработка эритропоэтинов
снижается. В связи с переходом на легочное
дыхание повышается эффективность
газообмена, отпадает
необходимость в избытке эритроцитов и
гемоглобина, у доношенных новорожденных
содержание его быстро
снижается до 110—
119 г/л. Это происходит
за счет гемолиза и гемодилюции вследствие
быстрого увеличения
размеров тела.
Максимальное снижение показателей
у доношенных детей происходит к 2,5-3
месяцам с нормализацией к году. Средний
объем эритроцита уменьшается до 80 фл к
6 месяцам.
В крови плода и новорожденного
первых часов жизни встречается много
стволовых клеток; по данным А. Г.
Румянцева, содержание клеток-предшественников
в пуповинной крови в 6—8 раз выше, чем в
аналогичном объеме пунктата костного
мозга взрослого. Особенностью новорожденных
детей является легкость возврата к
экстрамедуллярному кроветворению. В
онтогенезе происходит смена «пластов»
— клонов кроветворных клеток,
обусловливающая особенности системы
крови в различные периоды.
Лейкоцитарная
формула у новорожденных имеет особенности.
В первые дни жизни лейкоцитарная формула
сдвинута влево,
преобладают нейтрофилы,
функция которых у новорожденных снижена
за счет уменьшения активности опсонинов
плазмы. В первые сутки после рождения
относительное число лимфоцитов
составляет: Т-50%; В-35%; 0-15%. Изменения
выражаются в падении числа нейтрофилов
и увеличении количества Т- и В-лимфоцитов.
Абсолютное число нейтрофилов наибольшее
у новорожденных, на первом году жизни
их число уменьшается. На
5-й день жизни число нейтрофилов и
лимфоцитов сравнивается (так
называемый первый перекрест). Затем
происходит дальнейшее возрастание
числа лимфоцитов к 10-му дню.
Таким образом, лейкоцитарная формула
грудного ребенка характеризуется
относительно большим количеством
лимфоцитов и малым – нейтрофилов.
После
года вновь начинает увеличиваться число
нейтрофилов на
фоне снижения лимфоцитов. В возрасте
5 лет происходит второй
перекрест Е
лейкоцитарной формуле, когда число
нейтрофилов и лимфоцитов вновь становится
равным. В дальнейшем
продолжается нарастание числа нейтрофилов.
С 12-летнего возраста гемограмма ребенка
не отличается от таковой взрослого
человека. СОЭ в течение детства
существенно не меняется.
Особенностями
системы гемостаза к моменту рождения
является относительно низкая активность
витамин-К-зависимых факторов свертывания
(II; VII; IX; X). Активность их снижается до
3-го дня, что может быть причиной развития
геморрагической болезни
новорожденных, затем начинает
возрастать. Количество тромбоцитов
практически не отличается от такового
у взрослых, однако функциональная их
активность в первые дни жизни ниже.
В
первые 3 мес. жизни ребенка:
- слюна
вязкая и вырабатывается в небольшом
количестве, необходимом для
герметизации полости рта при сосании;
— желудок находится в состоянии
физиологического гипертонуса,
имеет небольшой объем, не должен и не
может служить резервуаром и органом
перемешивания пищи. Кардиальный отдел
желудка развит слабо, а пилорический
— хорошо (феномен «открытой
бутылки»), что создает предпосылки
к возникновению срыгивания в случаях
перекорма и заглатывания ребенком
воздуха. Кислотообразование в
желудке находится на низком уровне.
Сразу после рождения происходит
кратковременное «закисление» (в основном
за счет молочной кислоты) желудка
(рН=2,0), выполняющее барьерную роль при
становлении биоценоза пищеварительного
тракта, с последующим установлением рН
на уровне 4—6. В желудке функционируют
лишь две фракции пепсинов:
химозин и гастриксин, а также
желудочная липаза, адаптированные
к низкому уровню интрагастральной
кислотности; Основным действующим
ферментом желудочного сока является
химозин (сычужный фермент, лабфермент),
обеспечивающий первую фазу пищеварения
— створаживание молока. Пепсин (в
присутствии соляной кислоты) и липаза
продолжают гидролиз белков и жиров
створоженного молока.
В грудном возрасте
желудок расположен горизонтально.
По мере роста и развития в период, когда
ребенок начинает ходить, желудок
постепенно принимает вертикальное
положение, и к 7-10 годам он располагается
так же, как у взрослых. Емкость желудка
постепенно увеличивается: при рождении
она составляет 7 мл, в 10 дней –
80 мл, в год – 250 мл, в 3 года –
400–500 мл, в 10 лет – 1500 мл.Рассчитать
объем разового приема пищи для детей
первого года жизни можно по формуле Н.
Ф. Филатова:V =
30 мл + 30 × n,где n – возраст в месяцах.
Созревание секреторного аппарата
желудка происходит раньше и интенсивнее
у детей, находящихся на искусственном
вскармливании, что связано с адаптацией
организма к более трудно перевариваемой
пище.
— поджелудочная железа:
функциональные возможности ограничены.
Липолитическая активность пищеварительных
соков обеспечивает липолиз
жира грудного молока благодаря
участию в пищеварении липазы желудочного
сока и, что особенно важно, липазы
женского молока; Внешнесекреторная
функция заключается в выработке
панкреатического сока. В его состав
входят альбумины, глобулины, микроэлементы
и электролиты, а также большой набор
ферментов, необходимых для переваривания
пищи, в том числе протеолитических
(трипсин, химопсин, эла-стаза и др.),
липолитических (липаза, фосфолипаза А
и В и др.) и амилолитичес-ких (а- и р-амилаза,
мальтаза, лактаза и др.). Внутрисекреторная
функция поджелудочной железы осуществляется
путем синтеза гормонов (инсулин, глюкагон,
липокаин), участвующих в регуляции
углеводного и жирового обмена.
—
печень: У детей печень имеет
относительно большие размеры, масса ее
у новорожденных составляет 4 — 6% от
массы тела (у взрослых — 3%). Паренхима
печени малодифференцирована, дольчатость
строения выявляется только к концу
первого года жизни, она полнокровна,
вследствие чего быстро увеличивается
в размерах при различной патологии,
особенно при инфекционных заболеваниях
и интоксикациях. К 8-летнему возрасту
морфологическое и гистологическое
строение печени такое же, как у
взрослых.
Печень выполняет разнообразные
и очень важные функции: 1) вырабатывает
желчь, которая участвует в кишечном
пищеварении, стимулирует моторную
деятельность кишечника и санирует его
содержимое; 2) депонирует
питательные вещества, в основном
избыток гликогена; 3) осуществляет
барьерную функцию, ограждая организм
от экзогенных и эндогенных патогенных
веществ, токсинов, ядов, и принимает
участие в метаболизме лекарственных
веществ; 4) участвует в
обмене веществ и преобразовании
витаминов A, D, С,
B12, К; 5) в период внутриутробного развития
является кроветворным органом.
Функциональные
возможности печени у маленьких детей
сравнительно низкие. Особенно
несостоятельна ее ферментативная
система у новорожденных. В частности,
метаболизм непрямого
билирубина, высвобождающегося при
гемолизе эритроцитов, осуществляется
не полностью, результатом чего
является физиологическая желтуха.
Желчный пузырь. У
новорожденных желчный пузырь расположен
глубоко в толще печени и
имеет веретенообразную форму, длина
его около 3 см. Типичную грушевидную
форму он приобретает к 6 —7 мес и достигает
края печени к 2 годам. Желчь детей по
своему составу отличается от желчи
взрослых. Она бедна желчными кислотами,
холестерином и солями, но богата
водой, муцином, пигментами, а в
период новорожденности, кроме того, и
мочевиной.
Характерной и благоприятной
особенностью желчи ребенка является
преобладание таурохолевой кислоты
над гликохолевой, так как таурохолевая
кислота усиливает бактерицидный
эффект желчи, а также ускоряет отделение
панкреатического сока. Желчь
эмульгирует жиры, растворяет жирные
кислоты, улучшает перистальтику.
—
тонкая кишка относительно роста
длиннее (на 1/3), чем у взрослых, и имеет
наиболее высокую в
сравнении с другими отделами
пищеварительного тракта степень
морфофункциональной зрелости.
Активность лактазы
максимальна — в 10 раз выше, чем у
взрослых. В связи с большой пищевой
нагрузкой и дистальным типом пищеварения
(у старших детей и взрослых пищеварение
в основном происходит в проксимальных
отделах тонкой кишки) резервные
возможности пищеварительно-транспортного
конвейера ребенка первого года жизни
очень ограничены. Наряду с полостным,
мембранным и симбиотическим (бактериальным)
пищеварением у ребенка первых месяцев
жизни важную роль играет пиноцитоз.
Пиноцитоз является одновременно формой
внутриклеточного (вакуольного) пищеварения
и везикулярного всасывания, характерной
именно для неонатального периода.
Пиноцитоз обеспечивает всасывание
через кишечную стенку в нерасщепленном
виде непосредственно
в кровь белков
грудного молока
(лактоальбумина и лактоглобулина),
а также иммуноглобулинов.
При естественном вскармливании это
оптимизирует белковый обмен и поддерживает
уровень пассивного иммунитета. При
искусственном вскармливании пиноцитоз
неизмененных белков коровьего молока
и пептидов может стать причиной
сенсибилизации к ним;
— толстая
кишка: после рождения происходит
заселение пищеварительного тракта
микрофлорой. В становлении микробного
пейзажа, в преодолении транзиторного
дисбиоценоза исключительно важную роль
выполняет раннее прикладывание
новорожденного к груди. микрофлора
у детей, находящихся на исключительно
грудном вскармливании, представлена
преимущественно бифидобактериями
и бифидобактероидами (титр 10 10—10 2
). На долю сопутствующей (кишечная
палочка, лактобактерии, ацидофильные
палочки и энтерококки) и остаточной
флоры (стафилококк, протей) приходится
не более 1—4%. Нормальный биоценоз и
барьерная функция кишечника поддерживается
только благодаря иммуноглобулинам,
лизоциму и ряду других защитных
факторов материнского молока. В случае
перевода ребенка на искусственное и
смешанное вскармливание увеличивается
представительство кишечной палочки и
энтерококков, количество бифидобактерий
уменьшается. Активная моторика
отражается на частоте опорожнения
кишечника. У грудных детей дефекация
происходит рефлекторно, в первые 2 нед
жизни до 3—6 раз в сутки, затем реже, к
концу первого года жизни она становится
произвольным актом. В первые 2—3 дня
после рождения ребенок выделяет меконий
(первородный кал) зеленовато-черного
цвета. Он состоит из желчи, эпителиальных
клеток, слизи, энзимов, проглоченных
околоплодных вод. Испражнения здоровых
новорожденных, находящихся на естественном
вскармливании, имеют кашицеобразную
консистенцию, золотисто-желтую окраску,
кисловатый запах.
С 4—5 месяцев до
1 года:
— слюноотделение
становится обильным, достигая к 1-му
году 150 мл/сут. Слюна приобретает
способность ослизнення
пищи и пенообразования, возрастает
ее бактерицидность;
— желудок:
сохраняется физиологический гипертонус,
объем постепенно увеличивается,
после введения прикормов
кислотность желудочного сока возрастает;
— печень относительно велика
(край правой доли печени по среднеключичной
линии выступает на 1—2 см ниже реберной
дуги). Выделение желчных кислот невелико,
что при искусственном вскармливании
создает предпосылки к развитию стеатореи;
— кишечник: сохраняется
преимущественно тонкокишечный
тип пищеварения, но пиноцитоз
прекращается, барьерная функция
кишечной стенки возрастает;
—
микрофлора кишки с введением прикорма
меняется — увеличивается представительство
ГР-флоры, кишечной палочки — 300-600 млн/г,
в том числе возможно появление (до 10%)
ее дефектных форм, титр бифидобактерий
снижается до 10 '—10~и , кокки составляют
до 25% всей микрофлоры. Ранний перевод
ребенка на искусственное вскармливание
способствует сенсибилизации, а также
форсирует темпы созревания пищеварительного
тракта ребенка. При этом происходит
пролиферация в слизистой оболочке
антрального отдела желудка G-клеток,
продуцирующих гастрин, и Eel-клеток,
вырабатывающих гистамин. Это один из
факторов, создающих в перспективе
предпосылки к формированию интрагастральной
гиперацидности и хронической
гастродуоденальной патологии.
После
1 года: — желудок приобретает
пластический тонус, объем желудка
и кислотность желудочного сока с
возрастом увеличиваются. Основной
протеазой желудка становится пепсиноген
А;
— поджелудочная железа:
выработка панкреатического секрета
и ферментов возрастает;
— печень:
до 7 лет
правая доля по среднеключичной линии
выступает из-под реберной дуги на
1—1,5 см, в более старшем возрасте ее
пальпируют у края реберной дуги;
—
кишечник: снижается
активность лактазы. Область наиболее
интенсивного усвоения питательных
веществ смещается в проксимальные
отделы тонкой
кишки.
16.Особенности пищеварения
у детей. Бактериальная флора
кишечника.
Пищеварение с ротовой
полости, там амилаза, лизоцим, пептидаза.
Эвакуация через 1-2 часа при естественном,
3-4 при искуственном. Переваривание в
тонкой кишке за счет пакреатических
ферментов. Интенсивный гидролиз и
всасывание. В толстом – реабсорбция
воды, солей и органических в-в.
Первые
3 мес.
— микрофлора у детей,
находящихся на исключительно грудном
вскармливании, представлена преимущественно
бифидобактериями и бифидобактероидами
(титр 10 10—10 2 ). На долю сопутствующей
(кишечная палочка, лактобактерии,
ацидофильные палочки и энтерококки) и
остаточной флоры (стафилококк, протей)
приходится не более 1—4%. Нормальный
биоценоз и барьерная функция кишечника
поддерживается только благодаря
иммуноглобулинам, лизоциму и ряду
других защитных факторов материнского
молока. В случае перевода ребенка на
искусственное и смешанное вскармливание
увеличивается представительство
кишечной палочки и энтерококков,
количество бифидобактерий уменьшается.
4-5
мес до года.
— микрофлора кишки с
введением прикорма меняется — и ГР-
увеличивается представительство
кишечной палочки — 300-600 млн/г, в том
числе возможно появление (до 10%) ее
дефектных форм, титр бифидобактерий
снижается до 10 '—10~и , кокки составляют
до 25% всей микрофлоры. Ранний перевод
ребенка на искусственное вскармливание
способствует сенсибилизации, а также
форсирует темпы созревания пищеварительного
тракта ребенка. При этом происходит
пролиферация в слизистой оболочке
антрального отдела желудка G-клеток,
продуцирующих гастрин, и Eel-клеток,
вырабатывающих гистамин. Это один из
факторов, создающих в перспективе
предпосылки к формированию интрагастральной
гиперацидности и хронической
гастродуоденальной патологии.
Микрофлора. В
период внутриутробного развития кишечник
плода стерилен. Заселение его
микроорганизмами происходит сначала
при прохождении родовых путей матери,
затем через рот при контакте детей с
окружающими предметами. Желудок
и двенадцатиперстная кишка содержат
скудную бактериальную флору. В
тонком и особенно толстом кишечнике
она становится разнообразнее, количество
микробов увеличивается; микробная флора
зависит в основном от вида вскармливания
ребенка. При вскармливании материнским
молоком основной флорой является В.
bifidum, росту которой способствует
(бетта-лактоза женского молока. При
введении в питание прикорма или
переводе ребенка на вскармливание
коровьим молоком в кишечнике преобладает
грамотрицательная кишечная палочка,
представляющая собой условно-патогенный
микроорганизм. В связи с этим у детей,
находящихся на искусственном
вскармливании, чаще наблюдаются
диспепсии. По современным представлениям,
нормальная кишечная флора выполняет
три основные функции: 1) создание
иммунологического барьера; 2) окончательное
переваривание остатков пищи и
пищеварительных ферментов; 3) синтез
витаминов и ферментов. Нормальный
состав микрофлоры кишечника (эубиоз)
легко нарушается под влиянием
инфицирования, неправильного режима
питания, а также нерационального
использования антибактериальных средств
и других препаратов, приводящих к
состоянию кишечного
дисбактериоза.
17.Анатомо-физиологические
особенности органов мочевыделения у
детей.
К моменту рождения
морфологическое и функциональное
созревание почек еще не закончено.
У детей младшего возраста размеры почек
относительно больше, отношение их массы
к массе тела новорожденного составляет
1:100, к массе тела у взрослых — 1:200. Верхний
полюс находится на уровне XI—XII грудных
позвонков, нижний — на уровне IV поясничного
позвонка, т.е. ниже гребешка подвздошной
кости. К 2 годам эти топографические
особенности исчезают. В дальнейшем рост
почек соответствует росту тела. Строение
их в первые годы жизни дольчатое.
Жировая капсула выражена слабо,
поэтому у детей младшего возраста почки
более подвижны.
Недостаточно развиты и почечные
канальцы, юкстагломерулярный аппарат
у детей младшего возраста не сформирован.
Морфологическое созревание коркового
вещества заканчивается к 3—5 годам, а
почки в целом — к школьному возрасту.
Почки
выполняют две основные функции:
1) регулируют
состав внеклеточной жидкости и
кислотно-основного состояния
организма;
2) обеспечивают
выведение из организма токсических
веществ или продуктов метаболизма,
подлежащих удалению.
При замене
материнского молока коровьим белковая
нагрузка резко возрастает, увеличивается
количество продуктов, подлежащих
удалению, почки работают с большим
напряжением, рН крови легко сдвигается
в кислую сторону.
Низкая величина клубочковой
фильтрации приводит к так называемому
физиологическому ацидозу, от которого
зависят такие клинические симптомы,
как расстройство глубины и ритма дыхания,
цианоз. К этому метаболическому
ацидозу присоединяется канальцевый
ацидоз, возникающий из-за сниженной
активности ферментов, участвующих в
выведении водородных ионов. Способность
почек к выведению избытка Н+ развивается
лишь во втором полугодии жизни.
Мочеточники.
У детей раннего возраста мочеточники
относительно шире, чем у взрослых,
более извилисты, гипотоничны: их
мышечные и эластические волокна
развиты слабо. Все это предрасполагает
к застою мочи и присоединению
микровоспалительного процесса в
вышележащих отделах.
Мочевой
пузырь. У грудных детей расположен
выше, чем у взрослых, имеет овальную
форму и более развитую слизистую
оболочку. По мере роста ребенка
происходит утолщение мышечного слоя
и эластических волокон. Емкость пузыря
у новорожденного — до 50 мл, у
годовалого ребенка — до 200 мл.
В первые 3—4 дня жизни мочи
выделяется очень мало или ее вовсе
нет в связи с экстраренальными потерями
и малым поступлением воды. Моча может
содержать небольшое количество белка
и эритроцитов, что нельзя рассматривать
как признак воспаления. Число мочеиспусканий
у новорожденных — 20—25, у грудных детей
— не менее 15 в сутки. По сравнению со
взрослыми дети выделяют мочи относительно
больше в связи с интенсивным обменом
веществ и своеобразиями рациона питания.
Большое влияние на диурез оказывает
температура воздуха. При высокой
температуре количество мочи уменьшается,
при низкой, наоборот, увеличивается.
Имеет значение и питьевой режим. У детей
после года происходит быстрое нарастание
выделения фосфатов, калия, хлоридов. В
то же время количество мочевой кислоты
остается на одном и том же уровне. Очень
высокое содержание мочевой кислоты и
ее солей у новорожденного наблюдается
на 3—4-й день жизни.
Формирование
условного рефлекса и навыков
опрятности можно начинать с 5—6
мес. К концу первого года жизни в
периоды бодрствования ребенок должен
проситься на горшок. Однако во время
сна, увлекательных игр, волнения
непроизвольное мочеиспускание может
наблюдаться у детей до
трехлетнего возраста.
Вследствие
адаптации, количество выделяемой мочи
значительно уменьшается. Так как мочевая
кислота не выводится полностью из
организма и задерживается в почках, её
концентрация возрастает. В связи с этим,
моча ребенка становится не прозрачной
и приобретает характерный окрас. Первые
симптомы возникают, как правило, к концу
первой недели жизни младенца и зачастую
исчезают в течение 2-3 дней.
18.
Особенности кроветворения и характеристика
периферической крови у детей в различные
возрастные периоды.
Кровь
новорожденного. Общее количество крови
у детей не является постоянной
величиной и зависит от массы тела,
времени перевязки пуповины, доношенности
ребенка. В среднем у новорожденного
объем крови составляет около 14,7% его
массы тела, т. е. 140—150 мл на 1 кг (500мл)
массы тела, а у взрослого — соответственно
5,0—5,6%, или 50—70 мл/кг.
В периферической
крови здорового новорожденного
повышено содержание гемоглобина
(170—240 г/л) и эритроцитов (5—7-1012/л),
а цветовой показатель колеблется от
0,9 до 1,3. С первых же часов после рождения
начинается распад
эритроцитов, что клинически
обусловливает появление
физиологической желтухи.
К
рождению фетальный гемоглобин
составляет 60-85%, а взрослый 15-40%. После
рождения количество HbF в циркулирующей
крови снижается примерно на 3% в неделю,
достигая к 6 месяцам 2—3%.
Эритроциты
полихроматофильны, имеют различную
величину (анизоцитоз), преобладают
макроциты. Диаметр
эритроцитов в первые дни жизни составляет
7,9—8,2 мкм (при норме 7,2—7,5 мкм). Ретикулоцитоз
в первые дни достигает 22—42 % (у
взрослых и детей старше 1 мес 6—8 %),
встречаются ядерные формы
эритроцитов — нормобласты. Минимальная
резистентность (осмотическая стойкость)
эритроцитов несколько ниже, т. е. гемолиз
наступает при больших концентрациях
NaCl — 0,48—0,52%, а максимальная — выше
0,24—0,3%. У взрослых и детей школьного и
дошкольного возраста минимальная
резистентность равна 0,44—0,48%, а максимальная
— 0,28—0,36%.
Эритропоэз при рождении
протекает в 5 раз интенсивнее, чем у
детей старше года и взрослых, но после
рождения выработка эритропоэтинов
снижается. В связи с переходом на легочное
дыхание повышается эффективность
газообмена, отпадает
необходимость в избытке эритроцитов и
гемоглобина, у доношенных новорожденных
содержание его быстро
снижается до 110—
119 г/л. Это происходит
за счет гемолиза и гемодилюции вследствие
быстрого увеличения
размеров тела.
Максимальное снижение показателей
у доношенных детей происходит к 2,5-3
месяцам с нормализацией к году. Средний
объем эритроцита уменьшается до 80 фл к
6 месяцам.
В крови плода и новорожденного
первых часов жизни встречается много
стволовых клеток; по данным А. Г.
Румянцева, содержание клеток-предшественников
в пуповинной крови в 6—8 раз выше, чем в
аналогичном объеме пунктата костного
мозга взрослого. Особенностью новорожденных
детей является легкость возврата к
экстрамедуллярному кроветворению. В
онтогенезе происходит смена «пластов»
— клонов кроветворных клеток,
обусловливающая особенности системы
крови в различные периоды.
Лейкоцитарная
формула у новорожденных имеет особенности.
В первые дни жизни лейкоцитарная формула
сдвинута влево,
преобладают нейтрофилы,
функция которых у новорожденных снижена
за счет уменьшения активности опсонинов
плазмы. В первые сутки после рождения
относительное число лимфоцитов
составляет: Т-50%; В-35%; 0-15%. Изменения
выражаются в падении числа нейтрофилов
и увеличении количества Т- и В-лимфоцитов.
Абсолютное число нейтрофилов наибольшее
у новорожденных, на первом году жизни
их число уменьшается. На
5-й день жизни число нейтрофилов и
лимфоцитов сравнивается (так
называемый первый перекрест). Затем
происходит дальнейшее возрастание
числа лимфоцитов к 10-му дню.
Таким образом, лейкоцитарная формула
грудного ребенка характеризуется
относительно большим количеством
лимфоцитов и малым – нейтрофилов.
После
года вновь начинает увеличиваться число
нейтрофилов на
фоне снижения лимфоцитов. В возрасте
5 лет происходит второй
перекрест Е
лейкоцитарной формуле, когда число
нейтрофилов и лимфоцитов вновь становится
равным. В дальнейшем
продолжается нарастание числа нейтрофилов.
С 12-летнего возраста гемограмма ребенка
не отличается от таковой взрослого
человека. СОЭ в течение детства
существенно не меняется.
Особенностями
системы гемостаза к моменту рождения
является относительно низкая активность
витамин-К-зависимых факторов свертывания
(II; VII; IX; X). Активность их снижается до
3-го дня, что может быть причиной развития
геморрагической болезни
новорожденных, затем начинает
возрастать. Количество тромбоцитов
практически не отличается от такового
у взрослых, однако функциональная их
активность в первые дни жизни ниже.
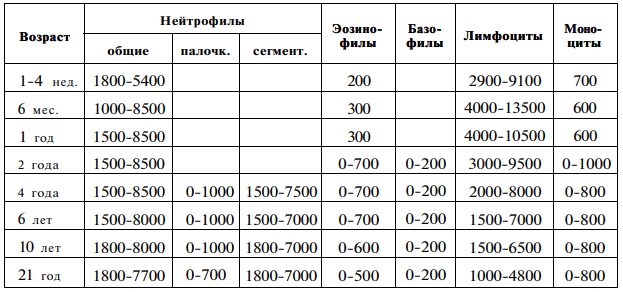
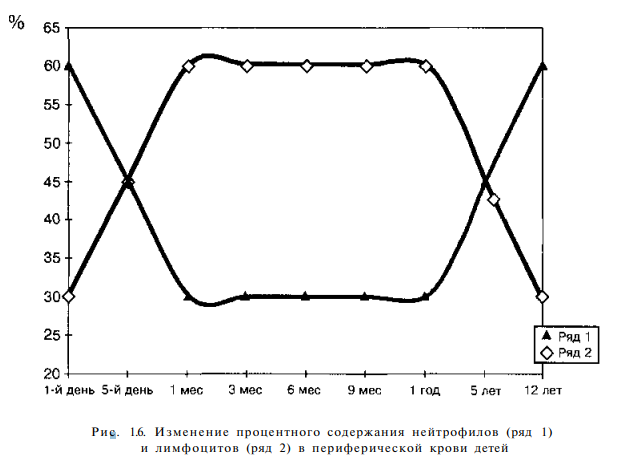 Примерно
у 5% здоровых доношенных детей в возрасте
около 2-3 месяцев жизни уровень гемоглобина
снижается до 95-100 г/л. При этом у детей
не находят никаких отклонений физического
и психомоторного развития, погрешностей
в диете, данных за железо- или
витаминодефицитные состояния, аномалий
синтеза гемоглобина, латентные или
явные очаги инфекции. Типичным признаком
таких детей являются очень
активные прибавки массы тела. У
недоношенных детей такая анемия может
развиться в возрасте 3-6 недель и
уровень гемоглобина достигать 70-90 г/л
- ранняя анемия недоношенных. Генез
этой физиологической анемии младенцев
не ясен. Полагают, что в основе лежит, с
одной стороны, относительная недостаточность
синтеза эритропоэтинов, с другой —
«разведение» крови, укороченная
продолжительность жизни эритроцитов.
19.
Особенности иммунологической защиты
в детском возрасте.
У детей
отмечаются значительные особенности
иммуногенеза. Известно, что плод человека
получает антитела от матери через
плаценту, причем только IgG. Антитела,
представленные IgA и IgM, через плаценту
не проникают из-за большего размера их
молекул. Функциональная слабость
собственного лимфоидного аппарата,
пониженная активность комплемента,
низкий уровень пропердина, лизоцима и
антител способствуют генерализации
инфекций. В такой ситуации для ребенка
спасительным фактором является
материнское молоко. Естественный дефицит
собственных иммуноглобулинов
компенсируется иммуноглобулинами и
другими противоинфекционными факторами
молока матери.
В процессе роста
ребенка и развития его иммунной системы
выделяют “критические” периоды, которые
являются периодами
максимального риска развития неадекватных
или парадоксальных реакций иммунной
системы при встрече иммунной системы
ребенка с антигеном.
Примерно
у 5% здоровых доношенных детей в возрасте
около 2-3 месяцев жизни уровень гемоглобина
снижается до 95-100 г/л. При этом у детей
не находят никаких отклонений физического
и психомоторного развития, погрешностей
в диете, данных за железо- или
витаминодефицитные состояния, аномалий
синтеза гемоглобина, латентные или
явные очаги инфекции. Типичным признаком
таких детей являются очень
активные прибавки массы тела. У
недоношенных детей такая анемия может
развиться в возрасте 3-6 недель и
уровень гемоглобина достигать 70-90 г/л
- ранняя анемия недоношенных. Генез
этой физиологической анемии младенцев
не ясен. Полагают, что в основе лежит, с
одной стороны, относительная недостаточность
синтеза эритропоэтинов, с другой —
«разведение» крови, укороченная
продолжительность жизни эритроцитов.
19.
Особенности иммунологической защиты
в детском возрасте.
У детей
отмечаются значительные особенности
иммуногенеза. Известно, что плод человека
получает антитела от матери через
плаценту, причем только IgG. Антитела,
представленные IgA и IgM, через плаценту
не проникают из-за большего размера их
молекул. Функциональная слабость
собственного лимфоидного аппарата,
пониженная активность комплемента,
низкий уровень пропердина, лизоцима и
антител способствуют генерализации
инфекций. В такой ситуации для ребенка
спасительным фактором является
материнское молоко. Естественный дефицит
собственных иммуноглобулинов
компенсируется иммуноглобулинами и
другими противоинфекционными факторами
молока матери.
В процессе роста
ребенка и развития его иммунной системы
выделяют “критические” периоды, которые
являются периодами
максимального риска развития неадекватных
или парадоксальных реакций иммунной
системы при встрече иммунной системы
ребенка с антигеном.
Первый критический период - это период новорожденности (до 29 дней жизни). В этот период постнатальной адаптации становление иммунной системы только начинается. Организм ребенка защищен почти исключительно материнскими антителами, полученными через плаценту и с грудным молоком. Чувствительность новорожденного ребенка к бактериальным и вирусным инфекциям в этот период очень высока. Второй критический период (4 - 6 мес.жизни) характеризуется утратой пассивного иммунитета, полученного от матери, в связи с катаболизмом в организме ребенка материнских антител. Способность к формированию собственного активного иммунитета у ребенка развивается постепенно и в этот период ограничивается преимущественным синтезом иммуноглобулинов M - антител без формирования иммунологической памяти. Недостаточность местной защиты слизистых связана с более поздним накоплением секреторного иммуноглобулина A. В связи с этим чувствительность ребенка ко многим воздушно-капельным и кишечным инфекциям в этот период очень высока. Третий критический период ( 2-й год жизни), когда значительно расширяются контакты ребенка с внешним миром и с возбудителями инфекций. Иммунный ответ ребенка на инфекционные антигены остается неполноценным: преобладает синтез иммуноглобулинов M, а синтез иммуноглобулинов G страдает недостаточностью продукции одного из наиболее важных для антибактериальной защиты субкласса G2. Местная защита слизистых все еще остается несовершенной из-за низкого уровня секреторного IgA. Чувствительность ребенка к респираторным и кишечным инфекциям все еще высока. Четвертый критический период ( 6 - 7-й годы жизни), когда в крови у ребенка уменьшается абсолютное и относительное количество лимфоцитов. В этот период уровни иммуноглобулинов М и G в крови ребенка приближаются к уровням взрослых, но уровень иммуноглобулина A все еще остается более низким, с чем связана слабая местная защита слизистых. Содержание иммуноглобулина E, напротив, достигает максимального уровня в сравнении с другими возрастными периодами, что отражает высокую степень риска паразитарных инвазий и аллергических реакций у ребенка данной возрастной группы. Иммунорегуляция к этому возрасту приобретает черты зрелости. Чувствительность детей этого возраста к инфекция все еще высока. Пятый критический период - подростковый возраст ( у девочек с 12 - 13 лет, у мальчиков с 14 - 15 лет), когда пубертатный скачок роста сочетается с уменьшением массы лимфоидных органов, а начавшаяся секреция половых гормонов (в том числе, андрогенов) служит причиной угнетения клеточных механизмов иммунитета. В этом возрасте резко возрастают внешние, часто неблагоприятные, воздействия на иммунную систему. Дети этого возраста характеризуются высокой чувствительностью к вирусным инфекциям. Клеточный иммунитет: Содержание зрелых Т-лимфоцитов в крови снижено: 45 – 53% ( у взрослых 72 – 74%) Физиологический лимфоцитоз в периферической крови Выработка ИЛ1 и ИЛ2 не нарушена Продукция α–интерферона не нарушена Синтез γ–интерферона, осуществляющего противовирусную защиту снижен в 30 раз (составляет 13 ед/мл, у взрослых 446 ед/мл), нормализуется только к 3 летнему возрасту Характерны незавершенный фагоцитоз. Гуморальный иммунитет: В-лимфоциты синтезируют только IgМ IgG новорожденного – пассивно приобретенный Синтез В-лимфоцитами – IgM достигает значений взрослого человека к 1 году IgG – к 5-6 годам IgA – к 10 годам недостаточность гуморального иммунитета обусловлена: Незрелостью В-лимфоцитов, Т-хелперов Наличием функционирующих Т-супрессоров. Селезенка-место разруш стареющих эритроцитов и тромбоцитов. В ней происходит частичный синтез иммуноглоб и антител. Лимф узлы форм со 2-го месяца внутриутр развития: вначале шейно-подключ, легочные, ретроперитонеал, паховые. При рождении в крови ребенка преобладают нейтрофилы, часто со сдвигом лейкоцитарной формулы влево до миелоцитов. К концу первой недели жизни происходит выравнивание количества нейтрофилов и лимфоцитов - так называемый “первый перекрест” - с последующим нарастанием количества лимфоцитов, которые в последующие 4 - 5 лет жизни остаются преобладающими клетками среди лейкоцитов крови ребенка. “Второй перекрест” происходит у ребенка в возрасте 6 - 7 лет, когда уменьшается абсолютное и относительное количество лимфоцитов и лейкоцитарная формула приобретает вид, характерный для взрослых. Гранулоциты новорожденных отличаются пониженной функциональной активностью, недостаточной бактерицидностью. Функциональная недостаточность нейтрофилов новорожденных детей в какой-то степени компенсируется большим количеством этих клеток в крови. К тому же гранулоциты новорожденных и детей первого года жизни отличаются от гранулоцитов взрослых более высоким уровнем рецепторов для IgG, необходимых для опосредованного специфическими антителами очищения организма от бактерий. Абсолютное количество моноцитов крови у новорожденных выше, чем у детей более старшего возраста, но они отличаются низкой бактерицидной активностью и недостаточной миграционной способностъю. Защитная роль фагоцитоза у новорожденных детей лимитируется недоразвитием системы комплемента, которая необходима для усиления фагоцитоза. Моноциты новорожденных отличаются от моноцтов взрослых более высокой чувствительностью к активирующему действию гамма-интерферона, чем компенсируется их исходная низкая функциональная активность, т.к. гамма-интерферон активирует все защитные функции моноцитов, способствуя их дифференцировке в макрофаги. Содержание лизоцима в сыворотке новорожденного превосходит уровень материнской крови уже при рождении, уровень этот нарастает в течение первых дней жизни, а к 7 - 8-ому дню жизни несколько снижается и достигает уровня взрослых людей. Лизоцим является одним из факторов, обеспечивающих бактерицидность крови новорожденных. В слезной жидкости новорожденных содержание лизоцима ниже, чем у взрослых, с чем связана повышенная частота конъюнктивитов у новорожденных. Как видно из выше сказанного, у новорожденных детей резко ослаблены все основные механизмы неспецифической защиты организма от патогенных бактерий и вирусов, чем объясняется высокая чувствительность новорожденных и детей первого года жизни к бактериальным и вирусным инфекциям. После рождения иммунная система ребенка получает сильнейший стимул быстрого развития в виде потока чужеродных (микробных) антигенов, поступающих в организм ребенка через кожу, слизистые дыхательных путей, желудочно-кишечного тракта, активно заселяемые микрофлорой в первые часы после рождения. Быстрое развитие иммунной системы проявляется увеличением массы лимфатических узлов, которые заселяются Т- и В-лимфоцитами. После рождения ребенка абсолютное количество лимфоцитов в крови резко повышается уже на 1-й неделе жизни (первый перекрест в формуле белой крови). Физиологический возрастной лимфоцитоз сохраняется на протяжении 5 - 6 лет жизни и может рассматриваться как компенсаторный. Функциональная активность Т-лимфоцитов новорожденных имеет свои особенности: высокая пролиферативная активность клеток сочетается с пониженной способностью Т-лимфоцитов реагировать пролиферацией на контакт с антигенами. Особеннм остью Т-лимфоцитов новорожденных является присутствие в их крови около 25% клеток, несущих признаки ранних стадий внутритимической дифференцировки Т-клеток. Это свидетельствует о выходе в кровоток недозрелых тимоцитов. Лимфоциты новорожденного обладают повышенной чувствительностью к действию интерлейкина-4, чем предопределено преобладание у них дифференцировки Th2. У новорожденного тимус полностью сформировани в течение первого года жизни достигает максимальных размеров. Из тимуса в кровоток и в лимфоидные органы поступают только такие Т-лимфоциты, которые несут рецепторы, способные распознавать чужеродные антигены в комплексе с собственными антигенами гистосовместимости. Такие зрелые Т-лимфоциты отвечают на распознавание антигена пролиферацией, дифференцировкой и активацией защитных функций в ходе специфического иммунного ответа. Быстрое нарастание массы тимуса в первые 3 месяца жизни продолжается более медленными темпами вплоть до 6 - летнего возраста, после чего масса тимуса начинает снижаться. В течение первых трех лет жизни проводится плановая вакцинация детей против всех наиболее опасных и частых инфекционных заболеваний: туберкулеза, поломиелита, дифтерии, столбняка, коклюша, кори. 20.Признаки нормотрофии. О дистрофии можно говорить в случае, если статус ребенка не соответствует понятию нормотрофии. Классики отечественной педиатрии М. С. Маслов, Г. Н. Сперанский, А. Ф. Тур при описании нормотрофи и (эйтрофии) отмечали следующие характеристики ребенка: 1) чистая, розовая, бархатистая кожа без признаков гиповитаминозов; 2) нормальная толщина подкожного жирового слоя, хороший тургор тканей и тонус мышц; 3) соответственное возрасту развитие скелета и отсутствие признаков рахита; 4) соответствующее возрасту психомоторное развитие, положительный психоэмоциональный тонус; 5) хороший аппетит и нормальная работа всех органов; 6) хорошая сопротивляемость к инфекции и редкие, нетяжело протекающие инфекционные заболевания и процессы; 7) масса и длина тела, индексы физического развития отличаются от нормы не более чем на 5%. 8) Правильное нервно-психическое развитие, статические функции, развитие условных рефлексов, речи, психики, спокойный глубокий сон, живое выражение глаз, хорошее настроение. 21.Причины и профилактика рождения недоношенных детей. Анатомо-физиологические особенности недоношенного ребенка. ПРИЧИНЫ. Социально-биологические факторы: 1. Возраст первородящий женщины до 18 лет и старше 35 лет (в некоторых источниках – 30 лет); 2. Возраст отца моложе 18 и старше 50 лет (в некоторых источниках – 40 лет); 3. Особенности конституции женщины: низкорослость (рост менее 150 см) и масса на 25% выше или ниже нормы, субтильность; 4. Состояние психического здоровья женщины во время беременности. Сидоровым А.Е. (2003) было установлено, что у женщин с пограничными психическими нарушениями угроза преждевременных родов отмечается в 3,3 раза чаще. Клинические (медицинские) факторы: 1. Акушерско-гинекологический анамнез (характер менструального цикла, исходы предыдущих беременностей и родов, гинекологические заболевания, пороки развития матки, малый промежуток между родами); 2. Экстрагенитальные заболевания (острые инфекции во время беременности, пороки сердца, гипертоническая болезнь, заболевания почек, сахарный диабет). 3. Осложнения настоящей беременности (тяжелые опг-гестозы, резус-сенсибилизация, антифосфолипидный синдром, многоводие, многоплодие, предлежание плаценты). 4. Эндокринные нарушения (гиперандрогения надпочечникового и яичникового генеза, нарушение функции щитовидной и поджелудочной желез). Социально-экономические факторы: 1. Отсутствие или недостаточность медицинской помощи; 2. Плохое питание беременной, наличие авитаминозов. 3. Неудовлетворительные жилищно-бытовые условия, низкий уровень материальной обеспеченности семьи; 4. Наличие у женщины и у мужчины профессиональных вредностей, вредных привычек (алкоголизм, токсикомания, курение, наркомания); 5.Неблагоприятная климатическая и экологическая среда обитания. Психосоциальные факторы: 1.Незапланированная беременность; 2.Нежеланная беременность; 3.Эмоциональная напряженность в семье: дисгармоничные отношения с супругом, близкими родственниками; 4.Наступление беременности в неблагоприятную стадию формирования супружеского холона (холон - нечто, одновременно являющееся и целым само по себе, и частью чего-то ещё) (вне брака, на стадиях конфронтации, экзистенциального личностного кризиса); 5.Течение беременности на фоне значительных повседневных перегрузок; ПРОФИЛАКТИКА ПРЕЖДЕВРЕМЕННЫХ РОДОВ 1. Первичная профилактика (вне беременности): • ограничение повторных внутриматочных манипуляций (выскабливание полости матки); • информирование общественности о повышенном риске преждевременного рождения детей, зачатых с помощью вспомогательных репродуктивных технологий. Ограничение количества переносимых эмбрионов в зависимости от возраста пациентки и прогноза. • Увеличить период между беременностями. Существует повышенная вероятность преждевременных родов при беременности сразу или в течение непродолжительного времени после родов. На самом деле, увеличение риска более чем в два раза отмечается для интервала менее 6 месяцев между беременностями. • Соблюдение режима отдыха и питья. Адекватный режим отдыха и достаточное количество жидкости способствуют хорошей циркуляции крови, кислорода, витаминов и питательных веществ для растущего плода. • Если имеется риск преждевременных родов, то во время критических сроков (2-3, 4-12 и 18-22 недели) рекомендуется обязательная госпитализация в роддом. В стационаре проводится профилактическая терапия, направленная на сохранение беременности. Степень зрелости недоношенных детей зависит от срока гестации и массы тела при рождении. Гестационный возраст (gestatio – беременность) – это возраст ребенка от зачатия до рождения. Он является самым важным показателем оценки степени зрелости новорожденного ребенка и его способности адаптироваться к условиям внешней среды. указывают срок беременности и соотношение массы со сроком, по центильным таблицам. Выделяют четыре степени недоношенности:
Степень недоношенности |
Гестационный возраст |
Масса тела |
I степень |
37-35 недель |
2500-2000 г |
II степень |
34-32 недели |
2000-1500 г |
III степень |
31-29 недель |
1500-1000 г |
IV степень |
28-22 недели |
Менее 1000 г |
Недоношенность состояние новорожденного родившегося со сроком гестации меньше 37 недель, с массой тела менее 2500г и длиной тела менее 45 см, длинные пушковые волосы на лице, спине; мягкость ушной раковины; ногтевые пластинки не закрывают полностью ногтевое ложе; нарушение опущения яичек в мошонку у мальчиков и зияние половой щели у девочек; относительная мягкость костей черепа; отсутствует ядро окостенения в нижнем эпифизе бедренной кости, слабо выраженный подкожный жировой слой; расположение пупка в нижней трети средней линии живота; голова относительно большая (третья часть длины тела), слабо выражены околососковые кружки. Морфологические признаки недоношенности. Для недоношенных детей характерно непропорциональное телосложение: относительно большие голова и туловище, короткие шея и ноги, низкое расположение пупка. Вертикальный размер головы составляет 1/3 от длины тела. Отмечается преобладание мозгового черепа над лицевым, кости черепа податливы, широко раскрыты швы и роднички. У глубоконедоношенных новорожденных с очень низкой и экстремально низкой массой тела наблюдается выраженная гиперемия кожного покрова. Типично обильное лануго (пушковые волосы) не только на плечиках и спинке (как у доношенного ребенка), но и на щеках, бедрах и ягодицах. У детей, родившихся в сроке менее 35 недель беременности, ногти не достигают кончиков пальцев. Вследствие недоразвития хрящевой ткани ушные раковины у недоношенных детей мягкие. Функциональные особенности недоношенного ребенка заключаются в сонливости (неохотно открывают глаза), вялости, слабом крике, отсутствии или снижении сосательного рефлекса, снижении мышечного тонуса (именно поэтому для них типична «поза лягушки»), а также в несовершенстве терморегуляции. Недоношенные дети легко переохлаждаются и перегреваются. Головной мозг: сглаженность борозд, слабая дифференцировка серого и белого вещества. Незрелость коры обуславливает преобладание подкорковой деятельности: движения хаотичны, вздрагивания, тремор рук, клонус стоп. Вследствие незрелости терморегуляторных механизмов легкое охлаждение ( сниженная теплопродукция и повышенная теплоотдача), отсутствует адекватное повышение температуры тела на инфекционные процессы и легкое перегревание. Перегреванию способствует недоразвитие потовых желез. Дыхание недоношенного ребенка отличается большей частотой и лабильностью: оно бывает поверхностным, неравномерным по глубине, у глубоко недоношенных детей наблюдаются эпизоды апноэ (остановки дыхания на 10 с и более). Частота дыханий от 36 до 62 в мин. У недоношенных детей часто возникают гемодинамические нарушения, поскольку замедлена перестройка кровообращения (поздно закрываются артериальный проток и овальное окно) и повышена вязкость крови. Преобладает тонус симпатического отдела нервной системы, поэтому любые раздражители вызывают учащение сердцебиений и повышение артериального давления. ЧСС в периоде новорожденности составляет 140-160, а при беспокойстве может достигать 200-220 ударов в мин. Со стороны почек отмечается низкая клубочковая фильтрация, почти полная реабсорбция ионов натрия, снижение концентрационной и секреторной функции. Для недоношенных детей типична лабильность вводно-электролитного баланса. Гипонатриемия, гипоальбуминемия и низкий диурез вызывают склонность к отекам. Максимальная убыль в массе у недоношенных детей составляет 9-14%, а восстановление первоначальной массы тела происходит ко второй – третьей неделе жизни. Пищеварительная система отличается малым объемом желудка, слабостью кардиального сфинктера, наклонностью к частым срыгиваниям, низкой протеолитической активностью желудочного сока, ферментов поджелудочной железы и кишечника. Транзиторная гипербилирубинемия у недоношенных новорожденных наблюдается значительно чаще и продолжительнее, чем у детей, родившихся в срок. Из-за незрелости мозговых структур высок риск возникновения ядерной желтухи при относительно низкой концентрации билирубина (170 мкмоль/л). Склонность к инфекционным заболеваниям обусловлена такими особенностями иммунитета, как снижение функциональной активности Т-лимфоцитов, уровня лизоцима и β-лизинов, титра пропердина и комплимента. Проявления гормонального криза у глубоко недоношенных детей практически не отмечаются. Следует иметь в виду, что для недоношенного ребенка, во всяком случае на первом году жизни, характерны несколько иные, чем для доношенного, закономерности физического развития. Пуповинный остаток отпадает позже, чем у доношенных, пупочная ранка заживает к 12-15-му дню, при массе менее 1000 грамм – на 1-2 недели позже. Допустимая физиологическая убыль массы тела после рождения у недоношенных детей следующая: для детей с массой тела при рождении более 1500 г - 7-9%, для недоношенных с массой тела от 1500 до 1000 г - 10—12% и, наконец, у экстремально маловесных новорожденных первоначальная убыль массы тела может достигать 14—15%. Дальнейшее нарастание у недоношенного ребенка массы тела после физиологической убыли зависит от течения постнатального периода. Если ребенок здоров и ему обеспечены адекватный уход и питание, то удвоение массы тела происходит в возрасте от 2,5 до 3,5 месяцев, в случае заболеваний — позже. Месячные прибавки у здоровых недоношенных детей на первом году жизни зависят от степени недоношенности. Если в первый месяц жизни они ниже, чем у доношенных детей, то затем их интенсивность значительно возрастает. Нормальные прибавки за 1 месяц 1 степени- 300-40г, 2 степени – 450-675г, 3 степени – 600-900, также и на 2 месяце. На 3 месяце 800г, на 4 месяце 750, на 5- 700. РОСТ. У детей с массой менее 1000г в первые 6 месяцев 2,5-5,5 см в месяц, во 2 полугодии 0,5-3 см. За первый год длина увеличивается на 26,6-38 мс. Быстрее растут глубоконедоношенные, их рос к году 70,2-77,5 см. Прирост ГОЛОВЫ в первые 3 месяца 0,07-0,13 см (измерение каждые 5 дней). В 1 полугодии 3- 2,1 см, во втором 1- 0,5 см за месяц. К концу 1 года увеличивается на 15-19 и достигает 44,5-46,5 см. Перекрест окружностей голов и груди между 3 и 5 месяцами. 22.Критерии определения недоношенности. Этапное выхаживание. Недоношенными считаются дети, родившиеся в период с 22-й по 37 -ю неделю беременности с массой тела менее 2500-2700 г и длиной те-менее 45—47 см. Выделяют четыре степени недоношенности:
Степень недоношенности |
Гестационный возраст |
Масса тела |
I степень |
37-35 недель |
2500-2000 г |
II степень |
34-32 недели |
2000-1500 г |
III степень |
31-29 недель |
1500-1000 г |
IV степень |
28-22 недели |
Менее 1000 г |
Недоношенность состояние новорожденного родившегося со сроком гестации меньше 37 недель, с массой тела менее 2500г и длиной тела менее 45 см, длинные пушковые волосы на лице, спине; мягкость ушной раковины; ногтевые пластинки не закрывают полностью ногтевое ложе; нарушение опущения яичек в мошонку у мальчиков и зияние половой щели у девочек; относительная мягкость костей черепа; отсутствует ядро окостенения в нижнем эпифизе бедренной кости, слабо выраженный подкожный жировой слой; расположение пупка в нижней трети средней линии живота; голова относительно большая (третья часть длины тела), слабо выражены околососковые кружки. Морфологические признаки недоношенности. Для недоношенных детей характерно непропорциональное телосложение: относительно большие голова и туловище, короткие шея и ноги, низкое расположение пупка. Вертикальный размер головы составляет 1/3 от длины тела. Отмечается преобладание мозгового черепа над лицевым, кости черепа податливы, широко раскрыты швы и роднички. У глубоконедоношенных новорожденных с очень низкой и экстремально низкой массой тела наблюдается выраженная гиперемия кожного покрова. Типично обильное лануго (пушковые волосы) не только на плечиках и спинке (как у доношенного ребенка), но и на щеках, бедрах и ягодицах. У детей, родившихся в сроке менее 35 недель беременности, ногти не достигают кончиков пальцев. Вследствие недоразвития хрящевой ткани ушные раковины у недоношенных детей мягкие. К неврологическим признакам недоношенности относят мышечную гипотонию, снижение физиологических рефлексов, двигательной активности, нарушение терморегуляции, слабый крик. Глубоконедоношенный ребенок (III-- IV степень) при рождении лежит с вытянутыми руками и ногами; сосательный, глотательный и другие безусловные рефлексы отсутствуют или слабо выражены. Температура тела непостоянная (может снижаться до 32--34° С и легко повышается). При рождении после 30-й недели гестации у недоношенного отмечается частичное сгибание в коленных и тазобедренных суставах; сосательный рефлекс хороший. У ребенка, родившегося на 36--38-й неделе беременности, сгибание конечностей полное, но неустойчивое; вызывается отчетливый хватательный рефлекс. Снижение двигательной активности, мышечного тонуса, рефлексов, непостоянный тремор, косоглазие, горизонтальный нистагм удерживаются у недоношенного на протяжении 2--3 нед жизни. Выхаживание недоношенных детей осуществляется в 2 этапа: в родильном доме и специализированном отделении. Затем ребенок поступает под наблюдение поликлиники. Сразу после рождения недоношенный ребенок должен быть принят в стерильные теплые пеленки ("оптимальный комфорт"). В первые дни и недели жизни глубоконедонош дети находятся в кувезах. В родильном зале недоношенных немедленно и бережно обсушивают теплыми пеленками и сразу помещают в инкубатор для предупреждения потери тепла и неощутимых потерь воды с поверхности кожи. Детям, рожденным в состоянии гипоксии, в вену пуповины вводят смесь, включающую 10% раствор Глюкозы ( 7-8 мл/ кг), кокарбоксилазу (0,5 – 1 мл), 5% раствор аскорбиновой кислоты ( 0,5 – 1 мл), 10% раствор кальция глюконата(1 мл). При асфиксии или выраженной гипоксии после отсасывания содержимого из дыхательных путей производят ИВЛ с помощью маски или методом интубации. Одновременно в вену пуповины вводят указанную выше смесь с добавлением преднизолона (1 мг/ кг), этилимидазолдикарбоната метиламида (Этимизола, 1 мг/ кг) или 2,4 % раствора аминофиллина (Эуфиллина, 0,1 -0,15 мл). При отсутствии видимого эффекта ребенка переводят в реанимационный блок. Температурная реакция сразу после рождения может быть продолжением того состояния, которое ребенок перенес в родах. Предупреждение холодового стресса в группе маловесных детей имеет жизненное значение. Все манипуляции в родильном зале выполняют в условиях, исключающих охлаждение ребенка. При тяжелой асфиксии температурный контроль отключается, и температура тела часто не поддерживается на должном уровне. Реанимационные процедуры должны проводиться с особым вниманием к тепловому контролю. Применяют утепленные пеленальные столики с электроподогревом, реанимационные кровати. После перевязки и обработки пуповины детей с массой тела при рождении 1500 грамм и ниже и резко выраженными нарушениями терморегуляции помещают в закрытый кувез с температурой окружающего воздуха 32-34 градусов. Детей с легкой степенью недоношенности разрешается приложить к телу матери через 10-20 минут после родов. Температура в кювезе регулируется с учетом температуры тела ребенка ( при измерении в прямой кишке она должна быть 36.6 – 37.1 градус). В кювез подается кислород из расчета 2 л/ минуту. Открытый кувез или кровать используются для детей с массой тела более 1500 грамм при рождении или достигших такой массы тела. Длительность пребывания здорового недоношенного ребенка в закрытом кувезе в случае массы при рождении более 1200 грамм обычно ограничивается 2-4 днями. В случае меньшей массы тела при рождении она может составлять от 7-8 дней до нескольких недель, причем чем длительнее пребывание ребенка в кувезе, тем больше вероятность его инфицирования. Предупреждение инфицирования достигается регулярной (каждые три дня) заменой кувеза и тщательной его обработкой. В условиях закрытого кувеза в первые дни влажность воздуха высокая – в пределах 90-95%, через 2-3 дня она может быть снижена и на 2-й неделе достигает 50-60%. Оптимальная температура воздуха в помещении должна составлять около 25°С. Проводятся оксигенотерапия, коррекция кислотно-основного равновесия путем введения раствора глюкозы с аскорбиновой кислотой и кокарбоксилазой. Ликвидация гипогликемии, гипопротеинемии обеспечивается с помощью растворов глюкозы и альбумина. При острой необходимости проводят переливание плазмы и гемотрансфузии. Большинство детей с недоношенностью ill—IV степени получают антибиотики. Показанием к их назначению служат тяжелое общее состояние ребенка, гнойно-воспалительные заболевания у матери, преждевременное излитие околоплодных вод, роды вне медицинского учреждения. Здоровый недоношенный, способный поддерживать нормальную температуру тела без дополнительного обогрева, регулярно прибавляющий массу тела и при ее достижении 2000 грамм, может быть выписан домой в случае хорошей эпителизации пупочной ранки, нормальных показателях гемограммы и наличии справки из туберкулезного диспансера о возможности выписки по данному адресу новорожденного, невакцинированного против туберкулеза. Чаще выписка производится не ранее 8-10 суток жизни. Здоровые недоношенные, не достигшие в первые две недели массы 2000 грамм, и больные дети, независимо от массы тела, переводятся на второй этап выхаживания. Проводят профилактику рахита и анемии. В комплекс лечебных мероприятий входят массаж и гимнастика. Детей выписывают домой при массе тела более 2000 г, ее положительной динамике и хорошем сосательном рефлексе. Перевод недоношенного ребенка в зависимости от его состояния осуществляется специализированной бригадой скорой медицинской помощи. Первые 3 суток после перевода из родильного дома ребенок адаптируется к новым условиям и требует особо бережного отношения. Все изменения режима по отношению к недоношенному ребенку следует вводить постепенно, под контролем его функционального состояния. Создание оптимального температурнго режима выхаживания (температура в детской палате, где выхаживаются недоношенные дети 24-260 С. Темератуа тела недоношенного новорожденного должна быть в пределах 36,4-37,00С. Методы выхаживания – кроватка грелка или кувез. В кувез помещаются дети родившиеся в асфиксии, с родовой травмой, с массой тела 2000гр. и менее, неспособные поддерживать собственную температуру тела, с отечным и аспирационным синдромами, при РДС II-III ст. и при тяжелых состояниях, обусловленных различной патолгией периода новорожденности). Обеспечение рационального вскармливания. Способы вскармливания: грудное, из рожка, через зонд (срыгивания, медленная прибавка в массе, РДС 5 баллов, при ИВЛ, в случае обширных врожденных дефектах твердого и мягкого неба, низкий или отсутствие сосательного и глотательного рефлексов), парентеральное (рвота, плоская или отрицательная весовая кривая, парез кишечника, если остаточный объем пищи перед кормлением составляет более 1 мл/кг, при хирургической патологии ЖКТ и др.). Идеальной пищей для недоношенных детей является грудное молоко. Естественное вскармливание обеспечивает максимальный успех в выхаживании этих детей. Женское молоко способствует преобладанию в кишечнике грудных детей бифидобактерий, препятствующих росту гнилостной флоры кишечника, и содержит вещества, способствующие становлению у новорожденного физиологического иммунитета. Так же при преждевременных родах грудное молоко имеет отличительные питательные и энергетические свойства от молока женщины при срочных родах. Оно содержит большее количество белка, углеводов, витаминов А, Е,С, микроэлементов, полиненасыщенных жирных кислот, которые необходимы для роста и развития организма недоношенного ребенка,и в первую очередь ЦНС, чем у женщин, родивших в срок. Срок 1-го кормления зависит от состояния ребенка, степени недоношенности, чаще оно бывает через 6-9 часов, если ребенок родился в сроки от 32 до 37 недель, и через 12-36 часов- если он родился в срок менее 32 недель. Если ребенок родился менее 32 недель, то ему вводят парентерально 10% раствор Глюкозы. Детей массой тела более 1800 грамм можно прикладывать к груди, детей массой тела менее 1800 грамм кормят через соску, а при отсутствии сосательного и глотательного рефлексов - через зонд. Во время кормления грудью следует помочь ребенку найти правильное положение и предупредить мать, что молоко не должно оставаться в ротовой полости новорожденного из- за опасности аспирации. Физиологическая кратность кормления недоношенных детей 7-8 раз, глубоконедоношенных (3 и 4 степени)- до 10 раз в сутки. Количество молока, необходимое для кормления в первые 10 дней жизни, вычисляют по формуле: 10 ккал* масса тела (кг) х сутки жизни. В дальнейшем для определения количества молока, необходимого недоношенному ребенку, используют так же калорийный расчет. Энергетическая ценность пищи составляет к 10-14-му дню жизни 100-120 ккал/ кг в сутки. К концу 1-го месяца жизни недоношенные дети должны ежедневно получать 135-140 ккал/ кг. Недоношенный ребенок должен ежесуточно получать на 1 килограмм массы тела белка до 2 недель жизни 2-2,5 грамм, до 1 месяца – 2,5 – 3 грамма. Потребность в жире у недоношенных детей составляет 5-6 г/кг в сутки, в углеводах – 13-15 г/кг. Антропометрические измерения проводят в день поступления, а затем повторяют ежемесячно. Исключение представляют определение массы тела и окружности головы. Взвешивание детей проводят ежедневно. Окружность головы измеряют не реже 1 раза в неделю. Ежедневный туалет ребенка персонал проводит по тем же принципам, что и у доношенных новорожденных, - используются стерильные ватные шарики, стерильные пипетки, стерильные стеклянные палочки. Пеленание детей проводят перед каждым кормлением. Во время каждого пеленания проводится осмотр кожи младенца и стул, при появлении патологических изменений сразу сообщает об этом врачу. Для ухода за кожей целесообразно использовать детское масло на основе растительных и эфирных масел или вазелин. Соблюдается строгий санитарно-гигиенический режим. Пеленальные столы обрабатывают после пеленания детей 1% раствором Хлорамина Б двукратно в течение 15 минут. Влажная убора палат проводится 3 раза в день с использованием дезрастворов. 23.Структура перинатальной и младенческой смертности. Пути их снижения. Перинатальный период- период с 22 недель беременности до 8-го дня жизни после рождения (7 полных суток). (антенатальный, интранатальный, ранний неонатальный). Анте- с 22 недель внутриутробного до рождения. Интра- родовая деятельность. Неонатальный период – период жизни ребенка от момента рождения до достижения им 28 дней (7 сут). Перинатальная смертность- кол-во умерших плодов и новорожденных с 22 нед беременности до начала родовой деятельности, во время родов, в первые 7 суток неонатального периода. Младенческая смертность — смертность среди детей младше одного года;
Число мертворожденных + число умерших детей в первые 168 часов.
Перинатальная смертность = ------------------------------------------------------------- х 1000 смертности Число всех родившихся (живыми и мертвыми).
Число детей, умерших в первые168 часов. Ранняя неонатальная=------------------------------------------------------------- х 1000. Число родившихся живыми Число мертворожденных
Мертворождаемость= ----------------------------------------------------------------х 1000. Число родившихся детей ( живых+мертвых) Число умерших в текущем году детей до 1 года
Младенческая смертность = --------------------------------------------------------х1000%%. Число родившихся в текущем году
Причины:
К перинатальным факторам риска синдрома
внезапной смерти младенцев авторы
относят юный
возраст матери на
момент первой беременности, недоношенность
и низкую массу тела ребенка
при рождении, перенесенные жизнеугрожающие
состояния в
неонатальном периоде, наличие у ребенка
признаков
морфофункциональной незрелости,
а также дефекты
ухода
за ребенком .
Асфиксия;Врожденные
аномалии;Дыхательные
расстройства;Инфекционные заболевания;
Семейное
положение;Вредные
условия труда матери;Вредные
привычки (курение,
алкоголь);Сопутствующая экстрагенитальная
патология (заболевания кроме относящихся
к женским);Количество предыдущих
родов;
Врожденные аномалии,
внутриутробная гипоксия, асфиксия при
рождении, респираторные нарушения.
Профилактика.
–Планирование беременности. –Обследование
и лечение партнеров до беременности. –
Выделение групп риска по перинатальной
патологии. – Регулярное наблюдение
беременных. – Профилактика недонашивания
и перенашивания беременности.
Пути
снижения:
1.Улучшение санитарно-просветительной
работы среди женщин,
статуса и здоровья и особенно
репродуктивного здоровья 2.Совершенствование
антенатального ухода,
включая исследование признаков угрожающих
осложнений или преждевременных
родов. 3.Совершенствование
ухода во время беременности и
родов.4.Совершенствование
организации системы направления на
получение специализированной помощи
и для женщин, и для новорожденных
(региональный подход ухода).5.Улучшение
неонатального ухода.6.идентификация
женщин с риском акушерских осложнений
или очень
преждевременных родов и оказание
необходимого ухода (направление матери
в специализированное учреждение, когда
это необходимо) 7.активное
наблюдение и ведение родов,
раннее выявление осложнений процесса
родов и патологии плода 8.дружелюбная
обстановка во время родов,
содействие привязанности между матерью
и новорожденным 9.поддержание
температуры тела 10.инициация
спонтанного дыхания 11.начало
грудного вскармливания как можно раньше
после родов 12.профилактика
инфекций и их лечение.
24.Новорожденный
ребенок. Признаки доношенности.
Пограничные состояния.
Доношенный
плод при сроке беременности 37—41 неделя
имеет следующие средние размеры: длина
49-52 см (с колебаниями от 47 до 56 см и
более), массу 3200-3500 г (с колебаниями от
2500 г до 4000 г и выше). Длина плода - более
постоянная величина, чем масса тела,
поэтому она точнее отражает степень
зрелости плода.
Признаки:
крик
громкий, активные
движения, хорошо
выраженные мышечный тонус и
сосательный
рефлекс, кожа
розовая эластичная,
п/к-жировой слой хорошо развит,пушковый
покров не выражен,
длина волос на голове достигает 2 см;
кости
черепа эластичные,
боковые роднички
закрыты, ушные
раковины упругие,
пупочное
кольцо нах-ся посередине между
лобком и мечевидным отростком, ногти
заходят за кончики пальцев,
у девочек большие половые губы закр.
малые, у мальчиков яички опущены в
мошонку.
Пограничные
состояния
новорожденного ребенка это
парафизиологические состояния связанные
с адаптацией тела ребенка к окружающей
среде.
1.
Физиологическая убыль массы тела. Для
восполнения энергетических трат в
первые 3-5 дней после рождения организм
ребенка использует собственные
запасы специального высококалорийного
бурого жира,
который впоследствии заменяется на
«взрослый» белый жир. Это основная
причина
потери не более 10%
веса у всех детей.
Считается, что при достаточном количестве
молока у матери здоровый малыш должен
восстановить
свою первоначальную массу тела к 12
суткам.
2.
Транзиторная
гипотермия — в
первые 30 мин температура тела ребенка
снижается на 0,1–0,3 °С в минуту и достигает
около 35,5–35,8 °С, которая восстанавливается
к 5–6 ч жизни. Это обусловлено особенностями
компенсаторно-приспособительных реакций
ребенка. Температура в детской должна
быть от 20 до 22 градусов С (у недоношенных
23-24).
Пути потери тепла:
- излучение
(отдача тепла через стенки кувеза);
-
кондукция (контакт с холодной
поверхностью);
- конвенция (сквозняки);
-
испарение (через поверхность тела,
особенно если она влажная).
Транзиторная гипертермия. Несовершенство
процессов терморегуляции, активный
распад жировых клеток, недостаточное
поступление жидкости в первые дни после
рождения приводят к тому, что у многих
здоровых
новорожденных на 2-4 сутки жизни может
повышаться температура тела до 38,5
градусов.
Основная причина — обезвоживание,
перегревание, недопаивание, катаболическая
направленность обменных процессов.
3.
Физиологическая желтуха. Распад
большого количества плодного (фетального)
гемоглобина с
выделением в кровь свободного билирубина
на фоне низкой активности ферментов
незрелой печени ребенка вызывает
желтушное окрашивание кожи, склер и
слизистых оболочек. Более
выражена желтуха при позднем начале
кормления, при недостатке молока у
матери, а также у
недоношенных малышей. Сниженной
способностью к связыванию и транспортировке
НБ в кровяном
русле, вследствие гипоальбуминемии (1
г альбумина связывает 0,85 мг НБ).
замедленной экскрецией
конъюгированного билирубина из гепатоцита
вследствие узости желчных протоков.
4.
Транзиторная диспепсия. Только
что родившемуся младенцу необходимо
длительное время, чтобы наладились
процессы пищеварения, а ЖКТ заселился
полезными микроорганизмами.
Процесс становления нормальной
деятельности кишечника у всех детей
протекает с симптомами кишечных
расстройств,
считающихся в этом возрасте нормой.
Имеется определенная
стадийность в изменении окраски и
консистенции стула 1-2 дня – очень густой
дегтеобр меконий скудными порциями;
с 3-5 – 7 сутки –
жидкая, даже водянистая кашица, цвет
которой постепенно меняется с
темно-зеленого на желтый.
При этом частота
дефекаций может доходить до 10-15 в сутки
и сопровождаться
избыточным газообразованием и коликами;
со 2недели —
нормальный стул:
желтая
густая кашица без примеси зелени.
Могут быть белые комочки створоженного
молока в небольшом количестве.
5.
Половой криз. Обусловлен
влиянием на организм новорожденного
высокого
уровня материнских половых гормонов,
накапливающихся в его крови в последние
дни беременности и во время родов. Может
наблюдаться:нагрубание
(припухлость, уплотнение и увеличение)
молочных желез,
в некоторых случаях даже с выделением
капель молозива;выделение
из половой
щели у девочек густой слизи серовато-белого
цвета, а в небольшом
проценте случаев – с кровянистыми
прожилками;увеличение
мошонки, клитора, больших и малых половых
губ из-за их отека.
6.
Транзиторные изменения функции
почек. Небольшая
потеря белка с мочой в первые дни после
родов наблюдается у подавляющего
большинства младенцев и
считается проявлением становления
нормальной функции клубочков почек. А
об активизации
деятельности их канальцев
свидетельствует так называемый мочекислый
инфаркт: примерно
у каждого шестого ребенка хотя бы
однократно на пеленке после мочеиспускания
остается кирпично-красный
солевой остаток.
Время проявления — 1-я
неделя жизни. Это
состояние связано с нарушением обмена
веществ в почках и отложением в них
кристаллов солей мочевой кислоты.
7.
Физиологические проявления на коже:
Простая эритема —
реактивная краснота кожи, возникающая
после удаления первородной смазки или
первой ванны. На 2 сутки эритема более
яркая, к концу 1-й недели она исчезает,
у недоношенных детей она может сохраняться
до 2–3-х недель, а затем крупнопластинчатое
шелушение, захватывающее практически
все тело;
нежная
чувствительная кожица младенца реагирует
красными
пятнами токсической эритемы на аллергены,
химические и физические раздражители.
Элементы сыпи могут быть разного размера:
от точечных до сантиметра, не
зудят, а по краям могут иметь светло-желтый
ареол; Для
острого течения характерно появление
сыпи на 2–3 сутки жизни и исчезновение
ТЭ к 5–7 дню. При затяжном течении время
начала высыпаний вариабильно, от 1 суток
до 3–4 дня жизни. Сыпь может сохраняться
до 14 и более дней.
на
лице часто можно увидеть белые
пузырьки размером с булавочную головку
– милиа.
Преимущественно они локализуются на
спинке и крыльях носа, на подбородке и
переносице. Значительно реже отдельные
элементы можно заметить на других
участках тела. Это сигнал о начале
деятельности сальных желез;
8.
Преходящая неврологическая
симптоматика. Сдавление
головы во время родов
вызывает небольшой отек мозга, а обилие
информации, поступающей от всех
чувствительных рецепторов, обуславливает
сбой в равновесии процессов возбуждения
и торможения нервной системы. Поэтому
часто
наблюдается вздрагивание, мелкое
дрожание подбородка при плаче,
непостоянство мышечного тонуса и
рефлексов, раздраженные и даже болезненные
нотки в крике.
25.Работа
педиатра на участке. Диспансерное
наблюдение здоровых детей первого года
жизни.
Ведущей
фигурой в организации внебольничной
помощи детям является участковый
врач-педиатр детской городской
поликлиники. Он осуществляет динамическое
наблюдение за
состоянием здоровья,
физическим и нервно-психическим
развитием детей;
занимается профилактикой
заболеваний и травматизма
среди детей; обеспечивает своевременную
и качественную диагностику
с целью выявления преморбидных
состояний и ранних форм заболеваний;
лечение больных детей в поликлинике и
на дому; отбор детей, нуждающихся
в лечении у врачей «узких» специальностей,
госпитализации, санаторно-курортном
лечении; проводит
профилактическую и лечебную работу в
детских организованных коллективах.
Вся деятельность
участкового врача-педиатра строится в
соответствии с задачами детской
поликлиники в четырех основных
направлениях:
—
профилактическая
работа;
—
лечебная
работа;
—
противоэпидемическая
работа;
—
лечебно-профилактическая работа в
детских организованных коллективах.
Участковым
педиатром и медсестрой
поликлиники должны быть
проведены не менее двух дородовых
патронажей. В
ходе дородовых патронажей проводится
сбор и оценка данных генеалогического,
биологического и социального анамнеза.
Проводится выявление групп риска и
направленности риска. Даются рекомендации
по режиму и питанию беременной,
социально-гигиеническим условиям жизни,
профилактике пограничных состояний и
заболеваний, уходу за новорожденным и
его вскармливанию.
Первый
дородовый патронаж проводится после
поступления
сведений о беременной из женской
консультации,
второй — обычно на 3
1-32 неделях
беременности участковой медсестрой
детской поликлиники. Наряду с сестринскими
патронажами при необходимости
осуществляется и врачебный
патронаж к беременной с целью
наблюдения женщин групп риска.
В случае отягощенного акушерского
анамнеза, неблагополучного протекания
беременности участковый педиатр проводит
третий дородовый патронаж, непосредственно
перед родами.
Врач
проводит тщательный осмотр ребенка,
определяет его нервно-психическое и
физическое развитие, наличие отклонений
в состоянии здоровья, определяет группу
здоровья на
основании комплексной оценки данных.
После этого даются обоснованные
рекомендации по режиму,
питанию и уходу за ребенком,
режиму и питанию кормящей матери.
В
соответствии с этим выделены группы
здоровья:
I
критерий обуславливает здоровье, II–VI
критерии характеризуют здоровье.
Первая
(I) группа здоровья
объединяет детей, не имеющих отклонений
по всем избранным для оценки критериям
здоровья, не болевших или редко болевших
за период наблюдения, имеющих отставание
в нервно–психическом развитии не более
чем на 1 эпикризный срок, а также детей,
имеющих единичные морфологические
отклонения (аномалии ногтей, деформация
ушной раковины и др.), не влияющие на
состояние здоровья ребенка и не требующие
коррекции.
II–A
“угрожаемые дети”,
имеющие отягощенный биологический,
генеалогический или социальный анамнез,
но не имеющие отклонений по всем остальным
критериям здоровья.
II–Б
группа “риска” –
дети, имеющие некоторые функциональные
и морфологические изменения, часто
болеющие дети (4 и более раз в год), дети
с аномалиями конституции и другими
отклонениями в состоянии здоровья.
Третья
(III) группа здоровья
объединяет больных детей с наличием
хронических болезней или врожденной
патологии в состоянии компенсации, т.е.
с редкими, нетяжелыми по характеру
течения обострениями хронического
заболевания без выраженного нарушения
общего самочувствия и поведения, редкими
интеркуррентными заболеваниями, наличием
функциональных отклонений только одной,
патологически измененной системы или
органа (без клинических проявлений
функциональных отклонений других
органов и систем).
Четвертая
(IV) группа включает
в себя детей с хроническими болезнями,
врожденными пороками развития в состоянии
субкомпенсации, которое определяется
наличием функциональных отклонений не
только патологически измененного
органа, системы, но и других органов и
систем, с частыми обострениями основного
заболевания с нарушением общего состояния
и самочувствия после обострения, с
затяжными реконвалесцентными периодами
после интеркуррентного заболевания.
Пятая
(V) группа – дети
с тяжелыми хроническими заболеваниями,
тяжелыми врожденными пороками развития
в состоянии декомпенсации, т.е. угрожаемые
по инвалидности или инвалиды.
Согласно
существующему положению, врач-педиатр
и медицинская сестра детской поликлиники
посещают новорожденного
в первые 3 дня после выписки
из родильного дома. Если в семье родился
первый ребенок, двойня или у матери нет
молока, патронажное посещение рекомендуется
сделать в первый же день после выписки.
В дальнейшем участковая медсестра
посещает ребенка на дому через 1 —2 дня
в течение первой недели и еженедельно
- в течение первого месяца жизни. (мс
каждую неделю).
Второй врачебный
патронаж на 14-й день жизни.
Третий
врачебный патронаж (по приказу - второй)
на 21-й день жизни.
От
28-ого дня жизни до 1 месяца первое
посещение здоровым ребенком поликлиники.
На
втором месяце жизни здоровый ребенок
дважды посещает
поликлинику - в 1,5 и 2 месяца.
Если
ребенок здоров, то со второго месяца
жизни до года он посещает поликлинику
ежемесячно
(±5 дней относительно даты рождения).
Текущие
эпикризы пишутся в 1, 3, 6, 9 и 12 месяцев.
Патронаж
медицинской сестры.
На
первой неделе жизни - совместный первый
врачебно-сестринский патронаж, далее
активно, через один - два дня.
На первом
месяце жизни - еженедельно (всего 5-6
посещений в течение первого месяца
жизни).
Примечания.
а)
с 7 лет ежегодно измеряется
артериальное давление;
б)
с 13 лет - флюорография;
в) с 8 класса -
определение группы крови и Rh.
г) с 1
года до 2 лет включительно здоровый
ребенок осматривается участковым
педиатром ежеквартально;
с 2 до 3 лет - один
раз в полгода;
старше 3 лет - один раз в год.
Врач-педиатр
разрабатывает комплекс лечебно-оздоровительных
мероприятий, обеспечивает
контроль за выполнением режима,
за рациональным
питанием,
своевременным проведением мероприятий
по профилактике
у детей алиментарных расстройств,
рахита, анемии и
других заболеваний.
Педиатр обеспечивает иммунопрофилактику
детей, направляет
их на консультации
к врачам-специалистам,
проводит динамическое наблюдение за
детьми с хронической патологией,
состоящими на диспансерном наблюдении,
обеспечивает подготовку
к поступлению в образовательные
учреждения,
осуществляет работу по охране
репродуктивного здоровья подростков.
На педиатра возложены и обязанности по
дополнительному
лекарственному обеспечению детей,
имеющих право на получение набора
социальных услуг. Участковый детский
врач выдает заключения о
необходимости направления детей в
санаторно-курортные учреждения,
проводит мероприятия по профилактике
и раннему
выявлению у детей гепатитов B и C,
ВИЧ-инфекции, наблюдает
детей с наследственными заболеваниями,
выявленными в результате неонатального
скрининга, и патронаж семей, имеющих
детей указанной категории.
В возрасте
3,6,9, 12 месяцев (декретированные возраста)
участковый врач на основании тщательного
осмотра ребенка, антропометрических
измерений, беседы с матерью составляет
подробный эпикриз,
в котором дает оценку состояния
здоровья ребенка,
его физического и
нервно-психического
развития в динамике, а также составляет
план наблюдения и
оздоровительных мероприятий,
если в этом есть необходимость, на
последующий 1 период.
Диспансерное
наблюдение за здоровыми детьми первого
года жизни
Осмотр:
педиатр на первом месяце
жизни не менее 3-х раз,
в послед не
реже 1 раза в месяц;
хирург (ортопед) офтальмолог, невропатолог,
оториноларинголог на 1-ом году
жизни.
Контроль за режимом дня,
вскармливанием ребенка, массажа,
рекомендаций по воспитанию, проф рахита,
анемии, хрон рас-тв питания, инф
заб-й.
Объективный
осмотр: массу тела
и рост, окружность головы и груди, оценку
нерв-псих и физ развития, прорезывание
зубов, прикус, поведение, сос-е кожи,
костно-мыш системы, внутр органов,
следовую реакцию от вакцинации БЦЖ,
наличие врожд заболеваний, аномалии
развития.
Доп
методы: антропометрия
1 раз в месяц, клин
анализ крови и мочи к 3-м
месяцам
жизни и в 1
год.
Проф
и оздоровит мероприятия:
режим, организация рационал вскармливания,
достаточное пребывание на свежем
коздухе; проведение массажа, гимнастики
закаливающие процедуры, задачи воспитания,
спец проф рахита, профилактика анемии,
лечение выявленной патологии.
Критерии
эффективности :
показатели нервно-псих и физ развития,
поведение, данные клинич обслед, частота
заболеваний.
26.Диспансерное
наблюдение за здоровыми детьми от года
до семи лет.
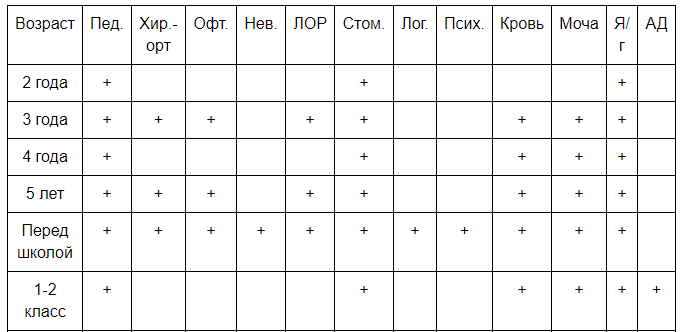
2 год: педиатр 1 раз в квартал, стоматолог по показаниям. При проведении профилактических осмотров осуществляется контроль за режимом дня, питания, проведением гимнастики и закаливающих процедур, выполнением рекомендаций по воспитанию, профилактике рахита, подготовке к детскому дошкольному учреждению. При объективном осмотре: особое внимание обращается на динамику массы тела и роста, зубную формулу, состояние прикуса, оценку психомоторного развития (проводится в КЗР), поведение, состояние кожных покровов, костно-мышечной. системы, состояние зубов и характер прикуса, состояние внутренних органов. Дополнительные методы обследования: антропометрия 1 раз в квартал, клинический анализ крови, мочи и кала на яйца глистов 1 раз в год. Определяется прогноз адаптации к детскому учреждению. По результатам диспансеризации дается комплексная оценка состояния здоровья и назначается комплекс профилактических и оздоровительных мероприятий. Критерии эффективности диспансеризации: показатели психомоторного и физического развития, данные клинического обследования и частота заболеваний, степень тяжести адаптации к детскому учреждению. 3 год: педиатр 1 раз в полугодие; офтальмолог, невропатолог, стоматолог, хирург, ортопед, оториноларинголог 1 раз в год. Контроль за режимом дня, питанием, воспитанием. Особое внимание обращается на динамику массы тела и роста, на состояние зубов, прикус, оценку нервно-психического и физического развития, состояние кожных покровов, лимфатической системы, носоглотки, осанки, наличие плоскостопия, состояние внутренних органов. Дополнительные методы обследования: антропометрия, определение остроты зрения и слуха, клинический анализ крови, мочи, кала на яйца глист. с 3 до 7 лет: педиатр 1 раз в год; отоларинголог, невропатолог, стоматолог, хирург, ортопед, окулист — в 5 лет и перед школой, др. специалисты — по показаниям. Контроль за режимом дня, питанием, физическим воспитанием и закаливанием, мероприятия по подготовке к школе. Особое внимание обращается на состояние физического развития, включая осанку, наличие и отсутствие плоскостопия, остроту зрения и слуха, физиометрические показатели, показатели психического здоровья (вегетативный статус, эмоциональный статус, психомоторная стабильность), состояние носоглотки, зубов, состояние внутренних органов (нервно-психическое развитие определяется в кабинете здорового ребенка). Дополнительные методы обследования: клинический анализ крови, мочи, анализ кала на яйца глистов, острота зрения и слуха, спиро и динамометрия ежегодно; в 5—6 лет и перед школой — определение соответствия паспортного возраста биологическому и школьной зрелости, артериальное давление с 5 лет. Если ребенок относится к I группе здоровья, то наблюдение в соответствии с представленной схемой считается достаточным. Если ребенок относится ко II, III, IV или V группе, то ему необходима реабилитация. Эффективность работы участкового врача со здоровым ребенком оценивается ежегодно по показателям физического, нервного и психического развития, резистентности и реактивности организма, функциональному состоянию основных органов и систем, наличию или отсутствию хронических болезней (в том числе врожденных и наследственных). Кабинет здорового ребенка-структурное подразделение детской поликлиники, выполняющее роль методического центра по проведению профилактической работы среди детей раннего возраста. Он обеспечивает консультативно-методическую помощь врачам-педиатрам, медицинским сестрам, молодым матерям и беременным женщинам. Основной задачей кабинета здорового ребенка является обучение молодых матерей теоретическим знаниям и практическим навыкам по вопросам ухода, воспитания, особенностям развития здоровых детей раннего и дошкольного возраста. Ведут здесь по графику приемы здоровых детей первого года жизни, определяют степень их физического и нервно-психического развития, беседуют с матерями о методах ухода за детьми и их воспитания, о рациональном питании исходя из индивидуальных особенностей ребенка. На базе кабинета проходят занятия школы будущих матерей, отцов, проводятся беседы со школьницами старших классов о будущем материнстве. 27.Распределение детей по группам здоровья в поликлинике. Критерии для определения группы здоровья. Группу здоровья определяет педиатр, учитывая осмотры специалистов. При исследовании состояния здоровья ребенка учитываются в качестве основополагающих следующие критерии: I критерий – наличие или отсутствие отклонений в раннем онтогенезе, II критерий – уровень физического развития и степень его гармоничности, III критерий – уровень нервно–психического развития, IV критерий – резистентность организма, V критерий – функциональное состояние органов и систем, VI критерий – наличие или отсутствие хронических болезней или врожденных пороков развития. Комплексная оценка с определением группы здоровья проводится по совокупности перечисленных критериев. Группа здоровья дает более широкое представление о состоянии здоровья ребенка, чем диагноз.
Первая (I) группа здоровья объединяет детей, не имеющих отклонений по всем избранным для оценки критериям здоровья, не болевших или редко болевших за период наблюдения, имеющих отставание в нервно–психическом развитии не более чем на 1 эпикризный срок, а также детей, имеющих единичные морфологические отклонения (аномалии ногтей, деформация ушной раковины и др.), не влияющие на состояние здоровья ребенка и не требующие коррекции. Вторую (II) группу здоровья составляют также здоровые дети, но имеющие "риск" формирования хронических заболеваний. В раннем возрасте принято выделять 2 подгруппы среди детей со II группой здоровья. II–A “угрожаемые дети”, имеющие отягощенный биологический, генеалогический или социальный анамнез, но не имеющие отклонений по всем остальным критериям здоровья. II–Б группа “риска” – дети, имеющие некоторые функциональные и морфологические изменения, часто болеющие дети (4 и более раз в год), дети с аномалиями конституции и другими отклонениями в состоянии здоровья. Третья (III) группа здоровья объединяет больных детей с наличием хронических болезней или врожденной патологии в состоянии компенсации, т.е. с редкими, нетяжелыми по характеру течения обострениями хронического заболевания без выраженного нарушения общего самочувствия и поведения, редкими интеркуррентными заболеваниями, наличием функциональных отклонений только одной, патологически измененной системы или органа (без клинических проявлений функциональных отклонений других органов и систем). Четвертая (IV) группа включает в себя детей с хроническими болезнями, врожденными пороками развития в состоянии субкомпенсации, которое определяется наличием функциональных отклонений не только патологически измененного органа, системы, но и других органов и систем, с частыми обострениями основного заболевания с нарушением общего состояния и самочувствия после обострения, с затяжными реконвалесцентными периодами после интеркуррентного заболевания. Пятая (V) группа – дети с тяжелыми хроническими заболеваниями, тяжелыми врожденными пороками развития в состоянии декомпенсации, т.е. угрожаемые по инвалидности или инвалиды. При отнесении детей ко 2 – 5 группам здоровья не обязательно наличие отклонений по всем критериям здоровья, достаточно по одному из них, но может быть и по нескольким. Группа здоровья определяется по самому тяжелому отклонению или диагнозу. 28. Основные показатели работы участкового врача - педиатра. Критериями оценки эффективности работы врача-педиатра участкового считаются: 1. Показатели профилактической работы врачей-педиатров участковых: а) охват дородовыми патронажами беременных. б) охват патронажем детей первого года жизни. в) полнота охвата профилактическими осмотрами детей (не менее 95% от общего числа детей соответствующего возраста, подлежащих профилактическим осмотрам, в том числе на первом году жизни ребенка - 100% (в 1 месяц, 3 месяца, 6 месяцев, 9 месяцев, 12 месяцев жизни ребенка); г) полнота охвата профилактическими прививками детей в соответствии с Национальным календарем профилактических прививок (не менее 95% от общего числа детей, подлежащих прививкам); д) удельный вес числа детей первого года жизни, находящихся на грудном вскармливании (в возрасте 3 месяцев - не менее 80%; 6 месяцев - не менее 50%; 9 месяцев - не менее 30%). 2. Показатели качества медицинской помощи детям на врачебном (педиатрическом) участке: а) качество диспансерного наблюдения детей: - удельный вес детей, состоящих под диспансерным наблюдением, в общем числе детей, прикрепленных к педиатрическому участку; - полнота охвата диспансерным наблюдением по нозологическим формам (не менее 90% от общего числа детей, состоящих под диспансерным наблюдением); - удельный вес детей, снятых с диспансерного наблюдения по выздоровлению (не менее 10% от общего числа детей, состоящих под диспансерным наблюдением); - удельный вес детей с улучшением состояния здоровья (не менее 10% от общего числа детей, состоящих под диспансерным наблюдением); - динамика численности детей-инвалидов; б) полнота охвата лечебно-профилактической помощью детей, состоящих под диспансерным наблюдением: - удельный вес детей, госпитализированных в плановом порядке, от общего числа детей, состоящих под диспансерным наблюдением и нуждающихся в плановой госпитализации; - удельный вес детей, направленных в плановом порядке в санаторно-курортные учреждения, от общего числа детей, состоящих под диспансерным наблюдением и нуждающихся в плановом санаторно-курортном лечении; - удельный вес детей, получивших противорецидивное лечение, от общего числа детей, состоящих под диспансерным наблюдением и нуждающихся в противорецидивном лечении; в) удельный вес количества выполненных индивидуальных программ реабилитации детей-инвалидов от общего числа детей-инвалидов; г) обоснованность назначения лекарственных средств и соблюдение правил выписки рецептов пациентам, в том числе имеющим право на получение набора социальных услуг. 3. Показатели динамики заболеваемости детей: а) динамика показателя первичной заболеваемости у детей. б) динамика показателя общей заболеваемости (распространенность) у детей. Динамический анализ уровней общей и впервые выявленной заболеваемости у детей по нозологическим формам позволяет выявить дефекты в оказании медицинской помощи, отрицательно сказывающиеся на диагностику, профилактику и лечение, что в дальнейшем поможет планировать мероприятия по их устранению. 4. Анализ случаев смерти детей на дому, в том числе детей первого года жизни. 5. Анализ случаев досуточной летальности детей в стационаре, в том числе детей первого года жизни. 29. Система профилактических прививок в нашей стране. Календарь прививок, показания и противопоказания. Профилактическая прививка — это введение в организм человека медицинских иммунобиологических препаратов для создания специфической невосприимчивости к инфекционным болезням. Национальный календарь профилактических прививок включает профилактические прививки против гепатита В, дифтерии, коклюша, кори, краснухи, полиомиелита, столбняка, туберкулеза, эпидемического паротита. Показания: также показаниями к введению вакцин являются появление или угроза распространения инфекционных заболеваний, возникновение вспышек или эпидемий тех или иных инфекций. Постоянные противопоказания
Сильная реакция или осложнение на предыдущую дозу;
Первичные иммунодефицитные состояния.
Временные противопоказания
Острые или хронические заболевания; Общие рекомендации на этот счет говорят, что вакцины должны вводиться через 2 недели после выздоровления. В отдельных случаях интервал может быть укорочен до 1 недели или удлинен в случае тяжелых заболеваний до 4-6 недель. В некоторых случаях, наличие у ребенка легкого заболевания (например, легкий насморк без температуры) не является противопоказанием к применению вакцин, особенно если ребенок часто страдает от инфекций верхних дыхательных путей или аллергическим ринитом. Повышенная температура сама по себе не является противопоказанием к иммунизации. Однако, если лихорадка или другие проявления указывают на наличие средней тяжести или тяжелого заболевания, ребенка нельзя прививать до полного выздоровления.
Введение иммуноглобулинов, компонентов крови; · после введения вакцины нужно выждать минимум 2 недели перед введением иммуноглобулина; · после введения иммуноглобулина необходим перерыв минимум 6 недель (желательно 3 месяца) до введения вакцины. Именно это время требуется для разрушения антител. Исключение составляют вакцины против полиомиелита и желтой лихорадки.
Иммуносупрессивная терапия;
Злокачественные новообразования;
Беременность.
Иммунодефицитное состояние (первичное). Противопоказаны вакцины: БЦЖ, ОПВ, коревая, паротитная, краснушная. Злокачественные новообразования. Противопоказаны вакцины: БЦЖ, ОПВ, АКДС, коревая, паротитная, краснушная. Беременность. Противопоказаны все живые вакцины. Запрет на введение живых вакцин связан не столько с опасностью их тератогенного влияния (предполагаемого лишь теоретически), сколько с возможностью связать с вакцинацией, например, врожденные дефекты новорожденного. Поэтому противопоказания в этой части надо рассматривать, в первую очередь, как средство защиты медицинского работника, проводящего вакцинацию, от возможных обвинений.
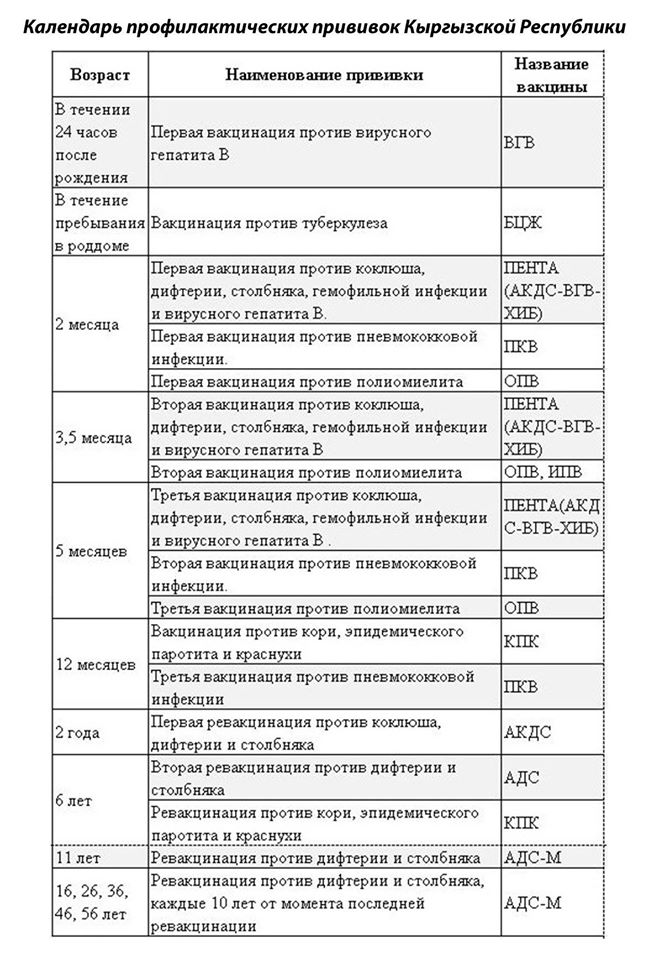
Состояния, которые имели место до вакцинации, но к настоящему времени уже отсутствуют (в анамнезе) также не являются противопоказанием для прививок:
· Умеренные местные реакции на предыдущее введение вакцины
· Недоношенность
· Перинатальная энцефалопатия
· Гемолитическая болезнь (желтуха) новорожденных
· Сепсис, болезнь гиалиновых мембран
30.Меры
борьбы с внутрибольничной инфекцией.
ВБИ-любые
клинически выраженные заболевания
микробного происхождения, кот. Поражают
больного в результате его поступления
в больницу или обращения за леч. Помощью,
вне зависимости от появления следов
заболевания во время пребывания в
больнице или после его выписки, а также
заболевания сотрудников вследствие их
работы в данном учреждении.
В
родовспомогательных учреждениях,
согласно официальным данным, частота
ВБИ у новорожденных составляет
0,3—0,6—1,0%. До настоящего времени в
родильных домах превалирует инфекция,
вызванная золотистым
стафилококком,
его госпитальными штаммами,
обладающими множественной лекарственной
устойчивостью. Но вспышки ВБИ, как
правило, обусловлены грамотрицательными
бактериями
(эшерихии,
синегнойная палочка, клебсиеллы,
протей).
В
целом, в связи с переходом родильных
домов на систему работы по принципу
мать—дитя, семейно-ориентированное
родовспоможение (раннее отсечение
пуповины, раннее прикладывание к груди,
сокращение времени пребывания в
стационаре) наблюдается тенденция к
снижению заболеваемости и значительному
уменьшению числа вспышек.
Для
борьбы с внутрибольничными инфекциями (ВБИ)
используются бактерицидные
дезинфектанты,
но их действие имеет избирательный
характер и некоторым бактериям удаётся
выжить после бактерицидной обработки
и попав в организм способствовать
развитию инфекционного заболевания не
страшась антибиотиков применяемых для
лечения.
-Неспецефическая
проф:
1)сан-планировочные
меропр(зонирование,рационал
размещение отделений по этажам; изоляция
секций,палат...;
соблюдение
потоков больных,персонала).
2)сан-технич
мер-я(правильное
оборудование вентиляции;
прав оборудование
водоотведения...)
3)сан-противоэпид(обеспечение
сан-гигиенич и сан-противоэпид режима;
контроль
за сан состоянием и режимом стационара;
обеспечение необход мед мероприятий;
контроль
за бактер обсемененностью внутрибольничной
среды; выявление носителей
среди персонала и больных;
сан-просветит работа среди персонала
и больных).
4)дезинфекц-стерилизац
мероприятия(механич обработка; применение
физиич методов; применение хим
методов).
-Спецефич
проф:проведение
плановой и экстренной иммунизации.
31.Физиология
лактации (анатомо-физиологические
особенности, правила и техника
кормления).
Лактация
– процесс
образования,
накопления
и выведения
молока – это
физиологический процесс.
Молочная
железа состоит из
альвеол,
по форме напоминающих пузырьки. Клетки
альвеолы производят молоко
из компонентов крови.
Снаружи
альвеола покрыта мышечными
клетками, их
сокращение
приводит к энергичному продвижению
молока по протоку,
отходящему от каждой альвеолы. Десятки
альвеол вместе с объединяющимися между
собой выводными протоками формируют
долю железы.
Молочная железа состоит обычно
из 15-20 таких долей,
расположенных вокруг ареолы
(пигментированной области вокруг соска)
и разделенных между собой прослойками
из соединительной и жировой тканей.
Молочные протоки,
спускаясь по всем радиусам железы, в
области ареолы образуют своеобразные
мешотчатые расширения - синусы,
где, как в цистернах, скапливается
молоко. Каналы
от каждого синуса идут к соску и
открываются
на его верхушке.
За время беременности молочная железа
достигает полного
развития и уже с середины беременности
становится способной вырабатывать
молоко. Но
вплоть до родов эта способность
тормозится гормонами плаценты.
Лактация
начинается после родов
и поддерживается регулярным
сосанием груди ребенком. Прикладывание
ребенка к груди в течение первого часа
после рождения способствует более
раннему становлению лактации.
Захватив грудь и сдавливая
деснами ареолу, новорожденный активно
сосет молоко,
создавая при этом разрежение в 200-220 мм
рт.ст. Своим сосанием он вызывает
выработку в организме матери пролактина
– гормона,
запускающего образование молока в
опустошаемых альвеолах
и поступление его в молочные ходы. Таким
образом, когда ребенок активно сосет
грудь, он не только утоляет голод, но и
запускает
процесс образования новых порций молока.
Чем больше он высосет молока, тем больше
образуется молока к следующему кормлению.
Таким образом, действует естественная
система регуляции, обеспечивающая
выработку молока по потребностям
ребенка.
Сосание
груди запускает (с некоторым опозданием)
выработку
еще одного гормона – окситоцина.
Окситоцин стимулирует
сокращение
мышечных клеток, окружающих альвеолы.
Это обеспечивает энергичное
продвижение молока по протокам и синусам
с активным «выбросом» его через сосок.
Окситоцин,
таким образом, влияет на эффективность
выделения молока из груди.
Кроме
сосания груди ребенком, выделение
молока могут запустить и другие факторы,
ассоциирующиеся у кормящей женщины с
кормлением: прикосновение к ребенку,
его крик, мысленные образы и т.п.
У
родившей женщины выделение молока, как
правило, начинается со 2-го или 3-го дня
после родов и
устанавливается в течение некоторого
времени. Этот
период является критическим для лактации
потому, что рефлекс выделения молока
очень раним и легко подавляется.
Нарушить выделение молока могут тревога,
страх, психическое напряжение или
травма, болевые и прочие дискомфортные
ощущения, равно
как и физическая усталость. Вот почему
для поддержания стабильной и достаточной
лактации так важны психологический
комфорт, уверенность
женщины в своих возможностях и полноценный
отдых.
Если
рефлекс выделения
подавлен, молоко задерживается в груди.
Процесс выработки молока в альвеолах
прекращается и одновременно тормозится
выделение гормонов, стимулирующих
лактацию - пролактина и окситоцина. В
итоге, естественно, образуется
меньшее количество молока. Если ситуация
с неполным опорожнением груди повторяется,
это неизбежно запускает процесс
подавления лактации.
Задержка
молока в груди
может также провоцироваться нерегулярным
и неадекватным по силе сосанием груди
ребенком или недостаточным сцеживанием
молока. Поэтому
кормящие матери должны помнить, что
регулярное активное сосание ребенка
(или сцеживание) является главным
условием поддержания эффективной
лактации.
Следует различать несколько
понятий, связанных с лактацией:
•
маммогенез — развитие молочной железы;
•
лактогенез — инициация секреции
молока;
• галактопоэз — поддержание
секреции молока;
• галактокинез —
удаление молока из железы.
Секреторный
цикл, протекающий
в эпителиальной клетке молочной железы,
состоит из 5 фаз:
1. поглощение клеткой
из крови и тканевых жидкостей веществ,
необходимых для образования молока;
2.
внутриклеточный
синтез молекул;
3.
формирование
капель или гранул
секрета;
4. передвижение
секрета к апикальному концу клетки;
5.
выход (экструзия) секрета
из клетки в просвет альвеолы.
В
первые 5 дней
после родов грудное молоко представляет
собой молозиво, в течение следующих
6-10 дней
жизни ребенка молоко носит черты
переходного, на более поздних стадиях
лактации (после 15-го
дня) вырабатывается
зрелое молоко.
Правила
естественного вскармливания:
1.
перед кормление помыть грудь (не каждый
раз);
2. кормление в удобном сидячем
состоянии; тело
ребенка должно быть прижато к телу
матери, лицо к груди; тело и голова
ребенка находятся в одной плоскости;
3.
при каждом кормлении прикладывать
только к одной груди, чередуя;
4.
вначале сцедить
несколько струек молока, затем
прикладывать;
захват
не только соска, но и большей части
ареолы, плотно
прижат подбородок
ребенка к груди;
рот открыт, нижняя
губа вывернута наружу;
5.
после
кормления необходимо сцеживать молоко;
вытереть молочную железу;
6.
продолжительность
кормления средняя – 20-30 мин (помнить
о: ленивых,проворных сосунах; молоко
отличается по качеству в начале и в
конце кормления);
7. если ребенок не
хочет есть → молоко
сцедить;
8.
степень лактации определять по
контрольному вскармливанию. Раннее
прикладывание к груди и ≪свободное
вскармливание≫
–
ключевые
факторы
полноценной
лактации.
9.
Если мать почувствовала
боль в груди при
кормлении ребенка -это значит, что
ребенок неправильно взял грудь. При
этом надо осторожно прикоснуться пальцем
к губам ребенка, чтобы он открыл рот, а
не тянуть насильно. Попытаться приложить
к груди повторно.
10. Кормить ребенка
необходимо
по потребности.
В первые дни до 10-14 раз в сутки. После
становления лактации {приблизительно
через 2-3 недели) режим устанавливается
самостоятельно и составляет 6-7 кормлений
в день.
11. Не рекомендуется делать
ночных перерывов в кормлении.
12. Не
надо давать никакой
дополнительной пищи,
кроме грудного молока, ребенку до 3-4
месяцев.
13. Необходимо помнить, что
в течение
дня ребенок высасывает разное количество
молока.
14.
После окончания кормления ребенка
необходимо подержать в вертикальном
положении.
32.Биологические
свойства грудного молока.
Молозиво
(первые 5 дней) представляет собой густую,
клейкую, желтого цвета жидкость.
-содержит
больше белков (2,3г/100мл,
против 1,1г/100 в сравнении со зрелым
молоком).
-Преобладают альбумины.
-в
2-10 раз больше
витамина А и каротина.
-в
2-3 раза больше
аскорбиновой кислоты антиоксиданты.
-больше
витамина
В12 и Е, цинка, селена.
-в
1,5 раза больше
солей.
-много
Ig A.
-молозивные
тельца – лейкоциты в стадии жирового
перерождения.
-лимфоциты способствуют
продукции Ig.
-в 1 мл – 2000 макрофагов.
-мало
жиров.
Состав
и количество молозива
(оно невелико) соответствуют еще слабым
пищеварительным возможностям
новорожденного. По сравнению со зрелым
молоком в молозиве содержится больше
белка, причем альбуминовая
и глобулиновая фракции белков превалируют
над казеином (казеин
появляется лишь с 4-5-го дня лактации и
его количество постепенно нарастает);
в 2-10 раз больше витамина А и каротина,
в 2-3 раза – аскорбиновой кислоты; больше
содержится витаминов В12 и
Е; в 1,5 раза больше солей, цинка, меди,
железа, лейкоцитов, среди которых
доминируют лимфоциты. Особенно много
в молозиве иммуноглобулинов класса А
(секреторный),
что наряду с другими факторами способствует
уже сразу после рождения высокой
эффективности кишечного иммунологического
барьера. Поэтому
молозиво иногда относят к фактору,
обеспечивающему первую
вакцинацию, или, как говорят, «теплую»
иммунизацию ребенка
в отличии от «холодной» (ампульной).
Содержание жира
и молочного
сахара
(лактозы), наоборот, в молозиве ниже, чем
в зрелом молоке.
Многие белки молозива (альбумины,
глобулины и др.) могут всасываться в
желудке и кишечнике в неизмененном
виде, так как они идентичны белкам
сыворотки крови ребенка. Молозиво
является весьма важной промежуточной
формой питания между периодами
гемотрофного и амниотрофного питания
и периодом энтерального (лактотрофного)
питания ребенка.
Переходное
молоко – это молоко
на промежуточных стадиях биологической
зрелости, выделяется в течение
индивидуально различных сроков после
родов. При
нарастании его количества грудные
железы наполняются, набухают и становятся
тяжелыми. Этот
момент называют «приходом» или «приливом»
молока. Преходное молоко по сравнению
с молозивом содержит меньшее
количество белка
и минеральных веществ, а количество
жира в нем повышается.
Одновременно растет и количество
вырабатываемого молока, что отвечает
возможности ребенка усваивать большие
объемы пищи.
Зрелое
молоко – это
молоко, вырабатывающееся к началу
3-ей недели после родов (так
происходит у подавляющего большинства
женщин; у 5-10 % женщин зрелое молоко может
появиться на неделю раньше). Состав
женского молока во многом зависит от
индивидуальных особенностей кормящей
матери, качества ее питания и некоторых
других факторов.
Биологически
активные соединения, содержащиеся в
женском молоке:


 33.Защитные
свойства грудного молока.
Содержит
все классы иммуноглобулинов –A,
M, G, E, секреторные IgA, IgM.
Секреторный
IgA содержит
антитела к вирусам гриппа, полиомиелита,
дифтерии, столбняка, краснухи и
т.д.
Клеточные элементы грудного
молока – лимфоциты
и макрофаги.
B-лимфоциты
синтезируют иммуноглобулины, интерферон,
интерлейкины, эпителиальные факторы
роста.
Бифидогенные
факторы.
Клеточный
состав грудного молока разный у молозива
и зрелого молока:
Молозиво
содержит 0,1-10 млн.
клеток в мл, из них около 50% - макрофагов,
40-45% - нейтрофильных
лейкоцитов, 5-10%
- лимфоцитов.
Зрелое
молоко – 10 000-200
000 клеток в мл, из них около 85% - макрофагов,
10% - лифоцитов, 5% - нейтрофильных
лейкоцитов.
Желудочно-кишечный
тракт ребенка
первых
лет жизни (а
отнюдь не первых месяцев, как считалось
ранее) обладает пониженным рН и другим
рядом свойств, что позволяет
определять клетки именно иммунной
системы, не расщеплять их и позволять
им длительно работать в кишечнике
ребенка. Более
того, лактоферрин, белок грудного молока,
обладающий максимальным набором защитных
качеств, не расщепляется и у взрослого
человека и способен помочь в борьбе с
очень большим рядом распространенных
заболеваний. Продукты же расщепления
других белков также способны
противодействовать микробной флоре,
сохраняя свою активность в ЖКТ на
протяжении длительного срока, стимулируя
правильное развитие иммунной системы
ребенка.
Липаза-водорастворимый
фермент,который компенсирует низкое
количество собственных ферментов
новорожденного, расщепляя жиры в его
желудочно-кишечном тракте. При этом
высвобождает
жирные кислоты, которые обладают
антивирусным и антибактериальным
свойством, в
частности против патогенных
простейших.
Лизоцим-
фермент, который разрушает
стенку бактериальной клетки,
в результате чего происходит её
растворение и уничтожение. Играет роль
неспецифического
антибактериального барьера,
особенно в местах контакта с внешней
средой (слёзы, слюна, слизистая оболочка
носа).
Лактопероксидаза-
очень важный антибактериальный элемент
противомикробной защиты.
Это очень мягкий противомикробный
агент,который одновременно стимулирует
рост полезных бактерий и
борется с ростом патогенных.
Лактоферрин-
наиболее полифункциональный белок
грудного молока. Лактоферрин является
одним из важнейших компонентов иммунной
системы организма, принимает участие
в системе
неспецифического гуморального иммунитета.
Защитные свойства лактоферрина уникальны,
природа собрала в нем максимум полезных
свойств - он обладает антибактериальной,
антивирусной, антипаразитарной,
различными каталитическими активностями,
а также противораковым, антиаллергическим,
иммуномоделирующим действиями
и радиопротективными свойствами.
34.Состав
зрелого молока и молозива.
Молозиво
(первые 5 дней) представляет собой густую,
клейкую, желтого цвета жидкость.
-содержит
больше белков (2,3г/100мл,
против 1,1г/100 в сравнении со зрелым
молоком).
-Преобладают альбумины.
-в
2-10 раз больше
витамина А и каротина.
-в
2-3 раза больше
аскорбиновой кислоты антиоксиданты.
-больше
витамина
В12 и Е, цинка, селена.
-в
1,5 раза больше
солей.
-много
Ig A.
-молозивные
тельца – лейкоциты в стадии жирового
перерождения.
-лимфоциты способствуют
продукции Ig.
-в 1 мл – 2000 макрофагов.
-мало
жиров.
Состав и
свойства груного молока:
-87,5% состоит
из воды.
Содержание
сухих веществ от
10 до 17 г/100мл:
-1. Углеводы 7 г/100 мл.
-2.Жиры
4 г/ 100мл.
-3. Белки 1г/100 мл.
-4.Минеральные
вещества -0,2 г/100 мл.
Белок
и аминокислоты женского молока
(0,9-1,3 г/100
мл).
-Идентичны
белкам сыворотки крови ребенка.
-Всасываются
путем диффузии.
-Сывороточные протеины
(70-80%) (метаболизирующие белки), (высокая
усвояимость).
-Соотношение сывороточного
протеина (образуют
мелкодисперстный сгусток) и казеина
(βфракция) 3:2
(в коровьем молоке 1:4)
-альфа-лактальбумин
(25-35%) (богат триптофаном и цистеином,
способствует росту
бифидобактерий,
усвоению
кальция и цинка, синтез лактозы из
глюкозы.
-альфа-лактальбумин в
соединении с олеиновой кислотой (HAMLET)
препятствует росту злокачественных
клеток.
Большое
количество иммуноглобулинов,
особенно IgA
(95,2%), IgG 2,9%, IgМ 1,9% лизоцима (неметаболизирующие
белки), защита от ОКИ, ОРВИ и
др.инфекций.
Аминокислота
таурин – модулятор
роста, обеспечивает
рост нервных клеток, симпатических и
сенсорных нейронов, эпидермального
покрова.
-аполактоферрин-
гликопептид, аналог
трансфферина крови (связывание
и транспорт железа).
Аминокислотный
состав грудного молока:
В
раннем детском возрасте незаменимы не
8, а 9 аминокислот.
У
детей на естественном вскармливании
интеллект выше.
Аминокислота
таурин – модулятор
роста, обеспечивает рост нервных клеток,
симпатических и сенсорных нейронов,
эпидермального покрова.
Липиды
женского молока
(триглицериды,фосфолипиды,жирные
кислоты,стеролы- от 31-35
г/л до 41-52
г/л).
-Преобладают
ПНЖК
(57%) над
насыщенными.
-Две
незаменимые ЖК –
линолевая и
α-линоленовая
(предшественники фосфолипидов,
простагландинов, ПНЖК, арахидоновой и
докозагексаеновой) присутствуют
в необходимом и достаточном количестве
в грудном молоке (необходимы для развития
мозга, пролиферации клеток, миелинизации
нервных волокон, формированию сетчатки
глаз).
-Высокая степень
дисперсности облегчает эмульгирование
жира и его всасывание.
-Усвоение
жира 80-95% (из
коровьего молока – 60%).
-Липаза
женского молока – компенсирует
низкую активность липазы поджелудочной
железы.
-Высокой
утилизации жира способствуют триглицериды
(98%).
-Триглицериды
резорбируются
без участия панкреатической
липазы.
-Холестерин
- высокий уровень (формирование
клеточных мембран, тканей нервной
системы, ряда
БАВ, включая витамин Д).
Углеводы
женского молока
(от 68-74 г/л):
Лактоза
(дисахарид)– молочный сахар, в женском
молоке 85%; обладают
в 2 раза большей энергетической ценностью,
но такой же осмолярностью, как
моносахариды.
β-лактоза
(в коровьем молоке α-лактоза)– усваивается
медленнее, успевает дойти до толстого
кишечника, стимулирует
рост Гр+ флоры,
стимулирует синтез витаминов группы В
и бифидум –флору (свойства пребиотика);
улучшение всасывания
Ca, Fe, Zn, P.
Лактоза
состоит из (галактозы
– способствует синтезу галактоцереброзидов
мозга, рецепторов
и сигнальных молекул
клеточного узнавания)
и глюкозы.
Олигоаминосахара
– обеспечивают
защиту от вирусов, бактерий, токсинов,
оказывают пробиотическое действие (15%
от углеводов).
Лактоза — это так
называемый «молочный сахар», углевод,
содержащийся в молоке и молочных
продуктах. Лактаза — фермент, необходимый
для расщепления лактозы на остаток
глюкозы и остаток галактозы.
Лактаза
необходима для полноценного
переваривания и ферментации лактозы.
У
части детей фермент лактаза созревает
поздно, может совсем отсутствовать.
В
грудном молоке
присутствует собственный фермент
лактаза.
Детям
с лактазной недостаточностью необходимо
продолжать естественное
вскармливание.
Олигосахартды.
Не подвергаются расщеплению ферментами
пищеварительного тракта, не всасываются.
В
толстой кишке ферментируются, где
являются субстратом
для роста бифидобактерий.
Имеют
рецепторы для бактерий, вирусов
(ротавирусов), токсинов и антител
(протективное действие в отношение
кишечных инфекций).
Минералы
женского молока:
Содержание минеральных
веществ
в молозиве выше (соли
Na, Fe, Zn, Cu, K).
В женском молоке
соотношение Ca : P,
2 : 1 ( в коровьем молоке 1 : 1), Са связан
с сывороточными белками (усвояимость
58%, из коровьего-
38%).
Усвоение Fe из женского молока -
50% (высокая
биодоступность связь с лактоферрином);
из коровьего – 10 – 30%.
Витамины
женского молока:
В женском молоке
больше жирорастворимых
витаминов (А, Д,
Е), чем в коровьем.
Активность
витамина Д значительно выше за счет
активных метаболитов (от
14 МЕ/л до 180 МЕ/л).
Грудное молоко
обеспечивает
поступление в детский организм витаминов
группы А, В, С.
Биологически
активные соединения, содержащиеся в
женском молоке:
35.Сравнительная
характеристика грудного и коровьего
молока по основным компонентам (белки,
жиры, углеводы, витамины, микроэлементы).
Преимущества естественного вскармливания.
33.Защитные
свойства грудного молока.
Содержит
все классы иммуноглобулинов –A,
M, G, E, секреторные IgA, IgM.
Секреторный
IgA содержит
антитела к вирусам гриппа, полиомиелита,
дифтерии, столбняка, краснухи и
т.д.
Клеточные элементы грудного
молока – лимфоциты
и макрофаги.
B-лимфоциты
синтезируют иммуноглобулины, интерферон,
интерлейкины, эпителиальные факторы
роста.
Бифидогенные
факторы.
Клеточный
состав грудного молока разный у молозива
и зрелого молока:
Молозиво
содержит 0,1-10 млн.
клеток в мл, из них около 50% - макрофагов,
40-45% - нейтрофильных
лейкоцитов, 5-10%
- лимфоцитов.
Зрелое
молоко – 10 000-200
000 клеток в мл, из них около 85% - макрофагов,
10% - лифоцитов, 5% - нейтрофильных
лейкоцитов.
Желудочно-кишечный
тракт ребенка
первых
лет жизни (а
отнюдь не первых месяцев, как считалось
ранее) обладает пониженным рН и другим
рядом свойств, что позволяет
определять клетки именно иммунной
системы, не расщеплять их и позволять
им длительно работать в кишечнике
ребенка. Более
того, лактоферрин, белок грудного молока,
обладающий максимальным набором защитных
качеств, не расщепляется и у взрослого
человека и способен помочь в борьбе с
очень большим рядом распространенных
заболеваний. Продукты же расщепления
других белков также способны
противодействовать микробной флоре,
сохраняя свою активность в ЖКТ на
протяжении длительного срока, стимулируя
правильное развитие иммунной системы
ребенка.
Липаза-водорастворимый
фермент,который компенсирует низкое
количество собственных ферментов
новорожденного, расщепляя жиры в его
желудочно-кишечном тракте. При этом
высвобождает
жирные кислоты, которые обладают
антивирусным и антибактериальным
свойством, в
частности против патогенных
простейших.
Лизоцим-
фермент, который разрушает
стенку бактериальной клетки,
в результате чего происходит её
растворение и уничтожение. Играет роль
неспецифического
антибактериального барьера,
особенно в местах контакта с внешней
средой (слёзы, слюна, слизистая оболочка
носа).
Лактопероксидаза-
очень важный антибактериальный элемент
противомикробной защиты.
Это очень мягкий противомикробный
агент,который одновременно стимулирует
рост полезных бактерий и
борется с ростом патогенных.
Лактоферрин-
наиболее полифункциональный белок
грудного молока. Лактоферрин является
одним из важнейших компонентов иммунной
системы организма, принимает участие
в системе
неспецифического гуморального иммунитета.
Защитные свойства лактоферрина уникальны,
природа собрала в нем максимум полезных
свойств - он обладает антибактериальной,
антивирусной, антипаразитарной,
различными каталитическими активностями,
а также противораковым, антиаллергическим,
иммуномоделирующим действиями
и радиопротективными свойствами.
34.Состав
зрелого молока и молозива.
Молозиво
(первые 5 дней) представляет собой густую,
клейкую, желтого цвета жидкость.
-содержит
больше белков (2,3г/100мл,
против 1,1г/100 в сравнении со зрелым
молоком).
-Преобладают альбумины.
-в
2-10 раз больше
витамина А и каротина.
-в
2-3 раза больше
аскорбиновой кислоты антиоксиданты.
-больше
витамина
В12 и Е, цинка, селена.
-в
1,5 раза больше
солей.
-много
Ig A.
-молозивные
тельца – лейкоциты в стадии жирового
перерождения.
-лимфоциты способствуют
продукции Ig.
-в 1 мл – 2000 макрофагов.
-мало
жиров.
Состав и
свойства груного молока:
-87,5% состоит
из воды.
Содержание
сухих веществ от
10 до 17 г/100мл:
-1. Углеводы 7 г/100 мл.
-2.Жиры
4 г/ 100мл.
-3. Белки 1г/100 мл.
-4.Минеральные
вещества -0,2 г/100 мл.
Белок
и аминокислоты женского молока
(0,9-1,3 г/100
мл).
-Идентичны
белкам сыворотки крови ребенка.
-Всасываются
путем диффузии.
-Сывороточные протеины
(70-80%) (метаболизирующие белки), (высокая
усвояимость).
-Соотношение сывороточного
протеина (образуют
мелкодисперстный сгусток) и казеина
(βфракция) 3:2
(в коровьем молоке 1:4)
-альфа-лактальбумин
(25-35%) (богат триптофаном и цистеином,
способствует росту
бифидобактерий,
усвоению
кальция и цинка, синтез лактозы из
глюкозы.
-альфа-лактальбумин в
соединении с олеиновой кислотой (HAMLET)
препятствует росту злокачественных
клеток.
Большое
количество иммуноглобулинов,
особенно IgA
(95,2%), IgG 2,9%, IgМ 1,9% лизоцима (неметаболизирующие
белки), защита от ОКИ, ОРВИ и
др.инфекций.
Аминокислота
таурин – модулятор
роста, обеспечивает
рост нервных клеток, симпатических и
сенсорных нейронов, эпидермального
покрова.
-аполактоферрин-
гликопептид, аналог
трансфферина крови (связывание
и транспорт железа).
Аминокислотный
состав грудного молока:
В
раннем детском возрасте незаменимы не
8, а 9 аминокислот.
У
детей на естественном вскармливании
интеллект выше.
Аминокислота
таурин – модулятор
роста, обеспечивает рост нервных клеток,
симпатических и сенсорных нейронов,
эпидермального покрова.
Липиды
женского молока
(триглицериды,фосфолипиды,жирные
кислоты,стеролы- от 31-35
г/л до 41-52
г/л).
-Преобладают
ПНЖК
(57%) над
насыщенными.
-Две
незаменимые ЖК –
линолевая и
α-линоленовая
(предшественники фосфолипидов,
простагландинов, ПНЖК, арахидоновой и
докозагексаеновой) присутствуют
в необходимом и достаточном количестве
в грудном молоке (необходимы для развития
мозга, пролиферации клеток, миелинизации
нервных волокон, формированию сетчатки
глаз).
-Высокая степень
дисперсности облегчает эмульгирование
жира и его всасывание.
-Усвоение
жира 80-95% (из
коровьего молока – 60%).
-Липаза
женского молока – компенсирует
низкую активность липазы поджелудочной
железы.
-Высокой
утилизации жира способствуют триглицериды
(98%).
-Триглицериды
резорбируются
без участия панкреатической
липазы.
-Холестерин
- высокий уровень (формирование
клеточных мембран, тканей нервной
системы, ряда
БАВ, включая витамин Д).
Углеводы
женского молока
(от 68-74 г/л):
Лактоза
(дисахарид)– молочный сахар, в женском
молоке 85%; обладают
в 2 раза большей энергетической ценностью,
но такой же осмолярностью, как
моносахариды.
β-лактоза
(в коровьем молоке α-лактоза)– усваивается
медленнее, успевает дойти до толстого
кишечника, стимулирует
рост Гр+ флоры,
стимулирует синтез витаминов группы В
и бифидум –флору (свойства пребиотика);
улучшение всасывания
Ca, Fe, Zn, P.
Лактоза
состоит из (галактозы
– способствует синтезу галактоцереброзидов
мозга, рецепторов
и сигнальных молекул
клеточного узнавания)
и глюкозы.
Олигоаминосахара
– обеспечивают
защиту от вирусов, бактерий, токсинов,
оказывают пробиотическое действие (15%
от углеводов).
Лактоза — это так
называемый «молочный сахар», углевод,
содержащийся в молоке и молочных
продуктах. Лактаза — фермент, необходимый
для расщепления лактозы на остаток
глюкозы и остаток галактозы.
Лактаза
необходима для полноценного
переваривания и ферментации лактозы.
У
части детей фермент лактаза созревает
поздно, может совсем отсутствовать.
В
грудном молоке
присутствует собственный фермент
лактаза.
Детям
с лактазной недостаточностью необходимо
продолжать естественное
вскармливание.
Олигосахартды.
Не подвергаются расщеплению ферментами
пищеварительного тракта, не всасываются.
В
толстой кишке ферментируются, где
являются субстратом
для роста бифидобактерий.
Имеют
рецепторы для бактерий, вирусов
(ротавирусов), токсинов и антител
(протективное действие в отношение
кишечных инфекций).
Минералы
женского молока:
Содержание минеральных
веществ
в молозиве выше (соли
Na, Fe, Zn, Cu, K).
В женском молоке
соотношение Ca : P,
2 : 1 ( в коровьем молоке 1 : 1), Са связан
с сывороточными белками (усвояимость
58%, из коровьего-
38%).
Усвоение Fe из женского молока -
50% (высокая
биодоступность связь с лактоферрином);
из коровьего – 10 – 30%.
Витамины
женского молока:
В женском молоке
больше жирорастворимых
витаминов (А, Д,
Е), чем в коровьем.
Активность
витамина Д значительно выше за счет
активных метаболитов (от
14 МЕ/л до 180 МЕ/л).
Грудное молоко
обеспечивает
поступление в детский организм витаминов
группы А, В, С.
Биологически
активные соединения, содержащиеся в
женском молоке:
35.Сравнительная
характеристика грудного и коровьего
молока по основным компонентам (белки,
жиры, углеводы, витамины, микроэлементы).
Преимущества естественного вскармливания.
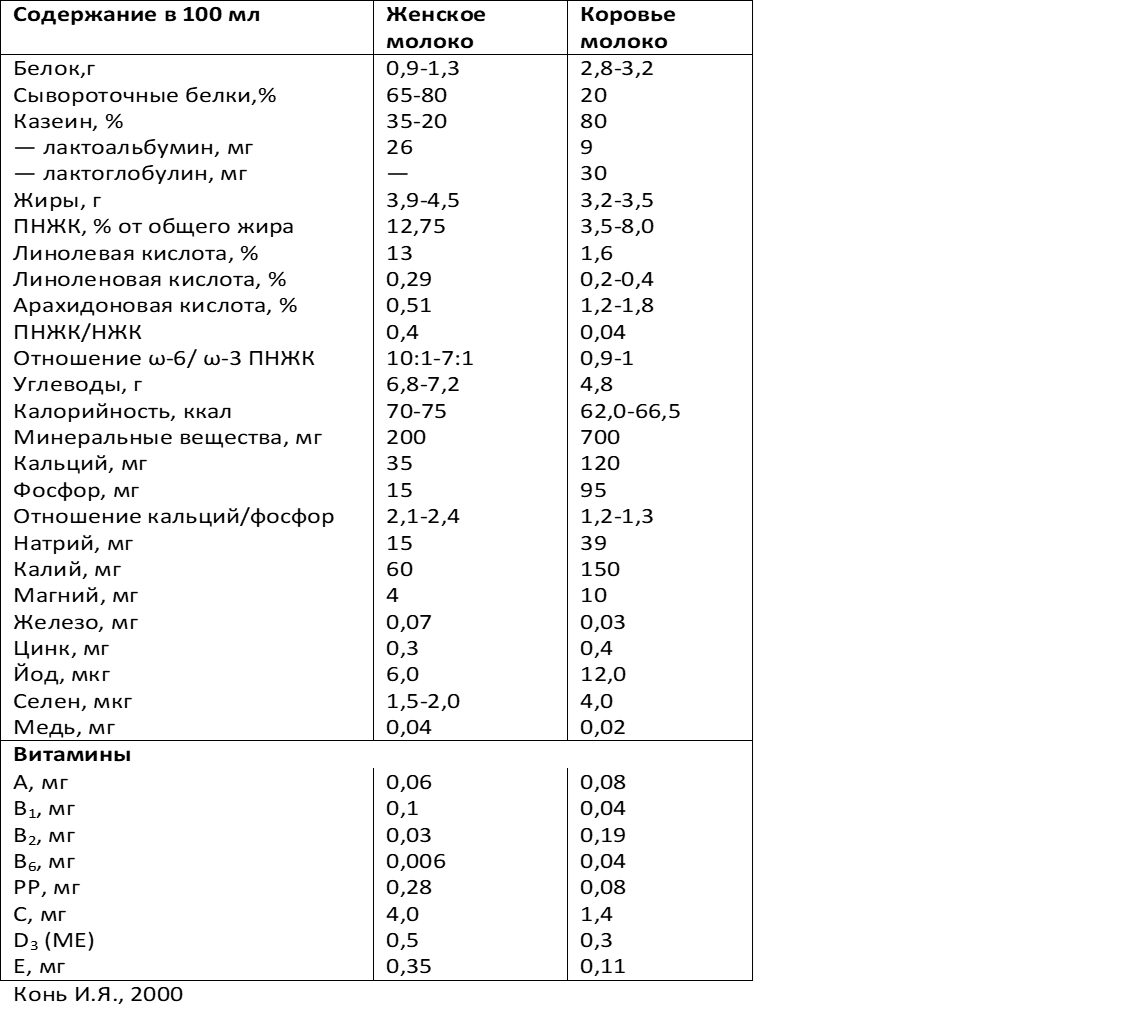 Соотношение
сывороточного
протеина (образуют
мелкодисперстный сгусток) и казеина
(βфракция) 3:2 (в коровьем молоке
1:4).
Усвоение
жира 80-95% (из коровьего молока – 60%).
В
женском молоке соотношение Ca : P, 2 : 1 ( в
коровьем молоке 1 : 1), Са связан с
сывороточными белками (усвояимость
58%, из коровьего- 38%).
Белки
(в коровьем молоке их в 2,5 - 3 раза больше,
чем в женском) представлены в основном
казеинами,
отношение которых к сывороточным
белкам составляет
80:20,
в то время как в женском молоке это
отношение оптимально и составляет
40:60. Казеины
коровьего молока (альфа-казеины)
при створаживании
в желудке ребенка образуют более грубый,
рыхлый сгусток и
медленнее
перевариваются
по сравнению с казеинами (бета-казеины)
женского молока. Казеины
образуют
с кальцием и фосфором
сложные соединения (казеин-фосфат-кальциевые
комплексы), препятствующие выпадению
казеина в осадок и
улучшающие усвоение кальция и фосфора
из молока. Белки коровьего молока, как
и женского, содержат все жизненно важные
незаменимые аминокислоты. Особенно
богаты незаменимыми аминокислотами
белки сыворотки, поэтому пищевая ценность
их выше, чем казеина. Усвоение белков
молока составляет 90 %.
Жиры
коровьего молока качественно
отличаются от
жиров женского молока. В них твердые
(тугоплавкие)
жиры и насыщенные жирные кислоты
преобладают над легкоусвояемыми
ненасыщенными кислотами.
Насыщенные жирные
кислоты, которых
в коровьем молоке
в 1,5 - 3 раза больше, чем в женском,
являются раздражителями
слизистой оболочки желудочно-кишечного
тракта (особенно
у детей раннего возраста) и могут вызвать
его функциональные расстройства. Как
по количественному, так и по качественному
составу полиненасыщенных
жирных кислот коровье молоко уступает
женскому (например,
линолевой кислоты
в нем в 5 раз меньше).
В коровьем молоке, как и в женском,
содержатся необходимые для организма
ребенка жироподобные вещества-фосфатиды
(лецитин и др.). Молочный
жир находится в
коровьем молоке тоже в виде мелких
жировых шариков, покрытых тонкой белковой
оболочкой, благодаря чему он легче
переваривается и полнее усваивается
организмом.
Углеводы
представлены в коровьем
молоке в основном
дисахаридом
лактозой (альфа-лактоза).
В небольшом количестве в нем содержатся
простые сахара
(глюкоза и др.) и сложные соединения
углеводов с белками.
Альфа-лактоза
коровьего молока качественно
отличается от
бета-лактозы
женского молока,
так как расщепляется
уже в верхних отделах тонкого кишечника
и практически не доходит до толстого,
а значит, не является
питательной средой для бифидобактерий.
Однако это не снижает ценности
альфа-лактозы коровьего молока как
питательного продукта, поскольку при
расщеплении ее в желудочно-кишечном
тракте образуются необходимые организму
глюкоза и галактоза, в процессе обмена
которых выделяется значительное
количество энергии и поддерживается
оптимальный уровень сахара (глюкозы) в
крови.
Минеральные
вещества коровьего
молока, которых
содержится в нем примерно в 3
- 3,5 раза больше,
чем в женском, представлены полным
набором макро- и микроэлементов.
Особенно богато коровье молоко кальцием,
фосфором и натрием (их в 3 - 6 раз больше,
чем в женском).
Кальций и фосфор находятся в молоке в
основном в виде
соединений с казеином и поэтому хорошо
усваиваются организмом.
Витамины,
необходимые для организма ребенка
(жиро- и водорастворимые), также
представлены в коровьем молоке полным
набором. Однако
количество их
колеблется в зависимости от сезона года
и качества кормов животного.
В течение года отмечаются значительные
колебания в молоке витаминов Л, D, С,
количество
же витаминов группы В более стабильно.
Летом, когда рацион животных более
разнообразен и богат свежими кормами,
содержание витаминов в молоке значительно
выше, чем зимой. В любое время года
коровье молоко богаче женского витаминами
В1,
В2,
В3,
В12.
В женском
молоке больше
жирорастворимых витаминов
(А, Д, Е), чем в коровьем.
Преимущества
грудного вскармливания.
-Способствует
росту
здоровой кишечной микрофлоры с
преобладанием бифидобактерий (более
700 видов).
-Способствует развитию и
становлению
иммунных функций.
-Способствует
формированию
пищевой толерантности и
снижает
риск развития аллергических
состояний.
-Снижает
риск развития ожирения и сахарного
диабета, АГ,
атеросклероза - вследствие
невысокого содержания белка.
-Содержит
эссенциальные
полиненасыщенные жирные кислоты,
необходимые для развития
мозга и адекватного иммунного
статуса.
-Формирование
тесной
психоэмоциональной связи ребёнка с
кормящей матерью в
процессе длительного и тесного физического
и эмоционального контакта.
-Обеспечение
правильного
анатомического формирования зубочелюстной
системы, мозгового
черепа.
-Более благоприятные
показатели физического и нервно-психического
развития детей.
-Сохранение
физиологических темпов биологического
взросления.
6.Современные
тенденции естественного вскармливания:
режим, длительность, сроки пищевых
добавок и прикорма.
1.Начинать
ГВ в течении
получаса после родов (секреция
молока и сокращение матки).
2.Первые
2 часа ребенок и мать должны находиться
вместе и вместе переводиться в послеродовую
палату.
3.Кормить
младенца
часто, по требованию,
днем и ночью. 20-30 мин.
4.Не давать
новорожденным иной пищи или питья.
Исключительно
ГВ первые 6 месяцев!
5.После
6 месяцев, когда вводятся
прикормы ГВ должно предшествовать.
6.Продолжать
ГВ и на
втором году жизни, до 2 лет.
Уникальное содержание Ig, особенно A –
предотвращает заболевания.
7.Мать
больная туберкулезом, гепатитом, ОРВИ
может кормить ребенка грудью и может
быть вместе с ребенком.
8.Не давать
детям на ГВ устройств имитирующих
грудь.
9.Кормящая
мать не должна ограничивать себя в питье
и в еде, т.е. по аппетиту , не насиловать
себя.
10.Мама – лучший инкубатор.
Практиковать круглосуточное нахождение
матери и новорожденного в одной палате,
что предупреждает инфицирование и
гипотермию.
С
5-ти месяцев в питании ребенка начинается
важный этап -
введение
прикормов:
Первая
пищевая добавка в 4 мес.:
Фруктовые соки
(пюре) - яблочный, из белой черешни, из
белой смородины, абрикосовый, персиковый,
грушевый, сливовый (даны в порядке
предпочтения). Начинают вводить в рацион
с капель, постепенно увеличивая количество
до 40-60 мл. Желательно чтобы первые соки
ребенка были натуральными и свежими
(домашнего приготовления)
Творог
(кальцинированный) так же желателен
домашнего приготовления - на 200 мл молока
в момент закипания добавляется 1-2
столовые ложки СаСl2 , затем откидывается
на марлю, или молочной кухни, специального
детского питания. Начинают вводить в
рацион с крупинок и доводят до 40 грамм
в сутки
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков).
Первый
прикорм в 5-6 мес.:
Чаще в качестве первого прикорма
используют овощное пюре (картофель,
капуста, кабачок, тыква, и в последнюю
очередь морковь). Начинают
с 1 – 2 чайных ложек и
постепенно в течение 1- 2 недель заменяют
полностью 1 кормление (это примерно 150
мл). Далее 2 -3 недели не вводя ничего
нового – период адаптации.
Второй
прикорм в 6-7 мес.:
5% кашу (с 8 месяцев - 10%); (рисовая, манная,
гречневая, кукурузная) с добавлением 5
г сливочного масла, яичного желтка.
В
6-7 мес. Вводится также мясной
бульон (используют
для разведения овощного пюре), затем
мясо говядины, телятины в виде фарша.
Через
месяц вводят второй прикорм – кашу
(предпочтительнее начинать с безглютеновых
злаков – рис, кукурузная, гречневая
мука). Наиболее удобны сухие
растворимые каши:
они обогащены витаминами, кальцием,
железом, имеют гарантированный состав
и безопасность. У детей с хорошим весом
прикормы начинают с овощей, при
дефиците веса первым прикормом становится
каша. В овощное
пюре обычно вводится 5мл растительного
масла (желательно чередовать
подсолнечное, оливковое, кукурузное),
а в кашу сливочное.
Мясо отварное
(телятина, кролик, индейка) дважды
пропускается через мясорубку и дается
ребенку, начиная с
1 чайной ложки,
постепенно доведя количество до 60-80
грамм в сутки,
обычно в третье кормление.
С момента
введения первого прикорма ребенок
переходит на 5-ти
разовое питание.
Прикормы необходимо разделять кормлениями
грудью, обычно
первое,
третье
и последнее
кормление – грудное молоко или молочная
смесь, второе
– каша,
а четвертое
– овощи.
Третий
прикорм в 7-8 мес.:
неадаптированные молочные продукты:
молоко, кефир,
йогурты и полностью
грудным остается только первое и
последнее кормление.
С 9-10 мес. -
«кусочковое» питание.
С 10-11 мес. -
нежирные сорта рыбы не чаще 2-х раз в
неделю.
ПРАВИЛА
ВВЕДЕНИЯ ПРИКОРМОВ:
1.
Дается перед
кормлением грудью.
2.
Начинают с 3
- 4 чайных ложек (20
граммов), постепенно увеличивают, в
течение 2-х недель заменяют грудное
кормление.
3. Блюдо должно быть
гомогенезированным,
достаточно жидким, не вызывать затруднения
при глотании.
4.
Переходить
к другому виду прикорма следует только
после того, как ребенок привык к
предыдущему.
5.
Если ребенок плохо ест овощное пюре, в
качестве
первого прикорма можно использовать
5% кашу, а на второй
- дать овощное пюре.
РЕКОМЕНДУЕМЫЕ
ПРОДУКТЫ:
для овощного пюре - начинать
с одного вида овощей (картофель, кабачки),
переходя к смеси овощей (капуста, морковь,
тыква, свекла, томаты);
для каш -
рисовая, гречневая, овсяная мука.
37.10
принципов грудного вскармливания
(согласно рекомендациям ВОЗ).
1.Начинать
ГВ в течении
получаса после родов (секреция
молока и сокращение матки).
2.Первые
2 часа ребенок и мать должны находиться
вместе и вместе переводиться в послеродовую
палату.
3.Кормить
младенца
часто, по требованию,
днем и ночью. 20-30 мин.
4.Не давать
новорожденным иной пищи или питья.
Исключительно
ГВ первые 6 месяцев!
5.После
6 месяцев, когда вводятся
прикормы ГВ должно предшествовать.
6.Продолжать
ГВ и на
втором году жизни, до 2 лет.
Уникальное содержание Ig, особенно A –
предотвращает заболевания.
7.Мать
больная туберкулезом, гепатитом, ОРВИ
может кормить ребенка грудью и может
быть вместе с ребенком.
8.Не давать
детям на ГВ устройств имитирующих
грудь.
9.Кормящая
мать не должна ограничивать себя в питье
и в еде, т.е. по аппетиту , не насиловать
себя.
10.Мама – лучший инкубатор.
Практиковать круглосуточное нахождение
матери и новорожденного в одной палате,
что предупреждает инфицирование и
гипотермию.
38.Затруднения
и противопоказания при грудном
вскармливании.
Противопоказание
со стороны матери:
-эклампсия.
-сильные
кровотечения во время родов и в
послеродовом периоде.
-открытая форма
туберкулеза.
-состояние выраженной
декомпенсации при хронических заболеваниях
сердца, легких,
почек, печени, а также гипертиреоз.
-острые
психические
заболевания.
-особо
опасные инфекции (тиф, холера и
др.).
-герпетические
высыпания на соске молочной
железы (до их долечивания).
-ВИЧ-инфицирование
(риск заражения ребёнка 15%).
-острый
гепатит А.
- прием цитостатиков
в терапевтических дозах,
иммунносупрессивных препаратов,
антикоагулянтов типа фениндиона,
радиоизотопных контрастные вещества
для лечения или обследования, препаратов
лития, большинство противовирусных
препаратов (кроме
ацикловира, зидовудина, занамивира,
лимовудина, озельтамивира — с
осторожностью) противогельминтных
препаратов с осторожностью.
Соотношение
сывороточного
протеина (образуют
мелкодисперстный сгусток) и казеина
(βфракция) 3:2 (в коровьем молоке
1:4).
Усвоение
жира 80-95% (из коровьего молока – 60%).
В
женском молоке соотношение Ca : P, 2 : 1 ( в
коровьем молоке 1 : 1), Са связан с
сывороточными белками (усвояимость
58%, из коровьего- 38%).
Белки
(в коровьем молоке их в 2,5 - 3 раза больше,
чем в женском) представлены в основном
казеинами,
отношение которых к сывороточным
белкам составляет
80:20,
в то время как в женском молоке это
отношение оптимально и составляет
40:60. Казеины
коровьего молока (альфа-казеины)
при створаживании
в желудке ребенка образуют более грубый,
рыхлый сгусток и
медленнее
перевариваются
по сравнению с казеинами (бета-казеины)
женского молока. Казеины
образуют
с кальцием и фосфором
сложные соединения (казеин-фосфат-кальциевые
комплексы), препятствующие выпадению
казеина в осадок и
улучшающие усвоение кальция и фосфора
из молока. Белки коровьего молока, как
и женского, содержат все жизненно важные
незаменимые аминокислоты. Особенно
богаты незаменимыми аминокислотами
белки сыворотки, поэтому пищевая ценность
их выше, чем казеина. Усвоение белков
молока составляет 90 %.
Жиры
коровьего молока качественно
отличаются от
жиров женского молока. В них твердые
(тугоплавкие)
жиры и насыщенные жирные кислоты
преобладают над легкоусвояемыми
ненасыщенными кислотами.
Насыщенные жирные
кислоты, которых
в коровьем молоке
в 1,5 - 3 раза больше, чем в женском,
являются раздражителями
слизистой оболочки желудочно-кишечного
тракта (особенно
у детей раннего возраста) и могут вызвать
его функциональные расстройства. Как
по количественному, так и по качественному
составу полиненасыщенных
жирных кислот коровье молоко уступает
женскому (например,
линолевой кислоты
в нем в 5 раз меньше).
В коровьем молоке, как и в женском,
содержатся необходимые для организма
ребенка жироподобные вещества-фосфатиды
(лецитин и др.). Молочный
жир находится в
коровьем молоке тоже в виде мелких
жировых шариков, покрытых тонкой белковой
оболочкой, благодаря чему он легче
переваривается и полнее усваивается
организмом.
Углеводы
представлены в коровьем
молоке в основном
дисахаридом
лактозой (альфа-лактоза).
В небольшом количестве в нем содержатся
простые сахара
(глюкоза и др.) и сложные соединения
углеводов с белками.
Альфа-лактоза
коровьего молока качественно
отличается от
бета-лактозы
женского молока,
так как расщепляется
уже в верхних отделах тонкого кишечника
и практически не доходит до толстого,
а значит, не является
питательной средой для бифидобактерий.
Однако это не снижает ценности
альфа-лактозы коровьего молока как
питательного продукта, поскольку при
расщеплении ее в желудочно-кишечном
тракте образуются необходимые организму
глюкоза и галактоза, в процессе обмена
которых выделяется значительное
количество энергии и поддерживается
оптимальный уровень сахара (глюкозы) в
крови.
Минеральные
вещества коровьего
молока, которых
содержится в нем примерно в 3
- 3,5 раза больше,
чем в женском, представлены полным
набором макро- и микроэлементов.
Особенно богато коровье молоко кальцием,
фосфором и натрием (их в 3 - 6 раз больше,
чем в женском).
Кальций и фосфор находятся в молоке в
основном в виде
соединений с казеином и поэтому хорошо
усваиваются организмом.
Витамины,
необходимые для организма ребенка
(жиро- и водорастворимые), также
представлены в коровьем молоке полным
набором. Однако
количество их
колеблется в зависимости от сезона года
и качества кормов животного.
В течение года отмечаются значительные
колебания в молоке витаминов Л, D, С,
количество
же витаминов группы В более стабильно.
Летом, когда рацион животных более
разнообразен и богат свежими кормами,
содержание витаминов в молоке значительно
выше, чем зимой. В любое время года
коровье молоко богаче женского витаминами
В1,
В2,
В3,
В12.
В женском
молоке больше
жирорастворимых витаминов
(А, Д, Е), чем в коровьем.
Преимущества
грудного вскармливания.
-Способствует
росту
здоровой кишечной микрофлоры с
преобладанием бифидобактерий (более
700 видов).
-Способствует развитию и
становлению
иммунных функций.
-Способствует
формированию
пищевой толерантности и
снижает
риск развития аллергических
состояний.
-Снижает
риск развития ожирения и сахарного
диабета, АГ,
атеросклероза - вследствие
невысокого содержания белка.
-Содержит
эссенциальные
полиненасыщенные жирные кислоты,
необходимые для развития
мозга и адекватного иммунного
статуса.
-Формирование
тесной
психоэмоциональной связи ребёнка с
кормящей матерью в
процессе длительного и тесного физического
и эмоционального контакта.
-Обеспечение
правильного
анатомического формирования зубочелюстной
системы, мозгового
черепа.
-Более благоприятные
показатели физического и нервно-психического
развития детей.
-Сохранение
физиологических темпов биологического
взросления.
6.Современные
тенденции естественного вскармливания:
режим, длительность, сроки пищевых
добавок и прикорма.
1.Начинать
ГВ в течении
получаса после родов (секреция
молока и сокращение матки).
2.Первые
2 часа ребенок и мать должны находиться
вместе и вместе переводиться в послеродовую
палату.
3.Кормить
младенца
часто, по требованию,
днем и ночью. 20-30 мин.
4.Не давать
новорожденным иной пищи или питья.
Исключительно
ГВ первые 6 месяцев!
5.После
6 месяцев, когда вводятся
прикормы ГВ должно предшествовать.
6.Продолжать
ГВ и на
втором году жизни, до 2 лет.
Уникальное содержание Ig, особенно A –
предотвращает заболевания.
7.Мать
больная туберкулезом, гепатитом, ОРВИ
может кормить ребенка грудью и может
быть вместе с ребенком.
8.Не давать
детям на ГВ устройств имитирующих
грудь.
9.Кормящая
мать не должна ограничивать себя в питье
и в еде, т.е. по аппетиту , не насиловать
себя.
10.Мама – лучший инкубатор.
Практиковать круглосуточное нахождение
матери и новорожденного в одной палате,
что предупреждает инфицирование и
гипотермию.
С
5-ти месяцев в питании ребенка начинается
важный этап -
введение
прикормов:
Первая
пищевая добавка в 4 мес.:
Фруктовые соки
(пюре) - яблочный, из белой черешни, из
белой смородины, абрикосовый, персиковый,
грушевый, сливовый (даны в порядке
предпочтения). Начинают вводить в рацион
с капель, постепенно увеличивая количество
до 40-60 мл. Желательно чтобы первые соки
ребенка были натуральными и свежими
(домашнего приготовления)
Творог
(кальцинированный) так же желателен
домашнего приготовления - на 200 мл молока
в момент закипания добавляется 1-2
столовые ложки СаСl2 , затем откидывается
на марлю, или молочной кухни, специального
детского питания. Начинают вводить в
рацион с крупинок и доводят до 40 грамм
в сутки
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков).
Первый
прикорм в 5-6 мес.:
Чаще в качестве первого прикорма
используют овощное пюре (картофель,
капуста, кабачок, тыква, и в последнюю
очередь морковь). Начинают
с 1 – 2 чайных ложек и
постепенно в течение 1- 2 недель заменяют
полностью 1 кормление (это примерно 150
мл). Далее 2 -3 недели не вводя ничего
нового – период адаптации.
Второй
прикорм в 6-7 мес.:
5% кашу (с 8 месяцев - 10%); (рисовая, манная,
гречневая, кукурузная) с добавлением 5
г сливочного масла, яичного желтка.
В
6-7 мес. Вводится также мясной
бульон (используют
для разведения овощного пюре), затем
мясо говядины, телятины в виде фарша.
Через
месяц вводят второй прикорм – кашу
(предпочтительнее начинать с безглютеновых
злаков – рис, кукурузная, гречневая
мука). Наиболее удобны сухие
растворимые каши:
они обогащены витаминами, кальцием,
железом, имеют гарантированный состав
и безопасность. У детей с хорошим весом
прикормы начинают с овощей, при
дефиците веса первым прикормом становится
каша. В овощное
пюре обычно вводится 5мл растительного
масла (желательно чередовать
подсолнечное, оливковое, кукурузное),
а в кашу сливочное.
Мясо отварное
(телятина, кролик, индейка) дважды
пропускается через мясорубку и дается
ребенку, начиная с
1 чайной ложки,
постепенно доведя количество до 60-80
грамм в сутки,
обычно в третье кормление.
С момента
введения первого прикорма ребенок
переходит на 5-ти
разовое питание.
Прикормы необходимо разделять кормлениями
грудью, обычно
первое,
третье
и последнее
кормление – грудное молоко или молочная
смесь, второе
– каша,
а четвертое
– овощи.
Третий
прикорм в 7-8 мес.:
неадаптированные молочные продукты:
молоко, кефир,
йогурты и полностью
грудным остается только первое и
последнее кормление.
С 9-10 мес. -
«кусочковое» питание.
С 10-11 мес. -
нежирные сорта рыбы не чаще 2-х раз в
неделю.
ПРАВИЛА
ВВЕДЕНИЯ ПРИКОРМОВ:
1.
Дается перед
кормлением грудью.
2.
Начинают с 3
- 4 чайных ложек (20
граммов), постепенно увеличивают, в
течение 2-х недель заменяют грудное
кормление.
3. Блюдо должно быть
гомогенезированным,
достаточно жидким, не вызывать затруднения
при глотании.
4.
Переходить
к другому виду прикорма следует только
после того, как ребенок привык к
предыдущему.
5.
Если ребенок плохо ест овощное пюре, в
качестве
первого прикорма можно использовать
5% кашу, а на второй
- дать овощное пюре.
РЕКОМЕНДУЕМЫЕ
ПРОДУКТЫ:
для овощного пюре - начинать
с одного вида овощей (картофель, кабачки),
переходя к смеси овощей (капуста, морковь,
тыква, свекла, томаты);
для каш -
рисовая, гречневая, овсяная мука.
37.10
принципов грудного вскармливания
(согласно рекомендациям ВОЗ).
1.Начинать
ГВ в течении
получаса после родов (секреция
молока и сокращение матки).
2.Первые
2 часа ребенок и мать должны находиться
вместе и вместе переводиться в послеродовую
палату.
3.Кормить
младенца
часто, по требованию,
днем и ночью. 20-30 мин.
4.Не давать
новорожденным иной пищи или питья.
Исключительно
ГВ первые 6 месяцев!
5.После
6 месяцев, когда вводятся
прикормы ГВ должно предшествовать.
6.Продолжать
ГВ и на
втором году жизни, до 2 лет.
Уникальное содержание Ig, особенно A –
предотвращает заболевания.
7.Мать
больная туберкулезом, гепатитом, ОРВИ
может кормить ребенка грудью и может
быть вместе с ребенком.
8.Не давать
детям на ГВ устройств имитирующих
грудь.
9.Кормящая
мать не должна ограничивать себя в питье
и в еде, т.е. по аппетиту , не насиловать
себя.
10.Мама – лучший инкубатор.
Практиковать круглосуточное нахождение
матери и новорожденного в одной палате,
что предупреждает инфицирование и
гипотермию.
38.Затруднения
и противопоказания при грудном
вскармливании.
Противопоказание
со стороны матери:
-эклампсия.
-сильные
кровотечения во время родов и в
послеродовом периоде.
-открытая форма
туберкулеза.
-состояние выраженной
декомпенсации при хронических заболеваниях
сердца, легких,
почек, печени, а также гипертиреоз.
-острые
психические
заболевания.
-особо
опасные инфекции (тиф, холера и
др.).
-герпетические
высыпания на соске молочной
железы (до их долечивания).
-ВИЧ-инфицирование
(риск заражения ребёнка 15%).
-острый
гепатит А.
- прием цитостатиков
в терапевтических дозах,
иммунносупрессивных препаратов,
антикоагулянтов типа фениндиона,
радиоизотопных контрастные вещества
для лечения или обследования, препаратов
лития, большинство противовирусных
препаратов (кроме
ацикловира, зидовудина, занамивира,
лимовудина, озельтамивира — с
осторожностью) противогельминтных
препаратов с осторожностью.
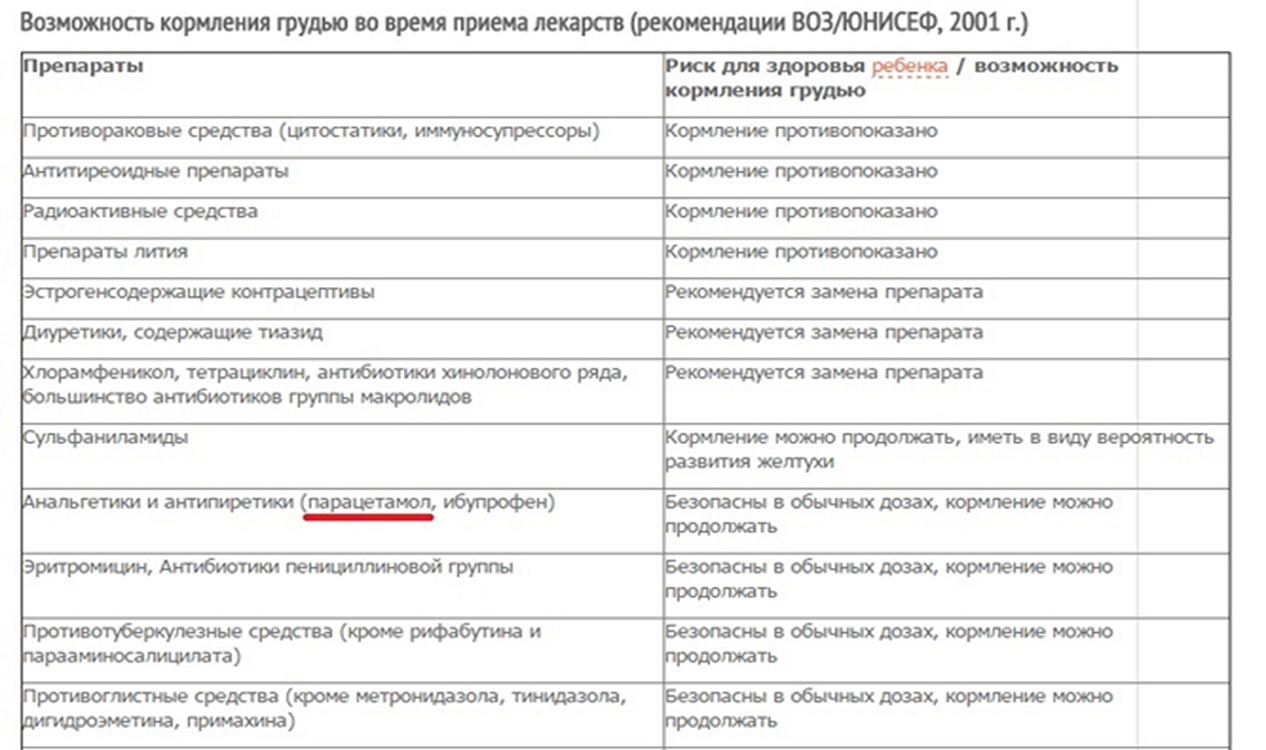 -Ветряная
оспа, корь, эпидемический паротит,
цитомегаловирусная инфекция, простой
герпес, острые кишечные и острые
респираторно-вирусные инфекции,
если они протекают без выраженной
интоксикации,
кормление грудью при соблюдении правил
общей гигиены не
противопоказано;
можно при условии введения
ребенку иммуноглобулина.
-При маститах
грудное вскармливание продолжается.
Однако оно
временно прекращается при обнаружении
массивного роста в грудном молоке
золотистого стафилококка в
количестве 250 КОЕ и более в 1 мл и единичных
колоний представителей семейства
Enterobacteriacae или вида Pseudomonas aeruginosa
(Методические рекомендации по
бактериологическому контролю грудного
молока, Москва, 1984);
-Абсцесс
молочной железы является
возможным осложнением мастита и наиболее
вероятен при резком
прерывании кормления грудью.
Кормление из
здоровой железы должно продолжаться,
а молоко из инфицированной
груди следует осторожно сцеживать и
выливать;
-Кормление
грудью во
время наступления новой беременности
может продолжаться.
Противопоказания
со стороны ребенка:
-оценка
состояния новорожденного по шкале Апгар
ниже 7 баллов при
тяжелой
асфиксии новорожденного,
-родовой
травме,
-судорогах,
-синдроме дыхательных расстройств
СДР.
- глубокая
недоношенность,
-тяжелые пороки
развития (желудочно-кишечного
тракта, челюстно-лицевого аппарата,
сердца).
Абсолютные
противопоказания
к грудному вскармливанию со стороны
ребенка очень ограничены — наследственные
энзимопатии (галактоземия
и др.).
При
фенилкетонурии
объем грудного
молока в сочетании с лечебными продуктами
устанавливается индивидуально ,
болезнь «моча с запахом кленового
сиропа».
39.Режим
и диета беременной женщины и кормящей
матери.
Режим:
здоровый сон,мало нагрузок, прогулки.
Значение полноценного,
сбалансированного питания беременной
для нормального развития плода,
благоприятного течения и исхода
беременности доказано многочисленными
исследованиями.
Кормящая
мать, наряду с правильным питанием,
нуждается в полноценном отдыхе,
ночной сон – не менее 8 ч, дневной – 1 –
2 ч, в достаточном пребывании на свежем
воздухе, спокойной обстановке дома.
Физическая нагрузка матери должна быть
умеренной, так как доказано, что сильное
утомление отрицательно сказывается на
составе грудного молока (ухудшается
качество белка, снижается количество
витаминов).
-Ветряная
оспа, корь, эпидемический паротит,
цитомегаловирусная инфекция, простой
герпес, острые кишечные и острые
респираторно-вирусные инфекции,
если они протекают без выраженной
интоксикации,
кормление грудью при соблюдении правил
общей гигиены не
противопоказано;
можно при условии введения
ребенку иммуноглобулина.
-При маститах
грудное вскармливание продолжается.
Однако оно
временно прекращается при обнаружении
массивного роста в грудном молоке
золотистого стафилококка в
количестве 250 КОЕ и более в 1 мл и единичных
колоний представителей семейства
Enterobacteriacae или вида Pseudomonas aeruginosa
(Методические рекомендации по
бактериологическому контролю грудного
молока, Москва, 1984);
-Абсцесс
молочной железы является
возможным осложнением мастита и наиболее
вероятен при резком
прерывании кормления грудью.
Кормление из
здоровой железы должно продолжаться,
а молоко из инфицированной
груди следует осторожно сцеживать и
выливать;
-Кормление
грудью во
время наступления новой беременности
может продолжаться.
Противопоказания
со стороны ребенка:
-оценка
состояния новорожденного по шкале Апгар
ниже 7 баллов при
тяжелой
асфиксии новорожденного,
-родовой
травме,
-судорогах,
-синдроме дыхательных расстройств
СДР.
- глубокая
недоношенность,
-тяжелые пороки
развития (желудочно-кишечного
тракта, челюстно-лицевого аппарата,
сердца).
Абсолютные
противопоказания
к грудному вскармливанию со стороны
ребенка очень ограничены — наследственные
энзимопатии (галактоземия
и др.).
При
фенилкетонурии
объем грудного
молока в сочетании с лечебными продуктами
устанавливается индивидуально ,
болезнь «моча с запахом кленового
сиропа».
39.Режим
и диета беременной женщины и кормящей
матери.
Режим:
здоровый сон,мало нагрузок, прогулки.
Значение полноценного,
сбалансированного питания беременной
для нормального развития плода,
благоприятного течения и исхода
беременности доказано многочисленными
исследованиями.
Кормящая
мать, наряду с правильным питанием,
нуждается в полноценном отдыхе,
ночной сон – не менее 8 ч, дневной – 1 –
2 ч, в достаточном пребывании на свежем
воздухе, спокойной обстановке дома.
Физическая нагрузка матери должна быть
умеренной, так как доказано, что сильное
утомление отрицательно сказывается на
составе грудного молока (ухудшается
качество белка, снижается количество
витаминов).
 Распределение
продуктов в течение дня:
мясо, рыба, крупы - на завтрак и обед;
молочно-растительная пища – во II половине
дня.
Калорийность: 1-й завтрак – 30%;
2-й завтрак – 15%; обед – 35%; ужин –
20%.
Исключить раздражающие вещества
– наваристые бульоны, уксус, пряности,
соленья, копчености.
Общее кол-во
жидкости - 1,2-1,5 л/день, воду, чай, кофе,
соки, супы.
Поваренная соль – до 8
г/день, при отеках, гипертонии – 5-6
г/день.
Обеспечение железом (потребность
– 15-20 мг-сут.) – блюда из печени, мяса,
яичного желтка, гречневой и овсяной
каш, свежих яблок.
Прием пищи 5-7 раз
в день.
Полноценным питание считается
тогда, когда оно обеспечивает нормальное
функционирование всех органов и систем,
как самой беременной женщины, так и
будущего ребенка. В
первой половине беременности, когда
плод еще мал, питание будущей матери не
требует особых изменений. Во
второй половине беременности важно
повысить в рационе женщины содержание
белка, кальция,
железа, пищевых волокон, витаминов и
микроэлементов и ограничить потребление
жидкости и соли. Сбалансированное
питание кормящей является основой
гармоничного роста и развития ребенка,
а также сохранения здоровья самой
матери. Питание беременной должно быть
не столько обильным, сколько полноценным.
Согласно рекомендациям института
питания РАМН, потребность
беременной женщины
(период 5 – 9 мес.) в белке
составляет 100 гр./сут.,
что на 30% выше потребности здоровой
женщины детородного возраста.
Предусматривается также увеличение
доли белка животного происхождения,
который в рационе беременной должен
составлять 60% от общего количества
белка. Потребность
беременных женщин в энергии увеличивается
до 2900 ккал, что на 400 ккал выше, чем у
здоровых женщин детородного возраста
(2500 ккал в день). Почти в 2 раза повышается
потребность в кальции. Она составляет
1500 мг в день. Потребность
в витаминах во время беременности
значительно возрастает; особенно высока
потребность в аскорбиновой кислоте,
витамине
А и фолацине.
В первую очередь, в рацион
беременной женщины
необходимо включать продукты, содержащие
полноценные белки животного происхождения,
- молоко, творог, простоквашу, кефир,
яйца и др. Из жиров используют сливочное
масло, а также различные растительные
масла. Тугоплавкие и менее полноценные
жиры (бараний, говяжий и свиное сало)
следует ограничить. Во
второй половине беременности следует
избегать
мясных и рыбных бульонов, заменяя их
овощными и молочными супами.
Мясо и рыбу лучше употреблять в вареном,
а не жареном виде.
Учитывая, что в
последние годы отмечается заметный
рост числа аллергических заболеваний
среди детей, беременной женщине
рекомендуется ограничить прием продуктов,
вызывающих аллергию (шоколад, какао,
орехи, цитрусовые, кофе, грибы).
Калорийность
суточного рациона по сравнению со второй
половиной беременности должна быть
повышена на 700-1000
ккал, так как мать расходует дополнительно
питательные вещества на образование
молока.
Средняя
ежедневная секреция молока у подавляющего
числа женщин колеблется от 850 до 1200 мл.
Кормящей.
Полноценное разнообразное питание с
исключением аллергенных продуктов,
специй и пряностей и любых алкогольных
напитков.
В зависимости от роста и
массы тела, трофологического статуса
и двигательной активности кормящая
мать должна получать
Распределение
продуктов в течение дня:
мясо, рыба, крупы - на завтрак и обед;
молочно-растительная пища – во II половине
дня.
Калорийность: 1-й завтрак – 30%;
2-й завтрак – 15%; обед – 35%; ужин –
20%.
Исключить раздражающие вещества
– наваристые бульоны, уксус, пряности,
соленья, копчености.
Общее кол-во
жидкости - 1,2-1,5 л/день, воду, чай, кофе,
соки, супы.
Поваренная соль – до 8
г/день, при отеках, гипертонии – 5-6
г/день.
Обеспечение железом (потребность
– 15-20 мг-сут.) – блюда из печени, мяса,
яичного желтка, гречневой и овсяной
каш, свежих яблок.
Прием пищи 5-7 раз
в день.
Полноценным питание считается
тогда, когда оно обеспечивает нормальное
функционирование всех органов и систем,
как самой беременной женщины, так и
будущего ребенка. В
первой половине беременности, когда
плод еще мал, питание будущей матери не
требует особых изменений. Во
второй половине беременности важно
повысить в рационе женщины содержание
белка, кальция,
железа, пищевых волокон, витаминов и
микроэлементов и ограничить потребление
жидкости и соли. Сбалансированное
питание кормящей является основой
гармоничного роста и развития ребенка,
а также сохранения здоровья самой
матери. Питание беременной должно быть
не столько обильным, сколько полноценным.
Согласно рекомендациям института
питания РАМН, потребность
беременной женщины
(период 5 – 9 мес.) в белке
составляет 100 гр./сут.,
что на 30% выше потребности здоровой
женщины детородного возраста.
Предусматривается также увеличение
доли белка животного происхождения,
который в рационе беременной должен
составлять 60% от общего количества
белка. Потребность
беременных женщин в энергии увеличивается
до 2900 ккал, что на 400 ккал выше, чем у
здоровых женщин детородного возраста
(2500 ккал в день). Почти в 2 раза повышается
потребность в кальции. Она составляет
1500 мг в день. Потребность
в витаминах во время беременности
значительно возрастает; особенно высока
потребность в аскорбиновой кислоте,
витамине
А и фолацине.
В первую очередь, в рацион
беременной женщины
необходимо включать продукты, содержащие
полноценные белки животного происхождения,
- молоко, творог, простоквашу, кефир,
яйца и др. Из жиров используют сливочное
масло, а также различные растительные
масла. Тугоплавкие и менее полноценные
жиры (бараний, говяжий и свиное сало)
следует ограничить. Во
второй половине беременности следует
избегать
мясных и рыбных бульонов, заменяя их
овощными и молочными супами.
Мясо и рыбу лучше употреблять в вареном,
а не жареном виде.
Учитывая, что в
последние годы отмечается заметный
рост числа аллергических заболеваний
среди детей, беременной женщине
рекомендуется ограничить прием продуктов,
вызывающих аллергию (шоколад, какао,
орехи, цитрусовые, кофе, грибы).
Калорийность
суточного рациона по сравнению со второй
половиной беременности должна быть
повышена на 700-1000
ккал, так как мать расходует дополнительно
питательные вещества на образование
молока.
Средняя
ежедневная секреция молока у подавляющего
числа женщин колеблется от 850 до 1200 мл.
Кормящей.
Полноценное разнообразное питание с
исключением аллергенных продуктов,
специй и пряностей и любых алкогольных
напитков.
В зависимости от роста и
массы тела, трофологического статуса
и двигательной активности кормящая
мать должна получать
110-140 г/сут белка,
80-110 г/сут жиров,
325-450 г/сут углеводов.
Общая энергоценность суточного рациона составляет 2500-3200 ккал При недостаточной лактации дополнительно: гол. сыр – 100 г, сметана – 10 г, сок черной смородины – 100 г, грецкие орехи – 5-6 шт., жидкие пивные дрожжи. Ежедневно кормящая женщина должна получать: мяса или рыбы - 200 г; молока или кефира - до 1 литра; творога - 100-200 г; яиц - 1 шт.; растительного масла - 30 г; сливочного масла - 30 г; хлеба - 200 г; круп и макарон - 50-60 г; картофеля и др.овощей - 500 г; фруктов и ягод - 200-500 г.
-Питьевой режим: не менее 1000 мл жидкости (чай, молоко,соки, напитки и др.) -Обогащение суточного рациона кормящей женщины за счет включения например питательной смеси «Мама и Я» («Нестле») по 100-150 г в сутки в течение первых 2-3 месяцев кормления грудью или в течение всего времени кормления, приходящегося на зимне-весенний период года. -Учитывая дополнительные высокие потребности организма кормящей матери в витаминах, должны назначаться поливитаминные комплексы (1 драже «Гендевит», 1 таблетка «Маттерна» или 30 г «Гравинова гранулят» и др.).
Число приемов пищи = число кормлений. За ½ ч до кормления –прием сладких фруктов, чая, молока. Учитывая содержание белка в молоке, можно считать, что кормилица ежедневно выделяет около 15,0 г белков. На выработку 1,0 г белка грудного молока требуется около 2,0 г белка пищи. Поэтому содержание белка в пищевом рационе кормящей грудью, должен быть повышен примерно на 30-40 г и составлять не менее 110-120 г. Несколько увеличивается и суточная потребность кормящей грудью в жирах (до 120 г), углеводах (до 500-520 г).Питание нес-ко раз в день.Суточная потребность кормящей в витаминах и микроэлементах в среднем составляет: 2,5 мг витамина А, 2,5 мг витамина B1, 3,5 мг витамина В6, 120 мг витамина С, 25 мг витамина РР, 4 мг витамина B, 500 М.О. витамина D, 1,8-2,0 г кальция, 3,8 г фосфора, 1,25 г магния. Количество жидкости в суточном рационе матери не должно превышать 2 л (с учетом супа, молока, кефира, соков, чая и т.п.), так как при чрезмерном употреблении жидкости может ухудшиться качество молока: уменьшится содержание белка, жира, витаминов, минеральных веществ. Также следует избегать употребления избыточных количеств пряностей, экстрактивных веществ и продуктов с сильным запахом (чеснок), так как это может придать молоку неприятный привкус и запах. Следует также ограничить в диете такие продукты, как шоколад, какао, цитрусовые, мед, орехи, которые могут вызвать у ребенка аллергические реакции. Так, отделение молока несколько улучшается, если за 10 – 15 мин до кормления ребенка выпить стакан чая с молоком, отвар шиповника или компот. Благоприятное воздействие на лактационную способность женщины оказывает также УФО-облучение молочных желез, что одновременно является мерой профилактики трещин сосков. При наличии болезненных трещин сосков иногда снижается количество грудного молока. Поэтому очень важно своевременно обеспечить их профилактику и лечение. При образовании трещин сосков необходимо смазывать 1 % спиртовым раствором бриллиантовой зелени 2 – 3 раза в день. Можно применять также различные мази, в состав которых входят анестезин, витамин А, дезинфицирующие средства. В тяжелых случаях приходится прервать прикладывание ребенка к груди на 12 – 4 ч, сцеживая молоко или кормить ребенка через накладку. Потери железа из организма матери с молоком во время грудного вскармливания меньше, чем потери при менструации. Таким образом, грудное вскармливание помогает предупредить анемию, и страдающим анемией матерям следует рекомендовать продолжать кормление грудью. 40.Диагностика и лечение гипогалактии. Гипоголактия — сниженная секреторная деятельность молочных желез в период лактации. Чаще всего она развивается в случае нарушении техники кормления ребенка (недостаточное опорожнение грудных желез, жесткое повременное регламентирование режима кормления новорожденных, ограничение числа кормлений и т. п.) или погрешностей в диете, переутомления, недосыпания, отрицательных эмоций, заболеваний матери. Важную роль играет отсутствие у женщины и членов ее семьи мотивации к кормлению своего ребенка грудью, основанной на четком представлении о безусловном преимуществе грудного вскармливания перед искусственным, а также твердого психологического настроя на длительное естественное вскармливание. Гипогалактии бывают ранние (в первые 10 дней после родов) и поздние. В зависимости от дефицита молока по отношению к суточной потребности ребенка выделяют четыре степени гипогалактии: I — дефицит суточной секреции не выше 25%; II - до 50%; III - до 75%; IV - свыше 75%. Диагностика: При подозрении на гипогалактию следует провести не менее чем трехкратное контрольное кормление с точным учетом высосанного молока. При своевременном устранении причин возникновения гипогалактии и рациональном лечении можно восстановить лактацию. Для оценки уровня лактогенеза проводится контрольное взвешивание малыша в течение суток до и после кормления, после чего полученные данные и разницу в весе суммируют с количеством сцеженного молока. УЗИ груди. Сонографическое исследование позволяет оценить структуру молочной железы, развитость паренхимы, выявить возможные очаговые и инволютивные изменения. Обнаружение во время УЗИ очаговой патологии молочных желез является основанием для назначения маммографии и цитологического исследования материала, полученного методом пункционной биопсии. Гормональные исследования. Наибольшее диагностическое значение при гипогалактии играет определение концентрации в крови пролактина, эстрадиола, прогестерона, ФСГ, ЛГ. В лечении гипогалактии важно соблюдение женщиной режима дня (особенно необходим достаточный сон — 8—10 часов в сутки), рациональное разнообразное питание с обязательным включением в диету молока в объеме не менее литра или кисломолочных продуктов, психотерапия. Применяют медикаментозные средства: никотиновую кислоту (0,05 г 3 раза в день за 20—30 мин до кормления, лучше в сочетании с витаминами С, В,, В2, В6); апилак 0,01 г под язык, 2—3 раза в день в течение 15 дней; витамин Е по 0,01 — 0,015 г 2 раза в день; аскорбиновую кислоту по 1 г 2 раза в день; глютаминовую кислоту по 0,5 г 3 раза в день. Лактопоэтическим эффектом обладает пирроксан. Его назначают по 0,015 г 2 раза в сутки внутрь курсом на 5—7 дней. Неплохой эффект оказывает фитотерапия: отвар крапивы, экстракты чистеца и боярышника, настой из семян укропа, тминный напиток, свежеотжатый морковный сок и т. д. Крайне важно соблюдать режим и тщательно сцеживать молоко после кормления. Показано У Ф О молочных желез. Профилактику гипогалактии назначают еще во время беременности: рациональное питание и отдых, подготовка грудной железы и сосков, психотерапия и др. Существует понятие «периконцепционная» профилактика и диетология. Имеется в виду то, что для поддержания нормальной лактации и, что также очень важно, оптимального состава грудного молока необходимо, чтобы уже к моменту планируемой беременности состояние питания женщины было вполне удовлетворительным, она не имела признаков тех или иных пищевых дефицитов. Питание беременной, а затем и кормящей женщины должно быть также адекватным и мультисбалансированным. В современных условиях важным мероприятием диетологической поддержки женщины к моменту зачатия, во время беременности и кормления грудью является применение специальных молочных смесей — нутрицевтиков типа «Энфамама» (фирма «МидДжонсон»), «Думил Мама плюс» (фирма «Данон»), «Фемилак-1» и «Фемилак-2» (фирма «Нутритек-Нутриция»), а иногда и сапплементов с витаминами или солями и микроэлементами. 41.Особенности вскармливания новорожденных и недоношенных детей. Вскармливание недоношенных детей (энтеральное питание).Определенные трудности, возникающие при кормлении недоношенных детей, связаны с их физиологической незрелостью: 1) Способность к сосанию и глотанию, координация этих рефлексов не развиты до 32-34 нед.; 2) малый объем желудка и удлинении времени эвакуации его содержимого при несформированном нижнем пищеводном сфинктере приводят к склонности к срыгиванию; 3) способность кислотообразования и продукция пепсиногена в желудке низкая; 4) снижена перстальтика киш-ка, что приводит к вздутию живота, перерастяжению киш-ка; 5) снижена активность лактазы; 6) всасывание жиров низкая из-за пониженной продукции солей желчных кислот и панкреатической липазы, сниженной способности образования мицелл; 7) расщепление белков неполное; 8) секреция иммуноглобулинов в киш-ке и иммунологический ответ снижены; 9) уровень клеточной пролиферации и миграции в стенке киш-ка низкий; 10) снижение функциональной активности органов (печень - незрелость ферментов, почки - снижена способность сохранять важные электролиты, как натрий и хлориды, легкие - продолжается созревание легочной ткани), что требует дополнительных затрат энергии. В связи с этим предлагают в питание таких детей добавлять (одновременно с грудным молоком) смеси-фортификаторы, например Enfamil H M F (Mead Johnson), Similac Natural Care (Ross), Care Neonatal BMF (Nutriсіа), которые коррегируют состав женского молока, делают его состав более оптимальным для маловесных детей. Это позволяет сохранить основные преимущества и защитные свойства естественного вскармливания маловесного ребенка и дать ему возможность интенсивно развиваться. Первое кормление - зависит от гестационного возраста, массы тела и состояния здоровья. В случае отсутствия соматической патологии энтеральное питание начинают с первых суток, расчет идет по разным методам: 1) Гестационный возраст больше 33-34 нед, при массе тела больше 2,5 кг. При наличии достаточной силе сосательных движений, координации сосания и глотания, достаточной моторике киш-ка первое кормление начинают через 2-3 час после рождения грудью или сцеженным молоком ч-з соску. 2) Гестационный возраст меньше 33-34 нед, при массе тела меньше 2 кг. Принцип: осторожность и постепенность! Первое пробное введение пищи в виде дистиллированной воды, если все нормально (не было срыгивания и ухудшения состояния ребенка) то 2 и 3 кормление проводят 5% глюкозой с постепенным увеличением объема, далее кормят молоком или смесью; при массе 1,5-2 кг объем первого кормления дистиллированной водой 5-7 мл, далее увеличивают объем кормления ч-з 3 часа с возможным ночным перерывом для детей больше 2 кг. В мировой литературе приводится очень большой диапазон начального объема трофического питания от 0.1 до 20мл\кг\день, чаще 10-14 мл\кг\день. Вскармливание в этом объеме продолжается от 7 до 14 дней, затем медленно увеличивают концентрацию и объем смеси. При массе тела 1-1.5 кг объем первого кормления 2-4 мл и далее постепенно увеличивают на 3-5 мл, интервал м-ду кормлениями 3 час без ночного перерыва, т.о. 8-10 кормлений. При массе менее 1000 г объем первого кормления 1 мл и далее постепенно увеличивают на 1 мл в течении 8 час, далее интервал 2 часа и увеличение объема на 2 мл , пока не достигается объем 12 мл (5% глюкоза). Перевод на грудное вскармливание только через 16-48 час ч-з соску, а если масса меньше 700 г через зонд Режим кормления ч-з зонд м.б. прерывистым и продолженным (капельным, микроструйным). При болюсном введении молока зонд используют для доставки разовой порции молока после кормления сразу удаляют ( обычно каждые 3 час). Зонд вводят на длину, равную расстоянию от переносицы до мечевидного отростка, что составляет 1012 см. На свободном конце имеется отверстие для ввода шприца с молоком, молоко д б теплым. Орогастральное введение зонда предпочтительнее, чем назогастральное, т. К. м. б. апноэ. Разовое введение зонда приводит к циклическому выбросу гормонов, и это стимулирует рост и развитие ЖКТ. Детям весом менее 1500г вводят постоянный зонд, т к есть тенденция к застою кишечного содержимого. Такой зонд находится в желудке 7-10 дней, молоко вводится и капельно с заданной скоростью при помощи инфузомата, некоторые исследования показывают, что при капельном введении прибавка в весе больше. Необходимо отсасывать содержимое желудка при каждом следующем кормлении, если при этом получают 10% от предыдущего кормления следует уменьшить дозу молока, в случае наличия патологических примесей энтеральное кормление прекращают. Срыгивание, рвота, вздутие живота служит показанием для отмены стандартной схемы вскармливания до выяснения причин, их вызвавших. При появлении сосательных движений возможно перевести на соску. Потребности в нутриентах: белки -составляет 3.5-4 г\кг\день, для поддержания роста необходимо 9-12 % от общей калорийности. Для поддержания иммунной системы орг-ма необходимы нуклеотиды, смеси. Содержащие нуклеотиды продолжают разрабатываться. Углеводы -у недоношенных есть транзиторное затруднение усвоение лактозы, объем от общего суточного каллоража д б 35-55%. Жиры -должны составлять 40-55% от общего суточного аклоража. В смеси для недоношенных обязательно входит омега-3 жирная кислота, присутствующая в женском молоке и линолевая кислота. Витамины и минералы -быстрый рост недоношенных детей требует в первую очередь повышенного содержания кальция, фосфора, а также вит Д для оптимальной минерализации костей. Недоношенные дети способны абсорбировать вит Д и преобразовывать его в активную форму (1,25 гидроксихолекальциферол). Ежедневное введение 400 МЕ вит Д достаточно для большинства детей, хотя рекомендуемый диапазон от 400 до 800 МЕ. Дополнительно надо давать кальций - 50 мг\кг\день, фосфор - 30 мг\кг\день (если ребенок получает только грудное молоко). Дополнительное введение железа для детей на грудном вскармливании, так и у детей на смеси должно начинаться с 2 мес по 2 мг\кг\день с предварительным насыщением орг-ма вит Е (внутрь 25 МЕ\кг\день с началом полного энтерального питания). Рекомендуемая доза фолиевой к-ты от 50 до 70 мкг\день. Появились белково-витаминные добавки к грудному молоку: «Пре-Сэмп протеин и минерал», разработанный для детей с массой при рождении менее 1500 гр. Применяется с первых месяцев жизни и до достижения ребенком массы тела 2000-2500 г. Расчет питания для недоношенных. Расчет питания производится на массу тела при рождении, и только с начало нарастания производится на существующую массу тела. Формула Малышевой до 10 дня: Сут объем = 14×М ( кг) × дни жизни. Объем 1 кормления = 3× М тела × дни жизни, расчет у детей с физической потерей массы на массу при рождении, до того как не стал набирать. После 10-го дня «калорийный метод». На каждый день жизни прибавляют по 10 ккал (1 день - 10 ккал + 2-ой день 10 ккал и т.д. до 10 дня, т.о. в 10 дней 100 кал; на 14 день – 120 ккал\кг\сут; 21 день- 130 ккал\кг\сут; 1 мес – 135-140 ккал\кг\сут; 2 мес - в зависимости от массы при рождении, если масса ≥ 1.5 кг , то 130 ккал\кг\сут или чуть меньше, если масса при рождении ≤ 1.5 кг, то 135-140 ккал\кг\сут, такой расчет делают до 3-го мес включительно, с 4-го мес уменьшают до 130 ккал\кг\сут, 130ккал\кг\сут принято считать у детей с ЭНМТ, у более старших детей – 120 ккал\кг\сут. При невозможности питания через рот (из-за состояния здоровья, при срыгиваниях, в первые часы и дни жизни у детей, с очень маленькой и эстремально низкой массой тела) младенцы получают питательные растворы внутривенно( растворы глюкозы, аминокислот, липидов) – так называемое “парентеральное питание”, которое обеспечивает организм самыми важными компонентами для обеспечения жизнедеятельности. 42.Основные критерии для оценки правильного вскармливания здорового ребенка. Отнятие ребенка от груди. Оценка эффективности питания проводится по ряду клинических параметров, из которых показательными являются клинико-морфологические: общий статус ребенка, динамика роста и массы тела, нервно-психическое развитие, заболеваемость, лабораторные данные. При клинической оценке общего статуса ребенка учитывается общее состояние, эмоциональный тонус, развитие статических и локомотивных функций, состояние кожи и слизистых, тургор тканей, развитие подкожно-жирового слоя, мышечной и костной систем, функционального состояния желудочно-кишечного тракта и других органов. Для оценки гармоничности развития- антропометрическими индексами. Например, индекс Тура вычисляется по соотношению окружности груди и окружности головы. При рождении у здорового ребенка окружность груди меньше окружности головы на 1-2 см, к 2-3 месяцам эти величины сравниваются, и после 3-х месяцев наступает перекрест. К году окружность груди становится больше окружности головы на 1,5-2 см. Из лабораторных анализов, которые могут служить критериями эффективного питания, наибольшее значение имеет клинический анализ крови, определение общего белка сыворотки крови и его фракций. Для оценки реакции ребенка на характер вскармливания можно использовать и копролограмму. Обнаружение в кале мышечных волокон, большого количества непереваренной клетчатки, крахмала, нейтрального жира, жирных кислот свидетельствует о несоответствии пищи функциональным возможностям желудочно-кишечного тракта ребенка. Клинически это проявляется снижением аппетита, срыгиванием, диспептическими расстройствами. Иследования функции мочевыделительной системы. Высокое содержание солей в моче, продуктов азотистого обмена, высокий уровень осмомерности говорит о повышенной нагрузке на почки ребенка в результате избыточного содержания в рационе солей и азота. Частота заболеваемости детей, особенно острыми респираторными и кишечными заболеваниями, так как при неправильном питании снижается иммунитет и уменьшается сопротивляемость детского организма. Правила отнятия от груди:
Рекомендуемый возраст ребенка – старше 1 года.
При правильной организации питания к 1 году грудное молоко уже теряет свою значимость как источник питания, его количество в сточном рационе ребенка составляет не более 200-300 мл и сложности отнятия от груди связаны только с психологической зависимостью ребенка от процесса кормления (защита, положительные эмоции, сон).
Не отнимать от груди ребенка, находящегося в стрессовом состоянии: во время болезни, проведении профилактических прививок, если предстоит длительная поездка (в поезде, например), смена обстановки и окружения ребенка, в жаркое время года (молок продолжает оставаться для ребенка источником жидкости), в первые недели пребывания ребёнка в ДДУ.
При значительном количестве молока женщине рекомендуется уменьшить количество жидкости в рационе, тугое бинтование молочной железы.
Нежелательно длительное сохранение грудного вскармливания (у детей старше 3 лет), т.к. это затрудняет процесс социализации личности ребенка, развития самостоятельности.
Сокращайте количество дневных кормлений постепенно, вводя прикорм.
Приучите ребенка засыпать днем, не прикладывая его к груди. Постепенное отнятие ребенка от груди. Этот способ хотя и длительный, но наиболее щадящий для психики и здоровья мамы и малыша. Его суть состоит в последовательном прекращении сначала дневных кормлений, затем утренних и вечерних, а после – ночных.
Необходим более частый физический и психологический контакт мамы с малышом, чтобы после отнятия от груди ребенок не чувствовал себя брошенным. Это могут быть поглаживания, прижатие к себе, усаживание на колени, совместный просмотр книг, игры и прочие взаимодействия.
Как узнать готов ли ребенок к отлучению или нет? -Ребенку больше 1,5 лет и у него прорезались основные молочные зубы. -Ребенок хорошо ест твердую пищу, и его дневной рацион включает три основных приема пищи и пару перекусов у груди. - Ребенок не сильно протестует, когда мать отказывается дать ему грудь. Он успокаивается при попытке отвлечь и занять его чем-нибудь другим. Если же, ребенок проявляет большое беспокойство, плачет и не соглашается на ваши предложения, значит он еще не готов к отлучению. -Мать кормит ребенка грудью не чаще 3-4 раз в сутки. Если чаще, тогда необходимо уменьшить количество кормлений в день, и только потом приступать к отлучению. - Ребенок умеет засыпать без прикладывания к груди.
43.Прикормы и сроки их назначения при естественном вскармливании. Сроки введения в рацион ребенка пищевых добавок и прикормов очень индивидуальны и зависят:
Характера вскармливания – на грудном вскармливании они вводятся позже, на искусственном раньше.
Характера лактации и темпов физического развития ребенка – если лактация достаточная, ребенок хорошо растет и развивается, то добавки и прикормы вводят не раньше 6 месяцев (коррекция питания через материнское молоко).
Времени года и климатической зоны проживания – осенью и зимой, в северных широтах сбалансированное питание кормящей женщины не всегда возможно и приходится вести коррекцию питания ребенка, раньше вводя пищевые добавки и прикормы.
Состояния здоровья, режима питания и дня кормящей женщины и состояния здоровья ребенка.
Готовности ребенка к усвоению качественно новой пищи: угасание рефлекса «выталкивания» пищи (языком) при хорошо скоординированном рефлексе проглатывания; готовность ребёнка к жевательным движениям при попадании в рот соски или других предметов, состоявшееся или текущее прорезывание зубов.
Наличие признаков относительной недостаточности питания: уменьшение подкожно-жирового слоя, замедление прироста массы тела.
Различают такие витаминные и белковые добавки, как: с 4 месяцев. Фруктовые соки (пюре) - яблочный, из белой черешни, из белой смородины, абрикосовый, персиковый, грушевый, сливовый (даны в порядке предпочтения). Начинают вводить в рацион с капель, постепенно увеличивая количество до 40-60 мл. Желательно чтобы первые соки ребенка были натуральными и свежими (домашнего приготовления). Творог (кальцинированный) так же желателен домашнего приготовления - на 200 мл молока в момент закипания добавляется 1-2 столовые ложки СаСl2, затем откидывается на марлю, или молочной кухни, специального детского питания. Начинают вводить в рацион с крупинок и доводят до 40 грамм в сутки. Яичный желток вкрутую сваренного яйца. С крупинок до 1/12 – 1/8 добавляют в молоко или овощное пюре (с осторожностью вводить в рацион аллергиков). Прикорм – это качественно новый вид питания ребенка, который полностью заменяет одно из кормлений и дается до прикладывания к груди или дачи молочной смеси. Первый прикорм в 5-6 мес.: Чаще в качестве первого прикорма используют овощное пюре (картофель, капуста, кабачок, тыква, и в последнюю очередь морковь). Начинают с 1 – 2 чайных ложек и постепенно в течение 1- 2 недель заменяют полностью 1 кормление (это примерно 150 мл). Далее 2 -3 недели не вводя ничего нового – период адаптации. Второй прикорм в 6-7 мес.: 5% кашу (с 8 месяцев - 10%); (рисовая, манная, гречневая, кукурузная) с добавлением 5 г сливочного масла, яичного желтка. В 6-7 мес. Вводится также мясной бульон (используют для разведения овощного пюре), затем мясо говядины, телятины в виде фарша. Через месяц вводят второй прикорм – кашу (предпочтительнее начинать с безглютеновых злаков – рис, кукурузная, гречневая мука). Наиболее удобны сухие растворимые каши: они обогащены витаминами, кальцием, железом, имеют гарантированный состав и безопасность. У детей с хорошим весом прикормы начинают с овощей, при дефиците веса первым прикормом становится каша. В овощное пюре обычно вводится 5мл растительного масла (желательно чередовать подсолнечное, оливковое, кукурузное), а в кашу сливочное. Мясо отварное (телятина, кролик, индейка) дважды пропускается через мясорубку и дается ребенку, начиная с 1 чайной ложки, постепенно доведя количество до 60-80 грамм в сутки, обычно в третье кормление. С момента введения первого прикорма ребенок переходит на 5-ти разовое питание. Прикормы необходимо разделять кормлениями грудью, обычно первое, третье и последнее кормление – грудное молоко или молочная смесь, второе – каша, а четвертое – овощи. Третий прикорм в 7-8 мес.: неадаптированные молочные продукты: молоко, кефир, йогурты и полностью грудным остается только первое и последнее кормление. С 9-10 мес. - «кусочковое» питание. С 10-11 мес. - нежирные сорта рыбы не чаще 2-х раз в неделю. 44.Прикормы и сроки их назначения при искусственном вскармливании. Перед введением прикорма убедитесь, что организм ребенка готов к нему. Признаки, на которые нужно обратить внимание:
зрелость желудочно-кишечного тракта;
ослабление рефлекса выталкивания твердой пищи;
готовность ребенка к жевательному процессу — появление первых зубов;
способность младенца устойчиво находиться в сидячем положении;
эмоциональная готовность малыша к знакомству с новыми вкусовыми ощущениями.
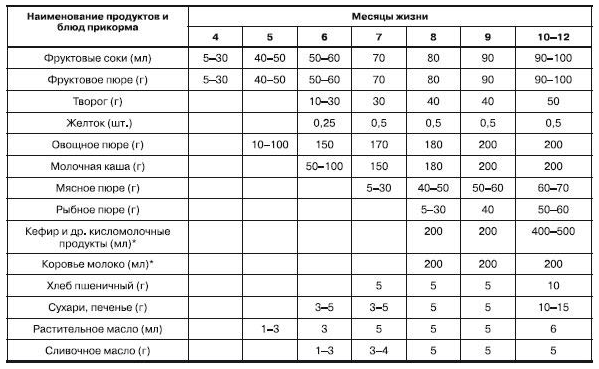 Введение
прикорма детям как на грудном, так и на
искусственном вскармливании рекомендовано
начинать в возрасте 4–6 мес. Прикорм
вводится на 2-4 недели раньше, чем при
естественном вскармливании.
Различают
такие витаминные
и белковые добавки,
как: с 3 месяцев.
Фруктовые соки и пюре следует назначать
с 3 и 3,5 месяцев, соответственно. Допустимо
и более раннее (с 1,5 месяца) введение
соков с учетом их индивидуальной
переносимости.
Творог
(кальцинированный) так же желателен
домашнего приготовления -
на 200 мл молока в момент закипания
добавляется 1-2 столовые ложки СаСl2,
затем откидывается на марлю, или молочной
кухни, специального детского питания.
Начинают вводить в рацион с крупинок и
доводят до 40 грамм в сутки.
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков).
Это обусловлено
тем, что дети
уже получают в составе заменителей
женского молока значительное количество
«чужеродных» пищевых продуктов:
коровье молоко, сладкие сиропы,
растительные масла, содержащие достаточно
большое количество
новых пищевых веществ
— белков, олигосахаридов, липидов,
отличных по строению от этих ингредиентов
женского молока. Таким образом, дети в
известной степени адаптированы к
«чужеродному» питанию.
Первый
прикорм (овощное
пюре) при искусственном вскармливании
вводят в рацион с 4,5—5 месяцев, второй
прикорм (на злаковой
основе) — с 5,5—6 месяцев. Однако с учетом
индивидуальных особенностей развития,
так же как и при естественном вскармливании,
в качестве первого прикорма могут быть
использованы и каши, лучше — обогащенные
железом, витаминами, микроэлементами.
Желток целесообразно использовать
с возраста 6 месяцев, мясо — с
7 месяцев.
Кефир,
другие кисломолочные продукты и цельное
коровье молоко в качестве блюд прикорма
можно вводить в питание с 8
месяцев, однако и
у этих детей препочтительнее использовать
«последующие» формулы.
45.Методы
определения объема пищи грудному
ребенку.
Один
из главных показателей достаточности
ребенку грудного молока — его поведение.
Если после очередного кормления малыш
спокойно отпускает грудь, имеет довольный
вид, имеет достаточный сон до следующего
кормления, значит, молока ему хватает.
Объективными признаками
адекватного объема молока являются
равномерные, в соответствии с возрастными
нормами, прибавки в массе тела, увеличение
других антропометрических показателей
(длина тела, окружность головы), хорошее
состояние кожи, упругий тургор мягких
тканей, нормальная кратность мочеиспусканий
и стула.
Введение
прикорма детям как на грудном, так и на
искусственном вскармливании рекомендовано
начинать в возрасте 4–6 мес. Прикорм
вводится на 2-4 недели раньше, чем при
естественном вскармливании.
Различают
такие витаминные
и белковые добавки,
как: с 3 месяцев.
Фруктовые соки и пюре следует назначать
с 3 и 3,5 месяцев, соответственно. Допустимо
и более раннее (с 1,5 месяца) введение
соков с учетом их индивидуальной
переносимости.
Творог
(кальцинированный) так же желателен
домашнего приготовления -
на 200 мл молока в момент закипания
добавляется 1-2 столовые ложки СаСl2,
затем откидывается на марлю, или молочной
кухни, специального детского питания.
Начинают вводить в рацион с крупинок и
доводят до 40 грамм в сутки.
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков).
Это обусловлено
тем, что дети
уже получают в составе заменителей
женского молока значительное количество
«чужеродных» пищевых продуктов:
коровье молоко, сладкие сиропы,
растительные масла, содержащие достаточно
большое количество
новых пищевых веществ
— белков, олигосахаридов, липидов,
отличных по строению от этих ингредиентов
женского молока. Таким образом, дети в
известной степени адаптированы к
«чужеродному» питанию.
Первый
прикорм (овощное
пюре) при искусственном вскармливании
вводят в рацион с 4,5—5 месяцев, второй
прикорм (на злаковой
основе) — с 5,5—6 месяцев. Однако с учетом
индивидуальных особенностей развития,
так же как и при естественном вскармливании,
в качестве первого прикорма могут быть
использованы и каши, лучше — обогащенные
железом, витаминами, микроэлементами.
Желток целесообразно использовать
с возраста 6 месяцев, мясо — с
7 месяцев.
Кефир,
другие кисломолочные продукты и цельное
коровье молоко в качестве блюд прикорма
можно вводить в питание с 8
месяцев, однако и
у этих детей препочтительнее использовать
«последующие» формулы.
45.Методы
определения объема пищи грудному
ребенку.
Один
из главных показателей достаточности
ребенку грудного молока — его поведение.
Если после очередного кормления малыш
спокойно отпускает грудь, имеет довольный
вид, имеет достаточный сон до следующего
кормления, значит, молока ему хватает.
Объективными признаками
адекватного объема молока являются
равномерные, в соответствии с возрастными
нормами, прибавки в массе тела, увеличение
других антропометрических показателей
(длина тела, окружность головы), хорошее
состояние кожи, упругий тургор мягких
тканей, нормальная кратность мочеиспусканий
и стула.
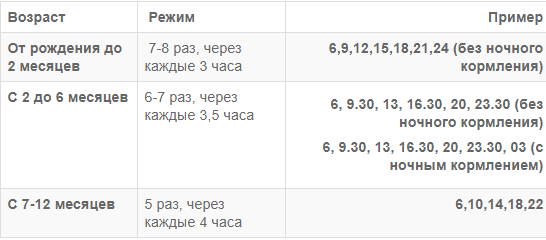 В
первые 10 дней жизни
необходимое количество молока для
доношенного ребенка можно определить
по формулам :
• Формула
Финкельштейна в
модификации А. Ф. Тура: при расчете
учитывается масса
тела ребенка при
рождении: если
масса тела 3200 г и менее, то коэффициент
– 70 (мл), если
масса тела при рождении
более 3200 г - коэффициент 80 (мл).
Объем
молока в (мл) V=
коэффициент (70-80) × n (где n — число дней
жизни ребенка).
В периоде
новорожденности рекомендуется 7 кормлений
в сутки (перерыв между кормлениями 3,5—3
часа, ночной перерыв — 6,5—6 часов). В
возрасте от 2 до 5
месяцев — 6
кормлений (перерыв
между кормлениями 3,5 часа, ночной перерыв
6,5-7 часов), от 5 до
12 месяцев — 5
кормлений (перерыв
между кормлениями 4 часа, ночной
перерыв — 8 часов). Первое кормление
начинается в 6.00.
(Пример 1: Рассчитать
суточный и разовый объем пищи ребенка
7 дней с массой тела при рождении 3 800
г.
Ответ:
Суточный
объем: 80 (мл) × 7
= 560 мл.
Для
определения объема
разового кормления,
необходимо: суточный объем разделить
на число кормлений. Например, 560 мл :
7(раз) = 80 мл.)
•
Формула Н. П.
Шабалова:
Количество
молока на 1 кормление (мл)
= 3 мл х день жизни х массу тела (кг);
•
Формула Н. Ф. Филатова
в модификации Г. И. Зайцевой:
метод используется главным образом при
расчете суточного объема пищи для детей,
которые имеют
вес при рождении более 4 кг.
Количество
молока в сутки (мл)
= 2% массы тела х день жизни.
(Пример:
Рассчитать суточный объем пищи ребенку
8 дней с массой тела при рождении 4 200
г.
Ответ: 2% от массы = (4 200 (г) × 2):100% = 84
г
объем пищи за сутки = 84 (г) × 8 = 672 (мл)
= 670 мл.)
Начиная
с 10-го дня жизни (2 недели)
суточное количество молока вычисляют
двумя способами:
• «Объемный»
способ по
Гейбнер-Черни. Объем пищи назначается
в зависимости от возраста и массы тела.
При этом масса тела должна соответствовать
средним возрастным нормам.
Суточное
количество пищи составляет:
в возрасте от 10 дней (2 недели) до 1,5
месяцев (6 недель) — 1/5 часть фактической
массы тела;
в возрасте 1,5 (6 недель)
-4 месяцев - 1/6 часть
от долженствующей массы тела;
в
возрасте 4- 6 месяцев - 1/7 часть
от долженствующей массы тела;
в
возрасте старше 6 месяцев - 1/8 массы тела.
Метод
используют до 9 месяцев.
После 9 месяцев – 1 литр так, как объем
пищи на первом году жизни не должен
превышать 1 литра в сутки.
(Пример:
Рассчитать суточный
и разовый
объем пищи ребенка 3-х мес., родившегося
с массой тела 3 200 г.
Ответ: 1. долженствующая
масса – 3200 + 600 +
800 + 800 = 5 400
г.
2. суточный
объем пищи - 5
400 : 6 = 900 (мл)
3.
количество кормлений – 6
раз
4. разовый
объем – 900 мл :
6 = 150 мл.)
В
первые 10 дней жизни
необходимое количество молока для
доношенного ребенка можно определить
по формулам :
• Формула
Финкельштейна в
модификации А. Ф. Тура: при расчете
учитывается масса
тела ребенка при
рождении: если
масса тела 3200 г и менее, то коэффициент
– 70 (мл), если
масса тела при рождении
более 3200 г - коэффициент 80 (мл).
Объем
молока в (мл) V=
коэффициент (70-80) × n (где n — число дней
жизни ребенка).
В периоде
новорожденности рекомендуется 7 кормлений
в сутки (перерыв между кормлениями 3,5—3
часа, ночной перерыв — 6,5—6 часов). В
возрасте от 2 до 5
месяцев — 6
кормлений (перерыв
между кормлениями 3,5 часа, ночной перерыв
6,5-7 часов), от 5 до
12 месяцев — 5
кормлений (перерыв
между кормлениями 4 часа, ночной
перерыв — 8 часов). Первое кормление
начинается в 6.00.
(Пример 1: Рассчитать
суточный и разовый объем пищи ребенка
7 дней с массой тела при рождении 3 800
г.
Ответ:
Суточный
объем: 80 (мл) × 7
= 560 мл.
Для
определения объема
разового кормления,
необходимо: суточный объем разделить
на число кормлений. Например, 560 мл :
7(раз) = 80 мл.)
•
Формула Н. П.
Шабалова:
Количество
молока на 1 кормление (мл)
= 3 мл х день жизни х массу тела (кг);
•
Формула Н. Ф. Филатова
в модификации Г. И. Зайцевой:
метод используется главным образом при
расчете суточного объема пищи для детей,
которые имеют
вес при рождении более 4 кг.
Количество
молока в сутки (мл)
= 2% массы тела х день жизни.
(Пример:
Рассчитать суточный объем пищи ребенку
8 дней с массой тела при рождении 4 200
г.
Ответ: 2% от массы = (4 200 (г) × 2):100% = 84
г
объем пищи за сутки = 84 (г) × 8 = 672 (мл)
= 670 мл.)
Начиная
с 10-го дня жизни (2 недели)
суточное количество молока вычисляют
двумя способами:
• «Объемный»
способ по
Гейбнер-Черни. Объем пищи назначается
в зависимости от возраста и массы тела.
При этом масса тела должна соответствовать
средним возрастным нормам.
Суточное
количество пищи составляет:
в возрасте от 10 дней (2 недели) до 1,5
месяцев (6 недель) — 1/5 часть фактической
массы тела;
в возрасте 1,5 (6 недель)
-4 месяцев - 1/6 часть
от долженствующей массы тела;
в
возрасте 4- 6 месяцев - 1/7 часть
от долженствующей массы тела;
в
возрасте старше 6 месяцев - 1/8 массы тела.
Метод
используют до 9 месяцев.
После 9 месяцев – 1 литр так, как объем
пищи на первом году жизни не должен
превышать 1 литра в сутки.
(Пример:
Рассчитать суточный
и разовый
объем пищи ребенка 3-х мес., родившегося
с массой тела 3 200 г.
Ответ: 1. долженствующая
масса – 3200 + 600 +
800 + 800 = 5 400
г.
2. суточный
объем пищи - 5
400 : 6 = 900 (мл)
3.
количество кормлений – 6
раз
4. разовый
объем – 900 мл :
6 = 150 мл.)
• Калорийный способ М. С. Маслова. исходят из калорийности того вида молочного питания, каким вскармливается ребенок, и его физиологической калорийной потребности в зависимости от возраста. Метод используется только до введения прикорма и при условии одного вида пищи. Энергетическая ценность питания на 1 кг массы тела ребенка должна быть: в 1-ю четверть года (1-3 мес) — 120 ккал/кг/сут.; во 2-ю четверть года (3-6 мес) — 115 ккал/кг/сут.; в 3-ю четверть года (7-9 мес) — 110 ккал/кг/сут.; в 4-ю четверть года (10-12 мес) - 105 ккал/кг/сут. Один литр женского молока имеет калорийность примерно 700 ккал/л. (Пример: Ребенку 4 мес., масса при рождении 3 000 г, находится на естественном вскармливании. Рассчитать суточный и разовый объем пищи. Ответ: 1.Калорийная потребность = 115 ккал/кг в сутки. 2. Долженствующая масса = 3000 + 600 + 800 + 800 + 750 = 5 950 (г). 3. Калорийная суточная потребность 115 (ккал)× 5 950 (г) = 684,25 ккал/сут.
1000
мл женского молока — 750 ккал
Х мл
женского молока — 684,25 ккал.
4.
Суточный объем =
1000 х 684,25 : 750 = 912,33мл = 900
мл.
5. Количество
кормлений — 6
6. Объем
на одно кормление ==
900 : 6 = 150
мл.)
Например,
ребенок в возрасте 1 месяца должен
получать в сутки 800 мл молока. При
7-разовом кормлении объем каждого
кормления будет равен 110 мл молока, а
при 6-разовом — 130 мл. Ребенок на первом
году жизни не должен получать в сутки
более 1000- 1100 мл пищи.
46.Смешанное
вскармливание, основные принципы
(определение количества докорма,
качественная и количественная
характеристика докорма, понятие
контрольного вскармливания).
Под
смешанным вскармливанием понимают
кормление ребенка на
первом ПОЛУГОДИИ
жизни грудным молоком в количестве не
менее 1/5 суточного объема (150-200
мл) в сочетании
с детскими молочными смесями.
д о к о р м (коровье молоко,
молочные и безмолочные искусственные
смеси).
Возможные
соотношения между объемом указанных
питательных продуктов: 2:1,1:1 и 1:2. Если
материнское молоко
составляет больше половины общего
объема (2:1), то такой
вариант смешанного вскармливания
приближается к естественному.
Если в суточном объеме преобладает
приготовленная смесь
(1:2), такое вскармливание ближе к
искусственному.
Перевод ребенка на искусственное
вскармливание,
особенно в первые месяцы жизни для него
далеко не безразличен, являясь своеобразным
«метаболическим
стрессом». Ни
одна даже самая современная искусственная
смесь не может являться полноценной
заменой материнского молока. В связи с
этим большое внимание врачей и среднего
медицинского персонала должно уделяться
правильному выбору «заменителей»
женского молока с учетом индивидуальных
особенностей здоровья, физического
развития и аппетита.
Получение
искусственной смеси при смешанном
вскармливании называется ДОКОРМ.
Причины
и показания
смешанного вскармливания:
-
гипогалактия;
-
социально-бытовые условия
(мама выходит на
работу, занимается в учебном заведении
и т.п.);
- компенсированные заболевания
матери
(сердечно-сосудистой, почечной и других
систем);
- неполноценное
материнское
молоко (недостаточное количество
ингредиентов), когда у ребенка постепенно
при естественном вскармливании
развиваются гипотрофия и анемия тяжелой
степени.
Существует 2 методики
смешанного вскармливания (в зависимости
от его причины):
1. При
гипогалактии и
неполноценности
грудного молока
(в последнем случае часть его необходимо
заменить более калорийным продуктом)
при каждом кормлении после
грудного молока ребенок получает
искусственную смесь.
Почему вначале малыша нужно приложить
к груди? Потому что: именно тогда у
ребенка наиболее выражено чувство
аппетита, и он активно будет сосать
грудь, пока не высосет все молоко. Если
же сначала дать ребенку искусственную
смесь, то мы, во-первых, не знаем, какое
количество ее дать, а во-вторых, после
удовлетворения аппетита малыш не захочет
сосать грудь.
Таким образом, для
максимального его сосания мать всегда
должна вначале приложить ребенка к
груди, а потом докормить заранее
приготовленной искусственной смесью.
Эта методика смешанного вскармливания
является более оптимальной.
2. В случае
социально-бытовых условий при лечении
некоторых заболеваний матери
ребенок в течение дня 2-4
раза получает искусственную смесь,
а остальные кормления — грудное
молоко.
Правила
1.Докорм(искусственную
смесь) следует давать только после
прикладывания
ребенка к обеми грудным железам
и после полного их опорожнения, даже
при мин кол-ве молока.
2.Докорм лучше
давать из ложечки (если
его объем не очень большой), так как
более легкое поступление смеси из
бутылочки может способствовать тому,
что ребенок откажется от гуди. При
большом объеме докорма используют
бутылочку. Бутылочка должна быть с
достаточно упругой соской с мелкими
отверстиями.
3. Режим питания-свободный.
Но можно кормить ребенка и по графику,
в этом случае частота кормления может
быть уменьшена на одно кормление по
сравнению с естественным вскармливанием;
4.
Смесь, бутылочки, соски
должны быть стерильными.
Т готовой смеси — 37-38 градусов;
5.Прикорм
вводиться на 2-3 недели раньше, чем при
естественном вскармливании.
Для
расчета потребностей ребенка в пищевых
ингредиетнах
учитывают возраст ребенка, к какому
виду вскармливания приближено питание
(искусственному или естественному), вид
применяемой смеси (адаптированная,
неадаптированная).
Ввиду того, что
по сравнению с естественным при смешанном
вскармливании возможность как перекорма,
так и недокорма ребенка больше, докорм
таким детям надо давать лишь в действительно
необходимом им количестве с таким
расчетом, чтобы общий объем и калорийность
пищи не уклонялись резко от средних
потребностей ребенка данного
возраста.
Пример.
Ребенку 3 месяца, вес 5400 г. Суточный объем
питания 1/6 от массы =900 мл. Из груди ребенок
съедает за сутки 600 мл (определено при
контрольном взвешивании). Следовательно,
для докорма требуется 900-600 =300 мл смеси,
или по 50 мл смеси на 1 кормление при 6
разовом питании.
Для
этого необходимо учесть, сколько грудного
молока ребенок может получить фактически.
Это сравнительно легко в тех случаях,
когда речь идет не о недостатке молока
у матери, а о необходимости по каким-либо
причинам отказаться от одного или
нескольких грудных кормлений.
Несколько
труднее учесть количество получаемого
ребенком грудного молока в случае
гипогалактии у матери; в закрытых детских
учреждениях, где мать и ребенок находятся
под постоянным наблюдением, это можно
сделать достаточно точно, взвешивая
в течение 1—2 суток ребенка до и после
каждого кормления.
В условиях работы в поликлинике обычно
приходится ограничиваться приблизительными
данными на основании 2—3 контрольных
взвешиваний.
Для определения количества
недостающего ребенку молока можно
воспользоваться формулой А. Н.
Антонова:
Количество
недостающего молока
= Q*(P-p)/3P
Р — нормальная прибавка в
весе ребенка данного возраста за данный
промежуток времени; р — фактическая
прибавка в весе данного ребенка за этот
же промежуток времени; Q — количество
грудного молока (или калорий), считающееся
нормой для ребенка данного возраста.
(П
р и м е р. Ребенок Н. в возрасте 3 месяцев
весит 5375 г: р — за последние 2 недели он
прибавился в весе на 200 г; Р — нормальная
прибавка веса в этом возрасте за 2 недели
составляет 325 г; Q — 3-месячный ребенок
должен получать за сутки грудного молока
850 г; х — недостающее ребенку ежедневно
количество молока составляет:
X=850(325-200)/3
* 325 примерно равно 109 г.)
Методы
определения количества докорма:
потребность в белке у детей, находящихся
на смешанном вскармливании, зависит от
количества грудного молока в рационе.
Если грудное молоко составляет 2/3
суточного количества пищи, ребенок
должен получать 3
г белка на кг
долженствующего веса. При равном
количестве грудного молока и докорма
— 3,5 г, при 1/3 грудного и 2/3 коровьего —
4 г на кг веса. Жиры и углеводы дают в тех
же количествах, как и при естественном
вскармливании. Целевая
калорийность рациона — 120–160
ккал/кг в сутки, в
исключительных случаях — до 220 ккал/кг
в сутки. Рекомендованный уровень
поступления белка — от 3–4,5 до 6 г/кг в
сутки
Расчет
объема смеси производится на фактическую
массу тела только калорийным методом
— 115 ккал/кг на протяжении первых 6 мес
жизни. Однако при этом объем питания у
ребенка в возрасте 3 мес не должен
превышать 850 мл/сут, 4 мес — 900 мл/сут, а
после 5 мес — 1000 мл/сут.
Адаптированные
молочные смеси —
продукция детского питания, произведенная
в жидкой или порошкообразной форме на
основе коровьего молока или молока
других продуктивных животных и максимально
приближенная по химическому составу к
женскому молоку в целях удовлетворения
физиологических потребностей детей
первого года жизни в необходимых
веществах и энергии. В
настоящее время в качестве сырья для
производства адаптированных молочных
смесей разрешено использование только
коровьего
и козьего молока.
Адаптированные
молочные смеси вводятся в питание
ребенка постепенно: в первые сутки —
по 10–15 мл в каждое кормление, во вторые
— по 20 мл, в третьи —по 30 мл, далее объем
новой смеси увеличивается ежедневно
на 30 мл в каждое кормление (60; 90; 120 мл и
т.д.) до полной замены продукта, который
получал ребенок ранее. Новая смесь
готовится отдельно и затем смешивается
в одной бутылочке с предыдущей. Это
правило относится и к лечебным продуктам.
Качественный
и количественный состав
смесей постоянно совершенствуется.
Особое внимание уделяется:
•
белковому компоненту.
В современных молочных смесях для детей
первого
полугодия жизни количество
белка варьирует в пределах от 12,4
до 15 г/л. Особое
значение имеет приближение аминокислотного
спектра адаптированной смеси к
аминокислотному спектру грудного
молока, что, в частности, может быть
достигнуто преобладанием сывороточных
белков,
обеспечивающих достаточную биологическую
ценность белкового компонента смеси;
•
составу жировой
композиции. Она
состоит из комплекса растительных
масел, являющихся
источником всех необходимых жирных
кислот, в том
числе полиненасыщенных (прежде всего
линолевой
и альфалиноленовой).
Тенденцией последних лет является
включение в состав смесей молочного
жира как источника
насыщенных жирных кислот, а также
холестерина,
фосфолипидов, ганглиозидов и
других компонентов, важных для формирования
и функционирования мембран всех клеток,
становления и развития центральной
нервной и иммунной систем ребенка.
Источником минорных липидов служат
также добавленные в отдельные продукты
мембраны
жировых глобул молока.
Эссенциальными компонентами являются
и длинноцепочечные полиненасыщенные
жирные кислоты — докозагексаеновая и
арахидоновая,
оказывающие положительное влияние на
процессы развития мозга и зрительного
анализатора;
• включению
пребиотиков
(галактоолигосахаридов
или их сочетания
с фруктоолигосахаридами) в состав
углеводного компонента. Перспективным
направлением является использование
биологически синтезированных
олигосахаридов, гомологичных человеческим
(2 FL, LNnT и др.);
•
пробиотики,
в качестве которых применяются изученные
и безопасные
штаммы лактобацилл и бифидобактерий.
Современные технологии позволяют
обеспечивать сохранность микроорганизмов
в продуктах на протяжении всего срока
годности, а их эффективность
и способность достигать толстой кишки
в живом виде
доказана в ходе клинических исследований;
•
поиску новых биологически
активных компонентов,
повышающих качество продукта. Так, в
ряд детских молочных смесей введен
каротиноид
лютеин, присутствующий в грудном молоке.
Его роль заключается в защите сетчатки
от повреждающего действия голубого
света и свободных радикалов, образующихся
под его воздействием.
• В состав
детских молочных смесей включен
необходимый комплекс
витаминов и минеральных веществ
в соответствии с физиологическими
потребностями детей первого года жизни,
обеспечивающий оптимальное формирование
и функционирование различных органов
и систем ребенка. Имеет значение не
только количество минеральных веществ,
но и их соотношение. Оптимальное
содержание микронутриентов обеспечивает
адекватное их усвоение. Количество
витаминов и минеральных веществ в
адаптированных молочных смесях в среднем
на 15–20% больше,
чем в женском молоке, так как их усвояемость
из смесей несколько ниже.
Калорийный
коэффициент суточного
пищевого рациона ребенка, получающего
смешанное кормление, должен быть на
5—10% выше, чем при естественном
вскармливании. Несколько меняется и
соотношение между белками, жирами и
углеводами, так как количество белка,
даваемого ребенку на 1 кг его веса,
несколько увеличивается,
а количество жира
и углеводов остается почти без перемен.
Это соотношение в зависимости от
количества вводимого докорма приближается
к 1:2:4.
47.Показания
для перевода на искусственное
вскармливание. Техника проведения.
Искусственное
вскармливание —
питание смесями (заменителями женского
молока), даже при наличии однократного
прикладывания к груди или суммарного
объема материнского молока до 50-100 мл и
независимо от наличия или отсутствия
прикормов.
Грудное
молоко составляет менее 1/5 от общего
рациона или совсем отсутствует, и
кормление осуществляется только молочной
смесью. Вскармливание
донорским молоком по эффективности
приближается к смешанному вскармливанию,
так как при
пастеризации женского молока неизбежно
утрачивается часть витаминов,
иммуноглобулинов и других важных
нутриентов.
Противопоказание
со стороны матери:
-эклампсия.
-сильные
кровотечения во время родов и в
послеродовом периоде.
-открытая форма
туберкулеза.
-состояние выраженной
декомпенсации при хронических заболеваниях
сердца, легких,
почек, печени, а также гипертиреоз.
-острые
психические
заболевания.
-особо
опасные инфекции (тиф, холера и
др.).
-герпетические
высыпания на соске молочной
железы (до их долечивания).
-ВИЧ-инфицирование
(риск заражения ребёнка 15%).
-острый
гепатит А.
- прием цитостатиков
в терапевтических дозах,
иммунносупрессивных препаратов,
антикоагулянтов типа фениндиона,
радиоизотопных контрастные вещества
для лечения или обследования, препаратов
лития, большинство противовирусных
препаратов (кроме
ацикловира, зидовудина, занамивира,
лимовудина, озельтамивира — с
осторожностью) противогельминтных
препаратов с осторожностью.
!!
-Ветряная
оспа, корь, эпидемический паротит,
цитомегаловирусная инфекция, простой
герпес, острые кишечные и острые
респираторно-вирусные инфекции,
если они протекают без выраженной
интоксикации,
кормление грудью при соблюдении правил
общей гигиены не
противопоказано;
можно при условии введения
ребенку иммуноглобулина.
-При маститах
грудное вскармливание продолжается.
Однако оно
временно прекращается при обнаружении
массивного роста в грудном молоке
золотистого стафилококка в
количестве 250 КОЕ и более в 1 мл и единичных
колоний представителей семейства
Enterobacteriacae или вида Pseudomonas aeruginosa
(Методические рекомендации по
бактериологическому контролю грудного
молока, Москва, 1984);
-Абсцесс
молочной железы является
возможным осложнением мастита и наиболее
вероятен при резком
прерывании кормления грудью.
Кормление из
здоровой железы должно продолжаться,
а молоко из инфицированной
груди следует осторожно сцеживать и
выливать;
-Кормление
грудью во
время наступления новой беременности
может продолжаться.
Противопоказания
со стороны ребенка:
-оценка
состояния новорожденного по шкале Апгар
ниже 7 баллов при
тяжелой
асфиксии новорожденного,
-родовой
травме,
-судорогах,
-синдроме дыхательных расстройств
СДР.
- глубокая
недоношенность,
-тяжелые пороки
развития (желудочно-кишечного
тракта, челюстно-лицевого аппарата,
сердца).
Абсолютные
противопоказания
к грудному вскармливанию со стороны
ребенка очень ограничены — наследственные
энзимопатии (галактоземия
и др.).
При
фенилкетонурии
объем грудного
молока в сочетании с лечебными продуктами
устанавливается индивидуально,
болезнь «моча с запахом кленового
сиропа».
Техника:
1) Надо помнить,
что при искусственном вскармливании
ребенок может оказаться как в условиях
недокармливания, так и в условиях
перекармливания. Следует систематически
проводить расчет энергетической ценности
пищи, содержания белков, жиров, углеводов
в суточном рационе и при каждом его
изменении.
2) Объем
пищи в сутки при искусственном
вскармливании должен быть таким же,
как и при естественном вскармливании:
Суточный
объём пищи, необходимый грудному
ребёнку.:
Суточное
количество пищи составляет:
в возрасте от 10 дней (2 недели) до 1,5
месяцев (6 недель) — 1/5 часть фактической
массы тела;
в возрасте 1,5 (6 недель)
-4 месяцев - 1/6 часть
от долженствующей массы тела;
в
возрасте 4- 6 месяцев - 1/7 часть
от долженствующей массы тела;
в
возрасте старше 6 месяцев - 1/8 массы тела.
Соотношение
между основными пищевыми компонентами
(белками, жирами,
углеводами) до
введения прикорма должно составлять
1:3:6,
после введения прикорма - 1:2:4.
До 4-6 мес
потребность в белках
составляет 2-2,5 г/кг,
жирах - 6,5 г/кг,
углеводах - 13 г/кг,
а после
введения прикорма -
соответственно 3-3,5,
6-6,5 и 13 г/кг.
3) потребность ребенка в калориях,
белках, жирах и углеводах, а также
соотношение между пищевыми ингредиентами
зависит от той молочной смеси, которой
вскармливается ребенок.
При
вскармливании
детей смесями "Малютка", "Малыш",
"Виталакт"
энергетическая потребность сохраняется
такой же, как и при естественном
вскармливании:
в I четверть первого
года жизни- 120 ккал/кг массы;
во II -
115 ккал/кг массы;
в III - 110 ккал/кг массы;
в IV- 100 ккал/кг массы;
в белке
2,5-3,0 г/кг массы, в
жире 7,0-5,0
(в зависимости от первого - второго
полугодия первого года жизни), в углеводах
12-14 г/кг массы в
сутки. При этом соотношение между
белками, жирами, углеводами приближается
к 1 : 3 : 5.
4) При искусственном вскармливании,
пища
дольше задерживается в желудке.
Поэтому промежутки
между кормлениями увеличивают, а число
кормлений уменьшают.
5)
Смеси дают всегда стерильные
и подогретые до 35-40°С.
Отверстие соски не должно быть слишком
больших размеров (молоко должно вытекать
через него при опрокинутой вниз бутылочке
каплями).
6) Бутылочку при кормлении
нужно держать так, чтобы горлышко
ее было все время заполнено молоком,
так как в противном случае ребенок
заглатывает воздух, что обычно ведет к
обильному срыгиванию или рвоте.
48.Простые
смеси. Техника их приготовления.
Молочные
смеси, применяемые при кормлении детей
первого года жизни (физиологические),
подразделяют на простые
смеси (коровье
молоко и его разведения или молоко
других животных)
и адаптированные
смеси, качественный
состав которых максимально приближен
к женскому молоку. И те и другие смеси
могут быть либо сладкими, либо подвергнутыми
кисломолочному брожению.
Простые
смеси получают путем разведения
коровьего молока в
определенной пропорции водой (смеси
№ 1, № 2, № 3) или 5—10% отварами круп (смеси
А, Б, В).
Смесь № 1 состоит из 1 : 2 частей
воды, смесь № 2 — из 1 : 1 части воды, смесь
№ 3 — из 2 : 1 части воды; смесь А — из 1 :
2 частей отвара, смесь Б — из 1 : 1 части
отвара, смесь В — из 2 частей молока и 1
части отвара. в соотношении 1:1 — смесь
№ 2 (в первые
2 недели жизни);
2:1 - смесь №3
(в возрасте от 2
недель до 3 месяцев).
Разведением молока добиваются прежде
всего уменьшения
количества белка в единице объема.
Недостающее
количество углеводов
восполняют добавлением сахара,
а жира —
сливками.
После
3 месяцев детям
дают цельное
коровье молоко с добавлением 5% сахара
(смесь
№ 5).
Отвары
повышают секрецию пищеварительных
желез, уменьшают брожение углеводов,
способствуют образованию более
нежных сгустков казеина коровьего
молока. Слизистые
отвары для разведения молока готовятся
из рисовой, овсяной, гречневой и перловой
круп или из муки этих же круп. При выборе
крупы для приготовления отвара нужно
учитывать индивидуальные особенности
ребенка. Рисовый
отвар,
особенно 10% концентрации, следует
применять при кормлении детей с
неустойчивым, жидким стулом,
овсяный
— при склонности детей к запорам.
Детям с анемией
целесообразнее давать молочную смесь,
приготовленную на гречневом
отваре, т.
к. гречневая" крупа богата железом и
нек-рыми незаменимыми аминокислотами.
Однако,
согласно современным рекомендациям,
неадаптированные смеси (и сладкие, и
кефиры) можно давать не ранее 8—9 месяцев.
При этом кисломолочные продукты (в том
числе и адаптированные) должны составлять
не более 50% от общего
суточного объема заменителей женского
молока и (или)
«последующих» смесей, получаемого
ребенком, поскольку их
большое количество может вызвать у
младенцев сдвиги в кислотно-щелочном
равновесии. Введение
неадаптированных смесей в рацион в
более младшем возрасте может оказать
неблагоприятное влияние на азотистый
метаболизм, функции незрелых
почек.
49.Адаптированные
смеси в питании детей первого года
жизни.
Адаптированными
молочными смесями
(заменителями женского молока) — называют
пищевые продукты в жидкой или
порошкообразной форме, изготовленные
на основе коровьего молока,
молока других сельскохозяйственных
животных, предназначенные для использования
в качестве заменителей женского молока
и максимально
приближенные к нему по химическому
составу с целью
удовлетворения физиологических
потребностей детей первого года жизни
в пищевых веществах и энергии.
По
возрасту:
-«начальные»
или «стартовые» смеси — для детей первых
6 месяцев жизни;
-«последующие» смеси» — для детей
второго
полугодия жизни
-смеси
от «0 до 12 месяцев» — могут применяться
на
протяжении всего первого года жизни
ребенка.
По
консистенции:
-сухие
("Бебилак" (Россия-Голландия),
"Нутрилак" (Россия), "Хумана"
(Германия), "Фрисолак" (Голландия),
"Нан" (Швейцария), "Нутрилон"
(Голландия), "HIPP" (Австрия), ""Энфамил"
(США), "Сэмпер Бэби" (Швеция) и
другие).
-жидкие
(«Агуша -1»)
По
рН:
-пресные
(«НАН-1», «НАН-2», «Нестожен»)
-кисломолочные
(«Нан кисломолочный»)
Начальные
смеси содержат
сывороточные
белки, при этом
уровень белка снижен (в большинстве
этих смесей в 100 мл готового к употреблению
продукта содержится 1,4
– 1,6 г белка,
а минимальный уровень
— 1,2 г/100 мл
(содержание белка в 100 мл зрелого женского
молока составляет 0,9—1,3 г); чтобы
приближается к его содержанию в женском
молоке. Белковый компонент таких
продуктов представлен легкоусвояемыми
сывороточными белками и казеином в
соотношении 60:40,
50:50, в отдельных
смесях 70:30;
Начальные смеси всегда обогащены
таурином
– свободной аминокислотой, необходимой
для правильного формирования мозга,
зрительного анализатора, способствующей
перевариванию и
всасыванию жиров.
Эта аминокислота для детей первых
месяцев жизни, особенно недоношенных
относится к числу незаменимых.
Таурин содержится
в грудном молоке и отсутствует в коровьем.
Состав жирового компонента «начальных»
смесей также максимально приближен к
составу жиров женского молока. Для
улучшения усвоения жира в молочную
смесь вводят небольшие
количества природных эмульгаторов
(лецитина,
моно- и диглицеридов),
которые способствуют лучшему раздроблению
жировых шариков и более легкому всасыванию
жира. В некоторые
смеси введен а-лактальбумин;.
Большое количество искусственных смесей
содержит в своем составе нуклеотиды.
Для
адаптации жирового
компонента «начальных» смесей в их
состав вводятся:
1.Растительные
масла, богатые полиненасыщенными жирными
кислотами (линолевой
и а-линоленовой
жирных кислот в смесях последнего
поколения приближается к таковому в
женском молоке, составляя 10:1).
2.В состав большинства смесей добавлен
L-карнитин,
способствующий ассимиляции жирных
кислот на клеточном уровне.
3.Обогащения
смесей длинноцепочечными полиненасыщенными
жирными кислотами
(арахидоновой
и докозагексаеновой),
которые являются предшественниками
эйкозаноидов (простагландинов,
тромбоксанов, лейкотриенов), необходимых
для миелинизации нервных волокон,
дифференцировки клеток сетчатки глаза,
участвующих в формировании и стабилизации
клеточных мембран и др.
В качестве
углеводного
компонента
используется:
-лактоза
или ее комбинация с мальтодекстрином
(до 25%).
1.обладающим бифидогенным
действием;
2.снижающим осмолярность
продукта;
-галакто-
и фруктоолигосахариды, обладающие
пребиотическими свойствами и способствующие
избирательному росту в кишечнике
преимущественно бифидобактерий.
-лактулоза
(пребиотиком).
Во все смеси включен
необходимый набор витаминов
и минеральных веществ
в соответствии с физиологическими
потребностями детей первых месяцев
жизни, обеспечивающих оптимальное
формирование и функционирование
различных органов и систем ребенка.
-1.Это в первую очередь железо,
медь, цинк, йод. В
ряд смесей введен селен, обладающий
выраженными антиоксидантными
свойствами.
-2.Соотношение кальция
и фосфора в смесях
находится в диапазоне 1,5:1—2,0:1,
что обеспечивает правильное развитие
костной ткани и предупреждает
появление рахита.
-3.Для улучшения
усвоения железа и
его использования в процессах кроветворения
очень важно наличие в продукте достаточного
количества аскорбиновой
кислоты (5—10 мг в
100 мл), а также оптимальное соотношение
железа и цинка
— 2:1
и железа и меди
— 20:1,
при таком балансе всасывание этих
микроэлементов оптимально.
Уровень
витаминов в
адаптированных молочных смесях превышает
таковой в женском молоке
в среднем на
15—20%, так как их усвояемость более
низкая, чем из женского молока!
-витамин
D, участвующего в
процессах обмена кальция и минерализации
костной ткани. Его содержание в 100 мл
готовой смеси составляет 40—50
ME.
Во все смеси
добавлены витамины группы
В, витамин Е,
обладающий антиоксидантной активностью,
витамин А,
принимающий участие в иммунных реакциях
организма, а в некоторые смеси введен
В-каротин.
Смеси,
используемые на протяжении всего первого
года жизни: могут
содержать сывороточные
белки и таурин,
но могут и не иметь
их. Жировой компонент
этих смесей состоит из растительных
жиров или из
смеси растительных
масел и молочного жира.
В качестве углеводного компонента
используются лактоза,
декстрин-мальтоза,
иногда применяется и сахароза,
крахмал.
Нельзя
допускать приготовления как слишком
концентрированной,
так и более разведенной смеси. То и
другое одинаково вредно! При использовании
более концентрированной смеси ребенок
получает избыточное количество всех
пищевых веществ, в связи чем, у него
могут развиться нарушения пищеварения
– возникнуть срыгивания, рвота, возможно
появление неустойчивого стула, а иногда
и аллергических реакций. Если давать
ребенку более разведенное, чем положено
питание, то малыш получит недостаточное
количество «пластического» материала
и будет отставать в физическом
развитии.
50.Адаптированные
детские питательные смеси и их преимущества
перед простыми.
1)для
определенных возрастов.
2)АМС в
наибольшей степени приближены по составу
к женскому молоку.
В них снижено
по сравнению с коровьим молоком общее
содержание белка
до 1,5-1,7/100 мл, что предохраняет незрелые
системы ребёнка от перегрузки белком.
Скоррегирован качественный
состав белков:
соотношение казеина (основной белок
коровьего молока) и сывороточных
альбуминов (превалирующих в женском
молоке) доведено до 40:60 или 50:50. Это
способствует образованию
мелкодисперсного, нежного сгустка в
желудке ребёнка
и обеспечивает более
высокую степень переваривания и усвоения
белка. Во многие
смеси вносят условно эссенциальную
гликокислоту таурин
(до 4-5 мг/100 мл), содержание которой в
коровьем молоке значительно ниже, чем
в женском. Таурин играет важную роль в
формировании мозга, сетчатки, является
модулятором роста и дифференцировки
тканей. Особенно велика потребность в
этой аминокислоте у детей I полугодия
жизни, а во II полугодии она снижается
по мере введения злаковых блюд прикорма.
В АМС содержание жира
составляет 3,5-3,7
г/100 мл, приблизительно так же, как в
женском молоке. Но в них изменён
качественный состав жиров: молочный
жир частично или полностью заменён
на смесь растительных жиров
(используются кукурузное, кокосовое,
соевое, подсолнечное, пальмовое, рапсовое
и др. масла). Такая замена необходима
для оптимизации соотношения между
насыщенными
и ненасыщенными жирными кислотами,
чтобы увеличить содержание ПНЖК семейства
ω:6 (линолевая) и ω:3 (α-линоленовая,
докозагексаеновая, эйкозапентаеновая)
и приблизить жирнокислотный состав
молочных смесей к таковому женского
молока.
В АМС уровень линолевой
кислоты составляет 0,5-0,6 г/100 мл,
а соотношение ω6 (линолевая кислота) и
ω3 (α-линоленовая кислота) составляет
от 10:1 до 15:1
(в женском молоке 9-10:1). Для улучшения
усвоения жира в АМС
добавляют В-каротин
(1-1,5 мг/100 мл) – витаминоподобное
соединение, способствующее внутриклеточному
транспорту и окислению жирных кислот.
В АМС добавляют молочный
сахар, повышая уровень углеводов до
7-7,2 г/100
мл. Это необходимо для обеспечения
ребёнка быстроутилизируемой
энергией и, кроме
того, галактоза, входящая в состав
лактозы, необходима для формирования
нервной системы (галактоцереброзиды).
В состав многих АМС в небольшом количестве
включают декстринмальтозу
(природный полимер глюкозы).
Наряду
с оптимизацией минерального состава
предусматривается дополнительное
внесение в АМС ряда микроэлементов
(железа, цинка, йода, меди, марганца), а
также водо- и
жирорастворимых витаминов,
причём с учётом более низкой усвояемости
этих элементов из молочный смесей по
сравнению с женским молоком. Поэтому
фактическое содержание этих микронутриентов
в АМС несколько выше физиологических
потребностей (в 1-2 раза).
51.Адаптированные
молочно-кислые смеси, их преимущества
и недостатки.
АЦИДОФИЛЬНЫЕ.
В настоящее время в питании грудных
детей широко и успешно используются
адаптированные
кисломолочные продукты
«Нутрилак кисломолочный» и «НАН
кисломолочный». Как и кисломолочные
продукты, «кислые» смеси производят
путем сквашивания
молока молочнокислыми бактериями.
В кисломолочных смесях
белок находится в створоженном состоянии,
и они медленнее удаляются из желудка,
чем пресное молоко.
Для их приготовления
подбирают специальные
штаммы лактобактерии:
bulgaricus, helvetics, acidopfillus,
a также Str.
termophylus. После
сквашивания в продукты вводят
пробиотические штаммы B.lactis
(BB 12).
В процессе молочнокислого
брожения продукты приобретают ряд
важных свойств:
1.Снижается
уровень лактозы.
2.Накапливаются
бактерицидные
вещества, молочная
кислота.
3.Происходит частичное
расщепление молочного белка,
что облегчает
переваривание
продукта и его усвоение.
4.Несколько
снижает
антигенность белкового компонента.
5. Уровень
казеиновых
белковых фракций, на которые у крохи
может возникнуть аллергия, в них
минимален,
уменьшено и содержание жира. Все это
облегчает усвоение «кислых» смесей.
Кроме того, обогащенные лакто-
и бифидобактериями,
они помогают поддерживать у малыша
здоровую микрофлору и защищать его от
инфекций, а также способствуют нормализации
стула, устраняют
дискомфорт в кишечнике и метеоризм.
Кислая среда стимулирует работу ферментов
печени и поджелудочной железы, ускоряет
перистальтику кишечника,
улучшает всасывание
питательных веществ.
Адаптированные
кисломолочные смеси могут вводиться в
питание детей наряду с пресными
молочными формулами с первых недель
жизни. При этом
возможно комбинировать
их в соотношении
2:1 — 1:1, особенно при нарушениях процессов
пищеварения и риске развития
алиментарно-зависимых заболеваний.
Применение только кисломолочных смесей
(особенно с высокой кислотностью) может
вызвать срыгивания,
отказ ребенка от продукта.
Недостатки:
-Ведь кислая среда
может приводить к частым
срыгиваниям и к излишней активности
ферментов печени и
поджелудочной железы.
- Обычно
рекомендации по введению таких продуктов
получают младенцы с проблемами в
пищеварении и со склонностью к запорам.
-
Переваривание и усвоение кисломолочных
смесей требует напряжения
метаболических систем (повышенная
экскреция с мочой
аммиака, повышенное
выведение солей и др.)
- Введение
большого количества кислых радикалов
вызывает напряженность процессов их
нейтрализации.
Но по сравнению с
кефиром, ряженкой или йогуртом в подобных
смесях меньше
белков и жира,
поэтому они не нагружают незрелые почки
младенца. Кефир и другие неадаптированные
кисломолочные продукты недопустимо
вводить в питание детей первого полугодия.
В настоящее время рекомендовано их
использование, начиная с 8 месяцев!
52.Сроки
и техника введения соков, фруктового
пюре, яичного желтка на первом году
жизни при естественном, смешанном и
искусственном вскармливании.
Введение
прикорма детям как на грудном, так и на
искусственном вскармливании рекомендовано
начинать в возрасте 4–6 мес.
С
5-ти месяцев в питании ребенка начинается
важный этап -
введение
прикормов:
Первая
пищевая добавка в 4 мес.:
Фруктовые соки
(пюре) - яблочный, из белой черешни, из
белой смородины, абрикосовый, персиковый,
грушевый, сливовый (даны в порядке
предпочтения). Начинают вводить в рацион
с капель, постепенно увеличивая количество
до 40-60 мл. Желательно чтобы первые соки
ребенка были натуральными и свежими
(домашнего приготовления). До
6 месяцев ребенку дают пюре из одного
фрукта, после 6 месяцев можно давать
поликомпонентные пюре. Не
забывайте вводить в рацион ребенка
черносливовое
пюре. Чернослив
мягко нормализует работу кишечника, а
также является чемпионом среди фруктов
по содержанию антиоксидантов, которые
укрепляют иммунитет. Также для зрения
вашего малыша очень полезно черничное
пюре.
Творог
(кальцинированный) так же желателен
домашнего приготовления - на 200 мл молока
в момент закипания добавляется 1-2
столовые ложки СаСl2 , затем откидывается
на марлю, или молочной кухни, специального
детского питания. Начинают вводить в
рацион с крупинок и доводят до 40 грамм
в сутки
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков). Если
у ребенка есть какая-то пищевая аллергия,
то в этом случае сроки введения желтка
продлеваются; Белок вводят в рацион
ребенка с 1,5 лет, т.к. белок является
аллергенным продуктом.
Первый
прикорм в 5-6 мес.:
Чаще в качестве первого прикорма
используют овощное пюре (картофель,
капуста, кабачок, тыква, и в последнюю
очередь морковь). Начинают
с 1 – 2 чайных ложек и
постепенно в течение 1- 2 недель заменяют
полностью 1 кормление (это примерно 150
мл). Далее 2 -3 недели не вводя ничего
нового – период адаптации.
Второй
прикорм в 6-7 мес.:
5% кашу (с 8 месяцев - 10%); (рисовая, манная,
гречневая, кукурузная) с добавлением 5
г сливочного масла, яичного желтка.
В
6-7 мес. Вводится также мясной
бульон (используют
для разведения овощного пюре), затем
мясо говядины, телятины в виде фарша.
Через
месяц вводят второй прикорм – кашу
(предпочтительнее начинать с безглютеновых
злаков – рис, кукурузная, гречневая
мука). Наиболее удобны сухие
растворимые каши:
они обогащены витаминами, кальцием,
железом, имеют гарантированный состав
и безопасность. У детей с хорошим весом
прикормы начинают с овощей, при
дефиците веса первым прикормом становится
каша. В овощное
пюре обычно вводится 5мл растительного
масла (желательно чередовать
подсолнечное, оливковое, кукурузное),
а в кашу сливочное.
Мясо отварное
(телятина, кролик, индейка) дважды
пропускается через мясорубку и дается
ребенку, начиная с
1 чайной ложки,
постепенно доведя количество до 60-80
грамм в сутки,
обычно в третье кормление.
С момента
введения первого прикорма ребенок
переходит на 5-ти
разовое питание.
Прикормы необходимо разделять кормлениями
грудью, обычно
первое,
третье
и последнее
кормление – грудное молоко или молочная
смесь, второе
– каша,
а четвертое
– овощи.
Третий
прикорм в 7-8 мес.:
неадаптированные молочные продукты:
молоко, кефир,
йогурты и полностью
грудным остается только первое и
последнее кормление.
С 9-10 мес. -
«кусочковое» питание.
С 10-11 мес. -
нежирные сорта рыбы не чаще 2-х раз в
неделю.
Прикорм
вводится на 2-4 недели раньше, чем при
естественном вскармливании.
Различают
такие витаминные
и белковые добавки,
как: с 3 месяцев.
Фруктовые соки и пюре следует назначать
с 3 и 3,5 месяцев, соответственно. Допустимо
и более раннее (с 1,5 месяца) введение
соков с учетом их индивидуальной
переносимости.
Творог
(кальцинированный) так же желателен
домашнего приготовления -
на 200 мл молока в момент закипания
добавляется 1-2 столовые ложки СаСl2,
затем откидывается на марлю, или молочной
кухни, специального детского питания.
Начинают вводить в рацион с крупинок и
доводят до 40 грамм в сутки.
Яичный
желток вкрутую сваренного яйца.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков).
Это обусловлено
тем, что дети
уже получают в составе заменителей
женского молока значительное количество
«чужеродных» пищевых продуктов:
коровье молоко, сладкие сиропы,
растительные масла, содержащие достаточно
большое количество
новых пищевых веществ
— белков, олигосахаридов, липидов,
отличных по строению от этих ингредиентов
женского молока. Таким образом, дети в
известной степени адаптированы к
«чужеродному» питанию.
Первый
прикорм (овощное
пюре) при искусственном вскармливании
вводят в рацион с 4,5—5 месяцев, второй
прикорм (на злаковой
основе) — с 5,5—6 месяцев. Однако с учетом
индивидуальных особенностей развития,
так же как и при естественном вскармливании,
в качестве первого прикорма могут быть
использованы и каши, лучше — обогащенные
железом, витаминами, микроэлементами.
Желток целесообразно использовать
с возраста 6 месяцев, мясо — с
7 месяцев.
Кефир,
другие кисломолочные продукты и цельное
коровье молоко в качестве блюд прикорма
можно вводить в питание с 8
месяцев, однако и
у этих детей препочтительнее использовать
«последующие» формулы.
53.Режим
кормления и потребности в различных
пищевых ингредиентах и калориях у детей
первого года жизни на естественном,
смешанном и искусственном вскармливании.
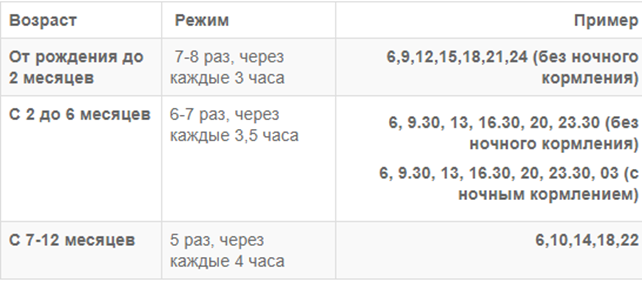 1)
Рекомендуемые часы
кормлений: при 7-разовом питании - 6, 9,
12, 18, 21, 24 ч; при 6-разовом — 6 ч, 9 ч 30 мин,
13 ч, 16 ч 30 мин, 20 ч, 23 ч 30 мин; при 5-разовом
- 6, 10, 14, 18, 22 ч. Допустимы отклонения от
режима в пределах получаса. Причем важны
не столько конкретные часы кормлений,
сколько промежутки между кормлениями.
Разумеется, и в случае смешанного
вскармливания ночные прикладывания к
груди не запрещают, поскольку они, как
указывалось выше, способствуют поддержанию
лактации.
2) Объем
пищи в сутки при искусственном
вскармливании должен быть таким же,
как и при естественном вскармливании:
Суточный
объём пищи, необходимый грудному
ребёнку.:
Суточное
количество пищи составляет:
в возрасте от 10 дней (2 недели) до 1,5
месяцев (6 недель) — 1/5 часть фактической
массы тела;
в возрасте 1,5 (6 недель)
-4 месяцев - 1/6 часть
от долженствующей массы тела;
в
возрасте 4- 6 месяцев - 1/7 часть
от долженствующей массы тела;
в
возрасте старше 6 месяцев - 1/8 массы тела.
Соотношение
между основными пищевыми компонентами
(белками, жирами,
углеводами) до
введения прикорма должно составлять
1:3:6,
после введения прикорма - 1:2:4.
До 4-6 мес
потребность в белках
составляет 2-2,5 г/кг,
жирах - 6,5 г/кг,
углеводах - 13 г/кг,
а после
введения прикорма -
соответственно 3-3,5,
6-6,5 и 13 г/кг.
3) потребность ребенка в калориях,
белках, жирах и углеводах, а также
соотношение между пищевыми ингредиентами
зависит от той молочной смеси, которой
вскармливается ребенок.
При
вскармливании
детей смесями "Малютка", "Малыш",
"Виталакт"
энергетическая потребность сохраняется
такой же, как и при естественном
вскармливании:
в I четверть первого
года жизни- 120 ккал/кг массы;
во II -
115 ккал/кг массы;
в III - 110 ккал/кг массы;
в IV- 100 ккал/кг массы;
в белке
2,5-3,0 г/кг массы, в
жире 7,0-5,0
(в зависимости от первого - второго
полугодия первого года жизни), в углеводах
12-14 г/кг массы в
сутки. При этом соотношение между
белками, жирами, углеводами приближается
к 1 : 3 : 5.
54.Особенности
вскармливания детей с рахитом, анемией,
аллергодерматозом.
Больному
рахитом ребенку
надо как можно
дольше сохранять грудное вскармливание.
Но это не исключает необходимости
проводить необходимую коррекцию его
рациона. Нарушение при рахите обмена
минеральных веществ и витаминов, особенно
значительное снижение в крови витаминов
группы В и аскорбиновой кислоты, требуют
тщательного контроля за содержанием
витаминов в рационе ребенка. При
вынужденном
переводе ребенка на смешанное и
искусственное вскармливание
необходимо помнить, что минеральные
соли, в том числе кальций
и фосфор, из коровьего молока усваиваются
хуже, чем из
грудного несмотря на то, что абсолютное
содержание их выше. Поэтому более
рационально при организации смешанного
и искусственного вскармливания
использовать
адаптированные молочные смеси,
приближенные по основным пищевым
веществам и минеральному составу к
женскому молоку.
Очень
важно своевременно вводить фруктовые
и овощные соки и пюре, овощные отвары,
желток, творог и другие продукты,
содержащие в достаточном количестве
пищевые вещества и витамины. Детям с
проявлениями рахита настоятельно
рекомендуется в качестве первого
I прикорма овощное
пюре, которое в ряде случаев дается
раньше обычных сроков — с 3,5—4 мес.
Второй прикорм
— каша на овощном отваре или с добавлением
овощей и фруктов. С 5 мес ребенку
рационально назначить печень
в виде суфле.
Мясное пюре можно вводить с 6—6,5 мес,
чередуя его с пюре из куриного
мяса, печени, почек, мозгов.
При
наличии у ребенка признаков рахита
необходимо использовать продукты
с высоким содержанием кальция
и фосфора. В
рацион этих детей целесообразно вводить
кисломолочные продукты, благотворно
влияющие на процессы усвоения пищевых
веществ, в том числе кальция. При этом,
выбирая исходные продукты, следует
обращать внимание на содержание в них
витамина
С, солей кальция и фосфора.
Этими компонентами богаты черная
смородина, шиповник,
лимон, апельсин, кизил, вишня, черешня,
хурма. Все блюда
желательно обогащать хорошо
измельченной огородной зеленью.
Необходимо также часто использовать в
питании яичный
желток, богатый
жирорастворимыми витаминами, солями
кальция, фосфора, микроэлементами. Кроме
того, в нем содержится витамин D (от 200
до 500 ME в 100 г). В качестве полноценного
животного белка и кальция в пищевой
рацион систематически вводятся творог
и мясо. При
разработке рационов для этих детей в
первую очередь внимание уделяется
достаточному поступлению белка
и жира,
которые принимают самое активное участие
в процессах всасывания витамина D,
кальция и фосфора.
Поступающие в организм белки должны
быть полноценными
по аминокислотному
составу.
Анемия
значительно чаще
возникает у детей, находящихся на
искусственном вскармливании,
и особенно у тех, кто потребляет коровье
молоко. В то же время у детей, вскармливаемых
грудью, заболевание развивается редко.
По содержанию железа и
меди, а также по витаминному составу
оно значительно превосходит коровье,
в котором после обязательной пастеризации
значительная часть витаминов разрушается.
Важно обеспечить ребенка, больного
анемией, достаточным
количеством
белка,
железа
и таких минеральных
веществ, как
медь,
цинк, марганец
и др., являющихся
основным материалом для построения
гемоглобина. Основными источниками
указанных компонентов являются мясные
продукты, в том числе печень,
язык. Помимо
диетотерапии необходимо использовать
лекарственные препараты
железа, которые дают сразу после
кормления,
желательно в сочетании с аскорбиновой
кислотой, а
также с натуральными или консервированными
(лучше специализированными – для
детского питания) соками из черной
смородины, облепихи,
цитрусовых.
Если
же ребенок находится на искусственном
вскармливании, то
для его питания необходимо использовать
адаптированные
молочные смеси,
специально
предназначенные для детей с анемией.
Для
некоторых категорий больных детей, в
лечении которых важнейшее значение
имеет лечебное
питание,
промышленностью выпускаются так
называемые энпиты
— сухие
лечебные молочные смеси.
Они обладают повышенной биологической
ценностью как за счет специальной
обработки белкового
и жирового
компонентов, так и в результате обогащения
этих смесей витаминами A, D, Е, В1, В2, В6,
РР, C, а также железом.
Для
питания детей различного возраста,
больных анемией, создан "Энпит
противоанемический",
который содержит повышенное
количество белка и железа
и обогащен водо- и жирорастворимыми
витаминами. Это мелкий порошок
серовато-коричневого
цвета со специфическим запахом и
вкусом.
(Для
приготовления 100 мл жидкого продукта в
чистую посуду наливают 30—40 мл холодной
кипяченой воды, растворяют в ней 15 г
сухого порошка до исчезновения комочков,
добавляют воду до 100 мл, нагревают до
кипения и кипятят 1—2 минуты при
непрерывном помешивании. После охлаждения
до 36—38° смесь готова к употреблению.
При необходимости готовый жидкий продукт
можно хранить в холодильнике в течение
суток, подогревая его перед употреблением
до 36—38°.)
Поскольку противоанемический
энпит имеет специфический вкус и запах,
а также темный цвет, дети нередко
отказываются принимать его в чистом
виде. При вскармливании ребенка первого
года жизни энпит обычно добавляют
в грудное молоко или заменяющую его
детскую молочную смесь,
равномерно распределяя суточную
порцию.
Здоровым детям, как правило,
соки начинают давать с трехнедельного
— месячного возраста,
а пюре — с 1,5 месяцев. При
анемии же эти добавки необходимо
назначать раньше:
соки — с двух
недель, пюре —
с месячного
возраста.
Для приготовления
фруктовых и ягодных соков можно
использовать самые разнообразные фрукты
и ягоды, но в первую очередь те, которые
богаты железом,
медью и другими
микроэлементами. Это яблоки,
сливы, вишни, груши, абрикосы, персики,
лимоны, садовая земляника,
крыжовник, черная и красная смородина,
малина, шиповник.
Последний по содержанию железа является
чемпионом среди перечисленных плодов
и ягод. Детям более старшего возраста
предпочтительнее давать их в натуральном
виде, что значительно повышает пищевую
ценность фруктово-ягодных добавок.
В
питании ребенка, больного анемией,
особое внимание следует уделить
своевременному и рациональному
использованию блюд прикорма. В качестве
первого прикорма
детям, как правило, рекомендуется давать
овощное пюре, являющееся источником
минеральных веществ. Более
того, больному ребенку овощное пюре
необходимо начать давать на 2—3 недели
раньше, чем здоровому, т. е. с
3,5-месячного
возраста.
Особенно
богаты железом
белокочанная и цветная
капуста, морковь, редис, редька, свекла,
томаты, зеленый горошек.
В редисе, свекле, а также в картофеле,
баклажанах содержится значительное
количество меди.
Через
3—4 недели после
введения первого прикорма малышу
начинают давать
второй прикорм —
молочную кашу
из рисовой, овсяной, гречневой или манной
крупы. При анемии
особенно полезны овсяная
и гречневая крупы,
превосходящие все остальные по содержанию
железа и меди.
Высокую пищевую ценность
для малыша, страдающего анемией, имеет
желток
куриного яйца.
Он содержит полноценные высокоусвояемые
белки, а также значительное количество
железа, меди, кобальта, марганца.
С
четырехмесячного
возраста и до конца первого года жизни
ежедневная норма желтка — 1/2.
Исключительно
важную роль в питании ребенка, больного
анемией, играют мясные
продукты. Их
пищевая ценность в первую очередь
определяется животным
белком, необходимым для образования
гемоглобина.
Кроме того, в состав мяса
входят жиры,
минеральные соли, витамины,
различные экстрактивные вещества,
облегчающие усвоение пищи. Поэтому
грудным детям, больным анемией, мясо
начинают давать с пятимесячного
возраста
(напомним, что в рацион здорового ребенка
мясо вводится лишь к концу
седьмого месяца жизни).
Особенно полезна при
анемии печень
(говяжья, телячья), богатая не только
полноценным белком, но и биологически
активными фосфатидами липидов,
а также легкоусвояемыми соединениями
железа и меди, необходимыми для синтеза
гемоглобина. Нежная структура ткани
печени позволяет рано включать ее в
рацион малыша.
1)
Рекомендуемые часы
кормлений: при 7-разовом питании - 6, 9,
12, 18, 21, 24 ч; при 6-разовом — 6 ч, 9 ч 30 мин,
13 ч, 16 ч 30 мин, 20 ч, 23 ч 30 мин; при 5-разовом
- 6, 10, 14, 18, 22 ч. Допустимы отклонения от
режима в пределах получаса. Причем важны
не столько конкретные часы кормлений,
сколько промежутки между кормлениями.
Разумеется, и в случае смешанного
вскармливания ночные прикладывания к
груди не запрещают, поскольку они, как
указывалось выше, способствуют поддержанию
лактации.
2) Объем
пищи в сутки при искусственном
вскармливании должен быть таким же,
как и при естественном вскармливании:
Суточный
объём пищи, необходимый грудному
ребёнку.:
Суточное
количество пищи составляет:
в возрасте от 10 дней (2 недели) до 1,5
месяцев (6 недель) — 1/5 часть фактической
массы тела;
в возрасте 1,5 (6 недель)
-4 месяцев - 1/6 часть
от долженствующей массы тела;
в
возрасте 4- 6 месяцев - 1/7 часть
от долженствующей массы тела;
в
возрасте старше 6 месяцев - 1/8 массы тела.
Соотношение
между основными пищевыми компонентами
(белками, жирами,
углеводами) до
введения прикорма должно составлять
1:3:6,
после введения прикорма - 1:2:4.
До 4-6 мес
потребность в белках
составляет 2-2,5 г/кг,
жирах - 6,5 г/кг,
углеводах - 13 г/кг,
а после
введения прикорма -
соответственно 3-3,5,
6-6,5 и 13 г/кг.
3) потребность ребенка в калориях,
белках, жирах и углеводах, а также
соотношение между пищевыми ингредиентами
зависит от той молочной смеси, которой
вскармливается ребенок.
При
вскармливании
детей смесями "Малютка", "Малыш",
"Виталакт"
энергетическая потребность сохраняется
такой же, как и при естественном
вскармливании:
в I четверть первого
года жизни- 120 ккал/кг массы;
во II -
115 ккал/кг массы;
в III - 110 ккал/кг массы;
в IV- 100 ккал/кг массы;
в белке
2,5-3,0 г/кг массы, в
жире 7,0-5,0
(в зависимости от первого - второго
полугодия первого года жизни), в углеводах
12-14 г/кг массы в
сутки. При этом соотношение между
белками, жирами, углеводами приближается
к 1 : 3 : 5.
54.Особенности
вскармливания детей с рахитом, анемией,
аллергодерматозом.
Больному
рахитом ребенку
надо как можно
дольше сохранять грудное вскармливание.
Но это не исключает необходимости
проводить необходимую коррекцию его
рациона. Нарушение при рахите обмена
минеральных веществ и витаминов, особенно
значительное снижение в крови витаминов
группы В и аскорбиновой кислоты, требуют
тщательного контроля за содержанием
витаминов в рационе ребенка. При
вынужденном
переводе ребенка на смешанное и
искусственное вскармливание
необходимо помнить, что минеральные
соли, в том числе кальций
и фосфор, из коровьего молока усваиваются
хуже, чем из
грудного несмотря на то, что абсолютное
содержание их выше. Поэтому более
рационально при организации смешанного
и искусственного вскармливания
использовать
адаптированные молочные смеси,
приближенные по основным пищевым
веществам и минеральному составу к
женскому молоку.
Очень
важно своевременно вводить фруктовые
и овощные соки и пюре, овощные отвары,
желток, творог и другие продукты,
содержащие в достаточном количестве
пищевые вещества и витамины. Детям с
проявлениями рахита настоятельно
рекомендуется в качестве первого
I прикорма овощное
пюре, которое в ряде случаев дается
раньше обычных сроков — с 3,5—4 мес.
Второй прикорм
— каша на овощном отваре или с добавлением
овощей и фруктов. С 5 мес ребенку
рационально назначить печень
в виде суфле.
Мясное пюре можно вводить с 6—6,5 мес,
чередуя его с пюре из куриного
мяса, печени, почек, мозгов.
При
наличии у ребенка признаков рахита
необходимо использовать продукты
с высоким содержанием кальция
и фосфора. В
рацион этих детей целесообразно вводить
кисломолочные продукты, благотворно
влияющие на процессы усвоения пищевых
веществ, в том числе кальция. При этом,
выбирая исходные продукты, следует
обращать внимание на содержание в них
витамина
С, солей кальция и фосфора.
Этими компонентами богаты черная
смородина, шиповник,
лимон, апельсин, кизил, вишня, черешня,
хурма. Все блюда
желательно обогащать хорошо
измельченной огородной зеленью.
Необходимо также часто использовать в
питании яичный
желток, богатый
жирорастворимыми витаминами, солями
кальция, фосфора, микроэлементами. Кроме
того, в нем содержится витамин D (от 200
до 500 ME в 100 г). В качестве полноценного
животного белка и кальция в пищевой
рацион систематически вводятся творог
и мясо. При
разработке рационов для этих детей в
первую очередь внимание уделяется
достаточному поступлению белка
и жира,
которые принимают самое активное участие
в процессах всасывания витамина D,
кальция и фосфора.
Поступающие в организм белки должны
быть полноценными
по аминокислотному
составу.
Анемия
значительно чаще
возникает у детей, находящихся на
искусственном вскармливании,
и особенно у тех, кто потребляет коровье
молоко. В то же время у детей, вскармливаемых
грудью, заболевание развивается редко.
По содержанию железа и
меди, а также по витаминному составу
оно значительно превосходит коровье,
в котором после обязательной пастеризации
значительная часть витаминов разрушается.
Важно обеспечить ребенка, больного
анемией, достаточным
количеством
белка,
железа
и таких минеральных
веществ, как
медь,
цинк, марганец
и др., являющихся
основным материалом для построения
гемоглобина. Основными источниками
указанных компонентов являются мясные
продукты, в том числе печень,
язык. Помимо
диетотерапии необходимо использовать
лекарственные препараты
железа, которые дают сразу после
кормления,
желательно в сочетании с аскорбиновой
кислотой, а
также с натуральными или консервированными
(лучше специализированными – для
детского питания) соками из черной
смородины, облепихи,
цитрусовых.
Если
же ребенок находится на искусственном
вскармливании, то
для его питания необходимо использовать
адаптированные
молочные смеси,
специально
предназначенные для детей с анемией.
Для
некоторых категорий больных детей, в
лечении которых важнейшее значение
имеет лечебное
питание,
промышленностью выпускаются так
называемые энпиты
— сухие
лечебные молочные смеси.
Они обладают повышенной биологической
ценностью как за счет специальной
обработки белкового
и жирового
компонентов, так и в результате обогащения
этих смесей витаминами A, D, Е, В1, В2, В6,
РР, C, а также железом.
Для
питания детей различного возраста,
больных анемией, создан "Энпит
противоанемический",
который содержит повышенное
количество белка и железа
и обогащен водо- и жирорастворимыми
витаминами. Это мелкий порошок
серовато-коричневого
цвета со специфическим запахом и
вкусом.
(Для
приготовления 100 мл жидкого продукта в
чистую посуду наливают 30—40 мл холодной
кипяченой воды, растворяют в ней 15 г
сухого порошка до исчезновения комочков,
добавляют воду до 100 мл, нагревают до
кипения и кипятят 1—2 минуты при
непрерывном помешивании. После охлаждения
до 36—38° смесь готова к употреблению.
При необходимости готовый жидкий продукт
можно хранить в холодильнике в течение
суток, подогревая его перед употреблением
до 36—38°.)
Поскольку противоанемический
энпит имеет специфический вкус и запах,
а также темный цвет, дети нередко
отказываются принимать его в чистом
виде. При вскармливании ребенка первого
года жизни энпит обычно добавляют
в грудное молоко или заменяющую его
детскую молочную смесь,
равномерно распределяя суточную
порцию.
Здоровым детям, как правило,
соки начинают давать с трехнедельного
— месячного возраста,
а пюре — с 1,5 месяцев. При
анемии же эти добавки необходимо
назначать раньше:
соки — с двух
недель, пюре —
с месячного
возраста.
Для приготовления
фруктовых и ягодных соков можно
использовать самые разнообразные фрукты
и ягоды, но в первую очередь те, которые
богаты железом,
медью и другими
микроэлементами. Это яблоки,
сливы, вишни, груши, абрикосы, персики,
лимоны, садовая земляника,
крыжовник, черная и красная смородина,
малина, шиповник.
Последний по содержанию железа является
чемпионом среди перечисленных плодов
и ягод. Детям более старшего возраста
предпочтительнее давать их в натуральном
виде, что значительно повышает пищевую
ценность фруктово-ягодных добавок.
В
питании ребенка, больного анемией,
особое внимание следует уделить
своевременному и рациональному
использованию блюд прикорма. В качестве
первого прикорма
детям, как правило, рекомендуется давать
овощное пюре, являющееся источником
минеральных веществ. Более
того, больному ребенку овощное пюре
необходимо начать давать на 2—3 недели
раньше, чем здоровому, т. е. с
3,5-месячного
возраста.
Особенно
богаты железом
белокочанная и цветная
капуста, морковь, редис, редька, свекла,
томаты, зеленый горошек.
В редисе, свекле, а также в картофеле,
баклажанах содержится значительное
количество меди.
Через
3—4 недели после
введения первого прикорма малышу
начинают давать
второй прикорм —
молочную кашу
из рисовой, овсяной, гречневой или манной
крупы. При анемии
особенно полезны овсяная
и гречневая крупы,
превосходящие все остальные по содержанию
железа и меди.
Высокую пищевую ценность
для малыша, страдающего анемией, имеет
желток
куриного яйца.
Он содержит полноценные высокоусвояемые
белки, а также значительное количество
железа, меди, кобальта, марганца.
С
четырехмесячного
возраста и до конца первого года жизни
ежедневная норма желтка — 1/2.
Исключительно
важную роль в питании ребенка, больного
анемией, играют мясные
продукты. Их
пищевая ценность в первую очередь
определяется животным
белком, необходимым для образования
гемоглобина.
Кроме того, в состав мяса
входят жиры,
минеральные соли, витамины,
различные экстрактивные вещества,
облегчающие усвоение пищи. Поэтому
грудным детям, больным анемией, мясо
начинают давать с пятимесячного
возраста
(напомним, что в рацион здорового ребенка
мясо вводится лишь к концу
седьмого месяца жизни).
Особенно полезна при
анемии печень
(говяжья, телячья), богатая не только
полноценным белком, но и биологически
активными фосфатидами липидов,
а также легкоусвояемыми соединениями
железа и меди, необходимыми для синтеза
гемоглобина. Нежная структура ткани
печени позволяет рано включать ее в
рацион малыша.
Экссудативный диатез является выражением аллергической перестройки организма ребенка. У большинства детей с экссудативным диатезом на первый план выступают явления так называемой пищевой аллергии (повышение чувствительности к пищевым продуктам). Из пищевого рациона детей, страдающих атопическим дерматитом, исключают продукты, содержащие пищевые добавки (красители, консерванты, эмульгаторы), а также бульоны, острые, соленые, жареные блюда, копчености, пряности, консервированные продукты, печень, рыбу, икру, морепродукты, яйца, сыры острые и плавленые, мороженое, кетчуп, грибы, орехи, тугоплавкие жиры и маргарин, газированные фруктовые напитки, квас, кофе, какао, мед, шоколад, карамель, торты, кексы. Ребенка, страдающего атопическим дерматитом, желательно держать на грудном вскармливании. Из диеты кормящей матери исключаются облигатные аллергены (цитрусовые, тропические фрукты, клубника, шоколад, икра, рыба, яйца, крепкий чай, кофе, острые сыры, пряности, копчености и т.д.), а также продукты, вызывающие аллергические реакции у конкретного ребенка . Кроме того, кормящим мамам не следует перегружать свой рацион продуктами из свежего молока — лучше заменить их кисломолочными. Детям, находящимся на смешанном и искусственном вскармливании , следует максимально сократить поступление белка коровьего молока. Необходимо следить, чтобы используемые смеси были адаптированными, до 1/3-1/2 суточного рациона могут составлять кисломолочные смеси. При выраженной реакции на молоко применяются специальные смеси для детей с аллергией к белкам коровьего молока или смеси, рекомендованные при поливалентной аллергии (в частности, приготовленные на основе сои). К сожалению, аллергия на белок коровьего молока в 20-30% случаев сопровождается реакцией и на соевый белок. В таком случае назначают смеси на основе гидролизатов белка. Высокой сенсибилизирующей активностью обладают также белок куриного яйца, глютен, белок банана, рыбы. Причиной аллергии у детей первого года жизни в 20–25% случаев является белок сои. В настоящее время участились аллергические реакции на белки злаковых культур — гречиха, кукуруза, рис. В питании детей первого года жизни, страдающих аллергией, используются две основные группы искусственных смесей: -лечебные смеси, приготовленные на основе гидролизатов молочного белка (сывороточных белков или казеина); В смесях «Нутрамиген» и "Прегестимил" источником белка является ферментативный гидролизат казеина, содержащий аминокислоты и небольшие белковые молекулы, которые для снижения аллергенности были подвергнуты обработке активированным углем. -соевые смеси (на основе изолята соевого белка). Кисломолочные продукты обладают антибактериальными свойствами и нормализуют микрофлору кишечника, которая нарушается при экссудативном диатезе. Наличие в них молочной кислоты способствует лучшему усвоению кальция, снижающего аллергическую "настроенность” организма. Для детей первых месяцев жизни предпочтительнее использовать адаптированные смеси— ацидофильную смесь «Малютка», "Балбобек", кисломолочный «Витолакт». С третьего месяца можно давать "Биолакт", "Балдырган", кефир, но при наличии адаптированных ацидофильных продуктов целесообразнее использовать именно их. Детям первых двух месяцев жизни ацидофильные смеси лучше давать по 10—20 мл перед каждым грудным кормлением.
При
производстве первой группы смесей
(«гидролизатов») используются различные
виды обработки молочного белка: ферментный
гидролиз, ультрафильтрация, нагревание.
В результате этой обработки образуются
высоко- и низкомолекулярные петиды, а
также свободные аминокислоты. При этом
чем меньше молекулярная масса
образовавшихся пептидов, тем меньшей
аллергизирующей активностью обладает
смесь.
Не следует
торопиться с прикормом,
если ребенок страдает диатезом. Чем
позже будет введен прикорм, тем выше
вероятность того, что пищеварительная
система и ферменты малыша «дозреют», и
продукт будет
нормально усваиваться.
В любом случае, не
следует вводить прикорм раньше
5-6-месячного возраста.
Прикорм
вводят с особой осторожностью, фиксируя
реакцию на каждый новый продукт в
специальном «пищевом» дневнике. Каждый
продукт вводят, начиная с минимального
его количества (пол чайной ложечки),
постепенно увеличивая (удваивая)
дозу и в течение
нескольких недель доводя до возрастной
нормы. При появлении аллергической
реакции продукт отменяют (попробовать
ввести его вновь можно будет только
через полгода).
Начинать необходима
с яблочного сока,
предпочтительнее из яблок зеленых
сортов (антоновка, ренет Семиренко,
белый налив и пр.). Как правило, не вызывают
аллергической реакции соки из белой
смородины, грушевый, капустный, а из
фруктовых пюре — яблочное, грушевое,
банановое. Фруктовое
пюре начинают вводить с 5 г, постепенно
увеличивая его объем до возрастной
нормы. В качестве
первого прикорма рекомендуется
использовать овощное пюре, но вводить
его можно значительно раньше — 5-месячного
возраста. Второй
продукт можно добавить лишь через 3—4
дня, если хорошо
переносится первый. Так постепенно
увеличивают ассортимент овощей в блюде,
добавляя цветную капусту, брюкву, репу,
тыкву. Любую кашу нужно варить не на
цельном молоке, а на разведенном на 1/2
или 2/3 водой. Однако если у ребенка на
коровье молоко возникает выраженная
аллергическая реакция, то в этом случае
молоко необходимо полностью исключить,
а кашу готовить на овощном или фруктовом
отварах. Крупу перед варкой рекомендуется
предварительно вымочить в холодной
воде в течение 12—18 часов.
Продукты,
наиболее часто вызывающие аллергические
реакции, следует вводить в последнюю
очередь и очень осторожно. В зависимости
от возраста к ним относятся:
До
1 года. Основные аллергены:
коровье молоко, а точнее, белок коровьего
молока или молочный сахар (лактоза),
пюре и соки из оранжевых или красных
плодов. Признаки диатеза: частый и жидкий
стул с пеной или зеленоватым оттенком,
боли в животике, сыпь, покраснения на
щечках.
От 1 года
до 3 лет. Основные аллергены:
цитрусовые, фрукты и ягоды с красной
окраской (клубника, малина, вишня, персики
и пр.), злаковые культуры. Признаки
диатеза: нарушение стула, першение в
горле, захлебывающийся кашель, зуд кожи
или сыпь.
Старше
3 лет. Основные аллергены:
шоколад, какао, арахис, крабы, креветки,
раки, рыба, соленья, маринады и приправы.
Проявления: сыпь или зуд кожи.
55.Понятие
пищевых добавок (виды, состав, сроки
введения).
Первая
пищевая добавка в 4 мес.:
Фруктовые соки
(пюре) - яблочный,
из белой черешни, из белой смородины,
абрикосовый, персиковый,
грушевый, сливовый (даны в порядке
предпочтения). Начинают вводить в рацион
с капель, постепенно увеличивая количество
до 40-60 мл. Желательно чтобы первые соки
ребенка были натуральными и свежими
(домашнего приготовления). Соки
содержат также значительные количества
калия и железа. Апельсиновый,
мандариновый, клубничный соки,
принадлежащие к числу продуктов с
высокой потенциальной аллергенностью,
не следует давать детям младше 6—7
месяцев.
До 6 месяцев
ребенку дают пюре из одного фрукта,
после 6 месяцев можно давать поликомпонентные
пюре. Не забывайте
вводить в рацион ребенка черносливовое
пюре. Чернослив
мягко нормализует работу кишечника, а
также является чемпионом среди фруктов
по содержанию антиоксидантов, которые
укрепляют иммунитет. Также для зрения
вашего малыша очень полезно черничное
пюре.
«Обучающий» прикорм лучше
давать ребенку во второе кормление,
после того как он высосал немного молока
из груди, еще сохранил чувство голода,
но получил удовольствие от кормления.
Небольшое количество фруктового пюре
с кончика чайной ложки вводят на среднюю
часть языка ребенка.
Творог
(кальцинированный) так же желателен
домашнего приготовления - на 200 мл молока
в момент закипания добавляется 1-2
столовые ложки СаСl2 , затем откидывается
на марлю, или молочной кухни, специального
детского питания. Начинают вводить в
рацион с крупинок и доводят до 40 грамм
в сутки.
Яичный
желток вкрутую сваренного яйца.
С 6 мес.
С крупинок до 1/12 – 1/8 добавляют в молоко
или овощное пюре (с осторожностью вводить
в рацион аллергиков). Если
у ребенка есть какая-то пищевая аллергия,
то в этом случае сроки введения желтка
продлеваются; Белок
вводят в рацион ребенка с 1,5 лет,
т.к. белок является аллергенным
продуктом.
56.Молочные
кухни, их значение в организации
рационального вскармливания детей
раннего возраста.
Небольшую
молочную кухню возглавляет средний
медицинский работник, крупные молочные
кухни — врач.
Молочная кухня — это
пищевое предприятие, оснащенное всеми
видами современных механизмов, установок
и приспособлений для приготовления,
хранения
и отпуска
детской
пищи в строго
гигиенических условиях. Как правило,
для удобства населения при молочной
кухне создаются несколько раздаточных
пунктов в отдельных местах города или
района.
Молочная кухня - учреждение
общественного питания, задача которого
— приготовление
пищевых смесей для здоровых детей
грудного возраста,
находящихся на смешанном и искусственном
вскармливании, для детей, получающих
прикорм, а также для больных детей первых
3 лет жизни.
Важную роль в правильной
организации питания детей первых месяцев
жизни играют донорские,
сливные пункты по сбору женского молока,
которые обычно организуются при молочных
кухнях или при детских консультациях-поликлиниках.
Здоровые женщины,
имеющие избыток молока,
привлекаются в качестве доноров.
Мать-донор находится под систематическим
врачебным контролем не реже 1 раза в
месяц. Первичное обследование проводят
терапевт, фтизиатр, венеролог. Собирают
и хранят донорское молоко в максимально
гигиенических условиях.
Одна из них является приемной, где
женщина-донор раздевается, надевает
специальный халат и моет руки. Во второй
комнате происходит сцеживание
молока.
Получить
питание в молочной кухне можно только
по рецепту врача,
необходим также предварительный
заказ на питание,
т.е. питание
можно получить на второй день после
сдачи рецепта и его оплаты.
В молочной кухне отпускают также питание
бесплатно по документам, которые
оформляются участковым врачом и
участковой медицинской сестрой.
Бесплатное, льготное питание получают
многодетные семьи, одинокие матери и
ряд других категорий.
Молоко на
молочную кухню доставляется на специальном
транспорте в запломбированных бидонах
или цистернах. При приеме молока
определяется его кислотность
по Тернеру
(принимается
молоко, у которого кислотность
не более 20 °Т).
Жирность
молока должна составлять 3—4
%.
Обычно молоко
на молочные кухни доставляется со
специальных молочных ферм, на которых
установлен усиленный ветеринарный и
санитарный надзор. Таким образом, молоко
является полноценным по своим питательным
качеством и минимально загрязненным
бактериальной флорой.
Такое молоко называется гарантийным.
Как правило, молоко доставляется рано
утром и в тот же день перерабатывается.
Сразу же после поступления на молочную
кухню молоко должно быть
профильтровано.
Приготовление
молочных смесей,
молочных каш, овощных и мясных блюд
проводится в варочном цехе по определенной
технологии. Приготовление кисломолочных
блюд производится в отдельной комнате
(где температура
поддерживается в пределах 21—22
°С) — кефирном
цехе. Это светлая
теплая комната, выложенная кафелем и
выкрашенная масляной краской. В этой
комнате должна соблюдаться особенная
чистота для того, чтобы не занести
случайно в молоко вместе с кефирной
закваской других микроорганизмов. В
кефирный
цех доставляется кипяченое молоко в
больших емкостях и в мерных бутылочках.
Здесь к молоку добавляют
кефирную
закваску и оставляют его до утра
следующего дня.
Утром кефир в бутылочках отправляют
в комнату для выдачи и хранят его в
холодильнике. Из
остального кефира готовят творог.
Приготовление
творога: кастрюлю
с кефиром ставят на специальные печи,
на которых она подогревается до 70—80
°С. Кефир
створаживается.
Затем при помощи центрифуги отделяют
творог от сыворотки и при необходимости
протирают творог сквозь сито или сразу
непотертый творог развешивают по
порциям. Таким же образом, как кефир и
творог, из сухой закваски готовят
ацидофильно-дрожжевое
молоко и ацидофильно-дрожжевую
пасту.
57.Потребность
в пищевых ингредиентах у здорового
ребенка старше года.
Дети
от 1 года до 3 лет
должны получать на
1 кг массы тела
4,3—4,0 г белка,
4,3—4,0 г жира,
17,0—16,0 г углеводов;
в возрасте от 3 до
7 лет —3,8—3,5
г белка, 3,8-3,5
г жира и примерно
15—14 г углеводов.
Например:
средний показатель массы тела ребенка
от 1 года до 1,5 лет — около 11 кг, потребность
в белке —4,3 г, суточная потребность в
белке для него составляет: 11 * 4,3 = 47,3
г, примерно 47—48
г.
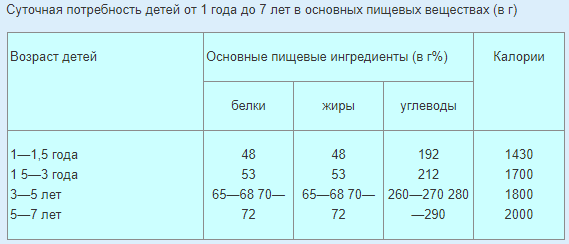 По-прежнему
большая роль принадлежит молоку и
молочным продуктам, которые должны
входить в ежедневный рацион ребенка
(молоко в любом
виде до 500-600 мл,
творог в среднем
50 г, сливки или
сметана 5 г).
Творог, сливки, сметану можно давать
через 1-2 дня, но в соответствующем
количестве.
Из мясных продуктов детям
старше года рекомендуются наряду с
говядиной мясо
кур, цыплят, кролика, нежирная свинина
и баранина.
Увеличивается
количество рыбы.
В среднем ребенку от 1 года до 3 лет
требуется 85 г мяса
и 25 г рыбы
в сутки. В течение недели он может
получать 4-5 дней мясо (по 100-120 г) и 2-3 дня
рыбу (по 70-100 г).
Ребенку старше года
можно давать целое
яйцо (через день,
либо по половине ежедневно), а не только
желток. Однако делать это надо с
осторожностью, так как у некоторых детей
белок куриного яйца может вызвать
аллергическую реакцию. В таких случаях
от белка следует отказаться и какое-то
время давать только желток.
Среди
круп полезны
овсяная и гречневая, разрешается ячневая,
перловая, пшеничная.
Макаронные
изделия (лапша,
вермишель) дают нечасто, так как они
бедны
витаминами и содержат избыток углеводов.
Бобовые
(горох, фасоль, соя) даются в ограниченном
количестве детям старше 1,5 лет в виде
протертых супов.
В среднем ребенку
требуется в сутки 15-20
г крупы, 5
г макаронных
изделий, около 100
г хлеба (в том числе
30-40 г ржаного), хлебобулочные изделия
(сухарики, баранки, булочки) при
соответствующем уменьшении количества
хлеба.
Основным
источником углеводов
в питании ребенка старше года является
сахар, однако его количество должно
быть строго ограничено. «Передозировка»
сахара может привести к нарушению обмена
веществ, избыточной массе тела, иногда
к ухудшению аппетита. Ребенку до 3 лет
требуется от 35 до
50 г сахара в сутки.
Общее количество
кондитерских изделий не
должно превышать 10-15 г в
сутки.
Овощи
разнообразные,
включая редис, редьку, зеленый лук,
чеснок, а также листовую зелень (укроп,
петрушку, щавель, шпинат, салат, крапиву).
В день ребенку нужно около 120-150
г картофеля и до
200 г других овощей.
В ежедневный рацион должны входить
свежие фрукты,
ягоды (до 200 г) и
соки (100-150 мл).
До
1,5 лет ребенок обычно находится еще на
5-разовом кормлении,
хотя некоторые дети уже в этом возрасте
отказываются от последнего (ночного)
кормления и переходят на 4-разовый прием
пищи: завтрак, обед, полдник и ужин.
Между кормлениями ребенку нельзя
давать какую-либо пищу, особенно сладости,
так как это приводит к нарушениям
нормального пищеварения и снижению
аппетита. Сказанное относится и к
фруктовым сокам, которые иногда
предлагаются ребенку вместо питья. В
таком случае лучше использовать морсы,
компоты, неподслащенные настои трав.
Нужно
следить, чтобы ребенок
получал соответствующий его возрасту
объем пищи. Так,
для ребенка в возрасте от
1 года до 1,5 лет он
должен составлять в среднем 1000-1200
мл, от 1,5
до 3 лет - 1400-1500
мл (соки, отвары и
другое питье в этот объем не входят).
Уменьшение количества пищи может
привести к недоеданию, превышение - к
снижению аппетита. Особенно нерационально
увеличивать объем первого блюда, что
нередко делают родители, если ребенок
охотно ест суп или бульон. Однако съев
много супа, ребенок не может уже справиться
со вторым блюдом, которое, как правило,
бывает более полноценным, так как
содержит мясо, овощи.
Содержание
калорий при пятикратном кормлении
в процентах к суточной калорийности
пищи:
Первый завтрак - около 20%.
Второй
завтрак - около 10-15%.
Обед - около
35-40%.
Полдник - около 10-15%.
Ужин
- около 20%.
58.Основные
принципы питания детей старше года.
Главные
требования к питанию ребенка после года
— разнообразие и
сбалансированность
по основным элементам питания. Основу
пищевого рациона малыша после года
должны составлять продукты
с большим содержанием животного белка:
молоко и молочные продукты, мясо, рыба,
птица, яйца. Овощи, фрукты, картофель,
сахар, хлеб, мясо, молоко ребенок должен
получать ежедневно. Сыр, творог, сметану,
рыбу, яйца, крупы дают несколько раз в
неделю из расчета их недельной
нормы.
По-прежнему большая роль
принадлежит молоку и молочным продуктам,
которые должны входить в ежедневный
рацион ребенка (молоко
в любом виде до 500-600 мл,
творог в среднем
50 г, сливки или
сметана 5 г).
Творог, сливки, сметану можно давать
через 1-2 дня, но в соответствующем
количестве.
Из мясных
продуктов детям
старше года рекомендуются наряду с
говядиной мясо
кур, цыплят, кролика, нежирная свинина
и баранина.
Увеличивается
количество рыбы.
В среднем ребенку от 1 года до 3 лет
требуется 85 г мяса
и 25 г рыбы
в сутки. В течение недели он может
получать 4-5 дней мясо (по 100-120 г) и 2-3 дня
рыбу (по 70-100 г).
Ребенку старше года
можно давать целое
яйцо (через день,
либо по половине ежедневно), а не только
желток. Однако делать это надо с
осторожностью, так как у некоторых детей
белок куриного яйца может вызвать
аллергическую реакцию. В таких случаях
от белка следует отказаться и какое-то
время давать только желток.
Среди
круп полезны
овсяная и гречневая, разрешается ячневая,
перловая, пшеничная.
Макаронные
изделия (лапша,
вермишель) дают нечасто, так как они
бедны
витаминами и содержат избыток углеводов.
Бобовые
(горох, фасоль, соя) даются в ограниченном
количестве детям старше 1,5 лет в виде
протертых супов.
В среднем ребенку
требуется в сутки 15-20
г крупы, 5
г макаронных
изделий, около 100
г хлеба (в том числе
30-40 г ржаного), хлебобулочные изделия
(сухарики, баранки, булочки) при
соответствующем уменьшении количества
хлеба.
Основным
источником углеводов
в питании ребенка старше года является
сахар, однако его количество должно
быть строго ограничено. «Передозировка»
сахара может привести к нарушению обмена
веществ, избыточной массе тела, иногда
к ухудшению аппетита. Ребенку до 3 лет
требуется от 35 до
50 г сахара в сутки.
Общее
количество кондитерских изделий не
должно превышать 10-15 г в
сутки.
Овощи
разнообразные,
включая редис, редьку, зеленый лук,
чеснок, а также листовую зелень (укроп,
петрушку, щавель, шпинат, салат, крапиву).
В день ребенку нужно около 120-150
г картофеля и до
200 г других овощей.
В ежедневный рацион должны входить
свежие фрукты,
ягоды (до 200 г) и
соки (100-150 мл).
До
1,5 лет ребенок обычно находится еще на
5-разовом кормлении,
хотя некоторые дети уже в этом возрасте
отказываются от последнего (ночного)
кормления и переходят на 4-разовый прием
пищи: завтрак, обед, полдник и ужин.
Между кормлениями ребенку нельзя
давать какую-либо пищу, особенно сладости,
так как это приводит к нарушениям
нормального пищеварения и снижению
аппетита. Сказанное относится и к
фруктовым сокам, которые иногда
предлагаются ребенку вместо питья. В
таком случае лучше использовать морсы,
компоты, неподслащенные настои трав.
Нужно
следить, чтобы ребенок
получал соответствующий его возрасту
объем пищи. Так,
для ребенка в возрасте от
1 года до 1,5 лет он
должен составлять в среднем 1000-1200
мл, от 1,5
до 3 лет - 1400-1500
мл (соки, отвары и
другое питье в этот объем не входят).
Уменьшение количества пищи может
привести к недоеданию, превышение - к
снижению аппетита. Особенно нерационально
увеличивать объем первого блюда, что
нередко делают родители, если ребенок
охотно ест суп или бульон. Однако съев
много супа, ребенок не может уже справиться
со вторым блюдом, которое, как правило,
бывает более полноценным, так как
содержит мясо, овощи.
Кулинарная
обработка пищи
для детей раннего возраста имеет свои
особенности, обусловленные своеобразием
их развития. До 1,5 лет малыш еще не имеет
достаточных возможностей для усвоения
грубой пищи, поэтому
его кормят пюре, жидкой кашей и
т. п. Но при этом ребенка надо приучать
есть более плотную пищу. Если дети
длительное время получают только
полужидкие и протертые блюда, у них
плохо развивается навык жевания и в
последующем они очень вяло и неохотно
едят мясо, сырые овощи и фрукты.
Детям
старше 1,5 лет дают
разваренные
(но уже не протертые) каши,
овощные и крупяные
запеканки, тушеные
овощи, нарезанные мелкими кусочками,
мясные и рыбные котлеты.
После
2 лет мясо
можно давать в виде жареных котлет,
мелко нарезанного рагу, рыбу
- вареную и жареную,
освобожденную от
костей.
Свежие
овощи в виде мелко нарезанных салатов,
а для детей до 1,5
лет - натертых
на крупной терке.
Салаты из сырых овощей можно давать не
только на обед, но и на завтрак и
ужин.
Молоко
можно кипятить не более 2-3 мин,
не допуская повторного кипячения. При
приготовлении каш, овощных пюре, запеканок
молоко добавляют в уже разваренные
крупы или овощи.
Мясо
после тщательной механической очистки
лучше варить крупным куском, опуская в
горячую воду. При этом на поверхности
мяса белки свертываются и мясной сок
не вытекает. Жарить мясо, котлеты надо
в кипящем жире, что также способствует
образованию корочки, удерживающей
мясной сок. Тушеное
мясо готовится путем легкого обжаривания
и затем варки в небольшом количестве
воды.
Очень
важно правильно обрабатывать овощи.
При чистке срезать как можно более
тонкий слой, именно в верхних слоях
содержится наибольшее количество
витаминов. Для
винегретов и салатов овощи лучше варить
в кожуре в небольшом количестве воды
или на пару.
Очищенные овощи нельзя надолго оставлять
в воде, чтобы не произошло вымывание
витаминов и минеральных веществ, а
варить их надо в малом количестве воды,
используя потом ее в пищу. Время
варки строго ограниченное:
картофель, капусту, морковь варят не
более 25-30 мин, свеклу - 1-1,5 ч, щавель,
шпинат - до 10 мин.
Овощи
и фрукты для сырых салатов
чистят и нарезают (натирают) непосредственно
перед приемом пищи, так как при воздействии
кислорода воздуха на очищенные и
измельченные продукты в них происходит
разрушение витаминов, особенно
аскорбиновой кислоты.
59.Гипоксические
поражения ЦНС у новорожденных. Этиология,
патогенез, Основные клинические
проявления.
Перинатальное
поражение ЦНС у новорожденных, проявляется
нарушениями в работе двигательного
аппарата, нарушением речи и психики.
Гипокс.
поражения-группа
патол. состояний, обусловленных
воздействием на НС плода или новорожденного
неблагоприятных факторов в антенатальном
периоде, начиная с 28 нед, во время родов
и первые 7 дн после рождения.
Перинатальное
поражение центральной нервной системы
(ППЦНС) — это не один, а несколько
диагнозов, которые подразумевают
нарушение функций работы в головном
мозге новорожденного ребенка и могут
привести к стойким неврологическим
последствиям в более старшем возрасте
(например, ДЦП, ЗПРР).
Основная
причина- внутиутр.
гипоксия при отягощенном соматич. и
акуш-гинек. анамнезе женщины, др.
повреждения-травм, метаболич.,
инфекц.
Причины, по которым может
развиться перинатальное поражение
центральной нервной системы достаточно
разнообразны, среди самых популярных:
–
соматическое заболевание
матери, которое сопровождается хронической
интоксикацией;
–
наличие острых инфекционных
заболеваний или
хронических очагов инфекции, в то время
когда будущая мать вынашивала ребенка;
–
в случае, если у женщины нарушен
процесс питания, или же она не созрела
для беременности и родов;
–
нарушение
маточно-плацентарного
кровотока во
время беременности;
– изменения
в обмене веществ
также влечет за
собой расстройство нервной системы у
будущего ребенка (повышение уровня
биллирубина, неонатальная желтуха);
–
в случае сильного
токсикоза, как на ранней стадии,
так и на поздней, или появление иных
проблем с вынашиванием ребенка;
–
окружающая среда выступает немаловажным
фактором в развитии заболевания;
–
появление патологии во время родов
— это может быть слабая
родовая деятельность,
ускоренные роды;
–
если ребенок рождается недоношенным,
то и его организм не развит полностью,
поэтому на данном фоне может появиться
нарушение в работе ЦНС;
Если четко
зафиксирован недостаток кислорода,
во время нахождения малыша внутри
организма матери (гипоксия), то
диагностируют гипоксическое
поражение ЦНС.
Хроническая
гипоксия плода
развивается при осложненном течении
беременности, фето-плацентарной
недостаточности или при заболеваниях
беременной, протекающих с гипоксемией
(пороки сердца, тяжелая анемия, хронические
болезни легких).
Острая
гипоксия (асфиксия)
чаще возникает в процессе родов в
результате нарушения маточно-плацентарного
кровообращения при преждевременной
отслойке плаценты,
пролапсе пуповины,
аномальном предлежании плода и плаценты,
гипертонусе и разрывах матки, острой
гипоксии у роженицы, а также вследствие
замедления кровотока при сжатии головки
плода и полости малого таза.
Патогенез.
Общим типом
поражения мозга для детей любого срока
гестации является также селективный
и диффузный некроз
нейронов.
Особенностью селективного некроза у
доношенных детей является его локализация
в коре головного мозга, таламусе,
мозжечке, стволе головного мозга и
спинном мозге, при этом острая
и тяжелая гипоксия
приводит, как правило, к стволовым
и спинальным
нарушениям, а
хроническая
и легкая гипоксия - к корковым.
При неблагоприятном исходе у детей
развиваются спастическая тетраплегия,
интеллектуальная
недостаточность, стволовая дисфункция,
судороги. У
недоношенных детей селективный некроз
нейронов преобладает в диэнцефальной
области и коре
головного мозга, что может сформировать
спастическую тетраплегию,
поражение краниальных
нервов, возможно, синдром дефицита
внимания и гипоталамический
синдром.
У плода гипоксия приводит
к сдвигу реакцию
крови и тканей в кислую сторону,
развивается метаболический ацидоз,
снижается активность ферментов,
обеспечивающих «синтез роста», нарушается
функция миокарда.
Появляются тахикардия и децелерация
сердечного ритма, экстрасистолии.
Регистрируется положительный –
нереактивный – нестрессовый
тест.
Продолжающаяся
гипоксия приводит
к активации
анаэробного гликолиза.
Нарастающий дефицит кислорода заставляет
организм снизить
оксигенацию кишечника, кожи, печени,
почек; происходит
перераспределение кровообращения с
преимущественным кровоснабжением
жизненно важных органов (головной мозг,
сердце, надпочечники). Централизация
кровообращения, в свою очередь, усугубляет
тканевой метаболический ацидоз
(резко увеличивается
в крови уровень лактата).
Развивается снижение двигательной
активности плода, частотной активности
на ЭЭГ, числа «дыхательных» экскурсий
грудной клетки, появляется
брадикардия.
Гипоксическая
энцефалопатия,
которая является грозным клиническим
проявлением тяжелой асфиксии, возникает,
прежде всего, вследствие
ишемии ткани головного мозга (артериальная
гипотензия при артериальном давлении
на локтевой артерии менее 50 мм рт. ст.,
тромбозы венул и артериол, нарушение
венозного оттока
из-за отека
головного мозга), дисэлектролитемии,
мелких кровоизлияний в ткань мозга и
субарахноидальное пространство. Наличие
таких кровоизлияний не служит главным
прогностическим признаком, как в остром
периоде, так и для дальнейшего
нервно-психического развития. Поражения
головного мозга обусловлены не только
изменениями его в момент гипоксии, но
и могут возникать в процессе реанимации
ребенка, в постгипоксическом периоде,
что объясняют накоплением в крови и
тканях избытка свободных радикалов и
продуктов перекисного окисления липидов
(«кислородный парадокс» - токсичность
избытка кислорода после периода
длительной гипоксии),
протеолитических ферментов, ионов
кальция, и др. Отсюда возникает опасность
чрезмерно активной, неконтролируемой
оксигенотерапии в неонатологии.
По-прежнему
большая роль принадлежит молоку и
молочным продуктам, которые должны
входить в ежедневный рацион ребенка
(молоко в любом
виде до 500-600 мл,
творог в среднем
50 г, сливки или
сметана 5 г).
Творог, сливки, сметану можно давать
через 1-2 дня, но в соответствующем
количестве.
Из мясных продуктов детям
старше года рекомендуются наряду с
говядиной мясо
кур, цыплят, кролика, нежирная свинина
и баранина.
Увеличивается
количество рыбы.
В среднем ребенку от 1 года до 3 лет
требуется 85 г мяса
и 25 г рыбы
в сутки. В течение недели он может
получать 4-5 дней мясо (по 100-120 г) и 2-3 дня
рыбу (по 70-100 г).
Ребенку старше года
можно давать целое
яйцо (через день,
либо по половине ежедневно), а не только
желток. Однако делать это надо с
осторожностью, так как у некоторых детей
белок куриного яйца может вызвать
аллергическую реакцию. В таких случаях
от белка следует отказаться и какое-то
время давать только желток.
Среди
круп полезны
овсяная и гречневая, разрешается ячневая,
перловая, пшеничная.
Макаронные
изделия (лапша,
вермишель) дают нечасто, так как они
бедны
витаминами и содержат избыток углеводов.
Бобовые
(горох, фасоль, соя) даются в ограниченном
количестве детям старше 1,5 лет в виде
протертых супов.
В среднем ребенку
требуется в сутки 15-20
г крупы, 5
г макаронных
изделий, около 100
г хлеба (в том числе
30-40 г ржаного), хлебобулочные изделия
(сухарики, баранки, булочки) при
соответствующем уменьшении количества
хлеба.
Основным
источником углеводов
в питании ребенка старше года является
сахар, однако его количество должно
быть строго ограничено. «Передозировка»
сахара может привести к нарушению обмена
веществ, избыточной массе тела, иногда
к ухудшению аппетита. Ребенку до 3 лет
требуется от 35 до
50 г сахара в сутки.
Общее количество
кондитерских изделий не
должно превышать 10-15 г в
сутки.
Овощи
разнообразные,
включая редис, редьку, зеленый лук,
чеснок, а также листовую зелень (укроп,
петрушку, щавель, шпинат, салат, крапиву).
В день ребенку нужно около 120-150
г картофеля и до
200 г других овощей.
В ежедневный рацион должны входить
свежие фрукты,
ягоды (до 200 г) и
соки (100-150 мл).
До
1,5 лет ребенок обычно находится еще на
5-разовом кормлении,
хотя некоторые дети уже в этом возрасте
отказываются от последнего (ночного)
кормления и переходят на 4-разовый прием
пищи: завтрак, обед, полдник и ужин.
Между кормлениями ребенку нельзя
давать какую-либо пищу, особенно сладости,
так как это приводит к нарушениям
нормального пищеварения и снижению
аппетита. Сказанное относится и к
фруктовым сокам, которые иногда
предлагаются ребенку вместо питья. В
таком случае лучше использовать морсы,
компоты, неподслащенные настои трав.
Нужно
следить, чтобы ребенок
получал соответствующий его возрасту
объем пищи. Так,
для ребенка в возрасте от
1 года до 1,5 лет он
должен составлять в среднем 1000-1200
мл, от 1,5
до 3 лет - 1400-1500
мл (соки, отвары и
другое питье в этот объем не входят).
Уменьшение количества пищи может
привести к недоеданию, превышение - к
снижению аппетита. Особенно нерационально
увеличивать объем первого блюда, что
нередко делают родители, если ребенок
охотно ест суп или бульон. Однако съев
много супа, ребенок не может уже справиться
со вторым блюдом, которое, как правило,
бывает более полноценным, так как
содержит мясо, овощи.
Содержание
калорий при пятикратном кормлении
в процентах к суточной калорийности
пищи:
Первый завтрак - около 20%.
Второй
завтрак - около 10-15%.
Обед - около
35-40%.
Полдник - около 10-15%.
Ужин
- около 20%.
58.Основные
принципы питания детей старше года.
Главные
требования к питанию ребенка после года
— разнообразие и
сбалансированность
по основным элементам питания. Основу
пищевого рациона малыша после года
должны составлять продукты
с большим содержанием животного белка:
молоко и молочные продукты, мясо, рыба,
птица, яйца. Овощи, фрукты, картофель,
сахар, хлеб, мясо, молоко ребенок должен
получать ежедневно. Сыр, творог, сметану,
рыбу, яйца, крупы дают несколько раз в
неделю из расчета их недельной
нормы.
По-прежнему большая роль
принадлежит молоку и молочным продуктам,
которые должны входить в ежедневный
рацион ребенка (молоко
в любом виде до 500-600 мл,
творог в среднем
50 г, сливки или
сметана 5 г).
Творог, сливки, сметану можно давать
через 1-2 дня, но в соответствующем
количестве.
Из мясных
продуктов детям
старше года рекомендуются наряду с
говядиной мясо
кур, цыплят, кролика, нежирная свинина
и баранина.
Увеличивается
количество рыбы.
В среднем ребенку от 1 года до 3 лет
требуется 85 г мяса
и 25 г рыбы
в сутки. В течение недели он может
получать 4-5 дней мясо (по 100-120 г) и 2-3 дня
рыбу (по 70-100 г).
Ребенку старше года
можно давать целое
яйцо (через день,
либо по половине ежедневно), а не только
желток. Однако делать это надо с
осторожностью, так как у некоторых детей
белок куриного яйца может вызвать
аллергическую реакцию. В таких случаях
от белка следует отказаться и какое-то
время давать только желток.
Среди
круп полезны
овсяная и гречневая, разрешается ячневая,
перловая, пшеничная.
Макаронные
изделия (лапша,
вермишель) дают нечасто, так как они
бедны
витаминами и содержат избыток углеводов.
Бобовые
(горох, фасоль, соя) даются в ограниченном
количестве детям старше 1,5 лет в виде
протертых супов.
В среднем ребенку
требуется в сутки 15-20
г крупы, 5
г макаронных
изделий, около 100
г хлеба (в том числе
30-40 г ржаного), хлебобулочные изделия
(сухарики, баранки, булочки) при
соответствующем уменьшении количества
хлеба.
Основным
источником углеводов
в питании ребенка старше года является
сахар, однако его количество должно
быть строго ограничено. «Передозировка»
сахара может привести к нарушению обмена
веществ, избыточной массе тела, иногда
к ухудшению аппетита. Ребенку до 3 лет
требуется от 35 до
50 г сахара в сутки.
Общее
количество кондитерских изделий не
должно превышать 10-15 г в
сутки.
Овощи
разнообразные,
включая редис, редьку, зеленый лук,
чеснок, а также листовую зелень (укроп,
петрушку, щавель, шпинат, салат, крапиву).
В день ребенку нужно около 120-150
г картофеля и до
200 г других овощей.
В ежедневный рацион должны входить
свежие фрукты,
ягоды (до 200 г) и
соки (100-150 мл).
До
1,5 лет ребенок обычно находится еще на
5-разовом кормлении,
хотя некоторые дети уже в этом возрасте
отказываются от последнего (ночного)
кормления и переходят на 4-разовый прием
пищи: завтрак, обед, полдник и ужин.
Между кормлениями ребенку нельзя
давать какую-либо пищу, особенно сладости,
так как это приводит к нарушениям
нормального пищеварения и снижению
аппетита. Сказанное относится и к
фруктовым сокам, которые иногда
предлагаются ребенку вместо питья. В
таком случае лучше использовать морсы,
компоты, неподслащенные настои трав.
Нужно
следить, чтобы ребенок
получал соответствующий его возрасту
объем пищи. Так,
для ребенка в возрасте от
1 года до 1,5 лет он
должен составлять в среднем 1000-1200
мл, от 1,5
до 3 лет - 1400-1500
мл (соки, отвары и
другое питье в этот объем не входят).
Уменьшение количества пищи может
привести к недоеданию, превышение - к
снижению аппетита. Особенно нерационально
увеличивать объем первого блюда, что
нередко делают родители, если ребенок
охотно ест суп или бульон. Однако съев
много супа, ребенок не может уже справиться
со вторым блюдом, которое, как правило,
бывает более полноценным, так как
содержит мясо, овощи.
Кулинарная
обработка пищи
для детей раннего возраста имеет свои
особенности, обусловленные своеобразием
их развития. До 1,5 лет малыш еще не имеет
достаточных возможностей для усвоения
грубой пищи, поэтому
его кормят пюре, жидкой кашей и
т. п. Но при этом ребенка надо приучать
есть более плотную пищу. Если дети
длительное время получают только
полужидкие и протертые блюда, у них
плохо развивается навык жевания и в
последующем они очень вяло и неохотно
едят мясо, сырые овощи и фрукты.
Детям
старше 1,5 лет дают
разваренные
(но уже не протертые) каши,
овощные и крупяные
запеканки, тушеные
овощи, нарезанные мелкими кусочками,
мясные и рыбные котлеты.
После
2 лет мясо
можно давать в виде жареных котлет,
мелко нарезанного рагу, рыбу
- вареную и жареную,
освобожденную от
костей.
Свежие
овощи в виде мелко нарезанных салатов,
а для детей до 1,5
лет - натертых
на крупной терке.
Салаты из сырых овощей можно давать не
только на обед, но и на завтрак и
ужин.
Молоко
можно кипятить не более 2-3 мин,
не допуская повторного кипячения. При
приготовлении каш, овощных пюре, запеканок
молоко добавляют в уже разваренные
крупы или овощи.
Мясо
после тщательной механической очистки
лучше варить крупным куском, опуская в
горячую воду. При этом на поверхности
мяса белки свертываются и мясной сок
не вытекает. Жарить мясо, котлеты надо
в кипящем жире, что также способствует
образованию корочки, удерживающей
мясной сок. Тушеное
мясо готовится путем легкого обжаривания
и затем варки в небольшом количестве
воды.
Очень
важно правильно обрабатывать овощи.
При чистке срезать как можно более
тонкий слой, именно в верхних слоях
содержится наибольшее количество
витаминов. Для
винегретов и салатов овощи лучше варить
в кожуре в небольшом количестве воды
или на пару.
Очищенные овощи нельзя надолго оставлять
в воде, чтобы не произошло вымывание
витаминов и минеральных веществ, а
варить их надо в малом количестве воды,
используя потом ее в пищу. Время
варки строго ограниченное:
картофель, капусту, морковь варят не
более 25-30 мин, свеклу - 1-1,5 ч, щавель,
шпинат - до 10 мин.
Овощи
и фрукты для сырых салатов
чистят и нарезают (натирают) непосредственно
перед приемом пищи, так как при воздействии
кислорода воздуха на очищенные и
измельченные продукты в них происходит
разрушение витаминов, особенно
аскорбиновой кислоты.
59.Гипоксические
поражения ЦНС у новорожденных. Этиология,
патогенез, Основные клинические
проявления.
Перинатальное
поражение ЦНС у новорожденных, проявляется
нарушениями в работе двигательного
аппарата, нарушением речи и психики.
Гипокс.
поражения-группа
патол. состояний, обусловленных
воздействием на НС плода или новорожденного
неблагоприятных факторов в антенатальном
периоде, начиная с 28 нед, во время родов
и первые 7 дн после рождения.
Перинатальное
поражение центральной нервной системы
(ППЦНС) — это не один, а несколько
диагнозов, которые подразумевают
нарушение функций работы в головном
мозге новорожденного ребенка и могут
привести к стойким неврологическим
последствиям в более старшем возрасте
(например, ДЦП, ЗПРР).
Основная
причина- внутиутр.
гипоксия при отягощенном соматич. и
акуш-гинек. анамнезе женщины, др.
повреждения-травм, метаболич.,
инфекц.
Причины, по которым может
развиться перинатальное поражение
центральной нервной системы достаточно
разнообразны, среди самых популярных:
–
соматическое заболевание
матери, которое сопровождается хронической
интоксикацией;
–
наличие острых инфекционных
заболеваний или
хронических очагов инфекции, в то время
когда будущая мать вынашивала ребенка;
–
в случае, если у женщины нарушен
процесс питания, или же она не созрела
для беременности и родов;
–
нарушение
маточно-плацентарного
кровотока во
время беременности;
– изменения
в обмене веществ
также влечет за
собой расстройство нервной системы у
будущего ребенка (повышение уровня
биллирубина, неонатальная желтуха);
–
в случае сильного
токсикоза, как на ранней стадии,
так и на поздней, или появление иных
проблем с вынашиванием ребенка;
–
окружающая среда выступает немаловажным
фактором в развитии заболевания;
–
появление патологии во время родов
— это может быть слабая
родовая деятельность,
ускоренные роды;
–
если ребенок рождается недоношенным,
то и его организм не развит полностью,
поэтому на данном фоне может появиться
нарушение в работе ЦНС;
Если четко
зафиксирован недостаток кислорода,
во время нахождения малыша внутри
организма матери (гипоксия), то
диагностируют гипоксическое
поражение ЦНС.
Хроническая
гипоксия плода
развивается при осложненном течении
беременности, фето-плацентарной
недостаточности или при заболеваниях
беременной, протекающих с гипоксемией
(пороки сердца, тяжелая анемия, хронические
болезни легких).
Острая
гипоксия (асфиксия)
чаще возникает в процессе родов в
результате нарушения маточно-плацентарного
кровообращения при преждевременной
отслойке плаценты,
пролапсе пуповины,
аномальном предлежании плода и плаценты,
гипертонусе и разрывах матки, острой
гипоксии у роженицы, а также вследствие
замедления кровотока при сжатии головки
плода и полости малого таза.
Патогенез.
Общим типом
поражения мозга для детей любого срока
гестации является также селективный
и диффузный некроз
нейронов.
Особенностью селективного некроза у
доношенных детей является его локализация
в коре головного мозга, таламусе,
мозжечке, стволе головного мозга и
спинном мозге, при этом острая
и тяжелая гипоксия
приводит, как правило, к стволовым
и спинальным
нарушениям, а
хроническая
и легкая гипоксия - к корковым.
При неблагоприятном исходе у детей
развиваются спастическая тетраплегия,
интеллектуальная
недостаточность, стволовая дисфункция,
судороги. У
недоношенных детей селективный некроз
нейронов преобладает в диэнцефальной
области и коре
головного мозга, что может сформировать
спастическую тетраплегию,
поражение краниальных
нервов, возможно, синдром дефицита
внимания и гипоталамический
синдром.
У плода гипоксия приводит
к сдвигу реакцию
крови и тканей в кислую сторону,
развивается метаболический ацидоз,
снижается активность ферментов,
обеспечивающих «синтез роста», нарушается
функция миокарда.
Появляются тахикардия и децелерация
сердечного ритма, экстрасистолии.
Регистрируется положительный –
нереактивный – нестрессовый
тест.
Продолжающаяся
гипоксия приводит
к активации
анаэробного гликолиза.
Нарастающий дефицит кислорода заставляет
организм снизить
оксигенацию кишечника, кожи, печени,
почек; происходит
перераспределение кровообращения с
преимущественным кровоснабжением
жизненно важных органов (головной мозг,
сердце, надпочечники). Централизация
кровообращения, в свою очередь, усугубляет
тканевой метаболический ацидоз
(резко увеличивается
в крови уровень лактата).
Развивается снижение двигательной
активности плода, частотной активности
на ЭЭГ, числа «дыхательных» экскурсий
грудной клетки, появляется
брадикардия.
Гипоксическая
энцефалопатия,
которая является грозным клиническим
проявлением тяжелой асфиксии, возникает,
прежде всего, вследствие
ишемии ткани головного мозга (артериальная
гипотензия при артериальном давлении
на локтевой артерии менее 50 мм рт. ст.,
тромбозы венул и артериол, нарушение
венозного оттока
из-за отека
головного мозга), дисэлектролитемии,
мелких кровоизлияний в ткань мозга и
субарахноидальное пространство. Наличие
таких кровоизлияний не служит главным
прогностическим признаком, как в остром
периоде, так и для дальнейшего
нервно-психического развития. Поражения
головного мозга обусловлены не только
изменениями его в момент гипоксии, но
и могут возникать в процессе реанимации
ребенка, в постгипоксическом периоде,
что объясняют накоплением в крови и
тканях избытка свободных радикалов и
продуктов перекисного окисления липидов
(«кислородный парадокс» - токсичность
избытка кислорода после периода
длительной гипоксии),
протеолитических ферментов, ионов
кальция, и др. Отсюда возникает опасность
чрезмерно активной, неконтролируемой
оксигенотерапии в неонатологии.
В
настоящее время предложены три гипотезы
патогенеза метаболических расстройств
ЦНС новорожденных. 1. Церебральная
гипотеза, согласно
которой триггерным фактором является
гипоксия,
а повреждающее
действие на головной мозг оказывают
продукты
патологического метаболизма.
Данная гипотеза объясняет прямую
взаимосвязь микроциркуляции крови с
метаболизмом в головном мозге.
2.
Глутаматная гипотеза
предполагает возникающие вследствие
гипоксии
и активации каскада клеточных биохимических
реакций
нарушения функции клеток,
приводящие к некрозу
и апоптозу,
при этом происходят накопление
в головном мозге глутамата,
гиперстимуляция глутаматных рецепторов
с последующим каскадом биохимических
реакций, сопровождающихся увеличением
комплекса Са2+ и
зависимых от него процессов.
3.
Гиперпродукция
оксида азота (NО).
При гипоксии,
возникшей у ребенка внутриутробно и
имеющей хроническое течение, повышается
устойчивость организма к повторяющимся
эпизодам кислородного голодания, что
обусловливает эволюционное
изменение
экспрессии генов,
кодирующих разные изоформы NO-зависимых
реакций. Таким
образом, гипоксическое поражение в
зависимости от степени повреждения
структур головного мозга имеет
прогредиентный характер, а выявление
психического и моторного дефицита на
протяжении раннего онтогенеза следует
рассматривать как феномен отсроченных
страданий.
Клиника.
Острый период длится от 7 до 10 дней,
крайне редко, но он может растянуться
и до месяца. Период,
в которым происходит восстановление
(восстановительный период), может длиться
до 6 мес. Если организм ребенка
восстанавливается медленно, то данный
период может занять до 2 лет.
–
Нарушение
мышечного тонуса.
Этот синдром диагностируется согласно
отклонениям от нормы в зависимости от
возраста грудного ребенка. В начальный
период времени жизни ребенка, достаточно
сложно диагностировать данный синдром,
так как помимо этого встречается
физиологический
гипертонус (физиологическая
скованность мышц
новорожденного).
–
Синдром
нервно-рефлекторной возбудимости -
синдром, связанный с нарушением
сна, дрожанием подбородка, вздрагиваниями
ребенка на любой шорох или прикосновение.
Данный синдром можно диагностировать
только в том случае, когда будет исключены
соматические заболевания новорожденного
(например, кишечные колики). При осмотре
такого ребенка невролог определяет
повышение
сухожильных рефлексов, а также усиление
(оживление) автоматизмов новорожденного
(рефлекс Моро).
– Синдром
угнетения нервной системы.
Такой синдром по своим характеристикам
противоположен предыдущему. Его
диагностируют у детей, которые
в первые
месяцы своей жизни не активны,
они много спят, у них понижен тонус, они
не могут удерживать голову, плохо
цепляются своими ручками.
–
Неблагоприятный прогноз для ребенка,
если развился синдром
внутричерепной гипертензии.
Основными его признаками являются
повышенная
возбудимость и нервозность, при этом
начинает набухать и уплотняться родничок.
Появляются частые
срыгивания. При
осмотре невролог замечает избыточный
рост окружности головы, возможно
расхождение швов черепа, симптом Грефе
(симптом «заходящего
солнца»).
– Одним из наиболее
опасных и тяжелых состояний при ППЦНС
является судорожный
синдром, именно
он является одним из наиболее серьезных
проявлений при перинатальном поражении
ЦНС.
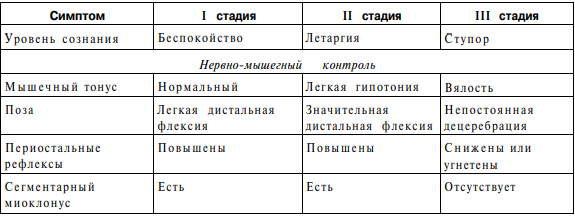 Лечение
ГИ Э включает в себя следующие этапы:
1. Лечение гипоксии.
2. Лечение
метаболических нарушений, вызванных
гипоксией.
3. Лечение гипоксического
отека мозга и нейронопротекция.
Лечение
ГИ Э включает в себя следующие этапы:
1. Лечение гипоксии.
2. Лечение
метаболических нарушений, вызванных
гипоксией.
3. Лечение гипоксического
отека мозга и нейронопротекция.
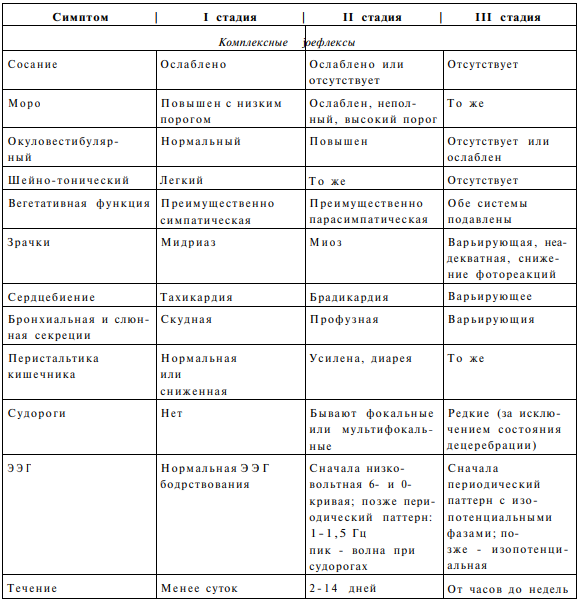 60.Гнойно-септические
заболевания новорожденных детей.
Заболевания
этой группы – одни из наиболее частых
у детей периода новорожденности (около
70–80 %). Это обусловлено незрелостью
барьерных функций кожи и слизистых
оболочек новорожденного
ребенка, сниженной сопротивляемостью
по отношению к бактериальной
инфекции.
Этиология:
кишечная палочка, клебсиелла,
энтеробактерии, протей, синегнойная
палочка.
Инфицирование
ребенка в постнатальном периоде
происходит через
руки персонала, матери
и при непосредственном контакте с
источником инфекции в окружающей среде
(пеленки, оборудование, инфузионные
растворы, питательные смеси и т.д.).
Источником кишечной инфекции может
быть заболевший ребенок, заразившийся
от матери или от бациллоносителя из
числа медицинского персонала.
Везикулопустулез
(стафилококковый перипорит) — заболевание,
которое может начаться в середине
неонатального периода:
на коже ягодиц, бедер, естественных
складок, головы появляются мелкие,
поверхностно расположенные пузырьки
размером до нескольких миллиметров,
наполненные
вначале прозрачным, а затем мутным
содержимым.
Морфологическим субстратом заболевания
является воспаление в области устьев
эккриновых потовых желез. Течение
заболевания, как правило, доброкачественное.
Пузырьки лопаются
через 2—3 дня с момента их появления.
Образовавшиеся вследствие этого
маленькие эрозии покрываются сухими
корочками, не оставляющими после
отпадения рубцов или пигментации.
Общее состояние детей
не нарушено, однако возможна генерализация
инфекции.
60.Гнойно-септические
заболевания новорожденных детей.
Заболевания
этой группы – одни из наиболее частых
у детей периода новорожденности (около
70–80 %). Это обусловлено незрелостью
барьерных функций кожи и слизистых
оболочек новорожденного
ребенка, сниженной сопротивляемостью
по отношению к бактериальной
инфекции.
Этиология:
кишечная палочка, клебсиелла,
энтеробактерии, протей, синегнойная
палочка.
Инфицирование
ребенка в постнатальном периоде
происходит через
руки персонала, матери
и при непосредственном контакте с
источником инфекции в окружающей среде
(пеленки, оборудование, инфузионные
растворы, питательные смеси и т.д.).
Источником кишечной инфекции может
быть заболевший ребенок, заразившийся
от матери или от бациллоносителя из
числа медицинского персонала.
Везикулопустулез
(стафилококковый перипорит) — заболевание,
которое может начаться в середине
неонатального периода:
на коже ягодиц, бедер, естественных
складок, головы появляются мелкие,
поверхностно расположенные пузырьки
размером до нескольких миллиметров,
наполненные
вначале прозрачным, а затем мутным
содержимым.
Морфологическим субстратом заболевания
является воспаление в области устьев
эккриновых потовых желез. Течение
заболевания, как правило, доброкачественное.
Пузырьки лопаются
через 2—3 дня с момента их появления.
Образовавшиеся вследствие этого
маленькие эрозии покрываются сухими
корочками, не оставляющими после
отпадения рубцов или пигментации.
Общее состояние детей
не нарушено, однако возможна генерализация
инфекции.
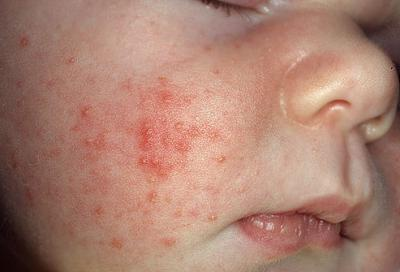 Пузырчатка
новорожденных
(пемфигус, пиококковый пемфигоид) может
протекать в двух формах: доброкачественной
и злокачественной.
Доброкачественная
форма характеризуется
появлением на фоне эритематозных
пятен пузырьков и
небольшого
размера пузырей (до
0,5—1 см в диаметре), наполненных
серозно-гнойным
содержимым.
Пузыри могут находиться на разных
стадиях развития, имеют незначительно
инфильтрированное основание, вокруг
пузыря отмечается венчик гиперемии.
Локализуются обычно на коже
нижней половины живота,
около пупка, на
конечностях, в естественных складках.
Высыпание пузырей может продолжаться
несколько дней. Симптом
Никольского (при
потирании или даже прикосновении
происходит десквамация, слущивание
эпидермиса)
отрицательный.
Характерно, что на месте бывших пузырей
появляются поверхностные
эрозии, но корки потом не образуются.
Состояние новорожденных детей может
быть не нарушено или среднетяжелое.
Возможно повышение температуры тела
до субфебрильной. Интоксикация при
данной форме заболевания обычно
отсутствует, вместе с тем дети могут
становиться беспокойными или вялыми.
Прибавка в массе тела отсутствует. При
своевременно начатом лечении выздоровление
наступает через 1—2 недели от начала
заболевания.
Злокачественная
форма пузырчатки
новорожденных детей характеризуется
появлением на коже
большого количества вялых пузырей,
преимущественно
больших размеров — до 2—3 см в диаметре
(такие пузыри
называют фликтенами). Кожа
между отдельными пузырями может
слущиваться.
Симптом
Никольского может быть положительным.
Состояние детей тяжелое, выражены
симптомы интоксикации. Температура
тела поднимается до фебрильной. Внешний
вид ребенка напоминает таковой у больного
сепсисом. В
клиническом анализе крови характерен
лейкоцитоз с нейтрофилезом и сдвигом
влево до молодых форм, СОЭ и анемия
разной степени тяжести. Заболевание
нередко заканчивается сепсисом (или
является его проявлением).
Лечение заключается
в прокалывании пузырей и обработке
спиртовыми растворами анилиновых
красителей. Целесообразно
ультрафиолетовое облучение кожи. При
необходимости проводится антибактериальная
и инфузионная терапия.
Пузырчатка
новорожденных
(пемфигус, пиококковый пемфигоид) может
протекать в двух формах: доброкачественной
и злокачественной.
Доброкачественная
форма характеризуется
появлением на фоне эритематозных
пятен пузырьков и
небольшого
размера пузырей (до
0,5—1 см в диаметре), наполненных
серозно-гнойным
содержимым.
Пузыри могут находиться на разных
стадиях развития, имеют незначительно
инфильтрированное основание, вокруг
пузыря отмечается венчик гиперемии.
Локализуются обычно на коже
нижней половины живота,
около пупка, на
конечностях, в естественных складках.
Высыпание пузырей может продолжаться
несколько дней. Симптом
Никольского (при
потирании или даже прикосновении
происходит десквамация, слущивание
эпидермиса)
отрицательный.
Характерно, что на месте бывших пузырей
появляются поверхностные
эрозии, но корки потом не образуются.
Состояние новорожденных детей может
быть не нарушено или среднетяжелое.
Возможно повышение температуры тела
до субфебрильной. Интоксикация при
данной форме заболевания обычно
отсутствует, вместе с тем дети могут
становиться беспокойными или вялыми.
Прибавка в массе тела отсутствует. При
своевременно начатом лечении выздоровление
наступает через 1—2 недели от начала
заболевания.
Злокачественная
форма пузырчатки
новорожденных детей характеризуется
появлением на коже
большого количества вялых пузырей,
преимущественно
больших размеров — до 2—3 см в диаметре
(такие пузыри
называют фликтенами). Кожа
между отдельными пузырями может
слущиваться.
Симптом
Никольского может быть положительным.
Состояние детей тяжелое, выражены
симптомы интоксикации. Температура
тела поднимается до фебрильной. Внешний
вид ребенка напоминает таковой у больного
сепсисом. В
клиническом анализе крови характерен
лейкоцитоз с нейтрофилезом и сдвигом
влево до молодых форм, СОЭ и анемия
разной степени тяжести. Заболевание
нередко заканчивается сепсисом (или
является его проявлением).
Лечение заключается
в прокалывании пузырей и обработке
спиртовыми растворами анилиновых
красителей. Целесообразно
ультрафиолетовое облучение кожи. При
необходимости проводится антибактериальная
и инфузионная терапия.
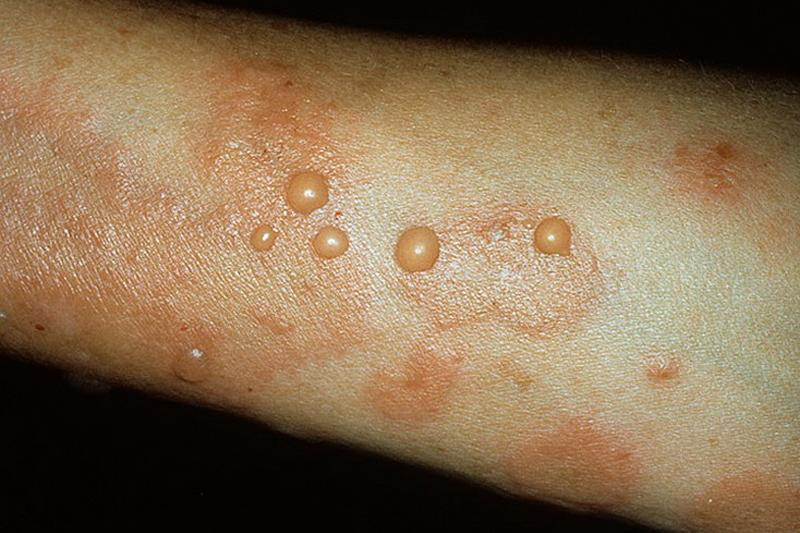
 Эксфолиативный
дерматит Риттера
- наиболее тяжелая форма стафилококковых
пиодермии новорожденных, которую можно
рассматривать как септический
вариант течения пузырчатки.
Вызывается госпитальными
штаммами золотистого стафилококка,
продуцирующими экзотоксин
— эксфолиатин.
Заболевание начинается в конце 1-й—начале
2-й недели жизни с появления покраснения,
мокнутья кожи и образования трещин в
области пупка, паховых складок, вокруг
рта. Раннее начало, как правило,
характеризуется наиболее тяжелым
течением болезни. В
течение нескольких часов яркая эритема
распространяется
на кожу живота, туловища, конечностей.
В дальнейшем на различных участках тела
появляются вялые
пузыри, трещины, наблюдается слущивание
эпидермиса,
оставляющее обширные эрозии. Симптом
Никольского у большинства детей
положительный.
Тело новорожденного ребенка имеет вид
обожженного
кипятком. На фоне
заболевания нередко возникают другие
очаги гнойной инфекции: омфалит, отит,
конъюнктивит, пневмония, энтероколит,
т. е. развивается
сепсис. Состояние
больных тяжелое, дети отказываются от
груди, становятся беспокойными, выражены
симптомы интоксикации. Заболевание
сопровождается фебрильной температурой,
резкими воспалительными изменениями
в анализе крови. Через 1—2 дня от начала
заболевания вся кожа новорожденного
гиперемирована и на больших участках
образуются эрозии вследствие накопления
экссудата под эпидермисом с последующей
отслойкой последнего. Присоединяются
симптомы, обусловленные появлением
эксикоза. В случае
благоприятного исхода заболевания
вслед за эритематозной и эксфолиативной
стадиями наступает эпителизация
эрозивных поверхностей без образования
рубцов или пигментации.
Псевдофурункулез
Фигнера —
заболевание, которое может начинаться
так же, как везикулопустулез, с дальнейшим
распространением процесса на всю потовую
железу. Воспаление
устьев волосяных фолликулов с дальнейшим
распространением процесса на всю потовую
железу - возникает абсцесс. Возможно
первичное появление
подкожных узлов размером от нескольких
миллиметров до 1 — 1,5 см багрово-красного
цвета. В дальнейшем
в центре
узлов появляется гнойное содержимое.
Наиболее частая локализация — кожа
волосистой части головы, задняя
поверхность шеи, кожа спины, ягодиц,
конечностей. В
клинической картине типичны: повышение
температуры тела, симптомы интоксикации,
реакция региональных лимфатических
узлов, метастазирование гнойных очагов.
По мере увеличения
размеров абсцессов (до 1-1,5 см) появляется
флюктуация,
при вскрытии - гной.
Характерны повышение температуры тела,
симптомы интоксикации, возможны
лимфадениты, развитие сепсиса.
Мастит
у новорожденных детей
— тяжелое заболевание, начинающееся
на фоне физиологического нагрубания
грудных желез. Клинически проявляется
увеличением
одной грудной железы, ее инфильтрацией.
Гиперемия в первые дни может отсутствовать
или быть слабо выраженной. Пальпация
грудной железы сопровождается
болезненностью — ребенок плачет,
проявляет беспокойство.
Вскоре гиперемия кожи над железой
усиливается, появляется флуктуация.
Состояние ребенка обычно ухудшается,
он плохо сосет, повышается температура
тела, появляются симптомы интоксикации.
Из выходных протоков грудной железы
при надавливании
на нее или спонтанно появляется гнойное
отделяемое.
Заболевание опасно метастатическими
гнойно-септическими осложнениями.
Эксфолиативный
дерматит Риттера
- наиболее тяжелая форма стафилококковых
пиодермии новорожденных, которую можно
рассматривать как септический
вариант течения пузырчатки.
Вызывается госпитальными
штаммами золотистого стафилококка,
продуцирующими экзотоксин
— эксфолиатин.
Заболевание начинается в конце 1-й—начале
2-й недели жизни с появления покраснения,
мокнутья кожи и образования трещин в
области пупка, паховых складок, вокруг
рта. Раннее начало, как правило,
характеризуется наиболее тяжелым
течением болезни. В
течение нескольких часов яркая эритема
распространяется
на кожу живота, туловища, конечностей.
В дальнейшем на различных участках тела
появляются вялые
пузыри, трещины, наблюдается слущивание
эпидермиса,
оставляющее обширные эрозии. Симптом
Никольского у большинства детей
положительный.
Тело новорожденного ребенка имеет вид
обожженного
кипятком. На фоне
заболевания нередко возникают другие
очаги гнойной инфекции: омфалит, отит,
конъюнктивит, пневмония, энтероколит,
т. е. развивается
сепсис. Состояние
больных тяжелое, дети отказываются от
груди, становятся беспокойными, выражены
симптомы интоксикации. Заболевание
сопровождается фебрильной температурой,
резкими воспалительными изменениями
в анализе крови. Через 1—2 дня от начала
заболевания вся кожа новорожденного
гиперемирована и на больших участках
образуются эрозии вследствие накопления
экссудата под эпидермисом с последующей
отслойкой последнего. Присоединяются
симптомы, обусловленные появлением
эксикоза. В случае
благоприятного исхода заболевания
вслед за эритематозной и эксфолиативной
стадиями наступает эпителизация
эрозивных поверхностей без образования
рубцов или пигментации.
Псевдофурункулез
Фигнера —
заболевание, которое может начинаться
так же, как везикулопустулез, с дальнейшим
распространением процесса на всю потовую
железу. Воспаление
устьев волосяных фолликулов с дальнейшим
распространением процесса на всю потовую
железу - возникает абсцесс. Возможно
первичное появление
подкожных узлов размером от нескольких
миллиметров до 1 — 1,5 см багрово-красного
цвета. В дальнейшем
в центре
узлов появляется гнойное содержимое.
Наиболее частая локализация — кожа
волосистой части головы, задняя
поверхность шеи, кожа спины, ягодиц,
конечностей. В
клинической картине типичны: повышение
температуры тела, симптомы интоксикации,
реакция региональных лимфатических
узлов, метастазирование гнойных очагов.
По мере увеличения
размеров абсцессов (до 1-1,5 см) появляется
флюктуация,
при вскрытии - гной.
Характерны повышение температуры тела,
симптомы интоксикации, возможны
лимфадениты, развитие сепсиса.
Мастит
у новорожденных детей
— тяжелое заболевание, начинающееся
на фоне физиологического нагрубания
грудных желез. Клинически проявляется
увеличением
одной грудной железы, ее инфильтрацией.
Гиперемия в первые дни может отсутствовать
или быть слабо выраженной. Пальпация
грудной железы сопровождается
болезненностью — ребенок плачет,
проявляет беспокойство.
Вскоре гиперемия кожи над железой
усиливается, появляется флуктуация.
Состояние ребенка обычно ухудшается,
он плохо сосет, повышается температура
тела, появляются симптомы интоксикации.
Из выходных протоков грудной железы
при надавливании
на нее или спонтанно появляется гнойное
отделяемое.
Заболевание опасно метастатическими
гнойно-септическими осложнениями.
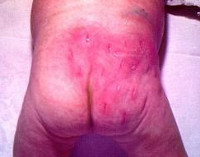 Некротическая
флегмона новорожденных
- наиболее тяжелое гнойно-воспалительное
заболевание новорожденных, начинающееся
с появления
на небольшом участке кожи красного
пятна, плотного на ощупь,
в дальнейшем развитии которого можно
выделить 4 стадии.
Начальная
стадия
(островоспалительный процесс)
характеризуется быстрым,
в течение нескольких часов, распространением
очага поражения, принимающего значительные
размеры. Темпы
поражения подкожной жировой клетчатки
(гнойное расплавление) обычно опережают
скорость изменения кожи. Этому способствует
наличие богатой
сети лимфатических сосудов и широких
лимфатических щелей.
Альтернативно-некротигеская
стадия возникает через 1 —2 суток от
начала заболевания, цвет
пораженного участка кожи приобретает
багрово-синюшный оттенок,
в центре
возникает размягчение.
В некоторых случаях при пальпации кожи
при переходе на пораженный участок
отмечается симптом
«минус ткани».
Стадия отторжения
характеризуется омертвением
отслоенной кожи,
после удаления которой образуются
раневые
дефекты с покрытыми краями и гнойными
карманами.
Стадия
репарации
сопровождается развитием грануляций,
эпителизацией раневой поверхности с
последующим образованием рубцов.
Заболевание у большинства детей протекает
с интоксикацией, присоединяющейся
обычно во II стадии. Характерны лихорадка,
рвота, диспепсические явления,
возникновение метастатических очагов
инфекции, что позволяет трактовать
данное состояние как сепсис.
Стрептодермии.
Первичное поражение при
роже чаще локализуется на коже лица или
в области пупка и
быстро распространяется на другие
участки кожи («путешествующая
рожа», «бродячая рожа»).
В типичных случаях заболевание начинается
с фебрильной температуры, озноба,
появления локальной
гиперемии (слабо
выраженной по сравнению с детьми старшего
возраста) и инфильтрации кожи и подкожной
жировой клетчатки. Края очага поражения
фестончатые, неправильной формы,
ограничительный валик отсутствует,
измененная
кожа теплая на ощупь, возможна гиперестезия.
У новорожденных может наблюдаться
«белая рожа», при
которой гиперемия отсутствует, пораженный
участок кожи бледнеет, иногда возникают
пузыри, подкожные
абсцессы, некрозы. Течение заболевания
обычно тяжелое, состояние детей быстро
ухудшается, ребенок становится вялым,
отказывается от груди, появляются
диспепсические расстройства, явления
миокардита, менингита и поражения
почек.
Интертригинозная
стрептодермия
проявляется резко отграниченной
гиперемией, иногда с незначительным
мокнутием за ушами и в естественных
складках. В области очага
поражения возможны
трещины, фликтены, по периферии —
пиококковые элементы.
При угасании воспалительных изменений
появляется отрубевидное
шелушение.
Папулоэрозивная
стрептодермия
характеризуется появлением на коже
ягодиц и задней поверхности бедер
плотноватых на ощупь,
синюшно-красного
цвета папул размером 0,1-0,3
мм. Папулы быстро эрозируются и покрываются
корочками, на близлежащих участках кожи
появляются новые элементы, в том числе
пиококковые.
Вульгарная
эктима - язвенная
форма стрептодермии. Кроме стрептококков,
в очагах поражения можно обнаружить
стафилококк,
Pseudomonas aeruginosa. Выделяют 2 формы заболевания.
Простая эктима
характеризуется образованием пустулы,
локализующейся чаще на коже нижних
конечностей.
После вскрытия пустулы образуется язва,
дно которой покрыто гноем и коричневатыми
корочками. Заживление язвы происходит
в течение нескольких недель с последующим
образованием рубца. Прободающая
эктима проявляется
возникновением
большого числа эктим, нередко сливающихся
между собой.
Характерная локализация — волосистая
часть головы. Сопровождается лихорадкой,
интоксикацией, увеличением регионарных
лимфатических узлов.
Паронихии
— инфекционное поражение
ногтевых валиков,
вызываемое стрептококками с наслоением
стафилококковой инфекции. Типичным для
поражения стрептококками является
появление пузырей на фоне гиперемии и
отека с последующим развитием эрозий.
В некоторых случаях возможен регионарный
лимфаденит.
Катаральный
омфалит (мокнущий
пупок). Клинически характеризуется
наличием серозного
отделяемого из пупочной ранки и
замедлением сроков ее эпителизации.
В некоторых случаях отмечается легкая
гиперемия и незначительная инфильтрация
пупочного кольца.
При образовании кровянистых корочек в
первые дни после отпадения пуповинного
остатка возможно скопление под ними
необильного серозно-гнойного отделяемого.
Состояние
новорожденного не нарушено, температура
тела нормальная.
Изменений в анализе крови нет. Пупочные
сосуды не пальпируются.
Омфалит.
Бактериальное
воспаление дна пупочной ранки,
пупочного кольца, подкожной жировой
клетчатки вокруг
пупочного кольца, пупочных сосудов.
Заболевание начинается в
конце раннего неонатального периода
или на 2-й неделе жизни,
нередко с симптомов катарального
омфалита. Через несколько дней появляется
гнойное отделяемое из пупочной ранки
— пиорея пупка,
отек и гиперемия пупочного кольца,
инфильтрация подкожной жировой клетчатки
вокруг пупка, вследствие которой пупок
выбухает над поверхностью передней
брюшной стенки. Кожа
вокруг пупка гиперемирована, горячая
на ощупь, характерно
расширение сосудов передней брюшной
стенки (усиление венозной сети), красные
полосы, обусловленные присоединением
лимфангоита. Появляются
симптомы, характерные для инфекционного
поражения пупочных сосудов. Состояние
больного нарушено, ребенок
становится вялым, хуже сосет грудь,
срыгивает,
уменьшается прибавка массы тела (возможна
потеря). Температура тела может быть
повышена до фебрильной. В анализе крови
— лейкоцитоз со сдвигом влево, увеличение
СОЭ.
Язва пупка
может возникнуть как осложнение пиореи
пупка или омфалита. Дно пупочной ранки
обычно покрыто
серозно-гнойным или гнойным отделяемым,
после удаления которого выявляется
изъязвление. Развитие ее наиболее
вероятно, если
во время обработки пупочной ранки не
снимать корочку, скрывающую от врача
дно пупочной ранки. Общее
состояние в первые дни заболевания
может быть не нарушено, в дальнейшем
присоединяются симптомы интоксикации.
Гангрена
пупогного канатика
(пуповинного остатка) при рождении
ребенка в родовспомогательном учреждении
практически не встречается. Заболевание
начинается в первые дни жизни и вызывается
анаэробной палочкой.
Мумификация
пуповинного остатка прекращается,
он становится влажным,
приобретает грязно-бурый оттенок и
источает неприятный гнилостный запах.
Отпадение пуповинного остатка запаздывает,
в пупочной ранке сразу появляется
гнойной отделяемое. Состояние
больного нарушено, характерна температурная
реакция, симптомы интоксикации,
изменения в анализе крови, соответствующие
тяжести инфекционного процесса. Обычно
развивается сепсис.
Конъюнктивиты.
Реактивные конъюнктивиты при современном
методе профилактики гонобленнореи
практически не встречаются. Таким
образом, все конъюнктивиты следует
считать проявлением инфекции (хламидии,
стафилококки, кишечная палочка
и т.д.). Чаще
болеют недоношенные, дети, инфицированные
в родах и от матерей,
перенесших ОРВ И в конце беременности.
Конъюнктивиты могут быть и следствием
дефекта ухода. В
клинике, кроме покраснения конъюнктивы,
характерно гнойное
отделяемое из глаз.
Общее состояние, как правило, не
нарушено.
Гонобленнорея
характеризуется чрезвычайно
обильным гнойным отделением из глаза
(«шапка гноя»),
резким
отеком и покраснением верхнего века.
В запущенных случаях
возможно кровянистое отделяемое
- вследствие изъязвления роговой
оболочки. Любой конъюнктивит является
показанием для срочного проведения
бактериоскопического
исследования гнойного отделяемого,
включающего тщательный поиск гонококка,
хламидий.
Остеомиелит
— воспаление костного мозга,
распространяющееся
на компактное и губчатое вещество кости
и надкостницу.
Чаще поражаются бедренные
и плечевые кости.
Микробы попадают в кость, как правило,
гематогенно. До недавнего времени
остеомиелиты у новорожденных детей
были почти исключительно эпифизарными
и вызывались золотистым патогенным
стафилококком,
протекали остро, с поражением
близлежащего сустава — артритом.
Заболевание
начинается с появления токсикоза
или резкого нарастания его интенсивности,
лихорадки,
ограничения
подвижности конечности,
болезненности при
пассивных движениях ее или пальпации
места поражения.
В это же время при пассивных движениях
конечностей под пальцами исследующего
ощущается своеобразный
«хруст» типа
крепитации в
области сустава и над местом воспаления.
Через
2—3 дня появляется припухлость сустава,
сглаженность его контуров, позже
возникают пастозность, отек, в дальнейшем
— плотный
инфильтрат вокруг эпифизарного конца
кости. При прорыве
гноя из-под надкостницы в мягкие ткани
появляется гиперемия
кожи, флюктуация.
Рентгенологически вначале обнаруживают
расширение суставной щели, а в конце
первой—начале второй недели болезни
определяют деструктивные изменения
ядер окостенения разной степени
выраженности. При переходе процесса на
метафиз (на 10— 14-й день болезни) видны
периостальные изменения.
61.
Сепсис. Этиология и патогенез,
классификация.
Сепсис
— генерализованная
гнойно-воспалительная инфекция,вызванная
условнопатоген. бактер. флорой с
развитием
воспалительной реакции
организма на фоне иммунной дисфункции
и присутствием
возбудителя в крови).
приводящий к генерализованному
повреждению эндотелия сосудистого
русла, стойким нарушениям
микроциркуляции,
расстройствам
гемостаза с
обязательным ДВС и дальнейшей полиорганной
недостаточностью.
Этиология.
Возбудителями сепсиса, начинающегося
в первые 4—5 дней жизни, наиболее часто
являются стрептококки
группы В, энтерококки и реже листерии,
т. е. бактериальная флора
родовых путей матери.
При сепсисе
новорожденных,
начавшемся позднее, доминируют
возбудители, попавшие к ребенку вследствие
перекрестного инфицированна через руки
персонала, оборудование, предметы ухода
(грамотрицательные бактерии — клебсиеллы,
эшерихии, палочка синезеленого гноя,
акинетобактеры, протеи).
Между тем в последние годы все чаще
стали выявлять при сепсисе стафилококки
— золотистый и коагулазоотрицательный
эпидермальный.
Патогенез.
Сутью септического процесса является
неспособность
организма уничтожать возбудителей,
связанная, прежде всего, с иммунодефицитным
состоянием (ИДС).
Проникновение
возбудителя через входные ворота
(чаще травмированная кожа или слизистые
оболочки) с развитием местной реакции
(первичного аффекта) — септического
очага.
Как правило,
первичный аффект (септический очаг)
совпадает с входными воротами, но иногда
он возникает в отдаленных от места
внедрения возбудителя тканях (например,
гематогенный остеомиелит при внедрении
инфекции через кожу).
Лимфогенное
распространение инфекции
ведет к развитию реактивного лимфангита,
лимфотромбоза и лимфаденита. Регионарная
лимфатическая система (структурная
основа так называемого местного, или
регионарного, иммунитета) является
серьезным
барьером для дальнейшего распространения
инфекционного агента.
При ее
«прорыве»
возможны генерализация
инфекции и распространение
токсинов далее по лимфатической системе,
где также происходит их инактивация
с последующим поступлением в
кровоток.
Гематогенное
распространение инфекции
вызывает развитие гнойного
флебита и тромбофлебита с последующим
расплавлением
тромбов и тромбо-бактериальной эмболией,
бактериемией и
токсемией. Поражение
сосудистой стенки на большом протяжении
приводит к образованию
инфицированных микротромбов, развитию
метастатических очагов,
обусловливающих абсцессы и инфаркты
внутренних органов.
Эндотоксин
грамотрицательных бактерий
(ЭТ) неспецифически стимулирует систему
мононуклеарных фагоцитов
с соответствующим
спектром цитокинов
и одновременно
вызывает
поликлональную активацию
В-лимфоцитов,
тромбоцитов и эндотелиоцитов, в результате
возникает системный воспалительный
ответ (СВО) —
узловое звено современного понимания
септического процесса. Стафилококковый
энтеротоксин,
являясь неспецифическим суперантигеном,
стимулирует
Т-хелперы
и способствует
гиперпродукции
интерлейкина-2 с
интоксикацией и даже клинической
картиной комы.
Эти цитокины
вызывают нейтрофильно-эндотелиальную
клеточную адгезию,
активируют механизмы свертывания крови
и обуславливают образование микротромбов.
Они также способствуют высвобождению
других медиаторов, включая лейкотриены,
липоксигеназу, гистамин, брадикинин,
серотонин и IL-2. Им
противостоят противовоспалительные
медиаторы, такие
как IL-4 и IL-10, в результате механизма
обратной отрицательной связи.
Сначала
артерии и артериолы
расширяются,
уменьшается периферическое артериальное
сопротивление; сердечный
выброс, как правило, увеличивается.
Этот этап называется тепловым шоком.
Позже, сердечный выброс может уменьшиться,
падает АД (с или без увеличения
периферического сопротивления), и
появляются типичные признаки шока.
Высвобождение токсических
кислородных продуктов-перекись водорода,
супероксиды, оксид азота.
Повреждение клеток и
нарушение перфузии. ШОК
, ПОЛИОРГАННАЯ НЕДОСТАТОЧНОСТЬ.
При
гиперэргическом сепсисе
максимально выражена пролиферативная
реакция соединительной ткани и крови,
доминируют
реакции чрезмерной активации продукции
провоспалительных цитокинов и каскада
плазменных протеаз («протеолитический
взрыв»), гранулоцитов, тромбоцитов,
эндотелия. Этот вариант сепсиса чаще
развивается у доношенных
детей и с массой тела более 1,5 кг.
Гиперэргический сепсис часто обусловлен
стрептококками В,
листериями, эшерихиями.
Гиперэргический сепсис возникает обычно
под влиянием супервирулентных, особых
штаммов микробов.
При
гипоэргическом отсутствует
адекватная инфекционному процессу
гиперпластическая реакция со
стороны органов кроветворения и
иммуногенеза, отсутствует или минимально
выражен локальный сосудисто-пролиферативный
компонент воспаления, адекватная реакция
нейроэндокринной системы, а также имеют
место тяжелые нарушения
обмена веществ,
и прежде всего энергетического.
Характерным является преобладание
деструктивных
изменений в очаге воспаления,
угнетение и дегенеративные изменения
в органах кроветворения и в клетках
периферической крови. Типичный
гипоэргический сепсис развивается у
детей с очень низкой
массой тела при рождении
(показано, что при массе тела менее 1,5
кг сепсис возникает в 10 раз чаще), ЗВУР
гипопластического и диспластического
типов, или первичными наследственными
иммунодефицитами, глубокими нейтропениями
различного генеза. У доношенных детей
примерами гипоэргического варианта
сепсиса могут быть кандида-сепсис,
синегнойный сепсис.
Классификация
сепсиса:
1. По
виду возбудителя
– стафилококковый, стрептококковый,
колибациллярный, неклостридиальный,
клостридиальный, смешанный;
2. По
расположению входных
ворот инфекции
– хирургический, урологический,
гинекологический, отогенный,
тонзилогенный;
3. По
наличию или отсутствию видимого
очага инфекции
– первичный (криптогенный), вторичный;
4.
По наличию или
отсутствию гнойных
метастазов –
септицемия (характеризуется массивным
поступлением в кровь токсинов с тяжелой
общей интоксикацией. Этот процесс обычно
не сопровождается гнойными метастазами),
септикопиемия (характеризуется
бактериемией и гнойными метастазами в
различные органы. Обычно при септикопиемии
из крови высевается стафилококк. При
этом процессе микроорганизмы, поступая
из первичного очага в кровеносное русло,
транспортируются в капилляры различных
органов, где и оседают, создавая гнойные
очаги. Иногда могут развиваться вторичные
гнойные метастазы);
5. По
клинической картине
– молниеносный, острый, подострый,
хронический.
Молниеносный сепсис
развивается очень быстро, уже в течение
нескольких часов после заражения
появляются клинические симптомы. Через
5-7 дней может наступить летальный исход
даже при своевременном лечении.
Острый
и подострый сепсис характеризуется
более благоприятным течением (более 3
или 6 недель); подострым также считают
сепсис давностью 2—12 недель.
Хронический
– длиться годами с периодическими
обострениями и ремиссиями.
от 12 недель
до нескольких лет.
6.
По фазам развития:
1. Фаза напряжения –
резкая мобилизация защитных сил организма
в результате стимуляции
гипофизарно-надпочечниковой системы.
2. Катаболическая
фаза – проявляется
катаболизмом белков, жиров и углеводов;
а также нарушениями водно-солевого и
кислотно-щелочного равновесия.
3. Анаболическая
фаза – проявляется
переходом метаболизма на анаболический
путь. В первую
очередь восстанавливаются структурные
протеины. 4. Реабилитационная
фаза – происходит
полное восстановление всех обменных
процессов.
62.Сепсис.
Современная классификация. Клиника,
диагностика, лечение, профилактика.
Сепсис
— генерализованная
гнойно-воспалительная инфекция,вызванная
условнопатоген. бактер. флорой с
развитием
воспалительной реакции
организма на фоне иммунной дисфункции
и присутствием
возбудителя в крови).
приводящий к генерализованному
повреждению эндотелия сосудистого
русла, стойким нарушениям
микроциркуляции,
расстройствам
гемостаза с
обязательным ДВС и дальнейшей полиорганной
недостаточностью.
Классификация
сепсиса:
1. По
виду возбудителя
– стафилококковый, стрептококковый,
колибациллярный, неклостридиальный,
клостридиальный, смешанный;
2. По
расположению входных
ворот инфекции
– хирургический, урологический,
гинекологический, отогенный,
тонзилогенный;
3. По
наличию или отсутствию видимого
очага инфекции
– первичный (криптогенный), вторичный;
4.
По наличию или
отсутствию гнойных
метастазов –
септицемия (характеризуется массивным
поступлением в кровь токсинов с тяжелой
общей интоксикацией. Этот процесс обычно
не сопровождается гнойными метастазами),
септикопиемия (характеризуется
бактериемией и гнойными метастазами в
различные органы. Обычно при септикопиемии
из крови высевается стафилококк. При
этом процессе микроорганизмы, поступая
из первичного очага в кровеносное русло,
транспортируются в капилляры различных
органов, где и оседают, создавая гнойные
очаги. Иногда могут развиваться вторичные
гнойные метастазы);
5. По
клинической картине
– молниеносный, острый, подострый,
хронический.
Молниеносный сепсис
развивается очень быстро, уже в течение
нескольких часов после заражения
появляются клинические симптомы. Через
5-7 дней может наступить летальный исход
даже при своевременном лечении.
Острый
и подострый сепсис характеризуется
более благоприятным течением (более 3
или 6 недель); подострым также считают
сепсис давностью 2—12 недель.
Хронический
– длиться годами с периодическими
обострениями и ремиссиями.
от 12 недель
до нескольких лет.
6.
По фазам развития:
1. Фаза напряжения –
резкая мобилизация защитных сил организма
в результате стимуляции
гипофизарно-надпочечниковой системы.
2. Катаболическая
фаза – проявляется
катаболизмом белков, жиров и углеводов;
а также нарушениями водно-солевого и
кислотно-щелочного равновесия.
3. Анаболическая
фаза – проявляется
переходом метаболизма на анаболический
путь. В первую очередь восстанавливаются
структурные протеины. 4. Реабилитационная
фаза – происходит
полное восстановление всех обменных
процессов.
Клиническая
картина. Специфических
клинических
симптомов сепсиса нет.
К наиболее частым симптомам сепсиса
относятся: утрата
коммуникабельности,
летаргия или гипервозбудимость, гипо-
или гипертермия,
анорексия, отсутствие
прибавок массы тела, вздутие живота,
срыгивания, диарея,
респираторные нарушения и апноэ,
тахикардия, нарушения
периферического кровообращения,
гипотензия, желтуха,
кожные сыпи, лактат-ацидоз, нестабильный
уровень глюкозы в крови (гипергликемия
или гипогликемия).
Диагностика.
У новорожденных надо
различать клинические
и лабораторные
критерии системного воспалительного
ответа (СВО).
Клинические
критерии СВО: 1.
Расстройство температурного гомеостата
(гипертермия
или гипотермия).
2. Одышка
или тахипноэ более
60 в 1 минуту. 3. Тахикардия
более 160 в 1 минуту
или брадикардия менее ПО в 1 минуту. 4.
Утрата
коммуникабельности,
анорексия, угнетение и/или судороги.
5. Олигурия
в течение 6 часов
и более на фоне адекватной инфузионной
терапии (диурез менее 1 мл/кг/ч).
Лабораторные
признаки СВО у
новорожденных:
1. Внезапно возникший
тяжелый
метаболический
лактат-ацидоз
с гипокапнией (последнее
при отсутствии поражения легких).
2.
Лейкоцитоз
(количество лейкоцитов у детей первого
дня жизни - более 30000, у детей в возрасте
2- 7 дней жизни - более 15000, у более старших
- свыше 15000 в 1 мкл капиллярной крови) или
лейкопения
(количество
лейкоцитов в 1 мкл крови менее 5000) с
нейтрофилезом
(количество нейтрофилов в 1 мкл капиллярной
крови у детей первого дня жизни - более
20000, от 2 до 7 дней жизни — более 7000, от 8
дней жизни и старше — более 6000) или
нейтропения
(соответственно
в указанные выше дни число нейтрофилов
— менее 5000, 2000 и 1750 в 1 мкл капиллярной
крови).
3. Регенераторный
или регенераторно-дегенеративный сдвиг
лейкоцитарной формулы
при числе палочкоядерных
и более молодых форм более
2000 в мкл (в первый день жизни — более
5000 в мкл).
4. Токсическая
зернистость
нейтрофилов.
5. Тромбоцитопения.
6. Анемия.
7. Внезапно возникшее укорочение
или удлинение активированного
частичного тромбопластинового времени
(АЧТВ)
или протромбинового
времени (ПТВ).
8. Повышение
уровня CR-протеина
или других острофазовых белков.
9.
Увеличение СОЭ более 10 мм/ч.
10.
Бактериемия.
11. Гипергликемия более 6,5
ммоль/л.
Важнейшим в диагностике
сепсиса является рациональное и
обстоятельное бактериологигеское
обследование.
Очень существен объем бактериологического
обследования, включающий
трехкратные посевы
крови (количество
крови для посева не менее 1 мл), посевы
мочи и всего того
субстрата, который необходимо получить
у больного, — содержимое дыхательных
путей, ликвор, гной
и т. д. В разных родильных домах и
отделениях патологии новорожденных
могут доминировать разные возбудители
сепсиса, но наиболее типично, что сепсис
в первые дни жизни чаще
вызывают стрептококки группы В,
в более поздние
периоды - грамотрицательные микробы -
эшерихии, клебсиеллы, палочка сине-зеленого
гноя. В последние
годы вновь увеличилась частота выделения
стафилококков, особенно коагулазаотрицательных,
как возбудителей неонатального сепсиса.
У
недоношенных детей с подозрением на
сепсис обязательно
обследование на внутриутробные инфекции
(как минимум на цитомегаловирусную,
герпетическую, микоплазменную, хламидийную
и токсоплазменную).
Лечение.
Сепсис следует
диагностировать у детей с факторами
высокого риска, имеющих 4
клинических и 4 лабораторных признака
СВО . Если у ребенка
имеется клинически очевидный
очаг инфекции или бактериемия,
то для диагностики сепсиса достаточно
четырех клинических
и трех лабораторных
признаков СВО .
При всех вариантах
основой лечения являются противоинфекционная
терапия —
рациональный выбор антибиотиков,
асептика и естественное вскармливание,
специфическая пассивная иммунотерапия.
При
раннем появлении признаков тяжелой
бактериальной инфекции (в первые три
дня жизни) начинают с назначения
ампициллина
(активен против стрептококков В,
энтерококков - стрептококков D ). Далее
антибиотик выбирают в зависимости
от выявленного возбудителя,
но чаще назначают «защищенные пенициллины»
(аминопенициллины
+ ингибиторы беталактамаз)
в сочетании с цефалоспоринами
III— IV поколения или аминогликозидами.
Очень редко (по жизненным показаниям)
применяют карбопенемы,
ципрофлоксацин.
Некротическая
флегмона новорожденных
- наиболее тяжелое гнойно-воспалительное
заболевание новорожденных, начинающееся
с появления
на небольшом участке кожи красного
пятна, плотного на ощупь,
в дальнейшем развитии которого можно
выделить 4 стадии.
Начальная
стадия
(островоспалительный процесс)
характеризуется быстрым,
в течение нескольких часов, распространением
очага поражения, принимающего значительные
размеры. Темпы
поражения подкожной жировой клетчатки
(гнойное расплавление) обычно опережают
скорость изменения кожи. Этому способствует
наличие богатой
сети лимфатических сосудов и широких
лимфатических щелей.
Альтернативно-некротигеская
стадия возникает через 1 —2 суток от
начала заболевания, цвет
пораженного участка кожи приобретает
багрово-синюшный оттенок,
в центре
возникает размягчение.
В некоторых случаях при пальпации кожи
при переходе на пораженный участок
отмечается симптом
«минус ткани».
Стадия отторжения
характеризуется омертвением
отслоенной кожи,
после удаления которой образуются
раневые
дефекты с покрытыми краями и гнойными
карманами.
Стадия
репарации
сопровождается развитием грануляций,
эпителизацией раневой поверхности с
последующим образованием рубцов.
Заболевание у большинства детей протекает
с интоксикацией, присоединяющейся
обычно во II стадии. Характерны лихорадка,
рвота, диспепсические явления,
возникновение метастатических очагов
инфекции, что позволяет трактовать
данное состояние как сепсис.
Стрептодермии.
Первичное поражение при
роже чаще локализуется на коже лица или
в области пупка и
быстро распространяется на другие
участки кожи («путешествующая
рожа», «бродячая рожа»).
В типичных случаях заболевание начинается
с фебрильной температуры, озноба,
появления локальной
гиперемии (слабо
выраженной по сравнению с детьми старшего
возраста) и инфильтрации кожи и подкожной
жировой клетчатки. Края очага поражения
фестончатые, неправильной формы,
ограничительный валик отсутствует,
измененная
кожа теплая на ощупь, возможна гиперестезия.
У новорожденных может наблюдаться
«белая рожа», при
которой гиперемия отсутствует, пораженный
участок кожи бледнеет, иногда возникают
пузыри, подкожные
абсцессы, некрозы. Течение заболевания
обычно тяжелое, состояние детей быстро
ухудшается, ребенок становится вялым,
отказывается от груди, появляются
диспепсические расстройства, явления
миокардита, менингита и поражения
почек.
Интертригинозная
стрептодермия
проявляется резко отграниченной
гиперемией, иногда с незначительным
мокнутием за ушами и в естественных
складках. В области очага
поражения возможны
трещины, фликтены, по периферии —
пиококковые элементы.
При угасании воспалительных изменений
появляется отрубевидное
шелушение.
Папулоэрозивная
стрептодермия
характеризуется появлением на коже
ягодиц и задней поверхности бедер
плотноватых на ощупь,
синюшно-красного
цвета папул размером 0,1-0,3
мм. Папулы быстро эрозируются и покрываются
корочками, на близлежащих участках кожи
появляются новые элементы, в том числе
пиококковые.
Вульгарная
эктима - язвенная
форма стрептодермии. Кроме стрептококков,
в очагах поражения можно обнаружить
стафилококк,
Pseudomonas aeruginosa. Выделяют 2 формы заболевания.
Простая эктима
характеризуется образованием пустулы,
локализующейся чаще на коже нижних
конечностей.
После вскрытия пустулы образуется язва,
дно которой покрыто гноем и коричневатыми
корочками. Заживление язвы происходит
в течение нескольких недель с последующим
образованием рубца. Прободающая
эктима проявляется
возникновением
большого числа эктим, нередко сливающихся
между собой.
Характерная локализация — волосистая
часть головы. Сопровождается лихорадкой,
интоксикацией, увеличением регионарных
лимфатических узлов.
Паронихии
— инфекционное поражение
ногтевых валиков,
вызываемое стрептококками с наслоением
стафилококковой инфекции. Типичным для
поражения стрептококками является
появление пузырей на фоне гиперемии и
отека с последующим развитием эрозий.
В некоторых случаях возможен регионарный
лимфаденит.
Катаральный
омфалит (мокнущий
пупок). Клинически характеризуется
наличием серозного
отделяемого из пупочной ранки и
замедлением сроков ее эпителизации.
В некоторых случаях отмечается легкая
гиперемия и незначительная инфильтрация
пупочного кольца.
При образовании кровянистых корочек в
первые дни после отпадения пуповинного
остатка возможно скопление под ними
необильного серозно-гнойного отделяемого.
Состояние
новорожденного не нарушено, температура
тела нормальная.
Изменений в анализе крови нет. Пупочные
сосуды не пальпируются.
Омфалит.
Бактериальное
воспаление дна пупочной ранки,
пупочного кольца, подкожной жировой
клетчатки вокруг
пупочного кольца, пупочных сосудов.
Заболевание начинается в
конце раннего неонатального периода
или на 2-й неделе жизни,
нередко с симптомов катарального
омфалита. Через несколько дней появляется
гнойное отделяемое из пупочной ранки
— пиорея пупка,
отек и гиперемия пупочного кольца,
инфильтрация подкожной жировой клетчатки
вокруг пупка, вследствие которой пупок
выбухает над поверхностью передней
брюшной стенки. Кожа
вокруг пупка гиперемирована, горячая
на ощупь, характерно
расширение сосудов передней брюшной
стенки (усиление венозной сети), красные
полосы, обусловленные присоединением
лимфангоита. Появляются
симптомы, характерные для инфекционного
поражения пупочных сосудов. Состояние
больного нарушено, ребенок
становится вялым, хуже сосет грудь,
срыгивает,
уменьшается прибавка массы тела (возможна
потеря). Температура тела может быть
повышена до фебрильной. В анализе крови
— лейкоцитоз со сдвигом влево, увеличение
СОЭ.
Язва пупка
может возникнуть как осложнение пиореи
пупка или омфалита. Дно пупочной ранки
обычно покрыто
серозно-гнойным или гнойным отделяемым,
после удаления которого выявляется
изъязвление. Развитие ее наиболее
вероятно, если
во время обработки пупочной ранки не
снимать корочку, скрывающую от врача
дно пупочной ранки. Общее
состояние в первые дни заболевания
может быть не нарушено, в дальнейшем
присоединяются симптомы интоксикации.
Гангрена
пупогного канатика
(пуповинного остатка) при рождении
ребенка в родовспомогательном учреждении
практически не встречается. Заболевание
начинается в первые дни жизни и вызывается
анаэробной палочкой.
Мумификация
пуповинного остатка прекращается,
он становится влажным,
приобретает грязно-бурый оттенок и
источает неприятный гнилостный запах.
Отпадение пуповинного остатка запаздывает,
в пупочной ранке сразу появляется
гнойной отделяемое. Состояние
больного нарушено, характерна температурная
реакция, симптомы интоксикации,
изменения в анализе крови, соответствующие
тяжести инфекционного процесса. Обычно
развивается сепсис.
Конъюнктивиты.
Реактивные конъюнктивиты при современном
методе профилактики гонобленнореи
практически не встречаются. Таким
образом, все конъюнктивиты следует
считать проявлением инфекции (хламидии,
стафилококки, кишечная палочка
и т.д.). Чаще
болеют недоношенные, дети, инфицированные
в родах и от матерей,
перенесших ОРВ И в конце беременности.
Конъюнктивиты могут быть и следствием
дефекта ухода. В
клинике, кроме покраснения конъюнктивы,
характерно гнойное
отделяемое из глаз.
Общее состояние, как правило, не
нарушено.
Гонобленнорея
характеризуется чрезвычайно
обильным гнойным отделением из глаза
(«шапка гноя»),
резким
отеком и покраснением верхнего века.
В запущенных случаях
возможно кровянистое отделяемое
- вследствие изъязвления роговой
оболочки. Любой конъюнктивит является
показанием для срочного проведения
бактериоскопического
исследования гнойного отделяемого,
включающего тщательный поиск гонококка,
хламидий.
Остеомиелит
— воспаление костного мозга,
распространяющееся
на компактное и губчатое вещество кости
и надкостницу.
Чаще поражаются бедренные
и плечевые кости.
Микробы попадают в кость, как правило,
гематогенно. До недавнего времени
остеомиелиты у новорожденных детей
были почти исключительно эпифизарными
и вызывались золотистым патогенным
стафилококком,
протекали остро, с поражением
близлежащего сустава — артритом.
Заболевание
начинается с появления токсикоза
или резкого нарастания его интенсивности,
лихорадки,
ограничения
подвижности конечности,
болезненности при
пассивных движениях ее или пальпации
места поражения.
В это же время при пассивных движениях
конечностей под пальцами исследующего
ощущается своеобразный
«хруст» типа
крепитации в
области сустава и над местом воспаления.
Через
2—3 дня появляется припухлость сустава,
сглаженность его контуров, позже
возникают пастозность, отек, в дальнейшем
— плотный
инфильтрат вокруг эпифизарного конца
кости. При прорыве
гноя из-под надкостницы в мягкие ткани
появляется гиперемия
кожи, флюктуация.
Рентгенологически вначале обнаруживают
расширение суставной щели, а в конце
первой—начале второй недели болезни
определяют деструктивные изменения
ядер окостенения разной степени
выраженности. При переходе процесса на
метафиз (на 10— 14-й день болезни) видны
периостальные изменения.
61.
Сепсис. Этиология и патогенез,
классификация.
Сепсис
— генерализованная
гнойно-воспалительная инфекция,вызванная
условнопатоген. бактер. флорой с
развитием
воспалительной реакции
организма на фоне иммунной дисфункции
и присутствием
возбудителя в крови).
приводящий к генерализованному
повреждению эндотелия сосудистого
русла, стойким нарушениям
микроциркуляции,
расстройствам
гемостаза с
обязательным ДВС и дальнейшей полиорганной
недостаточностью.
Этиология.
Возбудителями сепсиса, начинающегося
в первые 4—5 дней жизни, наиболее часто
являются стрептококки
группы В, энтерококки и реже листерии,
т. е. бактериальная флора
родовых путей матери.
При сепсисе
новорожденных,
начавшемся позднее, доминируют
возбудители, попавшие к ребенку вследствие
перекрестного инфицированна через руки
персонала, оборудование, предметы ухода
(грамотрицательные бактерии — клебсиеллы,
эшерихии, палочка синезеленого гноя,
акинетобактеры, протеи).
Между тем в последние годы все чаще
стали выявлять при сепсисе стафилококки
— золотистый и коагулазоотрицательный
эпидермальный.
Патогенез.
Сутью септического процесса является
неспособность
организма уничтожать возбудителей,
связанная, прежде всего, с иммунодефицитным
состоянием (ИДС).
Проникновение
возбудителя через входные ворота
(чаще травмированная кожа или слизистые
оболочки) с развитием местной реакции
(первичного аффекта) — септического
очага.
Как правило,
первичный аффект (септический очаг)
совпадает с входными воротами, но иногда
он возникает в отдаленных от места
внедрения возбудителя тканях (например,
гематогенный остеомиелит при внедрении
инфекции через кожу).
Лимфогенное
распространение инфекции
ведет к развитию реактивного лимфангита,
лимфотромбоза и лимфаденита. Регионарная
лимфатическая система (структурная
основа так называемого местного, или
регионарного, иммунитета) является
серьезным
барьером для дальнейшего распространения
инфекционного агента.
При ее
«прорыве»
возможны генерализация
инфекции и распространение
токсинов далее по лимфатической системе,
где также происходит их инактивация
с последующим поступлением в
кровоток.
Гематогенное
распространение инфекции
вызывает развитие гнойного
флебита и тромбофлебита с последующим
расплавлением
тромбов и тромбо-бактериальной эмболией,
бактериемией и
токсемией. Поражение
сосудистой стенки на большом протяжении
приводит к образованию
инфицированных микротромбов, развитию
метастатических очагов,
обусловливающих абсцессы и инфаркты
внутренних органов.
Эндотоксин
грамотрицательных бактерий
(ЭТ) неспецифически стимулирует систему
мононуклеарных фагоцитов
с соответствующим
спектром цитокинов
и одновременно
вызывает
поликлональную активацию
В-лимфоцитов,
тромбоцитов и эндотелиоцитов, в результате
возникает системный воспалительный
ответ (СВО) —
узловое звено современного понимания
септического процесса. Стафилококковый
энтеротоксин,
являясь неспецифическим суперантигеном,
стимулирует
Т-хелперы
и способствует
гиперпродукции
интерлейкина-2 с
интоксикацией и даже клинической
картиной комы.
Эти цитокины
вызывают нейтрофильно-эндотелиальную
клеточную адгезию,
активируют механизмы свертывания крови
и обуславливают образование микротромбов.
Они также способствуют высвобождению
других медиаторов, включая лейкотриены,
липоксигеназу, гистамин, брадикинин,
серотонин и IL-2. Им
противостоят противовоспалительные
медиаторы, такие
как IL-4 и IL-10, в результате механизма
обратной отрицательной связи.
Сначала
артерии и артериолы
расширяются,
уменьшается периферическое артериальное
сопротивление; сердечный
выброс, как правило, увеличивается.
Этот этап называется тепловым шоком.
Позже, сердечный выброс может уменьшиться,
падает АД (с или без увеличения
периферического сопротивления), и
появляются типичные признаки шока.
Высвобождение токсических
кислородных продуктов-перекись водорода,
супероксиды, оксид азота.
Повреждение клеток и
нарушение перфузии. ШОК
, ПОЛИОРГАННАЯ НЕДОСТАТОЧНОСТЬ.
При
гиперэргическом сепсисе
максимально выражена пролиферативная
реакция соединительной ткани и крови,
доминируют
реакции чрезмерной активации продукции
провоспалительных цитокинов и каскада
плазменных протеаз («протеолитический
взрыв»), гранулоцитов, тромбоцитов,
эндотелия. Этот вариант сепсиса чаще
развивается у доношенных
детей и с массой тела более 1,5 кг.
Гиперэргический сепсис часто обусловлен
стрептококками В,
листериями, эшерихиями.
Гиперэргический сепсис возникает обычно
под влиянием супервирулентных, особых
штаммов микробов.
При
гипоэргическом отсутствует
адекватная инфекционному процессу
гиперпластическая реакция со
стороны органов кроветворения и
иммуногенеза, отсутствует или минимально
выражен локальный сосудисто-пролиферативный
компонент воспаления, адекватная реакция
нейроэндокринной системы, а также имеют
место тяжелые нарушения
обмена веществ,
и прежде всего энергетического.
Характерным является преобладание
деструктивных
изменений в очаге воспаления,
угнетение и дегенеративные изменения
в органах кроветворения и в клетках
периферической крови. Типичный
гипоэргический сепсис развивается у
детей с очень низкой
массой тела при рождении
(показано, что при массе тела менее 1,5
кг сепсис возникает в 10 раз чаще), ЗВУР
гипопластического и диспластического
типов, или первичными наследственными
иммунодефицитами, глубокими нейтропениями
различного генеза. У доношенных детей
примерами гипоэргического варианта
сепсиса могут быть кандида-сепсис,
синегнойный сепсис.
Классификация
сепсиса:
1. По
виду возбудителя
– стафилококковый, стрептококковый,
колибациллярный, неклостридиальный,
клостридиальный, смешанный;
2. По
расположению входных
ворот инфекции
– хирургический, урологический,
гинекологический, отогенный,
тонзилогенный;
3. По
наличию или отсутствию видимого
очага инфекции
– первичный (криптогенный), вторичный;
4.
По наличию или
отсутствию гнойных
метастазов –
септицемия (характеризуется массивным
поступлением в кровь токсинов с тяжелой
общей интоксикацией. Этот процесс обычно
не сопровождается гнойными метастазами),
септикопиемия (характеризуется
бактериемией и гнойными метастазами в
различные органы. Обычно при септикопиемии
из крови высевается стафилококк. При
этом процессе микроорганизмы, поступая
из первичного очага в кровеносное русло,
транспортируются в капилляры различных
органов, где и оседают, создавая гнойные
очаги. Иногда могут развиваться вторичные
гнойные метастазы);
5. По
клинической картине
– молниеносный, острый, подострый,
хронический.
Молниеносный сепсис
развивается очень быстро, уже в течение
нескольких часов после заражения
появляются клинические симптомы. Через
5-7 дней может наступить летальный исход
даже при своевременном лечении.
Острый
и подострый сепсис характеризуется
более благоприятным течением (более 3
или 6 недель); подострым также считают
сепсис давностью 2—12 недель.
Хронический
– длиться годами с периодическими
обострениями и ремиссиями.
от 12 недель
до нескольких лет.
6.
По фазам развития:
1. Фаза напряжения –
резкая мобилизация защитных сил организма
в результате стимуляции
гипофизарно-надпочечниковой системы.
2. Катаболическая
фаза – проявляется
катаболизмом белков, жиров и углеводов;
а также нарушениями водно-солевого и
кислотно-щелочного равновесия.
3. Анаболическая
фаза – проявляется
переходом метаболизма на анаболический
путь. В первую
очередь восстанавливаются структурные
протеины. 4. Реабилитационная
фаза – происходит
полное восстановление всех обменных
процессов.
62.Сепсис.
Современная классификация. Клиника,
диагностика, лечение, профилактика.
Сепсис
— генерализованная
гнойно-воспалительная инфекция,вызванная
условнопатоген. бактер. флорой с
развитием
воспалительной реакции
организма на фоне иммунной дисфункции
и присутствием
возбудителя в крови).
приводящий к генерализованному
повреждению эндотелия сосудистого
русла, стойким нарушениям
микроциркуляции,
расстройствам
гемостаза с
обязательным ДВС и дальнейшей полиорганной
недостаточностью.
Классификация
сепсиса:
1. По
виду возбудителя
– стафилококковый, стрептококковый,
колибациллярный, неклостридиальный,
клостридиальный, смешанный;
2. По
расположению входных
ворот инфекции
– хирургический, урологический,
гинекологический, отогенный,
тонзилогенный;
3. По
наличию или отсутствию видимого
очага инфекции
– первичный (криптогенный), вторичный;
4.
По наличию или
отсутствию гнойных
метастазов –
септицемия (характеризуется массивным
поступлением в кровь токсинов с тяжелой
общей интоксикацией. Этот процесс обычно
не сопровождается гнойными метастазами),
септикопиемия (характеризуется
бактериемией и гнойными метастазами в
различные органы. Обычно при септикопиемии
из крови высевается стафилококк. При
этом процессе микроорганизмы, поступая
из первичного очага в кровеносное русло,
транспортируются в капилляры различных
органов, где и оседают, создавая гнойные
очаги. Иногда могут развиваться вторичные
гнойные метастазы);
5. По
клинической картине
– молниеносный, острый, подострый,
хронический.
Молниеносный сепсис
развивается очень быстро, уже в течение
нескольких часов после заражения
появляются клинические симптомы. Через
5-7 дней может наступить летальный исход
даже при своевременном лечении.
Острый
и подострый сепсис характеризуется
более благоприятным течением (более 3
или 6 недель); подострым также считают
сепсис давностью 2—12 недель.
Хронический
– длиться годами с периодическими
обострениями и ремиссиями.
от 12 недель
до нескольких лет.
6.
По фазам развития:
1. Фаза напряжения –
резкая мобилизация защитных сил организма
в результате стимуляции
гипофизарно-надпочечниковой системы.
2. Катаболическая
фаза – проявляется
катаболизмом белков, жиров и углеводов;
а также нарушениями водно-солевого и
кислотно-щелочного равновесия.
3. Анаболическая
фаза – проявляется
переходом метаболизма на анаболический
путь. В первую очередь восстанавливаются
структурные протеины. 4. Реабилитационная
фаза – происходит
полное восстановление всех обменных
процессов.
Клиническая
картина. Специфических
клинических
симптомов сепсиса нет.
К наиболее частым симптомам сепсиса
относятся: утрата
коммуникабельности,
летаргия или гипервозбудимость, гипо-
или гипертермия,
анорексия, отсутствие
прибавок массы тела, вздутие живота,
срыгивания, диарея,
респираторные нарушения и апноэ,
тахикардия, нарушения
периферического кровообращения,
гипотензия, желтуха,
кожные сыпи, лактат-ацидоз, нестабильный
уровень глюкозы в крови (гипергликемия
или гипогликемия).
Диагностика.
У новорожденных надо
различать клинические
и лабораторные
критерии системного воспалительного
ответа (СВО).
Клинические
критерии СВО: 1.
Расстройство температурного гомеостата
(гипертермия
или гипотермия).
2. Одышка
или тахипноэ более
60 в 1 минуту. 3. Тахикардия
более 160 в 1 минуту
или брадикардия менее ПО в 1 минуту. 4.
Утрата
коммуникабельности,
анорексия, угнетение и/или судороги.
5. Олигурия
в течение 6 часов
и более на фоне адекватной инфузионной
терапии (диурез менее 1 мл/кг/ч).
Лабораторные
признаки СВО у
новорожденных:
1. Внезапно возникший
тяжелый
метаболический
лактат-ацидоз
с гипокапнией (последнее
при отсутствии поражения легких).
2.
Лейкоцитоз
(количество лейкоцитов у детей первого
дня жизни - более 30000, у детей в возрасте
2- 7 дней жизни - более 15000, у более старших
- свыше 15000 в 1 мкл капиллярной крови) или
лейкопения
(количество
лейкоцитов в 1 мкл крови менее 5000) с
нейтрофилезом
(количество нейтрофилов в 1 мкл капиллярной
крови у детей первого дня жизни - более
20000, от 2 до 7 дней жизни — более 7000, от 8
дней жизни и старше — более 6000) или
нейтропения
(соответственно
в указанные выше дни число нейтрофилов
— менее 5000, 2000 и 1750 в 1 мкл капиллярной
крови).
3. Регенераторный
или регенераторно-дегенеративный сдвиг
лейкоцитарной формулы
при числе палочкоядерных
и более молодых форм более
2000 в мкл (в первый день жизни — более
5000 в мкл).
4. Токсическая
зернистость
нейтрофилов.
5. Тромбоцитопения.
6. Анемия.
7. Внезапно возникшее укорочение
или удлинение активированного
частичного тромбопластинового времени
(АЧТВ)
или протромбинового
времени (ПТВ).
8. Повышение
уровня CR-протеина
или других острофазовых белков.
9.
Увеличение СОЭ более 10 мм/ч.
10.
Бактериемия.
11. Гипергликемия более 6,5
ммоль/л.
Важнейшим в диагностике
сепсиса является рациональное и
обстоятельное бактериологигеское
обследование.
Очень существен объем бактериологического
обследования, включающий
трехкратные посевы
крови (количество
крови для посева не менее 1 мл), посевы
мочи и всего того
субстрата, который необходимо получить
у больного, — содержимое дыхательных
путей, ликвор, гной
и т. д. В разных родильных домах и
отделениях патологии новорожденных
могут доминировать разные возбудители
сепсиса, но наиболее типично, что сепсис
в первые дни жизни чаще
вызывают стрептококки группы В,
в более поздние
периоды - грамотрицательные микробы -
эшерихии, клебсиеллы, палочка сине-зеленого
гноя. В последние
годы вновь увеличилась частота выделения
стафилококков, особенно коагулазаотрицательных,
как возбудителей неонатального сепсиса.
У
недоношенных детей с подозрением на
сепсис обязательно
обследование на внутриутробные инфекции
(как минимум на цитомегаловирусную,
герпетическую, микоплазменную, хламидийную
и токсоплазменную).
Лечение.
Сепсис следует
диагностировать у детей с факторами
высокого риска, имеющих 4
клинических и 4 лабораторных признака
СВО . Если у ребенка
имеется клинически очевидный
очаг инфекции или бактериемия,
то для диагностики сепсиса достаточно
четырех клинических
и трех лабораторных
признаков СВО .
При всех вариантах
основой лечения являются противоинфекционная
терапия —
рациональный выбор антибиотиков,
асептика и естественное вскармливание,
специфическая пассивная иммунотерапия.
При
раннем появлении признаков тяжелой
бактериальной инфекции (в первые три
дня жизни) начинают с назначения
ампициллина
(активен против стрептококков В,
энтерококков - стрептококков D ). Далее
антибиотик выбирают в зависимости
от выявленного возбудителя,
но чаще назначают «защищенные пенициллины»
(аминопенициллины
+ ингибиторы беталактамаз)
в сочетании с цефалоспоринами
III— IV поколения или аминогликозидами.
Очень редко (по жизненным показаниям)
применяют карбопенемы,
ципрофлоксацин.
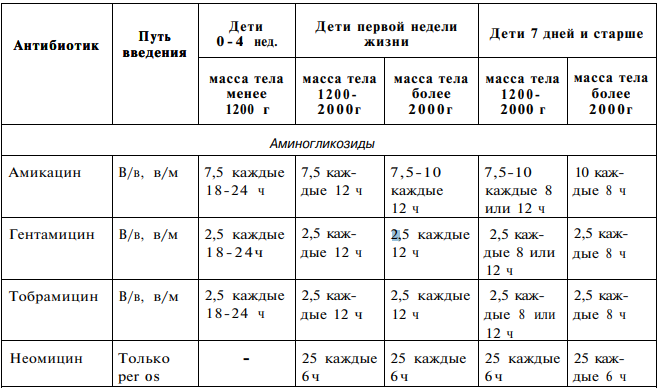
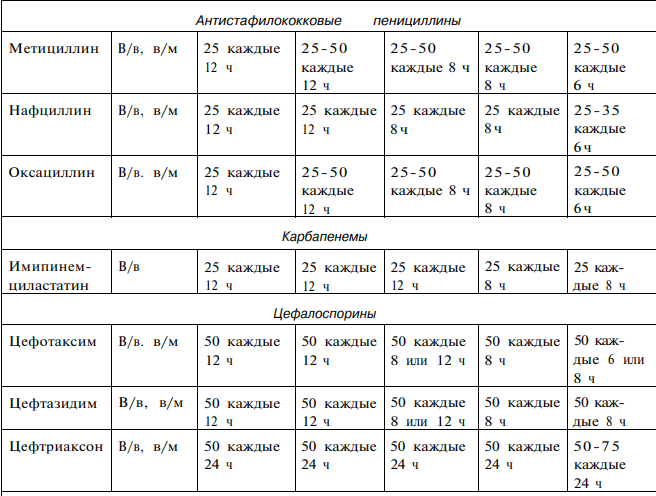
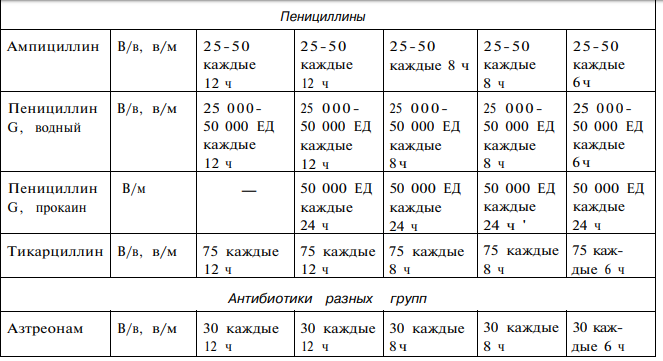 Современная
терапия в неонатологии — М.: МЕДпресс,
2000. 261 с.) рекомендуют начинать терапию
новорожденных гентамицином
или тобрамицином
с 5 мг/кг (нетилмицин - 6 мг/кг), вводимыми
внутривенно или внутримышечно каждые
24 ч.
Ухудшение при переливании свежей
крови и нейтрофильной массы при
гиперэргическом варианте, возможно,
связано с дополнительным поступлением
клеток медиаторов воспаления и
прокоагулянтов. При
гипоэргическом варианте с гранулоцитопенией
особенно показано переливание
гранулоцитарной массы,
применение гранулоцитарного гемопоэтина
и иногда переливание свежей крови, что
важно не только в плане коррекции дефекта
фагоцитарного звена (у новорожденных
в 4 раза меньший гранулоцитарный резерв,
чем у детей раннего возраста), но и
восполнения факторов свертывания крови
и антитромбина III, то есть терапии
ДВС-синдрома.
Эффективность
глюкокортикоидов
безусловна при осложнении сепсиса
надпочечниковой недостаточностью, т.
е. в качестве заместительной терапии.
Что касается использования больших доз
гормонов, воздействующих на многие
обменные процессы, мембраны, лимфоидную
ткань, то в настоящее время этот вопрос
нельзя считать научно разработанным,
скорее он носит эмпирический
характер.
Профилактика.
начинается со своевременного
выявления
и санации очагов хронического воспаления
(особенно в
мочеполовой сфере) у беременной женщины,
предупреждения у нее острых инфекций,
с динамических наблюдений ее в женской
консультации, создания условий для
благоприятного течения беременности
и ранней коррекции нарушений, предупреждения
недонашивания беременности.
Самым
существенным из них является
мытье рук (!!!)
сестрами и врачами антисептическим
мылом каждый раз до и после контакта с
новорожденным ребенком. Можно использовать
мыло с хлоргексидином или бетадином.
Перед мытьем рук следует завернуть по
локоть рукава одежды и халата, снять
часы и ювелирные украшения, которые
обсеменены часто большим количеством
патогенных микроорганизмов.
63.Заболевания
пупка новорожденных. Этиология, патогенез.
Клиника, лечение, профилактика.
Гнойно-септические
заболевания пупка у новорожденных по
частоте и по практической значимости
занимают одно из первых мест в структуре
заболеваемости детей 1-го месяца
жизни.
Омфалит
- воспалительный процесс
дна пупочной ранки,
кожи и подкожной
клетчатки вокруг пупка,
пупочных сосудов
у новорожденных.
Этиология.
Пупочная инфекция довольно часто
вызывается стафилококками
и стрептококками,
реже — другими микробами (кишечная
палочка, пневмококки, дифтерийная
палочка).
Заражение в редких случаях
может произойти до
рождения, во
время перевязки и
лигирования пупочного канатика. Однако
чаще всего инфицирование происходит
между 2-м
и 12-м днем жизни,
когда культя может загрязниться мочой,
испражнениями
ребенка или произойдет занос инфекции
с окружающих предметов или рук персонала;
заражение может произойти также путем
капельной передачи инфекции от ухаживающих
лиц.
Патогенез.
Возбудитель (преимущественно стафилококк)
проникает в ткани, прилежащие к пупку,
через культю
пуповины или через ранку
после ее отпадения.
Инфекция
может распространяться и фиксироваться
в пупочных сосудах (чаще в артериях,
реже в венах), вызывая продуктивное,
гнойное или некротическое воспаление.
Распространение
воспаления приводит
к развитию флегмоны
в области пупка. При вовлечении в процесс
пупочной вены
возникает флебит
(см.), к-рый может распространиться по
воротной вене во внутрипеченочные ее
разветвления. Нередко при этом по ходу
вен образуются
гнойные очаги,
иногда уже после заживления пупочной
раны.
Клиника.
Катаральный
омфалит (мокнущий
пупок). Клинически характеризуется
наличием серозного
отделяемого из пупочной ранки и
замедлением сроков ее эпителизации.
В некоторых случаях отмечается легкая
гиперемия и незначительная инфильтрация
пупочного кольца.
При образовании кровянистых корочек в
первые дни после отпадения пуповинного
остатка возможно скопление под ними
необильного серозно-гнойного отделяемого.
Состояние
новорожденного не нарушено, температура
тела нормальная.
Изменений в анализе крови нет. Пупочные
сосуды не пальпируются.
Лечение. Местно:
3-4 раза в сутки обрабатывают 3% р-ром
перекиси водорода, йодом или зеленкой,
УФО, мазь Вишневского. А/б в/в или в/м
(оксациллин с гентамицином или
цефалоспорины II поколения).
Флегманозный
Омфалит.
Бактериальное
воспаление дна пупочной ранки,
пупочного кольца, подкожной жировой
клетчатки вокруг
пупочного кольца, пупочных сосудов.
Заболевание начинается в
конце раннего неонатального периода
или на 2-й неделе жизни,
нередко с симптомов катарального
омфалита. Через несколько дней появляется
гнойное отделяемое из пупочной ранки
— пиорея пупка,
отек и гиперемия пупочного кольца,
инфильтрация подкожной жировой клетчатки
вокруг пупка, вследствие которой пупок
выбухает над поверхностью передней
брюшной стенки. Кожа
вокруг пупка гиперемирована, горячая
на ощупь, характерно
расширение сосудов передней брюшной
стенки (усиление венозной сети), красные
полосы, обусловленные присоединением
лимфангоита. Появляются
симптомы, характерные для инфекционного
поражения пупочных сосудов. Состояние
больного нарушено, ребенок
становится вялым, хуже сосет грудь,
срыгивает,
уменьшается прибавка массы тела (возможна
потеря). Температура тела может быть
повышена до фебрильной. В анализе крови
— лейкоцитоз со сдвигом влево, увеличение
СОЭ.
Язва пупка,
НЕКРОТИЧЕСКИЙ
может возникнуть как осложнение пиореи
пупка или омфалита. Некротический
омфалит: наблюдается у ослабленных
детей при присоединении
анаэробной инфекции.
Дно пупочной ранки обычно покрыто
серозно-гнойным или гнойным отделяемым,
после удаления которого выявляется
изъязвление.
Кожа в области
пупка имеет багрово-цианотичный цвет,
некроз тканей быстро распространяется
на все слои, образуется глубокая рана,
к-рая может привести к эвентрации
кишечника. Развитие ее наиболее вероятно,
если во
время обработки пупочной ранки не
снимать корочку, скрывающую от врача
дно пупочной ранки. Общее
состояние в первые дни заболевания
может быть не нарушено, в дальнейшем
присоединяются симптомы интоксикации.
Лечение.
Антибактериальная
терапия при флегмонозном и некротическом
омфалите до получения результатов
посева и чувствительности микрофлоры
рекомендуется парентеральное (внутривенно
или внутримышечно) назначение препаратов
из группы пенициллинов
в сочетании с аминогликозидами,
дозы, способ и кратность введения
определяются инструкцией к препарату.
В случае
неэффективности лечения в течение трех
дней, проводиться смена антибактериальной
терапии на
цефалоспорины
II поколения (цефуроксим),
дозы, способ и кратность введения
определяются инструкцией к препарату.
При идентификации метициллин-резистентном
Staphylococcus aureus (MRSA) назначаются препараты
из группы гликопептидов (ванкомицин),
дозы, способ и кратность введения
определяются инструкцией к препарату.
Если
отмечается только покраснение пупочного
кольца, без отека и распространения
эритемы на кожу вокруг пупочного кольца
лечение не требуется.
Местное
лечение:
Современная
терапия в неонатологии — М.: МЕДпресс,
2000. 261 с.) рекомендуют начинать терапию
новорожденных гентамицином
или тобрамицином
с 5 мг/кг (нетилмицин - 6 мг/кг), вводимыми
внутривенно или внутримышечно каждые
24 ч.
Ухудшение при переливании свежей
крови и нейтрофильной массы при
гиперэргическом варианте, возможно,
связано с дополнительным поступлением
клеток медиаторов воспаления и
прокоагулянтов. При
гипоэргическом варианте с гранулоцитопенией
особенно показано переливание
гранулоцитарной массы,
применение гранулоцитарного гемопоэтина
и иногда переливание свежей крови, что
важно не только в плане коррекции дефекта
фагоцитарного звена (у новорожденных
в 4 раза меньший гранулоцитарный резерв,
чем у детей раннего возраста), но и
восполнения факторов свертывания крови
и антитромбина III, то есть терапии
ДВС-синдрома.
Эффективность
глюкокортикоидов
безусловна при осложнении сепсиса
надпочечниковой недостаточностью, т.
е. в качестве заместительной терапии.
Что касается использования больших доз
гормонов, воздействующих на многие
обменные процессы, мембраны, лимфоидную
ткань, то в настоящее время этот вопрос
нельзя считать научно разработанным,
скорее он носит эмпирический
характер.
Профилактика.
начинается со своевременного
выявления
и санации очагов хронического воспаления
(особенно в
мочеполовой сфере) у беременной женщины,
предупреждения у нее острых инфекций,
с динамических наблюдений ее в женской
консультации, создания условий для
благоприятного течения беременности
и ранней коррекции нарушений, предупреждения
недонашивания беременности.
Самым
существенным из них является
мытье рук (!!!)
сестрами и врачами антисептическим
мылом каждый раз до и после контакта с
новорожденным ребенком. Можно использовать
мыло с хлоргексидином или бетадином.
Перед мытьем рук следует завернуть по
локоть рукава одежды и халата, снять
часы и ювелирные украшения, которые
обсеменены часто большим количеством
патогенных микроорганизмов.
63.Заболевания
пупка новорожденных. Этиология, патогенез.
Клиника, лечение, профилактика.
Гнойно-септические
заболевания пупка у новорожденных по
частоте и по практической значимости
занимают одно из первых мест в структуре
заболеваемости детей 1-го месяца
жизни.
Омфалит
- воспалительный процесс
дна пупочной ранки,
кожи и подкожной
клетчатки вокруг пупка,
пупочных сосудов
у новорожденных.
Этиология.
Пупочная инфекция довольно часто
вызывается стафилококками
и стрептококками,
реже — другими микробами (кишечная
палочка, пневмококки, дифтерийная
палочка).
Заражение в редких случаях
может произойти до
рождения, во
время перевязки и
лигирования пупочного канатика. Однако
чаще всего инфицирование происходит
между 2-м
и 12-м днем жизни,
когда культя может загрязниться мочой,
испражнениями
ребенка или произойдет занос инфекции
с окружающих предметов или рук персонала;
заражение может произойти также путем
капельной передачи инфекции от ухаживающих
лиц.
Патогенез.
Возбудитель (преимущественно стафилококк)
проникает в ткани, прилежащие к пупку,
через культю
пуповины или через ранку
после ее отпадения.
Инфекция
может распространяться и фиксироваться
в пупочных сосудах (чаще в артериях,
реже в венах), вызывая продуктивное,
гнойное или некротическое воспаление.
Распространение
воспаления приводит
к развитию флегмоны
в области пупка. При вовлечении в процесс
пупочной вены
возникает флебит
(см.), к-рый может распространиться по
воротной вене во внутрипеченочные ее
разветвления. Нередко при этом по ходу
вен образуются
гнойные очаги,
иногда уже после заживления пупочной
раны.
Клиника.
Катаральный
омфалит (мокнущий
пупок). Клинически характеризуется
наличием серозного
отделяемого из пупочной ранки и
замедлением сроков ее эпителизации.
В некоторых случаях отмечается легкая
гиперемия и незначительная инфильтрация
пупочного кольца.
При образовании кровянистых корочек в
первые дни после отпадения пуповинного
остатка возможно скопление под ними
необильного серозно-гнойного отделяемого.
Состояние
новорожденного не нарушено, температура
тела нормальная.
Изменений в анализе крови нет. Пупочные
сосуды не пальпируются.
Лечение. Местно:
3-4 раза в сутки обрабатывают 3% р-ром
перекиси водорода, йодом или зеленкой,
УФО, мазь Вишневского. А/б в/в или в/м
(оксациллин с гентамицином или
цефалоспорины II поколения).
Флегманозный
Омфалит.
Бактериальное
воспаление дна пупочной ранки,
пупочного кольца, подкожной жировой
клетчатки вокруг
пупочного кольца, пупочных сосудов.
Заболевание начинается в
конце раннего неонатального периода
или на 2-й неделе жизни,
нередко с симптомов катарального
омфалита. Через несколько дней появляется
гнойное отделяемое из пупочной ранки
— пиорея пупка,
отек и гиперемия пупочного кольца,
инфильтрация подкожной жировой клетчатки
вокруг пупка, вследствие которой пупок
выбухает над поверхностью передней
брюшной стенки. Кожа
вокруг пупка гиперемирована, горячая
на ощупь, характерно
расширение сосудов передней брюшной
стенки (усиление венозной сети), красные
полосы, обусловленные присоединением
лимфангоита. Появляются
симптомы, характерные для инфекционного
поражения пупочных сосудов. Состояние
больного нарушено, ребенок
становится вялым, хуже сосет грудь,
срыгивает,
уменьшается прибавка массы тела (возможна
потеря). Температура тела может быть
повышена до фебрильной. В анализе крови
— лейкоцитоз со сдвигом влево, увеличение
СОЭ.
Язва пупка,
НЕКРОТИЧЕСКИЙ
может возникнуть как осложнение пиореи
пупка или омфалита. Некротический
омфалит: наблюдается у ослабленных
детей при присоединении
анаэробной инфекции.
Дно пупочной ранки обычно покрыто
серозно-гнойным или гнойным отделяемым,
после удаления которого выявляется
изъязвление.
Кожа в области
пупка имеет багрово-цианотичный цвет,
некроз тканей быстро распространяется
на все слои, образуется глубокая рана,
к-рая может привести к эвентрации
кишечника. Развитие ее наиболее вероятно,
если во
время обработки пупочной ранки не
снимать корочку, скрывающую от врача
дно пупочной ранки. Общее
состояние в первые дни заболевания
может быть не нарушено, в дальнейшем
присоединяются симптомы интоксикации.
Лечение.
Антибактериальная
терапия при флегмонозном и некротическом
омфалите до получения результатов
посева и чувствительности микрофлоры
рекомендуется парентеральное (внутривенно
или внутримышечно) назначение препаратов
из группы пенициллинов
в сочетании с аминогликозидами,
дозы, способ и кратность введения
определяются инструкцией к препарату.
В случае
неэффективности лечения в течение трех
дней, проводиться смена антибактериальной
терапии на
цефалоспорины
II поколения (цефуроксим),
дозы, способ и кратность введения
определяются инструкцией к препарату.
При идентификации метициллин-резистентном
Staphylococcus aureus (MRSA) назначаются препараты
из группы гликопептидов (ванкомицин),
дозы, способ и кратность введения
определяются инструкцией к препарату.
Если
отмечается только покраснение пупочного
кольца, без отека и распространения
эритемы на кожу вокруг пупочного кольца
лечение не требуется.
Местное
лечение:
заключается в удалении отделяемого и обработки пупочной ранки антисептическими растворами (спиртовым раствором, бриллиантовым зеленым (зеленка) или раствором йода);
в случае гнойной формы местно назначаются антибактериальные мази, а также применяется дренирование раны (установка в рану специальной трубки для оттока гноя наружу с ее помощью);
иссечение (удаление хирургическим путем) « мертвых» (некротизированных) тканей;
применяется также физиолечение (УФО – ультрафиолетовое облучение, УВЧ – ультравысокочастоная терапия).
Профилактика. ежедневно обрабатывать до полного ее заживления; сначала ранка обрабатывается 3% раствором перекиси водорода, затем сухую ранку обрабатывают 2% раствором бриллиантовой зелени (зеленкой) или спиртом; частота обработки — 3-4 раза в сутки; если из ранки появляется гнойное (отличается желтым цветом, зловонным запахом и вязкой консистенцией) или с примесью крови отделяемое, необходимо сразу обратиться к врачу. Группой повышенного риска являются новорожденные дети, которым в лечебно-диагностических целях проводили катетеризацию пупочных сосудов. Гангрена пупогного канатика (пуповинного остатка) при рождении ребенка в родовспомогательном учреждении практически не встречается. Заболевание начинается в первые дни жизни и вызывается анаэробной палочкой. Мумификация пуповинного остатка прекращается, он становится влажным, приобретает грязно-бурый оттенок и источает неприятный гнилостный запах. Отпадение пуповинного остатка запаздывает, в пупочной ранке сразу появляется гнойной отделяемое. Клиника. Состояние больного нарушено, характерна температурная реакция, симптомы интоксикации, изменения в анализе крови, соответствующие тяжести инфекционного процесса. Обычно развивается сепсис. Лечение детей с инф-ми заб-ми пупочной ранки и пуповинного остатка проводят в отделениях патологии новорожденных детской больницы. Основным условием успешной терапии явл-ся своевременное назначение а/б, активно подавляющих стафиллококки (оксациллин с гентамицином или цефалоспорины второго поколения, «защищенные» аминопеннициллины), коррекция проводится после получения сведений о возбудителе и его чувств-ти к а/б. При выраженной интоксикации, большой потере массы тела показана инфузионная терапия. На фоне а/б терапии необходимо применение эубиотиков. СВЧ на пупочную ранку. Показан курс иммунотерапии (при стафилококковой инфекции — противостафилококковым иммуноглобулином). Лечение больных с гангреной пуповинного остатка начинают с его немедленного отсечения. При тромбофлебите пупогной вены пальпируется эластичный тяж над пупком. При тромбоартериите пупочные артерии пальпируются ниже пупочного кольца. В случае возникновения перифлебита и периартериита кожа над пораженными сосудами отечна и гиперемирована, возможно напряжение передней брюшной стенки, определяемое пальпаторно. В случае развития перифлебита и периартериита кожа над пораженными сосудами отечна и гиперемирована, возможно напряжение мышц передней брюшной стенки, которое можно определить пальпаторно (положительный симптом Краснобаева). При легких массирующих движениях от периферии пораженного сосуда к пупочному кольцу на дне пупочной ранки появляется гнойное отделяемое. Возможна вялость ребенка. Прогноз благоприятный при своевременно начатой комплексной терапии, однако в дальнейшем возможно возникновение портальной гипертензии. Лечение. При тромбофлебитах вследствие катетеризации пупочной вены в случае отсутствия явлений интоксикации и других признаков наслоения бактериальной инфекции проводят только местное лечение: смазывание участка кожи над веной гепариновой мазью и мазью с а/б (оптимально: мупипроцин-бактробан), чередуя их каждые 2 ч, систематическая обработка пупочной ранки, физиотерапия (СВЧ, УФ-облучение, электрофорез с а/б). 64.Гемолитическая болезнь новорожденных. Этиология, Патогенез. Клинические формы. Гемолитическая болезнь новорожденных (ГБН) - заболевание, обусловленное иммунологигеским конфликтом (изоиммунизация) вследствие несовместимости плода и матери по эритроцитарным АГ: системы «резус», АВО или более редким факторам. ГБН в России диагностируют у 0,6% новорожденных. Среди массы известных эритроцитарных АГ, а их выделяют более 400, объединенных в 14 основных групп, наибольшее значение в развитии ГБН имеют антигены системы «резус» и АВО. Система «резус» состоит из 6 основных антигенов, синтез которых определяют 3 пары генов. Для их обозначения используют две терминологии: Фишера (антигены при этом обозначают С,с; D,d; Е,е) и Виннера (антигены Rh', hr'; Rho, Hro, Rh", hr"). Резус-положительные эритроциты содержат D-фактор (Rho), а так называемые резус-отрицательные — его не имеют, хотя в них присутствуют (за редчайшими исключениями) другие антигены системы «резус». D-антиген — липопротеин располагается на внутренней поверхности цитоплазматической мембраны, в то время как А-, В-антигены — на наружной. Этиология. При резус-конфликте, как правило, имеет место предшествующая сенсибилизация матери (аборты, рождение резус-положительного ребенка при предшествующей беременности, так как в родах всегда имеет место небольшая фетоматеринская трансфузия). В связи с этим необходимо напомнить, что D-антигены появляются у эмбриона уже на 5—6-й неделе, следовательно, возможна сенсибилизация даже на ранних сроках абортов и не только эритроцитарными антигенами, но и тканевыми. При последующих беременностях и Rh-несовместимости формируется вторичный иммунный ответ с резким нарастанием специфических IgG. Патогенез. аборты, рождение резус-положительного ребенка при предшествующей беременности, так как в родах всегда имеет место небольшая фетоматеринская трансфузия - D-антигены появляются у эмбриона уже на 5—6-й неделе, следовательно, возможна сенсибилизация даже на ранних сроках абортов и не только эритроцитарными антигенами, но и тканевыми. При последующих беременностях и Rh-несовместимости формируется вторичный иммунный ответ с резким нарастанием специфических IgG. При АВО-несовместимости плода и матери ГБН может развиваться даже при первой беременности, так как ведущим патогенетическим моментом является нарушение плацентарного барьера, вызванное различными причинами: гестозом, соматическими заболеваниями матери, инфекцией, гипоксией, прививками. Антитела, возникшие после иммунизации матери групповыми антигенами и относящиеся к IgG, в отличие от естественных, свободно проходят и через нормальную плаценту, вызывая гемолиз. Наиболее часто ГБН в связи с конфликтом по системе АВО возникает при наличии у матери группы О (I), а у ребенка - А (II). В основе патогенеза ГБН, как уже указывалось, лежит изоиммунизация матери эритроцитарными АГ плода, транспорт антиэритроцитарных АТ матери через плаценту, внутриклеточный (внесосудистый), а иногда и внутрисосудистый гемолиз эритроцитов ребенка и гипербилирубинемия за счет неконъюгированной его фракции. Различия в локализации гемолиза связаны с классом и субклассом антител, обладающих свойствами гемагглютининов или гемолизинов (гемолитическими свойствами, в частности, обладают субклассы IgG, и IgG3). Антитела матери могут переходить из ее крови через плаценту в кровь плода до рождения. Антитела матери прикрепляются к эритроцитам плода и разрушают их (гемолиз). У плода быстрое разрушение эритроцитов начинается, когда он еще находится в матке, и продолжается после рождения. Характер и тяжесть повреждений при ГБН также связывают со сроком начала и длительностью транспорта антител от матери к плоду. Массивное поступление материнских антител имеет место в родах. Некоторое их количество может поступать с молоком матери. Изучают роль гиперчувствительности замедленного типа (ГЗТ) в патогенезе ГБН, так как в крови больных детей обнаруживается повышенное содержание цитотоксических Т-лимфоцитов (ЦТЛ), по-видимому, материнского происхождения. Именно с ними связывают наиболее тяжелую, отечную форму ГБН. Наибольшую опасность при ГБН представляет высокий уровень в крови — неконъюгированного билирубина (НБ), обладающего липотропностью и способностью проникать в мозг, вызывая ядерную желтуху. Клиника. Отечная форма - наиболее тяжелое проявление ГБН. В анамнезе матери типичны: выкидыши, мертворождения, повторные аборты, недонашивание. При ультразвуковом обследовании характерна «поза Будды» плода, ореол вокруг свода черепа. Резко увеличена масса плаценты вследствие отека (в норме она составляет 1/6—1/7 массы тела плода, а при отеке — 1/3 и даже равна массе тела плода). Течение беременности часто осложняется гестозом в форме преэклампсии и эклампсии. У ребенка при рождении имеется асцит, анасарка с выраженным отеком наружных половых органов, ног, головы. Резко увеличен живот (бочкообразный). Выражены гепато- и спленомегалия вследствие эритроидной метаплазии и фиброза. Имеются признаки расстройств центральной и периферической гемодинамики в виде расширения границ относительной сердечной тупости, приглушенности тонов, бледности кожных покровов, олигурии и дыхательной недостаточности (часто в результате гипопластических легких или болезни гиалиновых мембран). У детей с отечной формой нередко имеется геморрагический синдром (кровоизлияния в мозг, легкие, желудочно-кишечный тракт, кожу). У части этих детей гемостазиологически выявляют ДВС-синдром, но у всех отмечается очень низкий уровень в плазме прокоагулянтов, синтез которых осуществляется в печени. Характерны: гипопротеинемия, повышение в пуповинной крови общего билирубина (как за счет прямого, так и непрямого), тяжелая анемия (концентрация гемоглобина менее 100 г/л), разной степени выраженности нормобластоз и эритробластоз, тромбоцитопения. У выживших после активного лечения детей с врожденной отечной формой ГБН нередко развиваются тяжелые неонатальные инфекции, цирроз печени, энцефалопатии. Желтушная форма — наиболее часто диагностируемая форма ГБН. У части детей желтуха имеется уже при рождении (врожденная желтушная форма), у большинства она появляется в первые сутки жизни. Чем раньше появилась желтуха, тем обычно тяжелее течение ГБН. Необходимо подчеркнуть, что жесткой зависимости между уровнем НБ и степенью иктеричности кожи нет, хотя и считают, что прокрашивание ладоней характерно для уровня НБ более 205 мкмоль/л. При АВО конфликте гипербилирубинемия обычно появляется на 2—3-й сутки жизни и даже позже. Интенсивность и оттенок желтухи постепенно меняются. Характерны также гепатоспленомегалия, желтушное прокрашивание склер, слизистых оболочек, пастозность живота. По мере нарастания уровня НБ в крови у детей нарастают признаки синдрома угнетения ЦНС , связанные с билирубиновой интоксикацией. При врожденной желтушной форме у ребенка часто имеется иммунодефицит и, как следствие, инфекционные процессы. В анализах крови характерны: разной степени выраженности гиперрегенераторная анемия с ретикулоцитозом, нормобластозом и эритробластозом, что отражается в виде повышенного количества ядросодержащих клеток крови. Иногда наблюдается и истинный лейкоцитоз с лейкемоидной реакцией. Билирубиновая энцефалопатия (БЭ) — клинически редко выявляется в первые 36 ч жизни, обычно ее диагностируют на 3-6-е сутки. Выделяют четыре фазы течения: 1) доминирование признаков билирубиновой интоксикации, нарастающий синдром угнетения ЦНС : монотонный крик, выявление только первой фазы рефлекса Моро, снижение мышечного тонуса, отказ от пищи, срыгивание, рвота, патологическое зевание, блуждающий взгляд; 2) появление классических признаков ядерной желтухи — спастичность, ригидность затылочных мышц, опистотонус, отсутствие реакции на звуковое раздражение, периодическое возбуждение и пронзительный «мозговой» крик, выбухание большого родничка, подергивание мышц лица или полная амимия, крупноразмашистый тремор, судороги; глазная симптоматика: симптом «заходящего солнца», нистагм, симптом Грефе; отмечаются остановки дыхания, нарушения сердечного ритма, летаргия, иногда — повышение температуры; 3) период ложного благополугия — обратное развитие неврологической симптоматики, когда создается впечатление, что обратное развитие неврологической симптоматики приведет даже к полной реабилитации; 4) период формирования клинигеской картины неврологигеских осложнений — клиника детского церебрального паралича; атетоз, хореоатетоз, парезы, глухота; задержка нервно-психического развития; дизартрия — все эти признаки начинают проявляться в конце периода новорожденности или на 3—5-м месяце жизни. Летальный исход, как следствие поражений мозга, развитие дыхательной и/или сердечной недостаточности, нередко на фоне геморрагического синдрома, может быть в первые две фазы билирубиновой энцефалопатии. Отмечено, что у новорожденных, особенно у недоношенных, не всегда имеются классические признаки «ядерной желтухи», поэтому в настоящее время разрабатываются различные инструментальные методы ее диагностики, направленные на выявление снижения слуха. Анемическую форму ГБН диагностируют у 10—20% больных с ГБН. Дети бледные, вялые, вяло сосут и плохо прибавляют в массе тела. Часто отмечается гепатоспленомегалия, могут быть расстройства дыхания (тахипноэ вследствие гемической гипоксии). В периферической крови обнаруживают анемию разной степени выраженности. Чаще она сочетается со сфероцитозом, нормобластозом, ретикулоцитозом, т. е. является регенераторной. Так как в этом случае эритроциты не успевают полностью гемоглобинизироваться, то наблюдается гипохромия. Иногда отмечают гипорегенераторную анемию, что объясняется торможением функций костного мозга и задержкой выхода из него зрелых и незрелых форм эритроцитов, по-видимому, вследствие недостатка гемопоэтических факторов (возможно, цитокинов). Уровень НБ обычно нормальный или умеренно повышенный. Часто анемия бывает случайной находкой и впервые обнаруживается на 2-3-й неделе жизни. Необходимо подчеркнуть, что анемия может усиливаться на фоне естественного вскармливания (потенциальный источник аллоантител), а также при воздействии ОРВ И и других инфекций, лекарственных препаратов, что может привести к резкому усилению гемолиза и даже развитию желтухи, ДВС-синдрома. 65.Гемолитическая болезнь новорожденных. Клинические формы. Лечение. Профилактика Показания к заменному переливанию крови. Клиника. Отечная форма - наиболее тяжелое проявление ГБН. В анамнезе матери типичны: выкидыши, мертворождения, повторные аборты, недонашивание. При ультразвуковом обследовании характерна «поза Будды» плода, ореол вокруг свода черепа. Резко увеличена масса плаценты вследствие отека (в норме она составляет 1/6—1/7 массы тела плода, а при отеке — 1/3 и даже равна массе тела плода). Течение беременности часто осложняется гестозом в форме преэклампсии и эклампсии. У ребенка при рождении имеется асцит, анасарка с выраженным отеком наружных половых органов, ног, головы. Резко увеличен живот (бочкообразный). Выражены гепато- и спленомегалия вследствие эритроидной метаплазии и фиброза. Имеются признаки расстройств центральной и периферической гемодинамики в виде расширения границ относительной сердечной тупости, приглушенности тонов, бледности кожных покровов, олигурии и дыхательной недостаточности (часто в результате гипопластических легких или болезни гиалиновых мембран). У детей с отечной формой нередко имеется геморрагический синдром (кровоизлияния в мозг, легкие, желудочно-кишечный тракт, кожу). У части этих детей гемостазиологически выявляют ДВС-синдром, но у всех отмечается очень низкий уровень в плазме прокоагулянтов, синтез которых осуществляется в печени. Характерны: гипопротеинемия, повышение в пуповинной крови общего билирубина (как за счет прямого, так и непрямого), тяжелая анемия (концентрация гемоглобина менее 100 г/л), разной степени выраженности нормобластоз и эритробластоз, тромбоцитопения. У выживших после активного лечения детей с врожденной отечной формой ГБН нередко развиваются тяжелые неонатальные инфекции, цирроз печени, энцефалопатии. Желтушная форма — наиболее часто диагностируемая форма ГБН. У части детей желтуха имеется уже при рождении (врожденная желтушная форма), у большинства она появляется в первые сутки жизни. Чем раньше появилась желтуха, тем обычно тяжелее течение ГБН. Необходимо подчеркнуть, что жесткой зависимости между уровнем НБ и степенью иктеричности кожи нет, хотя и считают, что прокрашивание ладоней характерно для уровня НБ более 205 мкмоль/л. При АВО конфликте гипербилирубинемия обычно появляется на 2—3-й сутки жизни и даже позже. Интенсивность и оттенок желтухи постепенно меняются. Характерны также гепатоспленомегалия, желтушное прокрашивание склер, слизистых оболочек, пастозность живота. По мере нарастания уровня НБ в крови у детей нарастают признаки синдрома угнетения ЦНС , связанные с билирубиновой интоксикацией. При врожденной желтушной форме у ребенка часто имеется иммунодефицит и, как следствие, инфекционные процессы. В анализах крови характерны: разной степени выраженности гиперрегенераторная анемия с ретикулоцитозом, нормобластозом и эритробластозом, что отражается в виде повышенного количества ядросодержащих клеток крови. Иногда наблюдается и истинный лейкоцитоз с лейкемоидной реакцией. Билирубиновая энцефалопатия (БЭ) — клинически редко выявляется в первые 36 ч жизни, обычно ее диагностируют на 3-6-е сутки. Выделяют четыре фазы течения: 1) доминирование признаков билирубиновой интоксикации, нарастающий синдром угнетения ЦНС : монотонный крик, выявление только первой фазы рефлекса Моро, снижение мышечного тонуса, отказ от пищи, срыгивание, рвота, патологическое зевание, блуждающий взгляд; 2) появление классических признаков ядерной желтухи — спастичность, ригидность затылочных мышц, опистотонус, отсутствие реакции на звуковое раздражение, периодическое возбуждение и пронзительный «мозговой» крик, выбухание большого родничка, подергивание мышц лица или полная амимия, крупноразмашистый тремор, судороги; глазная симптоматика: симптом «заходящего солнца», нистагм, симптом Грефе; отмечаются остановки дыхания, нарушения сердечного ритма, летаргия, иногда — повышение температуры; 3) период ложного благополугия — обратное развитие неврологической симптоматики, когда создается впечатление, что обратное развитие неврологической симптоматики приведет даже к полной реабилитации; 4) период формирования клинигеской картины неврологигеских осложнений — клиника детского церебрального паралича; атетоз, хореоатетоз, парезы, глухота; задержка нервно-психического развития; дизартрия — все эти признаки начинают проявляться в конце периода новорожденности или на 3—5-м месяце жизни. Летальный исход, как следствие поражений мозга, развитие дыхательной и/или сердечной недостаточности, нередко на фоне геморрагического синдрома, может быть в первые две фазы билирубиновой энцефалопатии. Отмечено, что у новорожденных, особенно у недоношенных, не всегда имеются классические признаки «ядерной желтухи», поэтому в настоящее время разрабатываются различные инструментальные методы ее диагностики, направленные на выявление снижения слуха. Анемическую форму ГБН диагностируют у 10—20% больных с ГБН. Дети бледные, вялые, вяло сосут и плохо прибавляют в массе тела. Часто отмечается гепатоспленомегалия, могут быть расстройства дыхания (тахипноэ вследствие гемической гипоксии). В периферической крови обнаруживают анемию разной степени выраженности. Чаще она сочетается со сфероцитозом, нормобластозом, ретикулоцитозом, т. е. является регенераторной. Так как в этом случае эритроциты не успевают полностью гемоглобинизироваться, то наблюдается гипохромия. Иногда отмечают гипорегенераторную анемию, что объясняется торможением функций костного мозга и задержкой выхода из него зрелых и незрелых форм эритроцитов, по-видимому, вследствие недостатка гемопоэтических факторов (возможно, цитокинов). Уровень НБ обычно нормальный или умеренно повышенный. Часто анемия бывает случайной находкой и впервые обнаруживается на 2-3-й неделе жизни. Необходимо подчеркнуть, что анемия может усиливаться на фоне естественного вскармливания (потенциальный источник аллоантител), а также при воздействии ОРВ И и других инфекций, лекарственных препаратов, что может привести к резкому усилению гемолиза и даже развитию желтухи, ДВС-синдрома. Лечение. При врожденной отёчной форме ГБН необходимо немедленно, во избежание гиперволемии, пережать пуповину и срочно (в течение часа) начать заменное переливание крови (ЗПК) или переливание эритроцитной массы, если дети не желтушны. У детей при гиперволемии очень легко развивается сердечная недостаточность, поэтому вначале эритроцитную массу переливают лишь в объеме 10 мл, а при проведении первого ЗПК резус-отрицательной эритроцитной массой, (взвешенной в свежезамороженной плазме так, чтобы гематокрит был 0,7 л/л), ее общий объем иногда снижают до 75—80 мл/кг или, если проводят ЗПК в полном объеме (2 ОЦК на 1 кг, т. е. 170 мл/кг), то выпускают крови на 50 мл больше, чем вводят. Переливание необходимо делать очень медленно, контролируя ЦВД (3—5 см вод. ст.), частоту сердечных сокращений и АКД Часто у таких детей развивается дыхательная недостаточность (на фоне гипоплазии легких или СДР) и им требуется дополнительная подача кислорода с созданием положительного давления на выдохе, проведение ВИВЛ или ИВЛ. Наличие геморрагического синдрома требует переливания свежезамороженной плазмы или теплой донорской крови (10—15 мл/кг), викасола (1 мг/кг), при тяжелой тромбоцитопении (менее 30 ООО в 1 мкл) необходимо переливание тромбоцитной массы. При очень резкой гипопротеинемии (менее 40 г/л) показано введение 12,5% раствора альбумина (1 г/кг). При развитии сердечной недостаточности назначают дигоксин (доза насыщения 0,03 мг/кг дается за 2—3 дня). Как правило, необходимы повторные ЗПК. При желтушной форме кормление донорским молоком начинают через 2—6 ч после рождения в количестве, соответствующем возрасту, до исчезновения аллоантител в молоке матери, что обычно бывает на 2—3-й неделе жизни. Лечение собственно гипербилирубинемий с НБ в крови делится на консервативное и оперативное (заменное переливание крови, плазмаферез, гемосорбция). Фототерапия — в настоящее время наиболее широко используемый, эффективный и практически безопасный метод консервативного лечения гипербилирубинемий. Обычно источник голубого света (длина волны 450 нм) располагается в 45—50 см над ребенком, он должен создавать освещенность 5—30 микроватт/см2 /мин. В первый день жизни доношенным детям обычно вливают 60—65 мл/кг 5—10% растворов глюкозы, под контролем уровня глюкозы в крови. Далее добавляют по 20 мл/кг ежедневно, доводя объем раствора к 5-м суткам жизни до 150 мл/кг. Со вторых суток жизни производят коррекцию уровня кальция соответственно физиологической потребности (в норме у доношенного ребенка она составляет 75 мг/кг/сут.). Из других методов лечения рассматривают препараты, адсорбирующие в кишегнике НБ. Считается, что очистительная клизма в первые 2 ч жизни достоверно уменьшает выраженность максимального подъема уровня НБ крови. После 12 ч жизни такое лечение эффекта не имеет. Фенобарбитал, зиксорин, назначенные после рождения, способствуют активации образования БДГ и улучшают отток желчи. В первый день терапии фенобарбитал назначают в дозе 20 мкг/кг/сут. (разделить на 3 приема) и далее — по 3,5—5 мг/кг/сут. Профилактика. Необходимо отметить два важнейших обстоятельства, повышающих риск ГБН: 1) каждую девочку необходимо рассматривать как будущую мать, и поэтому в связи с опасностью сенсибилизаци переливание крови и ее препаратов должно проводиться только по жизненным показаниям. 2) риск ГБН (как и других форм тяжелой перинатальной патологии) значительно возрастает после абортов. Разъяснение женщинам вреда аборта может служить целям профилактики ГБН. Основным методом профилактики ГБН можно считать обеспечение нормального течения беременности, предотвращающее нарушение плацентарного барьера, возникающее вследствие инфекции, гипоксии любой этиологии, стресса, голодания и др. Анти-D антитела применяют уже 25 лет, что позволило снизить частоту развития ГБН у последующих детей резус-отрицательных матерей минимум на 90%. Сущность специфической профилактики заключается во введении всем резус-отрицательным женщинам в первые часы после родов или аборта (не позднее 72 часов) антител против D-антигена системы резус с целью связывания резус-положительных эритроцитов ребенка в организме матери и предотвращения инициации первичного иммунного ответа, т. е. сенсибилизации матери. Обязательным условием является отсутствие в момент родов резус-антител. В настоящее время считают, что минимальная доза должна составлять 100 мкг анти-D сыворотки на каждые 5 мл клеток крови плода, перешедшей к матери. Женщинам с высоким титром резус-антител в крови во время беременности для профилактики ГБН делают подсадку лоскута кожи мужа …. Показания. Заменное (обменное) переливание крови показания к заменному переливанию крови у новорожденных детей 24 – 168 часов жизни в зависимости от массы тела при рождении. Абсолютным и показаниям и у доношенных детей являются: 1) гипербилирубинемия выше 342 мкмоль/л; 2) темп нарастания билирубина выше 6 мкмоль/л/ч; 3) уровень его в пуповинной крови выше 60 мкмоль/л. Показаниями к ЗПК в 1-е сутк и жизни, кроме того, являются: а) появление желтухи или выраженной бледности кожных покровов в первые часы жизни у ребенка с увеличением размеров печени или селезенки; б) наличие в анализах крови тяжелой анемии (Hb менее 100 г/л), нормобластоза и доказанной несовместимости крови матери и ребенка по группе или резус-фактору, особенно при неблагоприятном для ГБН анамнезе. У детей с очень низкой массой тела при рождении показанием к ЗП К являются данные, приведенные в таблице.
При
резус-конфликте для ЗПК используют
кровь той же группы, что и ребенка,
резус-отрицательную, не более 2—3 дней
консервации, в количестве 170—180
мл/кг (при НБ
сыворотки крови более 400 мкмоль/л — в
объеме 250—300 мл/кг). При АВО-конфликте
переливают кровь 0 (1) с низким титром
агглютининов, но в меньшем объеме
(250—400 мл), помня, что на следующий
день надо сделать повторное ЗПК
в том же объеме.
66.Этиология
и патогенез рахита. Классификация
рахита.
Рахит
–полиэтиологическое заболевание
раннего возраста, характеризующееся
нарушениями
обмена веществ,
преимущественно фосфорно-кальциевого,
сопровождается поражением многих
органов и систем, развитием деформации
скелета.
Рахит
— нарушение минерализации растущей
кости, обусловленное временным
несоответствием между потребностями
растущего организма в фосфоре и кальции
и недостаточностью систем, обеспечивающих
их доставку в организм ребенка.
Этиология.
Экзогенные:
Недостаточное
поступление витамина Д,
фосфатов, кальция, магния, цинка и других
микроэлементов, витаминов,
аминокислот.
Недостаточное
пребывание ребенка на свежем воздухе
и недостаточная
инсоляция, что приводит к нарушению
образования витамина Д₃ из
7-дегидрохолестерина
в эпидермисе под
влиянием ультрафиолетовых лучей.
Рассматривая
алиментарный фактор, необходимо сказать,
что к развитию рахита могут привести:
позднее введение
в рацион ребенка животной пищи,
вегетарианское
питание с
использованием большого количества
фитина и лигнина, которые нарушают
абсорбцию кальция, фосфора, а также
экзогенного витамина D; отсутствие
специфической профилактики рахита;
вскармливание
недоношенного ребенка не обогащенными
фосфатами искусственными смесями.
Эдогенные
факторы:
Нарушение
процессов всасывание
витамина Д₃ в
кишечнике, при
мальабсорбции (всас) и мальдигестии
(пищевар).
Нарушение
процессов гидроксилирования
неактивных форм витамина
Д в активные
формы (Д₃) в
печени и почках. вследствие
недостаточного желчеотделения и
нарушения расщепления
жиров.
Нарушение
всасывания фосфора
и кальция
в кишечнике, их
повышенное выведение
с мочой, нарушение
утилизации костной тканью. При
синдроме массивной потери белков
(экссудативная энтеропатия, нефротический
синдром, ожоговая болезнь и пр.) могут
элиминироваться из организма а-глобулины
— переносчики активных
метаболитов D
вместе с последними.
Нарушение
функциональной
активности рецепторов
к витамину Д₃.
Патогенез.
В сложных механизмах
развития рахита основное место принадлежит
гиповитаминозу
D. Его специфическая
функция заключается в регуляции
процессов всасывания
кальция, фосфора
в кишечнике и
отложения
их в костную ткань,
а также реабсорбции
кальция и фосфатов в почечных
канальцах.
Витамин
D проявляет своё
специфическое действие не в виде
соединения, которое образуется в коже
под влиянием ультрафиолета или поступает
в организм с пищей, а
в форме активных
метаболитов,
последовательное преобразование которых
происходит в печени
и затем в почках
с участием специфических ферментов —
гидроксилаз.
Временное
отставание любой из этих систем,
участвующих в
утилизации витамина D,
может явиться причиной
нарушения минерального обмена.
К числу подобных причин могут относиться
нарушения всасывания
витамина D в кишечнике из-за недостаточного
образования и секреции желчи,
малая активность
25-гидроксилазы печени
и 1-альфа-гидроксилазы почек,
участвующих в
биосинтезе активных метаболитов,
нехватка белков,
транспортирующих активные формы витамина
D, дефицитная
эффективность систем, участвующих в
транспорте ионов Са через
энтероцит.
Нарушения
фосфорно-кальциевого обмена,
связанные с гиповитаминозом D, низким
уровнем тиреокальцитонина и
гиперпаратиреозом,
приводят к снижению
окислительных процессов,
развитию
ацидоза в кости,
углубляющего изменения
клеточного метаболизма и нарушающего
нормальный процесс обызвествления
хрящевой и остеоидной ткани.
Разнообразные нарушения в обмене
веществ сочетаются со значительными
сдвигами в системе
ферментов.
Установлено уменьшение
в крови активности фосфорилазы
и увеличение
активности щелочной
фосфатазы
(отщепляет
фосфор от органических соединений).
Повышенная активность щелочной фосфатазы,
стимулированная гормонами паращитовидных
желез, приводит
к перемоделированию кости за счёт
остеокластов и остеобластов.
Избыточная остеоидная
гиперплазия
объясняется также недостаточным
образованием 24,25-диокси-витамина D,
контролирующего синтез белковой стромы
кости (неконтролируемая остеоидная
гиперплазия).
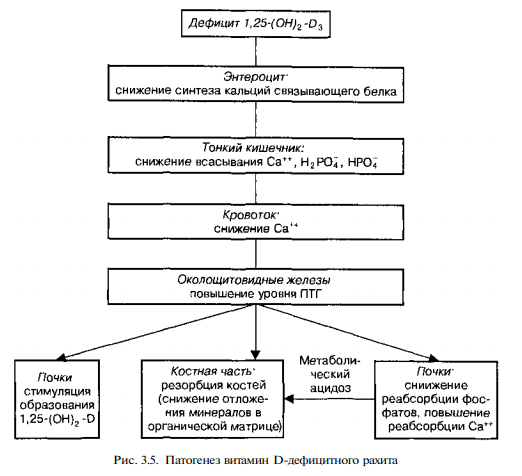
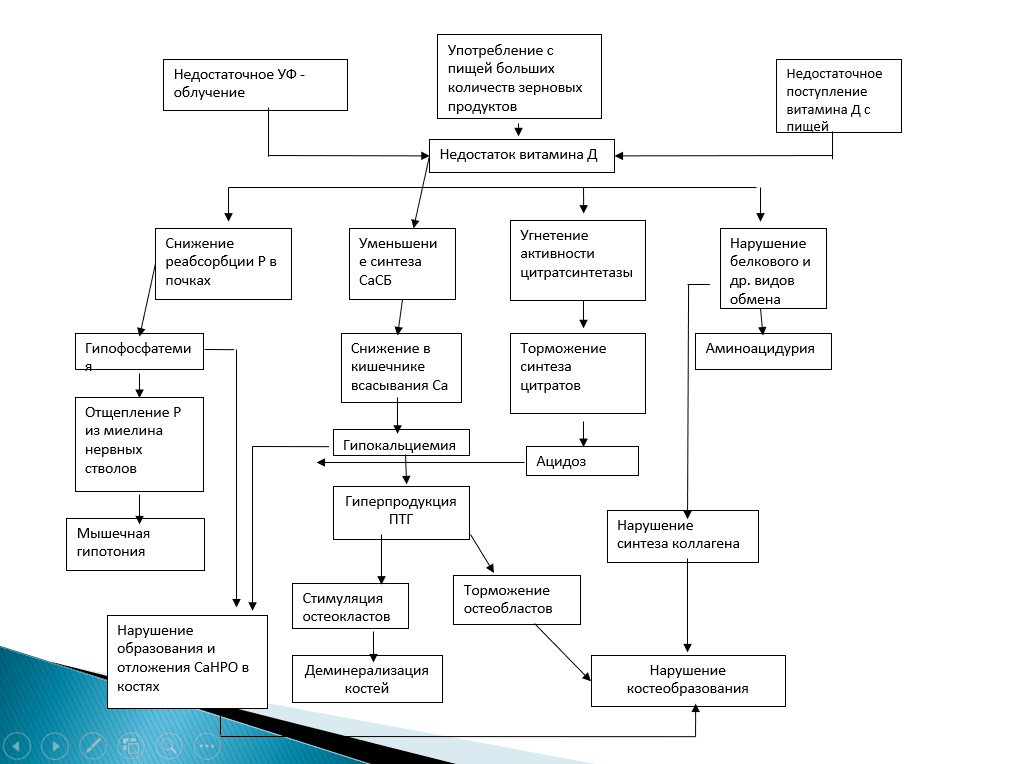
 Провитамин
D3 (холекальциферол)
синтезируется в базальтном
слое эпидермиса под
действием определенного спектра
солнечных лучей с длиной волн от 290-315
нм. При этом проявляется: феномен
«доза-эффект». За
данный спектр лучей с предшественником
D3 конкурирует меланин. Провитамин
D3 гидроксилируется
в печени, и
образуется более
активный метаболит — 25-OH-D3
(25-гидроксихолекальциферол).
Второе гидроксилирование
происходит в
эпителии канальцев почек,
и образуются дигидроксихолекальциферолы
- l,25-(OH)2-D3 и 24,25-(OH)2-D3.
Первый метаболит
синтезируется в условиях гипокальциемий,
второй - при нормальном уровне кальция.
l,25(OH)2-D3 высокоактивное и высокоспецифичное
соединение, поэтому оно относится к
группе гормонов — стероидов.
Необходимо
сказать, что на всех этапах цепи
метаболизма витамина D существуют
механизмы как стимулирующие, так и
тормозящие образование активных
метаболитов. Таким образом, происходит
гомеостазирование
витамина в организме.
Все метаболиты витамина D можно обнаружить
в крови. Они транспортируются витамин
D-связывающим глобулином, относящимся
к а-глобулинам.
l,25-(OH)2-D, обладает следующими
модулирующими
эффектами на
обмен кальция и фосфора в организме:
— воздействуя на ядро энтероцита
(клетки-мишени) экспрессирует
ген, контролирующий синтез клеткой
кальцийсвязывающего белка.
Последний является активным переносчиком
ионов кальция
через стенку
тонкой кишки.
Параллельно происходит пассивный
перенос ионов фосфатных
соединений:
Н2Р04" и НР04" и тем самым способствует
всасыванию фосфатов из кишечника;
— оказывает стимулирующее реабсорбционное
воздействие на ионы кальция в почечных
канальцах (совместно с паратгормоном).
ПТГ
обладает следующими модулирующим
и эффектам и на гомеостаз кальция и
фосфора в организме:
— резорбирует соли кальция и фосфора
из кости путем активации остеокластов
(деминерализация);
- стимулирует
реабсорбцию кальция в почечных канальцах
совместно с l,25-(OH)2-D3; - снижает
реабсорбцию фосфатов в канальцах почек,
вызывая фосфатурический эффект; -
экспрессирует ген
фермента 1а-гидроксилазы,
тем самым способствует
образованию 1,25-(ОН)2-Оз в почках.
Провитамин
D3 (холекальциферол)
синтезируется в базальтном
слое эпидермиса под
действием определенного спектра
солнечных лучей с длиной волн от 290-315
нм. При этом проявляется: феномен
«доза-эффект». За
данный спектр лучей с предшественником
D3 конкурирует меланин. Провитамин
D3 гидроксилируется
в печени, и
образуется более
активный метаболит — 25-OH-D3
(25-гидроксихолекальциферол).
Второе гидроксилирование
происходит в
эпителии канальцев почек,
и образуются дигидроксихолекальциферолы
- l,25-(OH)2-D3 и 24,25-(OH)2-D3.
Первый метаболит
синтезируется в условиях гипокальциемий,
второй - при нормальном уровне кальция.
l,25(OH)2-D3 высокоактивное и высокоспецифичное
соединение, поэтому оно относится к
группе гормонов — стероидов.
Необходимо
сказать, что на всех этапах цепи
метаболизма витамина D существуют
механизмы как стимулирующие, так и
тормозящие образование активных
метаболитов. Таким образом, происходит
гомеостазирование
витамина в организме.
Все метаболиты витамина D можно обнаружить
в крови. Они транспортируются витамин
D-связывающим глобулином, относящимся
к а-глобулинам.
l,25-(OH)2-D, обладает следующими
модулирующими
эффектами на
обмен кальция и фосфора в организме:
— воздействуя на ядро энтероцита
(клетки-мишени) экспрессирует
ген, контролирующий синтез клеткой
кальцийсвязывающего белка.
Последний является активным переносчиком
ионов кальция
через стенку
тонкой кишки.
Параллельно происходит пассивный
перенос ионов фосфатных
соединений:
Н2Р04" и НР04" и тем самым способствует
всасыванию фосфатов из кишечника;
— оказывает стимулирующее реабсорбционное
воздействие на ионы кальция в почечных
канальцах (совместно с паратгормоном).
ПТГ
обладает следующими модулирующим
и эффектам и на гомеостаз кальция и
фосфора в организме:
— резорбирует соли кальция и фосфора
из кости путем активации остеокластов
(деминерализация);
- стимулирует
реабсорбцию кальция в почечных канальцах
совместно с l,25-(OH)2-D3; - снижает
реабсорбцию фосфатов в канальцах почек,
вызывая фосфатурический эффект; -
экспрессирует ген
фермента 1а-гидроксилазы,
тем самым способствует
образованию 1,25-(ОН)2-Оз в почках.
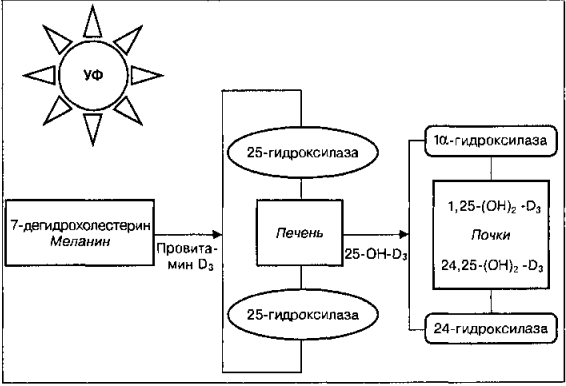 Витамин
D, поступающий в
организм с пищей,
соединяется с ОС2-гло6улином и поступает
в печень, где под действием фермента
25-гидроксалазы превращается в биологически
активный метаболит — 25-гидроксихолекальциферол
(25-OH-D,). (кальцндиол). Этот метаболит
поступает из печени в почки, где под
влиянием фермента la-гидроксилазы из
него синтезируется 2 метаболита:
•
1,25-дигидроксихолекальциферол
[lt25-(OH)2-D.J (кальцитриол), который в 5-10 раз
активнее витамина D. Это быстродействующее
активное соединение, играющее ключевую
роль в регуляции
всасывания кальция в кишечнике и доставке
его к органам и тканям.
•
24,25-дигидроксихолекальциферол
[24,25-(OH)2-D3], который обеспечивает фиксацию
кальция и фосфатов в костной ткани,
подавляет секрецию
паратгормона. Это
длительнодействующее соединение,
контролирующее минерализацию кости
при достаточной доставке кальция к
участкам её образования.
Недостаток
витамина D приводит к снижению
уровня активного метаболита в сыворотке
крови, что нарушает
всасывание ионов
кальция в кишечнике,
их реабсорбцию почечными канальцами,
а также снижает активность резорбции
кальция и фосфора из кости, что может
привести к гипокальциемии. Одновременно
паратгормон снижает реаб-сорбцию
фосфатов в канальцах почек, вследствие
чего фосфор выводится с мочой, развиваются
гиперфосфатурия и гипофосфатемия (более
ранний признак, чем гипокальциемия).
Снижение содержания
фосфора в плазме крови ведёт к замедлению
окислительных процессов в организме,
что сопровождается накоплением
недоокисленных метаболитов и развитием
ацидоза. Ацидоз также препятствует
обызвествлению костей, поддерживая
фосфорно-кальциевые соли в растворённом
состоянии. Основные патологические
изменения при рахите отмечают в
метаэпи-физарных зонах костей. Они
размягчаются, искривляются, истончаются.
Наряду с этим происходит разрастание
неполноценной (необызвествлённой)
остеоидной ткани.
Классификация.
—
по тяжести процесса
(легкая, средней тяжести и тяжелая —
соответственно I, II, III);
1.
Задействована нервная,
мышечная, костная (остеомаляция).
Податливость
родничков, плоский
затылок, вздрагивания,
потливость
(кисловатый), плаксивость, облысение
затылка, мышечная слабость.
беспокойство, плаксивость,
нарушение сна,
снижение аппетита и др.
2.
Задействованы все системы, костной –
остеоидная
гиперплазия
(перераспределение костной ткани,
реберные четки,
разрастание обедненной минеральными
солями остеоидной ткани в зонах роста
костей), бугры на
голове. Дых система-
деформация грудной клетки, ССС,
эндокринная, очень гипервозбудимый,
повышение СТГ. Метаболический
ацидоз, свойственный рахиту,
проявляется учащенным дыханием и
появлением аммиачного запаха
мочи.
остеомаляция
(размягчение костей, округлые участки
размягчения затылочной кости, легко
выявляемые при достаточно усиленном
надавливании пальцем), формированием
гаррисоновой борозды (втягивание
боковых поверхностей грудной клетки
на уровне прикрепления к ней диафрагмы),
появлением различных типов деформации
грудной клетки («куриная», грудь
«сапожника» и пр.), искривлением нижних,
а, иногда и верхних конечностей и т.д);
гипоплазия
(замедление
процессов роста, прежде всего нижних
конечностей,
позднее появление зубов и закрытия
большого родничка, костей таза);
Остеоидная
гиперплазия, клинически выглядят в виде
появления лобных и теменных бугров,
«четок» (утолщений в области перехода
костной ткани в хрящевую на ребрах),
«браслетов»
(утолщений в области лучезапястных
суставов), симптома
Марфана (утолщение
и раздвоение наружных лодыжек) и пр.
3.
Исключить рахитоподобные заболевания.
Переломы по типу «зеленой веточки»,
мышечная гипотония, симптом перочинного
ножа.
Деформация
костей черепа, грудной клетки, позвоночника
+ разнообразные изменения трубчатых
костей:
а)
верхние конечности:
искривление плечевой кости и костей
предплечья;
Деформация в области
суставов: «браслеты» (утолщение в области
лучезапястных суставов), «нити жемчуга»
(утолщение в области диафизов фаланг
пальцев).
б) нижние
конечности:
искривление бедер вперед и
кнаружи;
разнообразные искривления
нижних конечностей (О- или Х- образные
деформации,);
деформации в области
суставов.
— по
периоду болезни
(начальный, разгара репарации, остаточных
явлений);
1. Начальный – симптомы
остеомаляции, МАЛО КАЛЬЦИЯ и ФОСФОРА,
МНОГО ЩФ.
2. Период разгара – остеомаляция
(размягчение костей), гиперплазия, ОЧЕНЬ
МАЛО КАЛЬЦИЯ и ФОСФОРА, ОЧЕНЬ МНОГО
ЩФ.
3. Период остаточных явлений –
анализы в норме, но симптомы остаются.
—
по характеру течения
(острое, подострое, рецидивирующее).
1.
Острое – первые 3 месяца жизни.
Преобладание процессов
остеомаляции
над гиперплазией
остеоидной ткани («краниотабес»,
размягчение краев родничков и швов)
чаще у детей первого полугодия жизни,
у недоношенных, у детей от многоплодной
беременности, не получающих профилактические
дозы витамина Д
2. Подострое – от 3 до
года. Преобладание
гиперплазии
остеоидной ткани
в зонах роста костей («реберные четки»,
«браслеты», «бугры»
и др.). Чаще встречается во втором
полугодии, у детей, получающих недостаточную
профилактическую дозу витамина Д.
3.
Рецидивирующее. Повторное обострение
затихшего рахитического процесса. При
рентгенологическом обследовании костей
– определяются
полоски обызвествления в метафизарных
зонах трубчатых костей.
Данное течение более характерно для
вторичного или наследственных форм
рахита.
Витамин
D, поступающий в
организм с пищей,
соединяется с ОС2-гло6улином и поступает
в печень, где под действием фермента
25-гидроксалазы превращается в биологически
активный метаболит — 25-гидроксихолекальциферол
(25-OH-D,). (кальцндиол). Этот метаболит
поступает из печени в почки, где под
влиянием фермента la-гидроксилазы из
него синтезируется 2 метаболита:
•
1,25-дигидроксихолекальциферол
[lt25-(OH)2-D.J (кальцитриол), который в 5-10 раз
активнее витамина D. Это быстродействующее
активное соединение, играющее ключевую
роль в регуляции
всасывания кальция в кишечнике и доставке
его к органам и тканям.
•
24,25-дигидроксихолекальциферол
[24,25-(OH)2-D3], который обеспечивает фиксацию
кальция и фосфатов в костной ткани,
подавляет секрецию
паратгормона. Это
длительнодействующее соединение,
контролирующее минерализацию кости
при достаточной доставке кальция к
участкам её образования.
Недостаток
витамина D приводит к снижению
уровня активного метаболита в сыворотке
крови, что нарушает
всасывание ионов
кальция в кишечнике,
их реабсорбцию почечными канальцами,
а также снижает активность резорбции
кальция и фосфора из кости, что может
привести к гипокальциемии. Одновременно
паратгормон снижает реаб-сорбцию
фосфатов в канальцах почек, вследствие
чего фосфор выводится с мочой, развиваются
гиперфосфатурия и гипофосфатемия (более
ранний признак, чем гипокальциемия).
Снижение содержания
фосфора в плазме крови ведёт к замедлению
окислительных процессов в организме,
что сопровождается накоплением
недоокисленных метаболитов и развитием
ацидоза. Ацидоз также препятствует
обызвествлению костей, поддерживая
фосфорно-кальциевые соли в растворённом
состоянии. Основные патологические
изменения при рахите отмечают в
метаэпи-физарных зонах костей. Они
размягчаются, искривляются, истончаются.
Наряду с этим происходит разрастание
неполноценной (необызвествлённой)
остеоидной ткани.
Классификация.
—
по тяжести процесса
(легкая, средней тяжести и тяжелая —
соответственно I, II, III);
1.
Задействована нервная,
мышечная, костная (остеомаляция).
Податливость
родничков, плоский
затылок, вздрагивания,
потливость
(кисловатый), плаксивость, облысение
затылка, мышечная слабость.
беспокойство, плаксивость,
нарушение сна,
снижение аппетита и др.
2.
Задействованы все системы, костной –
остеоидная
гиперплазия
(перераспределение костной ткани,
реберные четки,
разрастание обедненной минеральными
солями остеоидной ткани в зонах роста
костей), бугры на
голове. Дых система-
деформация грудной клетки, ССС,
эндокринная, очень гипервозбудимый,
повышение СТГ. Метаболический
ацидоз, свойственный рахиту,
проявляется учащенным дыханием и
появлением аммиачного запаха
мочи.
остеомаляция
(размягчение костей, округлые участки
размягчения затылочной кости, легко
выявляемые при достаточно усиленном
надавливании пальцем), формированием
гаррисоновой борозды (втягивание
боковых поверхностей грудной клетки
на уровне прикрепления к ней диафрагмы),
появлением различных типов деформации
грудной клетки («куриная», грудь
«сапожника» и пр.), искривлением нижних,
а, иногда и верхних конечностей и т.д);
гипоплазия
(замедление
процессов роста, прежде всего нижних
конечностей,
позднее появление зубов и закрытия
большого родничка, костей таза);
Остеоидная
гиперплазия, клинически выглядят в виде
появления лобных и теменных бугров,
«четок» (утолщений в области перехода
костной ткани в хрящевую на ребрах),
«браслетов»
(утолщений в области лучезапястных
суставов), симптома
Марфана (утолщение
и раздвоение наружных лодыжек) и пр.
3.
Исключить рахитоподобные заболевания.
Переломы по типу «зеленой веточки»,
мышечная гипотония, симптом перочинного
ножа.
Деформация
костей черепа, грудной клетки, позвоночника
+ разнообразные изменения трубчатых
костей:
а)
верхние конечности:
искривление плечевой кости и костей
предплечья;
Деформация в области
суставов: «браслеты» (утолщение в области
лучезапястных суставов), «нити жемчуга»
(утолщение в области диафизов фаланг
пальцев).
б) нижние
конечности:
искривление бедер вперед и
кнаружи;
разнообразные искривления
нижних конечностей (О- или Х- образные
деформации,);
деформации в области
суставов.
— по
периоду болезни
(начальный, разгара репарации, остаточных
явлений);
1. Начальный – симптомы
остеомаляции, МАЛО КАЛЬЦИЯ и ФОСФОРА,
МНОГО ЩФ.
2. Период разгара – остеомаляция
(размягчение костей), гиперплазия, ОЧЕНЬ
МАЛО КАЛЬЦИЯ и ФОСФОРА, ОЧЕНЬ МНОГО
ЩФ.
3. Период остаточных явлений –
анализы в норме, но симптомы остаются.
—
по характеру течения
(острое, подострое, рецидивирующее).
1.
Острое – первые 3 месяца жизни.
Преобладание процессов
остеомаляции
над гиперплазией
остеоидной ткани («краниотабес»,
размягчение краев родничков и швов)
чаще у детей первого полугодия жизни,
у недоношенных, у детей от многоплодной
беременности, не получающих профилактические
дозы витамина Д
2. Подострое – от 3 до
года. Преобладание
гиперплазии
остеоидной ткани
в зонах роста костей («реберные четки»,
«браслеты», «бугры»
и др.). Чаще встречается во втором
полугодии, у детей, получающих недостаточную
профилактическую дозу витамина Д.
3.
Рецидивирующее. Повторное обострение
затихшего рахитического процесса. При
рентгенологическом обследовании костей
– определяются
полоски обызвествления в метафизарных
зонах трубчатых костей.
Данное течение более характерно для
вторичного или наследственных форм
рахита.
Рабочая классификация Лукьяновой Е.М. (1988г.) выделяют: 1. Классический витамин-Д- дефицитный рахит. 2. Витамин-Д- зависимый рахит связанный с генетическим дефектом синтеза 1,25(ОН)₂Д₃ в почках или с резистентностью к нему органов мишеней. 3. Витамин-Д-резистентный рахит(тубулопатии, гипофосфатазия). 4. Вторичный рахит при заболеваниях печени, синдром мальабсорбции и др. 67.Неспецифическое действие витамина Д. - Более чем в 40 тканях – мишенях определены рецепторы к витамину Д (РВД). - За счет рецепторного влияния витамин Д оказывает воздействие на биологические реакции организма через транскрипцию генов (геномный механизм) и быстрые реакции внегеномного генеза. Открыты рецепторы к витамину Д во многих клетках иммунной системы: Синтез активных метаболитов витамина Д возможен клетками многих органов и тканей: -макрофагах. -лимфоцитах тимуса (незрелых), -СД8 – клетках (зрелых). Открыта способность мононуклеарных фагоцитов к синтезу 1,25 дигидрооксикальциферола Д три. -лимфоцитах – активированных, - доказано участие витамина Д в функционировании иммунной системы. -Д – снижает активность приобретенного иммунитета. -Усиливает активность врожденного иммунитета. -В очаге воспаления локально повышается концентрация активных метаболитов Д, что имеет защитный характер. Обнаружено множество генов участников генома человека работа их регулируется витамином Д. Это гены, кодирующие пептиды (каталицидин и дефензин –β2), обладающие противомикробной активностью. Эти пептиды – природные антибиотики широкого спектра действия – активны в отношении многих бактерий, вирусов и грибов. Обнаружено иммунносупресорное воздействие витамина Д (посредством цитокинов). Это свойство витамина Д используется при лечении аутоиммунных заболеваний с гиперпродукцией цитокинов:
сахарный диабет 1-типа
рассеянный склероз
СКВ
ревматоидный артрит
хронические заболевания ЖКТ
Витамин Д участвует в регуляции пролиферации и дифференцировки клеток всех органов и тканей, в том числе клеток крови и иммуннокомпетентных клеток. Это применимо при лечении псориаза, Подавлении роста опухоли: рак толстой кишки, молочной железы, легких, поджелудочной железы, яичников, простаты). На ССС: РВД представлены в гладкомышечной ткани, эндотелии, кардиомиоцитах. Показано участие витамина Д в регуляции уровня АД через ренин- ангиотензиновую систему. Опосредуется через подавление воспалительной реакции, которая приводит к распространению атеросклероза и застойной сердечной недостаточности. В плаценте есть α1 – гидроксилаза. Витамин Д способствует имплантации. поддерживает нормальное течение беременности. рост плода. контролирует секрецию плацентарных гормонов. ограничивает синтез провоспалительных цитокинов. Основные физиологические функции витамина D: • поддержание концентрации кальция в организме на постоянном уровне; • регуляция всасывания ионов кальция и фосфора в кишечнике, отложение их в костях; • усиление реабсорбции кальция и фосфора в почечных канальцах; • способствование своевременному достижению пиковой костной массы; • модулирование физиологических процессов. • стимуляция иммунитета; • поддержание мышечного тонуса; • гормоноподобное действие метаболита витамина Dv
68.Содержание метаболита витамина Д у детей раннего возраста и подростков в России. На территории Россйской Федерации изучение статуса витамина D у детей и подростков носило разрозненный характер. Наибольшее количество исследований приходилось на территорию северной части Российской Федерации в связи с естественным низким уровнем инсоляции.
Общее
число включенных в исследование детей
составило 1230 человек. Полученные
в ходе исследования результаты
свидетельствуют о высокой
частоте недостаточности и дефиците
витамина D в
различных регионах РФ независимо от
географического положения. Самая
низкая распространенность витамина D
зарегистрирована в СевероЗападном и
Центральном регионах. Самая низкая
частота дефицита витамина D (> 10 нг/мл)
наблюдается у детей Москвы и Екатеринбурга,
что обусловлено наибольшей
частотой сапплементации рациона
препаратами холекальциферола
у детей раннего возраста, проживающих
в этих городах. Напротив,
низкие
уровни обеспеченности витамином D
выявлены в городах
Юга России и Дальнего Востока, расположенных
ниже 45-й широты Северного полушария.
Медиана
кальцидиола в Ставрополе
составила 24,7 нг/мл, при этом только 23,7%
детей имели достаточный уровень
кальцидиола. Это связано с необоснованно
низкой частотой применения препаратов
холекальциферола, которое
не может быть компенсировано инсоляцией
как минимум в осенне-весенний период
года.
В РФ только каждый
третий ребенок
имеет достаточный уровень витамина D
(> 30 нг/мл), дети
третьего года жизни
в 9,6% имеют нормальный уровень кальцидиола.
В частности, дефицит и недостаточность
витамина D [25(ОН)D < 30 нг/мл] встречались
у 60,6% детей до 6
месяцев жизни, у
40,4% детей второго
полугодия жизни,
у 71,3% детей второго
года и 86,8% детей
третьего года жизни.
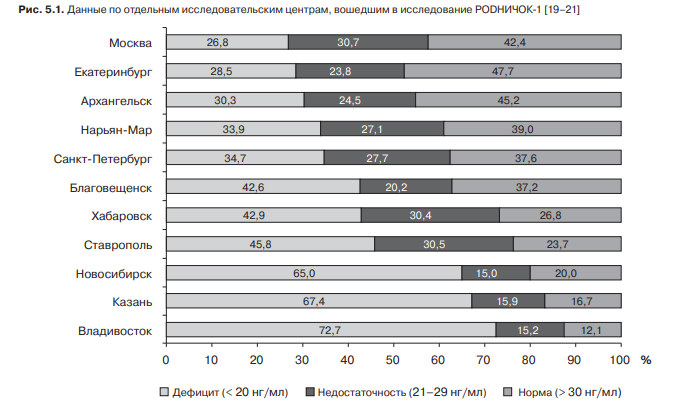
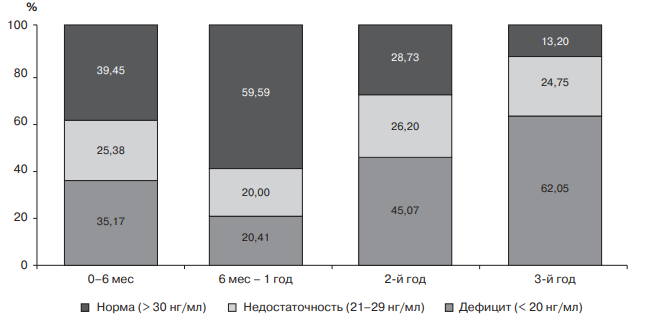 Показано,
что у детей на грудном
вскармливании уровень
кальцидиола на протяжении четырех
кварталов первого года ниже,
чем у их сверстников на искусственном
вскармливании. У
детей на естественном вскармливании
уровень кальцидиола не достигает
порогового значения 30 нг/мл в сыворотке
крови даже к возрасту 12 месяцев. Кривая
обеспеченности витамином D младенцев
на искусственном вскармливании
демонстрирует нарастание уровня 25(ОН)D
сыворотки крови с возрастом (до 7–9
месяцев), отражающее увеличение объема
получаемой смеси.
Зима, весна –
дефицит, лето- есть.Так, тяжелый дефицит
витамина D (< 10 нг/мл) наблюдается менее
чем у 8% пациентов. В то же время дефицит
витамина D (< 20 нг/мл) был установлен у
52%, а умеренный дефицит (пограничная
недостаточность) витамина (< 30 нг/мл)
— у 91% обследованных. Следовательно, в
когорте детей и подростков в возрасте
от 7 до 14 лет адекватно обеспечены
витамином D не более 10% обследованных.
69.Клиника
рахита I, II, III степени.
—
по тяжести процесса
(легкая, средней тяжести и тяжелая —
соответственно I, II, III);
1.
Задействована нервная, мышечная, костная
(остеомаляция). Податливость родничков,
плоский затылок, вздрагивания, потливость
(кисловатый), плаксивость, облысение
затылка, мышечная слабость.
беспокойство, плаксивость,
нарушение сна, снижение аппетита и
др.
Первыми симптомами рахита являются
вегетативные расстройства:
нарушения
сна;
раздражительность;
плаксивость;
повышенная
потливость: больше всего лица, волосистой
части головы;
«кислый» пот →трение
головы о подушку→облысение
затылка;
Красный
дермографизм.
Податливость
костей – края большого родничка→малого
родничка→стреловидного шва, (остеопороз
незначительный).
2.
Задействованы все системы, костной –
остеоидная
гиперплазия
(перераспределение
костной ткани,
реберные четки,
разрастание
обедненной минеральными солями остеоидной
ткани в зонах роста
костей), бугры на
голове. Дых система-
деформация грудной клетки, ССС,
эндокринная, очень гипервозбудимый,
повышение СТГ. Метаболический
ацидоз, свойственный рахиту,
проявляется учащенным дыханием и
появлением аммиачного запаха
мочи.
остеомаляция
(размягчение костей, округлые участки
размягчения затылочной кости, легко
выявляемые при достаточно усиленном
надавливании пальцем), формированием
гаррисоновой борозды (втягивание боковых
поверхностей грудной клетки на уровне
прикрепления к ней диафрагмы), появлением
различных типов деформации грудной
клетки («куриная», грудь «сапожника» и
пр.), искривлением нижних, а, иногда и
верхних конечностей и т.д);
гипоплазия
(замедление
процессов роста, прежде всего нижних
конечностей,
позднее появление
зубов и закрытия большого родничка,
костей таза);
Остеоидная гиперплазия,
клинически выглядят в виде появления
лобных и теменных бугров, «четок»
(утолщений в области перехода костной
ткани в хрящевую на ребрах), «браслетов»
(утолщений в области лучезапястных
суставов), симптома Марфана (утолщение
и раздвоение наружных лодыжек) и пр.
Появляются
более выраженные костные
изменения:
Голова:краниотабес
(размягчение участков теменных костей,
реже участков затылочной кости);
деформации
костей черепа;
лобные и теменные
бугры;
нарушение соотношения между
верхней и нижней челюстями;
позднее
закрытие большого родничка, нарушение
прорезывания зубов (несвоевременное,
неправильное), дефекты эмали зубов.
Грудная
клетка:
деформация
ключиц (усиление кривизны);
«реберные
чётки» (полушаровидное утолщение в
месте перехода хрящевой части ребра в
костную);
расширение нижней апертуры
и сужение верхней, сдавление грудной
клетки с боков;
Ладьевидные углубления
на боковых поверхностях грудной
клетки;
Деформация грудины («килевидная»,
«воронкообразная» грудь).
Позвоночник:
Кифоз
в нижнем отделе грудных позвонков, кифоз
или лордоз в поясничном отделе, сколиоз
в грудном отделе, плоский таз.
3.
Исключить рахитоподобные заболевания.
Переломы по типу «зеленой веточки»,
мышечная гипотония, симптом перочинного
ножа.
Деформация
костей черепа, грудной клетки, позвоночника
+ разнообразные изменения трубчатых
костей:
а)
верхние конечности:
искривление плечевой кости и костей
предплечья;
Деформация в области
суставов: «браслеты» (утолщение в области
лучезапястных суставов), «нити жемчуга»
(утолщение в области диафизов фаланг
пальцев).
б) нижние
конечности:
искривление бедер вперед и
кнаружи;
разнообразные искривления
нижних конечностей (О- или Х- образные
деформации,);
деформации в области
суставов.
70.Лечение
и профилактика рахита.
Лечение.
Выбор тактики лечения рахита зависит
от его формы, варианта течения, тяжести
и фазы болезни. Экзогенный дефицитный
рахит лечится в амбулаторных условиях.
Дети из плохих социально-бытовых
условий госпитализируются. Для рахита,
независимо от его форм, общим в лечении
является: — адекватное питание, режим
дня и прогулки; — массаж и ЛФК; — комплекс
витаминов групп А, В, С, лучше с минеральными
добавками (пленил и пр.).
ЕСЛИ ДЕФИЦИТ
И КАЛЬЦИЯ (2,25-2,75) И Д, ТО СНАЧАЛА КАЛЬЦИЙ
1 МЕС, ПОТОМ Д.
ЕСЛИ КАЛЬЦИЙ В НОМЕ, ТО
ВИТАМИН Д 400-500ЕД , ДО 1000ЕД.
Легение
экзогенного дефицитного рахита.
Назначение лечебных доз витамина D в
начальной фазе болезни без верификации
диагноза определением активности ЩФ
нецелесообразно. В этих случаях лучше
назначить профилактическую
дозу. Выбор дозы
препарата в фазе разгара (активности
процесса) решается индивидуально. Если
в качестве лечебного средства врачом
выбираются препараты провитамина
D2, то курсовая
доза должна
составлять от 200 ООО до 400 ООО ME. От
продолжительности запланированного
курса и выбранной курсовой дозы зависит
дневная доза витамина, которая обычно
варьирует от 2000 до 5000 ME. Если врач выбрал
в качестве исходного препарата активные
метаболиты D,
то проводится два
10-дневных курса с
интервалом в 2 недели по 1 мкг в день.
При эндогенных
вариантах дефицитного
рахита доза выбранного препарата может
быть удвоена. При этом обычно используют
активные метаболиты
D. Такие дети лечатся
в стационаре, так как возникает
необходимость лечить и основное
заболевание.
При
выраженной гипокальциемий
первоначальную дозу витамина целесообразно
удвоить. Кроме того, назначаются препараты
кальция Последние вводятся перорально,
парентерально, либо путем электрофореза.
Для перорального использования наиболее
пригодны глюконат
кальция, калтрейт-600,
кальцинова
(гранулят), растворимый
кальций и
пр.
ДОЗИРОВКА.
1ст. Суточная 2000 МЕ,
Курсовая 200 ЕД.
2ст. Суточная 4000 МЕ,
Курсовая 400 ЕД.
3ст. Суточная 6000 МЕ,
Курсовая 600 ЕД.
Профилактика: 400 МЕ.
От 400-1000.
Затем дозу
витамина D снижают до профилактической
(500 МЕ ежедневно) и применяют препарат
в течение 2 лет и на 3-м году жизни в зимнее
время.
Лечебная: 2500-3000 МЕ. (3-4 капсулы
1р в мес).
Преимущественно
используют водный раствор витамина
Д₃(холекальциферол),
в 1 капле содержится 500 МЕ. Во время
лечения витамином Д целесообразно
1 раз в неделю проводить пробу Сулковича
(определение
уровня кальция в моче.) После достижения
терапевтического эффекта переходят на
профилактическую дозу (400-500 МЕ в сутки),
которую ребенку назначают в течение 2
лет.
Вигантол (холекальциферол)
представляет собой масляный раствор
для приема внутрь с содержанием в 1 капле
около 650 МЕ активного вещества.
Аквадетрим.
Показано,
что у детей на грудном
вскармливании уровень
кальцидиола на протяжении четырех
кварталов первого года ниже,
чем у их сверстников на искусственном
вскармливании. У
детей на естественном вскармливании
уровень кальцидиола не достигает
порогового значения 30 нг/мл в сыворотке
крови даже к возрасту 12 месяцев. Кривая
обеспеченности витамином D младенцев
на искусственном вскармливании
демонстрирует нарастание уровня 25(ОН)D
сыворотки крови с возрастом (до 7–9
месяцев), отражающее увеличение объема
получаемой смеси.
Зима, весна –
дефицит, лето- есть.Так, тяжелый дефицит
витамина D (< 10 нг/мл) наблюдается менее
чем у 8% пациентов. В то же время дефицит
витамина D (< 20 нг/мл) был установлен у
52%, а умеренный дефицит (пограничная
недостаточность) витамина (< 30 нг/мл)
— у 91% обследованных. Следовательно, в
когорте детей и подростков в возрасте
от 7 до 14 лет адекватно обеспечены
витамином D не более 10% обследованных.
69.Клиника
рахита I, II, III степени.
—
по тяжести процесса
(легкая, средней тяжести и тяжелая —
соответственно I, II, III);
1.
Задействована нервная, мышечная, костная
(остеомаляция). Податливость родничков,
плоский затылок, вздрагивания, потливость
(кисловатый), плаксивость, облысение
затылка, мышечная слабость.
беспокойство, плаксивость,
нарушение сна, снижение аппетита и
др.
Первыми симптомами рахита являются
вегетативные расстройства:
нарушения
сна;
раздражительность;
плаксивость;
повышенная
потливость: больше всего лица, волосистой
части головы;
«кислый» пот →трение
головы о подушку→облысение
затылка;
Красный
дермографизм.
Податливость
костей – края большого родничка→малого
родничка→стреловидного шва, (остеопороз
незначительный).
2.
Задействованы все системы, костной –
остеоидная
гиперплазия
(перераспределение
костной ткани,
реберные четки,
разрастание
обедненной минеральными солями остеоидной
ткани в зонах роста
костей), бугры на
голове. Дых система-
деформация грудной клетки, ССС,
эндокринная, очень гипервозбудимый,
повышение СТГ. Метаболический
ацидоз, свойственный рахиту,
проявляется учащенным дыханием и
появлением аммиачного запаха
мочи.
остеомаляция
(размягчение костей, округлые участки
размягчения затылочной кости, легко
выявляемые при достаточно усиленном
надавливании пальцем), формированием
гаррисоновой борозды (втягивание боковых
поверхностей грудной клетки на уровне
прикрепления к ней диафрагмы), появлением
различных типов деформации грудной
клетки («куриная», грудь «сапожника» и
пр.), искривлением нижних, а, иногда и
верхних конечностей и т.д);
гипоплазия
(замедление
процессов роста, прежде всего нижних
конечностей,
позднее появление
зубов и закрытия большого родничка,
костей таза);
Остеоидная гиперплазия,
клинически выглядят в виде появления
лобных и теменных бугров, «четок»
(утолщений в области перехода костной
ткани в хрящевую на ребрах), «браслетов»
(утолщений в области лучезапястных
суставов), симптома Марфана (утолщение
и раздвоение наружных лодыжек) и пр.
Появляются
более выраженные костные
изменения:
Голова:краниотабес
(размягчение участков теменных костей,
реже участков затылочной кости);
деформации
костей черепа;
лобные и теменные
бугры;
нарушение соотношения между
верхней и нижней челюстями;
позднее
закрытие большого родничка, нарушение
прорезывания зубов (несвоевременное,
неправильное), дефекты эмали зубов.
Грудная
клетка:
деформация
ключиц (усиление кривизны);
«реберные
чётки» (полушаровидное утолщение в
месте перехода хрящевой части ребра в
костную);
расширение нижней апертуры
и сужение верхней, сдавление грудной
клетки с боков;
Ладьевидные углубления
на боковых поверхностях грудной
клетки;
Деформация грудины («килевидная»,
«воронкообразная» грудь).
Позвоночник:
Кифоз
в нижнем отделе грудных позвонков, кифоз
или лордоз в поясничном отделе, сколиоз
в грудном отделе, плоский таз.
3.
Исключить рахитоподобные заболевания.
Переломы по типу «зеленой веточки»,
мышечная гипотония, симптом перочинного
ножа.
Деформация
костей черепа, грудной клетки, позвоночника
+ разнообразные изменения трубчатых
костей:
а)
верхние конечности:
искривление плечевой кости и костей
предплечья;
Деформация в области
суставов: «браслеты» (утолщение в области
лучезапястных суставов), «нити жемчуга»
(утолщение в области диафизов фаланг
пальцев).
б) нижние
конечности:
искривление бедер вперед и
кнаружи;
разнообразные искривления
нижних конечностей (О- или Х- образные
деформации,);
деформации в области
суставов.
70.Лечение
и профилактика рахита.
Лечение.
Выбор тактики лечения рахита зависит
от его формы, варианта течения, тяжести
и фазы болезни. Экзогенный дефицитный
рахит лечится в амбулаторных условиях.
Дети из плохих социально-бытовых
условий госпитализируются. Для рахита,
независимо от его форм, общим в лечении
является: — адекватное питание, режим
дня и прогулки; — массаж и ЛФК; — комплекс
витаминов групп А, В, С, лучше с минеральными
добавками (пленил и пр.).
ЕСЛИ ДЕФИЦИТ
И КАЛЬЦИЯ (2,25-2,75) И Д, ТО СНАЧАЛА КАЛЬЦИЙ
1 МЕС, ПОТОМ Д.
ЕСЛИ КАЛЬЦИЙ В НОМЕ, ТО
ВИТАМИН Д 400-500ЕД , ДО 1000ЕД.
Легение
экзогенного дефицитного рахита.
Назначение лечебных доз витамина D в
начальной фазе болезни без верификации
диагноза определением активности ЩФ
нецелесообразно. В этих случаях лучше
назначить профилактическую
дозу. Выбор дозы
препарата в фазе разгара (активности
процесса) решается индивидуально. Если
в качестве лечебного средства врачом
выбираются препараты провитамина
D2, то курсовая
доза должна
составлять от 200 ООО до 400 ООО ME. От
продолжительности запланированного
курса и выбранной курсовой дозы зависит
дневная доза витамина, которая обычно
варьирует от 2000 до 5000 ME. Если врач выбрал
в качестве исходного препарата активные
метаболиты D,
то проводится два
10-дневных курса с
интервалом в 2 недели по 1 мкг в день.
При эндогенных
вариантах дефицитного
рахита доза выбранного препарата может
быть удвоена. При этом обычно используют
активные метаболиты
D. Такие дети лечатся
в стационаре, так как возникает
необходимость лечить и основное
заболевание.
При
выраженной гипокальциемий
первоначальную дозу витамина целесообразно
удвоить. Кроме того, назначаются препараты
кальция Последние вводятся перорально,
парентерально, либо путем электрофореза.
Для перорального использования наиболее
пригодны глюконат
кальция, калтрейт-600,
кальцинова
(гранулят), растворимый
кальций и
пр.
ДОЗИРОВКА.
1ст. Суточная 2000 МЕ,
Курсовая 200 ЕД.
2ст. Суточная 4000 МЕ,
Курсовая 400 ЕД.
3ст. Суточная 6000 МЕ,
Курсовая 600 ЕД.
Профилактика: 400 МЕ.
От 400-1000.
Затем дозу
витамина D снижают до профилактической
(500 МЕ ежедневно) и применяют препарат
в течение 2 лет и на 3-м году жизни в зимнее
время.
Лечебная: 2500-3000 МЕ. (3-4 капсулы
1р в мес).
Преимущественно
используют водный раствор витамина
Д₃(холекальциферол),
в 1 капле содержится 500 МЕ. Во время
лечения витамином Д целесообразно
1 раз в неделю проводить пробу Сулковича
(определение
уровня кальция в моче.) После достижения
терапевтического эффекта переходят на
профилактическую дозу (400-500 МЕ в сутки),
которую ребенку назначают в течение 2
лет.
Вигантол (холекальциферол)
представляет собой масляный раствор
для приема внутрь с содержанием в 1 капле
около 650 МЕ активного вещества.
Аквадетрим.
Лечение зависимой и резистентной форм рахита обычно проводят в специализированных лечебных учреждениях педиатр и ортопед. При этом используют большие (возрастающие) дозы активных метаболитов витамина D3 и оперативные вмешательства, нередко повторные. Такие дети обычно находятся на инвалидности. Профилактика. Профилактика рахита должна быть комплексной и начинаться еще до рождения ребенка. Будущая мама должна много времени проводить на свежем воздухе, соблюдать режим труда и отдыха, следить за характером питания (принимать больше овощей, фруктов, белка). В последние 3-4 месяца беременности рекомендуется принимать поливитаминные препараты (суточная потребность беременной в витамине D — 400 МЕ). Наилучшей профилактикой рахита для новорожденного является грудное вскармливание. Следует ежедневно гулять с ребенком, вывозить коляску на солнце. Обязательно делайте малышу массаж, гимнастику, закаливайте его. Профилактика вирусно- бактериальных и других заболеваний у беременной женщины. Своевременное лечение гестозов беременных. Профилактика невынашивания детей. Специфическая профилактика: МАТЬ Проводится в последние 2-3 месяца беременности в осенне- зимний период года. Назначают витамин Д по 400-500 МЕ каждый день. РЕБЕНОК Начинается с 3-4 недель (у недоношенных с 10-14 дня жизни). Каждый день ребенку дают 400-500 МЕ витамина Д₃ до 1- 1.5 года. В летние месяцы(2-3 мес.) витамин Д не дают в связи с интенсивной инсоляцей. Недоношенным детям и детям с повышенной пигментацией кожи ежедневную дозу витамина Д увеличивают до 800-1000 МЕ и дают в течение 1,5-2 лет, исключая летние месяцы. Для профилактики гипервитаминоза Д 1 раз в 2-7 недель необходима проводить пробу Сулковича. 71.Спазмофилия, Этиология, Патогенез. Спазмофилия (рахитогенная тетания) — это состояние, проявляющееся склонностью детей к тоническим и тонико-клоническим судорогам, возникающее на фоне течения рахита с выраженной гипокальциемией и сдвига кислотно-основного состояния в сторону алкалоза, ведущим к повышенной механической и гальванической нервно-мышечной возбудимости. О скрытой (латентной) спазмофилии клинически можно судить по появлению положительных симптомов: Хвостека, Труссо (при сдавливании плечевого нерва в течение 3 мин возникает спастическое сведение пальцев в виде «руки акушера») и ряду других феноменов, в частности, описанного М. С. Масловым (при легком уколе кожи ребенка отмечается временная остановка дыхания на высоте вдоха). Этиология. Спазмофилией болеют дети преимущественно раннего возраста от 3 мес до 2 лет с симптомами выраженного рахита. Дети старше 3 лет болеют сравнительно редко. Частота в раннем возрасте — 3—4 %. Спазмофилией болеют дети раннего возраста, находящиеся на искусственном вскармливании неадаптированными смесями, имеющие симптомы рахита. Чаще она развивается в весеннее время. Спазмофилия возникает в связи с остро развивающейся гипокальциемией на фоне электролитного дисбаланса и алкалоза, причиной которых является быстрое, почти внезапное увеличение количества активного метаболита витамина D в крови. Такая ситуация может возникнуть при одномоментном приеме большой дозы витамина D2 или D3 («ударный» метод лечения), а также при длительной экспозиции больших участков обнаженной кожи на весеннем солнце, радиация которого особенно богата ультрафиолетовыми лучами. Среди дополнительных причин развития судорожной готовности детей следует назвать снижение в крови уровня магния, натрия, хлоридов, витаминов В1 и В6. Патогенез. Критическим уровнем снижения общего кальция в сыворотке крови у детей раннего возраста считается концентрация ниже 1,75 ммоль/л. В этих случаях имеется высокий риск развития признаков явной спазмофилии, вплоть до судорожного синдрома. Однако следует сказать, что большую роль в возникновении тетании играет снижение не общего кальция, а его ионизированной формы (ниже 0,85 ммоль/л) на фоне алкалоза, возникающем при крике ребенка. Спазмофилия обычно патогенетически связана с периодом реконвалесценции среднетяжелого или тяжелого рахита. Остро возникшая гиперпродукция активной формы витамина D (1,25-(ОН)2-D) подавляет функцию паращитовидных желез, стимулирует всасывание солей кальция и фосфора в кишечнике и реабсорбцию их и аминокислот в почечных канальцах. Вследствие этого быстро повышается щелочной резерв крови вплоть до развития алкалоза, а имевшаяся ранее гипофосфатемия резко сменяется гиперфосфатемией. Кальций начинает усиленно откладываться в костях, поэтому уровень его в крови быстро падает до критического (ниже 1,7 ммоль/л). Одновременно повышается (хотя и относительно) уровень калия — биологического антагониста кальция, возникают явления гипопаратиреоидизма, алкалоза и гиперкалиемии. Гипокальциемия на неблагоприятном фоне гипопаратиреоидизма, алкалоза и гиперкалиемии обусловливает судорожную готовность ребенка, повышенную возбудимость его нервной и мышечной систем. В этих условиях любое внешнее воздействие, сопровождающееся испугом, сильными эмоциями, плачем, высокой температурой, рвотой, а также присоединением интеркуррентного заболевания могут спровоцировать спазм определенных мышечных групп или клонико-тонические судороги. 72. Спазмофилия. Клиника, Лечение. Профилактика. Спазмофилия (рахитогенная тетания) — это состояние, проявляющееся склонностью детей к тоническим и тонико-клоническим судорогам, возникающее на фоне течения рахита с выраженной гипокальциемией и сдвига кислотно-основного состояния в сторону алкалоза, ведущим к повышенной механической и гальванической нервно-мышечной возбудимости. О скрытой (латентной) спазмофилии клинически можно судить по появлению положительных симптомов: Хвостека, Труссо (при сдавливании плечевого нерва в течение 3 мин возникает спастическое сведение пальцев в виде «руки акушера») и ряду других феноменов, в частности, описанного М. С. Масловым (при легком уколе кожи ребенка отмечается временная остановка дыхания на высоте вдоха). Клиника. Согласно классификации, предложенной Е.М. Ленским в 1945 году, различают две формы спазмофилии — явную (манифестную) и латентную (скрытую). отличающиеся друг от друга степенью выраженности одного и того же патологического процесса. При скрытой форме внешне дети выглядят практически здоровыми, иногда избыточно упитанными, психомоторное развитие – в пределах нормы. Диагностировать у ребенка скрытую спазмофилию можно с помощью признаков гипервозбудимости: беспокойства, вздрагиваний, гиперестезии. симптом Хвостека — при легком поколачивании щеки между скуловой дугой и углом рта на соответствующей стороне происходит сокращение мимической мускулатуры в области рта, носа, нижнего, а иногда и верхнего века; симптом Труссо — судорожное сокращение кисти в виде «руки акушера» при сдавлении нервно-сосудистого пучка в области плеча; (при сдавливании плеча эластическим жгутом в течение 3мин). симптом Люста — поколачивание перкуссионным молоточком ниже головки малоберцовой кости вызывает быстрое отведение и подошвенное сгибание стопы; феномен Маслова — остановка дыхания на высоте вдоха при легком уколе кожи (у здорового ребенка — учащение и углубление дыхания); симптом Эрба — сокращение срединного нерва в локтевом сгибе при раздражении его гальваническим током силой менее 5 мА (в норме — больше 5 мА). Скрытая спазмофилия встречается часто, а под влиянием провоцирующих факторов (плач, высокая температура, инфекционное заболевание, рвота, испуг) может переходить в явную спазмофилию. Явная спазмофилия проявляется в виде ларингоспазма, карпопедального спазма и эклампсии, иногда сочетающихся между собой. При явной форме:
ларингоспазм — легкий или полный спазм голосовой щели. Цианоз, пучеглазие, ребенок покрывается липким потом. Затем шумный вдох — «петушиный крик». Длительность — от нескольких секунд до 1—2 мин. Приступы могут повторяться; Он проявляется звучным или хриплым вдохом при плаче и крике и остановкой дыхания на несколько секунд, при этом отмечаются испуганное выражение лица, цианоз, холодный пот, возможна потеря сознания и присоединение судорог.
карпопедальный спазм — тоническое сокращение мышц стопы и кистей. Кисти в виде «руки акушера», стопы в состоянии резкого плантарного сгибания; Нередко возникает спазм круговых мышц рта, губы принимают положение «рыбьего рта».
эклампсия — общий приступ тонико-клонических судорог с потерей сознания. Длительность — от нескольких секунд до 20—30 мин. Часто повторяющиеся приступы могут дать картину Statuseclampticus. Все симптомы скрытой и явной спазмофилии отмечаются на фоне симптомов рахита. Они возникают вслед за кратковременными тоническими судорогами. В легких случаях приступ проявляется внезапным побледнением лица, оцепенением, подергиванием мимической мускулатуры. Тяжелый приступ также начинается с подергивания мышц лица, далее судороги распространяются на шею, конечности, охватывая все большие мышечные группы, в том числе и дыхательную мускулатуру. Дыхание становится прерывистым, всхлипывающим, появляется цианоз. С самого начала приступа ребенок теряет сознание, происходит непроизвольное отхождение мочи и газов.
Лечение.
Купирование
судорожного синдрома противосудорожными
препаратами( седуксен
– 0,5% раствор 0,1
мл/кг в/м, ГОМК – 20% раствор 0,5 мл/кг в/м,
сульфат магния – 25%раствор 0,25 мл/кг
в/м).
При
ларингоспазме – обеспечить
доступ свежего воздуха,
поднести нашатырный спирт к носу,
раздражать слизистую оболочку носа,
крень языка и заднюю стенку
глотки
Восстановления
уровня кальция в крови введением 10%
раствора глюконата кальция из
расчета 0,5 мл/кг в/в медленно.
Ликвидация
алкалоза пероральным
назначением 3-5% раствора хлорида аммония
по чайной ложке
3 р. В день, витаминотерапия.
Назначение
лечебной дозы вит Д после восстановления
уровня кальция в крови для лечения
рахита.
Профилактика.
Первичная профилактика
включает предупреждение, раннюю
диагностику и адекватное
лечение рахита. Вторичная
профилактика направлена на своевременное
выявление и лечение скрытой формы
болезни, а также на длительную (в течение
6 мес — 1 года) послеприступную
противосудорожную терапию, барбитуратами
(люминал 2—3 раза
в сутки детям до 6 мес по 0,005 г, до 1 года
— по 0,005— 0,01 г, до 3 лет — по 0,01—0,075 г).
Кроме того, необходимо следить за
биохимическими показателями крови и
периодически назначать препараты
кальция.
73.Этиология
и патогенез хронических расстройств
питания у детей.
Дистрофия
- патологигеское состояние, возникающее
у детей при
хронигеском расстройстве питания,
характеризующееся отклонениями
в росте и развитии и понижением
сопротивляемости организма.
О
дистрофии можно говорить в случае, если
статус ребенка не соответствует понятию
нормотрофии.
Различают дистрофии: с
дефицитом массы
тела – гипотрофию;
с массой тела, соответствующей росту –
паратрофию;
с избыточной массой
тела –
ожирение.
Этиология:
1) экзогенная:
а) алиментарная:
несбалансированное
питание;
Нарушение всас- кишечные
ферментопатии, целиакия, муковисцидоз,
б-нь Крона, язвенный колит.
б) инфекционная;(
внутриутробные
инфекции, инфекционные заболевания
желудочно-кишечного тракта, повторные
острые
респираторные вирусные инфекции,
сепсис.) дизентерия,
колиэнтерит, сальмонеллез, вирусные
Инфекции, паразитарные инвазии,
дисбактериоз.
в) токсическая;
(использование некачественных
молочных смесей с
истекшим сроком хранения, гипервитаминозы
А и Д, лекарственные
отравления.)
г) нарушение
режима и другие неблагоприятные факторы;
экология, качество
питьевой воды, бедность
д) смешанная;
Аллергические
заболевания - пищевая аллергия,
бронхиальная астма, аллергодерматозы,
туберкулез, иммунодефициты, СПИД, хр.
заболевания.
2) эндогенная:
а) пороки
развития; внутриутробная
гипотрофия, прогерия, болезни обмена
веществ, ВПС, пороки почек, пилоростеноз,
б-нь Гиршпрунга, грыжи, «заячья
губа», «волчья пасть».
Неадекватное
обеспечение повышенных потребностей
в нутриентах (недоношенные дети, ВПС,
хроническая патология лёгких, тяжёлые
инфекции, сопровождающиеся катаболическим
стрессом и др.); интенсивный
рост. Стресс и др.
б) эндокринные
и неэндокринные расстройства;
(гипотиреоз,
адрено-генитальный синдром), гиповитаминозы,
гипервитаминозы,микроэлементозы.
в) первичные
(наследственные или врожденные)
энзимопатии.
Синдром мальабсорбции
первичной (дефицит
лактазы, сахарозы, мальтазы, муковисцидоз,
экссудативная энтеропатия) или вторичный
(непереносимость
белков коровьего молока,
синдром «короткой кишки» после обширных
резекций кишечника, вторичная
дисахаридазная недостаточность).
Этиология.
Среди причин
гипотрофии можно
выделить:
1. Пренатальные
факторы, приводящие к задержке
внутриутробного развития,—
недостаточное
питание и заболевания матери (в
ранние сроки беременности — гестоз; в
поздние сроки — патология плаценты с
нарушением маточно-плацентарного
кровообращения и внутриутробной
гипоксией плода, профессиональные
вредности, стрессы, вредные привычки,
внутриутробные инфекции).
2. Экзогенные
причины:
а)
алиментарные факторы: — количественный
недокорм
: при гипогалактии;
при затруднениях вскармливания грудью
матери — плоский, втянутый сосок, «тугая»
молочная железа; при затруднениях
вскармливания со стороны ребенка —
срыгивания, рвоты, маленькая нижняя
челюсть, короткая уздечка языка и др.;
— качественный
недокорм
: использование несоответствующей
возрасту смеси; позднее введение
прикормов; бедность суточного рациона
животными белками, жирами, витаминами,
железом, микроэлементами;
б)
инфекционные
факторы —
внутриутробные генерализованные
инфекции (цитомегалия и др.), интранатальные
инфекции, токсико-септические состояния,
пиелонефрит и инфекция мочевых путей.
Особенно часто причиной гипотрофии
являются инфекционные поражения
желудочно-кишечного тракта;
в)
токсигеские
факторы —
использование при искусственном
вскармливании молочных смесей с истекшим
сроком хранения, гипервитаминозы А и
D, отравления, в том числе лекарственные
и др.;
г) дефекты
ухода - дефицит
внимания к ребенку, ласки, психогенной
стимуляции, прогулок, массажа и гимнастики.
3. Эндогенные
причины:
а)
перинатальные
энцефалопатии,
бронхолегочная дисплазия;
б) врожденные
пороки
развития
желудочно-кишечного
тракта, а также сердечно-сосудистой
системы, синдром «короткой кишки» после
обширных резекций кишечника;
в)
наследственные
(первичные) иммунодефицитные
состояния (преимущественно
Т-системы) или вторичные иммунодефициты;
г) первичные, а также вторичные
мальабсорбции, наследственные аномалии
обмена веществ (галактоземия, фруктоземия,
лейциноз, ксантоматозы, болезни
Ниманна-Пика и Тея-Сакса и др.); д)
эндокринные заболевания (адреногенитальный
синдром, гипотиреоз, гипофизарный нанизм
и др.), диатезы.
Патогенез
гипотрофии:
При гипотрофии
нарушена утилизация
пищевых веществ (прежде
всего белков) как в кишечнике, так и в
тканях. У всех больных повышается
экскреция
азотистых продуктов с мочой с нарушением
соотношения между азотом мочевины и
общим азотом мочи.
Характерно снижение
ферментативной активности желудка,
кишечника, поджелудочной железы
и уровень дефицита соответствует тяжести
гипотрофии. Поэтому пищевая нагрузка,
адекватная здоровому ребенку, у больного
с гипотрофией II-III степени может вызвать
острое расстройство пищеварения. При
гипотрофии нарушаются
функции печени,
сердца, почек, легких, иммунной,
эндокринной, центральной нервной
системы.
Из нарушений обмена веществ
наиболее типичны: гипопротеинемия,
гипоальбуминемия, аминоацидурия,
склонность к гипогликемии, ацидоз,
гипокалиемия и гипокалийгистия,
гипокальциемия и гипофосфамения.
Снижение
ферментативной активности крови,
нарушение антитоксической, дезаминирующей,
гликоген- и протромбообразовательной
функции печени, полигиповитаминоз.
Повышенный
расход тканевых Белков, запасов жира,
Минеральных солей, микроэлементов.к
Патогенез
ожирения. Основной
причиной ожирения является энергетический
дисбаланс
между калорийностью пищи и энергетическими
затратами организма.
Это
состояние развивается в результате
погрешностей в питании: избыточное
поступление калорий с пищей и снижение
энергозатрат, нерациональное питание
(избыточное
количество углеводов или жиров), нарушение
режима питания – основной прием пищи
происходит в вечерние часы. Избыток
энергии, которая поступает с пищей,
откладывается в жировых клетках,
вследствие чего происходит увеличение
размеров адипоцитов и
повышение массы тела.
Избыточная
масса тела может являться результатом
нарушения расхода энергии в
организме вследствие метаболических,
ферментных нарушений. У здоровых людей
при увеличении
калорийности пищи повышается скорость
обменных процессов,
что способствует поддержанию постоянной
массы тела. У больных ожирением адаптации
основного обмена к изменению каллорийности
пищи не происходит.
74.Классификация
хронических расстройств питания у
детей.
Классификация
Зайцевой Г.А., Строгоновой Л.А.
В
зависимости от характера нарушений
трофики у детей первых двух лет жизни:
●
Дистрофия типа гипотрофия
– дефицит
массы тела по
отношению к росту
● Дистрофия типа
паратрофия
– избыток
массы тела по
отношению к росту
● Дистрофия типа
гипостатура
– равномерное отставание
массы тела и роста от
возрастных норм.
В зависимости от
характера нарушений
трофики у детей
более старших возрастов:
● Дистрофия
типа ожирения
● Дистрофия типа
алиментарного маразма (истощение,
кахексия у детей дошкольного и школьного
возрастов).
По времени
возникновения:
●
пренатальная (внутриутробная, врожденная)
●
постнатальная (приобретенная)
●
смешанная форма.
По
тяжести течения выделяют:
●
I степень (легкая) 10-20%
● II степень
(среднетяжелая) 20-30%
● III степень
(тяжелая) более 30%.
По
этиологии:
●
Экзогенная (алиментарная, инфекционная,
нарушение режима детей раннего возраста)
●
Эндогенная (синдром мальабсорбции,
пороки развития ЖКТ и других органов,
наследственные нарушения обмена веществ,
иммунодефицитные состояни, эндокринные
заболевания, выраженные поражения
ЦНС)
Период:
●
начальный
● прогрессирования
●
реконвалесценции
75.Клиника
гипотрофии I, II, III степени, диагностика.
 Z
-скор = 0 при величине стандартного
отклонения, равной 1,0.
ГИПОТРОФИЯ
- дистрофия,
характеризующаяся развитием истощения.
Наблюдается у 0,5-2% детей раннего
возраста.
1
СТЕПЕНЬ.
Дефицит
массы тела, достигающий 11-20% долженствующего
для данного возраста.
Последовательное
истончение
подкожного жирового слоя.
Снижение
тургора тканей.
Отсутствие
аппетита.
Нормальная
толерантность пищи.
Сохраненный
интерес к
окружающему.
Удовлетворительная
иммунологическая реактивность.
Умеренная
гипорефлексия.
Умеренная гипотония.
2
СТЕПЕНЬ.
Дефицит
массы тела 21-30%.
Бледность
кожных покровов,
эластичность снижена.
Тургор тканей
снижен.
Подкожный
жировой слой отсутствует на
животе и груди, истончен на бедрах.
Ф-ции
кишечника Снижены (в 3—4 раза).
Толерантность
пищи снижена.
Аппетит отсутствует.
Ребенок
апатичен, гиподинамичен.
Общая
иммунная
реактивность снижена.
Частые затяжные
рецидивирующие инфекции.
Гипопротеинемия,
аминоацидурия.
Гипогликемия.
Неспособность
образования новых условных
рефлексов.
Психомоторное развитие
отстает.
При насильственном кормлении
возникает рвота, нередко наблюдаются
запоры.
3
СТЕПЕНЬ.
Дефицит
массы тела более 31%.
Кожа
сухая, висит складками.
П\к
жировой слой отсутствует
практически везде (дубликатура
кожи).
Комочки Биша сохраняются на
щеках некоторое время.
Гипотермия.
Поверхностное,
аритмичное дыхание.
Тоны
сердца ослаблены.
Анорексия.
Ребенок
безразличен к окружающему.
Иммунологическая
реактивность организма резко снижена.
Частые инфекции со
стертым, атипичным септическим
течением.
Ф-ции кишечника - Резко
угнетены (в 5-10 раз).
Неустойчивый
стул (чаще
разжиженный, непереваренный, реже
запоры).
Отрицательный азотистый
баланс.
Нарушение гликогеногенеза.
Утрата
ранее приобретенных рефлексов.
Резкая
гипотония или ригидность.
Превалирует
угнетение, отрицательные эмоции и
апатия.
утрата
уже приобретенных навыков и умений.
По
внешнему виду ребенок похож на скелетик,
обтянутый сухой кожей бледно-серого
цвета, свисающей складками на ягодицах
и бедрах. Лицо – «старческое», морщинистое.
Выражены
признаки обезвоживания: жажда, западение
большого родничка и глазных яблок,
афония, сухость конъюнктив и роговицы,
яркое окрашивание слизистой губ, трещины
в углах рта («рот
воробья»).
76.Лечение
гипотрофии I, II, III степени. Диетотерапия
и медикаментозное лечение.
Профилактика.
Лечение
гипотрофии должно
быть комплексным и включает:
—
выявление
причин гипотрофии
и попытку их устранения или коррекции;
— диетотерапию;
— организацию рационального
режима, ухода, воспитания,
массаж и гимнастику;
— выявление
и лечение очагов инфекции,
рахита, анемии и других осложнений и
сопутствующих заболеваний;
—
ферменто- и витаминотерапию, стимулирующее
и симптоматическое лечение.
3.Адекватная
терапия включает в себя:
а)учёт
возраста, остроты, тяжести и характера
основного заболевания;
б)обеспечение
возрастных потребностей ребёнка в
энергии, макро- и
микронутриентах
путём постепенного увеличения
пищевой нагрузки
с учетом толерантности ребёнка к
пище;
4.организация адекватного
режима, ухода, массажа
5.заместительная
иммунотерапия
6.лечение сопутствующей
патологии и осложнений.
Основополагающим
принципом диетотерапии
при гипотрофии является трехфазное
питание :
1)
период выяснения
толерантности к пище;
2) переходный период;
3) период
усиленного (оптимального)
питания.
в)систематический учёт
фактического питания с расчётом
химического состава суточного
рациона по основным пищевым нутриентам
и энергии;
г)при гипотрофии 2-3ст.,
«омоложение
диеты» с
преимущественным использованием
грудного молока или специализированных
продуктов.
д)последовательное и
постепенное
введение продуктов прикорма
с учётом нутритивного статуса
ребёнка.
Z
-скор = 0 при величине стандартного
отклонения, равной 1,0.
ГИПОТРОФИЯ
- дистрофия,
характеризующаяся развитием истощения.
Наблюдается у 0,5-2% детей раннего
возраста.
1
СТЕПЕНЬ.
Дефицит
массы тела, достигающий 11-20% долженствующего
для данного возраста.
Последовательное
истончение
подкожного жирового слоя.
Снижение
тургора тканей.
Отсутствие
аппетита.
Нормальная
толерантность пищи.
Сохраненный
интерес к
окружающему.
Удовлетворительная
иммунологическая реактивность.
Умеренная
гипорефлексия.
Умеренная гипотония.
2
СТЕПЕНЬ.
Дефицит
массы тела 21-30%.
Бледность
кожных покровов,
эластичность снижена.
Тургор тканей
снижен.
Подкожный
жировой слой отсутствует на
животе и груди, истончен на бедрах.
Ф-ции
кишечника Снижены (в 3—4 раза).
Толерантность
пищи снижена.
Аппетит отсутствует.
Ребенок
апатичен, гиподинамичен.
Общая
иммунная
реактивность снижена.
Частые затяжные
рецидивирующие инфекции.
Гипопротеинемия,
аминоацидурия.
Гипогликемия.
Неспособность
образования новых условных
рефлексов.
Психомоторное развитие
отстает.
При насильственном кормлении
возникает рвота, нередко наблюдаются
запоры.
3
СТЕПЕНЬ.
Дефицит
массы тела более 31%.
Кожа
сухая, висит складками.
П\к
жировой слой отсутствует
практически везде (дубликатура
кожи).
Комочки Биша сохраняются на
щеках некоторое время.
Гипотермия.
Поверхностное,
аритмичное дыхание.
Тоны
сердца ослаблены.
Анорексия.
Ребенок
безразличен к окружающему.
Иммунологическая
реактивность организма резко снижена.
Частые инфекции со
стертым, атипичным септическим
течением.
Ф-ции кишечника - Резко
угнетены (в 5-10 раз).
Неустойчивый
стул (чаще
разжиженный, непереваренный, реже
запоры).
Отрицательный азотистый
баланс.
Нарушение гликогеногенеза.
Утрата
ранее приобретенных рефлексов.
Резкая
гипотония или ригидность.
Превалирует
угнетение, отрицательные эмоции и
апатия.
утрата
уже приобретенных навыков и умений.
По
внешнему виду ребенок похож на скелетик,
обтянутый сухой кожей бледно-серого
цвета, свисающей складками на ягодицах
и бедрах. Лицо – «старческое», морщинистое.
Выражены
признаки обезвоживания: жажда, западение
большого родничка и глазных яблок,
афония, сухость конъюнктив и роговицы,
яркое окрашивание слизистой губ, трещины
в углах рта («рот
воробья»).
76.Лечение
гипотрофии I, II, III степени. Диетотерапия
и медикаментозное лечение.
Профилактика.
Лечение
гипотрофии должно
быть комплексным и включает:
—
выявление
причин гипотрофии
и попытку их устранения или коррекции;
— диетотерапию;
— организацию рационального
режима, ухода, воспитания,
массаж и гимнастику;
— выявление
и лечение очагов инфекции,
рахита, анемии и других осложнений и
сопутствующих заболеваний;
—
ферменто- и витаминотерапию, стимулирующее
и симптоматическое лечение.
3.Адекватная
терапия включает в себя:
а)учёт
возраста, остроты, тяжести и характера
основного заболевания;
б)обеспечение
возрастных потребностей ребёнка в
энергии, макро- и
микронутриентах
путём постепенного увеличения
пищевой нагрузки
с учетом толерантности ребёнка к
пище;
4.организация адекватного
режима, ухода, массажа
5.заместительная
иммунотерапия
6.лечение сопутствующей
патологии и осложнений.
Основополагающим
принципом диетотерапии
при гипотрофии является трехфазное
питание :
1)
период выяснения
толерантности к пище;
2) переходный период;
3) период
усиленного (оптимального)
питания.
в)систематический учёт
фактического питания с расчётом
химического состава суточного
рациона по основным пищевым нутриентам
и энергии;
г)при гипотрофии 2-3ст.,
«омоложение
диеты» с
преимущественным использованием
грудного молока или специализированных
продуктов.
д)последовательное и
постепенное
введение продуктов прикорма
с учётом нутритивного статуса
ребёнка.
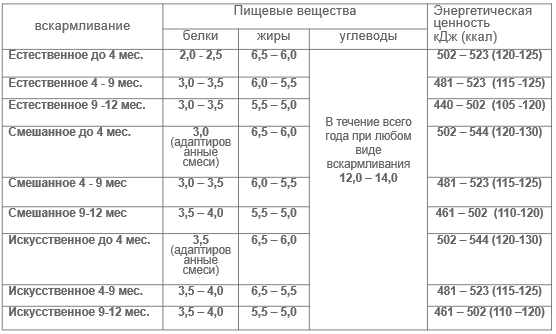 План
питания ребенка с гипотрофией
План
питания ребенка с гипотрофией
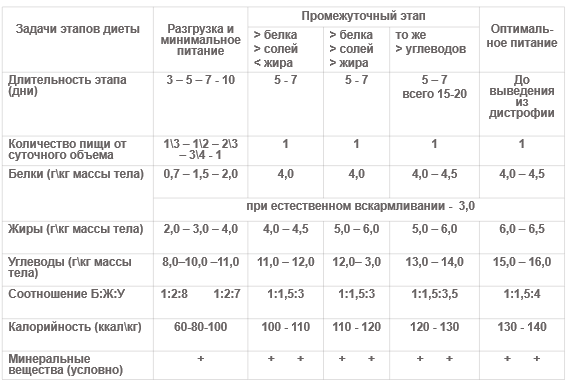
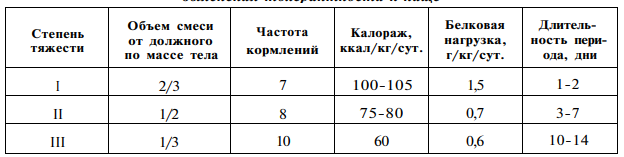 Важными
моментами диетотерапии у больных
гипотрофией являются:
Важными
моментами диетотерапии у больных
гипотрофией являются:
— использование на начальных этапах лечения лишь легкоусвояемой пищи (женское молоко, а при его отсутствии адаптированные низколактозные кисломолочные смеси, например лактофидус); — более частые кормления (7 — при гипотрофии I степени, 8 — при гипотрофии II степени, 10 кормлений при гипотрофии III степени); — систематический контроль питания (ведение дневника с отметками количества съеденной в каждое кормление пищи), стула, диуреза, количества выпитой и вводимой парентерально жидкости, солей и др.; регулярный (1 раз в 5-7 дней) расчет пищевой нагрузки по белкам, жирам, углеводам; дважды в неделю — копрограмма. Недостающую часть объема восполняют регидратационными растворами (регидрон, оралит, цитроглюкосолан, овощные отвары, изюмное питье). Необходимо, чтобы с первого же дня лечения ребенок не терял массу тела, а с 3—4-го дня, даже при тяжелых степенях гипотрофии, начал ее прибавлять по 10—20 г в сутки. При тяжелых формах гипотрофии назначают парентеральное питание — вводят глюкозу, растворы аминокислот, альбумин, солевые растворы. Целесообразна также коррекция растворов препаратами калия (до 4 ммоль/кг/сут.), кальция, фосфора, магния. В переходный период продолжают постепенное увеличение объема смеси, стремясь достичь объема питания, рассчитанного на массу, которую ребенок должен был бы иметь в этом возрасте (долженствующую массу), уменьшают количество кормлений, приступают к последовательному введению необходимых по возрасту прикормов. Нагрузку углеводами в переходный период доводят до 14-16 г/кг/сут. и после этого начинают увеличивать нагрузку белками и жирами. Повышения количества белков достигают добавлением белковых смесей и продуктов (белковый энпит); углеводов (включение сахарного сиропа, каш). Для увеличения в рационе жиров используют бифилин, жировой энпит, яичный желток. В период усиленного питания ребенок получает приблизительно такое же питание, как его сверстники, не имеющие гипотрофии. При этом энергетическое обеспечение и белковая нагрузка на фактическую массу тела больше, чем у здоровых детей. Профилактика. заключается в предупреждении, своевременном выявлении и лечении патологии беременности, в обеспечении оптимального питания и условий жизни матери и ребенку. Важны естественное вскармливание, раннее выявление и рациональное лечение гипогалактии, правильное питание с расширением его в соответствии с возрастом, достаточная витаминизация пищи, организация соответствующих возрасту ухода и режима, профилактика рахита. Очень большое значение имеют ранняя диагностика и правильное лечение рахита, анемий, инфекционных заболеваний органов дыхания, желудочно-кишечного тракта, почек, эндокринных заболеваний. Контроль за вскармливанием ребенка (контрольные взвешивания). 77.Латентный дефицит железа у детей, этиология, патогенез, диагностика. ЖДА наиболее часто наблюдается в раннем возрасте с максимальной частотой у детей второго полугодия жизни и в подростковом периоде (частота между 30 и 40%), ей предшествует период латентного дефицита железа (ЛДЖ). ЛДЖ встречаются примерно в 1,5—2 раза чаще, чем железодефицитные анемии. Латентный дефицит железа - характеризуется дефицитом железа в тканевых депо и уменьшением транспортного его фонда, но без снижения гемоглобина и развития анемии. Предлатентная. Запасы снижаются, но эритропоэз еще в норме. Эритропоэзом называют образование эритроцитов при участии железа в костном мозге. Латентная. Истощение запасов в депо. Манифестная (железодефицитная). Снижение запасов в депо и нарушение окислительно-восстановительных процессов сопровождаемые симптомами анемии. Этиология: I. Низкие запасы железа при рождении. Группы риска: — недоношенные, особенно с очень низкой массой тела при рождении; -депо Fe меньше (↓ объем крови), -истощение запасов из-за интенсивного роста к 1-2 мес. -хуже поступление Fe, т.к. чаще искусств.вскарм., высокая заболеваемость, снижена абсорбция в кишечнике. — дети от матерей с железодефицитной анемией во время беременности, в том числе дети-«погодки», т. е. родившиеся через год после старшего ребенка; — дети с задержкой внутриутробного развития; — дети с кровопотерей в перинатальном периоде. II. Алиментарные факторы — ведущая причина железодефицитных состояний, приводящая к недостаточному поступлению в организм железа. Группы риска: — дети, с рождения находящиеся на искусственном вскармливании неадаптированными смесями, в частности без добавления железа; — позднее введение прикорма и использование при прикорме растительных продуктов; — преимущественно вегетарианская пища в любом возрасте; — избыток цельного молока в рационе ребенка (более 0,5 л в сутки); III. Избытогные потери или потребление железа. Группы риска: — острые и хронические инфекционные заболевания, особенно желудочно-кишечные; — хронические неинфекционные, воспалительные заболевания желудочно-кишечного тракта (как вследствие избыточных потерь, так и недостаточного поступления железа при синдромах тотальной или селективной мальабсорбции — целиакия, муковисцидоз, экссудативная энтеропатия, недостаточность дисахаридаз и др.); — кровопотери, как явные (мелена, эпистаксис, гематурия, метроррагии и др.), так и оккультные (например, при избытке в питании цельного коровьего молока, гельминтозах, кишечных инфекциях, опухолях и др.), чаще являются причиной анемий у детей старшего возраста; — ювенильные гормональные перестройки; — токсические факторы (хроническое отравление солями свинца, ртути и др.); — эссенциальные (идиопатические), при которых явную причину не обнаруживают и полагают, что имеет место детерминированный сдвиг градиента всасывания железа с проксимальных отделов двенадцатиперстной и тонкой кишки к дистальным ее отделам, что значительно снижает всасывание железа (эти формы обычно семейные). К 6-месячному возрасту и во втором полугодии жизни ребенку необходимо (при достаточных запасах железа при рождении) примерно 1 мг/кг железа, тогда как 1 литр женского молока обеспечивает поступление лишь 0,5-0,6 мг железа. Патогенез. Латентный дефицит железа в организме - вторая стадия железодефицитного состояния. Развивается на фоне "обеднения" тканевых запасов железа и характеризуется снижением содержания как депонированного железа, так и транспортного его пула. Постепенно, из-за дефицита железа, уменьшается активность Fe-содержащих энзимов. При этом скорость синтеза гемоглобина, его общее содержание и насыщение эритроцитов гемоглобином не изменены. Причиной дефицита железа является нарушение его баланса в сторону преобладания расходования железа над поступлением, наблюдаемое при различных физиологических состояниях или заболеваниях. Железо входит в состав гема — соединения, способного обратимо связывать кислород. В депониронировании железа в организме основное значение имеет ферритин и гемосидерин. Транспорт железа в организме осуществляет белок трансферрин. При отрицательном балансе обмена железа вначале расходуется железо из депо (латентный дефицит железа), затем возникает тканевый дефицит железа, проявляющийся нарушением ферментативной активности и дыхательной функции в тканях, и только позже развивается железодефицитная анемия. Диагностика. Предлатентный. Лабораторные показатели остаются в норме. Тест абсорбции железа в норме 10–15%, но в этом периоде он повышен и составляет 50%. Латентный. Лабораторные показатели, такие как сывороточное железо, ферритин и трансферрин снижаются, тогда как эритроциты, гемоглобин, гематокрит, эритроцитарные индексы находятся в норме. Эритроцитарные индексы снижаются. Отмечается микроцитоз, анизоцитоз (изменение в размерах эритроцитов), пойкилоцитоз (измененные эритроциты перестали выполнять свои функции). Уровень трансферрина (транспортного белка железа). Норма его у мужчин 2,1–3,6, мг/л, у женщин – 2,5–3,8 мг/л. Уровень ферритина. Белок индикатор острой фазы заболеваний воспалительных, онкологических обычно повышен при таких процессах, но при ЛДЖ он снижен. При начальном дефиците железа первые изменения происходят в тканях — уменьшаются тканевые запасы железа, что находит отражение в снижении уровня ферритина в сыворотке крови (при средних величинах около 35 нг/мл происходит снижение до 10 нг/мл и менее), далее снижается насыщение трансферрина железом (ниже 25%) и его окисление, но повышается общая железосвязывающая способность сыворотки (до 3500 мкг/л и более) и уровень свободных эритроцитарных протопорфиринов - предшественников гема (норма около 2 мкг/г НЬ или 350 мкг/л цельной крови). Все указанные изменения развиваются у ребенка еще до снижения уровня железа в сыворотке крови (ниже 11,6 мкмоль/л) и концентрации гемоглобина, объема эритроцитов, т. е. до развития анемии. Таким образом, при ЛДЖ, еще до развития анемии, должны развиваться клинические признаки тканевого дефицита железа, но эти признаки — неспецифические и их достаточно непросто уловить. Возрастные нормативные значения сывороточного железа составляют:
у новорожденных 5,0 - 19,3 мкмоль/л;
у детей в возрасте старше 1 мес 10,6 - 33,6 ммоль/л.
Общая железосвязывающая способность сыворотки (ОЖСС) -биохимический лабораторный показатель, характеризующий общее количество железа, которое может связаться с имеющимся в плазме трансферрином. Косвенно отражает кол-во трансферрина в плазме. Нормальные значения ОЖСС 40.6 - 62,5 мкмоль/л. Латентная железосвязывающая способность сыворотки (ЛЖСС) - производный показатель, отражащий математическую разницу между значениями общей железосвязывающей способности сыворотки (ОЖСС) и сывороточного железа (СЖ): ЛЖСС = ОЖСС - СЖ. ЛЖСС - косвенно отражает количество свободного трансферрина. В норме значения ЛЖСС не должны быть меньше 47 мкмоль/л. Коэффициент насыщения трансферрина (КНТ) - производный показатель, отражающий удельный вес сывороточного железа СЖ) от общей железосвязывающей способности сыворотки ОЖСС): КНТ = (СЖ: ОЖСС)-100% В норме значения коэффициента насыщения трансферрина не должны быть менее 17%.
78.Клиника
латентного дефицита железа, лечение и
профилактика.
Дефицит
железа, даже при
невыраженной анемии,
влияет
на неврологический статус,
психомоторное развитие и интеллект.
Многочисленные исследования показали
наличие взаимосвязи между дефицитом
железа и задержкой развития у детей
9—24 месяцев. Данные нарушения могут
выявляться длительно: у детей, перенесших
ЖДА в раннем возрасте, в школьном
возрасте ниже
способность к обучению.
Астеноневротигеский
синдром: повышенные
утомляемость,
возбудимость, раздражительность,
эмоциональная неустойчивость, потливость;
отставание в психомоторном развитии;
вялость, астения, апатия; снижение
аппетита; нарушение способности к
концентрации внимания; негативизм; у
более старших детей головные боли,
головокружения, шум в ушах, мелькание
«мушек» перед глазами, боли в сердце, а
также извращенный аппетит с поеданием
извести, мела, сырых картофеля и мяса,
в том числе геофагия (поедание земли,
глины), пагофагия (потребление избытка
льда, мороженого), извращение обоняния;
дизурические расстройства.
Эпителиальный
синдром — бледность
кожи (особенно ладоней, ногтевых лож),
слизистых оболочек (характерна бледность
конъюнктивы век) и ушных раковин; сухость
и шелушение кожи; дистрофические
изменения кожи, ногтей (койлонихии —
вогнутость ногтей), волос (исчерченность,
тусклость, повышенная ломкость, тонкость,
редкость и др.), слизистых рта, языка
(«заеды» в углах рта, ангулярный стоматит,
сглаженность сосочков, полированный
язык, покраснение языка, жжение языка,
атрофический глоссит); синева склер;
симптом Пламмера-Винсона - нарушение
глотания твердой пищи; гастрит; дуоденит,
энтеропатия с мальабсорбцией и
мальдигестией, неустойчивый стул;
тошнота; иногда цвет кожи алебастрово-зеленый
(хлороз).
Сердечно-сосудистый
синдром: тахикардия
(одышка бывает редко), тенденция
к артериальной гипотонии,
ослабление тонов сердца и расширение
границ относительной сердечной тупости,
функциональный систолический шум на
верхушке, иногда шумы над крупными
сосудами.
Мышечный
синдром - мышечная
гипотония, быстрая утомляемость, энурез
и неудержание мочи из-за слабости
сфинктеров, запор.
Синдром
вторичного иммунодефицита:
частые ОРВИ, пневмонии, кишечные инфекции,
усугубляющие дефицит железа. К редким
симптомам дефицита железа относится:
увеличение печени и селезенки,
отечность.
Снижение
аппетита (снижение
кислотности желудочного сока),
Извращение аппетита:
земля, мел, известка, глина, волосы,
шерсть, гудрон. Пагофагия: замороженная
пища, мороженное, Снижение
обоняния, пристрастия к неприятным
запахам (токсикомания). Койлонихии:
уплощение ногтевого ложа 2 и 3 пальцев,
деформация ногтевого ложа, Атрофия
сосочков языка, полированный язык,
ангулярный стоматит, «заеды»,
Снижение эмоционального
тонуса, безучастность, малоподвижность,
негативность, утрата интереса к
окружающим.
Лечение.
Очень важным является
выявление потенциальных
причин и провоцирующих факторов,
попытка активного влияния на них. Режим
детей должен быть активный с достаточным
пребыванием на свежем воздухе.
Хотя
диетотерапия важна при лечении
железодефицитных состояний, следует
помнить, что лишь диетой устранить
дефицит железа в организме невозможно
— необходимо
назначать препараты железа.
Терапия
железодефицитных состояний должна
проводиться преимущественно препаратами
железа для перорального приема.
Терапия
железодефицитной анемии
не должна прекращаться после нормализации
уровня гемоглобина. длительность
назначения железа в лечебной дозе должна
быть не
менее 3 месяцев,
ибо на первом этапе это купирующая
терапия, восполняющая уровень гемоглобина
и периферические запасы железа (обычно
около 1—1,5 месяцев); на втором этапе
необходимо восстановить тканевые запасы
железа и на третьем — осуществить
противорецидивные мероприятия;
Гемотрансфузии
при железодефицитной анемии должны
проводиться только строго по жизненным
показаниям. К
переливанию
эритроцитной массы
прибегают лишь по жизненным показаниям
при уровне гемоглобина менее 40 г/л (3
мл/кг). К переливанию цельной крови
прибегать не следует!
препараты
железа надо давать в промежутке между
едой и запивать их свежими фруктовыми
или овощными соками; одновременное
назначение с препаратами железа
аскорбиновой кислоты и витамина Е
увеличивает эффект лечения;
нет
необходимости одновременно с препаратами
железа назначать витамины В6 и В12,
фолиевую кислоту при отсутствии
специальных показаний;
показаниями
для парентерального назначения
препаратов железа являются: наличие
патологии кишечника с нарушенным
всасыванием (синдромы мальабсорбции,
энтериты, язвенно-некротический
энтероколит), непереносимость принимаемых
внутрь препаратов железа;
 суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в
кг х 0,4;
вводят препарат вначале в
дозе 25 мг и далее через каждые 3 дня по
50 мг; после окончания курса необходимо
назначить препараты железа внутрь.
Для
детей до 3-х лет —
3 мг/кг/сутки элементарного железа для
солевых препаратов железа; 5 мг/кг/сутки
элементарного железа — для препаратов
комплекса гидроксида железа III с
полимальтозой.
Для
детей старше 3-х лет
— 45-60 мг/сутки.
Для
подростков —
до 80-150 мг/сутки (до 200 мг/сутки в тяжелых
случаях) элементарного железа.
Длительность
основного курса лечения составляет
6-10 недель.
Продолжительность курса
препаратами железа для создания депо
составляет:
При анемии легкой степени
— 6-8 недель
При анемии средней степени
— 8-10 недель
При анемии тяжелой степени
— 10-12 недель
суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в
кг х 0,4;
вводят препарат вначале в
дозе 25 мг и далее через каждые 3 дня по
50 мг; после окончания курса необходимо
назначить препараты железа внутрь.
Для
детей до 3-х лет —
3 мг/кг/сутки элементарного железа для
солевых препаратов железа; 5 мг/кг/сутки
элементарного железа — для препаратов
комплекса гидроксида железа III с
полимальтозой.
Для
детей старше 3-х лет
— 45-60 мг/сутки.
Для
подростков —
до 80-150 мг/сутки (до 200 мг/сутки в тяжелых
случаях) элементарного железа.
Длительность
основного курса лечения составляет
6-10 недель.
Продолжительность курса
препаратами железа для создания депо
составляет:
При анемии легкой степени
— 6-8 недель
При анемии средней степени
— 8-10 недель
При анемии тяжелой степени
— 10-12 недель
 Профилактика.
железодефицитных
состояний у детей раннего возраста
должна начинаться с предупреждения
его недостатка у женщин репродуктивного
возраста и
назначения всем
матерям на протяжении второй половины
беременности и в период лактации
препаратов железа,
например гемостимулина
по 1,0 г в сутки,
или другого препарата. Учитывая сказанное
выше, показано назначение всем доношенным
детям на естественном вскармливании
начиная с 3 месяцев одного
из препаратов железа
(орферон, сироп алоэ с железом или
какой-либо другой препарат) из расчета
по элементарному железу 1 мг/кг.
Недоношенным детям
суточную профилактическую дозу
препарата увеличивают до 2 мг/кг и
начинают давать с
месячного возраста,
а у детей с очень низкой массой при
рождении даже
раньше - с 3 недель. Естественное
вскармливание, рациональное расширение
питания и введение прикормов в
декретированные сроки, прогулки, массаж
и гимнастика, профилактика рахита —
существенные звенья профилактики
железодефицитных состояний. В настоящее
время рекомендуется
пользоваться кашами для детского питания
с добавлением препаратов железа.
Наконец, адаптированные смеси для
питания детей содержат добавки железа,
и если ребенок их получает, то нет
необходимости в дополнительном назначении
препаратов железа для профилактики его
дефицита.
79.
Дефицитные анемии у детей.
Классификация.
Классификация
дефицитных анемий (В.И. Калиничева,
1978):
I. Алиментарные
анемии:
А.
Дефицитные анемии:
1.
Пандефицитные (анемии при алиментарной
дистрофии).
2.
Преимущественно минералодефицитные
анемии (железодефицитная
анемия, анемия при дефиците меди,
кобальта, марганца, цинка).
3.
Преимущественно белководефицитные
(анемия при квашиоркоре, при одностороннем
мучном вскармливании).
4. Преимущественно
витаминодефицитные
анемии (анемии при
дефиците витаминов В2, РР, В6, фолиевой
кислоты и витамина В12: при длительном
вскармливании козьим молоком, анемия
типа Zuelzer-Ogden; анемия типа Gerbasi).
Б.
Анемии, вызванные
мальабсорбцией:
1.
Анемия при целиакии.
2. Анемия при
муковисцидозе.
3. Анемия при синдроме
Imerslund-Grasbeck.
II.Анемии,
связанные с потерей организмом
гемопоэтических веществ:
1.
Анемии постгеморрагические (острые и
хронические).
2. Анемии при экссудативных
энтеропатиях.
3. Анемия при широком
лентеце.
I степень — 90-110 г/л,
эритроциты 3*1012/л
II степень — 70-90 г/л,
эритроциты 2,5 *1012/л
III степень — меньше
70 г/л, эритроциты меньше 2,5*1012/л
Регенераторные
р>5‰
Гиперрегенераторная
р>50‰
Гипорегенераторная р снижено,
не адекватно степени тяжести.
80.Этиология,
патогенез, клиника, классификация,
диагностика железодефицитной
анемии.
Железодефицитная
анемия — крайний
вариант проявления дефицита железа,
лабораторно характеризуется: уменьшением
концентрации гемоглобина в единице
объема крови и в одном (каждом) эритроците;
микроцитозом, анизоцитозом, пойкилоцитозом
эритроцитов; низким
цветовым показателем;
низким содержанием
железа и ферритина сыворотки крови;
низким насыщением
трансферрина
железом;
увеличением
железосвязывающей способности сыворотки
и эритроцитарного протопорфирина.
Анемии
— группа заболеваний, характеризующихся
уменьшением гемоглобина и (или) количества
циркулирующих эритроцитов в единице
объема крови ниже нормального для
данного возраста и пола.
Этиология.
I. Низкие
запасы железа при рождении.
Группы риска:
— недоношенные,
особенно с очень низкой массой тела
при рождении; -депо Fe меньше (↓ объем
крови), -истощение запасов из-за
интенсивного роста к 1-2 мес. -хуже
поступление Fe, т.к. чаще искусств.вскарм.,
высокая заболеваемость, снижена абсорбция
в кишечнике.
— дети от матерей
с железодефицитной анемией во
время беременности, в том числе
дети-«погодки»,
т. е. родившиеся через год после старшего
ребенка;
— дети с задержкой
внутриутробного развития;
— дети
с кровопотерей в
перинатальном периоде.
II. Алиментарные
факторы — ведущая
причина железодефицитных состояний,
приводящая к недостаточному поступлению
в организм железа. Группы риска:
—
дети, с рождения находящиеся на
искусственном
вскармливании неадаптированными
смесями, в частности
без добавления железа;
— позднее
введение прикорма и
использование при прикорме растительных
продуктов;
— преимущественно
вегетарианская пища в любом возрасте;
— избыток
цельного молока в
рационе ребенка (более 0,5 л в сутки);
III.
Избытогные потери
или потребление железа.
Группы риска:
— острые и хронические
инфекционные заболевания,
особенно желудочно-кишечные;
—
хронические неинфекционные,
воспалительные заболевания
желудочно-кишечного
тракта (как вследствие избыточных
потерь, так и недостаточного поступления
железа при синдромах тотальной или
селективной мальабсорбции — целиакия,
муковисцидоз, экссудативная энтеропатия,
недостаточность дисахаридаз и др.);
—
кровопотери,
как явные (мелена, эпистаксис, гематурия,
метроррагии и др.), так и оккультные
(например, при избытке в питании цельного
коровьего молока, гельминтозах,
кишечных инфекциях,
опухолях и др.), чаще являются причиной
анемий у детей старшего возраста;
—
ювенильные гормональные
перестройки;
—
токсические
факторы (хроническое
отравление солями свинца, ртути и др.);
— эссенциальные (идиопатические),
при которых явную причину не обнаруживают
и полагают, что имеет место детерминированный
сдвиг градиента всасывания железа с
проксимальных отделов двенадцатиперстной
и тонкой кишки к дистальным ее отделам,
что значительно снижает всасывание
железа (эти формы обычно семейные).
Патогенез.
Экзогенный
или эндогенный дефицит железа в организме
характеризуется уменьшением
и постепенным истощением
резервов железа,
что проявляется исчезновением
гемосидерина(при
разрушении гемоглобина) в макрофагоцитах
печени и селезенки, снижением
до 2—5% в костном
мозге количества сидеробластов
(клетки, содержащие
железо в виде гранул ферритина; их число
в норме — 20—40%). В крови понижается
концентрация сывороточного железа (ги
п о си де р е м и я достигает 1,8— 2,7 мкм/л
вместо 12,5 — 30,4 мкм/л в норме) и степень
насыщения им трансферрина, что приводит
к уменьшению
транспорта железа в костный мозг.
Нарушается включение железа в
эритроцитарные клетки, снижается
синтез гема в гемоглобине
и некоторых железосодержащих и
железозависимых ферментов (каталазы,
глутатионпероксидазы) в эритроцитах,
что повышает их
чувствительность к гемолизирующему
действию
окислителей.
Увеличивается неэффективный
эритропоэз вследствие возросшего
гемолиза эритрокариоцитов
в костном мозге и эритроцитов в крови.
Продолжительность
жизни эритроцитов уменьшается.
В
организме при железодефицитной анемии
возникают компенсаторные
реакции — усиление
абсорбции железа в пищевом канале,
повышение
концентрации трансферрина,
гиперплазия эритроцитарного ростка,
увеличение
интенсивности гликолиза и активности
2,3-дифосфоглицерата в эритроцитах,
способствующее лучшей
отдаче кислорода тканям.
Однако эти реакции оказываются
недостаточными, чтобы восполнить дефицит
железа в организме и улучшить
кислородтранспортную функцию крови
при уменьшении общего количества
эритроцитов и содержания в них гемоглобина.
Возникают морфологические
изменения в эритроцитарных клетках
костного мозга:
гипохромия,
связанная с недостаточной гемоглобинизацией,
преобладание базофильных нормобластов
над ацидофильными в костном мозге,
микроцитоз,
деструкция ядерных клеток (нарушение
митоза, кариорексис, вакуолизация
цитоплазмы эритробластов и
нормобластов).
Наряду с патологическими
изменениями эритропоэза дефицит железа
в организме приводит к уменьшению
миоглобина и активности железосодержащих
ферментов
тканевого дыхания.
Следствием гемической и тканевой
гипоксии при железодефицитной анемии
являются атрофические
и дистрофические процессы
в тканях и органах, особенно выраженные
в пищевом канале (глоссит, гингивит,
кариес зубов, поражение слизистой
оболочки пищевода, атрофический гастрит
с ахилией) и сердце (дистрофия
миокарда).
Клиника.
Падение
уровня Hb ниже возрастной нормы.
Снижение
содержания ферритина сыворотки менее
12 мкг/л.
Повышение
уровня железотрансферрина
свыше 7 мг/л.
Снижение уровня Hb.
Снижение
цветового показателя < 0,85 или увеличение
RDW > 15%.
Снижение содержания Hb
в эритроците MCH<
25 пиктограмм. (27-32
пг/эритроцит)
Уменьшение объема
эритроцитов MCV<
75 фемолитров. (75-100
фл)
Уменьшение средней
концентрации Hb в эритроците
MCHC < 30г/л (32-36%)
Астеноневротигеский
синдром: повышенные
утомляемость, возбудимость,
раздражительность, эмоциональная
неустойчивость, потливость; отставание
в психомоторном развитии; вялость,
астения, апатия; снижение аппетита;
нарушение способности к концентрации
внимания; негативизм; у более старших
детей головные боли, головокружения,
шум в ушах, мелькание «мушек» перед
глазами, боли в сердце, а также извращенный
аппетит с поеданием извести, мела, сырых
картофеля и мяса, в том числе геофагия
(поедание земли, глины), пагофагия
(потребление избытка льда, мороженого),
извращение обоняния; дизурические
расстройства.
Эпителиальный
синдром — бледность
кожи (особенно ладоней, ногтевых лож),
слизистых оболочек (характерна бледность
конъюнктивы век) и ушных раковин; сухость
и шелушение кожи; дистрофические
изменения кожи, ногтей (койлонихии —
вогнутость ногтей), волос (исчерченность,
тусклость, повышенная ломкость, тонкость,
редкость и др.), слизистых рта, языка
(«заеды» в углах рта, ангулярный стоматит,
сглаженность сосочков, полированный
язык, покраснение языка, жжение языка,
атрофический глоссит); синева склер;
симптом Пламмера-Винсона - нарушение
глотания твердой пищи; гастрит; дуоденит,
энтеропатия с мальабсорбцией и
мальдигестией, неустойчивый стул;
тошнота; иногда цвет кожи алебастрово-зеленый
(хлороз).
Сердечно-сосудистый
синдром: тахикардия
(одышка бывает
редко), тенденция
к артериальной гипотонии,
ослабление тонов сердца и расширение
границ относительной сердечной тупости,
функциональный систолический шум на
верхушке, иногда шумы над крупными
сосудами.
Мышечный
синдром - мышечная
гипотония, быстрая утомляемость, энурез
и неудержание мочи из-за слабости
сфинктеров, запор.
Синдром
вторичного иммунодефицита:
частые ОРВИ, пневмонии, кишечные
инфекции,
усугубляющие дефицит железа. К редким
симптомам дефицита железа относится:
увеличение печени и селезенки,
отечность.
Снижение
аппетита (снижение
кислотности желудочного сока),
Извращение аппетита:
земля, мел, известка, глина, волосы,
шерсть, гудрон. Пагофагия: замороженная
пища, мороженное, Снижение
обоняния, пристрастия к неприятным
запахам (токсикомания). Койлонихии:
уплощение ногтевого ложа 2 и 3 пальцев,
деформация ногтевого ложа, Атрофия
сосочков языка, полированный язык,
ангулярный стоматит, «заеды»,
Снижение эмоционального
тонуса, безучастность, малоподвижность,
негативность, утрата интереса к
окружающим.
Классификация.
По
стадиям:
I
стадия – потеря
железа превышает его поступление,
постепенное истощение запасов, всасывание
в кишечнике компенсаторно увеличивается;
II
стадия – истощение
запасов железа (уровень
сывороточного железа – ниже
50 мкг/л,
насыщение трансферрина – ниже
16%)
препятствует нормальному эритропоэзу,
эритропоэз начинает падать;
III
стадия – развитие
анемии легкой степени (100–120
г/л гемоглобина, компенсированной), с
незначительным снижением цветового
показателя и других индексов насыщения
эритроцитов гемоглобином;
IV
стадия – выраженная (менее 100 г/л
гемоглобина, субкомпенсированная)
анемия с явным снижением насыщения
эритроцитов гемоглобином;
V
стадия – тяжелая анемия (60–80 г/л
гемоглобина) с циркуляторными нарушениями
и тканевой гипоксией.
По
степени тяжести:
•
легкая (содержание Нb – 90–120 г/л);
•
средняя (70–90 г/л);
•
тяжелая (менее 70 г/л).
81.Лечение и
профилактика железодефицитной
анемии.
Цель
терапии железодефицитных состояний —
устранение дефицита железа и восстановление
его запасов в организме.
Хотя
диетотерапия важна при лечении
железодефицитных состояний, следует
помнить, что лишь диетой устранить
дефицит железа в организме невозможно
— необходимо назначать препараты
железа.
Общими
принципами назнагения препаратов железа
в педиатрии являются:
• преимущественное назначение
препаратов внутрь
и редкость парентерального из-за
побочных эффектов (аллергические
реакции, постинъекционные абсцессы и
флебиты, гипотензия, увеличение риска
бактериальных инфекций вплоть до
сепсиса, гемосидероз и др.);
• препараты
закислого (двухвалентного)
железа лучше всасываются,
чем окислого (трехвалентного), а потому
их давать предпочтительнее;
•
суточная
доза должна составлять по элементарному
железу 5-6 мг/кг; большие
дозы не увеличивают эффективность
лечения, но дают больше побочных эффектов
(расстройства функции желудочно-кишечного
тракта, вплоть до изъязвлений, стенозов,
непроходимости; увеличение риска
кишечных инфекций), суточную дозу
препарата делят на 3 приема;
• в
первые несколько дней лечения для
установления переносимости препарата
доза может быть вдвое меньшей;
•
длительность назначения железа в
лечебной дозе должна быть не менее 3
месяцев, ибо на первом этапе это купирующая
терапия, восполняющая уровень гемоглобина
и периферические запасы железа (обычно
около 1—1,5 месяцев); на втором этапе
необходимо восстановить тканевые запасы
железа и на третьем — осуществить
противорецидивные мероприятия;
•
препараты железа надо давать в промежутке
между едой и запивать их свежими
фруктовыми или овощными соками; • нельзя
запивать препараты железа молоком;
•
одновременное
назначение с препаратами железа
аскорбиновой кислоты и
витамина Е увеличивает эффект лечения;
• нет необходимости одновременно
с препаратами железа назначать витамины
В6 и В12, фолиевую кислоту при отсутствии
специальных показаний;
• показаниями
для парентерального
назначения
препаратов железа являются: наличие
патологии кишечника с нарушенным
всасыванием (синдромы мальабсорбции,
энтериты, язвенно-некротический
энтероколит), непереносимость принимаемых
внутрь препаратов железа; суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в кг
х 0,4; вводят препарат вначале в дозе 25
мг и далее через каждые 3 дня по 50 мг;
после окончания курса необходимо
назначить препараты железа внутрь.
Ожидаемые
результаты применения препаратов
железа: через 72—96
ч — увеличение ретикулоцитоза и через
7-10 дней (лаг-период) - повышение уровня
гемоглобина (хороший результат примерно
5 г/л в неделю). После нормализации уровня
гемоглобина лечение препаратами железа
надо продолжать еще 4- 6 недель для
восстановления тканевых депо железа.
Во время лечения препаратами железа
определение его уровня в сыворотке
неинформативно.
К переливанию
эритроцитной массы
прибегают лишь по жизненным показаниям
при уровне гемоглобина менее 40 г/л (3
мл/кг). К переливанию цельной крови
прибегать не следует!
суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в
кг х 0,4;
вводят препарат вначале в
дозе 25 мг и далее через каждые 3 дня по
50 мг; после окончания курса необходимо
назначить препараты железа внутрь.
Для
детей до 3-х лет —
3 мг/кг/сутки элементарного железа для
солевых препаратов железа; 5 мг/кг/сутки
элементарного железа — для препаратов
комплекса гидроксида железа III с
полимальтозой.
Для
детей старше 3-х лет
— 45-60 мг/сутки.
Для
подростков —
до 80-150 мг/сутки (до 200 мг/сутки в тяжелых
случаях) элементарного железа.
Длительность
основного курса лечения составляет
6-10 недель.
Продолжительность курса
препаратами железа для создания депо
составляет:
При анемии легкой степени
— 6-8 недель
При анемии средней степени
— 8-10 недель
При анемии тяжелой степени
— 10-12 недель
Профилактика.
железодефицитных
состояний у детей раннего возраста
должна начинаться с предупреждения
его недостатка у женщин репродуктивного
возраста и
назначения всем
матерям на протяжении второй половины
беременности и в период лактации
препаратов железа,
например гемостимулина
по 1,0 г в сутки,
или другого препарата. Учитывая сказанное
выше, показано назначение всем доношенным
детям на естественном вскармливании
начиная с 3 месяцев одного
из препаратов железа
(орферон, сироп алоэ с железом или
какой-либо другой препарат) из расчета
по элементарному железу 1 мг/кг.
Недоношенным детям
суточную профилактическую дозу
препарата увеличивают до 2 мг/кг и
начинают давать с
месячного возраста,
а у детей с очень низкой массой при
рождении даже
раньше - с 3 недель. Естественное
вскармливание, рациональное расширение
питания и введение прикормов в
декретированные сроки, прогулки, массаж
и гимнастика, профилактика рахита —
существенные звенья профилактики
железодефицитных состояний. В настоящее
время рекомендуется
пользоваться кашами для детского питания
с добавлением препаратов железа.
Наконец, адаптированные смеси для
питания детей содержат добавки железа,
и если ребенок их получает, то нет
необходимости в дополнительном назначении
препаратов железа для профилактики его
дефицита.
79.
Дефицитные анемии у детей.
Классификация.
Классификация
дефицитных анемий (В.И. Калиничева,
1978):
I. Алиментарные
анемии:
А.
Дефицитные анемии:
1.
Пандефицитные (анемии при алиментарной
дистрофии).
2.
Преимущественно минералодефицитные
анемии (железодефицитная
анемия, анемия при дефиците меди,
кобальта, марганца, цинка).
3.
Преимущественно белководефицитные
(анемия при квашиоркоре, при одностороннем
мучном вскармливании).
4. Преимущественно
витаминодефицитные
анемии (анемии при
дефиците витаминов В2, РР, В6, фолиевой
кислоты и витамина В12: при длительном
вскармливании козьим молоком, анемия
типа Zuelzer-Ogden; анемия типа Gerbasi).
Б.
Анемии, вызванные
мальабсорбцией:
1.
Анемия при целиакии.
2. Анемия при
муковисцидозе.
3. Анемия при синдроме
Imerslund-Grasbeck.
II.Анемии,
связанные с потерей организмом
гемопоэтических веществ:
1.
Анемии постгеморрагические (острые и
хронические).
2. Анемии при экссудативных
энтеропатиях.
3. Анемия при широком
лентеце.
I степень — 90-110 г/л,
эритроциты 3*1012/л
II степень — 70-90 г/л,
эритроциты 2,5 *1012/л
III степень — меньше
70 г/л, эритроциты меньше 2,5*1012/л
Регенераторные
р>5‰
Гиперрегенераторная
р>50‰
Гипорегенераторная р снижено,
не адекватно степени тяжести.
80.Этиология,
патогенез, клиника, классификация,
диагностика железодефицитной
анемии.
Железодефицитная
анемия — крайний
вариант проявления дефицита железа,
лабораторно характеризуется: уменьшением
концентрации гемоглобина в единице
объема крови и в одном (каждом) эритроците;
микроцитозом, анизоцитозом, пойкилоцитозом
эритроцитов; низким
цветовым показателем;
низким содержанием
железа и ферритина сыворотки крови;
низким насыщением
трансферрина
железом;
увеличением
железосвязывающей способности сыворотки
и эритроцитарного протопорфирина.
Анемии
— группа заболеваний, характеризующихся
уменьшением гемоглобина и (или) количества
циркулирующих эритроцитов в единице
объема крови ниже нормального для
данного возраста и пола.
Этиология.
I. Низкие
запасы железа при рождении.
Группы риска:
— недоношенные,
особенно с очень низкой массой тела
при рождении; -депо Fe меньше (↓ объем
крови), -истощение запасов из-за
интенсивного роста к 1-2 мес. -хуже
поступление Fe, т.к. чаще искусств.вскарм.,
высокая заболеваемость, снижена абсорбция
в кишечнике.
— дети от матерей
с железодефицитной анемией во
время беременности, в том числе
дети-«погодки»,
т. е. родившиеся через год после старшего
ребенка;
— дети с задержкой
внутриутробного развития;
— дети
с кровопотерей в
перинатальном периоде.
II. Алиментарные
факторы — ведущая
причина железодефицитных состояний,
приводящая к недостаточному поступлению
в организм железа. Группы риска:
—
дети, с рождения находящиеся на
искусственном
вскармливании неадаптированными
смесями, в частности
без добавления железа;
— позднее
введение прикорма и
использование при прикорме растительных
продуктов;
— преимущественно
вегетарианская пища в любом возрасте;
— избыток
цельного молока в
рационе ребенка (более 0,5 л в сутки);
III.
Избытогные потери
или потребление железа.
Группы риска:
— острые и хронические
инфекционные заболевания,
особенно желудочно-кишечные;
—
хронические неинфекционные,
воспалительные заболевания
желудочно-кишечного
тракта (как вследствие избыточных
потерь, так и недостаточного поступления
железа при синдромах тотальной или
селективной мальабсорбции — целиакия,
муковисцидоз, экссудативная энтеропатия,
недостаточность дисахаридаз и др.);
—
кровопотери,
как явные (мелена, эпистаксис, гематурия,
метроррагии и др.), так и оккультные
(например, при избытке в питании цельного
коровьего молока, гельминтозах,
кишечных инфекциях,
опухолях и др.), чаще являются причиной
анемий у детей старшего возраста;
—
ювенильные гормональные
перестройки;
—
токсические
факторы (хроническое
отравление солями свинца, ртути и др.);
— эссенциальные (идиопатические),
при которых явную причину не обнаруживают
и полагают, что имеет место детерминированный
сдвиг градиента всасывания железа с
проксимальных отделов двенадцатиперстной
и тонкой кишки к дистальным ее отделам,
что значительно снижает всасывание
железа (эти формы обычно семейные).
Патогенез.
Экзогенный
или эндогенный дефицит железа в организме
характеризуется уменьшением
и постепенным истощением
резервов железа,
что проявляется исчезновением
гемосидерина(при
разрушении гемоглобина) в макрофагоцитах
печени и селезенки, снижением
до 2—5% в костном
мозге количества сидеробластов
(клетки, содержащие
железо в виде гранул ферритина; их число
в норме — 20—40%). В крови понижается
концентрация сывороточного железа (ги
п о си де р е м и я достигает 1,8— 2,7 мкм/л
вместо 12,5 — 30,4 мкм/л в норме) и степень
насыщения им трансферрина, что приводит
к уменьшению
транспорта железа в костный мозг.
Нарушается включение железа в
эритроцитарные клетки, снижается
синтез гема в гемоглобине
и некоторых железосодержащих и
железозависимых ферментов (каталазы,
глутатионпероксидазы) в эритроцитах,
что повышает их
чувствительность к гемолизирующему
действию
окислителей.
Увеличивается неэффективный
эритропоэз вследствие возросшего
гемолиза эритрокариоцитов
в костном мозге и эритроцитов в крови.
Продолжительность
жизни эритроцитов уменьшается.
В
организме при железодефицитной анемии
возникают компенсаторные
реакции — усиление
абсорбции железа в пищевом канале,
повышение
концентрации трансферрина,
гиперплазия эритроцитарного ростка,
увеличение
интенсивности гликолиза и активности
2,3-дифосфоглицерата в эритроцитах,
способствующее лучшей
отдаче кислорода тканям.
Однако эти реакции оказываются
недостаточными, чтобы восполнить дефицит
железа в организме и улучшить
кислородтранспортную функцию крови
при уменьшении общего количества
эритроцитов и содержания в них гемоглобина.
Возникают морфологические
изменения в эритроцитарных клетках
костного мозга:
гипохромия,
связанная с недостаточной гемоглобинизацией,
преобладание базофильных нормобластов
над ацидофильными в костном мозге,
микроцитоз,
деструкция ядерных клеток (нарушение
митоза, кариорексис, вакуолизация
цитоплазмы эритробластов и
нормобластов).
Наряду с патологическими
изменениями эритропоэза дефицит железа
в организме приводит к уменьшению
миоглобина и активности железосодержащих
ферментов
тканевого дыхания.
Следствием гемической и тканевой
гипоксии при железодефицитной анемии
являются атрофические
и дистрофические процессы
в тканях и органах, особенно выраженные
в пищевом канале (глоссит, гингивит,
кариес зубов, поражение слизистой
оболочки пищевода, атрофический гастрит
с ахилией) и сердце (дистрофия
миокарда).
Клиника.
Падение
уровня Hb ниже возрастной нормы.
Снижение
содержания ферритина сыворотки менее
12 мкг/л.
Повышение
уровня железотрансферрина
свыше 7 мг/л.
Снижение уровня Hb.
Снижение
цветового показателя < 0,85 или увеличение
RDW > 15%.
Снижение содержания Hb
в эритроците MCH<
25 пиктограмм. (27-32
пг/эритроцит)
Уменьшение объема
эритроцитов MCV<
75 фемолитров. (75-100
фл)
Уменьшение средней
концентрации Hb в эритроците
MCHC < 30г/л (32-36%)
Астеноневротигеский
синдром: повышенные
утомляемость, возбудимость,
раздражительность, эмоциональная
неустойчивость, потливость; отставание
в психомоторном развитии; вялость,
астения, апатия; снижение аппетита;
нарушение способности к концентрации
внимания; негативизм; у более старших
детей головные боли, головокружения,
шум в ушах, мелькание «мушек» перед
глазами, боли в сердце, а также извращенный
аппетит с поеданием извести, мела, сырых
картофеля и мяса, в том числе геофагия
(поедание земли, глины), пагофагия
(потребление избытка льда, мороженого),
извращение обоняния; дизурические
расстройства.
Эпителиальный
синдром — бледность
кожи (особенно ладоней, ногтевых лож),
слизистых оболочек (характерна бледность
конъюнктивы век) и ушных раковин; сухость
и шелушение кожи; дистрофические
изменения кожи, ногтей (койлонихии —
вогнутость ногтей), волос (исчерченность,
тусклость, повышенная ломкость, тонкость,
редкость и др.), слизистых рта, языка
(«заеды» в углах рта, ангулярный стоматит,
сглаженность сосочков, полированный
язык, покраснение языка, жжение языка,
атрофический глоссит); синева склер;
симптом Пламмера-Винсона - нарушение
глотания твердой пищи; гастрит; дуоденит,
энтеропатия с мальабсорбцией и
мальдигестией, неустойчивый стул;
тошнота; иногда цвет кожи алебастрово-зеленый
(хлороз).
Сердечно-сосудистый
синдром: тахикардия
(одышка бывает
редко), тенденция
к артериальной гипотонии,
ослабление тонов сердца и расширение
границ относительной сердечной тупости,
функциональный систолический шум на
верхушке, иногда шумы над крупными
сосудами.
Мышечный
синдром - мышечная
гипотония, быстрая утомляемость, энурез
и неудержание мочи из-за слабости
сфинктеров, запор.
Синдром
вторичного иммунодефицита:
частые ОРВИ, пневмонии, кишечные
инфекции,
усугубляющие дефицит железа. К редким
симптомам дефицита железа относится:
увеличение печени и селезенки,
отечность.
Снижение
аппетита (снижение
кислотности желудочного сока),
Извращение аппетита:
земля, мел, известка, глина, волосы,
шерсть, гудрон. Пагофагия: замороженная
пища, мороженное, Снижение
обоняния, пристрастия к неприятным
запахам (токсикомания). Койлонихии:
уплощение ногтевого ложа 2 и 3 пальцев,
деформация ногтевого ложа, Атрофия
сосочков языка, полированный язык,
ангулярный стоматит, «заеды»,
Снижение эмоционального
тонуса, безучастность, малоподвижность,
негативность, утрата интереса к
окружающим.
Классификация.
По
стадиям:
I
стадия – потеря
железа превышает его поступление,
постепенное истощение запасов, всасывание
в кишечнике компенсаторно увеличивается;
II
стадия – истощение
запасов железа (уровень
сывороточного железа – ниже
50 мкг/л,
насыщение трансферрина – ниже
16%)
препятствует нормальному эритропоэзу,
эритропоэз начинает падать;
III
стадия – развитие
анемии легкой степени (100–120
г/л гемоглобина, компенсированной), с
незначительным снижением цветового
показателя и других индексов насыщения
эритроцитов гемоглобином;
IV
стадия – выраженная (менее 100 г/л
гемоглобина, субкомпенсированная)
анемия с явным снижением насыщения
эритроцитов гемоглобином;
V
стадия – тяжелая анемия (60–80 г/л
гемоглобина) с циркуляторными нарушениями
и тканевой гипоксией.
По
степени тяжести:
•
легкая (содержание Нb – 90–120 г/л);
•
средняя (70–90 г/л);
•
тяжелая (менее 70 г/л).
81.Лечение и
профилактика железодефицитной
анемии.
Цель
терапии железодефицитных состояний —
устранение дефицита железа и восстановление
его запасов в организме.
Хотя
диетотерапия важна при лечении
железодефицитных состояний, следует
помнить, что лишь диетой устранить
дефицит железа в организме невозможно
— необходимо назначать препараты
железа.
Общими
принципами назнагения препаратов железа
в педиатрии являются:
• преимущественное назначение
препаратов внутрь
и редкость парентерального из-за
побочных эффектов (аллергические
реакции, постинъекционные абсцессы и
флебиты, гипотензия, увеличение риска
бактериальных инфекций вплоть до
сепсиса, гемосидероз и др.);
• препараты
закислого (двухвалентного)
железа лучше всасываются,
чем окислого (трехвалентного), а потому
их давать предпочтительнее;
•
суточная
доза должна составлять по элементарному
железу 5-6 мг/кг; большие
дозы не увеличивают эффективность
лечения, но дают больше побочных эффектов
(расстройства функции желудочно-кишечного
тракта, вплоть до изъязвлений, стенозов,
непроходимости; увеличение риска
кишечных инфекций), суточную дозу
препарата делят на 3 приема;
• в
первые несколько дней лечения для
установления переносимости препарата
доза может быть вдвое меньшей;
•
длительность назначения железа в
лечебной дозе должна быть не менее 3
месяцев, ибо на первом этапе это купирующая
терапия, восполняющая уровень гемоглобина
и периферические запасы железа (обычно
около 1—1,5 месяцев); на втором этапе
необходимо восстановить тканевые запасы
железа и на третьем — осуществить
противорецидивные мероприятия;
•
препараты железа надо давать в промежутке
между едой и запивать их свежими
фруктовыми или овощными соками; • нельзя
запивать препараты железа молоком;
•
одновременное
назначение с препаратами железа
аскорбиновой кислоты и
витамина Е увеличивает эффект лечения;
• нет необходимости одновременно
с препаратами железа назначать витамины
В6 и В12, фолиевую кислоту при отсутствии
специальных показаний;
• показаниями
для парентерального
назначения
препаратов железа являются: наличие
патологии кишечника с нарушенным
всасыванием (синдромы мальабсорбции,
энтериты, язвенно-некротический
энтероколит), непереносимость принимаемых
внутрь препаратов железа; суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в кг
х 0,4; вводят препарат вначале в дозе 25
мг и далее через каждые 3 дня по 50 мг;
после окончания курса необходимо
назначить препараты железа внутрь.
Ожидаемые
результаты применения препаратов
железа: через 72—96
ч — увеличение ретикулоцитоза и через
7-10 дней (лаг-период) - повышение уровня
гемоглобина (хороший результат примерно
5 г/л в неделю). После нормализации уровня
гемоглобина лечение препаратами железа
надо продолжать еще 4- 6 недель для
восстановления тканевых депо железа.
Во время лечения препаратами железа
определение его уровня в сыворотке
неинформативно.
К переливанию
эритроцитной массы
прибегают лишь по жизненным показаниям
при уровне гемоглобина менее 40 г/л (3
мл/кг). К переливанию цельной крови
прибегать не следует!
суммарная
доза препаратов железа для парентерального
введения на курс лечения (в мг) равна
(120 - НЬ больного в г/л) х масса тела в
кг х 0,4;
вводят препарат вначале в
дозе 25 мг и далее через каждые 3 дня по
50 мг; после окончания курса необходимо
назначить препараты железа внутрь.
Для
детей до 3-х лет —
3 мг/кг/сутки элементарного железа для
солевых препаратов железа; 5 мг/кг/сутки
элементарного железа — для препаратов
комплекса гидроксида железа III с
полимальтозой.
Для
детей старше 3-х лет
— 45-60 мг/сутки.
Для
подростков —
до 80-150 мг/сутки (до 200 мг/сутки в тяжелых
случаях) элементарного железа.
Длительность
основного курса лечения составляет
6-10 недель.
Продолжительность курса
препаратами железа для создания депо
составляет:
При анемии легкой степени
— 6-8 недель
При анемии средней степени
— 8-10 недель
При анемии тяжелой степени
— 10-12 недель
 Профилактика.
железодефицитных
состояний у детей раннего возраста
должна начинаться с предупреждения
его недостатка у женщин репродуктивного
возраста и
назначения всем
матерям на протяжении второй половины
беременности и в период лактации
препаратов железа,
например гемостимулина
по 1,0 г в сутки,
или другого препарата. Учитывая сказанное
выше, показано назначение всем доношенным
детям на естественном вскармливании
начиная с 3 месяцев одного
из препаратов железа
(орферон, сироп алоэ с железом или
какой-либо другой препарат) из расчета
по элементарному железу 1 мг/кг.
Недоношенным детям
суточную профилактическую дозу
препарата увеличивают до 2 мг/кг и
начинают давать с
месячного возраста,
а у детей с очень низкой массой при
рождении даже
раньше - с 3 недель. Естественное
вскармливание, рациональное расширение
питания и введение прикормов в
декретированные сроки, прогулки, массаж
и гимнастика, профилактика рахита —
существенные звенья профилактики
железодефицитных состояний. В настоящее
время рекомендуется
пользоваться кашами для детского питания
с добавлением препаратов железа.
Наконец, адаптированные смеси для
питания детей содержат добавки железа,
и если ребенок их получает, то нет
необходимости в дополнительном назначении
препаратов железа для профилактики его
дефицита.
82.Бронхиты
у детей: простой и обструктивный.
Этиология, патогенез, клиника,
дифференциальный диагноз, лечение.
Бронхит
— воспалительное заболевание бронхов
различной этиологии (инфекционной,
аллергической, физико-химической и
др.).
Выделяют следующие формы бронхитов
у детей:
• острый простой бронхит
(ОПБ);
• острый обструктивный бронхит
(ООБ);
• острый бронхиолит;
•
рецидивирующий бронхит (РБ);
•
рецидивирующий обструктивный бронхит
(РОБ);
• хронический бронхит (ХБ) —
первичный и вторичный;
• хронический
бронхиолит с облитерацией.
ОСТРЫЙ
ПРОСТОЙ БРОНХИТ
- бронхит, протекающий без
признаков обструкции бронхов.
Этиология.
Этиологическими факторами ОПБ являются
вирусы
(парагриппа I и
II типов, PC-вирусы, аденовирусы, вирусы
гриппа, цитомегаловирус). Возможна
активация и перемещение из
носоглотки аутофлоры при воздействии
физико-химических факторов, переохлаждении.
В большинстве случаев в этиологии ОПБ
подтверждаются вирусно-бактериальные
ассоциации, в
которых вирусы,
имеющие тропизм к эпителию дыхательных
путей, повреждают его,
снижают барьерные
свойства стенки
бронхов и создают условия
для развития бактериального воспалительного
процесса. Чаще
всего речь идет не о инвазивном, а
интраламинарном размножении
условно-патогенной бактериальной
аутофлоры. Бронхит, как правило, возникает
в процессе течения таких детских
инфекций, как коклюш
и корь. У детей
старшего возраста нередким этиологическим
фактором может быть Mycoplasma
pneumoniae, Chlamydia pneum.
Патогенез.
Инфекционное
воспаление слизистой оболочки бронхов
приводит к гиперсекреции
и изменению физико-химических свойств
(вязкости, эластичности,
адгезии) слизи, что изменяет
ее текучесть и затрудняет работу ресничек
цилиарных клеток,
приводит к нарушению
мукоцилиарного клиренса
— важнейшего механизма, обеспечивающего
санацию дыхательных
путей. Кашлевые
толчки, возникающие
вследствие раздражения
афферентных рецепторов блуждающего
нерва, усиливают
очищающую функцию
бронхов. При кашле
избыток слизи удаляется под давлением
300 мм рт. ст. со скоростью потока воздуха
5—6 л/с.
вирусы
тропны к эпителию бронхов,
размножаются на нем, повреждают
его, угнетают барьерные св-ва
стенки бронха, что создает условия
для присоед бак воспаления.
Некоторые вирусы могут
повреждать нервные волокна, что нарушает
нервную регуляцию и трофику бронха.
Из-за воспаления
повышается сосудистая
проницаемость,
миграция нейтрофилов
и макрофагов, отек бронхов (кашель,
хрипы, боль).
Продукция мокроты: отек, раздражение
слизистой и нервных окончаний, гибель
кл эпителия, макрофагов, нейтрофилов,
смешивается с секретом бронхов.
Клиника.
Во многом зависит от
этиологии. Заболевание обычно начинается
с повышения
температуры тела,
головной
боли, недомогания, снижения аппетита.
Поскольку ОПБ преимущественно развивается
в структуре респираторной
вирусной инфекции,
в первые дни заболевания присутствуют
симптомы поражения верхних дыхательных
путей. Основным симптомом ОПБ является
кашель.
В начале заболевания кашель
сухой, навязчивый.
При трахеобронхите
кашель может
сопровождаться чувством
"царапанья"
или болью за грудиной. Покраснение
лица и плач при кашле
— аналог
болей за грудиной у
детей раннего возраста. Через несколько
дней кашель
становится мягким, влажным, продуктивным.
Дети младшего возраста обычно проглатывают
мокроту.
повышение Т, общая интоксикация,
ринит, фарингит (покашливание, саднение
в горле), ларингит (охриплость голоса),
трахеит (саднение и боль за грудиной,
сухой и болезненный кашель), конъюнктивит.
Кашель вначале сухой, на 4-8 день болезни
становится влажным. Боль при кашле –
при трахеобронхите. Иногда возникает
2 волна лихорадки
– наслоение бак инф или другая вирусная.
Кашель более 3 нед – при микоплазме,
аденовирусе, РС-инф.
Аускультативно
ОПБ характеризуется жестким
дыханием, диффузными
сухими, влажными
среднепузырчатыми
хрипами, количество
которых уменьшается после откашливания.
Гематологические сдвиги указывают на
наличие вирусной инфекции или нетяжелого
бактериального воспаления. Длительность
ОПБ обычно не превышает 2 нед.
Диф.
Диагноз.
проводится с пневмонией,
бронхолегочными заболеваниями, обострения
которых могут протекать с клиникой ОПБ
(муковисцидоз, бронхоэктатическая
болезнь и др.). При подозрении на пневмонию
(асимметрия физикальных данных, выраженные
признаки интоксикации) обязательно
проводят рентгенографию грудной клетки.
Лечение.
обычно проводят на дому.
При вирусной этиологии бронхита лечение
аналогично лечению ОРВИ верхних
дыхательных путей. В
лечении бронхитов широко используют
средства, облегчающие
эвакуацию мокроты (отхаркивающие).
При назначении отхаркивающих
средств необходимо обеспечить достаточную
гидратацию,
поскольку потеря воды повышает вязкость
мокроты. Применяют микстуры на основе
настоя корня алтея с добавлением натрия
бензоата, калия иодида и нашатырно-анисовых
капель. Бронхикум, «Доктор Мом» также
относятся к отхаркивающим средствам.
Разжижающие
мокроту
(муколитические).
При заболевании нижних
дыхательных путей с образованием густой
вязкой мокроты целесообразно использовать
препараты, содержащие ацетилцистеин
(АЦЦ, мукомист, флуимуцил, мукобене).
Муколитическим действием
обладают производные алкалоида вазицина
— бромгексин, бизолвон, мукосалван.
Карбоцистеины (мукодин,
мукопронт, бронкатар) обладают одновременно
мукорегулирующим
и муколитическим
эффектами. Под действием препаратов
этой группы происходит регенерация
слизистой обологки бронхов, восстановление
ее структуры,
уменьшение количества бокаловидных
клеток, восстановление секреции IgA,
улучшение мукоцилиарного клиренса.
Ингаляции
теплой водой
или 2%
раствором натрия гидрокарбоната
обладают хорошим
муколитиическим эффектом, ненамного
уступающим муколитическим препаратам.
Постуральный
дренаж (дренаж
положением) и вибрационный массаж
являются мощными методами эвакуации
мокроты. Эффективны свешивания туловища
с кровати на животе с упором руками в
пол сразу после пробуждения на 15—20 мин
(с перерывами) с повторением манипуляции
2—3 раза в день.
При
наличии признаков бактериального
воспаления
необходимо назначить антибактериальную
терапию
(оральные
цефалоспорины, амоксициллин, макролиды)
в возрастной дозировке. Курс лечения
обычно 5—7 дней.
Острый
обструктивный бронхит
(ООБ) - бронхит, протекающий с синдромом
обструкции бронхов.
Возникает у детей значительно чаще и
протекает тяжелее, чем у взрослых.
Этиология.
Этиологическими факторами ООБ и
бронхиолита являются PC-вирусы,
вирусы парагриппа III типа,
аденовирусы.
У старших детей в возникновении ООБ
определенное место занимают Mycoplasma
рп. и Ch. pneumoniae.
Предрасполагает:
курение матери во время б-ти, пассивное
курение, грязный воздух, фетальный
алкогольный синдром, ЗВУР,
экссудативно-катаральная и
лимфатико-гипопластическая аномалия
конституции.
Патогенез.
нарушение
бронхиальной проходимости на
фоне острых и хронических заболеваний.
Основные компоненты обструкции бронхов
при бронхолегочных заболеваниях у детей
следующие:
• Утолщение
слизистой оболочки бронхов.
Основная причина этого компонента
обструкции — воспаление
(инфекционное, аллергическое), которое
приводит к отеку
и клеточной инфильтрации
слизистой и подслизистой оболочек. Чем
младше ребенок, тем больше значимость
утолщения слизистой оболочки бронхов
в формировании бронхообструктивного
синдрома; чем
меньше
калибр дыхательных путей,
тем существеннее доля воспалительного
утолщения слизистой и тем больше риск
развития необратимой облитерации.
Гиперплазия железистого аппарата
бронхов также влияет на степень утолщения
слизистой оболочки.
• Гиперсекреция
и изменение реологических свойств
бронхиального секрета
имеют существенное значение в формировании
бронхообструктивного синдрома у детей
раннего возраста. К гиперсекреции
склонны дети с экссудативно-катаральной
и лимфатико-гипопластической аномалиями
конституции. Обезвоживание
бронхиального секрета при уменьшении
диаметра бронхов,
обусловленном другими компонентами
обструкции, приводит к
повышению вязкости
избыточного
продуцированного бронхиального секрета
и формированию
плотных
слизистых пробок,
обтурирующих
просвет дыхательных путей.
Изменение реологических свойств мокроты
(вязкий секрет) является причиной
формирования бронхиальной обструкции
при муковисцидозе. При синдроме цилиарной
дискинезии
нарушается эвакуация
неизмененного или инфицированного
бронхиального секрета.
• Спазм гладкой
мускулатуры бронхов
— наиболее быстро развивающийся и легко
обратимый компонент обструкции. Его
значимость увеличивается с возрастом
ребенка и при повторных эпизодах
обструкции. Частый повторный или
длительно существующий спазм может
привести к гипертрофии гладкой мускулатуры
бронхов.
• Вздутие
легких, которое развивается при нарушении
бронхиальной проходимости,
усиливает обструкцию из-за
сдавления
воздухоносных путей эмфизематозной
легочной тканью.
Помимо
перечисленных механизмов обструкции,
сужение воздухоносных путей может быть
следствием компрессии
при тимомегалии,
увеличении внутригрудных лимфатических
узлов, врожденной долевой эмфиземе,
диафрагмальной грыже, опухолях средостения
и др.
При остром бронхиолите происходит
десквамация
эпителия, который
замещается
клетками росткового слоя, не имеющими
ресничек. Это
наиболее раннее поражение слизистой
оболочки мелких бронхов (менее 1 мм) и
бронхиол. Перибронхиальное пространство
инфильтрируется лимфоцитами,
выражен
отек подслизистой
оболочки и адвентиции. Спущенный
эпителий, волокна фибрина, слизь образуют
плотные пробки внутри мелких бронхов
и бронхиол, приводя к полной или частичной
обструкции бронхиол.
Степень обструкции, наличие или отсутствие
коллатеральной вентиляции определяют
развитие коллапса или гиперинфляции
(вздутия) участков легкого.
сужение
дыхательных путей из-за скопления
материала в просвете, утолщения стенки,
сокращения бронхиальных мышц, разрушения
дыхательных путей и компрессии бронха.
У детей чаще – от скопления слизи и
отека слизистой бронха. Спазм мускулатуры
чаще при аллергических бронхитах. Из-за
сужения бронхов выдох становится
свистящим, шумным.
Нарушается мукоцилиарный клиренс и
мокрота отходит хуже, скапливается в
просвете бронхов. Нарушаются свойства
слизи, возникает дефект местного и
секреторного им-та, дефект
макрофагальной системы.
Гиперреактивность бронхов, гипертрофия
мышечной тк, гиперплазия и метопалзия
слизистой бронхов.
Клиника.
• Начало ООБ острое с повышением
температуры тела, катаральными
изменениями со стороны верхних дыхательных
путей. Общее состояние ребенка, как
правило, нарушается не резко.
•
Признаки респираторного расстройства
могут появиться как в первый день
заболевания, так и на 3—5-й день болезни.
Постепенно увеличиваются
частота дыхания до 50 в 1 мин (реже до
60—70) и продолжительность
выдоха, который становится шумным,
свистящим.
• На фоне коробочного
оттенка перкуторного звука выслушивают
дыхание с усиленным удлиненным
выдохом, двусторонними сухими свистящими
хрипами. Чем младше ребенок, тем
чаще у него можно услышать среднепузырчатые
и мелкопузырчатые влажные хрипы,
обусловленные гиперсекрецией бронхиальных
желез и вовлечением в процесс бронхиол.
Хрипы могут быть слышны на расстоянии.
• На высоте развития обструкции
ребенок становится беспокойным,
раздражительным, старается принять
сидячее положение с
опорой на руки. Дыхание сопровождается
участием вспомогательной мускулатуры,
раздуванием крыльев носа, втяжением
эпигастрия и межреберных промежутков.
Нередко появляется легкий периоральный
цианоз. Большая выраженность цианоза
свидетельствует о значительной тяжести
состояния. Возможно – периоральный
цианоз, бледность кожи, беспокойство
ребенка, вынужденное положение.
•
Изменения периферической крови
соответствуют таковому при вирусной
инфекции (лейкопения, лимфоцитоз при
умеренно повышенной СОЭ).
•
Рентгенологически при ООБ определяют
признаки вздутия легких (повышение
прозрачности легочных полей, горизонтальное
стояние ребер, низкое стояние купола
диафрагмы)
Диф.
проводят с аспирацией
инородного тела, приступом бронхиальной
астмы, реже - с пневмонией.
Лечение.
Госпитализации подлежат
дети со среднетяжелым и тяжелым течением
ООБ.
• Кислородные
ингаляции —
необходимый метод лечения с обструктивными
нарушениями любой степени тяжести.
Применяется увлажненный
теплый 30—40% кислород.
У детей до года общее количество жидкости
с учетом грудного Молока или молочных
смесей должно быть 140—150 мл/кг массы в
сутки (1/3 объема — раствор для оральной
регидратации).
• Антибактериальная
терапия при ООБ показана только
при подозрении на пневмонию.
• Целесообразно применение селективных
Р2-адреномиметиков
и холинолитиков.
Однако преобладание
отечно-инфильтративных и обтурационных
компонентов обструкции у детей раннего
возраста объясняет умеренный и
кратковременный эффект при этом виде
терапии. При
нетяжелой обструкции
возможна дача сальбутамола
per os (1 мг на прием
в возрасте 2—4 месяцев и 2 мг — в возрасте
2—4 лет 2—3 раза в день). Вдыхание
препарата из дозированного ингалятора
производят с обязательным использованием
спейсера — специальной камеры с лицевой
маской. Вдыхание
1-2 доз сальбутамола (вентолина)
уменьшает обструкцию
через 10—15 мин. Применение небулайзера
(распылителя с компрессором) позволяет
подавать раствор сальбутамола через
маску под давлением с оптимальной
скоростью 8 л/мин. При отсутствии
ингаляционных средств доставки или
недостаточном эффекте от ингаляционного
применения адреномиметиков (что обычно
связано с плохой проходимостью дыхательных
путей) целесообразно внутримышечное
введение 0,05% раствора алупента (0,05% —
0,3 мл) или сальбутамола (0,2 мл детям в
возрасте 2—12 месяцев и 0,4 мл детям в
возрасте 2—4 лет).
• У ряда больных
удается добиться хорошего спазмолитического
эффекта при применении холинолитиков
(атровента или травентола в дозированном
ингаляторе или через небулайзер;
комбинированного препарата БЕРОДУАЛ).
•
Эуфиллин
per os назначается из расчета 15—24 мг/кг/сут.
с соблюдением равных интервалов между
четырехразовым приемом препарата.
Внутривенно капельно вводится 2,4% раствор
эуфиллина из расчета стартовой дозы
4—5 мг/кг в 100-150 мл изотонического раствора
натрия хлорида с последующим введением
по 1 мг/кг/ч.
• При тяжелом течении
PC-вирусного бронхиолита у недоношенных
детей с бронхолегочной дисплазией
применяют противовирусный
препарат рибавирин
20 мг/кг/сут. в
аэрозоле через небулайзер в течение
18—24 ч 3 — 5 дней. Препарат очень дорог и
не лишен побочных эффектов. В США есть
опыт применения паливизумаба (синаджиза)
при тяжелых формах бронхиолита. Этот
препарат представляет собой моноклональные
антитела к F-протеину РС-вируса.
•
При подозрении на
облитерацию
обязательно назначают лечение
глюкокортикостероидами
парентерально
и ингаляционно (раствор беклометазона
дипропионата
через небулайзер или спейсер), нестероидные
противовоспалительные препараты.
ПУЛЬМИКОРТ.
83.
Пневмонии у детей раннего возраста.
Классификация. Клиническая картина.
Лечение. Профилактика.
Пневмония
― острое инфекционное заболевание,
характеризующееся очаговым
поражением респираторных отделов легких
с внутриальвеолярной
экссудацией,
выявляемым при объективном и Rg -логическом
обследовании.
Большая
частота пневмоний
у детей раннего возраста обусловлена:
АФО органов дыхания, Своеобразием
иммунологической реактивности, низкая
барьерная функция кожи и слизистых
оболочек, в т.ч. и стенки бронхов;
пониженный синтез гуморальных антител,
секреторного Jg A; особенности Т-лимфоидной
системы.
Преобладает
у новорожденных
внутриутробное и нозокомиальное
инфицирование.
Стрептококк гр.В,
кишечная палочка, клебсиелла, реже St.
aureus.
Ассоциации с ЦМВ, грибами Candida,
вирусами герпеса. Редко –
пневмоцисты.
Классификация
острых пневмоний.
1.
Морфологическая форма:
Очаговая
(домашняя) – гемофильная, стафил, мико.
очаги чаще размером от 1 см и
более.
Очагово-сливная
(госпитальная) – Псевдомонады, клебсиеллы.
инфильтративные очаговые изменения в
нескольких сегментах или во всей доле
легкого, на фоне которых могут быть
видны более плотные участки инфильтрации
и/или полости деструкции.
Крупозная
(иммунодеф) – Пневмоцисты, ЦМВ. пневмония
диагностируется прежде всего по
клиническим данным.
Сегментарная
(перинатальная) – Стрептококк В,
хламидии, урео. весь
сегмент, который, как правило, находится
в состоянии ателектаза
или гиповентиляции.
Интерстициальная
(ИВЛ) – смешенная. поражен
прежде всего интерстиций.
2.
По месту возникновения и
этиологии:
Внебольничная
Внутрибольничная
Профилактика.
железодефицитных
состояний у детей раннего возраста
должна начинаться с предупреждения
его недостатка у женщин репродуктивного
возраста и
назначения всем
матерям на протяжении второй половины
беременности и в период лактации
препаратов железа,
например гемостимулина
по 1,0 г в сутки,
или другого препарата. Учитывая сказанное
выше, показано назначение всем доношенным
детям на естественном вскармливании
начиная с 3 месяцев одного
из препаратов железа
(орферон, сироп алоэ с железом или
какой-либо другой препарат) из расчета
по элементарному железу 1 мг/кг.
Недоношенным детям
суточную профилактическую дозу
препарата увеличивают до 2 мг/кг и
начинают давать с
месячного возраста,
а у детей с очень низкой массой при
рождении даже
раньше - с 3 недель. Естественное
вскармливание, рациональное расширение
питания и введение прикормов в
декретированные сроки, прогулки, массаж
и гимнастика, профилактика рахита —
существенные звенья профилактики
железодефицитных состояний. В настоящее
время рекомендуется
пользоваться кашами для детского питания
с добавлением препаратов железа.
Наконец, адаптированные смеси для
питания детей содержат добавки железа,
и если ребенок их получает, то нет
необходимости в дополнительном назначении
препаратов железа для профилактики его
дефицита.
82.Бронхиты
у детей: простой и обструктивный.
Этиология, патогенез, клиника,
дифференциальный диагноз, лечение.
Бронхит
— воспалительное заболевание бронхов
различной этиологии (инфекционной,
аллергической, физико-химической и
др.).
Выделяют следующие формы бронхитов
у детей:
• острый простой бронхит
(ОПБ);
• острый обструктивный бронхит
(ООБ);
• острый бронхиолит;
•
рецидивирующий бронхит (РБ);
•
рецидивирующий обструктивный бронхит
(РОБ);
• хронический бронхит (ХБ) —
первичный и вторичный;
• хронический
бронхиолит с облитерацией.
ОСТРЫЙ
ПРОСТОЙ БРОНХИТ
- бронхит, протекающий без
признаков обструкции бронхов.
Этиология.
Этиологическими факторами ОПБ являются
вирусы
(парагриппа I и
II типов, PC-вирусы, аденовирусы, вирусы
гриппа, цитомегаловирус). Возможна
активация и перемещение из
носоглотки аутофлоры при воздействии
физико-химических факторов, переохлаждении.
В большинстве случаев в этиологии ОПБ
подтверждаются вирусно-бактериальные
ассоциации, в
которых вирусы,
имеющие тропизм к эпителию дыхательных
путей, повреждают его,
снижают барьерные
свойства стенки
бронхов и создают условия
для развития бактериального воспалительного
процесса. Чаще
всего речь идет не о инвазивном, а
интраламинарном размножении
условно-патогенной бактериальной
аутофлоры. Бронхит, как правило, возникает
в процессе течения таких детских
инфекций, как коклюш
и корь. У детей
старшего возраста нередким этиологическим
фактором может быть Mycoplasma
pneumoniae, Chlamydia pneum.
Патогенез.
Инфекционное
воспаление слизистой оболочки бронхов
приводит к гиперсекреции
и изменению физико-химических свойств
(вязкости, эластичности,
адгезии) слизи, что изменяет
ее текучесть и затрудняет работу ресничек
цилиарных клеток,
приводит к нарушению
мукоцилиарного клиренса
— важнейшего механизма, обеспечивающего
санацию дыхательных
путей. Кашлевые
толчки, возникающие
вследствие раздражения
афферентных рецепторов блуждающего
нерва, усиливают
очищающую функцию
бронхов. При кашле
избыток слизи удаляется под давлением
300 мм рт. ст. со скоростью потока воздуха
5—6 л/с.
вирусы
тропны к эпителию бронхов,
размножаются на нем, повреждают
его, угнетают барьерные св-ва
стенки бронха, что создает условия
для присоед бак воспаления.
Некоторые вирусы могут
повреждать нервные волокна, что нарушает
нервную регуляцию и трофику бронха.
Из-за воспаления
повышается сосудистая
проницаемость,
миграция нейтрофилов
и макрофагов, отек бронхов (кашель,
хрипы, боль).
Продукция мокроты: отек, раздражение
слизистой и нервных окончаний, гибель
кл эпителия, макрофагов, нейтрофилов,
смешивается с секретом бронхов.
Клиника.
Во многом зависит от
этиологии. Заболевание обычно начинается
с повышения
температуры тела,
головной
боли, недомогания, снижения аппетита.
Поскольку ОПБ преимущественно развивается
в структуре респираторной
вирусной инфекции,
в первые дни заболевания присутствуют
симптомы поражения верхних дыхательных
путей. Основным симптомом ОПБ является
кашель.
В начале заболевания кашель
сухой, навязчивый.
При трахеобронхите
кашель может
сопровождаться чувством
"царапанья"
или болью за грудиной. Покраснение
лица и плач при кашле
— аналог
болей за грудиной у
детей раннего возраста. Через несколько
дней кашель
становится мягким, влажным, продуктивным.
Дети младшего возраста обычно проглатывают
мокроту.
повышение Т, общая интоксикация,
ринит, фарингит (покашливание, саднение
в горле), ларингит (охриплость голоса),
трахеит (саднение и боль за грудиной,
сухой и болезненный кашель), конъюнктивит.
Кашель вначале сухой, на 4-8 день болезни
становится влажным. Боль при кашле –
при трахеобронхите. Иногда возникает
2 волна лихорадки
– наслоение бак инф или другая вирусная.
Кашель более 3 нед – при микоплазме,
аденовирусе, РС-инф.
Аускультативно
ОПБ характеризуется жестким
дыханием, диффузными
сухими, влажными
среднепузырчатыми
хрипами, количество
которых уменьшается после откашливания.
Гематологические сдвиги указывают на
наличие вирусной инфекции или нетяжелого
бактериального воспаления. Длительность
ОПБ обычно не превышает 2 нед.
Диф.
Диагноз.
проводится с пневмонией,
бронхолегочными заболеваниями, обострения
которых могут протекать с клиникой ОПБ
(муковисцидоз, бронхоэктатическая
болезнь и др.). При подозрении на пневмонию
(асимметрия физикальных данных, выраженные
признаки интоксикации) обязательно
проводят рентгенографию грудной клетки.
Лечение.
обычно проводят на дому.
При вирусной этиологии бронхита лечение
аналогично лечению ОРВИ верхних
дыхательных путей. В
лечении бронхитов широко используют
средства, облегчающие
эвакуацию мокроты (отхаркивающие).
При назначении отхаркивающих
средств необходимо обеспечить достаточную
гидратацию,
поскольку потеря воды повышает вязкость
мокроты. Применяют микстуры на основе
настоя корня алтея с добавлением натрия
бензоата, калия иодида и нашатырно-анисовых
капель. Бронхикум, «Доктор Мом» также
относятся к отхаркивающим средствам.
Разжижающие
мокроту
(муколитические).
При заболевании нижних
дыхательных путей с образованием густой
вязкой мокроты целесообразно использовать
препараты, содержащие ацетилцистеин
(АЦЦ, мукомист, флуимуцил, мукобене).
Муколитическим действием
обладают производные алкалоида вазицина
— бромгексин, бизолвон, мукосалван.
Карбоцистеины (мукодин,
мукопронт, бронкатар) обладают одновременно
мукорегулирующим
и муколитическим
эффектами. Под действием препаратов
этой группы происходит регенерация
слизистой обологки бронхов, восстановление
ее структуры,
уменьшение количества бокаловидных
клеток, восстановление секреции IgA,
улучшение мукоцилиарного клиренса.
Ингаляции
теплой водой
или 2%
раствором натрия гидрокарбоната
обладают хорошим
муколитиическим эффектом, ненамного
уступающим муколитическим препаратам.
Постуральный
дренаж (дренаж
положением) и вибрационный массаж
являются мощными методами эвакуации
мокроты. Эффективны свешивания туловища
с кровати на животе с упором руками в
пол сразу после пробуждения на 15—20 мин
(с перерывами) с повторением манипуляции
2—3 раза в день.
При
наличии признаков бактериального
воспаления
необходимо назначить антибактериальную
терапию
(оральные
цефалоспорины, амоксициллин, макролиды)
в возрастной дозировке. Курс лечения
обычно 5—7 дней.
Острый
обструктивный бронхит
(ООБ) - бронхит, протекающий с синдромом
обструкции бронхов.
Возникает у детей значительно чаще и
протекает тяжелее, чем у взрослых.
Этиология.
Этиологическими факторами ООБ и
бронхиолита являются PC-вирусы,
вирусы парагриппа III типа,
аденовирусы.
У старших детей в возникновении ООБ
определенное место занимают Mycoplasma
рп. и Ch. pneumoniae.
Предрасполагает:
курение матери во время б-ти, пассивное
курение, грязный воздух, фетальный
алкогольный синдром, ЗВУР,
экссудативно-катаральная и
лимфатико-гипопластическая аномалия
конституции.
Патогенез.
нарушение
бронхиальной проходимости на
фоне острых и хронических заболеваний.
Основные компоненты обструкции бронхов
при бронхолегочных заболеваниях у детей
следующие:
• Утолщение
слизистой оболочки бронхов.
Основная причина этого компонента
обструкции — воспаление
(инфекционное, аллергическое), которое
приводит к отеку
и клеточной инфильтрации
слизистой и подслизистой оболочек. Чем
младше ребенок, тем больше значимость
утолщения слизистой оболочки бронхов
в формировании бронхообструктивного
синдрома; чем
меньше
калибр дыхательных путей,
тем существеннее доля воспалительного
утолщения слизистой и тем больше риск
развития необратимой облитерации.
Гиперплазия железистого аппарата
бронхов также влияет на степень утолщения
слизистой оболочки.
• Гиперсекреция
и изменение реологических свойств
бронхиального секрета
имеют существенное значение в формировании
бронхообструктивного синдрома у детей
раннего возраста. К гиперсекреции
склонны дети с экссудативно-катаральной
и лимфатико-гипопластической аномалиями
конституции. Обезвоживание
бронхиального секрета при уменьшении
диаметра бронхов,
обусловленном другими компонентами
обструкции, приводит к
повышению вязкости
избыточного
продуцированного бронхиального секрета
и формированию
плотных
слизистых пробок,
обтурирующих
просвет дыхательных путей.
Изменение реологических свойств мокроты
(вязкий секрет) является причиной
формирования бронхиальной обструкции
при муковисцидозе. При синдроме цилиарной
дискинезии
нарушается эвакуация
неизмененного или инфицированного
бронхиального секрета.
• Спазм гладкой
мускулатуры бронхов
— наиболее быстро развивающийся и легко
обратимый компонент обструкции. Его
значимость увеличивается с возрастом
ребенка и при повторных эпизодах
обструкции. Частый повторный или
длительно существующий спазм может
привести к гипертрофии гладкой мускулатуры
бронхов.
• Вздутие
легких, которое развивается при нарушении
бронхиальной проходимости,
усиливает обструкцию из-за
сдавления
воздухоносных путей эмфизематозной
легочной тканью.
Помимо
перечисленных механизмов обструкции,
сужение воздухоносных путей может быть
следствием компрессии
при тимомегалии,
увеличении внутригрудных лимфатических
узлов, врожденной долевой эмфиземе,
диафрагмальной грыже, опухолях средостения
и др.
При остром бронхиолите происходит
десквамация
эпителия, который
замещается
клетками росткового слоя, не имеющими
ресничек. Это
наиболее раннее поражение слизистой
оболочки мелких бронхов (менее 1 мм) и
бронхиол. Перибронхиальное пространство
инфильтрируется лимфоцитами,
выражен
отек подслизистой
оболочки и адвентиции. Спущенный
эпителий, волокна фибрина, слизь образуют
плотные пробки внутри мелких бронхов
и бронхиол, приводя к полной или частичной
обструкции бронхиол.
Степень обструкции, наличие или отсутствие
коллатеральной вентиляции определяют
развитие коллапса или гиперинфляции
(вздутия) участков легкого.
сужение
дыхательных путей из-за скопления
материала в просвете, утолщения стенки,
сокращения бронхиальных мышц, разрушения
дыхательных путей и компрессии бронха.
У детей чаще – от скопления слизи и
отека слизистой бронха. Спазм мускулатуры
чаще при аллергических бронхитах. Из-за
сужения бронхов выдох становится
свистящим, шумным.
Нарушается мукоцилиарный клиренс и
мокрота отходит хуже, скапливается в
просвете бронхов. Нарушаются свойства
слизи, возникает дефект местного и
секреторного им-та, дефект
макрофагальной системы.
Гиперреактивность бронхов, гипертрофия
мышечной тк, гиперплазия и метопалзия
слизистой бронхов.
Клиника.
• Начало ООБ острое с повышением
температуры тела, катаральными
изменениями со стороны верхних дыхательных
путей. Общее состояние ребенка, как
правило, нарушается не резко.
•
Признаки респираторного расстройства
могут появиться как в первый день
заболевания, так и на 3—5-й день болезни.
Постепенно увеличиваются
частота дыхания до 50 в 1 мин (реже до
60—70) и продолжительность
выдоха, который становится шумным,
свистящим.
• На фоне коробочного
оттенка перкуторного звука выслушивают
дыхание с усиленным удлиненным
выдохом, двусторонними сухими свистящими
хрипами. Чем младше ребенок, тем
чаще у него можно услышать среднепузырчатые
и мелкопузырчатые влажные хрипы,
обусловленные гиперсекрецией бронхиальных
желез и вовлечением в процесс бронхиол.
Хрипы могут быть слышны на расстоянии.
• На высоте развития обструкции
ребенок становится беспокойным,
раздражительным, старается принять
сидячее положение с
опорой на руки. Дыхание сопровождается
участием вспомогательной мускулатуры,
раздуванием крыльев носа, втяжением
эпигастрия и межреберных промежутков.
Нередко появляется легкий периоральный
цианоз. Большая выраженность цианоза
свидетельствует о значительной тяжести
состояния. Возможно – периоральный
цианоз, бледность кожи, беспокойство
ребенка, вынужденное положение.
•
Изменения периферической крови
соответствуют таковому при вирусной
инфекции (лейкопения, лимфоцитоз при
умеренно повышенной СОЭ).
•
Рентгенологически при ООБ определяют
признаки вздутия легких (повышение
прозрачности легочных полей, горизонтальное
стояние ребер, низкое стояние купола
диафрагмы)
Диф.
проводят с аспирацией
инородного тела, приступом бронхиальной
астмы, реже - с пневмонией.
Лечение.
Госпитализации подлежат
дети со среднетяжелым и тяжелым течением
ООБ.
• Кислородные
ингаляции —
необходимый метод лечения с обструктивными
нарушениями любой степени тяжести.
Применяется увлажненный
теплый 30—40% кислород.
У детей до года общее количество жидкости
с учетом грудного Молока или молочных
смесей должно быть 140—150 мл/кг массы в
сутки (1/3 объема — раствор для оральной
регидратации).
• Антибактериальная
терапия при ООБ показана только
при подозрении на пневмонию.
• Целесообразно применение селективных
Р2-адреномиметиков
и холинолитиков.
Однако преобладание
отечно-инфильтративных и обтурационных
компонентов обструкции у детей раннего
возраста объясняет умеренный и
кратковременный эффект при этом виде
терапии. При
нетяжелой обструкции
возможна дача сальбутамола
per os (1 мг на прием
в возрасте 2—4 месяцев и 2 мг — в возрасте
2—4 лет 2—3 раза в день). Вдыхание
препарата из дозированного ингалятора
производят с обязательным использованием
спейсера — специальной камеры с лицевой
маской. Вдыхание
1-2 доз сальбутамола (вентолина)
уменьшает обструкцию
через 10—15 мин. Применение небулайзера
(распылителя с компрессором) позволяет
подавать раствор сальбутамола через
маску под давлением с оптимальной
скоростью 8 л/мин. При отсутствии
ингаляционных средств доставки или
недостаточном эффекте от ингаляционного
применения адреномиметиков (что обычно
связано с плохой проходимостью дыхательных
путей) целесообразно внутримышечное
введение 0,05% раствора алупента (0,05% —
0,3 мл) или сальбутамола (0,2 мл детям в
возрасте 2—12 месяцев и 0,4 мл детям в
возрасте 2—4 лет).
• У ряда больных
удается добиться хорошего спазмолитического
эффекта при применении холинолитиков
(атровента или травентола в дозированном
ингаляторе или через небулайзер;
комбинированного препарата БЕРОДУАЛ).
•
Эуфиллин
per os назначается из расчета 15—24 мг/кг/сут.
с соблюдением равных интервалов между
четырехразовым приемом препарата.
Внутривенно капельно вводится 2,4% раствор
эуфиллина из расчета стартовой дозы
4—5 мг/кг в 100-150 мл изотонического раствора
натрия хлорида с последующим введением
по 1 мг/кг/ч.
• При тяжелом течении
PC-вирусного бронхиолита у недоношенных
детей с бронхолегочной дисплазией
применяют противовирусный
препарат рибавирин
20 мг/кг/сут. в
аэрозоле через небулайзер в течение
18—24 ч 3 — 5 дней. Препарат очень дорог и
не лишен побочных эффектов. В США есть
опыт применения паливизумаба (синаджиза)
при тяжелых формах бронхиолита. Этот
препарат представляет собой моноклональные
антитела к F-протеину РС-вируса.
•
При подозрении на
облитерацию
обязательно назначают лечение
глюкокортикостероидами
парентерально
и ингаляционно (раствор беклометазона
дипропионата
через небулайзер или спейсер), нестероидные
противовоспалительные препараты.
ПУЛЬМИКОРТ.
83.
Пневмонии у детей раннего возраста.
Классификация. Клиническая картина.
Лечение. Профилактика.
Пневмония
― острое инфекционное заболевание,
характеризующееся очаговым
поражением респираторных отделов легких
с внутриальвеолярной
экссудацией,
выявляемым при объективном и Rg -логическом
обследовании.
Большая
частота пневмоний
у детей раннего возраста обусловлена:
АФО органов дыхания, Своеобразием
иммунологической реактивности, низкая
барьерная функция кожи и слизистых
оболочек, в т.ч. и стенки бронхов;
пониженный синтез гуморальных антител,
секреторного Jg A; особенности Т-лимфоидной
системы.
Преобладает
у новорожденных
внутриутробное и нозокомиальное
инфицирование.
Стрептококк гр.В,
кишечная палочка, клебсиелла, реже St.
aureus.
Ассоциации с ЦМВ, грибами Candida,
вирусами герпеса. Редко –
пневмоцисты.
Классификация
острых пневмоний.
1.
Морфологическая форма:
Очаговая
(домашняя) – гемофильная, стафил, мико.
очаги чаще размером от 1 см и
более.
Очагово-сливная
(госпитальная) – Псевдомонады, клебсиеллы.
инфильтративные очаговые изменения в
нескольких сегментах или во всей доле
легкого, на фоне которых могут быть
видны более плотные участки инфильтрации
и/или полости деструкции.
Крупозная
(иммунодеф) – Пневмоцисты, ЦМВ. пневмония
диагностируется прежде всего по
клиническим данным.
Сегментарная
(перинатальная) – Стрептококк В,
хламидии, урео. весь
сегмент, который, как правило, находится
в состоянии ателектаза
или гиповентиляции.
Интерстициальная
(ИВЛ) – смешенная. поражен
прежде всего интерстиций.
2.
По месту возникновения и
этиологии:
Внебольничная
Внутрибольничная
- пневмококк - стафилококк - стафилококк - H.influenzae - H.influenzae - E.coli - стрептококк Пнеумония - Branchamella - микоплазма - Pseudomonas - Chlam. Pneum - протей - легионелла - Serratia - вирусы - вирусы Перинатальная При иммунодефиците
- Сhlam.trachomatis - бактериальная - пневмоцисты - пневмоцисты - уреаплазма -грибы - цитомегаловирус - микобактерии -цитомегаловирус 3. По течению: -острое -затяжное ( рецидивирующее). 4. По наличию осложнений: -неосложненная. -Осложненная (токсикоз, синпневмонический плеврит, метапневмонический плеврит, легочная деструкция, ДВС-синдром, инфекционно-токсический шок, респираторный дистресс- синдром(взрослого типа), отек легкого 2-го типа, пневмоторакс, пиопневмоторакс.) Внебольничные пневмонии — возникшие у ребенка в обычных условиях. Внутрибольничные пневмонии (госпитальные, нозокомиальные) — развившиеся через 48 ч пребывания ребенка в стационаре или в течение 48 ч после выписки из стационара. Внутриутробные пневмонии — развившиеся в первые 72 ч после рождения. Клиника. Основными диагностическими (опорными) критериями острой пневмонии является: кашель (вначале сухой, затем влажный), одышка (> 60 в мин.), участие вспомогательной мускулатуры, локальная крепитация, влажные разнокалиберные хрипы, участки укорочения легочного звука, инфильтративные тони на рентгенограмме, повышение температуры тела, явления интоксикации. Могут быть бледность кожи, цианоз носогубного треугольника, нарушение функции ССС, ЖКТ. односторонность патологического процесса, локальное укорочение перкуторного звука жёсткое, ослабленное или бронхиальное дыхание локальные, стабильные м/п влажные хрипы или крепитация. Если при осмотре у ребенка независимо от уровня температуры и при отсутствии обструкции имеется: — учащение дыхания: 60 в минуту у детей первого месяца жизни; 50 в минуту у детей 2—12 месяцев; 40 в минуту у детей 1—4 лет; — втяжение межреберий; — стонущее (кряхтящее) дыхание; — цианоз носогубного треугольника; — признаки токсикоза («больной» вид, отказ от еды и питья, сонливость, нарушение сознания, резкая бледность при повышенной температуре тела), то состояние расценивается как тяжелое с большой вероятностью пневмонии. Если у ребенка нет признаков, указанных в пункте 1, но есть: — температура тела 38 °С дольше 3 дней; — локальные физикальные признаки пневмонии; — асимметрия хрипов, то следует предположить наличие пневмонии. Если ребенок с ОРЗ и признаками бронхиальной обструкции имеет: — асимметрию хрипов; — «воспалительную» гемограмму, то следует исключить пневмонию проведением рентгенологического исследования. Госпитализации подлежат больные с признаками дыхательной недостаточности. S. Pneumoniae. Морфологическая форма: Очаговая, очагово-сливная, долевая (крупозная). Сливные очаги (часто в верхней и нижней доле справа), инфильтрация доли. Острое начало, лихорадка с ознобом, кашель; при крупозной — боль в боку, животе, покраснение щеки на стороне поражения, ржавая мокрота, герпес; укорочение перкуторного звука, ослабление дыхания, крепитация; быстрая (в течение 24—36 ч) положительная клиническая реакция на пенициллин. Обструктивный синдром не характерен. ЛЕЧ. Амоксициллин/клавуланат per os — 50 мг/кг/сут.; оспен per os — 100 мг/кг/сут. (препараты назначают при лечении нетяжелых пневмоний на дому); пенициллин в/в, в/м - 100-150 тыс ед/кг/сут.; цефалоспорины 1 — 2 поколения per os 30-4 0 мг/кг/сут. или в/в или в/м - 50-100 мг/кг/сут.; макролиды: эритромицин per os - 40-5 0 мг/кг/сут. или в/в - 40-5 0 мг/кг/сут.; азитромицин — 10-12 мг/кг/сут. в течение 5 дней influenzae типа В. До 3 лет; реже — дети более старшего возраста. Очаговая, долевая инфильтрация. Постепенное (реже острое) начало, непродуктивный кашель, высокая лихорадка, сопутствующий отит, эпиглоттит, ларинготрахеит; возможен обструктивный синдром. ЛЕЧ. Амоксициллин/клавуланат — per os — 40 мг/кг/сут. (нетяжелые формы); цефазолин в/м, в/в - 50-100 мг/кг/сут.; цефуроксим 75-150 мг/кг/сут. в/м, в/в. Streptococcus, gr. А. 2—7 лет, Очаговая, очагово-сливная; округлые множественные (часто с обеих сторон) очаги в разных фазах — от инфильтрации до абсцесса; Острое начало, лихорадка, озноб; нет четких перкуторных данных; хрипов мало, сопутствующий некротический трахеит, обструктивный синдром не характерен; атриовентрикулярная блокада при ЭКГ-исследовании, склонность к затяжному течению. ЛЕЧ. Пенициллин в/в, в/м — 100—150 тыс. ел./кг/сут.: цефалоспорины 1—2-го поколения per os 30-4 0 мг/кг/сут.; в/в. в/м - 50—100 мг/кг/сут.; макролиды: эритромицин per os — 40—50 мг/кг/сут.; в/в — 40—50 мг/кг/сут.; азитромицин — 10—12 мг/кг/сут. в течение 5 дней. Кишечная флора: Е. Coli, Klebsiella, pneum., Pseudomonas aeruginosae. Первые месяцы жизни; ослабленные дети любого возраста. Очаговая сливная инфильтрация средней плотности в виде лучистости, без четких границ, с мелкими множественными полостями деструкции; Выраженная интоксикация, дыхательная недостаточность, обструктивный синдром, часто двустороннее поражение; «пестрая» аускультативная картина. ЛЕЧ. Амоксициллин/клавуланат — в/в — 90—120 мг/кг/сут.; цефалоспорины 3-го поколения: клафоран, фортум — 75 — 150 мг/кг/сут., аминогликозиды: гентамицин в/м — 7,5 мг/кг/сут.; карбопенемы в/в - 60 мг/кг/сут.; в тяжелых случаях фторхинолоны — ципрофлоксацин в/в — 20 мг/кг/сут. Mycoplasma pneumoniae, Chlamydia pneumoniae. Очаговая; негомогенная, часто двусторонняя асимметричная инфильтрация, интерстициальная реакция. Длительный инкубационный период (1—3 нед.); постепенное начало, катаральные явления со стороны ВДП , конъюнктивит, сухой навязчивый кашель, скудная мокрота, аускультативные признаки бронхита, бронхиолита; затяжное течение, длительный субфебрилитет; «атипичная пневмония». ЛЕЧ. Макролиды per os: эритромицин per os - 40-5 0 мг/кг/сут.; в/в - 40-5 0 мг/кг/сут.; азитромицин — 10—12 мг/кг/сут. в течение 5 дней; тетрациклины — доксициклин у детей старше 8 лет per os — 5 мг/кг/сут., в/в — 2,5 мг/кг/сут. Chlamydia trachomatis. Новорожденные, первые 6 мес. Жизни. Очаговая Обширная инфильтрация, вздутие легких. Конъюнктивит, упорный кашель «стаккато»; тахипноэ без повышения температуры; диффузные мелкопузырчагые хрипы, обструкция не характерна. ЛЕЧ. Макролиды: эритромицин per os — 40—50 мг/кг/сут.; в/в — 40—50 мг/кг/сут.; азитромицин per os — 10-12 мг/кг/сут. в течение 5 дней. Лечение. • этиотропную терапию при установленном диагнозе или при тяжелом состоянии больного начинают незамедлительно, при сомнении в диагнозе у нетяжелого больного решение принимают после рентгенографии; • первичный выбор антибиотика проводят эмпирически. • показаниями к переходу на альтернативные препараты является отсутствие клинического эффекта от препарата первого выбора в течение 36—48 ч при нетяжелой и 72 ч при тяжелой пневмонии; развитие нежелательных побочных эффектов от препарата первого выбора; • пневмококки устойчивы к гентамицину и другим аминогликозидам, поэтому терапия внебольничных пневмоний антибиотиками данной группы недопустима; • при неосложненных нетяжелых пневмониях следует отдавать предпочтение назначению препаратов per os, заменяя их на парентеральное введение при неэффективности; если терапия была начата парентерально, после снижения температуры следует перейти на прием антибиотика per os; • после курса антибактериальной терапии целесообразно назначить биопрепараты. Постельный режим показан на весь лихорадочный период. Питание должно соответствовать возрасту и обязательно быть полноценным. • Объем жидкости в сутки для детей до года с учетом грудного молока или молочных смесей составляет 140—150 мл/кг массы. Целесообразно 1/3 суточного объема жидкости давать в виде глюкозо-солевых растворов (регидрон, оралит), что у 80—90% больных позволяет отказаться от инфузионной терапии. • При необходимости (эксикоз, коллапс, нарушение микроциркуляции, угроза синдрома ДВС) в вену вводится 1/3 суточного объема. При избыточной инфузии кристаллоидов возможно развитие отека легких. • В помещении, где находится ребенок, должен быть прохладный (18—19 °С), увлажненный воздух, способствующий урежению и углублению дыхания, а также снижающий потери воды. • Жаропонижающие средства не назначают, так как это может затруднить оценку эффективости антибактериальной терапии. Исключение составляют дети, имеющие преморбидные показания для снижения температуры тела. • Показано назначение СВЧ в остром периоде (10—12 сеансов), индуктотермии; электрофорез с 3% раствором калия иодида. • Массаж и ЛФК необходимы сразу же после нормализации температуры. • В стационаре детей помещают в отдельный бокс. Ребенок может быть выписан из стационара сразу же по достижении клинического эффекта для того, чтобы избежать перекрестной инфекции. Сохранение увеличенной СОЭ , хрипов в легких или остаточных рентгенологических изменений не является противопоказанием к выписке. Профилактика. — комплексе социально-гигиенических мероприятий; — рациональном питании, закаливании, улучшении экологии жилища; — предупреждении ОРВИ, вакцинопрофилактике пневмоний (конъюгированная вакцина против Н. influenzae, пневмококка, вакцинопрофилактика гриппа); — профилактике внутрибольничных пневмоний (госпитализация в боксы). 84. Этиология и патогенез острой пневмонии у детей. Классификация. Пневмония ― острое инфекционное заболевание, характеризующееся очаговым поражением респираторных отделов легких с внутриальвеолярной экссудацией, выявляемым при объективном и Rg -логическом обследовании. Этиология: Пневмококк, стафилококк, стрептококк, вирусы, микоплазма, хламидии, легионелла и др. Патогенез. Основной путь проникновения микробов - бронхолегочный с последующим распространением инфекта в респираторные отделы. Гематогенный путь возможен при септических (метастатических) и внутриутробных пневмониях. Лимфогенный путь — редкость, однако по лимфатическим путям процесс переходит из легочного очага в плевру. ОРВИ играют важную роль в патогенезе бактериальных пневмоний. Вирусная инфекция увеличивает продукцию слизи в верхних дыхательных путях и снижает ее бактерицидность; нарушает работу мукоцилиарного аппарата, разрушает эпителиальные клетки, снижает местную иммунологическую защиту, чем облегчает проникновение бактериальной флоры в нижние дыхательные пути и способствует развитию воспалительных изменений в легких. Начальные воспалительные изменения при бронхогенном пути проникновения инфекции обнаруживают в респираторных бронхиолах. Далее они распространяются на паренхиму легких. При кашле инфицированная слизь из очага воспаления попадает в крупные бронхи, а затем, распространяясь в другие респираторные бронхиолы, обусловливает новые очаги воспаления, т. е. распространение инфекции в легких может происходить бронхогенно. В участке клеточной инфильтрации возможно расплавление ткани с формированием абсцессов. Их опорожнение через бронх оставляет в легком полость, обычно заживающую небольшим рубцом. Прорыв абсцесса в плевральную полость ведет к пиопневмотораксу. Попадая в респираторные бронхиолы, инфекционный агент распространяется за их пределы, вызывая воспаление в паренхиме легких (т.е. пневмонию). При распространении бактерий и отечной жидкости через поры альвеол в пределах одного сегмента возникает сегментарная пневмония, а при более бурном распространении - долевая (крупозная) пневмония. Там же в процесс вовлекаются регионарные лимфатические узлы. На рентгенограммах это проявляется расширением корней легкого. Прогрессирует кислородная недостаточность. Развиваются изменения со стороны ЦНС, ССС, ЖКТ, нарушаются обменные процессы, прогрессирует ДН. Классификация острых пневмоний. 1. Морфологическая форма: Очаговая (домашняя) – гемофильная, стафил, мико. очаги чаще размером от 1 см и более. Очагово-сливная (госпитальная) – Псевдомонады, клебсиеллы. инфильтративные очаговые изменения в нескольких сегментах или во всей доле легкого, на фоне которых могут быть видны более плотные участки инфильтрации и/или полости деструкции. Крупозная (иммунодеф) – Пневмоцисты, ЦМВ. пневмония диагностируется прежде всего по клиническим данным. Сегментарная (перинатальная) – Стрептококк В, хламидии, урео. весь сегмент, который, как правило, находится в состоянии ателектаза или гиповентиляции. Интерстициальная (ИВЛ) – смешенная. поражен прежде всего интерстиций. 2. По месту возникновения и этиологии: Внебольничная Внутрибольничная
- пневмококк - стафилококк - стафилококк - H.influenzae - H.influenzae - E.coli - стрептококк Пнеумония - Branchamella - микоплазма - Pseudomonas - Chlam. Pneum - протей - легионелла - Serratia - вирусы - вирусы Перинатальная При иммунодефиците
-
Сhlam.trachomatis
- бактериальная
-
пневмоцисты - пневмоцисты
-
уреаплазма
-грибы
-
цитомегаловирус - микобактерии
-цитомегаловирус
3. По
течению:
-острое
-затяжное
( рецидивирующее).
4.
По наличию осложнений:
-неосложненная.
-Осложненная
(токсикоз, синпневмонический плеврит,
метапневмонический плеврит, легочная
деструкция, ДВС-синдром, инфекционно-токсический
шок, респираторный дистресс-
синдром(взрослого типа), отек легкого
2-го типа, пневмоторакс,
пиопневмоторакс.)
Внебольничные
пневмонии —
возникшие у ребенка в обычных условиях.
Внутрибольничные
пневмонии
(госпитальные, нозокомиальные) —
развившиеся через 48 ч пребывания ребенка
в стационаре или в течение 48 ч после
выписки из стационара. Внутриутробные
пневмонии —
развившиеся в первые 72 ч после рождения.
85.
Клиника острой пневмонии у детей.
Дифференциальный диагноз с острым
простым обструктивным
бронхитом.
Клиника.
Основными
диагностическими (опорными) критериями
острой пневмонии является: кашель
(вначале сухой, затем влажный), одышка
(> 60 в мин.), участие
вспомогательной мускулатуры,
локальная
крепитация,
влажные разнокалиберные
хрипы, участки
укорочения
легочного звука,
инфильтративные тони на рентгенограмме,
повышение температуры
тела, явления
интоксикации. Могут быть бледность
кожи, цианоз
носогубного треугольника, нарушение
функции ССС, ЖКТ. односторонность
патологического процесса, локальное
укорочение перкуторного звука жёсткое,
ослабленное или бронхиальное дыхание
локальные, стабильные м/п влажные хрипы
или крепитация.
кашель с отделением
мокроты. Вызывается при действии на
болевые рцепторы пораженной тк – кашель
сочетается с болью.
Отставание
больной части грудной
клетки. Если
нижнедолевая пневмония – боли в животе,
клиника аппендицита. Одышка из-за
выпадения участка легкого, интоксикации.
Инспираторного характера. Лихорадка.
Слабость, нарушение общего состояния.
Перкуторно и аускультативно изменения
в легких (сначала появляются первкуторные,
а затем аускультативные изменения).
Локальное бронхиальное дыхание,
ослабление. Инспираторная крепитация
при аускультации. Мелкопузырчатые
хрипы. Усиление
голосового дрожания.
Если при осмотре
у ребенка независимо от уровня температуры
и при отсутствии обструкции имеется: —
учащение
дыхания: 60 в минуту
у детей первого месяца жизни; 50 в минуту
у детей 2—12 месяцев; 40 в минуту у детей
1—4 лет; — втяжение
межреберий; —
стонущее
(кряхтящее) дыхание;
— цианоз
носогубного треугольника;
— признаки токсикоза («больной» вид,
отказ
от еды и питья,
сонливость, нарушение сознания, резкая
бледность при повышенной температуре
тела), то состояние расценивается как
тяжелое с большой вероятностью
пневмонии.
Если у ребенка нет признаков,
указанных в пункте 1, но есть: — температура
тела 38 °С дольше 3 дней;
— локальные
физикальные признаки пневмонии;
— асимметрия
хрипов, то следует
предположить наличие пневмонии.
Если
ребенок с ОРЗ и признаками бронхиальной
обструкции имеет: — асимметрию хрипов;
— «воспалительную» гемограмму, то
следует исключить пневмонию проведением
рентгенологического исследования.
Госпитализации подлежат больные с
признаками дыхательной недостаточности.
S.
Pneumoniae.
Морфологическая форма:
Очаговая, очагово-сливная, долевая
(крупозная). Сливные очаги (часто в
верхней и нижней доле справа), инфильтрация
доли. Острое
начало, лихорадка с ознобом,
кашель;
при крупозной
— боль в боку, животе, покраснение щеки
на стороне поражения, ржавая мокрота,
герпес; укорочение перкуторного звука,
ослабление дыхания, крепитация; быстрая
(в течение 24—36 ч) положительная клиническая
реакция на пенициллин. Обструктивный
синдром не характерен.
ЛЕЧ.
Амоксициллин/клавуланат
per os — 50 мг/кг/сут.;
оспен per os — 100 мг/кг/сут. (препараты
назначают при лечении нетяжелых пневмоний
на дому); пенициллин в/в, в/м - 100-150 тыс
ед/кг/сут.; цефалоспорины 1 — 2 поколения
per os 30-4 0 мг/кг/сут. или в/в или в/м - 50-100
мг/кг/сут.; макролиды: эритромицин per os
- 40-5 0 мг/кг/сут. или в/в - 40-5 0 мг/кг/сут.;
азитромицин — 10-12 мг/кг/сут. в течение
5 дней
influenzae
типа В. До
3 лет; реже — дети более старшего возраста.
Очаговая, долевая инфильтрация.
Постепенное (реже острое) начало,
непродуктивный
кашель, высокая
лихорадка,
сопутствующий отит,
эпиглоттит, ларинготрахеит; возможен
обструктивный синдром. ЛЕЧ.
Амоксициллин/клавуланат
— per os — 40 мг/кг/сут. (нетяжелые формы);
цефазолин в/м, в/в - 50-100 мг/кг/сут.;
цефуроксим 75-150 мг/кг/сут. в/м,
в/в.
Streptococcus,
gr. А. 2—7 лет,
Очаговая, очагово-сливная;
округлые множественные (часто с обеих
сторон) очаги в разных фазах — от
инфильтрации до абсцесса; Острое
начало, лихорадка,
озноб; нет четких перкуторных данных;
хрипов
мало, сопутствующий
некротический трахеит, обструктивный
синдром не характерен; атриовентрикулярная
блокада при ЭКГ-исследовании, склонность
к затяжному течению. ЛЕЧ.
Пенициллин в/в, в/м —
100—150 тыс. ел./кг/сут.: цефалоспорины
1—2-го поколения per os 30-4 0 мг/кг/сут.; в/в.
в/м - 50—100 мг/кг/сут.; макролиды: эритромицин
per os — 40—50 мг/кг/сут.; в/в — 40—50 мг/кг/сут.;
азитромицин — 10—12 мг/кг/сут. в течение
5 дней.
Кишечная
флора: Е. Coli, Klebsiella, pneum., Pseudomonas aeruginosae.
Первые месяцы жизни;
ослабленные дети любого возраста.
Очаговая сливная инфильтрация средней
плотности в виде лучистости, без четких
границ, с мелкими множественными
полостями деструкции; Выраженная
интоксикация,
дыхательная
недостаточность,
обструктивный синдром, часто
двустороннее поражение;
«пестрая» аускультативная картина.
ЛЕЧ.
Амоксициллин/клавуланат — в/в — 90—120
мг/кг/сут.; цефалоспорины 3-го поколения:
клафоран, фортум — 75 — 150 мг/кг/сут.,
аминогликозиды: гентамицин в/м — 7,5
мг/кг/сут.; карбопенемы в/в - 60 мг/кг/сут.;
в тяжелых случаях фторхинолоны —
ципрофлоксацин в/в — 20 мг/кг/сут.
Mycoplasma
pneumoniae, Chlamydia pneumoniae.
Очаговая; негомогенная, часто двусторонняя
асимметричная инфильтрация, интерстициальная
реакция. Длительный инкубационный
период (1—3 нед.); постепенное
начало, катаральные явления со стороны
ВДП , конъюнктивит,
сухой
навязчивый кашель,
скудная мокрота, аускультативные
признаки бронхита, бронхиолита; затяжное
течение, длительный
субфебрилитет; «атипичная пневмония».
ЛЕЧ.
Макролиды per os: эритромицин per os - 40-5 0
мг/кг/сут.; в/в - 40-5 0 мг/кг/сут.; азитромицин
— 10—12 мг/кг/сут. в течение 5 дней;
тетрациклины — доксициклин у детей
старше 8 лет per os — 5 мг/кг/сут., в/в — 2,5
мг/кг/сут.
Chlamydia
trachomatis.
Новорожденные, первые 6 мес. Жизни.
Очаговая Обширная инфильтрация, вздутие
легких. Конъюнктивит, упорный кашель
«стаккато»; тахипноэ
без повышения температуры;
диффузные мелкопузырчагые
хрипы, обструкция
не характерна. ЛЕЧ.
Макролиды: эритромицин per os — 40—50
мг/кг/сут.; в/в — 40—50 мг/кг/сут.; азитромицин
per os — 10-12 мг/кг/сут. в течение 5 дней.
Диф.
С простым бронхитом:
развивается на высоте ОРВИ, кашель
сухой, затем влажный, t0 субфебрильная
или фебрильная, одышка отсутствует или
при физической нагрузке, перкуторно
над лёгкими коробочный оттенок звука,
аускультативно:
жёсткое дыхание, влажные и сухие хрипы
с обеих
сторон, в анализе
крови: лейкопения, лимфоцитоз,
СОЭ ― N
или незначительно повышена, Rг: усиление
лёгочного рисунка, нарушена структурность
корней.
С
обструктивным бронхитом:
развивается на фоне ОРВИ, чаще РС-инфекции,
t0 - суфребрильная или фебрильная, кашель
спастический,
с трудно
отделяемой мокротой,
одышка
в покое экспираторного
или смешанного характера, участие
вспомогательной мускулатуры,
перкуторно над лёгкими
— коробочный звук, аускультация: дыхание
жёсткое, выдох
удлинён с обеих сторон,
грубые сухие и
влажные хрипы, в
небольшом количестве – свистящие,
в анализе крови: лейкопения, лимфоцитоз,
СОЭ ― N
или незначительно повышена, Rг: усиление
лёгочного рисунка, эмфизематозное
вздутие лёгких, периваскулярные и
перибронхиальные изменения.
Для
бронхита характерен диффузный
характер физикальных данных
при удовлетворительном
общем состоянии детей,
тогда как при пневмонии выражены признаки
инфекционного
токсикоза,
значительно нарушено общее состояние.
Лихор более длительная, в периферической
крови выражены воспалительные изменения:
нейтрофильный
лейкоцитоз,
увеличение СОЭ. Рентгенологически
определяются локальные
инфильтративные изменения лёгочной
ткани.
86.
Лечение и профилактика острой пневмонии
у детей. Посиндромная терапия осложненной
пневмонии у детей раннего возраста.
Лечение.
• этиотропную терапию
при установленном диагнозе или при
тяжелом состоянии больного начинают
незамедлительно, при сомнении в диагнозе
у нетяжелого больного решение принимают
после рентгенографии;
Пневмококк
,стрептококк гемолитический:
пенициллины, в т.ч. ингибитор -
защищенные(ИЗП): ампициллина сульбактам,
амоксициллина клавуланат (амоксиклав)
цефалоспорины 1 и 2 поколения (цефалексин,
цефаклор),
макролиды.
Золотистый
стафилококк: -
пенициллины, в т.ч. ингибитор защищенный(ИЗП):
- ампициллина
сульбактам амоксициллина клавуланат
(амоксиклав), цефалоспорины I и II
поколения, макролиды в комбинации с
аминогликозидами (2пок – гентамицин, 3
пок - амикацин).
Гемофильная
палочка:
полусинтетические пенициллины, в т.ч.
ингибитор -защищенные (ИЗП), цефалоспорины
II и III поколения (цефаклор,
цефиксим).
Кокки,
палочки (гр. + и гр.- флора):
полусинтетические пенициллины, в т.ч.
ингибитор ― защищенные (ИЗП): - ампициллина
сульбактам , - оксициллина клавуланат
(амоксиклав).
Микоплазмы:
макролиды (сумамед, кларитромицин),
линкомицин, тетрациклин ( до 8 лет
противопоказан), в комбинации с
аминогликозидами.
Хламидии:
макролиды (сумамед, кларитромицин),
бактрим, бисептол, ориприм.
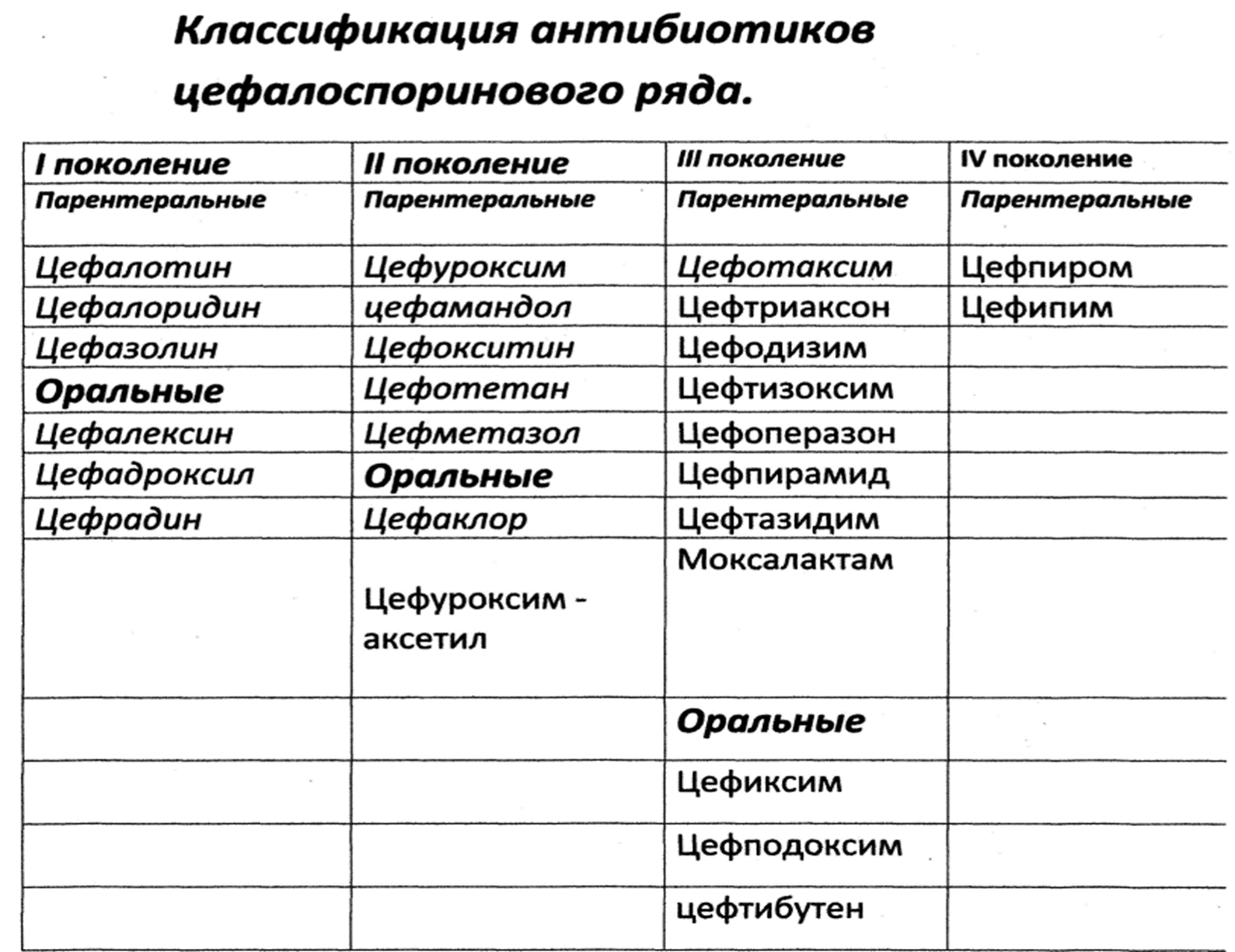 до
8 лет ― тетрациклины.
до 2 мес
-сульфаниламидные препараты (бактрим,
бисептол, ориприм).
до 1 года ―
ОСТОРОЖНО аминогликозиды.
• первичный
выбор антибиотика проводят эмпирически.
•
показаниями к переходу на альтернативные
препараты является отсутствие
клинического эффекта от препарата
первого выбора в течение 36—48 ч при
нетяжелой и 72 ч при тяжелой пневмонии;
развитие нежелательных побочных эффектов
от препарата первого выбора;
•
пневмококки устойчивы к гентамицину и
другим аминогликозидам, поэтому терапия
внебольничных пневмоний антибиотиками
данной группы недопустима;
• при
неосложненных нетяжелых пневмониях
следует отдавать предпочтение назначению
препаратов per os, заменяя их на парентеральное
введение при неэффективности; если
терапия была начата парентерально,
после снижения температуры следует
перейти на прием антибиотика per os;
•
после курса антибактериальной терапии
целесообразно назначить
биопрепараты.
Постельный
режим показан на
весь лихорадочный период. Питание
должно соответствовать возрасту и
обязательно быть полноценным.
•
Объем жидкости в сутки для детей до года
с учетом грудного молока или молочных
смесей составляет 140—150 мл/кг массы.
Целесообразно 1/3 суточного объема
жидкости давать в виде глюкозо-солевых
растворов (регидрон, оралит), что у 80—90%
больных позволяет отказаться от
инфузионной терапии.
• При необходимости
(эксикоз, коллапс, нарушение микроциркуляции,
угроза синдрома ДВС) в вену вводится
1/3 суточного объема. При избыточной
инфузии кристаллоидов возможно развитие
отека легких.
• В помещении, где
находится ребенок, должен
быть прохладный (18—19 °С), увлажненный
воздух, способствующий
урежению
и углублению дыхания, а
также снижающий потери воды.
•
Жаропонижающие
средства не назначают,
так как это может затруднить оценку
эффективости антибактериальной терапии.
Исключение составляют дети, имеющие
преморбидные показания для снижения
температуры тела.
• Показано
назначение СВЧ в остром периоде (10—12
сеансов), индуктотермии; электрофорез
с 3% раствором калия иодида.
•
Массаж и ЛФК необходимы сразу же после
нормализации температуры.
• В
стационаре детей помещают в отдельный
бокс. Ребенок может быть выписан из
стационара сразу же по достижении
клинического эффекта для того, чтобы
избежать перекрестной инфекции.
Сохранение увеличенной СОЭ , хрипов в
легких или остаточных рентгенологических
изменений не является противопоказанием
к выписке.
Профилактика.
—
комплексе социально-гигиенических
мероприятий;
— рациональном питании,
закаливании, улучшении экологии жилища;
— предупреждении ОРВИ, вакцинопрофилактике
пневмоний (конъюгированная вакцина
против Н. influenzae, пневмококка,
вакцинопрофилактика гриппа);
—
профилактике внутрибольничных пневмоний
(госпитализация в боксы).
Лечение
осложнений.
При
дыхательной
недостаточности
проводят кислородотерапию через носовые
канюли. Оптимальным методом оксигенотерапии
является спонтанная вентиляция
обогащенной кислородом газовой смесью
с положительным давлением в конце
выдоха. Обязательным условием успешной
оксигенотерапии является очищение
дыхательных путей после применения
муколитических средств,
стимуляция откашливания и/или удалением
мокроты при помощи отсоса.
Отек
легких обычно
развивается при избыточной инфузии
кристаллоидов, поэтому прекращение
инфузии —
предпосылка его лечения. При тяжелом
состоянии проводится ИВЛ в режиме
положительного давления на выдохе.
Внутрилёгочные
полости и абсцессы
после самоопроизвольного опорожнения
или хирургического вмешательства обычно
хорошо поддаются консервативному
лечению. Напряженные полости дренируют
либо проводят бронхоскопическую
окклюзию приводящего бронха.
Сердечная
недостаточность.
Из сердечных средств в экстренных
случаях вводят внутривенно строфантин
(0,1 мл 0,05% раствора
на год жизни) или коргликон
(по 0,1—0,15 мл 0,06%
раствора на год жизни). При
энергетически-динамической недостаточности
сердца показаны включение в терапию
панангина,
кортикостероиды используют как средство
борьбы с шоком, отеком мозга, кардиопатией,
отеком легкого и нарушением микроциркуляции.
Иммунотерапия направленного действия
проводится при тяжелых пневмониях
определенной этиологии (например,
стафилококковой).
ДВС-синдром
является показанием для назначения
свежезамороженной
плазмы, гепарина (по
100—250 ЕД/кг/сут. в зависимости от стадии).
гепарин в/в капельно или подкожно 200-400
ЕД/кг в сутки в 4 приема, реополиглюкин
15-20 мл/кг в сутки, гордокс ― 5000 ЕД/кг
сутки, контрикал ― 1000 ЕД/кг.
Препараты
железа при снижении
гемоглобина в остром периоде не назначают,
поскольку инфекционная анемия имеет
приспособительный характер и обычно
разрешается спонтанно на 3—4-й неделе
болезни. Гемотрансфузии проводят только
по жизненным показаниям при гнойном
деструктивном процессе у детей с
гемоглобином ниже 65 г/л, а также у
септических больных.
87.Деструктивная
пневмония. Этиология, патогенез.
Клинико-рентгенологическая картина у
детей.
Деструктивная
пневмония - патологическая
составляющая, хар-щаяся формированием
в легочной ткани абсцессов
и булл, склонных
к прорыву в плевральную полость с
развитием плевральных осложнений.
Этиология.
золотистый
стафилококк;
кишечная палочка; вирусы гриппа и
парагриппа; вульгарный протей.
Очень
часто заболевание возникает, как
осложнение респираторных инфекций. гемофильная
палочка, серотипы пневмококка, грамм
отриц. м/о-мы, клебсиелла, синегнойка,
стафилококк.
Возникновение плевритов,
особенно у детей раннего возраста,
обусловлено анатомо-физиологическими
и топографическими особенностями
плевры: малой подвижностью листков,
широкими синусами, обильной васкуляризацией,
густой сетью лимфатических сосудов,
тесной связью лимфатических сосудов
с лимфоузлами корня легких, средостения
и органов брюшной полости.
до
8 лет ― тетрациклины.
до 2 мес
-сульфаниламидные препараты (бактрим,
бисептол, ориприм).
до 1 года ―
ОСТОРОЖНО аминогликозиды.
• первичный
выбор антибиотика проводят эмпирически.
•
показаниями к переходу на альтернативные
препараты является отсутствие
клинического эффекта от препарата
первого выбора в течение 36—48 ч при
нетяжелой и 72 ч при тяжелой пневмонии;
развитие нежелательных побочных эффектов
от препарата первого выбора;
•
пневмококки устойчивы к гентамицину и
другим аминогликозидам, поэтому терапия
внебольничных пневмоний антибиотиками
данной группы недопустима;
• при
неосложненных нетяжелых пневмониях
следует отдавать предпочтение назначению
препаратов per os, заменяя их на парентеральное
введение при неэффективности; если
терапия была начата парентерально,
после снижения температуры следует
перейти на прием антибиотика per os;
•
после курса антибактериальной терапии
целесообразно назначить
биопрепараты.
Постельный
режим показан на
весь лихорадочный период. Питание
должно соответствовать возрасту и
обязательно быть полноценным.
•
Объем жидкости в сутки для детей до года
с учетом грудного молока или молочных
смесей составляет 140—150 мл/кг массы.
Целесообразно 1/3 суточного объема
жидкости давать в виде глюкозо-солевых
растворов (регидрон, оралит), что у 80—90%
больных позволяет отказаться от
инфузионной терапии.
• При необходимости
(эксикоз, коллапс, нарушение микроциркуляции,
угроза синдрома ДВС) в вену вводится
1/3 суточного объема. При избыточной
инфузии кристаллоидов возможно развитие
отека легких.
• В помещении, где
находится ребенок, должен
быть прохладный (18—19 °С), увлажненный
воздух, способствующий
урежению
и углублению дыхания, а
также снижающий потери воды.
•
Жаропонижающие
средства не назначают,
так как это может затруднить оценку
эффективости антибактериальной терапии.
Исключение составляют дети, имеющие
преморбидные показания для снижения
температуры тела.
• Показано
назначение СВЧ в остром периоде (10—12
сеансов), индуктотермии; электрофорез
с 3% раствором калия иодида.
•
Массаж и ЛФК необходимы сразу же после
нормализации температуры.
• В
стационаре детей помещают в отдельный
бокс. Ребенок может быть выписан из
стационара сразу же по достижении
клинического эффекта для того, чтобы
избежать перекрестной инфекции.
Сохранение увеличенной СОЭ , хрипов в
легких или остаточных рентгенологических
изменений не является противопоказанием
к выписке.
Профилактика.
—
комплексе социально-гигиенических
мероприятий;
— рациональном питании,
закаливании, улучшении экологии жилища;
— предупреждении ОРВИ, вакцинопрофилактике
пневмоний (конъюгированная вакцина
против Н. influenzae, пневмококка,
вакцинопрофилактика гриппа);
—
профилактике внутрибольничных пневмоний
(госпитализация в боксы).
Лечение
осложнений.
При
дыхательной
недостаточности
проводят кислородотерапию через носовые
канюли. Оптимальным методом оксигенотерапии
является спонтанная вентиляция
обогащенной кислородом газовой смесью
с положительным давлением в конце
выдоха. Обязательным условием успешной
оксигенотерапии является очищение
дыхательных путей после применения
муколитических средств,
стимуляция откашливания и/или удалением
мокроты при помощи отсоса.
Отек
легких обычно
развивается при избыточной инфузии
кристаллоидов, поэтому прекращение
инфузии —
предпосылка его лечения. При тяжелом
состоянии проводится ИВЛ в режиме
положительного давления на выдохе.
Внутрилёгочные
полости и абсцессы
после самоопроизвольного опорожнения
или хирургического вмешательства обычно
хорошо поддаются консервативному
лечению. Напряженные полости дренируют
либо проводят бронхоскопическую
окклюзию приводящего бронха.
Сердечная
недостаточность.
Из сердечных средств в экстренных
случаях вводят внутривенно строфантин
(0,1 мл 0,05% раствора
на год жизни) или коргликон
(по 0,1—0,15 мл 0,06%
раствора на год жизни). При
энергетически-динамической недостаточности
сердца показаны включение в терапию
панангина,
кортикостероиды используют как средство
борьбы с шоком, отеком мозга, кардиопатией,
отеком легкого и нарушением микроциркуляции.
Иммунотерапия направленного действия
проводится при тяжелых пневмониях
определенной этиологии (например,
стафилококковой).
ДВС-синдром
является показанием для назначения
свежезамороженной
плазмы, гепарина (по
100—250 ЕД/кг/сут. в зависимости от стадии).
гепарин в/в капельно или подкожно 200-400
ЕД/кг в сутки в 4 приема, реополиглюкин
15-20 мл/кг в сутки, гордокс ― 5000 ЕД/кг
сутки, контрикал ― 1000 ЕД/кг.
Препараты
железа при снижении
гемоглобина в остром периоде не назначают,
поскольку инфекционная анемия имеет
приспособительный характер и обычно
разрешается спонтанно на 3—4-й неделе
болезни. Гемотрансфузии проводят только
по жизненным показаниям при гнойном
деструктивном процессе у детей с
гемоглобином ниже 65 г/л, а также у
септических больных.
87.Деструктивная
пневмония. Этиология, патогенез.
Клинико-рентгенологическая картина у
детей.
Деструктивная
пневмония - патологическая
составляющая, хар-щаяся формированием
в легочной ткани абсцессов
и булл, склонных
к прорыву в плевральную полость с
развитием плевральных осложнений.
Этиология.
золотистый
стафилококк;
кишечная палочка; вирусы гриппа и
парагриппа; вульгарный протей.
Очень
часто заболевание возникает, как
осложнение респираторных инфекций. гемофильная
палочка, серотипы пневмококка, грамм
отриц. м/о-мы, клебсиелла, синегнойка,
стафилококк.
Возникновение плевритов,
особенно у детей раннего возраста,
обусловлено анатомо-физиологическими
и топографическими особенностями
плевры: малой подвижностью листков,
широкими синусами, обильной васкуляризацией,
густой сетью лимфатических сосудов,
тесной связью лимфатических сосудов
с лимфоузлами корня легких, средостения
и органов брюшной полости.
Патогенез. Начальные воспалительные изменения при бронхогенном пути проникновения инфекции обнаруживают в респираторных бронхиолах. Далее они распространяются на паренхиму легких. При кашле инфицированная слизь из очага воспаления попадает в крупные бронхи, а затем, распространяясь в другие респираторные бронхиолы, обусловливает новые очаги воспаления, т. е. распространение инфекции в легких может происходить бронхогенно. В участке клеточной инфильтрации возможно расплавление ткани с формированием абсцессов. Их опорожнение через бронх оставляет в легком полость, обычно заживающую небольшим рубцом. Прорыв абсцесса в плевральную полость ведет к пиопневмотораксу. Клиника. Ухудшение состояния на фоне ОРВИ , пиодермии, конъюнктивита, отита; одышка, стонущее дыхание, рвота, жидкий стул; звучные мелкопузырчатые хрипы, аускультативные признаки бронхита. сухим, а затем влажным кашлем с гнойной мокротой; синюшность носогубного треугольника при общей бледности кожных покровов; У заболевшего присутствует сердечно-сосудистая недостаточность, отмечается неприятный, запах изо рта, боль при дыхании и разговоре. РГ: в 2/3 случаев поражается правое лёгкое, негомогенный инфильтрат, который быстро увеличивается, частое развитие воздушных полостей (булл), обычно с уровнем жидкости, плеврит, пиопневмоторакс. 88.Клиника и диагностика деструктивной пневмонии. Особенности течения и лечения. I. 1) бронхогенная (первичная) - преимущественно односторонние очаги деструкции, единичные; 2) гематогенная (септическая), (вторичная) - следствие метастазирования из другого гнойно-септического очага, двустороннее поражение виде множественных мелких очагов. II. По локализации: 1) внутрилегочная (абсцессы, буллы); 2) легочно-плевральная - переход воспаления на плевру или в плевральную полость очагов деструкции; 3) медиастинальня форма. Клиника. Ухудшение состояния на фоне ОРВИ , пиодермии, конъюнктивита, отита; одышка, стонущее дыхание, рвота, жидкий стул; звучные мелкопузырчатые хрипы, аускультативные признаки бронхита. сухим, а затем влажным кашлем с гнойной мокротой; синюшность носогубного треугольника при общей бледности кожных покровов; У заболевшего присутствует сердечно-сосудистая недостаточность, отмечается неприятный, запах изо рта, боль при дыхании и разговоре. Диагностика: РГ: в 2/3 случаев поражается правое лёгкое, негомогенный инфильтрат, который быстро увеличивается, частое развитие воздушных полостей (булл), обычно с уровнем жидкости, плеврит, пиопневмоторакс. высокий лейкоцитоз (>20 х 10 9/л). выраженный нейтрофилёз со сдвигом влево. СОЭ более 40 мм/час. выраженная гипохромная анемия. Лечение: Золотистый стафилококк: - пенициллины, в т.ч. ингибитор защищенный(ИЗП): - ампициллина сульбактам амоксициллина клавуланат (амоксиклав), цефалоспорины I и II поколения, макролиды в комбинации с аминогликозидами (2пок – гентамицин, 3 пок - амикацин). Для устранения аллергических реакций на токсины, выделяемые микроорганизмами, назначают антигистаминные средства. В случае серьезных осложнений требуется оперативное вмешательство. Это может быть как пункция и дренаж, так и операция по удалению очага воспаления. После удаления гноя выполняют промывание пораженной области антисептическими растворами. Лечение пневмонии включает в себя как медикаментозное воздействие, так и ЛФК и физиопроцедуры. 89. Этиология, патогенез, клиника гриппа. Нейротоксикоз, неотложная помощь. Грипп (синонимы болезни: инфлюэнца) - острая инфекционная высококонтагиозная ЗООАНТРОПОНОЗНАЯ болезнь, вызывается вирусами гриппа, передается воздушно-капельным путем, характеризуется острым началом, коротким лихорадочным периодом, значительной интоксикацией, симптомами поражения слизистых оболочек верхних дыхательных путей и частыми осложнениями, преимущественно со стороны органов дыхания. Этиология. Возбудители гриппа — ортомиксовирусы (семейство Orthomyxoviridae) — РНК-содержащие сложноорганизованные вирусы. Семейство включает род Influenzavirus, содержащий вирусы 3 серотипов: А, В и С. Вирус гриппа А имеет два основных типа антигенов - гемагглютинин (Н, 11 подтипов) и нейраминидазу (N, 8 подтипов). Наиболее распространенной причиной сезонного гриппа являются вирусы подтипов H1N1 и H3N2 (H2N2 в некоторые сезоны), в меньшей степени вирусы гриппа B. Вирусы гриппа типа A характеризуются большой антигенной изменчивостью, что создает риск ежегодного заболевания и необходимость ежегодного обновления состава вакцины. В- большая стабильность, меньше вирулентность. С – не имеет нейраминидазы, Аг стабилен. Эпидемиология. Основной источник вируса — больной гриппом человек с клинически выраженной или стёртой формами течения заболевания. Механизм передачи вируса — аэрозольный. Путь передачи — воздушно- капельный. Роль воздушно-пылевого пути невелика. Больной человек уже в последние часы инкубационного периода и в первые 2-3 дня болезни выделяет огромное количество вируса в аэрозоле при дыхании, кашле, чиханье. На 4-7-й день от начала гриппа больные (реконвалесценты) уже незаразные. Возможно заражение через предметы, загрязнённые выделениями больного (игрушки, посуду, полотенца и др.). Вирус сохраняет свою жизнеспособность и вирулентность в жилых помещениях в течение 2–9 ч. Вирусы оставались жизнеспособными и вирулентными на руках человека в течение 5 мин. Патогенез. Попадая воздушно-пылевым или капельным путем с мелкими аэрозольными частицами на слизистые оболочки верхних дыхательных путей, вирус проникает в реснитчатые эпителиальные клетки, где происходит его репродукция. Вирусы гриппа А связываются через гемагглютинин с эпителиальными клетками верхних и нижних дыхательных путей, а затем пролиферируют в них, вызывая отек и некроз и десквамацию клеток эпителия трахеи, бронхов и бронхиол. Помимо реснитчатого эпителия, вирус гриппа может поражать альвеолярные макрофаги, бокаловидные клетки и альвеолоциты. Общие симптомы являются результатом действия цитокинов + интерферона, секреторные иммуноглобулины, освобождаемых во время воспалительной реакции. Через поврежденные эпителиальные барьеры вирус и продукты распада тканей проникают в кровоток, оказывая общетоксическое действие. Исключение составляет внелёгочная репликация вируса птичьего гриппа подтипа H5N1. Цикл репликации составляет 6–12 ч. По сравнению с обычными вирусами сезонного гриппа вирус A/H1N1pdm09 имеет более высокое сродство с эпителиальными клетками нижних дыхательных путей, он проникает глубже в дыхательные пути и поражает альвеолы. Возникают гемодинамические расстройства в различных органах и системах, что является ведущим звеном в патогенезе тяжелых форм болезни. Выраженные циркуляторные нарушения в ЦНС приводят к явлениям энцефалопатии, в легких — к сегментарному или распространенному геморрагическому отеку, в брыжейке — к абдоминальному синдрому. С самого начала- вирусемия и воздействие токсинов и аутотоксинов на ЦНС и ССС, поражая микроциркуляторное русло- расстройство микроциркуляции и гемостаза. Способствует активации аутофлоры и развитие бактериальных осложнений. Клиника. Тяжесть заболевания определяется выраженностью синдрома интоксикации (гипертермия), неврологических симптомов (головная боль, потеря сознания, судороги, менингеальные симптомы), геморрагического синдрома, нарушений сердечно-сосудистой деятельности. Грипп у новорожденных и детей первого года жизни. Заболевание обычно начинается постепенно с незначительного подъема температуры тела, симптомы гриппозной интоксикации отсутствуют или выражены неярко. Новорожденные отказываются от груди, у них снижается масса тела. Могут быть слабо выраженные катаральные явлений в виде кашля, заложенности носа, сопения, часто бывает повторная рвота. Синдром крупа у детей 1-го полугодия жизни развивается редко; сегментарное поражение легких нехарактерно. Несмотря на слабо выраженные начальные клинические проявления, течение гриппа у детей первого года жизни значительно более тяжелое в связи с частым присоединением бактериальной инфекции и возникновением гнойных осложнений (отит, пневмония и др.). Летальность в 3 раза выше, чем у детей старшего возраста. Для детей раннего возраста при гриппе характерно поражение всех отделов дыхательных путей, что в совокупности с несовершенством регуляторных механизмов создает условия для раннего появления дыхательной недостаточности и склонности к развитию пневмонии. Могут возникнуть явления ларингита, обусловленные отеком и спазмом гортани. Заболевание начинается остро, без продромальных признаков. В первые же часы температура становится высокой (38 °С и выше). У детей быстро появляются признаки инфекционного токсикоза: вялость, отказ от еды или рвота на высоте лихорадки у детей раннего возраста, нарушение сна. Дети школьного возраста могут отчетливо указать на такие признаки болезни, как головная боль (цефалгия в результате вовлечения в процесс тройничного нерва и барорецепторов) с характерной локализацией в области лба, висков и надбровных дуг, боль в глазных яблоках, особенно при движении глаз, светобоязнь, слезотечение, ломота в суставах, мышцах и костях, головокружение. Общая слабость, появляющаяся с самого начала болезни, прогрессивно нарастает. Ребенок выглядит апатичным и адинамичным, замкнутым, раздражительным, сонливым или, наоборот, возбужденным. Это признаки токсикоза с вовлечением центральной нервной системы (ЦНС). Лицо одутловато и гиперемировано, часто припухают нижние веки вследствие появления конъюнктивита. Наблюдаются инъекции сосудов склер. Изменение внешнего облика детей является результатом поражения шейных узлов симпатической нервной системы и сосудов головного мозга. Кожа влажная (общий гипергидроз), и это связано также с нарушением функционального состояния вегетативной НС. Головокружение и склонность к обморочным состояниям чаще всего наблюдаются у детей старшего возраста, рвота и понос — преимущественно в младшей возрастной группе. При тяжелой форме гриппа и выраженных циркуляторных расстройствах со стороны ЦНС может наблюдаться картина церебральной дисфункции: затемнение сознания, бред, галлюцинации, менингеальный симптомокомплекс при неизмененном ликворе (менингизм). У детей раннего возраста ежегодно регистрируются случаи отека-набухания головного мозга, ведущим признаком которого является церебральная недостаточность с синдромом угнетения сознания и судорог на фоне гипертермии Гриппозная интоксикация вызывает изменения со стороны сердечно-сосудистой системы. Сосудистые нарушения выражены преимущественно на уровне периферического кровообращения, что проявляется снижением тонуса мелких сосудов, повышением их проницаемости и ломкости. Отмечаются цианоз губ, слизистых оболочек, геморрагические проявления: носовые кровотечения, точечные геморрагии на мягком небе и даже на коже, кровоизлияния в конъюнктиву глаз. При тяжелой форме гриппа сосудистые расстройства наиболее выражены, что создает условия для застоя в капиллярной сети, возникновения отечного и геморрагического синдромов, развития дыхательной недостаточности вплоть до отека легких и мозга. Недостаточность кровообращения при гриппе у детей раннего возраста проявляется в виде централизации кровообращения и нарушении периферического кровотока («спазм периферии», или «белая гипертермия»). Клинически эта стадия проявляется тахикардией, артериальной гипертонией, бледностью и мраморностью кожных покровов. Применение сосудорасширяющих средств в сочетании с оксигенотерапией в этом случае приводит к нормализации периферического кровотока и температуры. Лихорадка и симптомы интоксикации при манифестных формах гриппа имеют две очень важные для диагностики особенности. Во-первых, температура тела быстро достигает высоких цифр и в первые два дня болезни всегда выше, чем на 3–4 дни. То же касается и интенсивности интоксикационного синдрома. Во-вторых, лихорадка при неосложненном гриппе всегда кратковременна. У большинства больных температурная реакция длится до 3 суток. Продолжительность лихорадки при неосложненном гриппе свыше 5–6 дней не встречается. Симптомы поражения дыхательных путей у детей появляются, как правило, на 1–2 дня позже начала общетоксических симптомов и выражены скудно: нос заложен, или имеются незначительные серозно-слизистые выделения, кашель сухой, болезненный. Таким образом, катаральный синдром при гриппе нередко запаздывает и из-за интоксикации как бы отступает на второй план. Нередки кровотечения из носа. Постоянным явлением при гриппе бывает гиперемия зева, легкая отечность дужек и язычка, мелкая зернистость задней стенки глотки. Дыхание, как правило, учащено даже при отсутствии осложнений. Типичным для гриппа является развитие трахеита с болями за грудиной. При аускультации характер дыхания обычно не изменяется, могут прослушиваться кратковременные сухие хрипы, иногда влажные. Это свидетельство гриппозного бронхита, и если он не гнойный, то поражения бронхов не могут рассматриваться как осложнение. Они возникают как результат гиперемии, набухания и усиления секреции слизистой оболочки бронхов. При рентгенологическом исследовании в ранние сроки бронхита наблюдается усиление сосудистого рисунка, расширение корней легких как следствие полнокровия и отека. Со стороны органов пищеварения отмечаются потеря аппетита, обложенный и нередко сухой язык, тошнота, иногда рвота, запор. У маленьких детей стул, наоборот, нередко становится жидким, они быстро теряют в весе. Иногда в первые дни болезни появляется абдоминальный болевой синдром, сопровождающийся рвотой и частым стулом при отсутствии явлений раздражения брюшины. Вирус гриппа не является энтеротропным, причиной возникновения диспепсического и болевого синдромов является токсическое поражение вегетативных отделов нервной системы. Печень и селезёнка при гриппе не увеличены. Нарушения мочеотделения при неосложнённой форме гриппа не возникают. Молниеносная форма заболевания с тяжёлым течением может закончиться смертью на 2–3-и сутки (развивается острый геморрагический отёк лёгких на фоне резкой интоксикации). С первых часов возникает высокая лихорадка, быстро нарастают одышка и цианоз. Появляется много кровянистой, иногда пенистой, мокроты. На рентгенограммах выявляют очаги затемнения округлой или неправильной формы. Приглушение перкуторного звука отсутствует или выражено незначительно. В последующие дни на фоне высокой температуры и резкой одышки нарастает ДН, развиваются гипоксическая кома и коллапс. Атипичные формы. Атипичная форма гриппа чаще встречающаяся в межэпидемический период и протекающая с клинической симптоматикой легкой формы гриппа без лихорадки и катаральных явлений. Явления интоксикации выражены слабо, температура тела либо остается нормальной (афебрильная форма), либо повышается не более 38 °С. В клинической картине болезни на первый план выступают симптомы ринита и фарингита. В случае, если воспалительный процесс локализуется в трахее при видимом отсутствии ринита и фарингита, речь идет о катаральной форме гриппа. Неотложка. Нейротоксикоз - токсическая энцефалопатия (воспалительное и токсическое поражение оболочек головного мозга с явлениями его отека), наиболее частый вариант токсикоза у детей, при котором доминируют неврологические расстройства на фоне прогрессирующей недостаточностей периферической гемодинамики; наиболее типичный; вариант течения периода генерализованной реакции. Это прежде всего неврологические расстройства, недостаточность периферического кровотока, нарушение терморегуляции. Нередко они сочетаются с дыхательной недостаточностью, признаками поражения почек, желудочно-кишечного тракта. Необходимо обеспечить приток свежего воздуха в помещение. Следует охладить голову с помощью пузыря со льдом. При судорогах надо придерживать больного, чтобы он не ударился, повернуть его голову набок для профилактики попадания содержимого желудка в дыхательные пути. При субфебрильной и фебрильной лихорадке - парацетамол 10-15 мг/кг или ибупрофен (детям старше 3 месяцев) 5-10 мг/кг внутрь, или per rectum. Перед транспортировкой больному вводят внутримышечно и внутривенно 60–80 мг фуросемида, 120 мг преднизолона, 1–2 мл 1%-ного раствора дифенгидрамина. Для устранения судорог вводят 20–60 мг диазепама. Для понижения температуры тела используют растворы ацетилсалициловой кислоты, метамизола натрия АНАЛЬГИН внутримышечно и внутривенно (по 0,5–2 мл). При ГИПЕРТЕРМИЧЕСКОМ СИНДРОМЕ: анальгин 50% раствор (из расчета 0,1-0,2 мл на 10 кг) + димедрол 1% раствор, или супрастин 2% раствор (из расчета: для детей до 7 лет – 0,1 мл на 1 год жизни, старше 7 лет – 1 мл) + 2% раствор папаверина или нош-пы (при спазме периферических сосудов) из расчета 0,1 мл/год жизни детям от 6 месяцев до 6 лет, по 2,0 мл для детей старше 6 лет. Детям до 6 месяцев папверин, но-шпа не водятся, или литическая смесь. физические методы охлаждения: - очистительная клизма с прохладной водой (t воды = 26-30С); - прохладная мокрая повязка на лоб; - холод на область крупных сосудов; - обтирание полуспиртовым раствором; - обдувание тела вентилятором. 5. При СУДОРОЖНОМ СИНДРОМЕ: в 20 мл 5% раствора глюкозы 0,5% раствор сибазона (диазепам, реланиум, седуксен) из расчета 0,2 мл/год жизни в/в медленно, оксибутират натрия 0,5 мг/кг в/в медленно, тиопентал натрия в разовой дозе 10 мг/кг под контролем ЧД, ЧСС, пульса на управляемой ИВЛ. 90. Клиника, осложнения и лечение гриппа у детей. Клиника. Тяжесть заболевания определяется выраженностью синдрома интоксикации (гипертермия), неврологических симптомов (головная боль, потеря сознания, судороги, менингеальные симптомы), геморрагического синдрома, нарушений сердечно-сосудистой деятельности. Грипп у новорожденных и детей первого года жизни. Заболевание обычно начинается постепенно с незначительного подъема температуры тела, симптомы гриппозной интоксикации отсутствуют или выражены неярко. Новорожденные отказываются от груди, у них снижается масса тела. Могут быть слабо выраженные катаральные явлений в виде кашля, заложенности носа, сопения, часто бывает повторная рвота. Синдром крупа у детей 1-го полугодия жизни развивается редко; сегментарное поражение легких нехарактерно. Несмотря на слабо выраженные начальные клинические проявления, течение гриппа у детей первого года жизни значительно более тяжелое в связи с частым присоединением бактериальной инфекции и возникновением гнойных осложнений (отит, пневмония и др.). Летальность в 3 раза выше, чем у детей старшего возраста. Для детей раннего возраста при гриппе характерно поражение всех отделов дыхательных путей, что в совокупности с несовершенством регуляторных механизмов создает условия для раннего появления дыхательной недостаточности и склонности к развитию пневмонии. Могут возникнуть явления ларингита, обусловленные отеком и спазмом гортани. Заболевание начинается остро, без продромальных признаков. В первые же часы температура становится высокой (38 °С и выше). У детей быстро появляются признаки инфекционного токсикоза: вялость, отказ от еды или рвота на высоте лихорадки у детей раннего возраста, нарушение сна. Дети школьного возраста могут отчетливо указать на такие признаки болезни, как головная боль (цефалгия в результате вовлечения в процесс тройничного нерва и барорецепторов) с характерной локализацией в области лба, висков и надбровных дуг, боль в глазных яблоках, особенно при движении глаз, светобоязнь, слезотечение, ломота в суставах, мышцах и костях, головокружение. Общая слабость, появляющаяся с самого начала болезни, прогрессивно нарастает. Ребенок выглядит апатичным и адинамичным, замкнутым, раздражительным, сонливым или, наоборот, возбужденным. Это признаки токсикоза с вовлечением центральной нервной системы (ЦНС). Лицо одутловато и гиперемировано, часто припухают нижние веки вследствие появления конъюнктивита. Наблюдаются инъекции сосудов склер. Изменение внешнего облика детей является результатом поражения шейных узлов симпатической нервной системы и сосудов головного мозга. Кожа влажная (общий гипергидроз), и это связано также с нарушением функционального состояния вегетативной НС. Головокружение и склонность к обморочным состояниям чаще всего наблюдаются у детей старшего возраста, рвота и понос — преимущественно в младшей возрастной группе. При тяжелой форме гриппа и выраженных циркуляторных расстройствах со стороны ЦНС может наблюдаться картина церебральной дисфункции: затемнение сознания, бред, галлюцинации, менингеальный симптомокомплекс при неизмененном ликворе (менингизм). У детей раннего возраста ежегодно регистрируются случаи отека-набухания головного мозга, ведущим признаком которого является церебральная недостаточность с синдромом угнетения сознания и судорог на фоне гипертермии Гриппозная интоксикация вызывает изменения со стороны сердечно-сосудистой системы. Сосудистые нарушения выражены преимущественно на уровне периферического кровообращения, что проявляется снижением тонуса мелких сосудов, повышением их проницаемости и ломкости. Отмечаются цианоз губ, слизистых оболочек, геморрагические проявления: носовые кровотечения, точечные геморрагии на мягком небе и даже на коже, кровоизлияния в конъюнктиву глаз. При тяжелой форме гриппа сосудистые расстройства наиболее выражены, что создает условия для застоя в капиллярной сети, возникновения отечного и геморрагического синдромов, развития дыхательной недостаточности вплоть до отека легких и мозга. Недостаточность кровообращения при гриппе у детей раннего возраста проявляется в виде централизации кровообращения и нарушении периферического кровотока («спазм периферии», или «белая гипертермия»). Клинически эта стадия проявляется тахикардией, артериальной гипертонией, бледностью и мраморностью кожных покровов. Применение сосудорасширяющих средств в сочетании с оксигенотерапией в этом случае приводит к нормализации периферического кровотока и температуры. Лихорадка и симптомы интоксикации при манифестных формах гриппа имеют две очень важные для диагностики особенности. Во-первых, температура тела быстро достигает высоких цифр и в первые два дня болезни всегда выше, чем на 3–4 дни. То же касается и интенсивности интоксикационного синдрома. Во-вторых, лихорадка при неосложненном гриппе всегда кратковременна. У большинства больных температурная реакция длится до 3 суток. Продолжительность лихорадки при неосложненном гриппе свыше 5–6 дней не встречается. Симптомы поражения дыхательных путей у детей появляются, как правило, на 1–2 дня позже начала общетоксических симптомов и выражены скудно: нос заложен, или имеются незначительные серозно-слизистые выделения, кашель сухой, болезненный. Таким образом, катаральный синдром при гриппе нередко запаздывает и из-за интоксикации как бы отступает на второй план. Нередки кровотечения из носа. Постоянным явлением при гриппе бывает гиперемия зева, легкая отечность дужек и язычка, мелкая зернистость задней стенки глотки. Дыхание, как правило, учащено даже при отсутствии осложнений. Типичным для гриппа является развитие трахеита с болями за грудиной. При аускультации характер дыхания обычно не изменяется, могут прослушиваться кратковременные сухие хрипы, иногда влажные. Это свидетельство гриппозного бронхита, и если он не гнойный, то поражения бронхов не могут рассматриваться как осложнение. Они возникают как результат гиперемии, набухания и усиления секреции слизистой оболочки бронхов. При рентгенологическом исследовании в ранние сроки бронхита наблюдается усиление сосудистого рисунка, расширение корней легких как следствие полнокровия и отека. Со стороны органов пищеварения отмечаются потеря аппетита, обложенный и нередко сухой язык, тошнота, иногда рвота, запор. У маленьких детей стул, наоборот, нередко становится жидким, они быстро теряют в весе. Иногда в первые дни болезни появляется абдоминальный болевой синдром, сопровождающийся рвотой и частым стулом при отсутствии явлений раздражения брюшины. Вирус гриппа не является энтеротропным, причиной возникновения диспепсического и болевого синдромов является токсическое поражение вегетативных отделов нервной системы. Печень и селезёнка при гриппе не увеличены. Нарушения мочеотделения при неосложнённой форме гриппа не возникают. Молниеносная форма заболевания с тяжёлым течением может закончиться смертью на 2–3-и сутки (развивается острый геморрагический отёк лёгких на фоне резкой интоксикации). С первых часов возникает высокая лихорадка, быстро нарастают одышка и цианоз. Появляется много кровянистой, иногда пенистой, мокроты. На рентгенограммах выявляют очаги затемнения округлой или неправильной формы. Приглушение перкуторного звука отсутствует или выражено незначительно. В последующие дни на фоне высокой температуры и резкой одышки нарастает ДН, развиваются гипоксическая кома и коллапс. Атипичные формы. Атипичная форма гриппа чаще встречающаяся в межэпидемический период и протекающая с клинической симптоматикой легкой формы гриппа без лихорадки и катаральных явлений. Явления интоксикации выражены слабо, температура тела либо остается нормальной (афебрильная форма), либо повышается не более 38 °С. В клинической картине болезни на первый план выступают симптомы ринита и фарингита. В случае, если воспалительный процесс локализуется в трахее при видимом отсутствии ринита и фарингита, речь идет о катаральной форме гриппа. Осложнения. Ни при одном инфекционном заболевании не встречается такого большого процента осложнений, как при гриппе (10%), при этом может возникнуть поражение любого органа токсического либо воспалительного характера. При всем клиническом многообразии ведущее положение среди осложнений гриппа у детей занимают пневмонии (80–90%). Второе по частоте место занимают осложнения со стороны ЛОР-органов (гнойный ринит, синусит, отит, ангина и т. д.), реже — гнойный менингит, пиелонефрит и другие заболевания внутренних органов. Трахеобронхит в первые дни заболевания гриппом является его основным проявлением, но изменение характера мокроты на гнойный уже свидетельствует о присоединении вторичной бактериальной инфекции. Отек мозга, легких, ДВС-синдрома (диссеминированное внутрисосудистое свертывание) интерстициальную пневмонию, невриты, отит, энцефалит и прочие токсические осложнения (сюда же можно отнести синдром Рея, синдром Уотерхауза–Фридериксена). Третья группа осложнений связана с аллергизирующим действием вируса антигенами, образующимися вследствие деструкции в органах и тканях, — менингоэнцефалит, миокардит, полирадикулоневрит и др. У детей возможно развитие гемолитико-уремического синдрома (синдрома Гассера), а также синдрома острой коронарной недостаточности (синдрома Гиша). Лечение. Базисная терапия проводится до исчезновения клинических симптомов и включает:
Постельный режим на период лихорадки.
Молочно-растительную диету, обогащенную витаминами.
Обильное питье в виде горячего чая, настоя шиповника, клюквенного или брусничного морса, щелочных минеральных вод. Суточный объем жидкости для детей раннего возраста должен составлять на период лихорадки 150 мл/кг массы тела, для детей старше 3 лет — 80 мл/кг массы тела.
Жаропонижающие препараты в возрастных дозах.
Так, суспензия (100 мг ибупрофена в 5 мл), которая имеет хорошие вкусовые качества, охотно принимается детьми раннего возраста (отсутствуют сахар, алкоголь и искусственные красители). При отказе ребенка от еды, наличии тошноты, синдрома рвоты и срыгивания возможно использование препарата в форме ректальных свечей (60 мг ибупрофена в свече). 5. Противокашлевую терапию. Показана для снижения вязкости мокроты и повышения мукоцилиарного клиренса, что улучшает дренажную функцию бронхов. Для стимуляции отхаркивания применяют Мукалтин или корень солодки или настойку алтея. Лекарственные растения оказывают мягкое терапевтическое действие, усиливая эффективность комплексной терапии, имеют незначительные побочные эффекты. 6. Муколитические препараты. относятся бромгексин, амброксол, ацетилцистеин. Противокашлевые средства (центрального действия) при повышенном кашлевом рефлексе, сухом непродуктивном навязчивом кашле: наркотические (кодеин) и ненаркотические (Синекод). Комбинированный препарат Коделак фито, в состав которого входят кодеин в субтерапевтической дозе и экстракты лекарственных трав (термопсис, солодка, чабрец), оказывает комплексное противокашлевое, отхаркивающее, противовоспалительное действие. При остром фаринготрахеите и бронхите и непродуктивном навязчивом кашле применяются ингаляции (можно назначать детям старше 2 лет и взрослым в первые дни болезни), 1%-м раствором натрия бикарбоната или щелочных минеральных вод типа «Боржоми»). Небулайзерная терапия (можно назначать детям грудного и раннего возраста и старше) в первые дни болезни с изотоническим раствором хлорида натрия, т. к. при гриппе больше выражено поражение крупных бронхов; 7. Аскорбиновую кислоту или поливитамины. Этиотропная терапия Этиотропная терапия включает химиопрепараты (рибавирин, римантадин, осельтамивир, занамивир), индукторы интерферонов (Кагоцел, Циклоферон, Арбидол), сами интерфероны и иммуноглобулины для парентерального применения. При среднетяжелых и тяжелых формах применяют Ремантадин по 50 мг 2 раза в день (детям от 3 до 10 лет) и по 50 мг 3 раза в день (детям старше 10 лет и взрослым). Ремантадин обладает активностью только по отношению к вирусу гриппа А. Занамавир в ингаляциях, осельтамивир подавляют нейраминидазу вируса гриппа А и В и практически блокируют размножение вируса и попадание его в кровь и, таким образом, уменьшают выраженность токсикоза. Донорский нормальный иммуноглобулин с высоким содержанием противогриппозных антител назначают при тяжелой форме гриппа детям младше 2 лет однократно в дозе 1,5 мл, от 3 до 7 лет — 3 мл, старше 7 лет — 4,5 мл, взрослым по 6 мл. При гипертоксической форме дозу иммуноглобулина можно повторить через 12 часов. Антибактериальная терапия Назначается при наличии бактериальных осложнений или в тех случаях, когда трудно исключить возможность их возникновения (у детей раннего возраста, при наличии хронических очагов инфекции, при тяжелой форме гриппа). Обычно используют аминопенициллины, макролиды, цефалоспорины перорально или внутримышечно. При тяжелых бактериальных осложнениях назначают препараты широкого спектра действия — цефалоспорины 3-го и 4-го поколений, респираторные фторхинолоны, имипенемы в различных сочетаниях. 91. Клинические проявления энтеровирусной инфекции у детей. Энтеровирусная инфекция – это группа острых инфекционных болезней, вызываемые кишечными вирусами (энтеровирусами), характеризующихся лихорадкой и полиморфизмом клинических симптомов. Энтеровирусы – это целая группа вирусов, относящихся к семейству пикорнавирусов. Все подобные вирусы являются РНК-содержащими. Это означает, что их генетическая информация заключена в молекуле РНК, а не в молекуле ДНК, как у подавляющего большинства других живых существ, в том числе, и вирусов. Существует несколько разновидностей энтеровирусов, из которых следует выделить эховирусы и вирусы Коксаки. Кроме того, к роду энтеровирусов относятся полиовирусы, вызывающие полиомиелит. Вирусы Коксаки представляют собой несколько серотипов вирусов, относящихся к трем видам рода Enterovirus: A, В и С. Вирусы Коксаки типа А вызывают такие тяжелые энтеровирусные заболевания, как герпетическая ангина, геморрагический конъюнктивит, асептический менингит. Эховирусы представляют большую опасность для новорожденных детей, так как могут вызвать у них миокардит, менингит и гепатит, что нередко приводит к смерти малышей. У детей старшего возраста и взрослых при заражении эховирусами заболевание протекает без осложнений. Энтеровирусы передаются различными путями. Наиболее распространенными из них являются:
воздушно-капельный (при чихании, кашле, разговоре),
бытовой (через предметы, которыми пользуется сразу несколько людей),
орально-фекальный (через немытые руки, загрязненную пищу и воду).
вертикальный путь передачи (от инфицированной беременной женщины к ребенку);
Особенностью энтеровирусных инфекций является то, что они чаще всего встречаются в летние и осенние месяцы, а не зимой или весной, когда происходят основные вспышки заболеваний. Примерно 80-90% заболевших энтеровирусными инфекциями составляют дети. Из них половина – дети дошкольного возраста. Наибольшую опасность заболевание представляет для детей до 3 лет. Энтеровирусная инфекция у детей может принимать разнообразные формы – от кишечных и респираторных до поражения нервной системы и сердца. По причине того, что энтеровирусы поражают многие ткани и органы человеческого организма (центральную нервную систему, сердце, печень, легкие, почки и другие органы),заболевание имеет разнообразные проявления. Заболевание начинается остро, с подъема температуры тела до 39° - 40°С. Появляется слабость, головная боль, рвота, боли в животе, судорожный синдром, насморк. Может отмечаться энтеритная диарея (понос). В случае, если входные ворота инфекции – носоглотка, развивается респираторная форма заболевания, среди симптомов которой - кашель, насморк, повышение температуры; возможны кишечные расстройства. Герпангина (энтерови́русный везикуля́рный фаринги́т): мелкие язвочки на задней стенке глотки, нёбе и реже на миндалинах, сопровождающиеся высокой температурой. Глотание при такой форме энтеровирусной инфекции болезненное. Для герпангины также характерно увеличение и болезненность подчелюстных и шейных лимфатических узлов, а также гиперсаливация (слюнотечение). Энтеровирусная экзантема: подъем температуры тела, слабость, головная боль. Через 1-2 дня на конечностях, туловище, в полости рта появляются различные по характеру высыпания. Один из вариантов энтеровирусной экзантемы - синдром « рука-нога-рот»: сыпь на лице, ладонях, стопах, во рту. Через 3-5 суток сыпь исчезает. В большинстве случаев кожные элементы исчезают через 2-3 дня; на месте их разрешения отмечается шелушение кожи, а верхние слои сходят большими фрагментами. Входные ворота – желудочно-кишечный тракт - острое начало: рвота, жидкий стул, подъем температуры. Гастроэнтерит. боли в абдоминальной области (чаще – справа); общая слабость и повышенная утомляемость; увеличение газообразования в кишечнике; Ещё одним вариантом энтеровирусной инфекции является лихорадочная форма, единственный симптом которой - высокая температура до 40о С. Других проявлений не наблюдается. Обратите внимание: при энтеровирусном конъюнктивите вначале поражается один глаз, но вскоре воспалительный процесс распространяется и на второй. При попадании вируса с током крови или лимфы на твердую мозговую оболочку развивается менингит:
Судороги;
Боль в глазных яблоках;
Нарушение сознания;
Тахикардия и другие аритмии.
Менингеальные симптомы сохраняются от 2 дней до полутора недель. В спинномозговой жидкости вирус может обнаруживаться в течение 2-3 недель. 92. Клинические проявления аденовирусной инфекции у детей. Гипертермический синдром, неотложная помощь. Аденовирусная инфекция — группа острых вирусных заболеваний, проявляющихся поражением слизистых оболочек дыхательных путей, глаз, кишечника и лимфоидной ткани преимущественно у детей и лиц молодого возраста. Аденовирусы, которые вызывают заболевание у детей, относятся к семейству Adenoviridae, роду Mastadenovirus ДНК-содержащих вирусов средних размеров. В настоящее время выделено около 50 серотипов этого вируса. Наиболее частыми возбудителями аденовирусной инфекции являются 3-й и 7-й серотипы. Источником инфекции является больной или вирусоноситель, пути передачи — воздушно-капельный, водный («болезнь плавательных бассейнов»), а также фекально-оральный. Наиболее восприимчивы к этому вирусу дети от 6 месяцев до 3 лет. АВ регистрируют повсеместно и круглогодично с подъемом заболеваемости в холодное время года. Инфекция распространяется при кашле или чихании. Капли, содержащие вирус, разлетаются по воздуху и приземляются на поверхности. Патогномоничная форма аденовирусной инфекции — аденофарингоконъюнктивальная лихорадка. Она протекает с подъемом температуры тела до 38–39 °С на протяжении 5–10 дней, фарингитом с зернистостью задней стенки глотки, увеличением и гиперемией миндалин, конъюнктивитом. Нередко развивается тонзиллит, проявляющийся гипертрофией, отечностью и умеренной гиперемией миндалин, а также аденоидит. В ряде случаев на задней стенке глотки, небных миндалинах появляются нежные белесоватые налеты (пленчатый фарингит и тонзиллит). Характерным для аденовирусной инфекции является синдром полиаденита — увеличение шейных и подчелюстных лимфатических узлов. Наблюдается увеличение печени и селезенки. Длительность катарального синдрома — 10–15 дней, иногда до 3–4 недель. вялость, слабость, головная боль; кашель (вначале сухой, а на 3–4 день влажный с отхождением мокроты), отечность миндалин и точечный гнойный налет на них; нарушения сна, общая слабость, вялость, бледность, повышенная раздражительность; О том, что перед нами именно аденовирус, чаще всего свидетельствует конъюнктивит, который сопровождает заболевание в большинстве случаев. Глаза болят, слезятся, краснеют, появляется ощущение насыпанного песка. Пострадать могут оба глаза или только один — зависит от индивидуального характера протекания заболевания. Второй отличительной особенностью аденовирусной инфекции является то, что период интоксикации продолжается всего 1–2 дня, в то время как неприятные симптомы (тошнота, головная боль, слабость и другие) при гриппе могут сохраняться до 7 суток и более. Третьим отличием аденовируса от других вирусных инфекций является длительность и характер лихорадки. Температура при аденовирусной инфекции может подниматься в первый день до 38°С, но держится высокой недолго. Если при гриппе лихорадка продолжается несколько дней, а температура достигает 39–40°С, то при аденовирусе изматывающая лихорадка отмечается достаточно редко. конъюнктивит — воспаление слизистой оболочки глаз; кератоконъюнктивит — сухость слизистой глаза, ощущение рези в глазах; ринофарингит — воспаление слизистой носа и глотки; ринофарингобронхит — к воспалению слизистых дыхательных путей добавляется воспаление бронхов; ринофаринготонзиллит — поражение слизистых дыхательных путей сопровождается воспалением миндалин; мезентериальный лимфаденит — воспаление лимфатических узлов живота. У детей аденовирус имеет свои, более выраженные, проявления. Так как новорожденные имеют остаточный иммунитет к вирусу, у них болезнь протекает при невысокой температуре, редко наблюдается конъюнктивит, не увеличиваются лимфоузлы. У детей первого года жизни нередко развивается пневмония. под действием аденовируса легкие ребенка становятся более восприимчивыми к бактериальным возбудителям этого серьезного заболевания. Пневмония сопровождается хрипами, у ребенка могут начаться судорожные припадки, одышка, рвота. Неотложка. Гипертермический синдром – это патологический вариант лихорадки, при котором отмечается быстрое и неадекватное повышение температуры тела, сопровождающееся нарушением микроциркуляции и дисфункцией жизненно важных органов и систем. 1. Красная гипертермия. Чувство жара. Кожа розовая, горячая, конечности тёплые, усиленное потоотделение. Учащение пульса и дыхания соответствует повышению температуры (на каждый градус свыше 37оС ЧСС увеличивается на 20 ударов в минуту, а ЧДД на 4 дыхания). Поведение ребёнка обычное.
2. Белая гипертермия. Озноб, чувство холода. Бледность, мраморность кожи. Конечности холодные. Пульс слабый, тахикардия. Одышка. Нарушения поведения ребёнка: безучастность, вялость или двигательное и речевое возбуждение, возможны бред и судороги. Возможна смерть на фоне асфиксии. Алгоритм неотложной помощи. Снижению подлежит температура выше 38,5оС; у детей с отягощённым анамнезом (судороги, патология ЦНС, порок сердца и т.п.) температура выше 38,0оС. 2. Если кожные покровы гиперемированы («красная лихорадка»), необходимо развернуть, раздеть ребенка, протереть кожные покровы 40° спиртовым раствором или завернуть ребенка во влажную пеленку, возможно использование обдувания вентилятором; применение очистительной клизмы с прохладной водой (приблизительно комнатной температуры, т.е. 18–20 °С).
3. Если кожные покровы бледные («бледная лихорадка»), перед применением физических методов охлаждения необходимо назначить никотинамид в дозировке 0,005–0,01 г, с периодичностью приема до 2–3 раз в течение 24 часов. физические методы охлаждения не применяют. При любой гипертермии: 3. Для увеличения теплоотдачи – физические методы охлаждения: - растирание кожи водно-спиртово-уксусной смесью, в состав которой входит вода, 40% этиловый спирт, 9% раствор уксуса в пропорции 1:1:1; 3. Обеспечить обильным тёплым питьём. 4. Приготовить лекарственные средства: парацетамол (панадол, калпол и т.п.) для энтерального введения - 50% раствор анальгина. - 1% раствор димедрола (2% раствор супрастина). - 2% раствор папаверина (2% раствор но-шпы). - 0,25% раствор дроперидола. 93. Парагриппозная инфекция у детей. Клиника, осложнения, лечение. Вирусы парагриппа – парамиксовирусы типов 1, 2, 3 и 4. У них имеется антигенная перекрестная реактивность, но они склонны вызывать болезни различной тяжести. Тип 4 обладает антигенной перекрестной реактивностью с вирусом паротита и не является, как правило, причиной респираторного заболевания. Вирус парагриппа нестоек во внешней среде. Через 2—4 ч пребывания при комнатной температуре он теряет инфекционные свойства. Источником парагриппозной инфекции является больной человек. Распространяется инфекция воздушно-капельным путем. Большинство авторов указывают на преимущественное поражение парагриппозной инфекцией детей первых лет жизни. Клиника. Характерным для парагриппозной инфекции является выраженный катар дыхательных путей (ринит, упорный кашель), появляющийся с первых часов заболевания. Сочетание первичного инфекционного токсикоза, нередко наблюдающегося в первые часы парагриппозного заболевания, с выраженными катаральными симптомами является особенностью парагриппа, отличающей его от гриппа. Как на особенность парагриппа указывают также на ларингиты и фарингиты, с большой частотой сопровождающие эту инфекцию. Отмечается упорный, грубый сухой кашель, боли в горле, насморк, заложенность носа. Выделения из носа сначала слизистые, позже могут стать слизисто-гнойными. При осмотре ротоглотки отмечают отечность, умеренную гиперемию слизистой оболочки, дужек, мягкого неба, задней стенки глотки, иногда обнаруживается экссудативный гнойный выпот в лакунах. В этих случаях среди полного здоровья ребенок неожиданно просыпается ночью от грубого, лающего кашля. Быстро присоединяются охриплость голоса, шумное дыхание и развивается стеноз гортани. Однако при парагриппе стеноз редко достигает II и еще реже — 3 степени. У большинства бывших под наблюдением больных (преимущественно в возрасте старше 2 лет) начало заболевания было острым и сопровождалось более или менее выраженными симптомами токсикоза: внезапным повышением температуры, нарушением общего состояния, вялостью, сонливостью, потерей аппетита, у некоторых больных рвотой. Почти все дети жаловались на головную боль, боли в горле. У 14% из них наблюдались признаки нейротоксикоза с кратковременными судорогами. Однако симптомы токсикоза при парагриппозной инфекции были выражены значительно слабее, чем при гриппе. Температурная реакция обычно была умеренной (38—38,5°), реже достигала -39° и выше, держалась кратковременно (2—3 дня), снижалась литичеаки, у некоторых детей с более или менее продолжительным субфебрилитетом. Повторные температурные волны, возникавшие за счет реактивизации основного процесса, возникали у детей после 1—2 дней апирексии, не вызывая значительного ухудшения общего состояния и усиления катаральных явлений. Тип 1 парагриппа чаще вызывает круп (ларинготрахеобронхит— Круп), прежде всего среди младенцев в возрасте 6–36 мес. Круп начинается с симптомов простуды. Позже развиваются лихорадка, лающий кашель, хрипота и свистящее дыхание. Дыхательная недостаточность из-за обструкции верхних дыхательных путей – редкое, но потенциально летальное осложнение. Вирус парагриппа типа 3 может вызвать пневмонию и бронхиолит среди младенцев ( Бронхиолит). Эти болезни в общем не отличаются от болезней, вызываемых респираторным синцитиальным вирусом (см. ниже), но часто менее серьезны. В остром периоде парагриппозной инфекции, протекающей без осложнений, над легкими определяется тимпанический оттенок перкуторного звука, аускультативно обнаруживаются жесткое дыхание, рассеянные сухие хрипы. В последующие дни аускультативные данные становятся богаче: наряду с сухими выслушиваются крупные влажные хрипы, количество которых нередко нарастает. Наличие хрипов и их длительность являются характерными симптомами парагриппозной инфекции: кашель и разнообразные хрипы нередко выслушиваются до 2—3 недель. Осложнения. К наиболее частым осложнениям относятся пневмония, обусловленная вторичной бактериальной флорой. У детей в первые годы жизни иногда возникает круп, обусловленный отеком и воспалительной инфильтрацией слизистой оболочки гортани, скоплением секрета в ее просвете и рефлекторным спазмом мышц – сложно дышать, стеноз. Лечение. Назначают постельный режим и симптоматические средства. Питание должно быть полноценным, легкоусвояемым, без существенного ограничения пищевых ингредиентов. Пищу дают в теплом виде. Специфического лечения парагриппа нет. Пациентам назначают противовирусные препараты, иммуномодуляторы. При температуре более 38,5°С назначают жаропонижающие средства. При кашле назначают отхаркивающие средства и препараты, разжижающие мокроту. При насморке назначают сосудосуживающие средства. Однако их нельзя применять дольше 5-7 дней. Кроме того, полезно промывать нос раствором морской соли. Широко используется при лечении парагриппа фитотерапия – потогонные (малина, липа), отхаркивающие (солодка, мать-и-мачеха), противовоспалительные (ромашка, шалфей, эвкалипт, календула) средства. Комнату страдающего парагриппом нужно обязательно проветривать несколько раз в день. Также необходима ежедневная влажная уборка. Назначение антибиотиков оправдано при тяжелых формах бронхита и пневмонии. В тяжелых случаях болезни применяется донорский иммуноглобулин. 94. Острый стенозирующий ларинготрахеит у детей. Этиология, патогенез, клиника, дифференциальный диагноз, лечение. Неотложная помощь. Анатомо-физиологические особенности строения гортани, особенности реактивности у детей с экссудативно-катаральной и лимфатико-гипопластической аномалиями конституции, аллергическим диатезом предрасполагают к развитию СЛТ — ложного крупа, который является основной причиной острой обструкции верхних дыхательных путей у детей от 6 месяцев до 3 лет. При вирусной этиологии стеноза преобладают отечно-инфильтративные изменения слизистой. При аллергической — отечные. При вирусно-бактериальной и бактериальной этиологии заболевания возможно развитие обтурационной формы СЛТ вследствие возникновения нисходящего бактериального фибринозного воспаления. 1. Острые респираторно-вирусные заболевания (парагрипп, грипп, аденовирусная инфекция, риносинцитиальная инфекция и др.). 2. Бактериальные инфекции (стрептококковая, стафилококковая и др.). 3. Аллергические реакции немедленного типа (отек Квинке, анафилактический шок). Патогенез. острого ларинготрахеита как синдрома ОРВИ связан с воздействием вирусов на слизистую оболочку дыхательных путей, в результате возникает ее отек и инфильтрация, спазм мышц гортани, скопление густого слизистого или слизисто-гнойного экссудата в просвете дыхательных путей. Это самые важные три звена патогенеза приводят к обструкции просвета гортани. Отек и инфильтрация слизистой оболочки подголосового отдела гортани приводят к его сужению. Из-за воспалительного экссудата в гортани (серозного, слизистого, гнойного) появляется кашель, нарастает спазм мышц гортани, в результате чего стеноз гортани усугубляется, а гипоксия становится более выраженной. Компенсация дыхания достигается сначала урежением и углублением дыхательных движений, затем – их учащением, участием вспомогательной дыхательной мускулатуры, дыханием через рот, что нарушает качество вдыхаемого воздуха (уменьшает его влажность, температуру). Это приводит к увеличению повреждения слизистых оболочек, прежде всего в месте наибольшего сужения – подголосовой области. Выделяющаяся в дыхательных путях слизь становится вязкой, трудно отделяется, усиливая стеноз. Работа вспомогательных мышц, сопровождаясь выделением тепла, быстро уменьшает энергетические запасы организма и способствует развитию гипертермии. Клиника. Круп относится к угрожающим жизни заболеваниям верхних дыхательных путей и независимо от этиологии характеризуется стенозом гортани различной степени выраженности, сопровождающимся «лающим» кашлем, дисфонией, инспираторной или смешанной одышкой. Симптомы ларинготрахеита появляются внезапно, чаще в ночное время: при отечной форме — в 1-3 сутки ОРВИ на фоне повышенной температуры и катаральных явлений. Различают четыре степени СЛТ. I степень (компенсированный стеноз) — осиплость голоса вплоть до афонии, лающий кашель. При нагрузке (кормление, плач, кашель) появляется нерезко выраженный приступ, характеризующийся затрудненным шумным вдохом (стридором) и небольшим втяжением яремной ямки. При инфекционном СЛТ тахикардия соответствует степени лихорадки. В покое одышки нет. Приступ продолжается от нескольких минут до 2—3 ч. II степень (неполной компенсации) — стридор, слышимый на расстоянии, инспираторная одышка с участием вспомогательной мускулатуры (втяжение нижних межреберных промежутков, яремной и подключичных ямок, мягких тканей шеи, раздувание крыльев носа) в покое с резким усилением при нагрузке. Тахикардия большая, чем выраженность лихорадки, потливость, незначительный цианоз, беспокойство ребенка. Артериальное кровяное давление повышено. III степень (декомпенсированный стеноз) — общее состояние тяжелое. Периоды беспокойства сменяются периодами адинамии. Резкая бледность кожных покровов, холодный пот, периоральный и акроцианоз в покое, переходящий в генерализованный при беспокойстве ребенка, затруднение вдоха и выдоха. Аускультативно — дыхание ослабленное. Артериальное кровяное давление умеренно снижено, дефицит пульса. IV степень (асфиксигеская) — постоянно бледно-цианотические кожные покровы, периодически цианоз резко нарастает. Аритмичное или парадоксальное дыхание, брадикардия, снижение артериального кровяного давления, остановка дыхания или сердечной деятельности. Диф. проводят с ларингоспазмом, острым эпиглоттитом, инородными телами дыхательных путей, персистирующим стридором, истинным (дифтерийным) крупом. Для истинного дифтерийного крупа характерно: постепенное нарастание стеноза, афоничный голос, субфебрильная температура тела, катаральные явления отсутствуют, на миндалинах пленчатые налеты грязно-серого цвета, гнилостный запах изо рта, увеличение подчелюстных лимфоузлов, выраженный отек шейной клетчатки, при ларингоскопии — на голосовых связках плотные фибринозные наложения. Для заглоточного абсцесса типично острое начало с фебрильной температурой, выраженные симптомы интоксикации, нарастающая инспираторная одышка, переходящая в удушье, храпящее дыхание, вынужденное положение ребенка — с головой, запрокинутой назад и в больную сторону, при фарингоскопии — выпячивание задней стенки глотки и симптом флюктуации. Лечение. Этиотропное лечение включает противовирусные препараты: циклоферон – индуктор интерферона (10 мг/кг/сут. внутрь натощак или в/м по схеме: 1, 2, 4, 6 дни); виферон в свечах – рекомбинантный интерферон; альгирем (0,2% сироп по 10 мл: в 1-ый день 3 раза, во 2 –3 дни – 2 раза, в 4 день – 1 раз в день) или ремантадин (не более 5 мг/кг/сут), афлубин, арбидол. Применяются ингаляции ДНК-азой. Патогенетическое лечение направлено на снятие спазма, уменьшение отека в гортани и на разжижение и уменьшение количества мокроты. Эффективны при ОЛТ ингаляции с адреналином (5 капель адреналина на 2 мл воды или физиологич. р-ра), раствором соды 2%, соли 3%. При сочетании с бронхоспастическим компонентом (одышка смешанного характера) ингаляции проводят с беродуалом. Из фитопрепаратов используют отхаркавающие сборы, включающие корень алтея, фиалки трехцветной, сосновых почек. Кора дуба, богатая танинами, обладает антивирусной активностью. В стадию неполной компенсации назначают: 1. увлажненный кислород. 2. инфузионную терапию, включающую гипертонические растворы хлористого кальция (10% 1 мл/год жизни), глюкозы (20% 10 – 20 мл), аскорбиновую кислоту (5% 1 мл/год жизни), глюкокортикостероидные препараты - преднизолон (1 – 3 мл/кг) или дексаметазон 0,6 мг/кг, эуфиллин (2,4% - 0,2 мл/кг). 3. седативные препараты (димедрол 1% - 0,2 – 0,5 мл при отсутствии вязкой мокроты в бронхах; реланиум, седуксен 0,1% - 0.5 – 1,0 2 –3 раза в сутки; оксибутират натрия 50 – 120 мг/кг в/в). 4. ультразвуковые ингаляции с адреналином и гидрокортизоном (небулайзерная терапия) каждый час. 5. коррекцию кислото-щелочного состояния, кардиотоники, диуретики, жаропонижающие средства. Неотложка. Неотложная помощь 1 степени. 1. Придать возвышенное положение в постели, обеспечить доступ свежего воздуха (по возможности увлажненного). Обильное теплое питье. 2. Отвлекающие процедуры: и если нет температуры. горчичники (при их переносимости) на икроножные мышцы, горячие ножные или ручные ванны, полуспиртовой согревающий компресс на область шеи и грудной клетки. Паровые ингаляции (над кастрюлей с содовым раствором из расчета 1 чайная ложка на 1 литр горячей воды) могут быть эффективны. 3. при отечной (преимущественно аллергической) форме стеноза назначают ингаляции через ультразвуковой ингалятор (или закапывание по 3—4 капли в каждую ноздрю) 0,05% раствора нафтизина; 4. при аллергической этиологии 'стеноза показано использование антигистаминных препаратов, подкожное введение 0,1% раствора адреналина (0,01 мл/кг, но не более 0,3 мл). 2 степени. 1. сохраняет свое значение оксигено- и отвлекающая терапия; 2. при отечной (преимущественно аллергической) форме стеноза назначают ингаляции через ультразвуковой ингалятор (или закапывание по 3—4 капли в каждую ноздрю) 0,05% раствора нафтизина; 3. при аллергической этиологии 'стеноза показано использование антигистаминных препаратов, подкожное введение 0,1% раствора адреналина (0,01 мл/кг, но не более 0,3 мл). 4. при отсутствии эффекта от терапии назначают дексазон или преднизолон из расчета 2 мг/кг массы тела парентерально. 3. При I степени стеноза: • в носовые ходы закапать сосудосуживающие капли (0,05% раствор нафтизина или галазолина); • ультразвуковые ингаляции с 0,025% раствором нафтизина (1:10) 2-3 раза в день, чередуя их при отечной форме с ингаляциями с соком подорожника (1:10) и/или раствором лазолвана для ингаляций (1:10), при обтурационной форме — с гипертоническим раствором натрия хлорида и соком подорожника. 4. При нарастании явлений стеноза (I-II степень, II-Ш степень): • оксигенотерапия; • ультразвуковые ингаляции при I-II степени — 3 раза в день, при II-Ш степени — постоянно в паракислородной палатке: при отечной форме проводить ингаляции аэрозоля с кортикостероидами (гидрокортизон — 12,5-25 мг в ингалируемом составе); при обтурационной форме — ингаляции с гипертоническим раствором натрия хлорида, при отсутствии эффекта с химотрипсином; • преднизолон в дозе 2-3 мг/кг в сутки внутрь; • при явно выраженном беспокойстве — 0,5% раствор седуксена 0,05 мл/кг (0,3 мг/кг) в/м. 5. При III-IV степени стеноза: немедленная интубация трахеи термопластическими трубками. • оксигенотерапия в условиях паракислородной палатки; • преднизолон в дозе 5-7 мг/кг в/м или в/в; • вызов реанимационной бригады для проведения прямой ларингоскопии и интубации трахеи; • при отсутствии эффекта от вышеперечисленных мероприятий обеспечить ИВЛ. Госпитализация детей со стенозирующим ларинготрахеитом обязательна после оказания неотложной помощи: при I-II степени стеноза — в инфекционное отделение, при III-IV степени — в реанимационное отделение. 95. Принципы лечения ОРВИ у детей. Борьба с респираторными заболеваниями в детских учреждениях. Лечение. ОРВИ. Обычно нетяжелые проявления вирусных заболеваний верхних дыхательных путей требуют проведения только симптоматической терапии: • температура в помещении, где находится больной ребенок, не должна превышать 20 °С; • целесообразно снижение температуры на 3—4 °С во время сна; • подвижность ребенка по возможности ограничивается; ПОСТЕЛЬНЫЙ РЕЖ. • суточный объем жидкости увеличивается в 1,5—2 раза за счет питья клюквенного морса, чая с лимоном, настоя шиповника, минеральной воды (не следует давать большую нагрузку жидкостью при СЛТ ввиду опасности усиления отека гортани); • туалет носа проводят закапыванием физиологического раствора, раствора морской соли, 2% раствора соды, настоя трав (шалфей, ромашка) по 2—3 пипетки в каждую ноздрю 3—4 раза в день; вводить растворы следует в положении лежа на спине со свешивающейся вниз и назад головой, чтобы омыть средний и верхний носовые ходы и свод носоглотки; после промывания ребенок отсмаркивается или ему проводят отсасывание слизи; • сосудосуживающие капли эффективны в 1—3-й день заболевания; их использование дольше 3 дней может привести к тахифилаксии (усилению ринита); для детей раннего возраста используют називин (0,01% и 0,025% раствор); старше 3—4 лет — отривин, галазолин, санорин, назол; виброцил назначают детям любого возраста; • для лечения ринита можно использовать 5% раствор -аминокапроновой кислоты (турунды в носовые ходы); • масляные капли применять нельзя из-за опасности вызвать липоидную пневмонию; • детям грудного возраста закапывание любых медикаментов в нос противопоказано в связи с возможной рефлекторной остановкой дыхания — все лекарственные средства им вводят в полость носа при помощи ватных «фитильков»; особенно тщательно эти процедуры проводят перед кормлением ребенка; • лечение ринита предотвращает развитие или облегчает течение острого отита; боль в ухе уменьшается при назначении полуспиртового или водного компресса, закапывании в наружный слуховой проход капель, обладающих местноанестезирующим действием (отипакс); • при фарингитах вирусной этиологии применяют домашние смягчающие средства: ингаляции с настоями трав, щелочные ингаляции, теплое питье; • при ларингитах несколько раз в день проводят паровые ингаляции (с соблюдением всех мер предосторожности от ожогов), теплые ножные и ручные ванны (температура от 37 °С с постепенным повышением до 40 °С), общие ванны той же температуры; делают горячие водные или полуспиртовые компрессы на шею и область икроножных мышц, дают частое питье небольшими порциями (теплое молоко пополам с боржоми); • необходимо ограничивать контакты больного ребенка, чтобы избежать перекрестной инфекции; • мучительный, навязчивый, малопродуктивный кашель, возникающий при фарингите и трахеите, является показанием к назначению противокашлевых препаратов центрального ненаркотического действия (синекод, глаувент) периферического действия (стоптуссин). Современные возможности этиотропной терапии вирусных инфекций весьма ограничены: • В первые 2 дня вирусного респираторного заболевания и в целях профилактики контактным детям применяется лейкоцитарный интерферон по 0,25 мл в оба носовых хода каждые 1,5—2 ч (в первые 3 дня заболевания) или 2 раза в день с целью профилактики. • При лечении гриппа А2 целесообразно назначение ремантадина — 4,4 мг/кг в сутки, разделенные на 2 приема детям старше года. • При гриппе и других ОРВИ детям школьного возраста назначают арбидол (лечение — внутрь 0,8 г/сут.; профилактика — 0,2 г/сут.). • При подозрении на гнойный отит назначают амоксициллин или амоксициллин/клавуланат — аугментин (40—50 мг/кг/сут.), оспен, возможно назначение эритромицина. • При остром стрептококковом тонзиллите препаратами выбора являются оспен — 50—100 мг/кг в сутки за 4 приема внутрь, макролиды. Лечение местными антисептическими пастилками не заменяет лечения антибиотиками при стрептококковом тонзиллите. Назначение антигистаминных средств при вирусных заболеваниях верхних дыхательных путей не оправдано. Нельзя забывать также, что источником инфицирования детей в детском учреждении могут быть воспитатели и другой персонал, больные острой респираторной инфекцией. Доступ таких лиц в группы и другие места возможного контакта с детьми должен быть закрыт. Особого внимания требует вопрос о сроках допуска переболевших детей в детское учреждение. Сроки допуска детей в коллектив после перенесенного острого респираторного заболевания должны определяться главным образом индивидуальными особенностями реконвалесцента и характером перенесенной инфекции. Большинство детей могут быть допущены в детское учреждение после исчезновения у них симптомов острого катара (насморка, конъюнктивита, фарингита) вне зависимости от срока, прошедшего от начала заболевания. Такой подход оправдан тем, что наиболее заразный период совпадет с периодом разгара катаральных явлений. Чаще всего при острых респираторных вирусных инфекциях катаральные явления держатся 5 - 6 дней, так что допуск в учреждение детей при отсутствии осложнений возможен на 7 день от начала заболевания. Во время эпидемической вспышки внимание персонала должно быть направлено на неукоснительное соблюдение санитарно-гигиенических правил, воздушного режима, обязательное проведение кварцевания групповых помещений. Сон детей на свежем воздухе, прогулки ни в коем случае не должны отменяться или сокращаться. При проведении санитарно-просветительной работы с родителями и персоналом в период эпидемической вспышки следует обращать особое внимание на соблюдение оптимального теплового и воздушного режима в квартирах, предотвращение контактов с заболевшими взрослыми и детьми. 96. Современные принципы классификации острых кишечных инфекций у детей. Секреторные и инвазивные диареи, их характеристики. Острая кишечная инфекция — острое расстройство пищеварения, вызванное различными микроорганизмами, передающимися преимущественно контактно-бытовым, водным или пищевым путем, проявляющееся синдромом гастроэнтероколита с явлениями интоксикации. Классификация. По этиологическому принципу: -ОКИ бактериальной природы, в том числе вызванные условно-патогенной микрофлорой (кампилобактер, протей, цитробактер, стафилококк). -ОКИ вирусной природы (ротавирусы, астро-, торо-, калици-, корона-, адено-, реоивурусы и энтеровирусы). -Протозойной этиологии (лямблиоз, амебиаз). -Дизентерия ( шигеллез). Занимает первое место среди заболеваний у детей, особенно дошкольного и школьного возраста. -Сальмонеллезы. Занимают 2-е место в структуре острых кишечных инфекций по частоте. Поражаются дети всех возрастных групп. -Коли инфекции ( эшерихиозы). Клиническая классификация. (по пусковому механизму и патогенезу): 1). Инвазивные ОКИ— в основе лежит воспалительный процесс в любом отделе ЖКТ и эндотоксикоз (токсемия) 2). Секреторные диареи— гиперсекреция воды и электролитов за счет продукции возбудителями энтеротоксина и дегидратация. 3). Осмотические диареи— дисахаридазная недостаточность, бродильный процесс (метеоризм) и дегидратация за счет нарушения всасывания воды и электролитов. 4). Смешанные диареи— при микстинфекции. По клинической форме заболевания ( посиндромный диагноз).
Острый гастрит, когда заболевание характеризуется только синдромом рвоты, нет расстройств со стороны кишечника. Это бывает у детей старшего возраста при пищевых отравлениях.
Острый энтерит: отсутствует синдром рвоты, но есть синдром диареи - стул частый, жидкий.
Острый гастроэнтерит встречает чаще всего: есть синдром рвоты, обезвоживания, диареи.
В ряде случаев когда ребенок заболевает тяжелой формой дизентерии симптомокомплекс реализуется в нижних отделах и характеризуется острым колитом: тенезмы, бескаловый стул с примесью крови.
Острый энтероколит - поражение всего кишечника.
ПО ТЯЖЕСТИ ЗАБОЛЕВАНИЯ: Типичные формы: легкая, среднетяжелая, тяжелая. Атипичные формы: Стертые формы: скудный симптомокомплекс - кашицеобразный стул 1-2 раза, субфебрильное однократное повышение температуры отсутствие рвоты, состояние удовлетворительное. Диагноз ставится по бактериологическому и серологическому подтверждению. Бессимптомная форма: полная отсутствие каких-либо симптомов. Диагноз ставят по высеву ребенка. Бактерионосительство. Многие педиатры когда не хотят иметь неприятностей с СЭС (с выпускниками санитарного факультета) ставят диагноз бактерионосительство. Следовательно, к этому диагнозу надо относится осторожно: бактерионосительство — это полное отсутствие клинических проявлений, имеется лишь транзиторное, однократное выделение микроба. Ставить такой диагноз достаточно рискованно, потому что возможности обследования в амбулаторных условиях нет, и лучше поставить диагноз - легкая форма. Гипертоксическая форма. Заболевание развивается очень бурно, остро, с развитием иногда инфекционно-токсического шока (1-3 степени), характеризующееся выраженными токсическими симптомами и практически отсутствием местных изменений (кишечник интактен так как изменения не успевают развиться). При острых кишечных инфекциях инфекционно-токсический шок встречается редко. Инфекционные диареи бывают: инвазивные (слизистые или кровянистые) и секреторные (водянистые). Инвазивные диареи вызываются патогенными, условно-патогенными бактериями и простейшими. По "инвазивному" типу диареи протекают ОКИ бактериальной этиологии, возбудители которых (шигеллы, сальмонеллы, клостридии и др.) способны к "инвазии", т.е. размножаться не только на поверхности эпителия кишечника, но и внутриклеточно, а в ряде случаев и проникать в кровь с развитием бактериемии и сепсиса. В основе "пускового" механизма развития инфекционного процесса при ОКИ "инвазивного" типа лежит воспалительный процесс в тонком и/или толстом отделе кишечника различной степени выраженности (от катарального до язвенно-некротического), которая и определяет тяжесть заболевания. Воспалительный процесс в кишечнике является основой появления рвоты, болевого синдрома, ускоренной перистальтики и быстрой эвакуации кишечного содержимого, нарушения всасывания воды из кишечника (диареи) и пищеварительной функции - нередко с развитием бродильной диспепсии (метеоризма). В испражнениях присутствуют патологические примеси (слизь, зелень, нередко примесь крови). Токсины бактерий, продукты воспаления и другие токсические соединения всасываются из кишечника в кровь и являются основной причиной (как и обезвоживание организма) развития тяжелых синдромов инфекционного токсикоза и интоксикации (эндотоксикоза), которые и определяют не только тяжесть, но и исход заболевания.
По "секреторному" типу диареи протекают ОКИ также бактериальной этиологии, возбудители которых (холерный вибрион, энтеротоксигенные эшерихии, клебсиеллы пневмония, кампилобактер и др.) размножаются только на поверхности эпителия тонкого кишечника и не проникают внутрь энтероцитов ("неинвазивные"). В основе патогенеза лежит гиперсекреция воды и электролитов эпителием в просвет кишечника и нарушение их всасывания за счет активации системы аденилатциклазы под воздействием секреторных агентов, главным образом - бактериального экзотоксина. При этом типе диареи в патологический процесс вовлекается только тонкий кишечник без развития воспалительного процесса, а кишечная инфекция сопровождается жидким, обильным водянистым стулом без патологических примесей. Как правило, заболевание начинается с появления частого жидкого стула без повышения температуры тела (или в пределах 37,2-37,8°C), затем появляется рвота и быстро наступает обезвоживание организма, которое и определяет основную тяжесть и исход заболевания. 97. Дизентерия. Этиология, эпидемиология, патогенез, классификация. ДИЗЕНТЕРИЯ (ШИГЕЛЛЕЗ)- это острое инфекционное заболевание, поражающее толстый кишечник. Дизентерия (шигеллез) – антропонозная бактериальная инфекционная болезнь с фекально-оральным механизмом передачи возбудителя, вызываемая шигеллами, характеризующаяся преимущественным поражением дистального отдела толстой кишки с развитием синдрома дистального спастического колита. Этиология. Возбудители дизентерии относятся к роду Shigella, семейству Enterobacteriaceae.
Различают 4 вида шигелл: 1) Sh. dyscnteria, к ним относятся бактерии Григорьева — Шиги, 2) Sh. flexneri 3) Sh. boydii; 4) Sh. sonnei. Гр- неподвижные палочки, не образуют спор и капсул. Хорошо растут на простых питательных средах., К- и О-АГ, основные факторы патогенности – способность к адгезии к энтероцитам, инвазии и размножению в них, эндотоксин (ЛПС) и экзотоксины (цитотоксин, повреждающий мембраны эпителиальных клеток, энтеротоксин, усиливающий секрецию жидкости и солей в просвет кишки, нейротоксин). Эпидемиология. Источник инфекции – больной человек, механизм передачи – фекально-оральный, путь передачи – алиментарный(зонне), водный(флекснера), контактный(григорьева-шиги). Факторами передачи заразного начала могут быть немытые руки, инфицированные предметы обихода, различные пищевые продукты, особенно молочные, вода из открытых водоисточников. Сезонный подъем заболеваемости наблюдается в летне-осеннее время. Иммунитет монотипоспецифичный, ненапряженный. Патогенез. Заражение происходит через рот. Часть бактерий гибнет в желудке под влиянием желудочного сока, остальные достигают толстого кишечника, где они размножаются, возникает местный воспалительный процесс. Основным фактором, который определяет тяжесть болезни, является токсин, выделяемый палочкой дизентерии. Входными воротами инфекции и местом развития инфекционного процесса является желудочно-кишечный тракт. Преодоление МБ кислотного желудочного барьера --> попадание возбудителя в тонкий кишечник --> размножение шигелл, гибель с выделением эндотоксина, вызывающего явления интоксикации и энтеротоксического экзотоксина, вызывающего повышенную секрецию жидкости в просвет кишки (патологические изменения в тонкой кишке слабовыражены из-за отсутствия на энтероцитах рецепторов для адгезии возбудителя) --> колонизация шигеллами толстой кишки, адгезия и массивная инвазия колоноцитов --> активное размножение МБ в колоноцитах с последующей их гибелью и поражением соседних клеток, выделение токсинов, вызывающих расстройства микроциркуляции в кишечной стенке, поражение ее нервно-мышечного аппарата с развитием гипермоторной дискинезии, спазмов, нарушение процессов пристеночного пищеварения и всасывания, общеинтоксикационные проявления. Заболевание возникает при проникновении в кровь токсинов шигелл. Дизентерийные токсины действуют на стенку сосудов, ЦНС, периферические нервные ганглии, симпатико-адреналовую систему, печень, органы кровообращения. При тяжелых формах дизентерии больные обычно умирают от инфекционно– токсического шока. Классификация. По типу: а) типичная форма и б) атипичные формы: стертая, бессимптомная, транзиторное бактерионосительство. Атипичная форма имеет четыре клинических варианта:
1) стертую форму, при которой нет проявлений интоксикации, отмечается неустойчивый стул, имеется высев возбудителя; 2) диспепсическую форму, чаще возникающую у детей первого года жизни, интоксикация слабо выражена и подтверждается бактериологически и серологически; 3) субклиническую форму, характеризующуюся выделением возбудителя при отсутствии клинических проявлений, при ректороманоскопии можно обнаружить морфологические изменения, нарастание титров антител в крови; 4) гипертоксическую форму, протекающую с выраженным нейротоксикозом (гипертермией, потерей сознания, судорогами, сердечно-сосудистой недостаточностью) и появлением диареи к концу первых суток болезни. По степени тяжести: а) легкая форма; б) среднетяжелая форма; в) тяжелая форма с преобладанием симптомов токсикоза или местных нарушений. (влияние – нарушения, частота стула, боль, зияние) По течению: а) острое (до 1 мес); б) подострое (1-3 мес); в) хроническое (свыше 3 мес): непрерывное, рецидивирующее, длительное бактериовыделение при нормальном стуле. 98. Дизентерия. Клиника, осложнения, лечение, профилактика. ДИЗЕНТЕРИЯ (ШИГЕЛЛЕЗ)- это острое инфекционное заболевание, поражающее толстый кишечник. Дизентерия (шигеллез) – антропонозная бактериальная инфекционная болезнь с фекально-оральным механизмом передачи возбудителя, вызываемая шигеллами, характеризующаяся преимущественным поражением дистального отдела толстой кишки с развитием синдрома дистального спастического колита. Клиника. Инкубационный период для возбудителя Shigella составляет 1–4 дня. По течению выделяют дизентерию острую и хроническую. Острая дизентерия протекает в нескольких вариантах: колитический, гастроэнтероколитический и гастроэнтеритический, каждый из которых может быть представлен в легкой, средней тяжести и тяжелой формах. Дизентерия характеризуется цикличностью течения. При этом в течении заболевания можно выделить 4 периода: начальный, разгара, угасания симптомов и выздоровления (остаточных явлений или перехода в хроническую форму). колитический вариант – наиболее типичен: - острое начало заболевания с синдрома общей интоксикации (повышение температуры тела, озноб, чувство разбитости, снижение аппетита. головная боль)
- боли в животе, вначале тупые, разлитые по всему животу, имеющие постоянный характер, затем более острые, схваткообразные, локализующиеся в нижних отделах живота, чаще слева, усиливаются перед дефекацией, сопровождаются тенезмами, ложными позывами; пальпаторно толстая кишка болезненна, спазмирована (особенно в области сигмовидного отдела).
- стул учащен, испражнения вначале каловые, затем уменьшаются в объеме, становятся жидкими, появляются патологические примеси в виде слизи и прожилок крови; в более тяжелых случаях при дефекации выделяется лишь небольшое количество слизи с прожилками крови («ректальный плевок»)
- симптомов обезвоживания организма нет. - при ректороманоскопии - катаральный, катарально-геморрагический или катарально-эрозивный диффузный проктосигмоидит. тяжелая — t 40-41º, резко выраженная интоксикация, стул без каловых масс гастроэнтероколитический вариант - характерно одновременное развитие синдромов общего токсикоза, гастроэнтерита и обезвоживания:
- острое начало с лихорадки, озноба, появления болей в подложечной области, тошноты и многократной рвоты. - через некоторое время появляются урчание и боли по всему животу, императивные позывы на дефекацию; испражнения обильные, жидкие, светло-желтой или зеленой окраски с кусочками непереваренной пищи и примесью слизи.
- объективно: признаки обезвоживания (заостренные черты лица, запавшие глаза, сниженная влажность конъюнктив, сухость слизистых ротовой полости и глотки, икота, частый нитевидный пульс, глухие тоны сердца, артериальная гипотензия); при пальпации живота грубое громкое урчание, шум плеска по ходу толстой кишки. - на 2-3-й день болезни появляются ложные позывы, тенезмы, в кале примесь слизи, иногда крови, пальпаторно - спазм и умеренная болезненность сигмовидной кишки; при ректороманоскопии – катаральный или катарально-эрозивный проктосигмоидит. ОСОБЕННОСТИ ТЕЧЕНИЯ ДИЗЕНТЕРИИ У ДЕТЕЙ ПЕРВОГО ГОДА ЖИЗНИ.
Дети первого года жизни дизентерией болеют достаточно редко, что связано с отсутствием контактов, грудным вскармливанием и антительной защитой матери. Следовательно, если у грудного ребенка отмечается диарейный синдром, то о дизентерии надо думать в последнюю очередь.
Заболевание протекает преимущественно в среднетяжелой или легкой форме, достаточно монотонно, температура чаще субфебрильная, рвота редка (вообще рвота не очень характерна для дизентерии) стул носит характер энтеритного (высокий стул - жидкий, с мелкой слизью, зеленого цвета, калового характера) - неклассический, с разной частотой.
У детей раннего возраста отсутствует такой классический симптом дизентерии как тенезмы (позыв на низ). Вместо этого симптома имеет место эквиваленты тенезм: перед актом дефекации ребенок резко возбужден, стучит ножками, кричит, гиперемия лица, выражена потливость, тахикардия, иногда напряжен живот, а после акта дефекации все эти явления проходят.
Наслоение интеркурентных заболеваний: если ребенок заболевает дизентерией, то не так сама дизентерия истощает его, сколько интеркурентные заболевания: гнойные отиты, ОРВИ, пневмонии, гнойничковые поражения кожи, инфекция мочевыводящих путей и так далее.
Течение дизентерии характеризуется медленным (нередко затяжным - свыше 1.5 мес.) монотонным течением, в связи с частым развитием (до 90% случаев) дисбактериоза, что приводит к длительному выделению микроба (месяцами), что трудно поддается лечению (лечение должно быть вариабельным).
ОСОБЕННОСТИ ТЕЧЕНИЯ ТОКСИЧЕСКОЙ ДИЗЕНТЕРИИ: Чаще вызывается Shigella Flexneri и преимущественно у детей школьного возраста (так как маленький ребенок в силу недоразвитости иммунной системы не может так отреагировать на инфекцию). Начало острое: повышение температуры до 39-40 градусов (молниеносно), выраженная головная боль, резкое возбуждение в первые часы сопровождающееся клонико-тоническими судорогами. В ряде случае возможна потеря сознания, может быть рвота и при объективном осмотре положительны менингеальные симптомы. Это типичная клиника серозного или гнойного менингита, и лучше такого ребенка госпитализировать. Сложность диагностики заключается в более позднем (через несколько часов или суток) появлении характерного кишечного синдрома - частого характерного стула, тенезм, болей в животе, что способствует неправильной госпитализации ребенка. Осложнения. Инфекционно-токсический шок + дегитратационный. Рецедивы в 5-15%, обострения геморроя, трещины анального сфинктера. Присоединение вторичной флоры: пневмония, восходящая урогенитальная инфекция, тяжелый дизбактериоз, прободение язв с перитонитом.
Лечение.
Больных дизентерией
госпитализируют в инфекционный стационар,
особенно больных со среднетяжелыми и
тяжелыми формами, детей – в возрасте
до 3 лет, ослабленных, а также при
невозможности организовать лечение на
дому.
Диетотерапия
проводится с учетом возраста. В первые
2—3 дня уменьшают объем пищи на 1/4—1/2 в
зависимости от тяжести состояния и
используют принципы механического
щажения.
С целью восполнения
потери жидкости и электролитов, коррекции
кислотно-основного состояния, обменных
нарушений проводится регидратационная
терапия.
В
качестве этиотропных
препаратов назначают антибиотики,
сульфаниламиды,
интетрикс, фуразолидон.
нитрофураны
(фуразолидон, фурадонин, эрсефурил /
нифуроксазид 0,2 г 4 раза/сут), оксихинолины
(нитроксолин, интетрикс), при среднетяжелой
форме – фторхинолоны
(офлоксацин
по или ципрофлоксацин)
, при тяжелой форме - фторхинолоны в
комбинации с аминогликозидами;
аминогликозиды в комбинации с
цефалоспоринами в первые 2-3 дня
парентерально, затем перорально;
Можно
использовать дизентерийный
бактериофаг. Назначают
комплекс витаминов.
Для восстановления микрофлоры назначают
биопрепараты
(бифидумбактерин, лактобактерин, линекс,
бификол и др.), ферментотерапию,
фитотерапию. При затяжном те-чении
применяют иммунокорригирующие препараты.
Для предупреждения рецидивов дизентерии
необходимо тщательное выявление и
лечение сопутствующих заболеваний.
При
легкой степени дегидратации
используется оральная
регидратация с
расчетом вводимой жидкости 40—50 мл/кг
веса. Регидратация занимает 4 ч.
При
среднетяжелой
степени обезвоживания
расчет жидкости составляет 60—90 мл/кг.
Регидратация проводится в течение 6 ч,
дальнейшее введение растворов назначается
с учетом потери жидкости с рвотой и
стулом. На каждую порцию потерянной
жидкости вводится раствор из расчета
10—15 мл/кг.
При
тяжелой степени
восполнение жидкости составляет 100—120
мл/кг. В этой стадии большая часть
растворов вводится
внутривенным путем.
Для оральной регидратации используются
следующие растворы: регидрон, хлоралит,
цитрат глюкосолан.
Степени
дегидратации у детей.
При многих инфекционных болезнях в
числе симптомов присутствуют рвота и
частый стул. Чаще всего это наблюдается
при кишечных инфекциях, вызванных
шигеллами, стафилококками, протеем,
сальмонеллами и др. Дегидратация чаще
развивается у детей в связи с компенсаторными
возможностями детского организма.
I
степень – легкая.
Потеря веса составляет до 5% массы тела.
Частота стула и рвоты – до
6 раз в сутки,
умеренная жажда, больные капризны,
возбуждены, тургор и эластичность кожи
сохранены, наблюдается некоторая сухость
слизистых, тоны сердца и качества пульса
в пределах нормы. Наблюдается умеренная
тахикардия, голос сохранен, диурез
уменьшен незначительно, температура
тела повышена.
II
степень – среднетяжелая.
Это стадия потери
внутриклеточного калия и натрия.
Дефицит веса – до 9%. Частота стула и
рвоты – до 10 раз в сутки, жажда резко
выражена, но больные
отказываются от питья,
так как присутствует тошнота. Состояние
беспокойства переходит в вялость и
заторможенность, тургор и эластичность
кожи снижены, складка собирается с
трудом, слизистые оболочки и глазные
яблоки сухие, сердечные тоны приглушены,
значительная тахикардия, пульс слабого
наполнения, температура тела высокая.
Диурез снижен.
Наблюдается небольшая осиплость
голоса.
III
степень – тяжелая.
Это стадия дефицита
солей. Потеря
массы тела составляет более 10%. Стул и
рвота – без счета, больные
отказываются от еды и питья,
наблюдается апатия и адинамия, черты
лица заострены, конечности
холодные на ощупь,
возможна потеря сознания. Тургор кожи
резко снижен, кожная складка не
расправляется, глаза резко запавшие,
мягкие глазные яблоки, слизистые сухие
и кровоточащие, развивается ДВС-синдром,
тоны сердца глухие, брадикардия, диурез
в стадии олигурии, переходящей в анурию.
Температура тела ниже нормы,
афония.
Профилактика.
Перенесшие
дизентерию пациенты выписываются не
ранее, чем через
3 дня после полного выздоровления.
Кроме того, необходимыми критериями
являются нормализация стула, температуры
тела, однократный
отрицательный бактериологический
анализ, который
должен проводиться не ранее чем через
2 дня
после отмены антибиотикотерапии.
Работники питания и лица, приравненные
к ним, а также больные хронической
дизентерией подлежат диспансерному
наблюдению. Срок диспансерного наблюдения
составляет 3—6 месяцев. В случаях, если
больной остается дома, в квартире
проводят текущую дезинфекцию. За лицами,
находившимися в контакте с больными,
устанавливают медицинское наблюдение
в течение 7 дней.
99.
Сальмонелез у детей. Этиология,
эпидемиология, патогенез, классификация,
клиника, лечение и профилактика.
Сальмонеллез
(salmonellosis) ‑
острая
инфекционная
болезнь,
вызываемая
бактериями
рода
Salmonella (кроме
брюшного
тифа
и
паратифов),
попадающими
в
организм
человека
с
пищевыми
продуктами животного происхождения.
Этиология. Возбудитель
заболевания – грамотрицательные
подвижные палочки
длиной 24 мкм и шириной 0,5 мкм, обладающие
высокой подвижностью, без способности
к образованию спор и капсул, имеющие
жгутики. Сальмонеллы являются
факультативными анаэробами и растут
на обычных питательных средах.
Губительной для сальмонелл
является высокая температура - кипячение
их убивает мгновенно. Salmonella
enterica enterica,
имеет разнообразные серотипы: agona,
enteritidis, typhimurium, heidelberg, newport и др. —
возбудители сальмонеллеза.
Эпидемиология.
Сальмонеллёз – зооноз.
Механизм передачи –
фекально-оральный. Пути передачи:
пищевой, контактно-бытовой, возможен
воздушно-пылевой. Факторы передачи –
до 80% мясо и мясные продукты (фарш, ливер,
студень), молоко, куриные яйца.
У детей
грудного возраста основным путем
заражения сальмонеллезом является
контактно-бытовой
- через соски, игрушки, предметы ухода,
грязные руки ухаживающих за ними
взрослых.
Патогенез.
Проникновение сальмонеллы
per os - Местом
первичной инфекции и внедрения
сальмонелл является область
тонкой кишки, в
инкубационном периоде происходит
размножение
микроба и
проникновение
его в лимфоузлы,
а оттуда зачастую в кровеносное
русло. Адгезия
к энтероцитам, колонизация, выделение
токсинов (эндо и экзо), трансцитоз в
подслизистый слой, захват макрофагами.
Энтеротоксин
- Активация аденилатциклазы - Выход
ионов и воды в просвет кишечника-
диарея.
Цитотоксины
- Гибель клеток, слущивание эпителия -
Умеренное воспаление слизистой кишки.
В
области слизистых оболочек кишки
возникают эрозии
и язвы, может быть
отек кишечной стенки, его инфильтрация
и кровоизлияния, зоны некроза.
У очень
ослабленных детей и малышей раннего
возраста сальмонеллы
могут проникать во внутренние органы
и вызывают в них дегенеративные изменения,
воспалительные очаги и абсцессы. Кроме
того, важную роль играет эндотоксин
сальмонелл – он поражает вегетативный
отдел нервной системы с явлениями
интоксикации, обменными нарушениями и
понижением массы тела. После перенесенного
сальмонеллеза иммунитет нестойкий,
поэтому заболевание может переноситься
неоднократно в жизни.
Классификация.
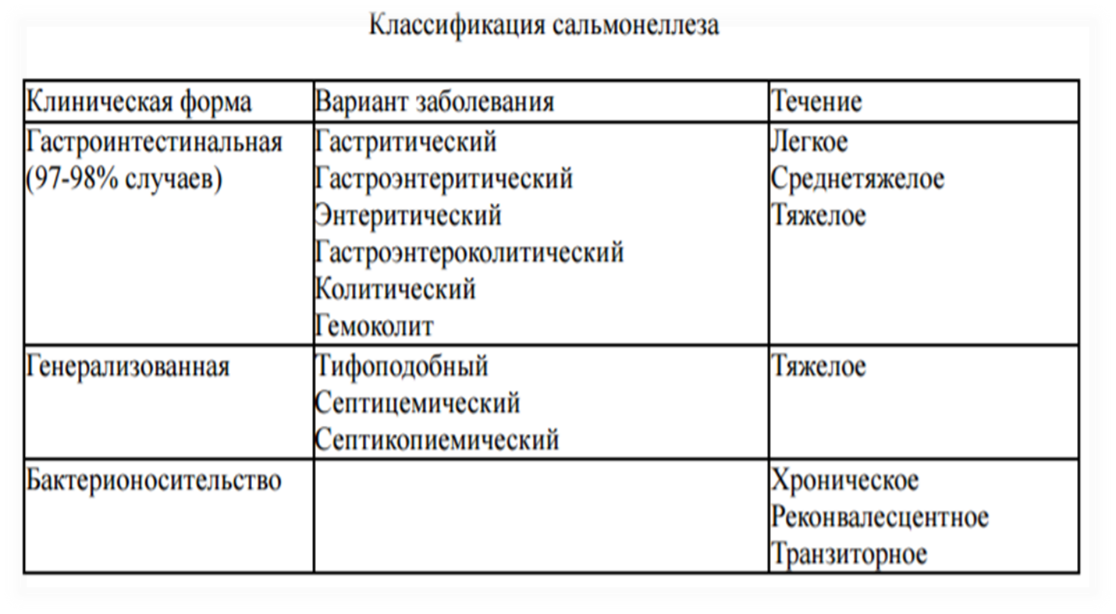 Клиника.
Тяжесть
заболевания зависит от возраста ребенка
и состояния его защитных сил, вида
сальмонелл, пути заражения, количества
микробов и их токсинов, попавших в
организм. Наиболее часто встречается
поражение желудочно-кишечного тракта,
куда микроб попадает, преодолев первый
естественный защитный барьер - соляную
кислоту желудочного сока.
У
детей грудного возраста заболевание
обычно начинается постепенно:
появляются вялость,
снижение аппетита,
повышенная
температура,
рвота,
жидкий стул -
вначале обычного цвета и умеренно
учащенный
(5-6 раз в сутки).
В последующие дни состояние ухудшается,
температура
повышается до 38 и выше,
испражнения становятся
более частыми (10 раз в сутки и чаще),
водянистыми, приобретают
зеленый цвет. К
5-7-у дню болезни в них
появляется слизь, иногда - прожилки
крови. При
отсутствии лечения в связи с потерей
организмом воды и солей натрия и калия
при рвоте и диарее может развиться
обезвоживание,
которое проявляется сухостью
слизистой оболочки рта и языка,
западением родничка, появлением жажды,
уменьшением выделения мочи. При дальнейшем
нарастании обезвоживания нарушения
водно-минерального обмена могут стать
необратимыми. У новорожденных детей
преобладают общие
симптомы над симптомами со стороны
желудочно-кишечного тракта.
Температура нередко остается нормальной.
Дети отказываются
от еды, перестают прибавлять в весе,
становятся беспокойными, срыгивают;
кожа бледная; конечности холодные; живот
вздут.
У детей
с ослабленным иммунитетом
(недоношенных, на искусственном
вскармливании, имеющих врожденную
патологию, часто болеющих) сальмонеллез
может протекать в виде
генерализованной инфекции (по
типу сепсиса), с поражением других
внутренних органов (печень, почки,
легкие, мозговые оболочки). Заболевание
протекает очень тяжело, с высокой
температурой в течение длительного
времени, сопровождается увеличением
печени и селезенки.
У
детей более старшего возраста
(дошкольного и школьного) заболевание
обычно начинается внезапно
- поднимается
температура
выше 38, появляются
головная
боль, головокружение, повторная обильная
рвота, слабость,
снижение аппетита. К этим симптомам
быстро присоединяются понос
и боли в животе.
Испражнения становятся жидкими,
водянистыми, темно-зеленого
цвета (похожими
на болотную
тину). При
своевременно начатом лечении заболевание
может ограничиться симптомами поражения
желудка и тонкой кишки (гастроэнтерит),
а при отсутствии лечения инфекционный
процесс распространяется и на толстую
кишку (колит) - в испражнениях появляются
слизь и
кровь, боли в животе усиливаются и
становятся схваткообразными
(заболевание
напоминает дизентерию). Кроме обезвоживания,
при тяжелом течении болезни опасными
осложнениями являются острая почечная
недостаточность и инфекционно-токсический
шок.
Заболевание
у детей старшего возраста обычно
заканчивается в течение
1-3 недель, а у детей
раннего возраста, особенно новорожденных
и ослабленных, может продолжаться в
течение нескольких недель и даже месяцев;
при этом возможны обострения и рецидивы,
а также длительное выделение сальмонелл
с испражнениями и даже мочой. После
перенесенного сальмонеллеза в течение
долгого времени (не менее 3 мес.) сохраняются
функциональные нарушения пищеварения,
такие как недостаточность выработки
ферментов поджелудочной железы (из-за
ее реактивного поражения), ферментов,
переваривающих молочный сахар; явления
дисбактериоза (особенно
при неумеренном лечении антибиотиками),
а у детей с неблагоприятным аллергическим
фоном - усиление проявлений пищевой
аллергии (особенно на белки молока). Все
эти явления могут протекать незаметно,
а могут сопровождаться "неустойчивым"
стулом (чередование
запоров и поносов),
вздутием и болями в животе, срыгиваниями,
усиливающимися при употреблении молочной
пищи. В ряде случаев может развиться
хроническая патология желудочно-кишечного
тракта (хронический колит, хронический
панкреатит), которая сохраняется
впоследствии и у взрослых.
Генерализованая:
Тифоподобный
вариант
Клиника.
Тяжесть
заболевания зависит от возраста ребенка
и состояния его защитных сил, вида
сальмонелл, пути заражения, количества
микробов и их токсинов, попавших в
организм. Наиболее часто встречается
поражение желудочно-кишечного тракта,
куда микроб попадает, преодолев первый
естественный защитный барьер - соляную
кислоту желудочного сока.
У
детей грудного возраста заболевание
обычно начинается постепенно:
появляются вялость,
снижение аппетита,
повышенная
температура,
рвота,
жидкий стул -
вначале обычного цвета и умеренно
учащенный
(5-6 раз в сутки).
В последующие дни состояние ухудшается,
температура
повышается до 38 и выше,
испражнения становятся
более частыми (10 раз в сутки и чаще),
водянистыми, приобретают
зеленый цвет. К
5-7-у дню болезни в них
появляется слизь, иногда - прожилки
крови. При
отсутствии лечения в связи с потерей
организмом воды и солей натрия и калия
при рвоте и диарее может развиться
обезвоживание,
которое проявляется сухостью
слизистой оболочки рта и языка,
западением родничка, появлением жажды,
уменьшением выделения мочи. При дальнейшем
нарастании обезвоживания нарушения
водно-минерального обмена могут стать
необратимыми. У новорожденных детей
преобладают общие
симптомы над симптомами со стороны
желудочно-кишечного тракта.
Температура нередко остается нормальной.
Дети отказываются
от еды, перестают прибавлять в весе,
становятся беспокойными, срыгивают;
кожа бледная; конечности холодные; живот
вздут.
У детей
с ослабленным иммунитетом
(недоношенных, на искусственном
вскармливании, имеющих врожденную
патологию, часто болеющих) сальмонеллез
может протекать в виде
генерализованной инфекции (по
типу сепсиса), с поражением других
внутренних органов (печень, почки,
легкие, мозговые оболочки). Заболевание
протекает очень тяжело, с высокой
температурой в течение длительного
времени, сопровождается увеличением
печени и селезенки.
У
детей более старшего возраста
(дошкольного и школьного) заболевание
обычно начинается внезапно
- поднимается
температура
выше 38, появляются
головная
боль, головокружение, повторная обильная
рвота, слабость,
снижение аппетита. К этим симптомам
быстро присоединяются понос
и боли в животе.
Испражнения становятся жидкими,
водянистыми, темно-зеленого
цвета (похожими
на болотную
тину). При
своевременно начатом лечении заболевание
может ограничиться симптомами поражения
желудка и тонкой кишки (гастроэнтерит),
а при отсутствии лечения инфекционный
процесс распространяется и на толстую
кишку (колит) - в испражнениях появляются
слизь и
кровь, боли в животе усиливаются и
становятся схваткообразными
(заболевание
напоминает дизентерию). Кроме обезвоживания,
при тяжелом течении болезни опасными
осложнениями являются острая почечная
недостаточность и инфекционно-токсический
шок.
Заболевание
у детей старшего возраста обычно
заканчивается в течение
1-3 недель, а у детей
раннего возраста, особенно новорожденных
и ослабленных, может продолжаться в
течение нескольких недель и даже месяцев;
при этом возможны обострения и рецидивы,
а также длительное выделение сальмонелл
с испражнениями и даже мочой. После
перенесенного сальмонеллеза в течение
долгого времени (не менее 3 мес.) сохраняются
функциональные нарушения пищеварения,
такие как недостаточность выработки
ферментов поджелудочной железы (из-за
ее реактивного поражения), ферментов,
переваривающих молочный сахар; явления
дисбактериоза (особенно
при неумеренном лечении антибиотиками),
а у детей с неблагоприятным аллергическим
фоном - усиление проявлений пищевой
аллергии (особенно на белки молока). Все
эти явления могут протекать незаметно,
а могут сопровождаться "неустойчивым"
стулом (чередование
запоров и поносов),
вздутием и болями в животе, срыгиваниями,
усиливающимися при употреблении молочной
пищи. В ряде случаев может развиться
хроническая патология желудочно-кишечного
тракта (хронический колит, хронический
панкреатит), которая сохраняется
впоследствии и у взрослых.
Генерализованая:
Тифоподобный
вариант
Лихорадка 1 – 3 недели постоянная или волнообразная.
Могут быть кишечные дисфункции 1 – 2 дня.
Интоксикация – головная боль, бессонница, общая слабость, снижение аппетита.
Гепатоспленомегалия.
В ОАК в первые дни болезни – лейкоцитоз, затем – лейкопения.
Септическая форма
• Высокая лихорадка неправильного типа с ознобами, потливость, интоксикация, гепатоспленомегалия.
• Вторичные септические очаги (остеомиелит, артрит, эндокардит).
Розеолезная сыпь на груди и животе.
Геморрагические высыпания
Лечение. При подозрении на пищевой путь заражения (многократная рвота, одновременное заболевание других членов семьи при употреблении одного и тою же пищевого продукта) надо начать промывание желудка (обильное питье - 2%-ный раствор соды) с последующим вызыванием рвоты. При гастроинтестинальных формах этиотропная терапия показана только при среднетяжелом и тяжелом течении заболевания (ципрофлоксацин по 1,0 г/сут, норфлоксацин или офлоксацин по 0,8 г/сут внутрь 3-5 дней). Антибиотики безусловно показаны лишь при тяжелых и генерализованных формах болезни у детей раннего возраста из групп риска (с ослабленным иммунитетом). Их назначение в стационаре проводится с учетом данных чувствительности к ним сальмонелл и тяжести болезни. Однако у таких детей даже правильно подобранные антибиотики не всегда эффективны, поэтому их целесообразно сочетать с иммунопрепаратами (лизоцим, комплексный иммуноглобулиновый препарат). Неспецифическая детоксикация - энтеросорбенты: энтеродез, энтеросорб, полифепан, полисорб МП и др. Регидратационная терапия: при легких формах - питье солевых р-ров или стандартные регидратационные р-ры - оралит, гастролит, глюкосалон); Выпаивание проводится только дробно - по 1 чайной, десертной или столовой ложке каждые 5 мин. Детям до 3 лет Регидрон чередуют с кипяченой водой или несладким чаем. При отсутствии Регидрона можно приготовить раствор самостоятельно (на 1 л воды - 1 столовая ложка сахара и 1 чайная ложка соли). при среднетяжелых формах, отсутствии рвоты и выраженных нарушений гемодинамики жидкость также можно вводить перорально; при повторной рвоте и нарастании обезвоживания растворы (ацесоль, трисоль, хлосоль, дисоль и др.) вводят в/в подогретом виде; Большое значение при лечении сальмонеллеза у детей имеет диета. Голодная диета ("водно-чайная" пауза) в настоящее время не рекомендуется, но целесообразно ограничение количества пищи в первые 3-5 дней болезни на 5-15% (в зависимости от тяжести процесса). Оптимальным для детей первого года жизни остается грудное молоко (непастеризованное), которое является не только наиболее полноценным питанием, незаменимым по составу белков, жиров, углеводов, витаминов и микроэлементов, но и содержит целый ряд биологически активных защитных веществ. Детям старше года в первые дни болезни необходима легко усвояемая протертая пища (отварной рис, супы, пюре из овощей) с ограничением жира и добавлением парового мяса и рыбы (с третьего-четвертого дня). На 2-3 недели из рациона исключаются продукты, усиливающие брожение и перистальтику кишечника (цельное молоко, ржаной хлеб, сырые овощи, кислые фрукты и ягоды), а также пряности и соления. Профилактика. Необходимо строго соблюдать правильную технологию и хранение продуктов, избегать употребления в пищу парного молока, сырых яиц, правильно обрабатывать игрушки и предметы ухода за детьми, особенно соски. И, конечно, не надо забывать, что мытье рук - наиболее простой и самый действенный способ профилактики ОКИ. Если один из членов семьи заболел сальмонеллезом, после изоляции больного необходимо провести дезинфекцию и обследовать членов семьи (бактериологическое обследование - анализ кала), а также назначить им с профилактической целью сальмонеллезный бактериофаг (по 1-2 таблетки 3-4 раза в день, в зависимости от возраста, в течение 5-6 дней). 100. Кишечная колиинфекция (эширихиозы). Этиология, эпидемиология, патогенез, клиника, лечение и профилактика. Эшерихиозы (коли-инфекция, коли-энтерит, диарея путешественников) — группа бактериальных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечной палочки, протекающих с симптомами общей интоксикации и поражением ЖКТ. Этиология. Бактерия Escherichia coli (E.coli), продуцирующая шигатоксин. Часто обнаруживается в кишечнике людей и теплокровных животных. Большинство штаммов E.coli безвредны, однако некоторые из них, например, т.н. STEC, могут вызывать тяжелые болезни. Эшерихии – аэробные грамотрицательные палочки размером (0,4-0,6) * (2-3) мкм. • энтеропатогенные (ЭПКП); • энтеротоксигенные (ЭТКП); • энтероивазивные (ЭИКП); • энтерогеморрагичные (ЭГКП); • энтероадгезивные (ЭАКП). Эпидемиология. Механизм передачи инфекции - фекально-оральный, также встречается пищевой, бытовой или водный путь заражения. Источник и резервуар инфекции – больной человек или животные. Факторы передачи – пищевые продукты (молочные, молочнокислые, рыба, мясо), органолептические свойства которых не изменяются при контаминации; вода, напитки, загрязненные предметы обихода, руки больных и бактерионосителей. Заболевания, вызванные ЭТКП, спорадические, реже групповые, регистрируются в странах с жарким климатом среди детей в возрасте до 2 лет и взрослых. ЭПКП вызывают спорадическую заболеваемость у детей, которые преимущественно находятся на искусственном вскармливании, регистрируются во всех климатических зонах. Патогенез. Механизм развития заболевания зависит от принадлежности диареегенных эшерихий к конкретным группам. ЭПКП вызывают колиэнтериты детей раннего возраста (E. coli 1-го класса) и сальмонелезоподобные гастроэнтероколиты (E. coli 2-го класса). Патогенез поражений обусловлен адгезией бактерий (фактор адгезии – Нер-2) к эпителию кишечника и повреждением микроворсинок, но не инвазией клеток. ЭТКП – возбудители холероподобных заболеваний. Факторы патогенности – фактор колонизации (пили, благодаря которым происходит адгезия к эпителию и колонизация нижних отделов тонкого кишечника), термостабильный и термолабильный энтеротоксины. Эффект последнего схож с действием токсина холерного вибриона (образование цАМФ и цГМФ, в результате чего в просвет кишечника секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстом кишечнике). ЭИКП вызывают шигеллезоподобое заболевание. Их механизм патогенности ограничивается способностью к проникновению в эпителий толстого кишечника, что приводит к воспалительной реакции, эрозии кишечной стенки и способствует увеличению всасывания в кровь эндотоксина бактерий. ЭГКП продуцируют цитотоксин SLT (Shiga-like toxin), который вызывает разрушение клеток эндотелия мелких кровеносных сосудов преимущественно проксимальных отделов толстой кишки, что приводит к ишемии кишечной стенки и появлению крови в стуле. ЭАКП вызывают нарушение функции тонкого кишечника за счет их агрегации и крепкого закрепления на поверхности эпителиальных клеток. Клиника. Вызванные ЭПКП (у детей раннего возраста): Инкубационный период 5-8 дней. Характерные признаки: - острое начало, - повышение t, интоксикация - жидкий водянистый стул (оранжевый или ярко желтой окраски) - развитие эксикоза. По тяжести: легкая, средней степени и тяжелая. ЭИКП (у детей дошкольного, школьного возраста). Синдромы: энтероколит, колит, гастроэнтероколит. - Повышение температуры до 38-39 °. - Общее состояние страдает незначительно. - Тенезмов нет. Стул до 5-10 раз (слизь, редко прожилки крови). острое начало, слабость, головная боль, боль в мышцах, лихорадка, непродолжительная водянистая диарея с примесями слизи и крови, присоединяются схваткообразные боли в животе, тенезмы, ложные позывы на дефекацию. ЭТКП ( у детей школьного возраста и взрослых). Инкубационный период от нескольких часов до 3-х дней. Клиника острого гастроэнтерита ( холероподобный синдром). - рвота повторная. - N или субфебрильная температура, - жидкий водянистый стул 10 раз и более. - живот вздут, в верхней половине умеренные боли. характерно холероподобное течение заболевания: острое начало, слабость, головокружение, нормальная или субфебрильная температура, тошнота, рвота, схваткообразные боли в животе, частый обильный водянистый стул. ЭГКП, характерны: острое начало, боль в животе, тошнота, рвота, нормальная или субфебрильная температура тела, жидкий стул без патологических примесей, который на 2-4-й день болезни учащается, в нем появляются примеси крови, присоединяются тенезмы. ЭАКП вызывают заболевание у пациентов с ослабленной иммунной системой. Кроме диареи, которая характеризуется легким, однако длительным течением, способна приводить к поражению мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны и септические формы (коли-сепсис, менингит). Лечение. Больных эшерихиозом госпитализируют по клиническим (тяжелые и среднетяжелые формы) и эпидемиологическим (лица, которые проживают в общежитиях, декретированное население) показанием. Другие лечатся амбулаторно. Диета: в остром периоде – стол № 4, при нормализации стула – №2, в период реконвалесценции – №13. В зависимости от тяжести течения, показаны: - при легком течении – оральная регидратация, ферменты, энтеросорбенты и кишечные антисептики; - при среднетяжелом течении – этиотропная (препараты фторхинолонового ряда или ко-тримазол) и регидратационная терапия, ферменты, энтеросорбенты, пробиотики, эубиотики, симптоматическая терапия; - в тяжелых случаях – этиотропная терапия (фторхинолоны + цефалоспорины 2-го или 3-го поколения), парентеральная регидратация и дезинтоксикация, ферментные препараты, энтеросорбенты, пробиотики, эубиотики, симптоматическая терапия. Профилактика. Для профилактики инфекции необходимо соблюдать контрольные меры на всех стадиях продовольственной цепи – от производства сельскохозяйственной продукции на фермах до переработки, обработки и приготовления пищевых продуктов как на коммерческих предприятиях, так и в домашних условиях. Качественно термически обработанными считаются продукты, достигшие температуры 70 градусов С. Настоятельно рекомендуется регулярное мытье рук, в частности перед приготовлением пищи, едой и после посещения туалета – особенно для людей, ухаживающих за детьми, пожилыми людьми и людьми с ослабленным иммунитетом. 101. Кишечный токсикоз с эксикозом, виды обезвоживания. Особенности клиники и лечения. Токсикоз с эксикозом — это своеобразный клинический синдром, характеризующийся обезвоживанием, циркуляторной не достаточностью, катастрофой обмена веществ и аутоинтоксикацией. При острых кишечных инфекциях это состояние является не осложнением, а составной частью основного заболевания, характеризующей его тяжесть. Кишечный токсикоз с эксикозом — патологическое состояние, являющееся результатом действия на макро-организм токсических продуктов и сопровождающееся нарушениями микроциркуляции, водно-электролитного обмена и кислотно-основного резерва. Токсикоз с эксикозом возникает у детей грудного и раннего возраста при кишечных бактериальных и вирусных инфекциях. Виды обезвоживания: — изотоническое (солевой состав крови нормальный); — гипертоническое (повышенная концентрация солей крови); — гипотоническая (сниженная концентрация солей крови) Степени обезвоживания: — легкое обезвоживание (потеря 5-6% или 1-2 л воды); — среднее (потеря 6-10% или 2-4 л); — тяжелое (потеря 10% или более 4 л); — острое (потеря более 10 л воды) – эта степень обезвоживания угрожает жизни.
Клиника.
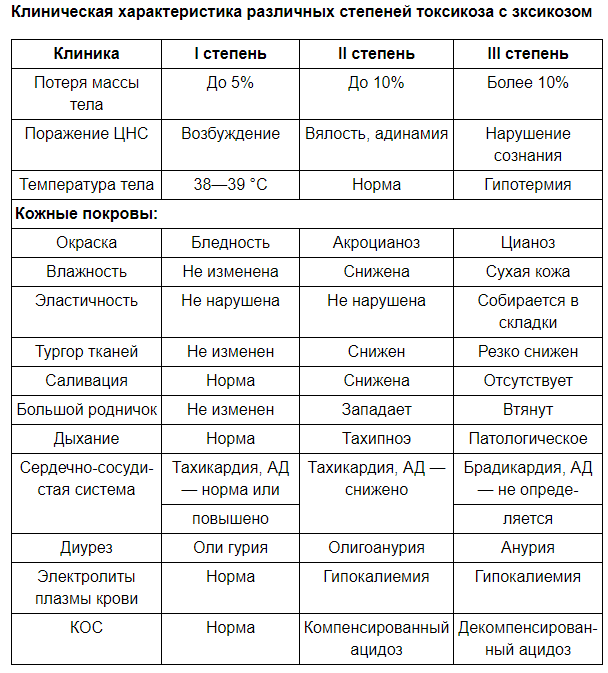 Степени
дегидратации у детей.
При многих инфекционных болезнях в
числе симптомов присутствуют рвота и
частый стул. Чаще всего это наблюдается
при кишечных инфекциях, вызванных
шигеллами, стафилококками, протеем,
сальмонеллами и др. Дегидратация чаще
развивается у детей в связи с компенсаторными
возможностями детского организма.
I
степень – легкая.
Потеря веса составляет до 5% массы тела.
Частота стула и рвоты – до
6 раз в сутки,
умеренная жажда, больные капризны,
возбуждены, тургор и эластичность кожи
сохранены, наблюдается некоторая сухость
слизистых, тоны сердца и качества пульса
в пределах нормы. Наблюдается умеренная
тахикардия, голос сохранен, диурез
уменьшен незначительно, температура
тела повышена.
II
степень – среднетяжелая.
Это стадия потери
внутриклеточного калия и натрия.
Дефицит веса – до 9%. Частота стула и
рвоты – до 10 раз в сутки, жажда резко
выражена, но больные
отказываются от питья,
так как присутствует тошнота. Состояние
беспокойства переходит в вялость и
заторможенность, тургор и эластичность
кожи снижены, складка собирается с
трудом, слизистые оболочки и глазные
яблоки сухие, сердечные тоны приглушены,
значительная тахикардия, пульс слабого
наполнения, температура тела высокая.
Диурез снижен.
Наблюдается небольшая осиплость
голоса.
III
степень – тяжелая.
Это стадия дефицита
солей. Потеря
массы тела составляет более 10%. Стул и
рвота – без счета, больные
отказываются от еды и питья,
наблюдается апатия и адинамия, черты
лица заострены, конечности
холодные на ощупь,
возможна потеря сознания. Тургор кожи
резко снижен, кожная складка не
расправляется, глаза резко запавшие,
мягкие глазные яблоки, слизистые сухие
и кровоточащие, развивается ДВС-синдром,
тоны сердца глухие, брадикардия, диурез
в стадии олигурии, переходящей в анурию.
Температура тела ниже нормы, афония.
Лечение.
По рекомендации ВОЗ проводится пероральная
регидратационная терапия с первых часов
заболевания. Растворы: регидрон,
глюкосалан, изюмный отвар, зеленый чай,
яблочный сок- вода 1:1. В домашних условиях:
на 1 л. кипяченой воды: сахар 8 ч.л., соль
1 ч.л., сода 1 ч.л., изюмный отвар. Соотношение
растворов: регидрон-вода: преобладает
рвота — 2:1, преобладает жидкий стул -
1:2.
I этап
регидратационной терапии: (первые 6
часов).
количество
жидкости за 1 час
= (m*p%*10) / 6
m —масса тела ребенка,
р
— процент потери массы тела
10 —
коэффициент пропорциональности
Жидкость
дается дробно, каждые 10-15 минут.
II
этап регидратационной терапии.
80-100
мл/кг/сут до выведения из эксикоза
Показания для внутривенной
инфузии:
эксикоз II-III ст.
ИТШ.
тяжелая
интоксикация + эксикоз.
олигурия,
анурия.
Сорбционная
терапия — энтеродез,
смекта, полифепам.
иммунотерапия:
пентоксил, лизоцим, КИП, лактоглобулины
направленного действия (шигеллез,
сальмонеллез, эшерихиоз)
ферменты,
бактериофаги, витаминотерапия,
фитотерапия: ромашка, зверобой, кора
дуба, корки граната, черемуха, черника.
противорвотные (церукал, мотилиум).
102.
Вирусные диареи. Этиология. Патогенез,
клиника, лечение, профилактика.
О
вирусной этиологии диареи (включая и
ротавирусную) следует думать лишь в том
случае, когда в патологический процесс
вовлечен только тонкий
отдел кишечника (по
типу энтерита, гастроэнтерита).
Этиология.
Степени
дегидратации у детей.
При многих инфекционных болезнях в
числе симптомов присутствуют рвота и
частый стул. Чаще всего это наблюдается
при кишечных инфекциях, вызванных
шигеллами, стафилококками, протеем,
сальмонеллами и др. Дегидратация чаще
развивается у детей в связи с компенсаторными
возможностями детского организма.
I
степень – легкая.
Потеря веса составляет до 5% массы тела.
Частота стула и рвоты – до
6 раз в сутки,
умеренная жажда, больные капризны,
возбуждены, тургор и эластичность кожи
сохранены, наблюдается некоторая сухость
слизистых, тоны сердца и качества пульса
в пределах нормы. Наблюдается умеренная
тахикардия, голос сохранен, диурез
уменьшен незначительно, температура
тела повышена.
II
степень – среднетяжелая.
Это стадия потери
внутриклеточного калия и натрия.
Дефицит веса – до 9%. Частота стула и
рвоты – до 10 раз в сутки, жажда резко
выражена, но больные
отказываются от питья,
так как присутствует тошнота. Состояние
беспокойства переходит в вялость и
заторможенность, тургор и эластичность
кожи снижены, складка собирается с
трудом, слизистые оболочки и глазные
яблоки сухие, сердечные тоны приглушены,
значительная тахикардия, пульс слабого
наполнения, температура тела высокая.
Диурез снижен.
Наблюдается небольшая осиплость
голоса.
III
степень – тяжелая.
Это стадия дефицита
солей. Потеря
массы тела составляет более 10%. Стул и
рвота – без счета, больные
отказываются от еды и питья,
наблюдается апатия и адинамия, черты
лица заострены, конечности
холодные на ощупь,
возможна потеря сознания. Тургор кожи
резко снижен, кожная складка не
расправляется, глаза резко запавшие,
мягкие глазные яблоки, слизистые сухие
и кровоточащие, развивается ДВС-синдром,
тоны сердца глухие, брадикардия, диурез
в стадии олигурии, переходящей в анурию.
Температура тела ниже нормы, афония.
Лечение.
По рекомендации ВОЗ проводится пероральная
регидратационная терапия с первых часов
заболевания. Растворы: регидрон,
глюкосалан, изюмный отвар, зеленый чай,
яблочный сок- вода 1:1. В домашних условиях:
на 1 л. кипяченой воды: сахар 8 ч.л., соль
1 ч.л., сода 1 ч.л., изюмный отвар. Соотношение
растворов: регидрон-вода: преобладает
рвота — 2:1, преобладает жидкий стул -
1:2.
I этап
регидратационной терапии: (первые 6
часов).
количество
жидкости за 1 час
= (m*p%*10) / 6
m —масса тела ребенка,
р
— процент потери массы тела
10 —
коэффициент пропорциональности
Жидкость
дается дробно, каждые 10-15 минут.
II
этап регидратационной терапии.
80-100
мл/кг/сут до выведения из эксикоза
Показания для внутривенной
инфузии:
эксикоз II-III ст.
ИТШ.
тяжелая
интоксикация + эксикоз.
олигурия,
анурия.
Сорбционная
терапия — энтеродез,
смекта, полифепам.
иммунотерапия:
пентоксил, лизоцим, КИП, лактоглобулины
направленного действия (шигеллез,
сальмонеллез, эшерихиоз)
ферменты,
бактериофаги, витаминотерапия,
фитотерапия: ромашка, зверобой, кора
дуба, корки граната, черемуха, черника.
противорвотные (церукал, мотилиум).
102.
Вирусные диареи. Этиология. Патогенез,
клиника, лечение, профилактика.
О
вирусной этиологии диареи (включая и
ротавирусную) следует думать лишь в том
случае, когда в патологический процесс
вовлечен только тонкий
отдел кишечника (по
типу энтерита, гастроэнтерита).
Этиология.
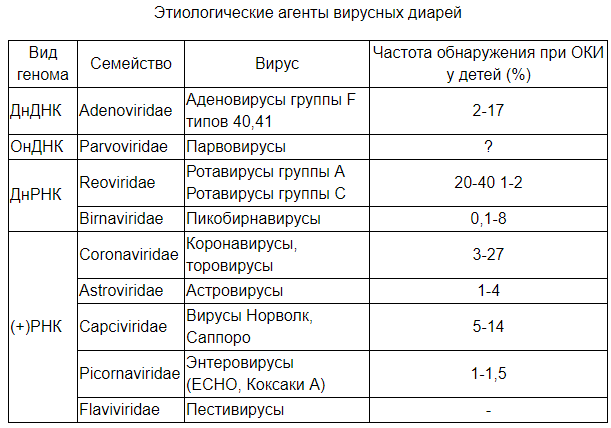 Ротавирусы,
энтеровирусы, астровирусы, корона-вирусы,
аденовирусы, вирусы гр. Норфолка и др.
Механизм
передачи вирусных диарей -
фекально-оральный, чаще через продукты,
которые не подвергаются термической
обработке (салаты, мороженое). Бывают
пищевые и водные вспышки вирусных
диарей.
Патогенез.
При попадании в
желудочно-кишечный тракт ротавирус
проникает в энтероциты
тонкой кишки, где
происходит его размножение.
Этот процесс заканчивается
дистрофическими изменениями
и частичным разрушением
эпителия ворсинок, в
которых, как известно, происходит синтез
дисахаридаз. Их
недостаточный синтез
обусловливает накопление
в просвете кишечника нерасщепленных
дисахаридов.
Нерасщепленные дисахариды и невсосавшиеся
простые сахара во все
возрастающем количестве попадают в
толстую кишку, вызывая
повышение осмотического давления в ее
просвете, что привлекает
воду в просвет кишки и препятствует ее
всасыванию. Гиперосмолярность
химуса. Вследствие этих изменений
возникает диарейный синдром, чему
способствуют снижение активности
натрийи калий-АТФазы и усиление
перистальтики кишечника (БАКТЕРИАЛЬНОЕ
БРОЖЕНИЕ УГЛЕВОДОВ).
В просвете
кишечника обнаруживаются секреторные
иммуноглобулины. Вируснейтрализующие
антитела находят также в грудном молоке,
особенно в молозиве. Присутствием этих
антител объясняют редкость заболеваний
ротавирусной инфекцией у детей,
находящихся на грудном вскармливании.
Напряженность местного и общего
постинфекционного иммунитета бывает
недостаточной, поэтому встречаются
повторные случаи ротавирусного
гастроэнтерита уже спустя 6-12 мес после
перенесенного заболевания. Причиной
повторных заболеваний может быть
заражение другим сероваром
ротавируса.
Клиника.
Вирусные диареи,
как правило, сопровождаются лейкопенией
и лимфоцитозом.
Вирусные
диареи протекают без развития
воспалительного процесса в толстом
кишечнике – поэтому в испражнениях
отсутствуют патологические примеси
(мутная слизь в большом количестве,
кровь), а в копрограмме – лейкоциты и
эритроциты.
Ротавирусная.
Инкубационный
период ( 15 часов) 1-5 дней. Начало
острое, симптомы
интоксикации.
триада
признаков: повышение
температуры, рвота, жидкий стул
(гастроэнтерит или энтерит). Рвота
обильная, водянистая, содержит
примеси пищи и слизи.
Стул
водянистый, пенистый
без патологических примесей,
цвет – желтый
или салатовый.
Вздутие
живота, урчание,
могут быть боли в животе (эпигастральная,
пупочная область).
Эксикоз I, II и III
ст.
Нередко вялость, слабость, снижение
аппетита, часто возникает респираторный
синдром. У части
больных вирусной диареей в первые дни
отмечают ринит,
отек язычка, гиперемию слизистой оболочки
ротоглотки и ее
зернистость. Язык с умеренным налетом,
суховат.
Частота стула:
легкая
форма - 2-5 раз в сутки .
тяжелая форма
- до 20 раз и более.
Длительность диареи
– 3-6 дней.
Диареи
энтеровирусной этиологии наблюдаются
преимущественно у детей раннего возраста
(до 2х лет). Кишечная форма болезни чаще
всего ассоциируется с вирусами ECHO
(5,17,18) и реже -
Коксаки В (1,2 и 5). Диарея может быть как
самостоятельным заболеванием, но чаще
всего развивается в ассоциации с другими
клиническими проявлениями этой инфекции
(эпидемическая миалгия, серозный
менингит, герпетическая ангина,
энцефаломиокардит и др.). Возможно
воспаление
небных миндалин и дужек (герпангина),
на 4-5-е сутки болезни может появляться
пятнистая или пятнисто-папулезная сыпь.
При изолированных формах диареи
заболевание протекает легко по типу
энтерита, летальные исходы не
зарегистрированы. Энтеровирусная диарея
у детей очень часто ассоциируется со
стафилококковой инфекцией и нередко,
особенно у новорожденных, имеет место
генерализация процесса с развитием
сепсиса и летальным исходом.
Диареи
Коксаки-вирусной этиологии у
большинства детей старше 2-3 лет и
школьников протекают в легкой форме на
фоне нормальной
или субфебрильной температуры.
В начале заболевания характерно появление
приступообразных
болей в животе
(иногда симулирующих клинику аппендицита)
и жидкого водянистого
стула (до 3-10 раз в сутки) без патологических
примесей. Спустя
2-3 дня испражнения нормализуются. Иногда
заболевание начинается остро с повышения
температуры тела, появления катаральных
явлений (небольшой ринит, редкий кашель,
гиперемия ротоглотки и др.). Одновременно
или через 1-3 дня появляются боли в животе
и жидкий стул энтеритного
характера, повторная рвота.
Лихорадка держится 3-5 дней, диарейный
синдром 2-3 дня.
У новорожденных
и детей первых 2-х
лет жизни чаще наблюдаются тяжелые
формы инфекции
с токсикозом и выраженным кишечным
синдромом.
Заболевание начинается остро с повышения
температуры тела до высоких цифр
(38-39°C), появляются вялость,
адинамия, повторная рвота,
реже - возбуждение, беспокойство,
судороги. Диарея возникает с первых
дней с частотой
стула до 12-15 раз.
Стул жидкий, обильный с непереваренными
комочками пищи, зеленого цвета, содержит
в небольшом количестве прозрачную
слизь. Нередко развиваются явления
метеоризма.
Одновременно с диарейным синдромом,
быстро приводящим к развитию обезвоживания
организма (токсикозу с эксикозом) и
гемодинамическим нарушениям, появляются
скудные
катаральные явления (заложенность
носа, покашливание, гиперемия и зернистость
задней стенки глотки, дужек и др.).
Катаральные явления
исчезают раньше, чем диарейный синдром.
При гладком течении болезни стул
нормализуется на 7-10 день болезни.
Диареи
ЕСНО-вирусной этиологии могут
быть как у детей, так и у взрослых. У
детей школьного возраста и взрослых
заболевание протекает
в легкой форме с незначительной
дисфункцией кишечника (тошнота,
иногда рвота, кратковременное учащение
стула). У детей первых 2-х лет жизни, в
том числе и у новорожденных, диареи
ЕСНО-вирусной этиологии также в
большинстве случаев протекают легко.
Заболевание начинается остро
с кратковременного (1-2 дня) подъема
температуры тела.
Катаральные явления
появляются одновременно с диареей, но
могут предшествовать или появляться
спустя 2-4 дня.
Поражение респираторного тракта скудное,
кратковременное, но могут иметь место
обильные
слизистые выделения из носа.
Испражнения сохраняют каловый характер,
имеют значительный
объем за счет пузырьков газа.
Каловые массы перемешаны с прозрачной
слизью, имеют ярко- или светло-желтый
цвет. Частота дефекаций не превышает
5-6 раз. У большинства детей увеличиваются
размеры печени и возникают осложнения
(пневмония, отит и др.).
Диареи
реовирусной этиологии чаще
всего наблюдаются при эпидемических
вспышках этой инфекции. Вспышки в детских
коллективах характеризуются симптомами
инфекционного токсикоза, наличием
респираторного
синдрома и диареи.
Чаще всего заболевание начинается
остро.
Температура тела, как правило, субфебрильная
(2-3 дня) или остается в пределах нормы.
Почти
у 1/3 больных со 2-3 дня болезни на лице,
шее и туловище появляется бледно-розовая
мелкопятнистая (типа «краснушной»)
сыпь, исчезающая через сутки без
пигментации.
Катаральные явления слабо выражены.
Характерны признаки двухстороннего
склерита. Одновременно
с катаральными явлениями появляются
боли в животе, вздутие его, учащенный
(до 2-5 раз) жидкий стул без
патологических примесей.
Испражнения обильные, водянистые, при
стоянии разделяются на три слоя:
оседающие вниз каловые массы серо-желтого
цвета, слегка
обесцвеченные, затем жидкая
часть, сверху
пенистый
слой. Нормализация
стула наступает на 5-7 день. У большинства
больных увеличиваются размеры печени
уже с 2-3 дня и отмечается субиктеричность
склер. Исход заболевания благоприятный.
Диареи
аденовирусной этиологии встречаются
довольно часто у детей первых 2-х лет
жизни и новорожденных. В этой возрастной
группе аденовирусная инфекция, более
чем у 50% детей, протекает в легкой
или среднетяжелой форме с развитием
диарейного синдрома.
Чаще всего болезнь начинается постепенно
с нарушений деятельности ЖКТ.
Интоксикация и лихорадка длительные,
часто наблюдается увеличение
лимфатических узлов, печени и селезенки.
Температура тела остается нормальной
или повышается в пределах 38,5°С. У
большинства детей в первые дни возникает
рвота
(1-2 раза). Отмечаются
бледность и одутловатость лица, нередко
- носогубный
цианоз, тахикардия, приглушение тонов
сердца. Кишечный
синдром характеризуется вздутием живота
и жидким стулом. Испражнения обычно не
теряют калового характера, но жидкие,
обильные, серо-зеленого или желто-зеленого
цвета. Частота
стула остается в пределах 3-5 раз в сутки.
Кишечные расстройства могут иметь место
при всех формах аденовирусной инфекции
(пленчатом конъюнктивите,
фарингоконъюнктивальной лихорадке,
пневмонии и др.) и, как правило, не
оказывают существенного влияния на
тяжесть состояния больного.
У детей грудного
возраста и новорожденных заболевание
может принять
тяжелое течение.
В данной возрастной группе чаще всего
начинается с характерных для этой
инфекции катаральных
явлений
(кашель, обильное
отделяемое из носа, одутловатость лица
и др.), но, в дальнейшем, желудочно-кишечные
расстройства выходят на первое место:
появляются срыгивания,
повторная рвота, частый жидкий стул,
вздутие живота.
Быстро развивается токсикоз с эксикозом
с гемодинамическими нарушениями. Нередко
развивается очаговая малосимптомная
пневмония. Характерным для аденовирусных
диарей является полиадения и
гепатоспленомегалия.
Лечение.
Диета. Из
рациона исключают продукты, которые
усиливают перистальтику, например
свежее молоко. Ограничивают употребление
жиров, поскольку они усиливают брожение,
что увеличивает интоксикацию и понос.
Назначают кисломолочные продукты для
ликвидации дисбиоза. Применяют при
вирусной диарее полиферментные препараты
внутрь, в частности фестал, мезим-форте,
панкреатин, пангрол.
По рекомендации
ВОЗ проводится пероральная регидратационная
терапия с первых часов заболевания.
Растворы: регидрон, глюкосалан, изюмный
отвар, зеленый чай, яблочный сок- вода
1:1. В домашних условиях: на 1 л. кипяченой
воды: сахар 8 ч.л., соль 1 ч.л., сода 1 ч.л.,
изюмный отвар. Соотношение растворов:
регидрон-вода: преобладает рвота — 2:1,
преобладает жидкий стул - 1:2.
I
этап регидратационной терапии: (первые
6 часов).
количество
жидкости за 1 час
= (m*p%*10) / 6
m —масса тела ребенка,
р
— процент потери массы тела
10 —
коэффициент пропорциональности
Жидкость
дается дробно, каждые 10-15 минут.
II
этап регидратационной терапии.
80-100
мл/кг/сут до выведения из эксикоза
Показания для внутривенной
инфузии:
эксикоз II-III ст.
ИТШ.
тяжелая
интоксикация + эксикоз.
олигурия,
анурия.
Сорбционная
терапия — энтеродез,
смекта, полифепам.
иммунотерапия:
пентоксил, лизоцим, КИП, лактоглобулины
направленного действия (шигеллез,
сальмонеллез, эшерихиоз)
Сокращает
продолжительность диареи применение
смекты и энтеросорбентов (силлардом П,
энтеросгель, атоксил, полифепан). Для
нормализации микрофлоры кишечника
показаны бактериальные препараты
(бифиформ, симбитер, лактобактерин,
бифидумбактерин и др.). Возможен позитивный
эффект интерферонотерапии (лаферон
ректально).
ферменты, бактериофаги,
витаминотерапия, фитотерапия: ромашка,
зверобой, кора дуба, корки граната,
черемуха, черника. противорвотные
(церукал, мотилиум).
Профилактика.
Больных вирусной
диареей детей изолируют на 10-15 дней.
Проводят текущую и заключительную
дезинфекцию помещения, камерную обработку
одежды и постельного белья.
103.
Простая диспепсия: этиология, патогенез,
клиника, лечение. Профилактика
желудочно-кишечных заболеваний у детей
раннего возраста.
Простая
диспепсия –
острое расстройство пищеварения
функционального характера, проявляющееся
рвотой
и поносом, без
значительного нарушения общего
состояния.
ЭТИОЛОГИЯ.
В этиологии ведущими являются алиментарный
фактор, дефекты
ухода (перегревание, нарушение режима
кормления), а также инфекционный фактор
(чаще всего — кишечная палочка).
Предрасполагающими
факторами являются:
раннее искусственное
и смешанное вскармливание,
рахит, экссудативно-катаральный диатез,
гипотрофия, недоношенность. Укорочение
интервалов в пище.
Патогенез.
При
приеме пищи, не соответствующей возрасту,
или при перекорме, в силу недостаточной
ферментативной активности и низкой
кислотности желудочного сока, у детей
раннего возраста пища недостаточно
обрабатывается в желудке, что приводит
к нарушению физиологического пищеварения.
В пищевом комке
начинают размножаться бактерии,
усиливаются
патогенные свойства постоянной микрофлоры
кишечника, что
приводит к усилению процессов гниения
и брожения,
образованию
газов и токсических
веществ. Раздражение
рецепторов слизистой приводит к усиленной
перистальтике кишечника,
увеличению слизеобразования,
что проявляется срыгиваниями
и поносом.
Бактериальное
расщепление путем гниения и брожения
в кишечнике содействует образованию
токсичных продуктов (индола, скатола,
уксусной кислоты) и газов.
Клиника.
Начинается
остро,
нарушается
сон, появляется
вялость,
снижается
аппетит. Отмечается
жидкий
стул зеленого
цвета, со слизью
и белыми комочками,
частотой 5-8 раз в
сутки, с кислым
запахом. Периодически
возникают кишечные
колики из-за скопившихся газов,
после отхождения которых ребенок
успокаивается. Температура тела чаще
нормальная, но может наблюдаться
субфебрилитет. При осмотре вне приступа
кишечной колики состояние ребенка
относительно удовлетворительное.
Отмечается некоторая бледность кожных
покровов, обложенный язык, иногда –
молочница на слизистой ротовой полости.
Живот вздут, при
пальпации – урчание, в области ануса –
опрелости.
У
ослабленных детей
простая диспепсия может трансформироваться
в токсическую
форму. При этом
появляется лихорадка,
неукротимая рвота, частый (до
15-20 раз в сутки) стул, который быстро
приобретает водянистый
характер с комочками слущенного эпителия.
Значительная потеря жидкости при рвоте
и диарее сопровождается обезвоживанием,
снижением тургора тканей, западением
большого родничка, резким уменьшением
массы тела. Лицо
ребенка приобретает маскообразные
черты с устремленным
в одну точку взглядом; кожа и слизистые
становятся сухими; рефлексы снижаются,
могут возникнуть судороги. Токсическая
диспепсия у детей может привести к
нарушению сознания, развитию комы и
гибели ребенка.
Лечение.
составляет
диетотерапия.
В соответствии с рекомендациями ВОЗ,
голодная водно-чайная диета не назначается
и режим питания не меняется. Ребенок
получает адаптированные смеси,
приготовленные на овоще-зерновой основе,
со сбалансированным углеводно-электролитным
составом и низкой
осмолярностью (HIPP,
ORS-200), которые
имеют абсорбирующие свойства,
уменьшают процессы
брожения, усиливают
процессы регидратации, или грудное
молоко с указанными смесями в соотношении
1:1 или 2:1. Через
4-8 часов ребенка постепенно переводят
на смеси, которые он получал до заболевания,
сначала в соотношении 1:1, затем 2:1, с
ORS-200. Положительное влияние оказывают
фруктовые пюре,
богатые пектинами, дубильными веществами,
витаминами и минеральными солями.
Детям, которые получали до заболевания
прикорм, возобновляют его прием с 3-4 дня
лечения. На фоне диетотерапии, назначают
ферментотерапию (креон 1 кап. х 3-4 раза
в сутки, во время приема пищи, с небольшим
количеством воды, ликреаза 1 кап. х 2-4
раза в сутки; содержимое капсулы раскрыть
и растворить в молоке в течение 2-х нед.).
Симптоматическое
лечение включает отведение
газов через газоотводную трубку,
назначение смекты
(1 пакетик в сутки
в 50 мл кипяченой воды, давать в течение
дня в течение 3-5 дней). При кишечной
колике используют компресс на живот,
лечебные клизмы с валерианой (1 капля
валерианы на месяц жизни ребенка). Для
восстановления кишечной микрофлоры
показаны эубиотики
курсом 2-3
нед.
Среднетяжелые
и тяжелые формы
диспепсии у детей необходимо лечить в
условиях стационара. В лечение включают
парентеральную гидратационную
терапию (переливание
плазмы, плазмозаменяющих и солевых
растворов), симптоматическую терапию
(введение противосудорожных, жаропонижающих,
сердечно-сосудистых средств и т. д.).
Токсическая диспепсия у детей требует
назначения антибактериальных препаратов.
Профилактика.
Рацион
питания ребенка должен соответствовать
его возрасту. Кормящим мамам необходимо
соблюдать сроки и последовательность
прикорма и гигиену кормления. Кроме
того, важно своевременно выявляться
общесоматические и инфекционные
заболевания у детей, чтобы не допустить
их осложнения.
1) Соблюдайте условия
питания и его режим. Полезным будет
частое питание, разделенное на мелкие
порции. Нежелательно пропускать приемы
пищи, особенно завтраки. Перед едой
обязательно необходимо тщательно мыть
руки и все те продукты, которые не будут
подвергнуты тепловой обработке. Это
обезопасит ваш организм от проникновения
в него болезнетворных микроорганизмов.
2)
Соблюдайте правильный рацион питания.
Полезным будет снижение употребления
жареной, жирной, копченой, пересоленной
еды. Кроме того, необходимо увеличить
в рационе содержание клетчатки (овощи
и фрукты, хлеб с отрубями, каши).
Употребляйте как можно больше
грубоволокнистой пищи, свежих салатов,
старайтесь использовать при готовке
меньше уксуса и подобных ему компонентов.
3)
Избегайте переедания. Питайтесь в меру,
помните, что стандартная порция пищи
не должна превышать 300-400 мл, если ее
представить в жидком состоянии. С другой
стороны, нельзя заставлять себя голодать,
питаться необходимо упорядоченно и
правильно.
Ротавирусы,
энтеровирусы, астровирусы, корона-вирусы,
аденовирусы, вирусы гр. Норфолка и др.
Механизм
передачи вирусных диарей -
фекально-оральный, чаще через продукты,
которые не подвергаются термической
обработке (салаты, мороженое). Бывают
пищевые и водные вспышки вирусных
диарей.
Патогенез.
При попадании в
желудочно-кишечный тракт ротавирус
проникает в энтероциты
тонкой кишки, где
происходит его размножение.
Этот процесс заканчивается
дистрофическими изменениями
и частичным разрушением
эпителия ворсинок, в
которых, как известно, происходит синтез
дисахаридаз. Их
недостаточный синтез
обусловливает накопление
в просвете кишечника нерасщепленных
дисахаридов.
Нерасщепленные дисахариды и невсосавшиеся
простые сахара во все
возрастающем количестве попадают в
толстую кишку, вызывая
повышение осмотического давления в ее
просвете, что привлекает
воду в просвет кишки и препятствует ее
всасыванию. Гиперосмолярность
химуса. Вследствие этих изменений
возникает диарейный синдром, чему
способствуют снижение активности
натрийи калий-АТФазы и усиление
перистальтики кишечника (БАКТЕРИАЛЬНОЕ
БРОЖЕНИЕ УГЛЕВОДОВ).
В просвете
кишечника обнаруживаются секреторные
иммуноглобулины. Вируснейтрализующие
антитела находят также в грудном молоке,
особенно в молозиве. Присутствием этих
антител объясняют редкость заболеваний
ротавирусной инфекцией у детей,
находящихся на грудном вскармливании.
Напряженность местного и общего
постинфекционного иммунитета бывает
недостаточной, поэтому встречаются
повторные случаи ротавирусного
гастроэнтерита уже спустя 6-12 мес после
перенесенного заболевания. Причиной
повторных заболеваний может быть
заражение другим сероваром
ротавируса.
Клиника.
Вирусные диареи,
как правило, сопровождаются лейкопенией
и лимфоцитозом.
Вирусные
диареи протекают без развития
воспалительного процесса в толстом
кишечнике – поэтому в испражнениях
отсутствуют патологические примеси
(мутная слизь в большом количестве,
кровь), а в копрограмме – лейкоциты и
эритроциты.
Ротавирусная.
Инкубационный
период ( 15 часов) 1-5 дней. Начало
острое, симптомы
интоксикации.
триада
признаков: повышение
температуры, рвота, жидкий стул
(гастроэнтерит или энтерит). Рвота
обильная, водянистая, содержит
примеси пищи и слизи.
Стул
водянистый, пенистый
без патологических примесей,
цвет – желтый
или салатовый.
Вздутие
живота, урчание,
могут быть боли в животе (эпигастральная,
пупочная область).
Эксикоз I, II и III
ст.
Нередко вялость, слабость, снижение
аппетита, часто возникает респираторный
синдром. У части
больных вирусной диареей в первые дни
отмечают ринит,
отек язычка, гиперемию слизистой оболочки
ротоглотки и ее
зернистость. Язык с умеренным налетом,
суховат.
Частота стула:
легкая
форма - 2-5 раз в сутки .
тяжелая форма
- до 20 раз и более.
Длительность диареи
– 3-6 дней.
Диареи
энтеровирусной этиологии наблюдаются
преимущественно у детей раннего возраста
(до 2х лет). Кишечная форма болезни чаще
всего ассоциируется с вирусами ECHO
(5,17,18) и реже -
Коксаки В (1,2 и 5). Диарея может быть как
самостоятельным заболеванием, но чаще
всего развивается в ассоциации с другими
клиническими проявлениями этой инфекции
(эпидемическая миалгия, серозный
менингит, герпетическая ангина,
энцефаломиокардит и др.). Возможно
воспаление
небных миндалин и дужек (герпангина),
на 4-5-е сутки болезни может появляться
пятнистая или пятнисто-папулезная сыпь.
При изолированных формах диареи
заболевание протекает легко по типу
энтерита, летальные исходы не
зарегистрированы. Энтеровирусная диарея
у детей очень часто ассоциируется со
стафилококковой инфекцией и нередко,
особенно у новорожденных, имеет место
генерализация процесса с развитием
сепсиса и летальным исходом.
Диареи
Коксаки-вирусной этиологии у
большинства детей старше 2-3 лет и
школьников протекают в легкой форме на
фоне нормальной
или субфебрильной температуры.
В начале заболевания характерно появление
приступообразных
болей в животе
(иногда симулирующих клинику аппендицита)
и жидкого водянистого
стула (до 3-10 раз в сутки) без патологических
примесей. Спустя
2-3 дня испражнения нормализуются. Иногда
заболевание начинается остро с повышения
температуры тела, появления катаральных
явлений (небольшой ринит, редкий кашель,
гиперемия ротоглотки и др.). Одновременно
или через 1-3 дня появляются боли в животе
и жидкий стул энтеритного
характера, повторная рвота.
Лихорадка держится 3-5 дней, диарейный
синдром 2-3 дня.
У новорожденных
и детей первых 2-х
лет жизни чаще наблюдаются тяжелые
формы инфекции
с токсикозом и выраженным кишечным
синдромом.
Заболевание начинается остро с повышения
температуры тела до высоких цифр
(38-39°C), появляются вялость,
адинамия, повторная рвота,
реже - возбуждение, беспокойство,
судороги. Диарея возникает с первых
дней с частотой
стула до 12-15 раз.
Стул жидкий, обильный с непереваренными
комочками пищи, зеленого цвета, содержит
в небольшом количестве прозрачную
слизь. Нередко развиваются явления
метеоризма.
Одновременно с диарейным синдромом,
быстро приводящим к развитию обезвоживания
организма (токсикозу с эксикозом) и
гемодинамическим нарушениям, появляются
скудные
катаральные явления (заложенность
носа, покашливание, гиперемия и зернистость
задней стенки глотки, дужек и др.).
Катаральные явления
исчезают раньше, чем диарейный синдром.
При гладком течении болезни стул
нормализуется на 7-10 день болезни.
Диареи
ЕСНО-вирусной этиологии могут
быть как у детей, так и у взрослых. У
детей школьного возраста и взрослых
заболевание протекает
в легкой форме с незначительной
дисфункцией кишечника (тошнота,
иногда рвота, кратковременное учащение
стула). У детей первых 2-х лет жизни, в
том числе и у новорожденных, диареи
ЕСНО-вирусной этиологии также в
большинстве случаев протекают легко.
Заболевание начинается остро
с кратковременного (1-2 дня) подъема
температуры тела.
Катаральные явления
появляются одновременно с диареей, но
могут предшествовать или появляться
спустя 2-4 дня.
Поражение респираторного тракта скудное,
кратковременное, но могут иметь место
обильные
слизистые выделения из носа.
Испражнения сохраняют каловый характер,
имеют значительный
объем за счет пузырьков газа.
Каловые массы перемешаны с прозрачной
слизью, имеют ярко- или светло-желтый
цвет. Частота дефекаций не превышает
5-6 раз. У большинства детей увеличиваются
размеры печени и возникают осложнения
(пневмония, отит и др.).
Диареи
реовирусной этиологии чаще
всего наблюдаются при эпидемических
вспышках этой инфекции. Вспышки в детских
коллективах характеризуются симптомами
инфекционного токсикоза, наличием
респираторного
синдрома и диареи.
Чаще всего заболевание начинается
остро.
Температура тела, как правило, субфебрильная
(2-3 дня) или остается в пределах нормы.
Почти
у 1/3 больных со 2-3 дня болезни на лице,
шее и туловище появляется бледно-розовая
мелкопятнистая (типа «краснушной»)
сыпь, исчезающая через сутки без
пигментации.
Катаральные явления слабо выражены.
Характерны признаки двухстороннего
склерита. Одновременно
с катаральными явлениями появляются
боли в животе, вздутие его, учащенный
(до 2-5 раз) жидкий стул без
патологических примесей.
Испражнения обильные, водянистые, при
стоянии разделяются на три слоя:
оседающие вниз каловые массы серо-желтого
цвета, слегка
обесцвеченные, затем жидкая
часть, сверху
пенистый
слой. Нормализация
стула наступает на 5-7 день. У большинства
больных увеличиваются размеры печени
уже с 2-3 дня и отмечается субиктеричность
склер. Исход заболевания благоприятный.
Диареи
аденовирусной этиологии встречаются
довольно часто у детей первых 2-х лет
жизни и новорожденных. В этой возрастной
группе аденовирусная инфекция, более
чем у 50% детей, протекает в легкой
или среднетяжелой форме с развитием
диарейного синдрома.
Чаще всего болезнь начинается постепенно
с нарушений деятельности ЖКТ.
Интоксикация и лихорадка длительные,
часто наблюдается увеличение
лимфатических узлов, печени и селезенки.
Температура тела остается нормальной
или повышается в пределах 38,5°С. У
большинства детей в первые дни возникает
рвота
(1-2 раза). Отмечаются
бледность и одутловатость лица, нередко
- носогубный
цианоз, тахикардия, приглушение тонов
сердца. Кишечный
синдром характеризуется вздутием живота
и жидким стулом. Испражнения обычно не
теряют калового характера, но жидкие,
обильные, серо-зеленого или желто-зеленого
цвета. Частота
стула остается в пределах 3-5 раз в сутки.
Кишечные расстройства могут иметь место
при всех формах аденовирусной инфекции
(пленчатом конъюнктивите,
фарингоконъюнктивальной лихорадке,
пневмонии и др.) и, как правило, не
оказывают существенного влияния на
тяжесть состояния больного.
У детей грудного
возраста и новорожденных заболевание
может принять
тяжелое течение.
В данной возрастной группе чаще всего
начинается с характерных для этой
инфекции катаральных
явлений
(кашель, обильное
отделяемое из носа, одутловатость лица
и др.), но, в дальнейшем, желудочно-кишечные
расстройства выходят на первое место:
появляются срыгивания,
повторная рвота, частый жидкий стул,
вздутие живота.
Быстро развивается токсикоз с эксикозом
с гемодинамическими нарушениями. Нередко
развивается очаговая малосимптомная
пневмония. Характерным для аденовирусных
диарей является полиадения и
гепатоспленомегалия.
Лечение.
Диета. Из
рациона исключают продукты, которые
усиливают перистальтику, например
свежее молоко. Ограничивают употребление
жиров, поскольку они усиливают брожение,
что увеличивает интоксикацию и понос.
Назначают кисломолочные продукты для
ликвидации дисбиоза. Применяют при
вирусной диарее полиферментные препараты
внутрь, в частности фестал, мезим-форте,
панкреатин, пангрол.
По рекомендации
ВОЗ проводится пероральная регидратационная
терапия с первых часов заболевания.
Растворы: регидрон, глюкосалан, изюмный
отвар, зеленый чай, яблочный сок- вода
1:1. В домашних условиях: на 1 л. кипяченой
воды: сахар 8 ч.л., соль 1 ч.л., сода 1 ч.л.,
изюмный отвар. Соотношение растворов:
регидрон-вода: преобладает рвота — 2:1,
преобладает жидкий стул - 1:2.
I
этап регидратационной терапии: (первые
6 часов).
количество
жидкости за 1 час
= (m*p%*10) / 6
m —масса тела ребенка,
р
— процент потери массы тела
10 —
коэффициент пропорциональности
Жидкость
дается дробно, каждые 10-15 минут.
II
этап регидратационной терапии.
80-100
мл/кг/сут до выведения из эксикоза
Показания для внутривенной
инфузии:
эксикоз II-III ст.
ИТШ.
тяжелая
интоксикация + эксикоз.
олигурия,
анурия.
Сорбционная
терапия — энтеродез,
смекта, полифепам.
иммунотерапия:
пентоксил, лизоцим, КИП, лактоглобулины
направленного действия (шигеллез,
сальмонеллез, эшерихиоз)
Сокращает
продолжительность диареи применение
смекты и энтеросорбентов (силлардом П,
энтеросгель, атоксил, полифепан). Для
нормализации микрофлоры кишечника
показаны бактериальные препараты
(бифиформ, симбитер, лактобактерин,
бифидумбактерин и др.). Возможен позитивный
эффект интерферонотерапии (лаферон
ректально).
ферменты, бактериофаги,
витаминотерапия, фитотерапия: ромашка,
зверобой, кора дуба, корки граната,
черемуха, черника. противорвотные
(церукал, мотилиум).
Профилактика.
Больных вирусной
диареей детей изолируют на 10-15 дней.
Проводят текущую и заключительную
дезинфекцию помещения, камерную обработку
одежды и постельного белья.
103.
Простая диспепсия: этиология, патогенез,
клиника, лечение. Профилактика
желудочно-кишечных заболеваний у детей
раннего возраста.
Простая
диспепсия –
острое расстройство пищеварения
функционального характера, проявляющееся
рвотой
и поносом, без
значительного нарушения общего
состояния.
ЭТИОЛОГИЯ.
В этиологии ведущими являются алиментарный
фактор, дефекты
ухода (перегревание, нарушение режима
кормления), а также инфекционный фактор
(чаще всего — кишечная палочка).
Предрасполагающими
факторами являются:
раннее искусственное
и смешанное вскармливание,
рахит, экссудативно-катаральный диатез,
гипотрофия, недоношенность. Укорочение
интервалов в пище.
Патогенез.
При
приеме пищи, не соответствующей возрасту,
или при перекорме, в силу недостаточной
ферментативной активности и низкой
кислотности желудочного сока, у детей
раннего возраста пища недостаточно
обрабатывается в желудке, что приводит
к нарушению физиологического пищеварения.
В пищевом комке
начинают размножаться бактерии,
усиливаются
патогенные свойства постоянной микрофлоры
кишечника, что
приводит к усилению процессов гниения
и брожения,
образованию
газов и токсических
веществ. Раздражение
рецепторов слизистой приводит к усиленной
перистальтике кишечника,
увеличению слизеобразования,
что проявляется срыгиваниями
и поносом.
Бактериальное
расщепление путем гниения и брожения
в кишечнике содействует образованию
токсичных продуктов (индола, скатола,
уксусной кислоты) и газов.
Клиника.
Начинается
остро,
нарушается
сон, появляется
вялость,
снижается
аппетит. Отмечается
жидкий
стул зеленого
цвета, со слизью
и белыми комочками,
частотой 5-8 раз в
сутки, с кислым
запахом. Периодически
возникают кишечные
колики из-за скопившихся газов,
после отхождения которых ребенок
успокаивается. Температура тела чаще
нормальная, но может наблюдаться
субфебрилитет. При осмотре вне приступа
кишечной колики состояние ребенка
относительно удовлетворительное.
Отмечается некоторая бледность кожных
покровов, обложенный язык, иногда –
молочница на слизистой ротовой полости.
Живот вздут, при
пальпации – урчание, в области ануса –
опрелости.
У
ослабленных детей
простая диспепсия может трансформироваться
в токсическую
форму. При этом
появляется лихорадка,
неукротимая рвота, частый (до
15-20 раз в сутки) стул, который быстро
приобретает водянистый
характер с комочками слущенного эпителия.
Значительная потеря жидкости при рвоте
и диарее сопровождается обезвоживанием,
снижением тургора тканей, западением
большого родничка, резким уменьшением
массы тела. Лицо
ребенка приобретает маскообразные
черты с устремленным
в одну точку взглядом; кожа и слизистые
становятся сухими; рефлексы снижаются,
могут возникнуть судороги. Токсическая
диспепсия у детей может привести к
нарушению сознания, развитию комы и
гибели ребенка.
Лечение.
составляет
диетотерапия.
В соответствии с рекомендациями ВОЗ,
голодная водно-чайная диета не назначается
и режим питания не меняется. Ребенок
получает адаптированные смеси,
приготовленные на овоще-зерновой основе,
со сбалансированным углеводно-электролитным
составом и низкой
осмолярностью (HIPP,
ORS-200), которые
имеют абсорбирующие свойства,
уменьшают процессы
брожения, усиливают
процессы регидратации, или грудное
молоко с указанными смесями в соотношении
1:1 или 2:1. Через
4-8 часов ребенка постепенно переводят
на смеси, которые он получал до заболевания,
сначала в соотношении 1:1, затем 2:1, с
ORS-200. Положительное влияние оказывают
фруктовые пюре,
богатые пектинами, дубильными веществами,
витаминами и минеральными солями.
Детям, которые получали до заболевания
прикорм, возобновляют его прием с 3-4 дня
лечения. На фоне диетотерапии, назначают
ферментотерапию (креон 1 кап. х 3-4 раза
в сутки, во время приема пищи, с небольшим
количеством воды, ликреаза 1 кап. х 2-4
раза в сутки; содержимое капсулы раскрыть
и растворить в молоке в течение 2-х нед.).
Симптоматическое
лечение включает отведение
газов через газоотводную трубку,
назначение смекты
(1 пакетик в сутки
в 50 мл кипяченой воды, давать в течение
дня в течение 3-5 дней). При кишечной
колике используют компресс на живот,
лечебные клизмы с валерианой (1 капля
валерианы на месяц жизни ребенка). Для
восстановления кишечной микрофлоры
показаны эубиотики
курсом 2-3
нед.
Среднетяжелые
и тяжелые формы
диспепсии у детей необходимо лечить в
условиях стационара. В лечение включают
парентеральную гидратационную
терапию (переливание
плазмы, плазмозаменяющих и солевых
растворов), симптоматическую терапию
(введение противосудорожных, жаропонижающих,
сердечно-сосудистых средств и т. д.).
Токсическая диспепсия у детей требует
назначения антибактериальных препаратов.
Профилактика.
Рацион
питания ребенка должен соответствовать
его возрасту. Кормящим мамам необходимо
соблюдать сроки и последовательность
прикорма и гигиену кормления. Кроме
того, важно своевременно выявляться
общесоматические и инфекционные
заболевания у детей, чтобы не допустить
их осложнения.
1) Соблюдайте условия
питания и его режим. Полезным будет
частое питание, разделенное на мелкие
порции. Нежелательно пропускать приемы
пищи, особенно завтраки. Перед едой
обязательно необходимо тщательно мыть
руки и все те продукты, которые не будут
подвергнуты тепловой обработке. Это
обезопасит ваш организм от проникновения
в него болезнетворных микроорганизмов.
2)
Соблюдайте правильный рацион питания.
Полезным будет снижение употребления
жареной, жирной, копченой, пересоленной
еды. Кроме того, необходимо увеличить
в рационе содержание клетчатки (овощи
и фрукты, хлеб с отрубями, каши).
Употребляйте как можно больше
грубоволокнистой пищи, свежих салатов,
старайтесь использовать при готовке
меньше уксуса и подобных ему компонентов.
3)
Избегайте переедания. Питайтесь в меру,
помните, что стандартная порция пищи
не должна превышать 300-400 мл, если ее
представить в жидком состоянии. С другой
стороны, нельзя заставлять себя голодать,
питаться необходимо упорядоченно и
правильно.
ЗАДАЧА
Мать с девочкой 3-х месяцев пришла на профилактический прием к участковому педиатру. Жалоб нет.
Ребенок от III беременности, протекавшей с анемией, гестозом I половины, ОРВИ в III триместре. Предыдущие беременности закончились рождением здоровых детей (мальчик 1,5 года и девочка 4 года). Девочка родилась в срок, с массой тела 3050 г, длиной – 52 см. Период новорожденности без осложнений. На естественном вскармливании до 1 месяца, далее смесь " Агу". Прибавка в массе тела за 3 месяца – 2100 г. В возрасте 2,5 месяцев перенесла ОРВИ. Лечилась симптоматически, на дому.
При осмотре: ребенок удовлетворительного питания. Состояние удовлетворительное. Кожные покровы чистые, бледные, сухие. Слизистые бледные, чистые. Лимфоузлы в группах в пределах возрастной нормы. В легких дыхание пуэрильное, хрипов нет. Тоны сердца ясные, ритмичные. Живот мягкий, безболезненный. Печень +2 см из-под края реберной дуги. Селезенка не пальпируется. Стул 2 раза в день, кашицеобразный, светло-коричневого цвета. Диурез нормальный.
Общий анализ мочи: рН – слабо кислая; белок – 0,33%0; лейкоциты – 1-3 в п/з.
В анализе периферической крови: Нb – 95 г/л (115-175), Эр – 3,7 х 1012/л (3,8-5,6), Ц.п. – 0,77 (0,85-1,15); Л – 8,5 (6,5-13,5) х 10 9л, п/я – 2%(0,5-4), с/я – 32% (15-45), б – 1% (0-1), э – 3% (0,5-7), л – 58% (40-76), м – 4% (2-12), СОЭ - 6 мм/час (4-8), гипохромия ++, анизоцитоз+.
Содержание гемоглобина в эритроцитах – 22 пг (норма 24-33 пг).
1. Ваш диагноз? 2. План лечения
ОТВЕТ: Железодефицитная анемия, легкой степени (1 степени). Леч: препараты железа (3 валентного 3мг/кг) 6-8 недель Сироп -Феррум лек,гемофер, аскорбиновая к-та. смесь «Симилак» с содержанием железа 4,6 мг/100 мл. При анемии же эти добавки необходимо назначать раньше: соки — с двух недель, пюре — с месячного возраста. Для приготовления фруктовых и ягодных соков можно использовать самые разнообразные фрукты и ягоды, но в первую очередь те, которые богаты железом, медью и другими микроэлементами. Это яблоки, сливы, вишни, груши, абрикосы, персики, лимоны, садовая земляника, крыжовник, черная и красная смородина, малина, шиповник. Особенно богаты железом белокочанная и цветная капуста, морковь, редис, редька, свекла, томаты, зеленый горошек.
ЗАДАЧА
Мать с мальчиком 5 месяцев пришла на очередной профилактический прием к педиатру для решения вопроса о проведении вакцинации.
Ребенок от 4 беременности, протекавшей на фоне токсикоза в 1 триместре. Роды в срок, со стимуляцией. Родился с массой тела 3600г, длиной – 53см. Закричал сразу. Естественное вскармливание до 2 месяцев, затем смесь «Агу». Профилактика рахита проводилась масляным раствором витамина D2 с 2 месяцев в течение 1,5 месяцев нерегулярно. В 3 месяца сделана 1 прививка АКДС + полиомиелит, реакции на прививку не наблюдалось. В 4 месяца на прием к врачу не явились.
В течение последних 2 месяцев мать обращает внимание на то, что ребенок стал сильно потеть, вздрагивает во сне, от памперсов резкий запах аммиака.
При осмотре: масса тела 7200г, длина – 64 см. Обращает внимание уплощение и облысение затылка, податливость костей черепа по ходу стреловидного и лямбдовидного швов, размягчение краев большого родничка. Нижняя апертура грудной клетки развернута, заметна Гаррисонова борозда, пальпируются реберные «четки». Большой родничок 4 х 4см. Мышечная гипотония, плохо опирается на ноги. В естественных складках кожи необильные элементы потницы, стойкий красный дермографизм. Слизистые чистые. Дыхание пуэрильное, хрипов нет. Тоны сердца ясные, ритмичные, ЧСС – 120 уд/мин. Живот большой, распластанный, безболезненный. Печень +2,5 см, селезенка + 0,5 см. Стул кашицеобразный, 2-3 раза в день.
Ваш диагноз? План лечения?
ОТВЕТ: Рахит II степени, стадия разгара, подострое течение. Лечение: ГУЛЯТЬ. До проведения анализов – профилактическая доза Вит Д (500-1000, лечебная 2500-3000). При 2 стадии – 4000 МЕ (8кап) суточная, 400ЕД курсовая. Аквадетрим 4-6 недель. С контролем бх и мочи. Начало с 1000 МЕ 3-5 дней. Сколько кальция – если мало, то месяц восполняем кальций. После лечения – профилактические дозы 500 МЕ в сутки.
ЗАДАЧА
Ребенок 6,5 месяцев, родился с массой тела 3200 г. На грудном вскармливании до 2 мес, затем переведен на кормление ацидофильной «Малюткой». С 4 месяцев получает манную кашу.
С 2 мес. потливость, беспокойный сон, пугливость, раздражительность.
Объективно: масса тела 7800, длина 63 см. Тургор тканей и мышечной тонус снижены. Голова гидроцефальной формы. Затылок уплощен. Большой родничок 3х3 см, края размягчены. Выражены лобные бугры. Грудная клетка уплощена, нижняя апертура развернута, выражена гаррисонова борозда, пальпируются «четки». Границы сердца: правая – по правой парастернальной линии, левая – на 1 см кнаружи от левой среднеключичной линии. ЧСС – 130 уд/мин. Тоны сердца ясные, чистые. В легких дыхание пуэрильное, хрипов нет. Живот распластан, мягкий, отмечается расхождение прямых мышц живота. Печень выступает из-под края реберной дуги на 2,5 см, селезенка не пальпируется. Стул со склонностью к запорам. Статомоторное развитие: не сидит, двигательная активность снижена. (6-8 мес)
Общий анализ мочи: эпителия - нет, слизи – нет, лейкоциты – 2-3 в п/з, эритроциты – нет, фосфаты ++.
В анализе периферической крови: Нb – 105 г/л (110-140), Эр – 4,0 х 1012/л, Л – 6,4 х 10 9л, п/я – 3%,с – 23%, э – 4%, л – 60%, м – 10%, СОЭ - 6 мм/час.
1. Ваш диагноз? 2. План лечения?
ОТВЕТ: Рахит II степени, стадия разгара, подострое течение. Лечение: ГУЛЯТЬ, питание. До проведения анализов – профилактическая доза Вит Д (500-1000, лечебная 2500-3000). При 2 стадии – 4000 МЕ (8кап) суточная, 400ЕД курсовая. Аквадетрим 4-6 недель. С контролем бх и мочи. Начало с 1000 МЕ 3-5 дней. Сколько кальция – если мало, то месяц восполняем кальций. После лечения – профилактические дозы 500 МЕ в сутки. При наличии у ребенка признаков рахита необходимо использовать продукты с высоким содержанием кальция и фосфора. В рацион этих детей целесообразно вводить кисломолочные продукты, благотворно влияющие на процессы усвоения пищевых веществ, в том числе кальция. При этом, выбирая исходные продукты, следует обращать внимание на содержание в них витамина С, солей кальция и фосфора. Этими компонентами богаты черная смородина, шиповник, лимон, апельсин, кизил, вишня, черешня, хурма. Все блюда желательно обогащать хорошо измельченной огородной зеленью. Необходимо также часто использовать в питании яичный желток, богатый жирорастворимыми витаминами, солями кальция, фосфора, микроэлементами.
ЗАДАЧА
Ребенок 5 месяцев от молодых, здоровых родителей, родился в срок, осенью. Масса при рождении 3850 г, длина 50 см. Оценка по шкале Апгар 7/8. К груди приложен на 2-е сутки. Грудное вскармливание до 1,5 месяцев, затем - искусственное. Получал неадаптированные смеси: В-рис, с 3 мес. цельное молоко, манную кашу 2 раза в день. Соки, фруктовые пюре не получал. В последние 2 месяца у ребенка отмечается беспокойство, усилилась потливость.
Объективно: облысение затылка, уплощение костей черепа, размягчение их вдоль сагиттального шва и по краям родничка, очаг размягчения теменной кости диаметром 0,8 – 0,9 см. Грудная клетка с развернутой нижней апертурой. Мышечный тонус резко снижен. Гиперестезия. Опора на ноги отсутствует. Живот распластан. Тургор тканей снижен. В легких пуэрильное дыхание, хрипов нет, ЧД – 28 в 1 минуту. Тоны сердца ясные, пульс 120 уд/мин. Печень выступает из-под реберной дуги на 3,5 см, мягкая, безболезненная. Селезенка не пальпируется. Стул со склонностью к запорам.
Общий анализ мочи: количество – 40 мл, лейкоциты – 2-3 в п/з, эритроциты – нет, фосфаты +++.
Общий анализ крови: Нb – 110 г/л (115-175), Эр – 3,6х 1012/л (3.8-5,6), Л – 5,6 х 10 9л, п/я – 2%,с – 31%, э – 2%, л – 56%, м – 9%, СОЭ - 6 мм/час.
1. Ваш диагноз? 2. План лечения?
ОТВЕТ: Рахит II степени, период разгара, острое течение. Лечение: ГУЛЯТЬ, питание. До проведения анализов – профилактическая доза Вит Д (500-1000, лечебная 2500-3000). При 2 стадии – 4000 МЕ (8кап) суточная, 400ЕД курсовая. Аквадетрим 4-6 недель. С контролем бх и мочи. Начало с 1000 МЕ 3-5 дней. Сколько кальция – если мало, то месяц восполняем кальций. После лечения – профилактические дозы 500 МЕ в сутки. При наличии у ребенка признаков рахита необходимо использовать продукты с высоким содержанием кальция и фосфора. В рацион этих детей целесообразно вводить кисломолочные продукты, благотворно влияющие на процессы усвоения пищевых веществ, в том числе кальция. При этом, выбирая исходные продукты, следует обращать внимание на содержание в них витамина С, солей кальция и фосфора. Этими компонентами богаты черная смородина, шиповник, лимон, апельсин, кизил, вишня, черешня, хурма. Все блюда желательно обогащать хорошо измельченной огородной зеленью. Необходимо также часто использовать в питании яичный желток, богатый жирорастворимыми витаминами, солями кальция, фосфора, микроэлементами.
ЗАДАЧА
Ребенок 10 месяцев, поступил в тяжелом состоянии с кашлем, резкой слабостью, выраженной мышечной гипотонией.
Ребенок от первой беременности, протекавшей с нефропатией, первых срочных родов. Первые 7 мес. беременности мать проживала на Севере, питалась в основном консервами. Ребенок до 2 мес. кормился грудью матери, с 2 мес. питание искусственное, адаптиррованными смесями, с 3 мес. – в основном кашами. Ребенок часто (каждые 2 мес.) болел ОРВИ, редко бывал на свежем воздухе. Заболевание началось с 1,5 мес., когда появились беспокойство, потливость, мышечная гипотония. Ребенок отстает в психоморотном развитии, 2 недели назад переболел ОРВИ.
При осмотре: температура тела 37,40С. Ребенок не сидит, не стоит. Масса тела 8200 г, длина 71 см. Кожа сухая, бледная, слизистые рта бледные. Зубы – 0/2, обломаны на уровне шеек, с дефектами эмали. Голова с резко выраженными лобными и затылочными буграми, "олимпийский лоб". Грудная клетка деформирована - "куриная грудь". Нижняя апертура грудной клетки развернута, на ребрах пальпируются выраженные "четки". При попытке посадить ребенка видна деформация позвоночника (кифоз). Ноги: Х-образное искривление. Правая нога короче левой на 1-1,5 см. Живот распластан. Дыхание шумное с удлиненным выдохом. Аускультивно: на фоне жесткого дыхания – сухие свистящие хрипы. ЧД – 36 в 1 минуту. Границы сердца не расширены. Аускультативно: дующий систолический шум на верхушке и в V точке. ЧСС – 136 уд/мин. Печень +4 см из-под реберного края. Селезенка - +2 см из подреберья. Стул через день "овечий". Нервно-психическое развитие: ребенок безучастен, не проявляет интереса к окружающим, игрушкам. Предречевое развитие задержано.
Общий анализ крови: Нb – 100 г/л (110-140), Эр – 3,5х 1012/л (3,5-4,8), Лейк – 7,5 х 10 9л, п/я – 2%,с – 13%, э – 1%, л – 63%, м – 3%, СОЭ - 10 мм/час.
Общий анализ мочи: количество – 40,0 мл (200-300), относительная плотность – 1,012 (1,003-1,035), лейкоциты – 2-3 в п/з, эритроциты – нет.
Биохимический анализ крови: общий белок – 65,0 г/л (57-73), холестерин – 4,6 ммоль/л (1,8-4,9), глюкоза – 4,3 ммоль/л (3,3-6,1), кальций – 2,0 ммоль/л (4,0-5,6), фосфор – 1,1 ммоль (1,3-2,3), ЩФ – 950 Ед/л (норма – до 644).
Рентгенограмма трубчатых костей: выраженный остеопороз, размытость и нечеткость зон предварительного обызвествления.
1. Ваш диагноз 2. План лечения? ОТВЕТ: Рахит III степени (тяжелый), период разгара, подострое течение; железодефицитная анемия I степени; ОРВИ, обструктивный бронхит, ДН0. Лечение: ГУЛЯТЬ, питание. Сначала восполняем КАЛЬЦИЙ 1 мес. КАРБОНАТ КАЛЬЦИЯ - Для лечения у детей кариеса или рахита употребляют по 300 или 600 мг в день. При 3 стадии – 5000 МЕ (10 -12кап) суточная, 500ЕД курсовая. Аквадетрим 4-6 недель. С контролем бх и мочи. Начало с 1000 МЕ 3-5 дней. После лечения – профилактические дозы 500 МЕ в сутки. При наличии у ребенка признаков рахита необходимо использовать продукты с высоким содержанием кальция и фосфора. В рацион этих детей целесообразно вводить кисломолочные продукты, благотворно влияющие на процессы усвоения пищевых веществ, в том числе кальция. При этом, выбирая исходные продукты, следует обращать внимание на содержание в них витамина С, солей кальция и фосфора. Этими компонентами богаты черная смородина, шиповник, лимон, апельсин, кизил, вишня, черешня, хурма. Все блюда желательно обогащать хорошо измельченной огородной зеленью. Необходимо также часто использовать в питании яичный желток, богатый жирорастворимыми витаминами, солями кальция, фосфора, микроэлементами. ЛЕЧЕНИЕ АНЕМИИ: препараты железа (3 валентного 3мг/кг) 6-8 недель Сироп -Феррум лек,гемофер, аскорбиновая к-та. ЛЕЧ ОРВИ: Кислородные ингаляции — необходимый метод лечения с обструктивными нарушениями любой степени тяжести. Применяется увлажненный теплый 30—40% кислород.
ЗАДАЧА
Мальчик 6,5 месяцев, поступил в больницу в плохим аппетитом, недостаточной прибавкой массы тела, неустойчивым стулом.
Ребенок от молодых, здоровых родителе, от первой беременности, протекавшей с токсикозом во второй половине. Во время беременности (на 33-й неделе) мать перенесла ОРВИ, лекарственные препараты не принимала. Роды на 38-й неделе. Мальчик родился в состоянии синей асфиксии. Масса при рождении 2900 г, длина 52 см. Период новорожденности протекал без особенностей. С 3 мес. вскармливание искусственное, беспорядочное, кефиром, с 3,5 мес. – кашами. За 6,5 месяцев ребенок прибавил в массе 3200 (4300) г.
В возрасте 2 мес. заболел пневмонией. Долго лечился антибиотиками в условиях стционара. После выписки из больницы у ребенка неустойчивый стул, часто с примесью зелени и слизи. Аппетит снижен.
При поступлении в стационар состояние ребенка средней тяжести. Масса тела 6100 (7200) г, длина 65 см. Мальчик вялый, иногда беспокоен. Температура тела нормальная. Кожные покровы сухие, бледные, с сероватым оттенком. Кожа с пониженной эластичностью, легко собирается в складки. Подкожно-жировой слой отсутствует на животе, слабо выражен на туловище и конечностях. Большой родничок 2х2 см со слегка податливыми краями. Затылок уплощен. Выражены теменные и лобные бугры, реберные "четки". В легких дыхание пуэрильное, хрипов нет. Границы сердца в пределах нормы. Тоны ритмичные, отчетливые. Над верхушкой сердца систолический шум с музыкальным оттенком, за пределы сердца не проводится. Живот мягкий, доступен глубокой пальпации. Печень выступает из-под края реберной дуги на 1,5 см, селезенка – на 0,5 см. Стул от 3 до5 раз в сутки, желто-зеленый, с неприятным запахом, жидкий.
Общий анализ крови: Нb – 99 г/л (110-140), Эр – 3,3х 1012/л (3,5-4,8), Лейк – 8,1 х 10 9л, п/я – 4%,с – 49%, э – 1%, л – 44%, м – 2%, СОЭ - 9 мм/час.
Общий анализ мочи: реакция - кислая, относительная плотность – 1,015, лейкоциты – 2-2 в п/з, эритроциты – нет.
Бактериологическое исследование кала: дизентерийная группа, кишечная палочка, стафилококк – не выделены.
1. Ваш диагноз? 2. План лечения? ОТВЕТ: Пренатально-постнатальная гипотрофия II ст, 18% ??1 степень; рахит II ст, стадия разгара, подострое течение; анемия I ст; дисбактериоз кишечника?, вторичный синдром нарушенного кишечного всасывания – ПРОСТАЯ ДИСПЕПСИЯ? Лечение: Рахит II степени, период разгара, острое течение. Лечение: ГУЛЯТЬ, питание. До проведения анализов – профилактическая доза Вит Д (500-1000, лечебная 2500-3000). При 2 стадии – 4000 МЕ (8кап) суточная, 400ЕД курсовая. Аквадетрим 4-6 недель. С контролем бх и мочи. Начало с 1000 МЕ 3-5 дней. Сколько кальция – если мало, то месяц восполняем кальций. После лечения – профилактические дозы 500 МЕ в сутки. При наличии у ребенка признаков рахита необходимо использовать продукты с высоким содержанием кальция и фосфора. В рацион этих детей целесообразно вводить кисломолочные продукты, благотворно влияющие на процессы усвоения пищевых веществ, в том числе кальция. При этом, выбирая исходные продукты, следует обращать внимание на содержание в них витамина С, солей кальция и фосфора. Этими компонентами богаты черная смородина, шиповник, лимон, апельсин, кизил, вишня, черешня, хурма. Все блюда желательно обогащать хорошо измельченной огородной зеленью. Необходимо также часто использовать в питании яичный желток, богатый жирорастворимыми витаминами, солями кальция, фосфора, микроэлементами. ЛЕЧЕНИЕ АНЕМИИ: препараты железа (3 валентного 3мг/кг) 6-8 недель Сироп -Феррум лек,гемофер, аскорбиновая к-та. ЛЕЧ. ГИПОТРОфИИ: трехфазное питание :
1) период выяснения толерантности к пище;
2) переходный период;
3) период усиленного (оптимального) питания.
в)систематический учёт фактического питания с расчётом химического состава суточного рациона по основным пищевым нутриентам и энергии;
г)при
гипотрофии 2-3ст., «омоложение диеты» с
преимущественным использованием
грудного молока или специализированных
продуктов.
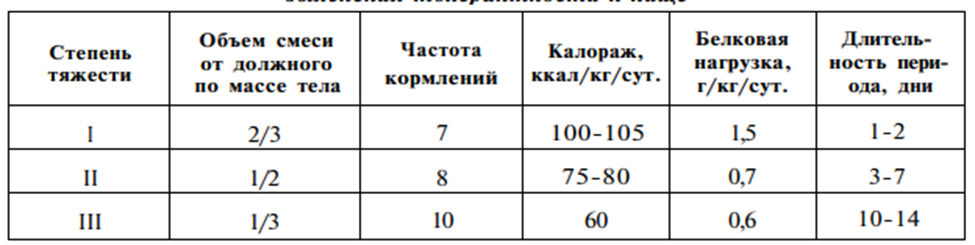 —
использование на начальных этапах
лечения лишь легкоусвояемой пищи
(женское молоко, а при его отсутствии
адаптированные низколактозные
кисломолочные смеси, например лактофидус);
—
использование на начальных этапах
лечения лишь легкоусвояемой пищи
(женское молоко, а при его отсутствии
адаптированные низколактозные
кисломолочные смеси, например лактофидус);
— более частые кормления (7 — при гипотрофии I степени, 8 — при гипотрофии II степени, 10 кормлений при гипотрофии III степени);
— систематический контроль питания (ведение дневника с отметками количества съеденной в каждое кормление пищи), стула, диуреза, количества выпитой и вводимой парентерально жидкости, солей и др.; регулярный (1 раз в 5-7 дней) расчет пищевой нагрузки по белкам, жирам, углеводам; дважды в неделю — копрограмма. Необходимо, чтобы с первого же дня лечения ребенок не терял массу тела, а с 3—4-го дня, даже при тяжелых степенях гипотрофии, начал ее прибавлять по 10—20 г в сутки.
ЗАДАЧА
Девочка 9 месяцев, с врожденным стридором (это высокочастотный, преимущественно инспираторный звук). Заболела остро, с подъема температуры тела до 38,80С, «лающего» кашля, осиплости голоса, слизистого отделяемого из полости носа. К вечеру состояние ухудшилось, появилось затрудненное дыхание, беспокойство. Ребенок был доставлен в больницу.
При поступлении: температура 38,20С, состояние тяжелое, выражена одышка (ЧД – 60 в минуту) инспираторного характера с раздуванием крыльев носа и участием вспомогательной мускулатуры грудной клетки, западение яремной ямки и эпигастрия. Отмечается цианоз носогубного треугольника и кончиков пальцев, «мраморный» оттенок кожи. Голос осиплый. Зев гиперемирован. Умеренно выражены катаральные явления. Беспокоит частый непродуктивный кашель. Тоны сердца приглушены, аритмичны (ЧСС – 100-130 в мин.) Выпадение пульсовой волны на вдохе. В легких дыхание жесткое.
Проведена ларингоскопия: вход в гортань 1-2 мм, во входе в гортань – большое количество слизистой мокроты прозрачного цвета, яркая гиперемия черпаловидных хрящей, подсвязочного пространства, подсвязочного пространства, отек голосовых связок.
На рентгенограмме грудной клетки усиление сосудистого рисунка, правая доля вилочковой железы увеличена, у корня правого легкого треугольная тень (ателектаз?).
КОС: рН – 7,31 (7,37-7,46) АЦИДОЗ; РСО2 – 41,1 (26-41) , РО2 – 70,1 (60-80), ВЕ=-3,6 (-6,4+ 0,4).
Вирусологическое исследование мазка из носоглотки в реакции иммунофлюоресценции:
Парагрипп (+) грипп (-) РС (-) Адено (-)
Клинический анализ крови: Нb – 130 г/л, Эр – 3,5 х 1012/л, Ц.п. –0,89, Лейк – 8,3 х 10 9л, п/я – 3%, с/я – 41%, э –2%, л – 45%, м – 9%, СОЭ - 10 мм/час;
1. Ваш диагноз? 2. План лечения? ОТВЕТ: ОРВИ (парагрипп), синдром крупа, стеноз гортани III степени. Лечение: Тип 1 парагриппа чаще вызывает круп. Назначают постельный режим и симптоматические средства. Питание должно быть полноценным, легкоусвояемым, без существенного ограничения пищевых ингредиентов. Пищу дают в теплом виде. При температуре более 38,5°С назначают жаропонижающие средства. При кашле назначают отхаркивающие средства и препараты, разжижающие мокроту. При насморке назначают сосудосуживающие средства. Однако их нельзя применять дольше 5-7 дней. Кроме того, полезно промывать нос раствором морской соли. Широко используется при лечении парагриппа фитотерапия – потогонные (малина, липа), отхаркивающие (солодка, мать-и-мачеха), противовоспалительные (ромашка, шалфей, эвкалипт, календула) средства. При III-IV степени стеноза: немедленная интубация трахеи термопластическими трубками.
• оксигенотерапия в условиях паракислородной палатки;
• преднизолон в дозе 5-7 мг/кг в/м или в/в;
• вызов реанимационной бригады для проведения прямой ларингоскопии и интубации трахеи;
• при отсутствии эффекта от вышеперечисленных мероприятий обеспечить ИВЛ.
при III-IV степени — в реанимационное отделение. 2. инфузионную терапию, включающую гипертонические растворы хлористого кальция (10% 1 мл/год жизни), глюкозы (20% 10 – 20 мл), аскорбиновую кислоту (5% 1 мл/год жизни), глюкокортикостероидные препараты - преднизолон (1 – 3 мл/кг) или дексаметазон 0,6 мг/кг, эуфиллин (2,4% - 0,2 мл/кг). 3. седативные препараты (димедрол 1% - 0,2 – 0,5 мл при отсутствии вязкой мокроты в бронхах; реланиум, седуксен 0,1% - 0.5 – 1,0 2 –3 раза в сутки; оксибутират натрия 50 – 120 мг/кг в/в). коррекцию кислото-щелочного состояния, кардиотоники, диуретики, жаропонижающие средства.
ЗАДАЧА
Девочка Р., 5 дней, от первой беременности, протекавшей с легким токсикозом в 1-й половине, срочных родов. Масса тела при рождении 3100 г, длина тела 51 см. Оценка по шкале Апгар 8/9 баллов. Закричала сразу, к груди приложена через 2 часа после рождения. Состояние за время наблюдения в последующие дни жизни удовлетворительное. Первые дни теряла в массе, масса тела на 4-е сутки составила 2950 г. На 5-е сутки появилось нагрубание молочных желез.
При осмотре на 5-й день жизни состояние удовлетворительное, сосет хорошо, активна, масса тела 3000 г. физиологические рефлексы вызываются. Мышечный тонус удовлетворительный. Кожные покровы розовые, на коже лица, больше на крыльях носа, переносице, имеются беловато-желтоватые мелкие узелки, на коже груди и живота – крупнопластинчатое шелушение. Молочные железы увеличены с обеих сторон до 2 см, при надавливании выделяется бело-молочная жидкость; пупочная ранка чистая. В легких дыхание пуэрильное, сердечные тоны отчетливые. Живот мягкий, безболезненный. Печень выступает из-под края реберной дуги на 1 см, умеренной плотности, селезенка не пальпируется. Стул с непереваренными комочками, прожилками слизи.
Общий анализ крови: Нb – 186 г/л, Эр – 5,6х 1012/л, Ц.п. – 0.94, Лейк – 6,4 х 10 9л, п/я – 5%,с – 42%, э – 1%, л – 45%, м – 7%, СОЭ - 2 мм/час.
Общий анализ мочи: цвет - соломенно-желтый, реакция – кислая, удельный вес – 1004 (1,003-1,035), белок отсутствует, эпителий плоский – много, лейкоциты – 2-3 в п/з. эритроциты – 4-5 в п/з, цилиндры нет. Соли – кристаллы мочевой кислоты.
Биохимический анализ крови: общий белок – 52.4 г/л (49-69), билирубин: непрямой – 51 (12,8-55,2) мкмоль/л, прямой – нет (4,3-12,8), мочевина – 4,2 ммоль/л (2,5-4,5), холестерин – 3,6 ммоль/л (1,6-3,0 холестаз), калий – 5,1 ммоль/л(4,5-6,5), натрий – 141 ммоль/л (135-155), кальций – 2,2 ммоль/л (2,2-2,5), фосфор – 1,9 ммоль (1,8-2,7).
Задание:
1. Какие пограничные состояния наблюдаются у данного ребенка?
2. За счет чего отмечалось падение веса в первые дни жизни?
3. Как должна вести себя весовая кривая в ближайшие дни?
4. Чем объяснить нагрубание молочных желез? Необходим ли осмотр хирурга?
5. Чем обусловлено наличие крупнопластинчатого шелушения? Необходим ли осмотр дерматолога?
ОТВЕТ: 1.пограничные состояния – физиологическая потеря массы тела (обезвоживание с дых и мочой), физиологическое шелушение, половой криз (нагрубание в железах из-за гормонов в молоке), транзиторный катар кишечника (бифидобактерии), мочекислая нефропатия (отложение мочевой кислоты в почках в виде кристаллов), милиа (сальные железы закупорка). 2. потеря массы тела в первые дни – физиологическая потеря (моча, кал, сниженное питание, дыхание). 3. Весовая кривая на 10 день должна достигнуть исходного уровня. В норме убыль массы не превышает 6—10 % и в значительной степени зависит от объема введения пищи и жидкости. Восстановление массы тела происходит к 6—8-му дню жизни. 4. нагрубание молочных желез – состояние появл. у 2/3 новорожденных детей(чаще девочки), связано с высоким уровнем половых гормонов в крови матери и пуповинной крови ребенка в женском молоке(прогестерон, эстрадиол, пролактин), достигает максимума к 8-10 дню, затем постепенно степень нагрубания снижается, нужно соблюдать правила гигиены и местно можно применять сухое тепло или компрессы с камфорным спиртом. 5. физиологическое шелушение кожных покровов возникает на 3-5 день жизни у детей с особенно яркой простой эритемой при ее угасании, чаще на животе и груди, особенно обильное шелушение отмечается у переношенных детей, проходит само. Реактивная краснота кожи возникает после удаления первородной смазки, первой ванны.
ЗАДАЧА
Девочка О., 4 дня, находится в родильном доме.
Из анамнеза известно, что ребенок от первой беременности, протекавшей с токсикозом в 1-й половине. Роды срочные. Масса тела при рождении 3100 г, длина тела 51 см. Оценка по шкале Апгар 8/9 баллов. Закричала сразу, к груди приложена через два часа после рождения. Сосала хорошо. На 3-и сутки появилась иктеричность кожных покровов.
При осмотре на 4-й день жизни состояние удовлетворительное, сосет хорошо, крик громкий. Кожные покровы чистые, умеренно иктеричны, пупочная ранка чистая. В легких дыхание пуэрильное, сердечные тоны звучные, живот мягкий, печень выступает из-под рая реберной дуги на 1 см, селезенка не пальпируется. Стул желтого цвета. Физиологические рефлексы вызываются. Мышечный тонус удовлетворительный.
Группа крови матери А (II) Rh-положительная.
Группа крови ребенка 0 (I) Rh-положительная.
Общий анализ крови: Нb – 196 г/л, Эр – 5,9х 1012/л, ретикулоциты – 1,5%, Ц.п. – 0.94, Лейк – 9,0х 10 9л, п/я – 5%,с – 42%, э – 1%, л – 47% (12-36), м – 5%, СОЭ - 2 мм/час.
Общий анализ мочи: цвет - соломенно-желтый, реакция – кислая, удельный вес – 1004, белок отсутствует, эпителий плоский – немного, лейкоциты – 2-3 в п/з. эритроциты – нет, цилиндры нет.
Биохимический анализ крови: на 4-й день жизни: общий белок – 52.4 г/л, билирубин: непрямой – 140 мкмоль/л (12,8-55,2), прямой – нет, мочевина – 4,2 ммоль/л, холестерин – 3,6 (до 3)ммоль/л, калий – 5,1 ммоль/л, натрий – 141 ммоль/л, АЛТ – 25 ммоль/ (до 40), АСТ – 18 ммоль/л (до 40). Задание:
1. Поставить диагноз?
2. Как вы оцениваете массо-ростовой показатель при рождении?
3. Оцените результаты общего анализа крови?
4. Оцените результаты общего анализа мочи?
5. Оцените результаты биохимического анализа крови. С чем связаны выявленные изменения?
1. физиологическая желтуха новорожденных. 2. массово/ростовой показатель = 60,7 (норма 60-80) 3. ретикулоцитоз связан с гемолизом фетального гемоглобина, С я.=Лф (физ.перекрест). 4. Норма. 5. повыш. непрямой Б т.к. повышен распад фет. гемоглобина, незначительно повышен холестерин, т.к. имеется холестаз.
ЗАДАЧА
Мальчик Г., 1 суток жизни, находится в родильном доме.
Из анамнеза известно, что матери 25 лет, она имеет А (II) Rh- отрицательную группу крови. Первая беременность была 3 года назад, закончилась медицинским абортом при сроке 9 недель, осложнений не было.
Настоящая беременность вторая, протекала с токсикозом в первом триместре, в третьем триместре периодически отмечались подъемы АД до 145/90 мм. рт. ст. В женской консультации наблюдалась нерегулярно. Роды срочные, самостоятельные 1-й период – 6 часов 30 минут. 2-й – 25 мину, безводный промежуток – 3 часа. Масса тела при рождении 3300 г, длина тела 51 см. Оценка по шкале Апгар 7/8 баллов. Сразу при рождении было отмечено желтушное прокрашивание кожных покровов, оболочек пуповины и околоплодных вод.
При первом осмотре педиатра выявлено увеличение размеров печени до +3 см и селезенки до 1.5 см.
При дополнительном обследовании:
Билирубин пуповинной крови составил 105 мкмоль/л (17-68).
В биохимическом анализе крови новорожденного, взятом в возрасте 4 часов жизни. Уровень непрямого билирубина составил 175 мкмоль/л (12,8-55,2).
Hb периферической крови, определенный по cito, 149 г/л (180-240).
Задание:
1. О каком заболевании с большей вероятностью можно думать в данном случае?
2. Оцените результаты исследования, проведенного новорожденному в родильном доме.
3. Какое обследование следует провести ребенку для уточнения диагноза?
4. Какие изменения можно ожидать в общем анализе крови?
5. Какие изменения можно выявить при проведении УЗИ органов брюшной полости?
ОТВЕТ: Гемолитическая болезнь новорожденных ГБН( вероятностно обусловленный Rh несовместимостью). 2. ЗПК: Б/р пуп крови>60 мкмоль/л(105), абс. показатель для ЗПК+низки. ур-нь Hb периф. крови – 149/г/л(абс пок-ль 100). При общем билирубине (ОБ) пуповинной крови ≥ 68 мкМ/л, гемоглобине (Hb) < 120 г/л проводится частичное заменное переливание крови (ЗПК) (замена 45-90 мл/кг крови ребенка на эритромассу О(I) Rh(-). 3. доп. обсл. для уточнения определение группы крови и Rh фак. Ребенка. 4. ОАК – анемия, рет-3, псевдолейк -3 из-за увеличен. нормо-, эритробластов. О безусловной эффективности проведенной ОПК свидетельствует более чем двукратное снижение концентрации билирубина к концу операции. 5. УЗИ увеличение печени и селезенки.
ЗАДАЧА
Мальчик А., 4 дней. Поступил в отделение патологии новорожденных из родильного дома по поводу выраженной желтухи.
Из анамнеза известно, что ребенок от женщины 23 лет, имеющей 0 (I) Rh-отрицательную группу крови. Отец ребенка имеет А (II) Rh- отрицательную группу крови.
Первая беременность закончилась медицинским абортом при сроке 10 недель. Настоящая беременность вторая, протекала с гестозом во второй половине. Роды срочные. Масса при рождении 3200 г, длина тела 52 см. Закричал сразу. Крик громкий. К концу первых суток отмечена иктеричность кожных покровов и склер. На вторые сутки желтуха усилилась.
При поступлении в стационар состояние тяжелое, выраженная иктеричность кожных покровов и склер, ребенок вялый, отмечается мышечная гипотония, гипорефлексия. Печень выступает из-под края реберной дуги на 2,5 см, селезенка у реберного края. Стул переходный.
Общий анализ крови: Нb – 141 г/л (180-240), Эр – 3,9х 1012/л (4,3-7,6), Ц.п. – 0.99, Лейк – 9,4х 10 9л, п/я – 7%,с – 53%, э – 1%, л – 32%, м – 7%, СОЭ - 2 мм/час.
Биохимический анализ крови на 2-й день жизни: общий белок – 54,4 г/л, билирубин: непрямой – 180 мкмоль/л (12,8-55,2), прямой – нет.
Задание:
1. Поставьте и обоснуйте диагноз.
2. Какие обследования надо провести дополнительно для уточнения диагноза?
3. Каковы возможные результаты дополнительного обследования?
4. Каков патогенез выявленных клинических симптомов?
5. Какие изменения могут быть выявлены при осмотре невропатолога?
ОТВЕТ:1. ГБН(гемолитическая болезнь новорожденных) обусл АВО несовм, обосн: мать1(0), отец 2(А), аборт при 1й бер-ти, желтуха на 1х сутках, интоксикация, незнач. увел. печени, Н. б/р – 180, анем Hb-141, белок – 54. Например, если мать имеет группу крови О, а плод имеет группу крови A или B, и организм матери производит антитела к А или B. 2. Доп. опред. гр.кр.ребенка, ОАК+ ретикулоциты, опред-е титра агглютинов в крови и молоке матери, проба Кумбса - анализ на антиэритроцитарные антитела. 3. Что м.б.в анал: Гр. кр2(а) в ОАК – ретикулоцитоз, Ув. титра иммун ат, прям, проба Кумбса слабо+. цитотоксических Т-лимфоцитов (ЦТЛ). 4. Антитела, возникшие после иммунизации матери групповыми антигенами и относящиеся к IgG, в отличие от естественных, свободно проходят и через нормальную плаценту, вызывая гемолиз. Развивающаяся анемия вызывает компенсаторную реакцию организма, возникновение экстрамедуллярных очагов кроветворения с последующей гепатоспленомегалией. Продукты распада эритроцитов стимулируют костный мозг к образованию молодых незрелых форм красной крови. В результате преобладания процессов разрушения у плода развивается анемия. Появление и усиление желтухи при гемолтической болезни связано с увелечением содержания в крови непрямого билирубина. При ограниченной возможности печени в отношении перевода непрямого билирубина в прямой, переработка продуктов обмена веществ оказывается для нее большой натрузкой в связи с чем наблюдается быстрое накопление непрямого билирубина. В результате происходит перегрузка печени железом, билирубиновыми пиг ментами и нарушается ее функция, особенно синтез белков, что ведет к гипопротеинемии и к усилению проницаемости сосудов. Возникает сердечная недостаточность и увеличенная печень приводят к выведению жидкости в ткани и развивается анасарка. 5. невропатол. монотонный крик, неполн. выр. рефлекс Моро(1фаза), «блуждающий взгляд». ЗАДАЧА
Ребенку 7 дней, масса тела 3500,0. Находится на естественном вскармливании. Назначьте питание на сутки.
