
- •Основные положения теории химического строения а.М.Бутлерова.
- •Изомерия: структурная, пространственная.
- •А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
- •Б) Пространственная изомерия алкенов
- •Строение электронных подуровней атома углерода. Гибридное состояние атомных орбиталей: sp3-; sp2-; sp-гибридизации. Понятие о σ и π- связях.
- •Классификация органических соединений. Понятие гомологический ряд. Функциональная группа.
- •1. Классификация органических соединений в зависимости от строения цепи (углеродного скелета)
- •2. Классы органических соединений в зависимости от природы функциональных групп
- •Механизмы химических реакций. Гомолитический и гетеролитический разрывы химической связи. Радикальный, электрофильный и нуклеофильный механизмы реакций (схемы).
- •1. Гомолитический (радикальный) разрыв связей.
- •1. Гомологический ряд алканов: общая формула, названия
- •2. Пространственное строение молекул
- •3. Номенклатура предельных углеводородов
- •4. Физические свойства
- •1. Реакции замещения
- •1.1. Галогенирование
- •1.2. Нитрование алканов
- •2. Реакции разложения
- •2.1. Дегидрирование и дегидроциклизация
- •2.2. Пиролиз (дегидрирование) метана
- •2.3. Крекинг
- •3. Реакции окисления алканов
- •3.1. Полное окисление – горение
- •3.2. Каталитическое окисление
- •4. Изомеризация алканов
- •Получение алканов
- •1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- •2. Водный или кислотный гидролиз карбида алюминия
- •3. Электролиз солей карбоновых кислот (электролиз по Кольбе)
- •4. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- •5. Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
- •6. Синтез Фишера-Тропша
- •7. Получение алканов в промышленности
- •2. Изомерия алкенов
- •А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
- •Б) Пространственная изомерия алкенов
- •4. Получение алкенов
- •5. Физические свойства алкенов
- •6. Химические свойства алкенов
- •Изомеризация алкенов
- •1. Химические свойства алкенов
- •11.2 Номенклатура алкинов (ацетилена)
- •11.3 Изомерия алкинов
- •2. Галогенирование.
- •11.5 Получение алкинов
- •11.6 Физические свойства алкинов
- •11.7 Реакции присоединения: реакция Кучерова (гидратация этина).
- •1. Строение спиртов
- •2. Номенклатура
- •3. Классификация
- •4. Изомерия спиртов
- •5. Физические свойства
- •6. Способы получения спиртов
- •7. Основно-кислотные свойства.
- •8. Химические свойства одноатомных спиртов
- •2. Окисление
- •3.Реакции отщепления
- •4. Реакции этерификации
- •Химические свойства альдегидов и кетонов. Реакции присоединения по двойной связи карбонильной группы (получение полуацеталей и ацеталей). Реакции конденсации.
- •Номенклатура
- •Классификация
- •В) Гетерофункциональные карбоновые кислоты
- •Лабораторный синтез Реакция Канниццаро:
- •Реакция Гриньяра:
- •Производные карбоновых кислот. Номенклатура. Способы получения солей, сложных эфиров, галогенангидридов, ангидридов, амидов, нитрилов. Понятия анион и ацил.
- •Осбенности строение ароматических аминов (на примере анилина)
- •1. Получение аминов при взаимодействии алкилгалогенидов с аммиаком (реакция Гофмана).
- •Ароматические углеводороды. Бензол: строение, изомерия, номенклатура
- •Структура бензола
4. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия:
![]()
5. Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
При гидрировании этилена образуется этан:
![]()
При полном гидрировании ацетилена также образуется этан:
![]()
При гидрировании циклопропана образуется пропан:
![]()
6. Синтез Фишера-Тропша
Из синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды:
nCO + (3n+1)H2 = CnH2n+2 + nH2O
Это промышленный процесс получения алканов.
7. Получение алканов в промышленности
В промышленности алканы получают из нефти, каменного угля, природного и попутного газа. При переработке нефти используют ректификацию, крекинг и другие способы.
Алкены. Двойная связь (sp2- гибридизация). Изомерия. Номенклатура. Способы получения: элиминирование галогеноводорода из алкилгалогенидов, элиминирование воды из спиртов, дегалогенирование виц-дигалогеналканов. Физические и химические свойства.
Алкены – это ненасыщенные, ациклические углеводороды, которые:
- имеют общую формулу молекул CnH2n, где n – число атомов углерода;
- второе название – «олефины»;
- первый представитель этого класса – этилен (этен по ИЮПАК) СН2=СН2, в связи с чем алкены также называются этиленовыми углеводородами;
Гибридизация алкенов (sp2-гибридизация)
В алкенах два атома углерода находятся в состоянии sp2-гибридизации и связаны друг с другом двойной, σ-π связью. Остальные атомы углерода в молекуле (при их наличии) находятся в состоянии sp3-гибридизации и связаны друг с другом одинарно σ связью.
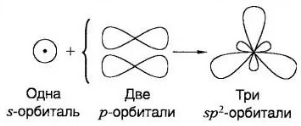
В гибридизации орбиталий атома углерода в этене участвуют:
- две p- орбитали и одна s- орбиталь,
Одна р - орбиталь не участвует в гибридизации.
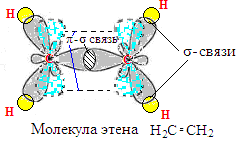
Всего в молекулу этена шесть связей:
- четыре одинарные σ –связи (углерода с водородом);
- двойная σ- π связь (между атомами углерода).
2. Изомерия алкенов
Для алкенов характерна структурная и пространственная изомерия.
А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
1. Изомерия цепи (углеродного скелета)- начиная с С4Н8.
Первые два члена гомологического ряда – этен и пропен – изомеров, относящихся к классу алкенов, не имеют.
Простейший алкен, у которого есть изомерия углеродного скелета — это бутен (С4Н8):
2. Изомерия положения двойной связи (также начинается с бутена - С4Н8):
3. Межклассовая изомерия, начиная с С3Н6 (алкены изомерны другому классу соединений — циклоалканам).
