- •Основные положения теории химического строения а.М.Бутлерова.
- •Изомерия: структурная, пространственная.
- •А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
- •Б) Пространственная изомерия алкенов
- •Строение электронных подуровней атома углерода. Гибридное состояние атомных орбиталей: sp3-; sp2-; sp-гибридизации. Понятие о σ и π- связях.
- •Классификация органических соединений. Понятие гомологический ряд. Функциональная группа.
- •1. Классификация органических соединений в зависимости от строения цепи (углеродного скелета)
- •2. Классы органических соединений в зависимости от природы функциональных групп
- •Механизмы химических реакций. Гомолитический и гетеролитический разрывы химической связи. Радикальный, электрофильный и нуклеофильный механизмы реакций (схемы).
- •1. Гомолитический (радикальный) разрыв связей.
- •1. Гомологический ряд алканов: общая формула, названия
- •2. Пространственное строение молекул
- •3. Номенклатура предельных углеводородов
- •4. Физические свойства
- •1. Реакции замещения
- •1.1. Галогенирование
- •1.2. Нитрование алканов
- •2. Реакции разложения
- •2.1. Дегидрирование и дегидроциклизация
- •2.2. Пиролиз (дегидрирование) метана
- •2.3. Крекинг
- •3. Реакции окисления алканов
- •3.1. Полное окисление – горение
- •3.2. Каталитическое окисление
- •4. Изомеризация алканов
- •Получение алканов
- •1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- •2. Водный или кислотный гидролиз карбида алюминия
- •3. Электролиз солей карбоновых кислот (электролиз по Кольбе)
- •4. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- •5. Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
- •6. Синтез Фишера-Тропша
- •7. Получение алканов в промышленности
- •2. Изомерия алкенов
- •А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
- •Б) Пространственная изомерия алкенов
- •4. Получение алкенов
- •5. Физические свойства алкенов
- •6. Химические свойства алкенов
- •Изомеризация алкенов
- •1. Химические свойства алкенов
- •11.2 Номенклатура алкинов (ацетилена)
- •11.3 Изомерия алкинов
- •2. Галогенирование.
- •11.5 Получение алкинов
- •11.6 Физические свойства алкинов
- •11.7 Реакции присоединения: реакция Кучерова (гидратация этина).
- •1. Строение спиртов
- •2. Номенклатура
- •3. Классификация
- •4. Изомерия спиртов
- •5. Физические свойства
- •6. Способы получения спиртов
- •7. Основно-кислотные свойства.
- •8. Химические свойства одноатомных спиртов
- •2. Окисление
- •3.Реакции отщепления
- •4. Реакции этерификации
- •Химические свойства альдегидов и кетонов. Реакции присоединения по двойной связи карбонильной группы (получение полуацеталей и ацеталей). Реакции конденсации.
- •Номенклатура
- •Классификация
- •В) Гетерофункциональные карбоновые кислоты
- •Лабораторный синтез Реакция Канниццаро:
- •Реакция Гриньяра:
- •Производные карбоновых кислот. Номенклатура. Способы получения солей, сложных эфиров, галогенангидридов, ангидридов, амидов, нитрилов. Понятия анион и ацил.
- •Осбенности строение ароматических аминов (на примере анилина)
- •1. Получение аминов при взаимодействии алкилгалогенидов с аммиаком (реакция Гофмана).
- •Ароматические углеводороды. Бензол: строение, изомерия, номенклатура
- •Структура бензола
Основные положения теории химического строения а.М.Бутлерова.
Зависимость свойств органических соединений от химического строения.
1-е положение. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям.
2-е положение. Свойства веществ зависят не только от качественного и количественного состава, но и от порядка соединения атомов в молекуле.
Явление, при котором может существовать несколько веществ, имеющих один и тот же состав и одну и ту же молекулярную массу, но различающихся строением молекул и свойствами, называют явлением изомерии.
С увеличением числа атомов углерода в молекулах углеводородов увеличивается число изомеров. Например, для состава С5Н12 существуют три изомера:
- нормальный пентан CH3(CH2)3СН3 (н-пентан),
- изопентан (СН3)2СНСН2СН3 (2-метилбутан)
- неопентан (СН3)4С (2,2-диметилпропан).
3-е положение. По свойствам вещества можно определить строение его молекулы, а по строению - предвидеть свойства.
Для примера, рассмотрим основные свойства алканов (класс насыщенных углеводородов):
- для представителей этого класса углеводородов не характерны реакции присоединения, поскольку все связи в молекуле одинарные (насыщенные, и очень прочные);
- алканы вступают в реакции замещения атома водорода на галоген (галогенирование) по радикальному механизму (замещение нейтрального атома водорода на нейтральный радикал галогена с неспаренным электроном);
- для алканов характерно взаимодействие с кислородом воздуха. При горении в качестве продуктов реакции выступает углекислый газ, водяные пары. Реакция сопровождается образованием значительного количества тепла;
- при взаимодействии метана с кислородом воздуха возможен взрыв. Подобный эффект характерен для всех алканов и их смесей.
Все перечисленные свойства алканов определяются одними и теми же особенностями их строения, а с другой стороны, можно сказать, что эти свойства позволяют определить структуру молекул.
4-е положение. Атомы и группы атомов в молекулах веществ взаимно влияют друг на друга.
Это положение можно доказать на примере неорганической химии. Для этого надо сравнить свойства водных растворов NН3, НС1, Н2О (аммиак, кислота, нейтральная среда). Во всех трех случаях в состав веществ входят атомы водорода, но они соединены с разными атомами, которые оказывают различное влияние на атомы водорода, поэтому свойства веществ различны.
Изомерия: структурная, пространственная.
Изомерия — явление, заключающееся в существовании химических соединений — изомеров, — одинаковых по атомному составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам.
Рассмотрим изомерию на примере алкенов
А) Структурная изомерия алкенов Виды структурной изомерии: изомерия углеродного скелета, изомерия положения двойной связи и межклассовая изомерия.
1. Изомерия цепи (углеродного скелета)- начиная с С4Н8.
Первые два члена гомологического ряда – этен и пропен – изомеров, относящихся к классу алкенов, не имеют.
Простейший алкен, у которого есть изомерия углеродного скелета — это бутен (С4Н8):
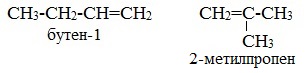
2. Изомерия положения двойной связи (также начинается с бутена - С4Н8):
![]()
3. Межклассовая изомерия, начиная с С3Н6 (алкены изомерны другому классу соединений — циклоалканам).