
- •Функции состояния и функции процесса. Понятие теплоты и работы. Понятия равновесного и неравновесного процесса.
- •Первый закон термодинамики. Принцип эквивалентности теплоты и работы. Опыт Джоуля.
- •Формулировки и аналитические выражения I закона термодинамики. Энергия и работа, их виды.
- •Формулировки и аналитические выражения I закона термодинамики. Понятия внутренней энергии и энтальпии, их свойства.
- •Уравнение I закона термодинамики для неравновесных процессов.
- •Уравнение I закона термодинамики для потока вещества (вывод, основные допущения, понятие входящих в уравнение величин).
- •Понятие идеального газа. Уравнение состояния идеального газа. Газовые постоянные. Термические коэффициенты идеального газа.
- •Понятие теплоемкости. Виды теплоемкости. Изохорная и изобарная теплоемкость, их связь.
- •Расчет адиабатного процесса с учетом зависимости теплоемкости от температуры. Функции и .
- •Политропный процесс. Соотношение между термическими параметрами в политропном процессе. Расчет работы расширения и теплоты в политропном процессе.
- •Основные характеристики смеси идеальных газов. Свойства смеси. Закон Дальтона. Закон Амага.
- •Понятие об обратимых и необратимых процессах. Примеры необратимых процессов. Причины необратимых процессов. Формулировки II закона термодинамики.
- •Круговые процессы или циклы. Прямой обратимый цикл Карно. Обратный обратимый цикл Карно. Характеристики эффективности циклов.
- •Цикл Карно. Кпд цикла Карно. Теорема Карно.
- •Понятие энтропии. Интеграл Клаузиуса. Свойства энтропии.
- •Вывод формулы для расчета изменения энтропии смеси газов.
- •-Диаграмма. Взаимное расположение изобары и изохоры в -диаграмме. Взаимное расположение в -диаграмме изобар различных давлений и изохор различных объемов.
- •Понятие среднеинтегральной температуры подвода (отвода) теплоты. Следствие теоремы Карно (вторая теорема Карно).
- •Изменение энтропии в необратимых процессах. Понятие энтропии изолированной системы.
- •Статистический характер II закона термодинамики. Термодинамическая вероятность. Взаимосвязь энтропии и термодинамической вероятности. Ограниченный характер II закона термодинамики.
- •Понятие эксергии. Эксергия неподвижной системы (графическое представление и вывод формулы).
- •Понятие эксергии. Эксергия потока вещества (графическое представление и вывод формулы).
- •Понятие эксергии. Эксергия источника теплоты с постоянной и переменной температурой. Эксергетическая функция.
- •Потери эксергии в необратимых процессах. Формула Гюи-Стодола. Эксергетический коэффициент полезного действия. Примеры вычисления эксергетического кпд.
- •Характеристические функции (определение, соответствующие им независимые переменные). Частные производные характеристических функций разных порядков.
- •Отличия свойств реальных газов от идеальных. Тройная точка, критическая точка. Фазовая -диаграмма для нормальных и аномальных веществ.
- •Условия фазового равновесия (вывод). Правило фаз Гиббса (примеры применения).
- •Вывод и физический смысл уравнения Клапейрона-Клаузиуса.
- •Основные термодинамические процессы с реальными газами: изотермический, изобарный, изохорный процесс. Определение теплоты и работы в процессах. Построение процессов в диаграммах .
- •Обратимый и необратимый адиабатный процесс реального газа. Расчет работы расширения и технической работы.
- •Адиабатное дросселирование. Представление процесса дросселирования водяного пара в -диаграмме. Коэффициент Джоуля-Томпсона.
- •Дифференциальное и интегральное уравнения адиабатного дроссель-эффекта. Кривая инверсии, ее уравнение и представление в -диаграммах.
- •Зависимость изобарной теплоемкости реального газа в однофазной области от температуры и давления.
- •Уравнение Ван-дер-Ваальса. Физический смысл поправок в его составе. Возможные решения уравнения. Устойчивые и неустойчивые состояния вещества.
- •Вириальное уравнение состояния. Вириальные коэффициенты, способы их определения.
- •Тепловая теорема Нернста. Третий закон термодинамики.
- •Следствия III закона термодинамики.
-
Понятие эксергии. Эксергия неподвижной системы (графическое представление и вывод формулы).
Эксергия – та часть энергии, которая может быть превращена в энергию организованных форм.
Мерой эксергии служит максимально возможная полезная работа, которую можно получить при абстрактном переходе этой системы по обратимым процессам от собственных параметров к параметрам окружающей среды.
Эксергия
– работоспособность.
Эксергия неподвижной системы
1-0 – обратимый процесс,
 ,
,
 ,
,
 ,
,
 ,
,
 – работа внешних
сил против системы,
– работа внешних
сил против системы,
 ,
,
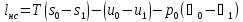 ,
,
 .
.
-
Понятие эксергии. Эксергия потока вещества (графическое представление и вывод формулы).
Эксергия – та часть энергии, которая может быть превращена в энергию организованных форм.
Мерой
эксергии служит максимально возможная
полезная работа, которую можно получить
при абстрактном переходе этой системы
по обратимым процессам от собственных
параметров к параметрам окружающей
среды.
Эксергия – работоспособность.
Эксергия потока вещества
 ,
,
изменением кинетической и потенциальной энергиями пренебрегаем,
 ,
,
 ,
,
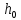 – энтальпия окружающей
среды,
– энтальпия окружающей
среды,
 ,
,
 .
.
Вычисление эксергии
потока вещества в
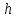 -диаграмме
сводится к вычислению разности между
энтальпией потока и энтальпией «прямой
среды».
-диаграмме
сводится к вычислению разности между
энтальпией потока и энтальпией «прямой
среды».
-
Понятие эксергии. Эксергия источника теплоты с постоянной и переменной температурой. Эксергетическая функция.
Эксергия – та часть энергии, которая может быть превращена в энергию организованных форм.
Мерой эксергии служит максимально возможная полезная работа, которую можно получить при абстрактном переходе этой системы по обратимым процессам от собственных параметров к параметрам окружающей среды.
Эксергия – работоспособность.

Эксергетическая функция
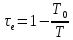 .
.
Эксергия источника теплоты с постоянной и переменной температурой
При постоянной температуре источника теплоты,
эксергия
источника теплоты
 равна работе цикла Карно
равна работе цикла Карно
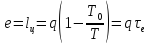 .
.
При переменной температуре источника
 ,
,
 ,
,
 ,
,
 ,
,
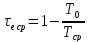 ,
,
 ,
,
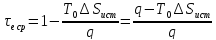 ,
,
 .
.
-
Потери эксергии в необратимых процессах. Формула Гюи-Стодола. Эксергетический коэффициент полезного действия. Примеры вычисления эксергетического кпд.
Потери эксергии в необратимых процессах
Реальные
процессы необратимы, что приводит к
уменьшению способности системы
производить работу. Это уменьшение
называется потерей эксергии.
Рассмотрим необратимый процесс адиабатного дросселирования,
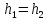 ,
,
 ,
,
эксергия газа:
 ,
,
 ,
,
 ,
,
 ,
– формула
Гюи-Стодолы.
,
– формула
Гюи-Стодолы.
Эксергетический коэффициент полезного действия
 ,
,
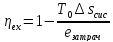 .
.
Для обратимого цикла Карно:
 ,
,
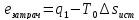 ,
,
 ,
,
эксергетический КПД любого обратимого цикла равен единице.
Примеры
вычисления эксергетического КПД
-
Прямой цикл

при постоянной
температуре
 ,
,
при переменной температуре
 ,
,
 ,
,
 ,
,
 .
.
-
Обратный цикл
 ,
,
 .
.
-
Эксергетический КПД турбины
 .
.
-
Эксергетический КПД компрессора
 .
.
-
Характеристические функции (определение, соответствующие им независимые переменные). Частные производные характеристических функций разных порядков.
Функция является характеристической, если ее самой, соответствующих ей независимых переменных и ее частных производных разных порядков по этим независимым переменным достаточно, чтобы в явном виде выразить любое термодинамическое свойство системы.
 ,
,
 ;
;
-
Внутренняя энергия – характеристическая функция в переменных энтропии и объема
 ,
,
 ,
,
 ,
,
 ;
;
-
Энтальпия – характеристическая функция в переменных энтальпии и давления
 ,
,
 ,
,
 ,
,
 ;
;
-
Функция Гельмгольца – характеристическая функция в переменных температуры и объема
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ;
;
-
Функция Гиббса – характеристическая функция в переменных температуры и давления
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 .
.
-
Дифференциальные уравнения термодинамики (назначение, виды). Уравнения Максвелла.
Дифференциальные уравнения термодинамики – дифференциальные уравнения в частных производных, связывающие различные термодинамические свойства веществ.
-
Уравнения Максвелла
 ,
,
 ,
,
 ,
,
 ,
,
 ;
;
 ,
,
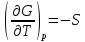 ,
,
 ,
,
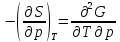 ,
,
 ;
;
 ,
– уравнения
Максвелла.
,
– уравнения
Максвелла.
-
Переменные температура и объем
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
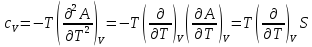 ,
,
 ,
,
 .
.
 .
.
-
Переменные температура и давление
 ,
,
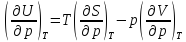 ,
,
 ,
,
 ,
,
 ,
,
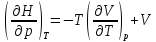 ,
,
 ,
,
 ,
,
 .
.
 .
.
-
Характеристические функции системы с изменяющейся массой.
Химический
потенциал
 вещества – удельная энергия Гиббса
вещества – удельная энергия Гиббса
 .
.
-
Внутренняя энергия
 ,
,
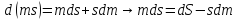 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 .
.
-
Энтальпия
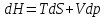 ,
,
 ,
,
 .
.
-
Энергия Гельмгольца
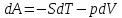 ,
,
 ,
,
 .
.
-
Энергия Гиббса
 ,
,
 ,
,
 .
.
В случае неоднородной системы (содержащей несколько различных веществ):
 ,
,
 ,
,
 ,
,
 .
.
-
Отличия свойств реальных газов от идеальных. Термодинамическая поверхность, фаза (определения). Фазовые переходы. Полная фазовая -диаграмма реального газа.
Отличия свойств реальных газов от идеальных:
-
вещество находится в разных фазах (наличие фазовых переходов);
-
уравнение состояния реального газа
 ,
,
 – коэффициент
сжимаемости – сложная функция температуры
и плотности (или давления);
– коэффициент
сжимаемости – сложная функция температуры
и плотности (или давления);
-
все калорические свойства помимо
 зависят и от второго параметра
зависят и от второго параметра
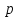 или
или

 .
.
Термодинамическая
поверхность
– геометрическое место точек в
пространственной системе координат
 ,
изображающих равновесные состояния
системы в функциях от термодинамических
параметров.
,
изображающих равновесные состояния
системы в функциях от термодинамических
параметров.
Фаза – однородная (гомогенная) область неоднородной (гетерогенной) системы, ограниченная поверхностью раздела и имеющая во всех своих точках одинаковые физические свойства.

Фазовым переходом называют переход вещества из одной фазы в другую, сосуществующую с первой.
Фазовые переходы:
-
пар ↔ жидкость – кипение и конденсация,
-
жидкость ↔ твердое тело – кристаллизация и плавление,
-
твердое тело ↔ пар – сублимация и десублимация.
Полная фазовая -диаграмма реального газа
 – тройная прямая,
– тройная прямая,
 и
и
 – левая и правая пограничные кривые
двухфазной области жидкость-пар (линия
насыщения, критическая точка). Для этого
перехода все свойства жидкости на левой
пограничной кривой обозначают индексом
‘, а свойства пара на правой пограничной
кривой – ‘‘.
– левая и правая пограничные кривые
двухфазной области жидкость-пар (линия
насыщения, критическая точка). Для этого
перехода все свойства жидкости на левой
пограничной кривой обозначают индексом
‘, а свойства пара на правой пограничной
кривой – ‘‘.
