
- •Институт холода и биотехнологий
- •Технические измерения и приборы Учебно-методическое пособие
- •Санкт-Петербург
- •Введение
- •Теоретические положения и условия задач
- •1. Измерение температуры
- •2. Измерение давления
- •3. Измерение уровня
- •4. Измерение расхода
- •5. Анализ состава сред
- •Список литературы
- •Содержание
- •Институт холода и биотехнологий
- •Технические измерения и приборы
5. Анализ состава сред
Под анализом состава сред понимается измерение концентрации растворов, измерение концентрации водородных ионов по водородному показателю рН, измерение содержания отдельных компонентов в газовых смесях, измерение влажности газов. Рассмотрим некоторые понятия и формулы, необходимые для решения задач.
Постоянная электролитической ячейки К – это коэффициент, определяющий соотношение между удельной электропроводностью χ0 раствора и электропроводностью χ ячейки, или ее сопротивлением Rя:
![]() .
.
Сопротивление измерительной электролитической ячейки зависит не только от концентрации раствора, но и от температуры. В узком температурном диапазоне (например 5–10 С) можно считать, что зависимость сопротивления ячейки Rяt от температуры имеет вид:
![]() ,
,
где Rя1 – сопротивление ячейки при температуре t1; β – температурный коэффициент электропроводности раствора.
Следует отметить, что в ряде задач рассматриваются два понятия: сопротивление электродной ячейки и сопротивление измерительной ячейки. Под сопротивлением электродной ячейки подразумевается сопротивление только жидкости, заполняющей межэлектродное пространство. Сопротивление измерительной ячейки – это сопротивление электродной ячейки и сопротивление шунта.
В задачах на измерение рН растворов следует прежде всего помнить общую зависимость между потенциалом Е измерительного электрода и концентрацией С ионов растворе (уравнение Нернста)
![]() ,
,
где
R = 8,317
Дж/(К·г·моль) – газовая постоянная; Т
– температура, К; n
– валентность иона; F=96522
Кл/г-экв – число Фарадея (заряд
грамм-эквивалента
ионов);
![]() – коэффициент активности ионов водорода;
[Н+]
– концентрация водородных ионов,
г-ион/л; Е0
– нормальный
электродный потенциал (потенциал,
который имеет электрод при погружении
в раствор с нормальной концентрацией
[Н+] = 1
г-ион/л), мВ. Следует отметить, что
фактически измеряется не концентрация
водородных ионов по
– коэффициент активности ионов водорода;
[Н+]
– концентрация водородных ионов,
г-ион/л; Е0
– нормальный
электродный потенциал (потенциал,
который имеет электрод при погружении
в раствор с нормальной концентрацией
[Н+] = 1
г-ион/л), мВ. Следует отметить, что
фактически измеряется не концентрация
водородных ионов по
![]() ,
а активность ионов водорода в растворе
,
а активность ионов водорода в растворе
![]() .
Во многих случаях
.
Во многих случаях
![]() ,
поэтому в задачах часто говорится об
измерении концентрации водородных
ионов по рН. Для водородного электрода
Е0 = 1
и n
= 1, поэтому
уравнение
,
поэтому в задачах часто говорится об
измерении концентрации водородных
ионов по рН. Для водородного электрода
Е0 = 1
и n
= 1, поэтому
уравнение
![]() принимает вид
принимает вид
![]() мВ
мВ
В общем случае разность потенциалов между измерительным электродом и электродом сравнения можно записать следующим образом:
![]() ,
мВ
,
мВ
где t – температура раствора; Еи и рНи – координаты изопотенциальной точки.
При решении задач по газовому анализу следует обратить внимание на физические основы работы различных газоанализаторов, их устройство и электрические схемы.
В задачах по термокондуктометрическим газоанализаторам предполагается, что измерительная камера представляет собой полый цилиндр, внутри которого коаксиально расположена платиновая нить (чувствительный элемент). Теплоотвод от единицы поверхности нити к стенкам осуществляется в основном теплопроводностью в соответствии с выражением
![]() ,
,
где
tн
и tс
– температура соответственно нити и
стенки камеры, С;
λ – теплопроводность смеси при
температуре, равной
![]() ,
Вт/(м·К).
,
Вт/(м·К).
Теплопроводность смеси следующим образом связана с теплопроводностью компонентов λi и их объемной концентрацией Сi:
![]() .
.
В задачах по термомагнитным газоанализаторам основным является выражение для силы, действующей на единичный объем парамагнитной смеси, находящейся в неоднородном магнитном поле:
![]() ,
,
где С – относительная концентрация компонента; χ0 – объемная магнитная восприимчивость компонента при нормальном давлении р0 = 760 мм рт. ст. и нормальной температуре Т0 = 273 К; Н – напряженность магнитного поля, А/м; Т1 – температура газа при входе в измерительные камеры, К; Т2 – температура газа после обогрева нитью, К.
Эта сила определяет интенсивность термомагнитной конвекции, которая в свою очередь влияет на отвод теплоты от чувствительного элемента, т. е. на его температуру. В реальных условиях интенсивность газовой конвекции определяется не только силой Fм, но и силой тепловой конвекции. Поэтому изменение показаний прибора при изменении температуры t и давления р газовой смеси отличается от расчетного только изменением Fм.
Наибольшее распространение при измерении влажности воздуха получили различные варианты психрометров и определение влажности по точке росы. Психрометрический метод основан на зависимости между влажностью воздуха и показаниями сухого tс и мокрого tм термометров. При использовании психрометров значение» психрометрической разности» tс – tм зависит не только от относительной влажности воздуха, но и от конструкции психрометра, определяющей интенсивность охлаждения мокрого термометра за счет испарения влаги.
Измерение влажности по методу точки росы является одним из точных методов, получивших широкое распространение в промышленности. Эти гигрометры имеют широкие пределы применения по температуре, давлению и влажности воздуха. Однако они отличаются некоторой сложностью конструкции, а также влиянием на результат измерения состояния поверхности зеркальца.
При решении задач настоящего раздела могут потребоваться данные о самых различных физических, химических и других свойствах веществ. Эти данные можно найти соответствующих справочниках.
Контрольные вопросы и задачи
5-1. Двухэлектродная электролитическая ячейка была заполнена раствором с удельной электропроводностью χ0 = 12,1 См/м. Определите постоянную ячейки, если ее сопротивление оказалось равным Rя = 13,7 Ом.
5-2. Постоянная
ячейки К = 11,2 м–1.
Ячейка заполнена раствором и ее
сопротивление при этом составляет 5
МОм. Определите концентрацию раствора,
если известно, что зависимость между
концентрацией С
и удельной проводимостью χ0
описывается уравнением
![]() ,
где а = 1,75·10–8
(См/м)/(мг/л).
,
где а = 1,75·10–8
(См/м)/(мг/л).
5-3. Возможна ли компенсация температурной погрешности концентратомера, если в качестве компенсатора использовать только медное сопротивление Rм. Электроды ячейки (рис. 5-1) не зашунтированы. Ячейка заполнена 5 %-м раствором КСl, удельная электропроводность при 20 С составляет 7,18 См/м, температурный коэффициент β = 0,02 К–1. Постоянная ячейки К = 190 м–1. Температурную компенсацию необходимо осуществить при температурах 20 и 40 С.
5-4. Электродная ячейка (рис 5-1) с постоянной К = 190 м–1 заполнена раствором КСl концентрацией 5 %, удельная проводимость раствора при 20 С составляет χ0 = 7,18 См/м. Температура раствора может меняться в интервале 20–40 С, при этом средний температурный коэффициент проводимости раствора равен β = 0,02 К–1. Определите сопротивление медного резистора Rм, обеспечивающего компенсацию изменения сопротивления ячейки в указанном температурном диапазоне. Сопротивление шунта примите равным сопротивлению электродной ячейки Rя при t = 20 С. Температурный коэффициент сопротивления меди α = 0,00426 К–1.

Рис. 5-1
5-5. Для
условия задачи 5-4 определите температуру,
при которой будет иметь место наибольшая
погрешность за счет неполной компенсации
изменения сопротивления ячейки изменением
сопротивления медного резистора. Оцените
эту погрешность, предполагая, что
зависимость удельной электропроводности
от концентрации имеет вид
![]() ,
См/м.
,
См/м.
5-6. Концентратомер, отградуированный в процентах по массе, имеет шкалу 5–10 %. Постоянная электродной ячейки 500 м–1. В интервале 5–10 % зависимость удельной электропроводности χ0 раствора NaCl от концентрации С приближенно можно описать уравнением
![]() .
.
Определите
показания концентратомера при пропускании
через него
6 %-го раствора КCl
с удельной электропроводностью
![]() = 8,564
См/м.
= 8,564
См/м.
5-7. Концентрация раствора NaCl измеряется электродным концентратомером. Номинальное значение концентрации раствора 100 мг/л Оцените изменение показаний прибора, вызванное случайным попаданием в раствор щелочи NaОН в концентрации 5 мг/л. Проводимость раствора NaОН превышает проводимость раствора NaCl той же концентрации в 2,8 раза.
5-8. Рассчитайте значения R1 и Rш безэлектродного концентратомера (рис. 5-2) для введения коррекции в показания на интервале температур от 20 до 50 С. Диапазон измерения концентратомера 5–15 % КCl. Оцените погрешность, которая может иметь место при концентрации 5 % КCl и t1 = 20 С, а также при концентрации 15 % КCl и t2 = 50 С. Расчет ведется на номинальное значение температуры раствора tн = 35 С. Постоянная жидкостного контура К = 700 м–1, удельные электропроводности раствора при t1 = 20 С и температурные коэффициенты имеют следующие значения:
С1 = 5 % КCl, χ01 = 7,177 См/м, β1 = 0,0201 К–1,
С2 = 10 % КCl, χ02 = 14,1 См/м, β2 = 0,0188 К–1,
С3 = 15 % КCl, χ03 = 20,9 См/м, β3 = 0,0179 К–1.
При температуре раствора tн = 35 С зависимость удельной элект-ропроводности от концентрации описывается выражением
![]() См/м.
См/м.
Напряжение питания Uпит = 127 В. Обмоточные данные схемы: n1 = 127 витков, n2 = 10 витков, nж = 1 виток. Максимальный компенсационный сигнал Uк.макс = 10 В. Начальное сопротивление терморезистора R0 = 5 кОм, коэффициент В = 2300.
5-9. С помощью каких резисторов (рис. 5-2) возможна подгонка начала и конца шкалы при заданных Rt, Rш, R1 и R2?
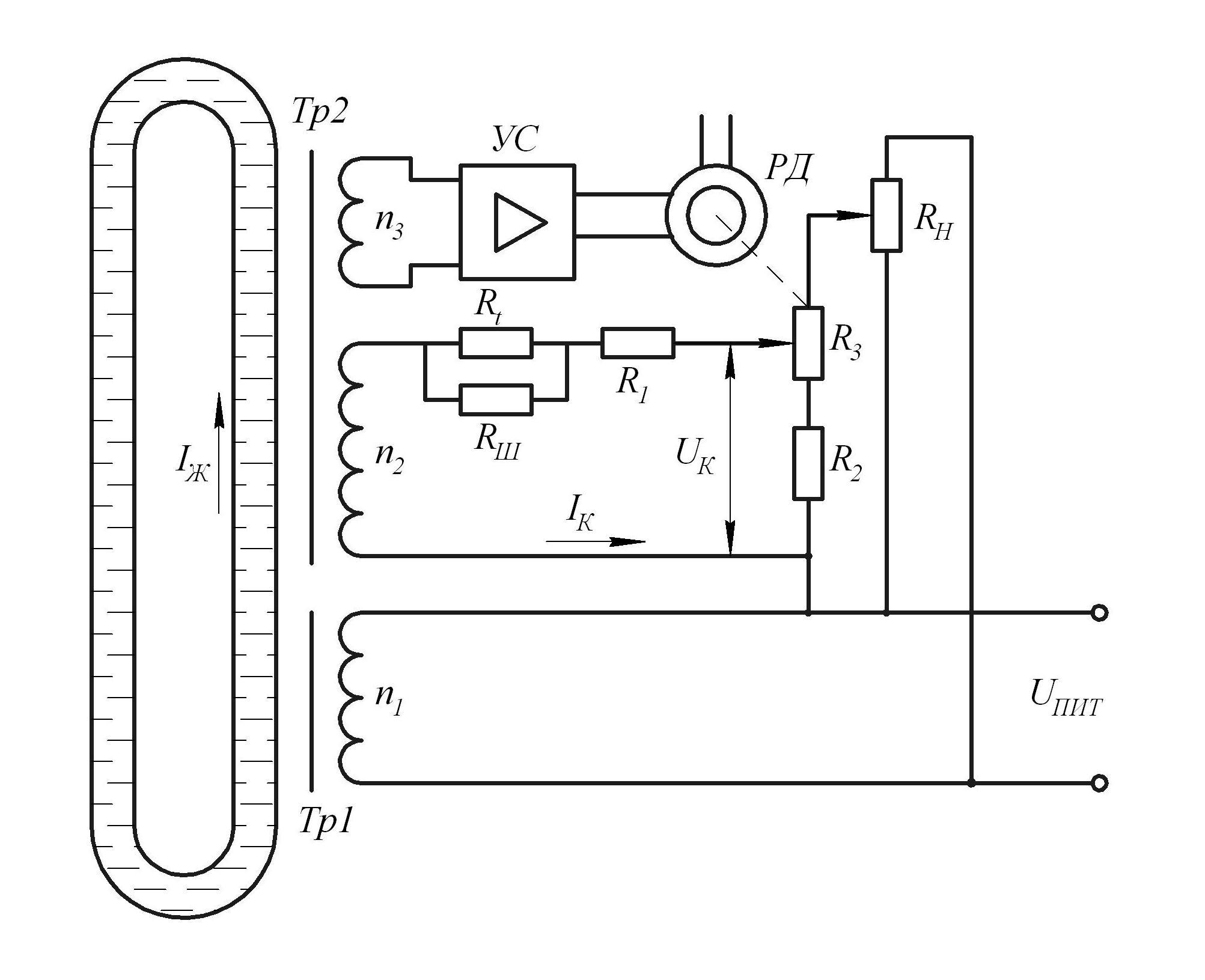
Рис. 5-2
5-10. ЭДС электродной системы, состоящей из измерительного стеклянного электрода и хлорсеребряного электрода сравнения, зависит от значения рН и температуры раствора:
![]() ,
мВ
,
мВ
Eн = –203 мВ; рНн = 4,13.
Определите значение погрешности при отсутствии температурной компенсации, если градуировка производилась при температуре t1 = 20 С, а действительное значение температуры t2 = 35 С. Действительное значение рН = 9.
5-11. Градуировка электродной системы производилась по стандартным буферным растворам. ЭДС электродной системы электродной системы имела следующие значения:
рН1 = 1,67 и t1 = 15 С……E1 = +1,27 мВ
рН2 = 1,77 и t2 = 80 С……E2 = +4,27 мВ
рН3 = 9,27 и t1 = 15 С……E3 = – 432,69 мВ
рН4 = 8,88 и t2 = 80 С……E4 = –494,14 мВ
Определите коэффициенты уравнения электродной системы.
5-12. Измерительный электрод имеет внутреннее сопротивление Rи= 50 МОм, электрод сравнения Rс= 20 кОм. ЭДС, развиваемая системой, 500 мВ. Для измерения ЭДС используется милливольтметр с диапазоном 0–0,5 В и входным сопротивлением Rвх = 0,5 кОм. Какими будут его показания при названных условиях?
5-13. Определите концентрацию кислорода в дымовых газах, если анализ производился объемно-абсорбционным газоанализатором и объем смеси после поглощения составил Vп = 95 мл. Объем смеси в измерительной бюретке до поглощения V0 = 100 мл, объем вредного пространства вне измерительной бюретки (объем распределительной гребенки и других соединительных частей) Vв.п = 2,5 мл. Коэффициент Кп, характеризующий отношение объема компонента, поглощенного в газоанализаторе, к объему этого компонента до поглощения, равен 0,95. Температура газа перед отбором пробы в газоанализатор t1 = 40 С. Во время анализа температура газа снизилась до t2 = 30 С.
5-14. Анализ содержания углекислого газа в продуктах горения осуществляется кондуктометрическим газоанализатором. Определите, как изменится температура чувствительного элемента (нити) газоанализатора, если через него первоначально пропускался воздух (при этом температура нити была 80 С), а затем стали пропускать продукты горения со следующим содержанием компонентов: кислород – 4 %, углекислый газ – 15 %, азот – 63 %, водяные пары – 18 %. Предполагается, что количество теплоты, передаваемое от чувствительного элемента к стенке, одинаково при любой газовой смеси. Предполагается также, что передача теплоты осуществляется только за счет теплопроводности, а температура стенок постоянна и равна tс = 20 С.
5-15. Для
условия задачи 5-14 определите, как
изменятся показания газоанализатора,
если печь для дожигания водорода в
газоанализаторе не работает, а в продуктах
горения содержится 0,2 % Н2
и состав смеси будет следующим:
![]() 15 %,
15 %,
![]() 4 %,
4 %,
![]()
![]()
![]() .
.
5-16. Оцените погрешность, которая может иметь место при эксплуатации термокондуктометрического газоанализатора, если его градуировка на СО2 осуществлялась на синтетических смесях (например, 10 % СО2 + 90 % воздуха или 10 % СО2 + 90 % N2), а средний состав продуктов горения природного газа следующий: СО2 – 10 %, О2 – 2 %, N2 – 70 % и Н2О – 18 %. При заполнении всех камер газоанализатора воздухом температура чувствительного элемента tн0 = 80 С. Температура стенки tс = 20 С.
5-17. Газоанализатор, определяющий состав смеси по теплопроводности, градуировался по синтетической смеси СО2+N2. Измерительная схема газоанализатора (рис. 5-3) представляет собой неуравновешенный мост, образованный четырьмя одинаковыми чувствительными элементами из платиновой проволоки с сопротивлением при 0 С R0 = 1,0 Ом. Полагаем, что зависимость сопротивления от температуры имеет вид
![]() ,
,
где α = 3,92·10–3 К–1.
Мост питается стабилизированным током I = 350 мА, при этом температура элементов R1 и R2, находящихся в азоте, равна 80 С. Разность потенциалов в измерительной диагонали измеряется милливольтметром с бесконечно большим входным сопротивлением. Внутренний диаметр измерительной камеры D = 6,6 мм, диаметр чувствительного элемента d = 0,05 мм, его длина l = 20 мм, температура стенок камеры tс = 20 С. Определите уравнение шкалы газоанализатора, если диапазон его измерения 0–20 % СО2, и рассчитайте напряжение на измерительной диагонали мости при С = 0; 5; 10; 15; 20 % СО2.

Рис. 5-3
5-18.
Содержание водорода Н2
в электролитическом кислороде О2
в интервале
значений от 0 до 10 % измеряется
термокондуктометрическим газоанализатором.
Установите связь между содержанием
водорода и температуры платиновой нити
чувствительного элемента газоанализатора.
Коэффициент черноты нити ε = 0,2,
диаметр нити d = 0,02
мм, длины нити l = 20
мм, диаметр камеры D = 5
мм, ток, протекающий
по нити, I = 51
мА, температура стенок камеры tс = 20
С.
Сопротивление нити изменяется по закону
![]() ,
где α = 3,92·10–3
К–1.
Удельное сопротивление платины
ρ = 0,0981·10–6
Ом·м. В
решении следует учесть все виды
теплообмена между стенкой и нитью.
,
где α = 3,92·10–3
К–1.
Удельное сопротивление платины
ρ = 0,0981·10–6
Ом·м. В
решении следует учесть все виды
теплообмена между стенкой и нитью.
5-19. Дымовые газы имеют следующий состав: кислород – 4 %, углекислый газ – 15 %, азот – 63 %, водяные пары – 18 %. Определите, как изменится относительная магнитная восприимчивость газов в следующих случаях:
а) если содержание О2 увеличится на 1 %, а содержание N2 уменьшится на 1 % при неизменной концентрации СО2 и Н2О;
б) если содержание СО2 увеличится на 1 %, а содержание N2 уменьшится на 1 % при неизменной концентрации О2 и Н2О.
Относительные объемные магнитные восприимчивости компонентов газовой смеси имеют следующие значения:
![]()
5-20. Через магнитный газоанализатор проходит смесь следующего состава: СО2 – 20 %, О2 – 5 % и N2 – 75 % при расчетной температуре t1 = 20 С, разряжении р1 = 300 кгс/см2. Изменится ли показание газоанализатора, если: а) при неизменной концентрации температура смеси возрастет до t2 = 50 С; б) при неизменной температуре возрастет разряжение до р2=1000 кгс/см2.
Предполагается, что на выходе из измерительной ячейки температура смеси равна tс = 100 С.
5-21. Для определения влажности воздуха в цехе завода при-меняется аспирационный психрометр. Определите относительную влажность воздуха φ, если сухой термометр показывает tс = 22,5 С, а мокрый tм = 18,5 С. Давление воздуха 760 мм рт. ст.
5-22. Абсолютная влажность воздуха, поступающего в нагревательную печь, f = 30 г/м3 сухого воздуха. Определите относительную влажность дутья при температуре 300 С. Избыточное давление воздуха ри = 2 кгс/см2.
5-23. Определите абсолютную влажность доменного газа, если известно, что измеритель влажности, работающий по методу точки росы, показывает температуру tт.р = 32,5 С при нормальном давлении.
5-24. При измерении влажности воздуха в цехе номинальное значение точки росы составляет 10 С. Однако после протирки зеркальца замасленной тряпкой температура точки росы снизилась до 0 С. Какова погрешность, возникшая при измерении относительной влажности воздуха (t = 20 С) при таком изменении точки росы, и какова причина такого изменения показаний влагомера?
Ответы
К разделу «Измерение температуры»
О1-3. tд = 46,1 С.
О1-5. t = 50 С.
О1-6.
t = 0,6 С.
О1-7.
t = 0,3 С.
О1-12.
![]() .
О1-15.
t = 593,5 С.
О1-21.
t = 7,5 С.
О1-29.
.
О1-15.
t = 593,5 С.
О1-21.
t = 7,5 С.
О1-29.
![]() .
О1-30.
.
О1-30. ![]()
![]() .
О1-31.
.
О1-31. ![]()
![]() .
О1-33.
.
О1-33. ![]() .
О1-35.
.
О1-35.![]() .
О1-37.
.
О1-37.
![]() .
О1-39.
tд = 0,78 С.
О1-45.
t = 11 С.
О1-46.
t = –39 С.
О1-47.
t = 70 С.
О1-48. t = 0,5 С.
О1-49.
tдин = 23 С.
О1-50.
То
= 17,8 с. О1-51.
То
0,001 с.
.
О1-39.
tд = 0,78 С.
О1-45.
t = 11 С.
О1-46.
t = –39 С.
О1-47.
t = 70 С.
О1-48. t = 0,5 С.
О1-49.
tдин = 23 С.
О1-50.
То
= 17,8 с. О1-51.
То
0,001 с.
К разделу «Измерение давления»
О2-2.
![]() .
О2-5.
.
О2-5.![]() О2-6.
О2-6.
![]() .
О2-10.
.
О2-10.
![]() .
О2-11.
.
О2-11.
![]() .
О2-14.
.
О2-14.
![]() .
О2-15.
.
О2-15.
![]() .
О2-21.
.
О2-21.
![]() .
.
К разделу «Измерение уровня»
О3-1. ![]() .
О3-2.
.
О3-2.
![]() .
О3-4.
.
О3-4.
![]() .
О3-5.
.
О3-5.
![]() .
О3-6.
.
О3-6.
![]() .
О3-9.
.
О3-9.
![]() .
О3-11.
.
О3-11.
![]()
![]()
![]() .
О3.13.
.
О3.13.
![]() .
О3-15.
.
О3-15.
![]() .
.
К разделу « Измерение расхода»
О4-1.
![]() .
О4-4.
.
О4-4.
![]() .
О4-5.
.
О4-5.
![]() .
О4-9.
.
О4-9. ![]() .
О4-10.
.
О4-10.
![]() .
О4-11.
.
О4-11.
![]() .
О4-12.
.
О4-12.
![]() .
О4-13.
.
О4-13.
![]() .
О4-14.
.
О4-14.
![]() .
О4-15.
.
О4-15.
![]()
![]()
![]()
![]()
![]() .
.
О4-16.
![]() .
О4-19.
.
О4-19.
![]() .
О4-20.
.
О4-20.
![]()
![]()
![]() .
.
